初中化学物质转化关系图(20200612011026)
九年级科学上册 2.2物质转化规律图(第1至第2课时)课件

⑥ +酸
④ + 酸或盐
⑤ + 非金属
⑥:金属(jīnshǔ)氧化物+酸=====盐 + 水
CuO +H2SO4 = CuSO4 + H2O Fe2O3 + 6HCl = 2 FeCl3+ 3H2O
第十二页,共十九页。
二、金属单质与其(yǔqí)化合物的转化
① (4 种) ②
③ +酸、非金属
金属 +O2 金属氧 ⑧+还原剂 化物
法 H2SO4
==MgSO4
H2SO4
H2SO4 H2SO4
==MgSO4
==MgSO4 ==MgSO4
第六页,共十九页。
二、金属(jīnshǔ)单质与其化合物的转化
① (4 种) 金属 +O2 金属氧
⑧+还原剂 化物
②
③ +酸、非金属
+H2O ⑦△
((可 不溶 溶性 性))碱
氧化物、盐
盐
⑥ +酸
+H2O ⑦△
((可 不溶 溶性 性))碱
氧化物、盐
盐
⑥ +酸
④ + 酸或盐
⑦★ :碱=△==金属氧⑤化+物非+金水属
(不溶)
Cu(OH)2 =△ CuO+H2O (蓝色固体(gùtǐ)变成黑色,试管口出现水珠)
2Fe(OH)3 ==△ Fe2O3+ 3H2O
△或高温
⑧:金属(jīnshǔ)氧化物C+还原剂========金属+非金属氧化物
置换反应
Zn + H2SO4 == ZnSOO44+ H2 ↑ ZZnn + CuSO4 == ZZnnSSOO4 4+ Cu Na + H2SO4 = (发生的反应不是(bùshi)置换反应)
转化关系图

重要的转化关系图1.碳及其化合物的转化关系图2.氮及其化合物的转化关系图NH 4N 324Mg 3N 23·H 2ONH 4+ OH -+Ca(OH)2,△HClH 2,催化剂高温 高压O 2 , 放电O 2H 2O NaOH O 2浓H 2SO 4△①浓酸,Cu ②见光或△③C点燃2O△△O 2 ,催化剂,3.磷及其化合物的转化关系图4.铁及其化合物的转化关系图5.镁及其化合物的转化关系图6氯及其化合物的转化关系图Cl 2CuCl 2PCl 3、PCl HClO O 2Ca(ClO)2①C O 2+H 2O②C l P ,点燃2点燃NaClNaOH H 2S O 4(浓)△MnO 2、△N a , △①电解熔融盐②电解食盐水H 2O光照A gN O3Ag N O 3Ca(OH)27硫及其化合物的转化关系图H 2SSSO 2SO 3Na 2SO 4FeS FeS 2Na 2SO 3H 2SO 3H 2SO 4BaSO 4HClH 2,△O 2,燃烧H 2SO 2,燃烧①加热分解②不完全燃烧O 2,催化剂,△NaOHNaOHO 2BaCl 2H 2OBaCl 2①浓酸,C u ,△②浓酸,C, △H 2OH2S O4O2,高温F e ,△8硅及其化合物的转化关系图[此文档可自行编辑修改,如有侵权请告知删除,感谢您的支持,我们会努力把内容做得更好]。
九级化学物质转化关系图

一、初中化学物质的转化关系1、氧气、氧化物、酸、氢气、水H2OKMnO4↘↓↑↗CO、CO2↗SO2H2SO4H2O2→→P2O5+ Mg Al Zn Fe→ H2→H2O ↘MgO HClKClO3↗↓↘Al2O3 Fe3O42、碳与碳的化合物3、氢氧化钠、碳酸钠、氯化钠+ CO2↗ Na2SO4 → BaSO4↓(白)NaOH → Na2CO3 → CaCO3↓(白)(变质)↘ NaCl → AgCl↓(白)4、含钙化合物的关系:↙↗―――――――↘↖CaCO3→CaO→Ca(OH)2→CaCl2↖CO2↙5、氧化钡、氢氧化钡与硫酸钡1 / 32 /3 ↗BaCl 2 → BaSO 4↓(白)BaO → Ba(OH)2 ↗↘ + CuS O 4↘Cu(OH)2↓(蓝)6、硫酸铜、碳酸氢钙、碳酸氢钠、碳酸氢铵CuO ↗ CO 2↙ ↘ Ca(HCO 3)2 → CaCO 3→CaOCuSO 4.5H 2O →CuSO 4→ Cu ↘ H 2O↗Na 2CO 3 ↗ NH 3 → NH 3.H 2O NaHCO 3 →CO 2 NH 4HCO 3 → H 2O↘H 2O → H 2CO 3 ↘ CO 2 → H 2CO 37、铝、镁、锌、铁、铜及其化合物↗ZnSO 4↖ ↗ AlCl 3↖Zn → ZnO Al → Al 2O 3 ↘ZnCl 2↙ ↘Al 2(SO 4)3↙Fe Al↗MgCl 2↖ ↙﹉﹉﹉﹉↗ CuCl 2↘↖Mg → MgO Cu ←→CuO Cu(OH)2 ↘MgSO 4↙ ↖____↘ CuSO 4↗↙ Fe Al↙ FeCl 3 ↖ C CO H 2 Mg Al ↗FeSO 4Fe(OH)3 Fe 2O 3 ←――――→ Fe↖Fe 2(SO 4)3↙ O 2 H 2O ↘ FeCl 2 8、常见物质的相互转化关系(即注明必要的反应物、反应条件)CO 2 CO C 或O 2 O 2 H 2O H 2O 2Al 2O 3 AlCl 3 Al CuO CuSO 4 Cu ⑴ ⑵ ⑶ ⑷ MgO MgSO 4 Mg Cu H 2 Fe CaO Ca(OH)2 CaCO 3 CaCl 2 Ca(OH)2CaCO 3 ⑸ ⑹ ⑺ ⑻CaCO3Na2CO3CO2CO2NaOHNa2CO3CO2O2H2ONaOH NH4ClNH3⑼⑽⑾⑿3 / 3。
各元素及其重要化合物间的相互转化关系图ppt课件

3.铁及其重要化合物间的转化关系
⒀
⑶⑵
⑷
⑻
⑸ ⑼⑽⑾
⑴
⑹ ⑿ ⒃
⑺
⒁ ⒂
⒄
⒅
ppt课件.
4
4.铜及其重要化合物间的转化关系
CuSO4
⑷
⒂
⑶
⒄
⑵
⑼
⑿ ⒁
⑴ O2
⒀
H2 ⑻
△
⑺
O2
⑹
⑽
⑾
(21)
HCl
⒅
⒃ห้องสมุดไป่ตู้
⒆ H2S
CuS
(20)或Na2S
ppt课件.
5
非金属元素及其化合物
ppt课件.
6
1.碳、硅及其重要化合物间的转化关系
⑷ ⑵
⑴
⑺
⑽
⒆
⑸ ⑼
⑿
⑾
⒃
⑹
⒀
⑻
⒁ ⑶
⒅ ⒂
⒄
⒇ (24)
(21) (23)
(27) (28)
(22)
(25)
(26) Na2CO3
(30)
ppt课件.
(29)
7
2.氯及其重要化合物间的转化关系
(23)
⑽ ⑼⑻⑶
⑵
⑷
⑹
⑸
⑴
⑺
⒀
⑿
(24)
(22) ⒄
⑾
(21)
⒃
⒅
⒇ 3
⒁
⒂
⒆
ppt课件.
8
3.硫及其重要化合物间的转化关系
⑷
⑸
⑴
⑼ ⑽
△
⑵
⑿
⑻⑺
⒇
⑶
⑹
⒀
⑾
⒁
2020年初中常见物质的转化关系框图

或 Ca(OH) 2 + (NH 4)2CO 3
CaCO3↓+ 2H 2O + 2NH 3↑
④ CaCl 2 + Na2CO 3
CaCO3↓ + 2NaCl
六、铝和铝的化合物
或 CaCl 2 + K 2CO 3
CaCO3↓ + K2 Cl
① 4Al + 3O 2
2Al 2O3 (铝不易锈蚀的原因 )
八、九种碱之间的转化
① Ba(OH) 2 + K 2CO 3
Al(OH) 3↓ +3KCl
或 2AlCl 3+ 3Ba(OH) 2
2Al(OH) 3↓ +3BaCl 2
或 2AlCl 3 + 3Ca(OH) 2
2Al(OH) 3↓ +3CaCl2
⑦ Al(OH) 3 + 3HCl
AlCl 3 + 3H 2O
* ⑧ 2Al(OH) 3
Al 2O3 + 3H 2O
MgSO 4 + Cu
或 Mg + FeSO 4
MgSO 4 + Fe
或 Mg + ZnSO 4
MgSO 4+ Zn
或 3Mg + Al 2 (SO4)3
3MgSO 4+ 2Al
④ MgO + H 2SO4
MgSO 4 + H 2O
⑨ 2Al(OH) 3 +3H 2SO4
Al 2(SO4)3 + 6H 2O
CaCl 2 + H 2O
或 2Al + 3ZnSO 4 ④ Al 2O3 + 3H 2SO4
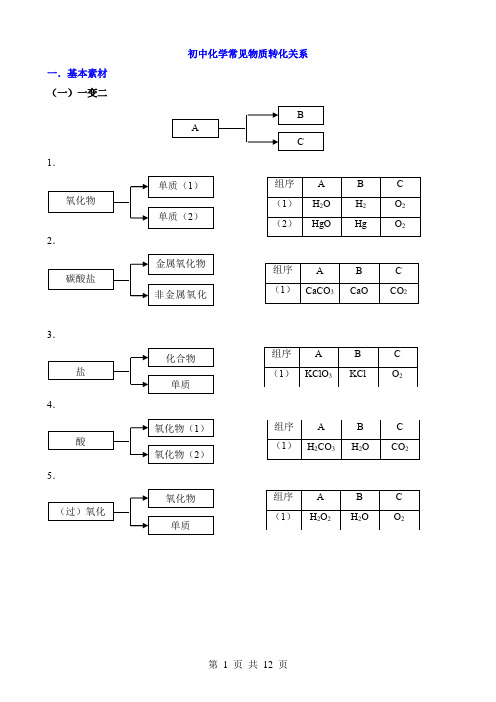
初中化学常见物质转化关系
初中化学常见物质转化关系
一.基本素材 (一)一变二
1.
2.
3.
4.
5.
1.
2.
3.
4.
1.置换类
2.还原类
3.氧化类
4.氧化物、酸碱盐类
二.特定素材 (一)直线型互变
1.直线型“两点”互变(含同元素)
(1) (2
) (3)
(4)
(5) (6)
(7)
(8)
2.直线型“三点”互变
(1 (2
(3
(4
三.试题常用框图素材 (一)同元素变化 1.循环类三角形变化
2.指向类三角形变化
3.指向返回类三角型变化
4.循环返回类三角型变化
(二)异元素变化 指向型三角形变化
(三)四边形类变化 1.殊途同归
2. 循环
(四)杂类 1.一变三
2.“二”变“三”
3.二变三
四.六个“核心”变化
O 2、H 2 、H 2O 、CO 2、CO 和Na 2CO 3等六种物质,在中考推断题中是不可缺少的命题“元素”,相关变化列举如下。
(一).二氧化碳的变化
(二).水的变化
(三).氧气的变化
(四).一氧化碳的变化
(五).氢气的变化
(六).碳酸钠的变化。
初中化学物质的相互转化规律 PPT课件 图文

下册共五个单元
第八单元 金属和金属材料 ——化学基础知识与运用
第九单元 溶液 第十单元 酸和碱 第十一单元 盐 化肥 ——化学规律与应用
第十二单元 化学与生活 ——化学与社会
第 一 单
走元 进 化
学 世 界
第 二 单 我元 们 周
围 的 空
气
第 三 单
H2SO3 → SO2
酸 → 酸性氧化物
完成下列化学方程式:
6、 Na + Cl2 — 金属 + 非金属 → 盐
7、 NaOH + HCl — Cu(OH)2+H2SO4— Ca(OH)2+HNO3— Fe(OH)3+HCl — 碱 + 酸 → 盐+水
8、 NaCl+AgNO3 — BaCl2+Na2SO4 — 盐+盐 → 盐+盐
金属+盐→ 盐+金属
盐+金属
盐+氢气
盐+碱
盐+酸
上册共七个单元
第一单元 走进化学世界 ——入门篇
第二单元 我们周围的空气 第三单元 自然界的水 ——认识身边的物质
第四单元 物质构成的奥秘 ——深入微观世界
第五单元 化学方程式 ——基本概念和技能
第六单元 碳和碳的氧化物 ——初中研究最细致的元素
初中化学新教材分析
34
第 十 二 单 化元 学 与 生 活
初中化学新教材分析
35
THAK YOU!
谢谢! 学妹给我打电话,说她又换工作了,这次是销售。电话里,她絮絮叨叨说着一年多来工作上的不如意,她说工作一点都不开心,找不到半点成就感。 末了,她问我:学姐,为什么想 找一
(完整版)各类有机物的转化关系图
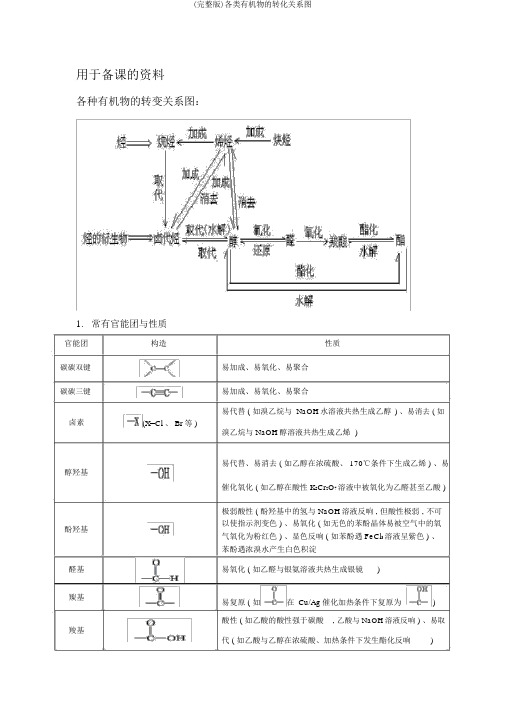
用于备课的资料各种有机物的转变关系图:1.常有官能团与性质官能团碳碳双键碳碳三键卤素醇羟基酚羟基醛基羰基羧基构造性质易加成、易氧化、易聚合易加成、易氧化、易聚合易代替 ( 如溴乙烷与 NaOH水溶液共热生成乙醇) 、易消去 ( 如(X=Cl 、 Br等 )溴乙烷与 NaOH醇溶液共热生成乙烯)易代替、易消去 ( 如乙醇在浓硫酸、 170℃条件下生成乙烯 ) 、易催化氧化 ( 如乙醇在酸性 K2Cr2O7溶液中被氧化为乙醛甚至乙酸 )极弱酸性 ( 酚羟基中的氢与 NaOH溶液反响 , 但酸性极弱 , 不可以使指示剂变色 ) 、易氧化 ( 如无色的苯酚晶体易被空气中的氧气氧化为粉红色 ) 、显色反响 ( 如苯酚遇 FeCl3溶液呈紫色 ) 、苯酚遇浓溴水产生白色积淀易氧化 ( 如乙醛与银氨溶液共热生成银镜)易复原 ( 如在Cu/Ag催化加热条件下复原为)酸性 ( 如乙酸的酸性强于碳酸, 乙酸与 NaOH溶液反响 ) 、易取代 ( 如乙酸与乙醇在浓硫酸、加热条件下发生酯化反响)易水解 ( 如乙酸乙酯在稀硫酸、加热条件下发生酸性水解, 酯基乙酸乙酯在 NaOH溶液、加热条件下发生碱性水解 )烷氧基如环氧乙烷在酸催化下与水一同加热生成乙二醇硝基复原 ( 如酸性条件下 , 硝基苯在铁粉催化下复原为苯胺) 2.有机反响种类与重要的有机反响反响种类重要的有机反响代替反响代替反响反响种类加成反响烷烃的卤代 :CH4+Cl 2CH3Cl+HCl烯烃的卤代 :卤代烃的水解 :CH3CH2Br+NaOH CH3CH2OH+NaBr皂化反响 :+3NaOH3C17H35COONa+酯化反响 : +CH OH +H O2 5 2糖类的水解 :C12H22O11+HOC6H12O6+C6H12O6蔗糖果糖葡萄糖2二肽的水解 :+H2O苯环上的卤代 :+Cl 2+HCl苯环上的硝化 :++H2O苯环上的磺化 :++H2O( 续表 )重要的有机反响烯烃的加成 :+HCl炔烃的加成 :+H2O苯环的加氢 :+3H2醇分子内脱水生成烯烃:C 2H5OH+H2O消去反响卤代烃脱 HX生成烯烃 :CH3CH2Br+NaOH+NaBr+H2O 单烯烃的加聚 :n加聚反响缩聚反响缩聚反响共轭二烯烃的加聚:( 别的 , 需要记着丁苯橡胶、氯丁橡胶的单体 )二元醇与二元酸之间的缩聚:n+nHOCH2CH2OH+2nH2O羟基酸之间的缩聚:+nH2 O氨基酸之间的缩聚:苯酚与 HCHO的缩聚 :n+nHCHO+nH2O氧化催化氧化 :2CH3 CH2OH+O22CH3CHO+2HO反响醛基与银氨溶液的反响:CH3CHO+2[Ag(NH3) 2 ]OH CH3COONH4+2Ag↓+3NH+H2O(注意配平 )醛基与新制氢氧化铜的反响:CH3CHO+2Cu(OH)+NaOH CH3COONa+Cu2↓ +3H2O醛基加氢 :CH3CHO+H2CH3CH2OH复原反响硝基复原为氨基:。
初中化学物质转化关系图
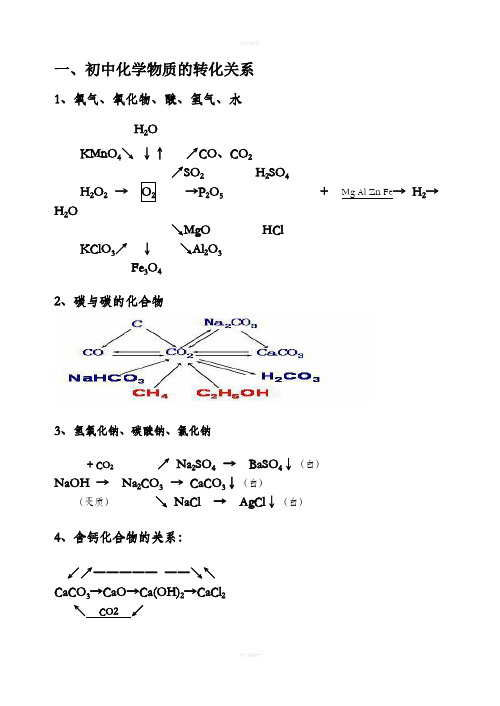
↗ Na2SO4 → BaSO4↓(白)
NaOH → Na2CO3 → CaCO3↓(白)
(变质)
↘ NaCl → AgCl↓(白)
4、含钙化合物的关系:
↙↗――――― ――↘↖ CaCO3→CaO→Ca(OH)2→CaCl2
↖ CO2 ↙
-可编辑-
精品教育
5、氧化钡、氢氧化钡与硫酸钡
↗BaCl2 → BaSO4↓(白)
精品教育
一、初中化学物质的转化关系
1、氧气、氧化物、酸、氢气、水
H2O
KMnO4↘ ↓↑ ↗CO、CO2
↗SO2
H2Sቤተ መጻሕፍቲ ባይዱ4
H2O2 → O2
→P2O5
H2O
↘MgO
HCl
KClO3↗ ↓ Fe3O4
↘Al2O3
2、碳与碳的化合物
+ Mg Al Zn Fe→ H2→
3、氢氧化钠、碳酸钠、氯化钠
+ CO2
BaO → Ba(OH)2
↗
↘ + CuSO4
↘Cu(OH)2↓(蓝)
6、硫酸铜、碳酸氢钙、碳酸氢钠、碳酸氢铵
CuO ↙↘ CuSO4.5H2O→CuSO4→ Cu
↗ CO2 Ca(HCO3)2 → CaCO3→CaO
↘ H2O
↗Na2CO3 NaHCO3 →CO2
↘H2O →
H2CO3
↗ NH3 → NH3.H2O NH4HCO3 → H2O
-可编辑-
精品教育
Fe Al
↙ FeCl3 ↖
Fe(OH)3
Fe2O3
↖Fe2(SO4)3↙
C CO H2 Mg Al
←――――→
O2 H2O
物质转化关系图

物质转化关系图1.氯及其化合物2.硫及其重要化合物3.氮气其重要化合物4.碳及其重要化合物5.硅及其重要化合物6.钠及其化合物7.镁及其化合物8.铝及其重要化合物9.铁及其重要化合物10.有关O2、H2、H2O、H2O2的转化关系。
11.磷及其重要化合物有关氯元素的转化关系NaClOHClOCl2HClNaClCuCl2FeCl3Ca(ClO)2AgClH2NaOHCuFeAgAgNO3AgNO3AgNO3H20NaOHCa(OH)2HClH2O光照S SO 2Na2SO3Na2SO4H2SO4SO 3H2SO3O2O2H2H2CuHClO3NaOH NaOH Na2SO3NH3N2NO NO2HNO3 NH4HCO3NH3.H2O4放电O2H2H2O2Ca(OH)2HCl△H2ONaOHCuCuO23.碳及其重要化合物硅及其重要化合物4.钠及其化合物NaNa2O2NaOH Na2CO3NaHCO3NaClNa2OSi SiO2Na2SiO3H2SiO3CaSiO3SiF4CO2CaCO3HFNaOH HClH2SiCl4Cl2镁及其化合物铝及其化合物MgMgCl2MgOMgCO3Mg(HCO3)2Mg(OH)2Mg2N3Cl2 HCl CuCl2HCl电解熔态O2 CO2(点燃)加水水解N2(点燃)H2O(反应慢)加热高温H2O+CO21、水中煮沸Al Al(OH)3NaAlO2Al23AlCl3O2△HClNaOHHClNaOHHClNaOH5.铁及其化合物10.有关O2、H2、H2O、H2O2的转化关系。
11.磷及其重要化合物HClHClO2H2OFeFe3O4FeOFe2O3FeCl2FeCl3Fe(OH)2Fe(OH)3Cl2Fe△HClNaOHH2O O2HCl。
最新整理初中化学物质转化关系图教学内容

一、初中化学物质的转化关系1、氧气、氧化物、酸、氢气、水H2OKMnO4↘↓↑↗CO、CO2↗SO2H2SO4H2O2→→P2O5+ Mg Al Zn Fe→ H2→H2O ↘MgO HClKClO3↗↓↘Al2O3 Fe3O42、碳与碳的化合物3、氢氧化钠、碳酸钠、氯化钠+ CO2↗ Na2SO4 → BaSO4↓(白)NaOH → Na2CO3 → CaCO3↓(白)(变质)↘ NaCl → AgCl↓(白)4、含钙化合物的关系:↙↗―――――――↘↖CaCO3→CaO→Ca(OH)2→CaCl2↖CO2↙5、氧化钡、氢氧化钡与硫酸钡↗BaCl2→ BaSO4↓(白)精品文档精品文档 BaO → Ba(OH)2 ↗↘ + CuS O 4↘Cu(OH)2↓(蓝)6、硫酸铜、碳酸氢钙、碳酸氢钠、碳酸氢铵CuO ↗ CO 2↙ ↘ Ca(HCO 3)2 → CaCO 3→CaOCuSO 4.5H 2O →CuSO 4→ Cu ↘ H 2O↗Na 2CO 3 ↗ NH 3 → NH 3.H 2O NaHCO 3 →CO 2 NH 4HCO 3 → H 2O↘H 2O → H 2CO 3 ↘ CO 2 → H 2CO 37、铝、镁、锌、铁、铜及其化合物↗ZnSO 4↖ ↗ AlCl 3↖Zn → ZnO Al → Al 2O 3 ↘ZnCl 2↙ ↘Al 2(SO 4)3↙Fe Al↗MgCl 2↖ ↙﹉﹉﹉﹉↗ CuCl 2↘↖Mg → MgO Cu ←→CuO Cu(OH)2 ↘MgSO 4↙ ↖____↘ CuSO 4↗↙ Fe Al↙ FeCl 3 ↖ C CO H 2 Mg Al ↗FeSO 4Fe(OH)3 Fe 2O 3 ←――――→ Fe↖Fe 2(SO 4)3↙ O 2 H 2O ↘ FeCl 2 8、常见物质的相互转化关系(即注明必要的反应物、反应条件)CO 2 CO C 或O 2 O 2 H 2O H 2O 2Al 2O 3 AlCl 3 Al CuO CuSO 4 Cu ⑴ ⑵ ⑶ ⑷ MgO MgSO 4 Mg Cu H 2 Fe CaO Ca(OH)2 CaCO 3 CaCl 2 Ca(OH)2 CaCO 3 ⑸ ⑹ ⑺ ⑻ CaCO 3 Na 2CO 3 CO 2 CO 2 NaOH Na 2CO 3 2 NaOH NH ClNH 3精品文档。
