第十五章杂环化合物祥解
合集下载
第十五章-杂环类药物的分析课件

样品:异烟肼+游离肼+对二 甲氨基苯甲醛
测定,对照法定量
.
41
456
.
42
.
43
测定方法:
对照品溶液制备与测定 精密称取
硫酸肼0。2031g,相当于游离肼
50mg,制成1ug/ml的肼标准液。
取50ml量瓶2个,各加肼标准液
5ml。其中一个加对-二甲氨基苯
甲醛试液20ml,
.
44
对-二甲氨基苯甲醛试液的制备: 取20g,加相对密度为1。18的盐 酸172。5ml,用水稀释至 1000ml,即得。
绿奎宁反应的基本机制。
.
61
.
62
硫酸奎宁和硫酸奎尼丁的绿奎宁 反应机制同上,取其水溶液,加溴试 液2一3滴和氨试液lml,即显翠绿色; 加酸成中性变成蓝色;酸性则呈紫红 色。翠绿色可转溶于醇、氯仿中而不 溶于醚。因此中国药典采用此反应鉴 别硫酸奎宁和奎尼丁。
.
63
鉴别方法:取本品约20mg,加水20m1 溶解后,分取溶液5m1,加溴试液3滴 与氨试液1 ml,即显翠绿色。
含 20 g 的溶液,照分光光度法(附录ⅣA)
测定,在 291 nm 的波长处有最大吸收,吸收
度约为0.78。
.
33
三、有关物质检查
(一)异烟肼中游离肼的检查 异烟肼不甚稳定,游离肼是诱变 剂与致癌物,由原料引入或贮藏 过程的降解。
.
34
薄层色谱法(TLC)(1) ChP
(2000)杂质对照品法
.
45
以对-二甲氨基苯甲醛试液的水
溶液为参比,在456nm处测吸
光度。
另一瓶加丙酮,以含有3%丙酮
的对-二甲氨基苯甲醛试液为参
测定,对照法定量
.
41
456
.
42
.
43
测定方法:
对照品溶液制备与测定 精密称取
硫酸肼0。2031g,相当于游离肼
50mg,制成1ug/ml的肼标准液。
取50ml量瓶2个,各加肼标准液
5ml。其中一个加对-二甲氨基苯
甲醛试液20ml,
.
44
对-二甲氨基苯甲醛试液的制备: 取20g,加相对密度为1。18的盐 酸172。5ml,用水稀释至 1000ml,即得。
绿奎宁反应的基本机制。
.
61
.
62
硫酸奎宁和硫酸奎尼丁的绿奎宁 反应机制同上,取其水溶液,加溴试 液2一3滴和氨试液lml,即显翠绿色; 加酸成中性变成蓝色;酸性则呈紫红 色。翠绿色可转溶于醇、氯仿中而不 溶于醚。因此中国药典采用此反应鉴 别硫酸奎宁和奎尼丁。
.
63
鉴别方法:取本品约20mg,加水20m1 溶解后,分取溶液5m1,加溴试液3滴 与氨试液1 ml,即显翠绿色。
含 20 g 的溶液,照分光光度法(附录ⅣA)
测定,在 291 nm 的波长处有最大吸收,吸收
度约为0.78。
.
33
三、有关物质检查
(一)异烟肼中游离肼的检查 异烟肼不甚稳定,游离肼是诱变 剂与致癌物,由原料引入或贮藏 过程的降解。
.
34
薄层色谱法(TLC)(1) ChP
(2000)杂质对照品法
.
45
以对-二甲氨基苯甲醛试液的水
溶液为参比,在456nm处测吸
光度。
另一瓶加丙酮,以含有3%丙酮
的对-二甲氨基苯甲醛试液为参
有机化学第十五章 杂环化合物

+
N
N
NO 2
N
N S O 3H
Br
B r2/H 2 S O 4
H+
+
N
N
B r 2 /CCl 4
OH -
Br Br
N
K MnO 4 /H +
CO 2 H
N
CO 2 H
H 2/P t N H
易发生亲电取代和氧化
5
8
N
易发生亲核取代和还原3
N +C3 H I
N
+ N C3 H I N
N
Br
+Br2 NH 2 N
1、亲电取代——困难:发生在β 位
混 酸 P hH室 温 P hN2O
混 酸
N2O
3 0 0 ℃ /1 天
N
N
H2SO4/H+g
220℃
N
N
SO3H
C3H N
H 2SO 4/K N3 O
100℃
C3H
C3H N
N2 O C3H
Br2/HcA Br NH 2 N
N—氧化物 δ+
NH 2 N
δ+
N
N+
吡唑和咪唑的分子聚合和互变异构:
b.p
水溶性
N
188
N
H N 263
N H
11 易溶
N
N
H
H
N
N
二聚体
N HN
N HN
N N
H
多聚体
嘌呤
N
N
N
NH
N
N
H 9—H
NH2
N
芳香杂环化合物

CH3
CH3
R'=(CH3)2CHCH2CH2(CH2CHCH2CH2)CH2C=C CH2
伊沙匹隆
OR
S
H3C
N
CH3 HO
H3C
OH
H3C CH3
CH3
O OH O
Epothilone A(R=H) ;B(R=CH3)
1993年被发现的一种高效抗癌物质
第一节 分类和命名
一 分类
杂环
单杂环
稠杂环
N
1
嘧啶
pyrimidine
3.若有多个不同杂原子时,则按O、S、 NH、N的先后顺序编号
43
5 1 N2 N H
4 N3
5
2
S
1
吡唑 pyrazole
噻唑 thiazole
4.有些有特定名称的稠杂环母体的编号 是固定的
5 6
7 8
4 3
2
N
1
67
1N 5 N
2
98
N4
3
N
H
喹啉
quinoline
5 氧化和还原
和苯环相比,不易被氧化,优先被还原
吡啶N-氧化物
在过氧化物条件下生成
亲电取代反应比较容易,也能进行亲核取代
反应,并且取代反应都发生在a位或γ位。
? 衍生物
二 喹啉和异喹啉
喹啉
异喹啉
奎宁(金鸡钠碱),是最早,也是最重 要的抗疟药物,至今仍广泛用于临床。
化学性质
1 亲电取代 主要发生在C-5与C-8
N O
异噁唑
isoxazole
六元环
4
5
3
6N 2
1
吡啶
十五章杂环化合物

N原子 sp2杂化
p sp2
H
H
H
O
H 呋喃
H
H
H
S
H 噻吩
p电子数 = 4n+2规则
H
H
H
NH
H 吡咯
• 五个原子含有六个π电子,富电子芳杂环, • 芳香稳定性不如苯环 • 亲电取代反应比苯
3.化学反应
比苯容易发生亲电取代反应 主要进入 α-位 活性:吡咯 > 呋喃 > 噻吩 >> 苯
1)卤代反应:
环状封闭的大π键,π电子数为6,符合4n+2规则 吡啶具有一定的芳香性
2.吡啶的 化学性质 (1)碱性 与质子酸成盐
+ HCl N
吡啶与路易斯酸作用,形成盐
N Cl 或 H 吡啶盐酸盐
HCl N
+ SO3 N
+ CrO3 N
N
( SO 3 )
N-磺酸吡啶
N
(一种温和的非质子性磺化试剂)
SO3
Cl2
O
-40℃
Br2 , 室温
S
AcOH
O Cl + Cl O Cl
S Br
78%
II
I2 , KI 或 HgO
N
IN I
H
H
2)硝化反应:
OO CH3COCCH3
+ HNO3
-5℃以下
O CH3CONO2 + CH3COOH
CH3COO-NO2+
O
-5~ -30℃
CH3COO-NO2+
S
Ac2O , -10℃
O CHO
Ag(NH3)2+
CH3COONa (CH3CO)2O
p sp2
H
H
H
O
H 呋喃
H
H
H
S
H 噻吩
p电子数 = 4n+2规则
H
H
H
NH
H 吡咯
• 五个原子含有六个π电子,富电子芳杂环, • 芳香稳定性不如苯环 • 亲电取代反应比苯
3.化学反应
比苯容易发生亲电取代反应 主要进入 α-位 活性:吡咯 > 呋喃 > 噻吩 >> 苯
1)卤代反应:
环状封闭的大π键,π电子数为6,符合4n+2规则 吡啶具有一定的芳香性
2.吡啶的 化学性质 (1)碱性 与质子酸成盐
+ HCl N
吡啶与路易斯酸作用,形成盐
N Cl 或 H 吡啶盐酸盐
HCl N
+ SO3 N
+ CrO3 N
N
( SO 3 )
N-磺酸吡啶
N
(一种温和的非质子性磺化试剂)
SO3
Cl2
O
-40℃
Br2 , 室温
S
AcOH
O Cl + Cl O Cl
S Br
78%
II
I2 , KI 或 HgO
N
IN I
H
H
2)硝化反应:
OO CH3COCCH3
+ HNO3
-5℃以下
O CH3CONO2 + CH3COOH
CH3COO-NO2+
O
-5~ -30℃
CH3COO-NO2+
S
Ac2O , -10℃
O CHO
Ag(NH3)2+
CH3COONa (CH3CO)2O
第十五章+杂环化合物
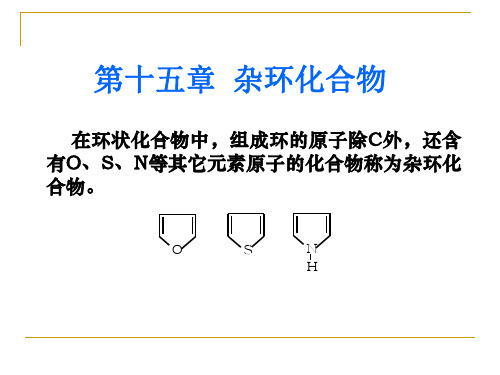
号时,把连有氢原子的杂原子编号为 , 号时,把连有氢原子的杂原子编号为1,并使其余 杂原子的位次尽可能小 。
CH3
4
N3
N 2 1
4 –甲基咪唑 甲基咪唑
(3)如果环上有多个不同杂原子时,按氧、硫、 )如果环上有多个不同杂原子时,按氧、
氮的顺序编号
H 3 C
4
N
3
H 3 C
5
S
1
2
4,5–二甲基噻唑 二甲基噻唑
+
H2 O
吡啶的硝化反应需在浓酸和高温下才能进行, 吡啶的硝化反应需在浓酸和高温下才能进行,硝基 主要进β-位 主要进 位。
(3)磺化反应 )
+
O N
+ SO 3
C2H4Cl2 室温三天 O SO 3H
+
N
+
N H
N
+
SO3Biblioteka -C2H4Cl2100 ℃
N H
SO3H
+
N
吡咯,呋喃对酸很敏感,强酸能使它们开环聚合, 吡咯 呋喃对酸很敏感,强酸能使它们开环聚合,常用温和的非质子 呋喃对酸很敏感 磺化试剂:吡啶与SO 的加成物。 磺化试剂:吡啶与 3的加成物。
4
N3
4 5
N3 S1
2
O
S
N H
5
N1
2
呋喃 噻吩 吡咯 (furan) (thiophene) (pyrrole)
咪唑 (imidazole)
H
噻唑 (thiazole)
4 5
N3 N1
2
O
吡喃 (pyran)
6
N
吡啶 (pyridine)
杂环化合物
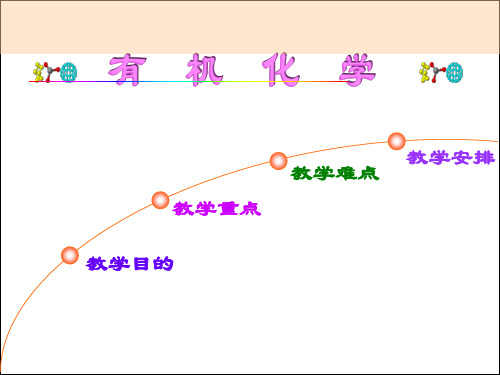
COOH
△
N
N
② 吡啶与过氧酸作用,生成N-氧化吡啶。
+ N
H2O2
CH 3COOH
65oC
N+
O-
吡啶N-氧化物易发生亲电取代和亲核取代反应,
且都发生在2或4位。
NO 2
HNO 3 H2SO4
N+
O-
90oC
亲电取代
+
N
O-
PCl 3
NO 2
N
NH2 H2 / Ni
或 Fe / H + N
( 1 ) PhMgBr
(二)杂环母核的编号
1、含一个杂原子的单杂环 从杂原子开始编号并兼顾取代基。
1
H
N
5
2
43
1H-pyrrole
吡咯
1
O
52 43
furan
呋喃
1
6 N 2α
5 4
3β
COOH
3-吡啶甲酸 β-吡啶甲酸
1
S
52 43
thiophene
噻吩
1 6N2 53
4
pyridine
吡啶
1 6O2 53
4
4H-pyran
isoxazole
异噁唑
1
S
52 4 N3
1,3-thiazole
噻唑
4、有特定音译名称的稠杂环
(1)一般按相应芳环的编号方式编号
7 1H
6
N
2
5 4
3
吲哚
54
6
3
7
N2
81
喹啉
5 6
7 8
4 3
N2 1
有机化学第十五章杂环化合物

第十五章 杂环化合物 糠醛经催化加氢转化为四氢糠醇,具有醇和醚的性 质,是优良的溶剂。
糠醛用KMnO4的碱溶液或用Cu或Ag的氧化物为催化 剂,用空气氧化生成糠酸。
糠醛作为溶剂,可选择性地从石油、植物油中萃取其中的 不饱和组分和含硫化合物。如从润滑油中萃取芳香烃等以精致 润滑油。在合成橡胶工业中用于提纯丁二烯和异戊二烯。
第十五章 杂环化合物 六元单杂环吡啶的结构与苯环很相似,氮原子与碳原子 处在同一平面上,原子间是以sp2杂化轨道相互交盖形成六个 σ键,键角为120°。环上每一原子还有一个电子在p轨道上, p轨道与环平面垂直,相互交盖形成包括六个原子在内的分 子轨道。π电子分布在环的上方和下方。每个碳原子的第三 个sp2杂化轨道与氢原子的s轨道交盖形成σ键。氮原子的第三 个sp2杂化轨道上有一对未共用电子对。 由于这些杂环化合物都是闭合的 共轭体系,所以环中的单、双键都不 同程度地趋向平均化,单键比普通单 键短,双键比普通双键长。
第十五章 杂环化合物 教学指导 杂环化合物的分类和命名法 杂环化合物的结构 杂环化合物的性质
第十五章 杂环化合物 教学目的: 了解一些常见的重要杂环化合物物理和化学性质; 熟悉杂环化合物命名规则; 掌握呋喃、吡咯及其衍生物的物理和化学性质。 教学难点:
杂环化合物命名规则;
呋喃、吡咯及其衍生物的物理和化学性质。 教学重点: 呋喃、吡咯及其衍生物的物理和化学性质。
第十五章 杂环化合物 2.吡咯及其衍生物 吡咯与呋喃相似,亲电取代也必须在缓和的条件下 进行,在酸性条件下同样极易发生开环、聚合反应。 溴化:
第十五章 杂环化合物 根据环数的多少分为单杂环和多杂环;单杂环又可根据 成环原子数的多少分为五元杂环及六元杂环等;多杂环可分 为稠杂环、桥杂环及螺杂环,其中以稠杂环较为常见。
第15章 杂环化合物

54
6
3
7
N2
81
异喹啉
isoquinoline
[命名] 音译名
(Imidazole)
H N
( Thiophene)
O
S
S
H
H
N
NN
N
N
吡咯 呋喃
(Pyrrole)(Furan)
噻吩 噻唑 咪唑 吡唑
( Thiazole)
(Pyrazole)
N N
N
吡啶Pyridine
喹啉Quinoline
异喹啉Isoquinoline
CH3COONO2
O
- 5~30oC
O NO2
(35%)
CH3COONO2
N H
OH-,5oC,Ac2O
N NO2 + H (83%)
NO2
N H
(7%)
当呋喃或吡咯环上连有吸电子基团时,环的稳定性
增 加,可用一般方法硝化。
O2N
N H
CCH3 O
HNO3 H2SO4
O2N
N H
CCH3 + O
N H
吡啶N
P
N
SP2
N 吡咯N
P
H
SP2
C
呋喃O(噻吩S)
P
P
SP2
SP2
“多π”芳杂环———六个电子由五个原子分配,每个碳 原子的电子云密度比苯环高,故亲电取代比苯容易。
H
O
S
N
2.33 10-30C.m 1.70 10-30C.m 6.03 10-30C.m
N原子
给电子共轭>> 吸电子诱导。
吡啶N:吸电子诱导+吸电子共轭
第十五章-杂环化合物

• 吡咯和噻酚发生正常亲电取代反应
AcONO2
N
Ac2O, oC
H
AcONO2
S
Ac2O-AcOH, 0oC
N
NO2 +
H
83%
S
NO2 +
60%
NO2
N H 17%
NO2
S 10%
• 呋喃发生加成反应(共轭烯烃性质)
AcONO2
O
5 ~ 30oC
AcO O NO2
加成
碱或 HOAc
消除
O NO2
10-羟基喜树碱 (抗癌药) HO O
SS
H2O
SS
TTF
HgOH
NaO
O
O
Br 红汞
Br CO2Na
Br
NaO
O
O
Br
曙红 (红墨水)
Br CO2Na
杂环化合物的类型
芳香杂环
N
O
S
重点内容
N
N
H
H
N
N
N
N
N
N
N H
N
普通杂环
O
环醚,内酯,内 O
O
酰胺,环状酸酐
N OO OO O H
§15.1 杂环化合物的分类、命名
AE
位取代
E+
A
E A
E H
H+
A
中间体只有二个主要共振式, 中间体较不稳定
E A
对亲电取代反应活性的解释
i. 由五员杂环的结构分析 杂原子起给电子基的作用,环上的电荷密度比苯环大
ii. 由中间体的稳定性分析
E+
A
AcONO2
N
Ac2O, oC
H
AcONO2
S
Ac2O-AcOH, 0oC
N
NO2 +
H
83%
S
NO2 +
60%
NO2
N H 17%
NO2
S 10%
• 呋喃发生加成反应(共轭烯烃性质)
AcONO2
O
5 ~ 30oC
AcO O NO2
加成
碱或 HOAc
消除
O NO2
10-羟基喜树碱 (抗癌药) HO O
SS
H2O
SS
TTF
HgOH
NaO
O
O
Br 红汞
Br CO2Na
Br
NaO
O
O
Br
曙红 (红墨水)
Br CO2Na
杂环化合物的类型
芳香杂环
N
O
S
重点内容
N
N
H
H
N
N
N
N
N
N
N H
N
普通杂环
O
环醚,内酯,内 O
O
酰胺,环状酸酐
N OO OO O H
§15.1 杂环化合物的分类、命名
AE
位取代
E+
A
E A
E H
H+
A
中间体只有二个主要共振式, 中间体较不稳定
E A
对亲电取代反应活性的解释
i. 由五员杂环的结构分析 杂原子起给电子基的作用,环上的电荷密度比苯环大
ii. 由中间体的稳定性分析
E+
A
第十五章杂环化合物

虽与苯相似,但C-N键变化很大,因此,其芳香性也比苯差。
10
吡啶和苯虽然都属等电子体系,但因氮原子的电负性较 大,从而使环上的电子云密度降低 ,故其亲电取代反应性能 不但比苯差,且亲电取代反应发生在电子云密度较高的β-位。 这一特性很类似于硝基苯。
综上所述,五元、六元杂环化合物虽然都具有芳香性, 但其环上的电子云的密度是不同的,其电子云密度由高到 低的顺序是:
此外,根据环上各键的键长并不相等,说明杂环中的电子密 度没有完全平均化芳香性弱于苯环。其电子密度的变化情况类似
7
于苯胺。
2、缺电子体系—六元杂环 A. 吡啶是典型的六元杂环化合物,环原子以sp2方式杂化。 B. 每个原子的未参加杂化p轨道上均只有一个单电子,组成 大Π键,符合4n+2休克尔规则,六元杂环化合物同样具有 芳香性。
B r2/C H 3C O O H
S
00C
S Br
15
D. Friedel-Crafts反应 主要是酰基化反应,烷基化反应得到混合物。
结论:五元杂环化合物的亲电取代反应活性高,所以,
一般选用弱的亲电试剂、在低温条件下、采用溶剂稀释
时反应,以防止五元杂环化合物氧化或聚合。
16
2、加成反应 A. 亲双烯加成反应 (了解内容)
8
二、杂环化合物的芳香性 具有闭合环结构,具有环多烯结构,具有共平面或近似平
面结构,π电子数符合4n+2规则。符合休克尔规则,因此具有 芳香性。 具有芳香性的杂环与苯环的异同点 1、五元杂环化合物
(1) 由此可见,苯分子中的键长完全平均化,而五元杂环化合 物分子中的键长只是有一定程度的平均化。因此,五元杂环化 合物的芳香性比苯差。其芳香性次序是:
康尼查罗反应
10
吡啶和苯虽然都属等电子体系,但因氮原子的电负性较 大,从而使环上的电子云密度降低 ,故其亲电取代反应性能 不但比苯差,且亲电取代反应发生在电子云密度较高的β-位。 这一特性很类似于硝基苯。
综上所述,五元、六元杂环化合物虽然都具有芳香性, 但其环上的电子云的密度是不同的,其电子云密度由高到 低的顺序是:
此外,根据环上各键的键长并不相等,说明杂环中的电子密 度没有完全平均化芳香性弱于苯环。其电子密度的变化情况类似
7
于苯胺。
2、缺电子体系—六元杂环 A. 吡啶是典型的六元杂环化合物,环原子以sp2方式杂化。 B. 每个原子的未参加杂化p轨道上均只有一个单电子,组成 大Π键,符合4n+2休克尔规则,六元杂环化合物同样具有 芳香性。
B r2/C H 3C O O H
S
00C
S Br
15
D. Friedel-Crafts反应 主要是酰基化反应,烷基化反应得到混合物。
结论:五元杂环化合物的亲电取代反应活性高,所以,
一般选用弱的亲电试剂、在低温条件下、采用溶剂稀释
时反应,以防止五元杂环化合物氧化或聚合。
16
2、加成反应 A. 亲双烯加成反应 (了解内容)
8
二、杂环化合物的芳香性 具有闭合环结构,具有环多烯结构,具有共平面或近似平
面结构,π电子数符合4n+2规则。符合休克尔规则,因此具有 芳香性。 具有芳香性的杂环与苯环的异同点 1、五元杂环化合物
(1) 由此可见,苯分子中的键长完全平均化,而五元杂环化合 物分子中的键长只是有一定程度的平均化。因此,五元杂环化 合物的芳香性比苯差。其芳香性次序是:
康尼查罗反应
有机化学第15章

(抗癌药) HO O
SS
H2O
SS
TTF
HgOH
NaO
O
O
Br 红汞
Br CO2Na
Br
NaO
O
O
Br 曙红 (红墨水)
Br CO2Na
杂环化合物的类型
芳香杂环
N
O
S
N H
N H
H
NN
N
N
N
N
N
N
普通杂环
O
O
O
N
OO O
O
H
环醚,内酰胺,环状酸酐,内酯等
OO
§15.1 杂环化合物的分类、命名
杂环分类:
+
S
(Hale Waihona Puke 量) 反应快H2SO4 r. t.
S SO3H 溶解于硫酸中
(3)五员芳杂环的Friedel-Crafts反应
(CH3CO)2O
N H
(CH3CO)2O
O
BF3
(CH3CO)2O
S
SnCl4
COCH3 N H
2-乙酰基吡咯
COCH3 O
2-乙酰基呋喃
COCH3 S
2-乙酰基噻吩
2)五员芳杂环的加成反应
H3C 4
3
N
5
2
N1
H
4-甲基咪唑
10
3. 含两个不同的杂原子:按O, S, N顺
3
N
4 序编号
2 S 5 CH3 5-甲基噻唑
1
4. 特殊编号
5 6
4 3
7
2
N
8
1
喹啉
Quinoline
5 6
第十五章 杂环

第十五章 杂环化合物—五元环性质
O B r2 O 0℃ 8 0% O C l2 - 4 0℃ O C H3 C O O N O 2 O Cl Br
+
Cl O Δ or Py O N O2 Cl
H - 5 ℃ - 3 0℃ C H C O O 2
-
H O N O2 H Cl
N
+
S O3 O S O3 -
O
S O3 H
( C H3 C O )2 O 0℃ B F3 E t2 O O C O C H3
第十五章 杂环化合物—五元环性质
Br 2 Cl 2 CH 3 COOH r, t 50 ℃ 36% S CH 3 COONO 2 S 95%H 2 SO 4 ( CH 3 CO) 2 O H 3 PO 4 25 ℃ S S -10 ℃ S 78% S Br + Cl Cl Cl + Cl Cl S 14% NO 2 + 70% S 67-76% S Cl 13% Cl NO 2 5%
第十五章 杂环化合物—概述 2、理论意义: 杂环化学中贯穿了大量的电子理论,是验证 电子学说和其它有关理论的园地 3、研究现状: (1)教学方面:作为选修课。 (2)研究方面: 杂环化学的研究目前主要集中在其生理活性 及其药用价值。此外,在非生物领域的应 用研究也取得很大进展,如:胶片的敏化 剂、橡胶工业的抗氧剂、硫化促进剂等, 多性能催化作用以及一些特殊性能的研究 都取得很大进展。
第十五章 杂环化合物—五元环性质 §15.3五元杂环化合物 一、呋喃、噻吩、吡咯的结构 成键特性:
第十五章 杂环化合物—五元环性质
分子 苯 噻吩
S
吡咯
N H
呋喃
O
第十五章 杂环化合物

+ H2SO4 S S SO3H
+ H2O
溶于酸
应用于除去石油和粗苯中的噻吩
6、吡咯的弱酸性
+ KOH N N K + H2O
吡咯钾
参与共轭
H
四氢吡咯的碱性明显大于吡咯,存在于脯氨酸中,P520
1) CO2
2-吡咯甲酸
N Na
类似苯酚钠
2) H3O+
N H
COOH
N H
+
N2Cl
pH=7-9
N H
N
N H
e. 重要衍生物 (P359)维生素PP和NAD+ , 维生素B6
COOH N
(2) 嘧啶
6 N N
CH N 尿嘧啶(Uracil) CH N OH
1
N 2 N 3
5
7 N 8
嘧啶
NH 2 N
4
N 9
嘌呤
OH N OH N CH 3 胸腺嘧啶
胞嘧啶(cytosine) N
烯醇式可重排为酮式
2-甲基-5-硝基吲哚(P352)
CH 2COOH N H 3-吲哚乙酸是植物生长调节剂
(P352 照书讲)
CH2CHCOOH CH2CH2NH2 N H 色胺
N H
NH2 色氨酸
是哺乳动物脑组织中与 中枢神经有关的物质。
HO CH 2CH 2NH 2 N H
5-羟色胺
吲哚环存在于1000多各生物碱天然产物中。
1. 咪唑
(1) 结构P521 弱酸
H N
H N
N原子sp2杂化
N N H 咪唑 imidazole
..
sp2
碱性
H H 分子间可能成氢键 m.p. 90℃
第15章 杂环化合物(dfj100620,已打印)

N
NH2NH2 HCl
CONHNH2 N
ì Ð Ñ Ë è Á
¸ Ó º
H2/Ni
N
orNa+C2H5OH
N H
ß ¤ £ ¬ ù À Æ à ß À ¤ ä Ï µ Ì × Õ © «Ó Ï Õ É
吡啶在有机化学中是一种常用的溶剂,它能溶解 许多有机化合物和部分无机盐; 吡啶及其衍生物在自然界分布较广,在药物中也 常见吡啶及其衍生物:
(1) 碱性与亲核性
填入sp2轨道中 未参与环状共轭 很容易给出 碱性、亲核性 与酸成盐 碱性>苯胺
N
é Ï » Ó £ ¹ R3N Kb :
例
6.2 10-5
NH2 N
2.3 10 -9
+
3.9
10 -10
¤Ð Í Ê ® Ð Í £ ©
N
(略)
+ HCl
N H
+
Cl- ¨ À £ß
N
+ CH3I
第15章 杂环化合物 (1学时)
(一) 杂环化合物的分类、命名和结构 (二) 五元杂环化合物及其化学性质 (三) 六元杂环化合物 (四) 稠杂环化合物(吲哚、喹啉)
本章重点讲解
• 几种重要环系的结构与性质: • 1、呋喃、噻吩、吡咯、吡啶的结构; • 2、呋喃、噻吩、吡咯、吡啶的性质:亲 电取代、氧化、还原、吡咯及吡啶的碱 性。
N CH3 N+
SO3
À £ß I- ¨
¤» ½ ê §Ð Í £ £
N
+ SO3
¨ß £ À ¤Ç ý Ð õ º ¯ À ò £ ¬ Á ¹ Í Ì º Æ º ¯ » À £ ©
第十五章杂环化合物祥解

PhCO 5 4
6 7
3
N
12
N H
NH2
SO3H
I
N
OH
2-氨基-5-苯甲酰基苯并咪唑
7-碘-8-羟基喹啉-5-磺酸
2-amino-5-benzoylbenzimidazole 7-iodo-8-hydroxuquinoline-5-sulfonic acid
O
PhCO
1
N
65
N7CH3
3
O 2 N4
N
8
CH3 9
1,3,7-三甲基嘌呤-2,6-二酮
1,3,7-thimethylpurine-2,6-dione
8. “标氢”或“指示氢”的标记方法:当环上已经含有最多数目的非累 积双键时,成环的饱和原子所连接的氢原子称为“标氢”或“指示氢”。当 杂环母核上连有标氢时,应给标氢尽可能低的编号,且将标氢用位次加H (斜体大写)的形式写在母体名称的前面。例如:
7N
62
N1
3
a b
2
4c
3
5OCON4N
6-(5-氯吡啶-2-基)-5-(4-甲基哌嗪-1-基)
甲酰氧基-7-氧代-6,7-二氢-5H-吡咯并
[3,4-b]吡嗪
N CH3
佐匹克隆(Zopiclone)
第二节 六元杂环化合物
N
N
N
N
吡啶
喹啉
异喹啉
b.p./℃ 115.5
238
242.2
水溶度 ∞
热水
Ph 5
不一致 6
4
N
1b
c
32 a
N 5-phenylimidazolo[2,1-b]thiazole
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
N
8
CH3 9
1,3,7-三甲基嘌呤-2,6-二酮
1,3,7-thimethylpurine-2,6-dione
8. “标氢”或“指示氢”的标记方法:当环上已经含有最多数目的非累 积双键时,成环的饱和原子所连接的氢原子称为“标氢”或“指示氢”。当 杂环母核上连有标氢时,应给标氢尽可能低的编号,且将标氢用位次加H (斜体大写)的形式写在母体名称的前面。例如:
N H
1
1
1
吡唑
咪唑
噻唑
噁唑
异噁唑
pyrazole
imidazole
thazole
oxazole
isoxazole
★ 含 两 个杂原子的六元单杂环
N N2
1
哒嗪 pyridazine
N3
N
1
嘧啶 pyrimidine
4
N
N
1
吡嗪 pyrazine
5N
5
4
H N
N33
6 NNH1 1 2
哌嗪 pyperazine
N H
1H-吡咯 1H-pyrrole
N
2H-吡咯 2H-pyrrole
O
2H-吡喃 2H-pyran
O
共
4H-吡喃
轭
4H-pyran
双
键
N H
1H-吲哚 1H-indole
N
3H-吲哚 3H-indole
9.“额外氢” 或“外加氢”,的标记方法:当环上不含有最多数目的非累 积双键时,多出的饱和氢原子称为“额外氢”或“外加氢”。当杂环母核上 连有额外氢时,要标明其位次和数目,全饱和时位次可略。例如:
PhCO 5 4
6 7
3
N
12
N H
NH2
SO3H
I
N
OH
2-氨基-5-苯甲酰基苯并咪唑
7-碘-8-羟基喹啉-5-磺酸
2-amino-5-benzoylbenzimidazole 7-iodo-8-hydroxuquinoline-5-sulfonic acid
O
PhCO
1
N
65
N7CH3
3
O 2 N4
★ 五元及六元稠杂环
4 5
6 7
3
2
N1 H
吲哚 indole
Байду номын сангаас
4 5
3 2
6
O1
7
苯并呋喃
benzofuran
4 5
3 2
6
S1
7
苯并噻吩
benzothiophene
4 5
6 7
N3
2
N H1
苯并咪唑 benzoimidazole
5 6
7 8
4 3
N1 2
喹啉 quinoline
5 6
7 8
4 3
6. 稠杂环有其固定的编号顺序(p466),一般从一端开始依次编号,共用 的碳原子一般不编号;注意使杂原子尽可能取较小的编号,并遵守杂原 子的优先顺序(p466 吩噻嗪) 嘌呤和异喹啉的编号是特例(p465)
7. 杂环母核的名称和编号确定后,可将取代基的名称连同位置编号以词头
或词尾的形式加在杂环名前和名后(p466-467)
稠(环)杂环 桥(环)杂环
丁公藤碱
螺(环)杂环
巨杂环
氮穴类化合物
杂环多面体
卟吩环系
大环醚
河豚毒素
二、 命 名
基本原则:
以IUPAC组织1979年制定的规则为标准,以具有特定俗名和半俗名的 45个杂环化合物为命名的基础,以我国的“音译法”为原则对杂环化合 物进行命名
(一) 特定杂环母核的命名规则
1. 单杂环母核编号一般从杂原子开始,顺着环依次编号;(p465) 2. 环上有取代基时,编号应使有取代基的碳原子的位次尽可能最小;(p466) 3. 若同一环上有多个杂原子时,应使杂原子的位数和尽可能最小;(p465) 4. 混多杂杂环化合物应按 O > S > —NH— > —N= 优先顺序编号;(p465)
三元杂环 四元杂环 五元杂环 六元杂环 七元杂环 八元杂环 大环杂环
常见杂环为 五元杂环 六元杂环
4. 根据杂原子数目分类
含一个杂原子
N3
4
N
N
5N N3
N
N2
N
S
H 含二N个杂原子
1
O
N
N
N
N
同多杂1杂环(含一种杂原1 子的多杂杂环)
含多个杂原子 混多杂杂N环(含两种以上杂原子的多杂杂环)
O
N
S
★ 含 一 个杂原子的五元单杂环
4
3
5
2 5
2
N H
N H
1
NO H
吡咯
呋喃
pyrrole
furan
3
2
NS H
噻吩 thiophene
★ 含 一 个杂原子的六元单杂环
4 3
4
5
3
N 2
1
6 N N C2H3
1
吡啶 pyridine
N
N H
CH3
六氢吡啶(哌 啶) piperidine
Et
3
ON
N2
1
异喹啉 isoquinoline
4
1 N5N6 5
3
7
NH 2
2
6N 4NN
3 79
8N 1 H
7H-嘌呤 purine
5
4
6
3
7 8
9
N
2
H1
咔唑 carbazole
9 8
10
N
1 2
7 6
N
5
3 4
吩嗪 phenazine
8
9
1
7
2
6 5
N
10
3 4
吖啶
acridine
10
9 H1
8
N
2
H 四氢呋喃(THF) tetrahedrofuran
4
5
3
6 NO 2
H1 2H-吡喃
2H-pyran
★ 含 两 个杂原子的五元单杂环
43
5
N2
N
H
1
5
4
4
5 N3 N NH2 H1
3
4
N2
5
4 4
N
3NN33
4
55
O
1
S1NH21
22 5
4 3 N3
4
4N 3
3
5
2
5
N2
NO2 5
NO2
O1
1
H
N
N
H
O
NN 发 烟 H2NSO4
SN
HgSO 4
250℃
N
H
N
O
N H
N
5. 根据环的数目分类
N H
S
NH2
单环杂环
NN
N
N
O
N
N
三聚氰胺 H2N-C≡N (氰胺)
H2N N NH2
N
二环O杂环 芳稠杂环(苯环N与杂环稠合) H
N
多环杂环 稠杂环(杂环与杂环稠合)
6. 根据多环的连接方式分类
Heterocyclic Compounds
有机化合物的基本类型
链状化合物 环状化合物
(C)n
纯碳环化合物 成环原子均为碳原子的环状化合物
杂环化合物 含有非碳成环原子的环状化合物
(C)n
杂原子
Z
常见杂原子为 N、O、S
第一节 分 类 和 命 名
一、 分 类
1. 根据是否有芳香性分类
芳杂环
N H
N H
NN
SS
符合Hückel规则 的平面型芳香性
杂环 NN
OO
NN 脂杂环
NN O
O
O
NN HH
NN
N
OO O
H
N
N
NN
2. 根据环状大π键的π电荷密度分类
富π芳杂环
S
O
N H
N H
具有斥电子
Π6 5
型电子结构的芳杂环
芳
杂
环
缺π芳杂环
N
N N
N N
NN
具有吸电子
Π6 6
型电子结构的芳杂环
N
N
3. 根据环的大小分类
7 6
S
5
3 4
吩噻嗪 phenothiazine
5. 只有一个杂原子的单杂环也可采用希腊字母表示法,从杂原子的邻近碳原子
依次编号;(p465-466)
COOH
H3C O CH3
N
α,α'-二甲基呋喃 α,α'-dimetylfuran
γ-吡啶甲酸 γ-pyridinecarboxylic acid
