同型半胱氨酸(HCY)测定试剂盒(酶循环法)产品技术要求sainuopu
同型半胱氨酸测定试剂盒(酶循环法)产品技术要求ruizhengshanda
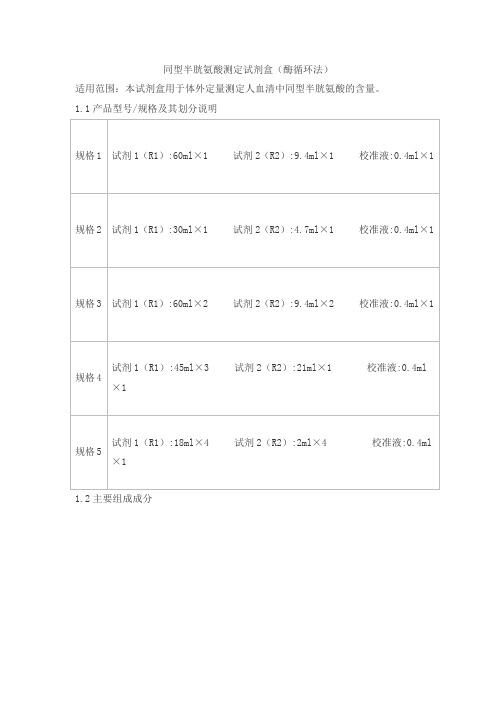
同型半胱氨酸测定试剂盒(酶循环法)适用范围:本试剂盒用于体外定量测定人血清中同型半胱氨酸的含量。
1.1产品型号/规格及其划分说明1.2主要组成成分2.1外观2.1.1 试剂1(R1)为无色或淡黄色液体,无混浊,无未溶解物;2.1.2 试剂2(R2)为无色或淡黄色液体,无混浊,无未溶解物;2.1.3 校准液应为无色澄清液体,无混浊,无未溶解物;2.1.4 试剂盒标签标识清晰,外包装完整无损。
2.2 净含量试剂1(R1)、试剂2(R2)和校准液的净含量不少于标示值。
2.3 试剂空白在主波长340nm、副波长405nm处(光径1cm),试剂空白吸光度A ≥1.0。
在主波长340nm、副波长405nm处(光径1cm),试剂空白吸光度变化率ΔA/min≤0.05。
2.4分析灵敏度测量1μmol/L的被测物时,吸光度变化率?A/min≥0.001。
2.5 线性范围在[3,45]μmol/L线性范围内,线性回归的相关系数r≥0.995。
在[3,10]μmol/L范围内,绝对偏差不超过±1μmol /L;在(10,45]μmol/L范围内,相对偏差不超过±10%。
2.6 精密度2.6.1 重复性重复测定(10±2)μmol/L的样品,变异系数CV≤5%;重复测定(20±4)μmol/L的样品,变异系数CV≤3%。
2.6.2 批间差相对极差≤10%。
2.7 准确度测定SRM1955,测定值与靶值的相对偏差不超过±15%。
2.8 稳定性原包装的HCY试剂盒在2℃~8℃避光保存,有效期为18个月。
试剂盒在规定的储存条件下保存至有效期满后,检测2.3、2.4、2.5、2.6.1、2.7项,结果应符合各项目的要求。
2.9 校准液溯源性按GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,试剂盒校准液溯源至NIST SRM1955。
同型半胱氨酸测定试剂盒(酶循环法)产品技术要求艾威德(北京)医疗

同型半胱氨酸测定试剂盒(酶循环法)适用范围:用于体外定量测定人血清中同型半胱氨酸的含量。
1.1 包装规格a) 试剂1:1×18mL 试剂2:1×5mLb) 试剂1:1×33mL 试剂2:1×9mLc) 试剂1:2×66mL 试剂2:2×18mLd) 试剂1:1×66mL 试剂2:1×18mL1.2 主要组成成分1.2.1试剂1主要组分试剂1:无色至浅黄色透明液体;试剂2:无色至浅黄色透明液体。
2.2 试剂装量应不低于试剂瓶标示装量。
2.3 试剂空白2.3.1试剂空白吸光度在340nm波长处测定试剂空白吸光度,应≥0.8。
2.3.2试剂空白吸光度变化率在340nm波长处测定其空白吸光度变化率|△A/min|<0.1。
2.4 分析灵敏度测定HCY含量为10μmol/L样本时,其|△A/min|应≥0.002。
2.5 线性范围2.5.1在(0,50)μmol/L范围内,线性回归的确定系数应不低于0.990;2.5.2测试浓度在(0,5] μmol/L范围内,线性绝对偏差应不超过±0.5 μmol/L;测试浓度在(5,50)μmol/L范围内,线性相对偏差应不超过±10%。
2.6 测量精密度2.6.1重复性:用两个水平质控血清重复测试其变异系数(CV)应不超过5%。
2.6.2批间差:抽取3个不同批号试剂,对同一份样本进行重复测定,相对极差≤10%。
2.7 准确度在样本中加入一定量的纯品,计算回收率,应在85%~115%范围内。
2.8 稳定性取在2℃~8℃条件下贮存达到12个月的试剂进行检测,应符合2.1、2.3、2.4、2.5、2.6.1、2.7的要求。
同型半胱氨酸测定试剂盒(酶循环法)产品技术要求jiuqiang

同型半胱氨酸测定试剂盒(酶循环法)适用范围:用于体外定量测定人血清或血浆中的同型半胱氨酸含量。
1.1 包装规格1.2 主要组成成分主要组成成分见表2。
表2 主要组成成分注:不同批号的校准品、质控品赋值有差异。
2.1 外观试剂1、2、3均为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;校准品为无色澄清液体,目测不得有任何沉淀及絮状悬浮物。
质控品为无色澄清液体,目测不得有任何沉淀及絮状悬浮物。
试剂盒标签标识清晰,外包装完整无损。
2.2 净含量试剂的净含量应不少于标称量。
2.3 试剂空白吸光度A340nm下测定空白吸光度应≥ 0.8000。
2.4 准确度用国际参考物质NIST SRM1955,对试剂盒进行测试,准确性偏差应不超过±15%。
2.5 分析灵敏度样本浓度为10.0 μmol/L时,其吸光度变化(ΔA)应≥ 0.0100。
2.6 线性区间线性区间在[1.5,50.0]μmoL/L,线性相关系数r应≥0.990,在[1.5,10.0]μmoL/L区间内测定的绝对偏差应不超过±1.0μmoL/L,在(10.0,50.0]μmoL/L范围内测定的相对偏差应不超过±10%。
2.7 测量精密度2.7.1重复性使用高、低不同浓度的血清样本或质控品重复测定10次,其测定值的变异系数(CV%)应不大于5%。
2.7.2批间差随机抽取三批试剂盒的批间相对极差(R)应不大于10%。
2.8 稳定性试剂盒在2℃~8℃密封避光保存,有效期为12个月。
取到效期后试剂盒进行检测,检测结果应符合2.1、2.3、2.4、2.5、2.6、2.7.1的要求。
2.9校准品溯源性按照GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,试剂盒校准品溯源至国际参考物质NIST SRM1955。
同型半胱氨酸检测试剂盒产品技术要求

同型半胱氨酸检测试剂盒产品技术要求同型半胱氨酸(Homocysteine, HCY)是一种重要的氨基酸,它在体内的代谢过程中,参与甲硫酸盐和硫酸葡萄糖胺的形成以及尿苯丙氨酸的代谢。
正常情况下,体内HCY的浓度较低,但如果HCY的产生量过高或清除速度减慢,就会导致HCY浓度升高,从而引发多种健康问题,如心血管疾病、新生儿缺陷、神经系统疾病等。
1.灵敏度:该检测试剂盒的灵敏度应足够高,能够准确测量HCY浓度的变化。
测量的线性范围应广泛,能够覆盖普通人群和高危人群的HCY浓度范围。
2.准确性:检测试剂盒应具有较高的准确性,能够在不同样本中精确测量HCY的浓度。
它应可靠地区分正常浓度和异常浓度,并提供准确的浓度结果。
3.精密度:检测试剂盒应具有较高的精密度,能够重复测量同一样本以获得一致的结果。
它应具有较低的内部和外部变异性,以确保可靠的实验重复性和结果比对性。
4.反应速度:检测试剂盒应能够在合理的时间内完成反应,并提供可靠的测量结果。
反应时间不宜过长,以节省实验时间。
5.操作简便性:检测试剂盒应具有操作简便的特点,使实验操作人员能够方便、快速地使用该试剂盒进行测量。
试剂盒应包含清晰明确的使用说明书,以便用户能够正确操作和解读结果。
6.安全性:检测试剂盒应符合安全性要求,不含有有害物质或重金属等对操作人员和环境有害的成分。
同时,应提供必要的标识和保护措施,以确保使用过程中的安全性。
7.长期稳定性:检测试剂盒应具有较长的稳定性,可以长期保存而不会失去活性。
试剂盒应提供有效期和储存条件等相关信息,以便用户能够合理储存和使用。
8.适用范围:检测试剂盒应适用于不同类型的样本,如血液、尿液等,以满足不同场景下HCY测量的需求。
总之,同型半胱氨酸检测试剂盒(酶法)的技术要求包括灵敏度、准确性、精密度、反应速度、操作简便性、安全性、长期稳定性和适用范围等方面,以确保该产品能够准确、可靠地测量HCY浓度,为相关疾病的诊断和治疗提供科学依据。
Hcy说明书

液体生化试剂使用说明书同型半胱氨酸测定试剂盒(酶法)【包装规格】【预期用途】本试剂适用于人血清或血浆中同型半胱氨酸含量的测定。
【检验原理】同型半胱氨酸被转化为游离型后,通过与共价底物反应,同时产生腺苷。
腺苷立即水解成氨和次黄嘌呤,氨在谷氨酸脱氢酶的作用下,使β-烟酰胺腺嘌呤二核苷酸还原性(NADH)转化为NAD+,样本中的同型半胱氨酸的浓度与NADH的变化成正比。
【主要组成成分】R1:S-腺苷甲硫氨酸盐(SAM)0.1mmol/L β-烟酰胺腺嘌呤二核苷酸还原性(NADH)0.2mmol/L三(2羧乙基)磷氯化氢(TCEP)0.5mmol/Lα- 酮戊二酸 5.0mmol/L修饰化Hcy甲基转移酶(HMTase) 5.0KU/L谷氨酸脱氢酶(GLDH)10.0KU/LR2:修饰化S-腺苷同型半胱氨酸(SAH)水解酶3.0KU/L 腺苷脱氨酶(ADA) 5.0KU/L【储存条件及有效期】试剂贮存于2-8℃、避光环境中,有效期为12个月。
【适用仪器】适用于日立7170、7060、7020、奥林巴斯、Beckman、东芝、利霸、迈瑞、岛津、欧宝、Microlab300等各种半自动、全自动生化分析仪。
【样本要求】样本为新鲜血清或肝素血浆。
请采血后立即离心分离血浆,或冷藏保存1小时内离心分离。
离心后样本在室温可稳定4天,0-2℃可稳定2周,-20℃下可稳定2个月。
【检验方法】1. 试剂准备液体试剂,直接使用,无需配制。
2. 基本参数测定模式速率法样本量13 ul延迟时间3分钟R1240 ul测定时间2-3分钟R265ul温度37℃主波长340nm光径1cm 副波长700nm值△A4. 结果计算采用合适的非线性模式,如logit/Log拟合多点定标的校准曲线;样品含量值通过校准曲线得出。
【参考值】3-15umol/L建议各实验室建立自己的参考值范围。
【检验结果的解释】如果不能确定检测结果的真实性则需直接重新测定或对样本进行稀释后重新测定。
同型半胱氨酸测定试剂盒(循环酶法)产品技术要求senmeixikema

同型半胱氨酸测定试剂盒(循环酶法)适用范围:用于体外定量检测人血清中同型半胱氨酸的浓度。
1.1规格a) 试剂1:1×30ml,试剂2:1×4.7ml;b) 试剂1:2×30ml,试剂2:1×9ml;c) 试剂1:2×60ml,试剂2:2×9ml;d) 试剂1:1×60ml,试剂2:1×9ml;e) 试剂1:2×240ml,试剂2:2×36ml;f) 试剂1:2×20ml,试剂2:2×3ml;g) 试剂1:12×20ml,试剂2:12×3ml;h) 试剂1:2×30ml,试剂2:2×6ml;i) 试剂1:1×30ml,试剂2:1×6ml;j) 试剂1:2×30ml,试剂2:2×9ml;k) 试剂1:1×48ml,试剂2:1×13ml;l) 试剂1:1×40ml,试剂2:1×10ml。
1.2 组成试剂主要组分见表1:表1 试剂主要组分2.1 外观外包装完整无破损,标签清晰;试剂1应为无色至淡黄色溶液;试剂2应为淡黄色溶液。
2.2 净含量应不低于试剂瓶标示装量。
2.3 试剂空白2.3.1 试剂空白吸光度在340nm处测定试剂空白吸光度,应≥1.0;2.3.2 试剂空白吸光度变化率试剂空白吸光度变化率(△A/min)应≤0.05。
2.4 分析灵敏度测定浓度为40μmol/L的样品,吸光度变化率(△A/min)应不低于0.01。
2.5 线性2.5.1在(0,50]μmol/L范围内,线性回归的相关系数应不低于0.990;2.5.2测试浓度[20,50]μmol/L的样品,相对偏差应不超过±10%;测试浓度(0,20)μmol/L的样品,绝对偏差应不超过±2μmol/L。
同型半胱氨酸测定试剂盒(酶循环法)产品技术要求zhongshengbeikong

同型半胱氨酸测定试剂盒(酶循环法)适用范围:本产品用于体外定量测定人血浆或血清中同型半胱氨酸的浓度。
1.1规格液体双剂型试剂1(R1):60mL×2,试剂2(R2):19mL×2,校准品(5个浓度):1mL ×5;试剂1(R1):60mL×1,试剂2(R2):19mL×1,校准品(5个浓度):1mL ×5;试剂1(R1):20mL×2,试剂2(R2):13mL×1,校准品(5个浓度):1mL ×5。
1.2规格划分说明根据净含量划分规格。
1.3主要组成成分试剂盒由试剂1(R1)液体、试剂2(R2)液体和校准品液体组成。
1.3.1 试剂1(R1)液体:脱氢酶 10KU/LNADH 0.4mmol/L稳定剂1.3.2 试剂2(R2)液体:共价结合底物 0.1mmol/L循环酶 3KU/L稳定剂1.3.3 校准品:人血清基质同型半胱氨酸校准品定值范围:0μmol/L~60μmol/L,5个浓度呈梯度增加(每批定值) 2.1 外观试剂盒中各组件的外观应满足:a) 试剂1(R1)应为浅黄色透明溶液,无混浊,无未溶解物,外包装完整无破损;b)试剂2(R2)应为无色或浅黄色透明溶液,无混浊,无未溶解物,外包装完整无破损;c)校准品应为浅黄色透明溶液,无混浊,无未溶解物,外包装完整无破损。
2.2 净含量液体试剂净含量应不少于标示值。
2.3 试剂空白吸光度在波长340nm(光径1cm)处,试剂空白吸光度(A)应≥0.800;试剂空白吸光度变化率(△A/min)≤0.015。
2.4 准确度测定SRM1955,相对偏差应不超过±15%。
2.5 分析灵敏度测试10µmol/L的Hcy时,吸光度变化率(△A/min)的绝对值应≥0.01。
2.6 重复性重复测试高浓度样本,变异系数(CV)应≤3%。
重复测试低浓度样本,变异系数(CV)应≤5%。
同型半胱氨酸检测试剂盒(酶法)产品技术要求

医疗器械产品技术要求编号:同型半胱氨酸检测试剂盒(酶法)1.产品型号/规格及其划分说明序号规格1R1:2×50ml、R2:2×5ml、R3:2×9ml(2×250Tests)2R1:2×50ml、R2:1×10ml、R3:1×18ml3R1:1×50ml、R2:1×5ml、R3:1×9ml2.性能指标2.1外观试剂R1溶液应呈粉红色、无颗粒、无杂质;试剂R2溶液应呈黄色、无颗粒、无杂质;试剂R3溶液应呈淡黄色、无颗粒、无杂质。
2.2净含量试剂盒各试剂装量应不小于标示值。
2.3试剂空白吸光度应为≤0.20。
用蒸馏水作为样品加入试剂测试,试剂空白吸光度A660nm2.4分析灵敏度测试40μmol/L被测物时,吸光度差值(△A)应不小于0.02。
2.5线性范围在(0~40)μmol/L范围内,其线性相关系数r≥0.990;浓度≥6μmol/L时,相对偏差≤20%;浓度<6μmol/L时,绝对偏差≤1μmol/L。
2.6测量精密度2.6.1重复性用控制血清重复测试所得结果的重复性(变异系数,CV)应≤10.0%。
2.6.2批间差批间差应≤10.0%。
2.7准确度用参考物质进行测试,其相对偏差应≤20.0%。
3.检验方法仪器基本要求a)波长:660nm;温度:37℃±1℃。
b)全自动生化分析仪。
测试方法按说明书规定,因不同机型使用试剂最终浓度相同。
在此推荐以本公司BECKMAN或HITACHI全自动生化分析仪进行测试。
3.1外观和性状目测检查,试剂R1、R2、R3溶液性状应符合2.1的要求。
3.2净含量用通用量具进行测量,应符合2.2的要求。
3.3试剂空白吸光度用蒸馏水作为样品测试试剂(盒),在测试波长660nm下,记录测试启动时的吸光度(A1)和约5min(t)后的吸光度(A2),A2测试结果即为试剂空白吸光度测定值,应符合2.3的要求。
同型半胱氨酸(Hcy)测定试剂(盒)(酶循环法)产品技术要求新产业

医疗器械产品技术要求编号:
同型半胱氨酸(H cy)测定试剂(盒)(酶循环法)
2.性能指标
2.1外观
试剂应为清澈透明的液体,无沉淀、悬浮物和絮状物。
2.2净含量
试剂装量的装量应按表 2,液体装量的最大允许负偏差应为 5%。
表 2 净含量
2.3试剂空白吸光度
试剂(盒)以纯化水为空白在 37 ℃±1℃ 、340 nm 波长、1 cm 光径条件下,试剂空白吸光度应≥1.50。
2.4分析灵敏度
试剂(盒)测试 28 μmol/L的被测物时,吸光度变化(ΔA)应在-0.180~-0.120 的范围内。
2.5线性范围
试剂(盒)在(0~50) μmol/L范围内的分析性能应符合如下要求:
a)线性相关系数r≥0.990;
b)(0~10) μmol/L范围内,线性绝对偏差应在±1μmol/L以内;(10~50) μmol/L
范围内,线性相对偏差应在±10%以内。
2.6测量精密度
2.6.1重复性
用校准品重复测试所得结果的变异系数CV≤4%。
2.6.2批间差
试剂(盒)批间相对偏差R≤6%。
2.7准确度
校准品的相对偏差 B 在±10%以内。
2.8分析特异性
血红蛋白浓度在 150 mg/dL 内、抗坏血酸浓度在 30 mg/dL 内、胆红素浓度在 20 mg/dL 内,对试剂检测结果的偏差影响应在±10%以内。
同型半胱氨酸测定试剂盒(酶循环法)产品技术要求丹大

同型半胱氨酸测定试剂盒(酶循环法)适用范围:用于体外定量测定人血清中同型半胱氨酸的含量。
1.1规格校准品(选配):规格1(0.3ml ×2;二个水平);规格2(0.5ml ×2;二个水平); 规格3(1.0ml ×2;二个水平); 质控品(选配):规格1(0.5ml ×2;二个水平);规格2(1.0ml ×2;二个水平); 1.2组成 试剂盒组成见表1表1 同型半胱氨酸(Hcy )测定试剂盒组成注:校准品及质控品赋值具有批特异性,每批次浓度详见标签。
2.1外观试剂盒外观应整洁,液体无渗漏,文字符号标识清晰;试剂Ⅰ为透明液体,不得有沉淀和絮状物;试剂Ⅱ为透明液体,不得有沉淀和絮状物。
校准品和质控品为淡黄色液体。
2.2装量每瓶不少于标示值。
2.3试剂空白吸光度在A340nm(主)处测定试剂初始吸光度不小于0.80。
2.4分析灵敏度测定10.0μmol/L样品,吸光度变化率(△A/min)≥0.01。
2.5线性范围2.5.1在[2.5,50.0]μmol/L内,相关系数R≥0.996。
2.5.2在[2.5, 10.0]μmol/L内,线性绝对偏差不超过±1.0μmol/L;(10.0,50.0] μmol/L内,线性相对偏差不超过±10%。
2.6 重复性a)重复测试(10.0±2.0)μmol/L的样本,所得结果的变异系数(CV%)应不大于5%。
b)重复测试(20.0±4.0)μmol/L的样本,所得结果的变异系数(CV%)应不大于3%。
2.7批间差测定(10.0±2.0)μmol/L样本,所得结果的批间相对极差(R)应不大于10%。
2.8准确度回收率应在90%-110%范围内。
2.9稳定性原包装试剂在2℃~8℃下存放有效期为12个月到效期后一个月内进行检测,测定结果应符合2.3-2.6、2.8和2.10项要求。
同型半胱氨酸测定试剂盒产品技术要求九强生物

同型半胱氨酸测定试剂盒产品技术要求九强生物一、样品要求1.样品类型:全血或血清样品。
2.储存条件:样品需要在-20℃下保存,并确保样品的冻结-解冻循环次数不超过三次。
3.样品预处理:样品需要去除蛋白质沉淀和红细胞。
二、试剂要求1.包装:试剂需密封,防止阳光直射和潮湿。
2.试剂稳定性:试剂应具有长期稳定性,一旦包装被打开,应在规定的时间内使用完。
3.试剂成分:试剂应包含同型半胱氨酸酶、辅助试剂和缓冲液等。
三、仪器设备要求1. 分光光度计:能够在340-412nm范围内进行检测。
2.移液器:能够准确分配不同容量的试剂。
3.震荡器:能够提供充分的震荡来混合试剂。
四、操作步骤1.样品准备:按照说明书中的提示,样品需要经过适当的处理和稀释。
2.试剂准备:根据说明书中的比例,将检测试剂和辅助试剂配制好。
3.试剂添加:将样品和试剂按照说明书中的顺序逐步添加到反应孔中。
4.反应孔处理:根据说明书的要求,对反应孔进行震荡混合和温度控制。
5.检测:在设定好的波长下使用分光光度计检测吸光度,并计算同型半胱氨酸的浓度。
五、结果解读1.结果计算:使用提供的标准曲线对吸光度进行计算,并得出同型半胱氨酸的浓度。
2.结果判读:根据相应的参考值范围,对结果进行判读,判断是否正常。
六、质量控制要求1.质量控制品:需要提供适当的质量控制品,用于每种批次的产品质量控制。
2.质量控制记录:需要记录质控样品的结果,并按照规定要求进行评估和分析。
七、结果报告1.报告模板:提供标准的结果报告模板,包括患者信息、样品信息、浓度结果等。
2.结果解释:提供相应的结果解释,包括可能的异常情况和需要采取的进一步检查。
以上是同型半胱氨酸测定试剂盒(酶循环法)的产品技术要求。
这些要求主要涉及样品和试剂的要求、仪器设备和操作步骤的要求、结果解读和质量控制的要求,以及结果报告的要求。
通过满足这些要求,可以确保试剂盒的性能和结果的准确性。
同型半胱氨酸(HCY)测定试剂盒(酶循环法)产品技术要求beiaotaikang

同型半胱氨酸(HCY)测定试剂盒(酶循环法)适用范围:本试剂盒用于体外定量检测人血清中同型半胱氨酸的浓度。
1.1 产品规格1.2 组成成份该试剂盒由试剂1(R1)、试剂2(R2)、校准品(选配)和质控品(选配)组成。
1.2.1试剂1(R1)主要组分:S-腺苷甲硫氨酸(SAM) 0.1mmol/LNADH 0.3mmol/ L三(2羧乙基)膦氯化氢(TCEP) 0.5mmol/L1.2.2试剂2(R2)主要组分:α-酮戊二酸 5.0mmol/L 同型半胱氨酸甲基转移酶(HMT)≥5.0KU/L谷氨酸脱氢酶(GLDH)≥10.0KU/LS-腺苷同型半胱氨酸水解酶(SAH)≥3.0KU/L腺苷胶氨酶(ADA)≥5.0KU/L1.2.3校准品(CaL)的组成PBS缓冲液 50mmol/L同型半胱氨酸:包含2个水平水平1:0.0-20.0μmol/L,具体浓度见瓶签;水平2:20.0-50.0μmol/L,具体浓度见瓶签。
1.2.4质控品(QC)的组成牛血清中添加同型半胱氨酸,稳定剂<1%。
定值范围:(8-16)μmol/L,(16-30)μmol/L。
2.1 外观a) 液体双试剂:试剂1应为透明溶液,无混浊,无未溶解物;试剂2应为透明溶液,无混浊,无未溶解物。
b) 校准品:无色至淡黄色溶液。
c) 质控品:无色至淡黄色液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 试剂空白吸光度试剂空白吸光度应≥0.800,试剂空白吸光度变化率应不大于0.050/min。
2.4 分析灵敏度HCY试剂盒测定浓度20.0μmol/L的被测物时,吸光度变化率(ΔA/min)应在0.010-0.200范围内。
2.5 线性范围在[3,50]μmol/L范围内,线性相关系数r应≥0.9900;在[3.0,20.0]μmol/L范围内线性绝对偏差应不超过2.0μmol/L,在(20.0,50.0]μmol/L范围内线性相对偏差应不超过±10%。
同型半胱氨酸测定试剂盒产品技术要求科美

同型半胱氨酸测定试剂盒产品技术要求科美同型半胱氨酸(HCY)是一种由半胱氨酸和甲硫氨酸经酶引起的脱氨作用产生的一种氨基酸。
其水平的增高与多种疾病的发病和发展密切相关,因此准确测定体内同型半胱氨酸的水平具有重要的临床意义。
为此,同型半胱氨酸测定试剂盒(酶循环法)被广泛应用于临床诊断和疾病研究。
产品技术要求1.灵敏度:同型半胱氨酸测定试剂盒的灵敏度应该达到或超过临床测量所需的水平。
灵敏度越高,能够检测到更低浓度的同型半胱氨酸,可以提高对疾病早期诊断的准确性。
2.精确度:试剂盒测定结果应该具有高度的准确性,即在重复测量中具有较小的变异性。
使用同一样本进行多次测量时,测定结果之间的差异应该尽可能小。
3.特异性:试剂盒测定方法应该具有高度的特异性,即不受与同型半胱氨酸结构相似的其他化合物的干扰。
特异性越高,测定结果越可靠。
4.稳定性:试剂盒的试剂和试剂原液应该具有良好的稳定性,能够在常规存储条件下保持其活性和性能的一致性。
这样可以减少试剂对环境条件的敏感性,并延长试剂盒的使用寿命。
5.操作简便性:试剂盒的操作步骤应该简洁明了,不需要繁琐的调样和稀释,以节省实验时间并降低实验操作的难度。
6.自动化程度:试剂盒应该能够适应自动化分析系统的要求,能够与常见的自动化分析设备无缝集成,实现更高的样本处理效率和分析准确性。
7.包装规格:试剂盒的包装规格应该根据实际需求进行选择,以满足不同规模实验室的使用要求。
8.临床应用:试剂盒的性能和结果应该符合临床应用的要求,可以用于各种人群的同型半胱氨酸测定,提供高质量的临床数据支持。
总结:同型半胱氨酸测定试剂盒(酶循环法)的产品技术要求包括灵敏度、精确度、特异性、稳定性、操作简便性、自动化程度、包装规格和临床应用等方面。
满足这些技术要求的试剂盒能够广泛应用于临床诊断和疾病研究,并为相关领域的科研人员提供可靠的实验工具。
同型半胱氨酸测定试剂盒(酶循环法)产品技术要求haifeng

同型半胱氨酸测定试剂盒(酶循环法)适用范围:本产品适用于体外定量测定人血清中的同型半胱氨酸(HCY)含量。
1.1 产品规格1.2 主要组成成分注:校准品、质控品具有批间、赋值特异性,具体值详见靶值单。
2.1 外观2.1.1试剂盒标签标识清晰,外包装完整无破损;2.1.2试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;2.1.3试剂2为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;2.1.4校准品:无色液体,目测不得有任何沉淀及絮状悬浮物;2.1.5质控品:无色液体,目测不得有任何沉淀及絮状悬浮物。
2.2 净含量净含量不低于标示值。
2.3 空白吸光度2.3.1 空白吸光度测定待检试剂在主波长340nm、副波长405nm、37℃条件下:A≥0.8;2.3.2 空白吸光度变化率空白吸光度变化率≤0.020/min(1cm,340nm/405nm 37℃)。
2.4 线性范围[3,50]μmol/L,相关系数r≥0.995;[3,10]µmol/L范围内绝对偏差≤±1.0µmol/L;(10,50]µmol/L范围内相对偏差应≤±10%。
2.5 分析灵敏度在产品说明书规定参数设定条件下,测定浓度为10.0μmol/L校准血清,△A/min≥0.01。
2.6 精密度2.6.1批内重复性CV≤5%。
2.6.2 批间差相对极差R≤10.0%。
2.7 准确度与已上市产品比对:[3,50]µmol/L范围内相关系数r≥0.990;[3,10]µmol/L范围内绝对偏差≤±1.0µmol/L;(10,50]µmol/L范围内相对偏差应≤±10%。
2.8 校准品均一性CV≤5%;2.9 质控品2.9.1赋值有效性测定值在质控靶值范围内。
2.9.2均一性CV≤5%。
2.10 稳定性未开封试剂2℃~8℃储存,可稳定12个月。
同型半胱氨酸(HCY)测定试剂盒(酶循环法)产品技术要求科美

同型半胱氨酸(HCY)测定试剂盒(酶循环法)适用范围:本试剂盒用于体外定量测定人血清中同型半胱氨酸(HCY)的浓度。
1.1包装规格1.2主要组成成分2.1.外观2.1.1试剂1应为无色或淡黄色透明溶液,无混浊,无未溶解物;2.1.2试剂2应为无色或淡黄色透明溶液,无混浊,无未溶解物;2.1.3校准品应为无色透明溶液,无混浊,无未溶解物;2.1.4质控品应为无色透明溶液,无混浊,无未溶解物;2.2.净含量液体试剂的净含量应不少于标示值。
2.3.试剂空白HCY试剂盒在波长340nm处测定空白样品的吸光度值,应不小于0.8000。
2.4.分析灵敏度HCY试剂盒测试10.0μmol/L HCY时,吸光度变化率(ΔA/min)应不小于0.0100。
2.5.准确度测定有证参考物质SRM1955,相对偏差应不大于15%。
2.6精密度2.6.1重复性重复测试(10.0±2.0)μmol/L的样本,所得结果的变异系数CV应不大于5%;重复测试(20.0±4.0)μmol/L的样本,所得结果的变异系数CV应不大于3%;2.6.2批间差测试(10.0±2.0)μmol/L的样本,所得结果的批间相对极差应不大于10%;2.7.线性范围HCY试剂盒在[3,50] μmol/L范围内,线性相关系数(r)应不小于0.995;在[3.0,10.0] μmol/L区间内,线性绝对偏差应不超过±1.0μmol/L;在(10.0,50.0] μmol/L区间内,线性相对偏差应不超过±10%。
2.8.质控品赋值有效性重复测定质控品,测定结果应在质控范围内。
2.9.稳定性原包装的试剂盒在2~8℃密封避光保存,有效期为12个月。
原包装校准品与质控品在2~8℃密封避光贮存,有效期为18个月。
在有效期满后2个月内,试剂性能应符合2.1、2.3、2.4、2.5、2.6.1、2.7、2.8的要求。
同型半胱氨酸(HCY)测定试剂盒(酶循环法)产品技术要求lideman

同型半胱氨酸(HCY)测定试剂盒(酶循环法)适用范围:本产品用于体外定量测定人体血清中同型半胱氨酸的含量。
1.1规格试剂1(R1):1×48mL、试剂2(R2):1×13mL;校准品(选配):低值1×1mL、高值1×1mL;低值质控品(选配):1×1mL;高值质控品(选配):1×1mL。
1.2 组成试剂盒由试剂、校准品(选配)和质控品(选配)组成。
试剂1(R1):腺苷甲硫氨酸(SAM):0.1 mmol/L;NADH :0.2 mmol/L;三乙羧乙基膦(TCEP) :0.5 mmol/L。
试剂2(R2):α-酮戍二酸:5.0 mmol/L;HCY甲基转移酶 (HMTase) :5.0 KU/L;谷氨酸脱氢酶:10 KU/L;S-腺苷同型半胱氨酸水解酶(SAHase):3.0 KU/L;腺苷脱氨酶:5.0 KU/L。
校准品的组成:2个水平的液体校准品,在人血清基质添加同型半胱氨酸(纯度>99%),添加人血清的比例为5%,稳定剂<0.1%;定值范围: (7.0~11.0) μmol/L、(26~38) μmol/L。
质控品的组成:2个水平的液体质控品,在人血清基质中添加同型半胱氨酸(纯度>99%),添加人血清的比例为5%,稳定剂<0.1%;定值范围:(10.0~17.9) μmol/L、(18.0~25.0) μmol/L。
2.1 外观液体双试剂:试剂1(R1)及试剂2(R2):无色至浅黄色澄清液体。
校准品:无色至浅黄色澄清液体。
质控品:无色至浅黄色澄清液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 溯源性:根据GB/T 21415及有关规定提供校准品的来源、赋值过程及测量不确定度等内容,该校准品溯源至参考物质(SRM1955,NIST)。
2.4 空白吸光度在37℃、340nm波长、1cm光径条件下,用去离子水或(生理盐水)作为样品加入试剂测试时,试剂空白吸光度应>0.80 ABS。
同型半胱氨酸测定试剂盒 (酶循环法)产品技术要求lepu

同型半胱氨酸测定试剂盒 (酶循环法) 适用范围:用于体外定量测定人血清中同型半胱氨酸的含量。
1.1规格试剂1:60mL×4,试剂2:9 mL×4;试剂1:60mL×1,试剂2:9 mL×1;试剂1:30mL×2,试剂2:9 mL×1;试剂1:47mL×1,试剂2:7 mL×1;试剂1:30mL×2,试剂2:60mL×1;试剂1:50mL×2,试剂2:5mL×2;试剂1:50mL×1,试剂2:5mL×1;试剂1:60mL×1,试剂2:6 mL×1;试剂1:5L×1,试剂2:0.5L×1;试剂1: 5L×2,试剂2:0.5L×2。
1.2 主要组成成分试剂1主要成分:试剂2主要成分:2.1 外观试剂1:无色至淡黄色溶液,试剂2:淡黄色溶液。
外包装完好、无破损,标签完好、字迹清晰。
2.2 净含量应不低于试剂瓶标示装量。
2.3 试剂空白2.3.1 试剂空白吸光度在340nm处测定试剂空白吸光度应≥0.8;2.3.2 试剂空白吸光度变化率试剂空白吸光度变化率ΔA/min≤0.1。
2.4 分析灵敏度测试10.0μmol/L的被测物时,吸光度变化率(ΔA/min)应不低于0.01。
2.5 准确度在样品中加入一定体积的标准溶液或纯品,计算回收率,应在(100±15)%范围内。
2.6 重复性2.6.1重复测试(10.0±2.0)μmol/L的样本,所得结果的变异系数(CV)应不大于5%。
2.6.2重复测试(20.0±4.0)μmol/L的样本,所得结果的变异系数(CV)应不大于3%。
2.7 线性在[3.0,45.0]μmol/L区间内,线性相关系数|r|应不小于0.995;在[3.0,10.0]μmol/L区间内,线性绝对偏差应不超过±1.0μmol/L,(10.0,45.0]μmol/L区间内线性相对偏差应不超过±10%。
同型半胱氨酸(HCY)测定试剂盒(酶循环法)说明书

同型半胱氨酸(HCY)测定试剂盒(酶循环法)说明书【产品名称】同型半胱氨酸(HCY)测定试剂盒(酶循环法)【包装规格】a)试剂1:1×18mL试剂2:1×5mLb)试剂1:1×33mL试剂2:1×9mLc)试剂1:2×66mL试剂2:2×18mLd)试剂1:1×66mL试剂2:1×18mL【预期用途】用于体外定量测定人血清中同型半胱氨酸的含量。
高HCY水平可导致动脉血管壁内皮片状脱落,同时刺激平滑肌细胞增生,引起血管损伤,出现类似动脉粥样硬化性病理改变。
测定同型半胱氨酸常用于冠心病、中风、高血压、老年痴呆等疾病的辅助诊断[1]。
【检验原理】同型半胱氨酸被转化为游离型后,通过与共价底物反应,同时产生腺苷。
腺苷立即水解成氨和次黄嘌呤,氨在谷氨酸脱氢酶的作用下,使β-烟酰胺腺嘌呤二核苷酸还原性(NADH)转化为NAD+,样本中的同型半胱氨酸的浓度与NADH的变化率成正相关。
【主要组成成分】试剂1主要组分磷酸盐缓冲液100mmol/L S-腺苷甲硫氨酸盐(SAM)0.1mmol/L β-烟酰胺腺嘌呤二核苷酸还原性(NADH)0.2mmol/L 三(2羧乙基)磷氯化氢(TCEP)0.5mmol/L α-酮戊二酸 5.0mmol/L 修饰化的HCY甲基转移酶(HMTase) 5.0KU/L 谷氨酸脱氢酶(GLDH)10.0KU/L ProClin300适量试剂2主要组分磷酸盐缓冲液100mmol/L 修饰化的S-腺苷同型半胱氨酸(SAH)水解酶 3.0KU/L 腺苷脱氨酶(ADA) 5.0KU/L ProClin300适量注:不同批号试剂盒中各组分未经试验不可互换。
【储存条件及有效期】1.试剂原包装在2~8℃储存,有效期为12个月,生产日期、有效期见标签。
2.开口后的试剂在仪器仓中(2~8℃)可稳定30天。
【适用仪器】艾威德AS-420/AS-660/AS-1200;日立HITACHI7020型/7060型/7180型/7600型/LABOSPECT008AS型;贝克曼AU400/AU480/AU640/AU680/ AU2700/AU5400/AU5800/AU5811/AU5821;佳能TBA-FX8/TBA-120FR/ TBA-2000FR;罗氏cobas8000c702/cobas8000c701/cobas8000c502;西门子SIEMENS ADVIA1800/ADVIA2400;雅培ABBOTT ARCHITECTc8000/ARCHITECT c16000/ARCHITECT ci8200;西森美康SYSMEX BM6010/C;科华KHB卓越310/卓越330/卓越400/卓越450/ZY-1200/ ZY-1280;迪瑞CS-240/CS-T300/CS-300B/CS-380/CS-400A/CS-400B/ CS-600A/CS-600B/CS-800A/CS-800B/CS-1200/CS-1200ISE/CS-1300B/ CS-1400;迈瑞MINDRAY BS-220/BS-330/BS-350E/BS-380/BS-390/ BS-400/BS-430/BS-600/BS-800/BS-2000M;颐兰贝ES-200/ES-380/ES-480;赛诺迈德SUNMATIK-9050型;雷杜Chemray420;英诺华D280;特康TC6010L;锦瑞GS400;普康6066。
同型半胱氨酸(HCY)测定试剂盒(酶循环法)产品技术要求sainuopu

同型半胱氨酸(HCY)测定试剂盒(酶循环法)产品技术要求sainuopu同型半胱氨酸(HCY)测定试剂盒(酶循环法)适⽤范围:⽤于体外定量测定⼈体⾎清中同型半胱氨酸的含量。
1.1 试剂盒包装规格试剂1:1×20ml,试剂2:1×5ml;试剂1:2×40ml,试剂2:2×10ml;试剂1:3×40ml,试剂2:3×10ml试剂1:4×60ml,试剂2:4×15ml;试剂1:2×400ml,试剂2:1×200ml;试剂1:1×8L,试剂2:1×2L。
校准品(选配):2×1ml(两⽔平)。
质控品(选配):2×1ml(两⽔平)。
1.2试剂盒主要组成成分2.1 外观试剂盒各组分应齐全,完整,液体⽆渗漏。
包装标签⽂字符号应清晰。
液体双试剂:试剂1⽆⾊⾄浅黄⾊澄清液体;试剂2⽆⾊⾄浅黄⾊澄清液体。
校准品:⽆⾊⾄淡黄⾊澄清液体。
质控品:⽆⾊⾄浅黄⾊澄清液体。
2.2 净含量液体试剂的净含量不得低于标⽰体积。
2.3 试剂空⽩吸光度在37℃、340nm波长、1cm光径条件下,试剂空⽩吸光度应不⼩于0.8。
2.4 分析灵敏度测定浓度为10µmol/L样本时,吸光度变化值(ΔA)应不⼩于0.02。
2.5 线性范围在(2.5,50) µmol/L范围内,线性相关系数∣r∣不⼩于0.995。
在(2.5,10]µmol/L区间内的线性偏差不超过±1.0µmol/L,(10,50) µmol/L区间内线性偏差不超过±10%。
2.6 重复性重复测试(10.0±2.0)µmol/L的样本,所得结果的变异系数(CV)应不⼤于5%。
重复测试(20.0±4.0)µmol/L的样本,所得结果的变异系数(CV)应不⼤于3%。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
同型半胱氨酸(HCY)测定试剂盒(酶循环法)
适用范围:用于体外定量测定人体血清中同型半胱氨酸的含量。
1.1 试剂盒包装规格
试剂1:1×20ml,试剂2:1×5ml;试剂1:2×40ml,试剂2:2×10ml;
试剂1:3×40ml,试剂2:3×10ml
试剂1:4×60ml,试剂2:4×15ml;试剂1:2×400ml,试剂2:1×200ml;
试剂1:1×8L,试剂2:1×2L。
校准品(选配):2×1ml(两水平)。
质控品(选配):2×1ml(两水平)。
1.2试剂盒主要组成成分
2.1 外观
试剂盒各组分应齐全,完整,液体无渗漏。
包装标签文字符号应清晰。
液体双试剂:试剂1无色至浅黄色澄清液体;试剂2无色至浅黄色澄清液体。
校准品:无色至淡黄色澄清液体。
质控品:无色至浅黄色澄清液体。
2.2 净含量
液体试剂的净含量不得低于标示体积。
2.3 试剂空白吸光度
在37℃、340nm波长、1cm光径条件下,试剂空白吸光度应不小于0.8。
2.4 分析灵敏度
测定浓度为10μmol/L样本时,吸光度变化值(ΔA)应不小于0.02。
2.5 线性范围
在(2.5,50) μmol/L范围内,线性相关系数∣r∣不小于0.995。
在(2.5,10]μmol/L区间内的线性偏差不超过±1.0μmol/L,(10,50) μmol/L区间内线性偏差不超过±10%。
2.6 重复性
重复测试(10.0±2.0)μmol/L的样本,所得结果的变异系数(CV)应不大于5%。
重复测试(20.0±4.0)μmol/L的样本,所得结果的变异系数(CV)应不大于3%。
2.7 批间差
不同批号试剂测试(10.0±2.0)μmol/L的样本,测定结果的批间相对极差(R)应不大于10%。
2.8 准确度
相对偏差:应不超过±15%。
2.9 质控品赋值有效性
测定结果在靶值范围内。
2.10 校准品溯源性
依据GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,校准品溯源至NIST生产的有证参考物质(SRM1955)。
2.11稳定性
效期稳定性:试剂盒在2℃~8℃下有效期为12个月,取失效期的试剂盒进行检测,试验结果满足2.3、2.4、2.5、2.6、2.8、2.9的要求。
