分光光度法测定铁含量精
分光光度法测定铁含量的方法汇总

标,绘制吸光度-显色剂用量曲线,确定显色剂的用量。 4.溶液适宜酸度范围的确定 在 9 只 50 mL 容量瓶中各加入 2.0 mL10-3
mol·L-1。铁标准溶液和 1.0 mL 100 mol·L-1 盐酸羟胺溶液,摇匀后放置 2 min。 各加 2 mL 1.5 g·L-1 邻二氮菲溶液,然后从滴定管中分别加入 0,2.00,5.00, 8.00,10.00,20.00,25.00,30.00,40.00 mL 0.1 mol·L-1NaOH 溶液摇匀,以 水稀释至刻度,摇匀。用精密 pH 试纸或酸度计测量各溶液的 pH。
3、试剂 1) 氢氧化钠溶液(300g/L) 2) 硝酸溶液(1+3) 3) 30%过氧化氢(密度为 1.11g/L) 4) 硫氰酸钠溶液(250g/L) 5) 铁标准溶液(此溶液 1ml 中含有 0.1mg 铁) 4、分析步骤
称取 0.0500g 试料于 250mL 锥形瓶中,加 5mL 氢氧化纳溶液,低温加热溶解后,加 20mL 硝酸溶液,煮沸约 20s,冷却。加 60mL 水、一滴过氧化氢、10mL 硫氰酸钠溶液, 放置 6min, 以空白夜做参比,1cm 比色皿,于 500nm 处,测定吸光度。同时做空白试验。 5、标准曲线的绘制
7.铁含量的测定试样溶液按步骤 1 显色后,在相同条件下测量吸光度, 由标准曲线计算试样中微量铁的质量浓度。
方案六 邻二氮菲分光光度法测定微量铁
一、实验目的
⒈学习确定实验条件的方法,Fra bibliotek握邻二氮菲分光光度法测定微量铁 的方法原理;
⒉掌握 721 型分光光度计的使用方法,并了解此仪器的主要构造。
二、实验原理
2.吸收曲线的绘制 在分光光度计上,用 1 cm 吸收池,以试剂空白溶液(1 号)为参比,在 440~560 nm 之间,每隔 10 nm 测定一次待测溶液(5 号)的吸光度 A,以波长为横坐标,吸光度为纵坐标,绘制吸收曲线,从而选择测定铁的最 大吸收波长。
分光光度法测定铁实验报告

分光光度法测定铁实验报告分光光度法测定铁实验报告引言:分光光度法是一种常用的分析方法,可以用于测定物质的浓度。
本实验旨在通过分光光度法测定铁的浓度,从而探究该方法的原理和应用。
实验目的:1. 了解分光光度法的基本原理;2. 掌握使用分光光度计进行测量的操作方法;3. 利用分光光度法测定铁的浓度。
实验原理:分光光度法利用物质对特定波长的光的吸收特性来测定其浓度。
在本实验中,我们将使用铁离子对可见光的吸收进行测量。
铁离子在紫外-可见光区域有明显的吸收峰,波长约为510 nm。
实验步骤:1. 准备工作:a. 清洗所使用的比色皿,确保其干净无污染;b. 使用去离子水冲洗分光光度计的比色皿槽,以确保无杂质干扰;c. 打开分光光度计,进行预热。
2. 标定分光光度计:a. 取一系列不同浓度的铁标准溶液,如0.1 mg/L、0.2 mg/L、0.3 mg/L等;b. 分别将这些标准溶液转移到比色皿中,注意避免溅出;c. 将比色皿放入分光光度计的比色皿槽中,记录各标准溶液的吸光度值;d. 绘制吸光度与浓度的标准曲线。
3. 测定待测样品:a. 取待测样品,如含铁离子的水溶液;b. 将待测样品转移到比色皿中,注意避免溅出;c. 将比色皿放入分光光度计的比色皿槽中,记录待测样品的吸光度值。
4. 计算铁的浓度:a. 根据标准曲线,找到待测样品吸光度对应的浓度;b. 根据比色皿中待测样品的容积,计算出待测样品中铁的质量;c. 根据待测样品的总体积,计算出待测样品中铁的浓度。
实验结果与讨论:通过实验测定,我们得到了标准曲线如下所示:[插入标准曲线图]根据待测样品的吸光度值,通过标准曲线的插值计算,我们得到了待测样品中铁的浓度为X mg/L。
在实验过程中,我们注意到分光光度计对比色皿中液体的体积和透明度要求较高,因此在操作过程中要小心,避免溅出或污染。
实验结论:本实验使用分光光度法成功测定了待测样品中铁的浓度。
通过标准曲线的插值计算,我们得到了待测样品中铁的浓度为X mg/L。
原子吸收分光光度法测铁、锰(精)

3.样品前处理: 采样前,所用聚乙烯瓶先用洗涤剂洗净, 再用硝酸(3/4)浸泡24h以上,然后用水冲 洗干净。 若仅测定可过滤态铁锰,样品采集后尽快 通过0.45μm滤膜过滤,并立即加硝酸 (3/1)酸化滤液,使pH为1-2。 测定铁、锰总量时,采集样品后立即按 (5/2)的要求酸化。
4.操作步骤: 测定铁、锰总量时,样品通常需要消解。混匀后 分取适量实验室样品于烧杯中。每100mL水样加 5mL硝酸(3/1),置于电热板上在近沸状态下将 样品蒸至近干,冷却后再加入硝酸(3/1)重复上述 步骤一次。必要时再加入硝酸(3/1)或高氯酸,直 至消解完全,应蒸近干,加盐酸(3/6)溶解残渣, 若有沉淀,用定量滤纸滤入50mL容量瓶中,加 氯化钙溶液(3/8)1mL,以盐酸溶液(3/6)稀释至 标线。
测量 在测量标准系列溶液的同时,测量样品溶 液及空白溶液的吸光度。由样品吸光度减 去空白吸光度,从校准曲线上求得样品溶 液中铁、锰的含量。测量可过滤态铁、锰 时,用(5.2)制备的试样直接喷入进行测量。 测量铁、锰总量时,用(6.1)中的试料。
结果的表示 实验室样品中的铁、锰浓度C(mg/L),按 下式计算,
校准曲线的绘制 分别取铁、锰混合标准操作液(3.11)于 50mL容量瓶中,用盐酸(3.6)稀释至标线, 摇匀。至少应配制5个标准溶液,且待测元 素的浓度应荡在这一标准系列范围内。根 据仪器说明书选择最佳参数,用盐酸溶液 (3.6)调零后,在选定的条件下测量其相应 的吸光度,绘制校准曲线。在测量过程中, 要定期检查校准曲线。
水质铁、锰的测定
火焰原子吸收分光光度法
(GB 11911-1989)
1、仪器检测条件:
分光光度法测定微量铁的含量实验报告

分光光度法测定微量铁的含量实验报告
实验目的:
通过分光光度法测定微量铁的含量。
实验原理:
实验仪器和试剂:
仪器:分光光度计、移液枪。
试剂:铁标准溶液、硝酸铵和硝酸亚铁、硫酸亚铁。
实验步骤:
1.取适量的硝酸铵和硝酸亚铁混合溶液,稀释成适宜的浓度。
2.在分光光度计上选择适当的波长,进行仪器的初步调试。
3.取一系列含有不同浓度的铁标准溶液,每个浓度分别进行三次测定,并计算平均值。
4.将测量所得的吸光度与浓度制成标准曲线。
5.将待测溶液纳入曲线范围内进行测定,计算出溶液中铁的含量。
实验结果和数据处理:
根据实验所得的吸光度和浓度数据,我们制成了铁的标准曲线。
通过
测量待测溶液的吸光度,我们进一步计算出溶液中铁的浓度。
实验讨论:
1.实验中所用的试剂的纯度对实验结果有重要影响。
如果试剂的纯度
不高,将会引入误差。
2.在实验过程中,仪器的选择和操作也会对实验结果产生一定的影响。
准确操作仪器,进行仪器的校准和调试是保证实验结果准确性的关键。
3.在实际应用中,还需要考虑样品的前处理,例如稀释、过滤等步骤。
4.在进行标准曲线绘制时,至少应该有三个不同浓度的标准溶液,每
个溶液进行三次测定,可以得到相对准确的结果。
实验结论:
通过分光光度法,我们成功测定了待测溶液中铁的含量。
该方法简便、准确,适用于微量铁含量的测定。
在实际应用中,我们应注意仪器的选择
和操作,以及试剂纯度对实验结果的影响。
通过合理的实验操作和数据处理,可以获得准确可靠的分析结果。
分光光度法测矿石中铁的含量实验报告

分光光度法测定矿石中铁的含量一、实验原理1、了解分光光度法测定试样中Fe(Ⅲ)含量的原理。
2、掌握分光光度计的工作原理及操作方法。
3、练习绘制标准工作曲线。
二、实验原理溶液中的物质在光的照射激发下,产生了对光吸收的效应,物质对光的吸收是具有选择性的,各种不同的物质都具有其各自的吸收光谱,因此当某单色光通过溶液时,其能量就会被吸收而减弱,光能量减弱的程度和物质的浓度有一定的比例关系,也即符合于比色原理---比耳定律。
T=I/I LogI0/I=KCL A=KCL其中:T 透射比I0 入射光强度I 透射光强度A 吸光度K 吸收系数L 溶液的光径长度C 溶液的浓度从以上的公式可以看出,当入射光、吸收系数和溶液的光径长度不变时,透过光是根据溶液的浓度而变化的。
三、仪器和药品仪器:722s分光光度计(配1cm比色皿4个),容量瓶(50mL,6个,分别编号为0~5),吸量管(5mL,2mL各一支),量筒(10mL,3个),烧杯(40mL),洗耳球。
药品:标准铁溶液(1.0×10-3mol/L),被测铁溶液(浓度约为1.0×10-3mol/L),KSCN 溶液(1.0mol/L),HNO3(1+1),H2O2(3%)。
四、实验步骤1、铁矿石的处理用天平称取0.5000g经研磨的矿粉,酸溶齐渣后得到总体积为250mL的Fe2(SO4)3溶液。
2、溶液配制在0至5号容量瓶中按教材所给图表配方量取各种试剂,用水稀释至刻度,摇匀待用。
3、吸光度的测量在480nm波长下,用1cm比色皿,以0号溶液为空白,依次测量1~5号溶液的吸光度值E。
五、数据处理1、绘制标准工作曲线对1~4号数据,以吸光度E为纵坐标,以[Fe3+]为横坐标,描出实验点并画直线穿过这些点,该直线为标准工作曲线。
2、被测溶液浓度的确定在标准工作曲线上,据5号溶液的吸光度值画一水平线与工作曲线橡胶,读出交点上的横坐标值,即为5号溶液的[Fe3+]值。
分光光度法测定铁含量的方法汇总

分光光度法测定铁含量的方法汇总1.原理:分光光度法测定铁含量的原理基于铁离子(Fe2+或Fe3+)与结合剂之间的络合反应。
铁离子与结合剂形成络合物时,会发生颜色变化,这种变化可以通过分光光度计测量。
2. 选择合适的结合剂:不同的结合剂适用于不同形态的铁离子。
比较常用的结合剂有邻苯二甲酸(1,10-苯基次甲基")(FERROXINE)、2,2'-联吡啶/Fe2+络合物(Bipyridyl/Fe)、硫巴比妥酸等。
3.样品前处理:对于一些含有浑浊物质的样品,需要进行前处理,如过滤或离心等,以去除干扰物。
4.准备标准曲线:制备一系列已知浓度的标准溶液,并测定它们的吸光度。
利用吸光度与浓度之间的线性关系绘制标准曲线。
标准曲线可以用来计算待测样品中铁离子的浓度。
5.测定样品吸光度:对于待测样品,将其溶液吸入分光光度计的比色皿中,调至适当的波长,并测量其吸光度。
注意要进行对比性测量,即测定样品的同时,还要测定一个空白试液的吸光度,用来做背景噪声的修正。
6.计算待测样品中铁离子的浓度:使用标准曲线,根据待测样品的吸光度值,可以通过插值或外推得到样品中铁离子的浓度。
7.质量控制:为了保证实验结果的准确性和可靠性,可以进行质量控制检查。
这包括对标准溶液进行重复测定、制备空白试液并测定其吸光度、进行样品间和试剂间的复测等。
8. 数据处理:根据测定得到的吸光度值和标准曲线,计算样品中铁元素的含量。
可以使用Excel等数据处理软件进行计算。
需要注意的是,实际操作中,具体的方法会根据不同的实验条件和目的进行调整,但是上述几点是分光光度法测定铁含量的基本步骤。
同时,对于一些特殊的样品,可能需要通过前处理或选择不同的结合剂来提高测定的准确性和灵敏度。
分光光度法测定微量铁的含量实验报告(标准曲线的测绘与铁含量的测定)

分光光度法测定微量铁的含量实验报告(标准曲线的测绘与铁含量的测定)实验报告:分光光度法测定微量铁的含量一、实验目的1.学习分光光度法测定微量铁含量的原理和方法。
2.掌握标准曲线的测绘方法,了解线性回归方程及其应用。
3.学会利用分光光度计测定样品中微量铁的含量。
二、实验原理分光光度法是一种常用的定量分析方法,其原理基于朗伯-比尔定律。
当一束单色光通过溶液时,光被吸收的程度与溶液的浓度和液层厚度成正比。
在一定波长下,吸光度A与溶液浓度C和液层厚度L的乘积成正比,即A=εCL。
其中,ε为摩尔吸光系数,L为液层厚度,C为溶液浓度。
通过绘制标准曲线,可以求得铁的含量。
三、实验步骤1.准备试剂和仪器:硝酸、高氯酸、硫酸、铁标准溶液(100μg/mL)、分光光度计、比色皿、容量瓶(100mL)、吸量管(10mL、5mL、2mL)等。
2.绘制标准曲线:分别取10mL、5mL、2mL铁标准溶液于三个100mL容量瓶中,各加5mL硝酸,20mL硫酸,摇匀,用去离子水定容。
将各溶液分别移入比色皿中,用分光光度计在562nm波长下测量吸光度。
记录数据并绘制标准曲线。
3.测定样品中铁的含量:将样品溶液移入比色皿中,用分光光度计在562nm波长下测量吸光度。
根据标准曲线查得铁的浓度,计算样品中铁的含量。
四、结果与分析1.标准曲线测绘结果在坐标纸上绘制标准曲线,横坐标为铁标准溶液的浓度(μg/mL),纵坐标为吸光度。
根据实验数据绘制标准曲线(图1)。
可以看出,随着铁浓度的增加,吸光度也逐渐增大。
表明铁浓度与吸光度之间存在线性关系。
可以得出线性回归方程为:y=kx+b(k为斜率,b为截距)。
根据实验数据可计算出斜率k和截距b的值。
图1 标准曲线(请在此处插入标准曲线图)2.铁含量测定结果将样品溶液移入比色皿中,用分光光度计在562nm波长下测量吸光度。
根据标准曲线查得铁的浓度(μg/mL),计算样品中铁的含量(mg/L)。
结果如表1所示。
讲稿9 分光光度法测定水样中铁的含量
实验九分光光度法测定水样中铁的含量一、实验目的1、了解利用可见分光光度法进行定量分析的原理和方法;2、初步掌握分光光度计的使用方法,学习测绘溶液的吸光度;3、掌握利用标准曲线法进行定量分析的操作与数据处理方法。
二、实验原理邻二氮菲(邻菲罗啉,phen)和Fe2+在pH为3-9的溶液中,生成一种稳定的橙红色络合物Fe(phen) 32+,其lgK=21.3,κ508=1.1 × 104L·mol-1·cm-1。
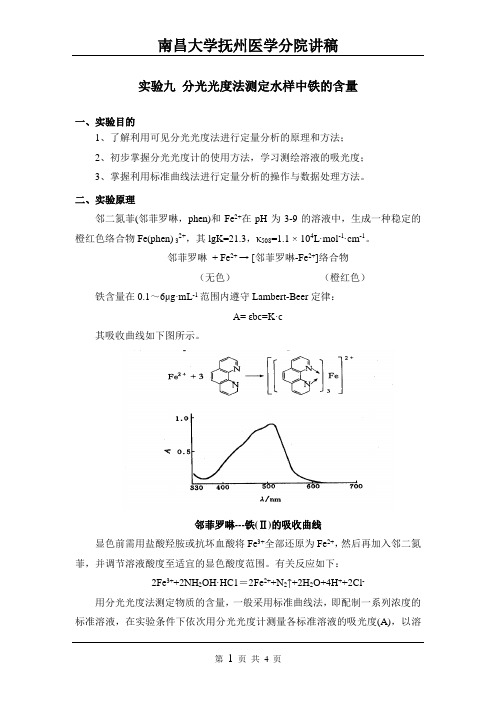
邻菲罗啉+ Fe2+ → [邻菲罗啉-Fe2+]络合物(无色)(橙红色)铁含量在0.1~6μg·mL-1范围内遵守Lambert-Beer定律:A= εbc=K·c其吸收曲线如下图所示。
邻菲罗啉---铁(Ⅱ)的吸收曲线显色前需用盐酸羟胺或抗坏血酸将Fe3+全部还原为Fe2+,然后再加入邻二氮菲,并调节溶液酸度至适宜的显色酸度范围。
有关反应如下:2Fe3++2NH2OH·HC1=2Fe2++N2↑+2H2O+4H++2Cl-用分光光度法测定物质的含量,一般采用标准曲线法,即配制一系列浓度的标准溶液,在实验条件下依次用分光光度计测量各标准溶液的吸光度(A),以溶液的浓度为横坐标,相应的吸光度为纵坐标,绘制标准曲线。
在同样实验条件下,测定待测溶液的吸光度,根据测得吸光度值从标准曲线上查出相应的浓度值,即可计算试样中被测物质的质量浓度。
三、实验仪器与试剂电子天平,容量瓶(25ml×7,或用比色管代替), 刻度移液管(1ml,2ml,5ml,10ml×2),752 型分光光度计,1 cm玻璃比色皿,滴管;2mmol/L铁标准溶液,待测含铁水样,1.5mol/L盐酸羟胺溶液,8mmol/L邻二氮菲溶液,1.0 mol/L 醋酸钠溶液,蒸馏水。
四、实验内容与步骤1、标准Fe2+溶液系列及待测溶液的配制按表1所示,在编号为1-7的50 mL容量瓶(或比色管)中分别按照表1的数据加入铁标准溶液或待测水样,然后分别加入1.00 mL 1.5mol/L盐酸羟胺溶液,摇匀后放置2 min,再各加入2.00 mL 8mmol/L邻菲罗啉溶液、5.00 mL 1.0 mol/L 乙酸钠溶液,以水稀释至刻度,摇匀。
实验分光光度法测定铁

实验分光光度法测定铁The following text is amended on 12 November 2020.实验十四邻二氮菲分光光度法测定铁的含量一、实验目的1.学习吸光光度法测量波长的选择方法;2.掌握邻二氮菲分光光度法测定铁的原理及方法;3.掌握分光光度计的使用方法。
二. 实验原理分光光度法是根据物质对光选择性吸收而进行分析的方法,分光光度法用于定量分析的理论基础是朗伯比尔定律,其数学表达式为:A=eb C邻二氮菲(乂称邻菲罗卩林)是测定微量铁的较好试剂,在pH二2〜9的条件下,二价铁离子与试剂生成极稳定的橙红色配合物。
摩尔吸光系数£ =11000 L • moE1• cm' ‘。
在显色前,用盐酸疑胺把Fe"还原为Fe=2F『+2NH;0HHClf 2Feh+\:+4H 十+ 2H:0+2C 厂Fe‘ + Phen = Fe‘ - Phen (橘红色)用邻二氮菲测定时,有很多元素干扰测定,须预先进行掩蔽或分离,如钻、银、铜、铅与试剂形成有色配合物;钩、釦、镉、汞与试剂生成沉淀,还有些金属离子如锡、铅、钮则在邻二氮菲铁配合物形成的pH范围内发生水解;因此当这些离子共存时,应注意消除它们的干扰作用。
三. 仪器与试剂1.醋酸钠:1 mol • L':;2.盐酸:6 mol • L"1;3.盐酸羟胺:10% (用时配制);4-邻二氮菲(%):邻二氮菲溶解在lOOmLl: 1乙醇溶液中;5-铁标准溶液。
(1)100 ng-mf1铁标准溶液:准确称取(NH4) 2 Fe (SO,) 2 - 12H:0于烧杯中, 加入20 mL 6 mo 1・I?盐酸及少量水,移至1L容量瓶中,以水稀释至刻度,摇匀.6.仪器:7200型分光光度计及1 cm比色皿。
四、实验步骤1.系列标准溶液配制(1)用移液管吸取10mL100 u g • ml?铁标准溶液于100mL容量瓶中,加入2mL 6 mol - L"盐酸溶液,以水稀释至刻度,摇匀.此溶液F』浓度为10 u g • mL'1.(2)标准曲线的绘制:取50 mL比色管6个,用吸量管分别加入0 mL, 2 mL, 4 mL, 6 mL, 8 mL和10 mLlO u g • ml?铁标准溶液,各加1 mL盐酸羟胺,摇匀;经再加2mL邻二氮菲溶液,5mL酷酸钠溶液,摇匀,以水稀释至刻度,摇匀后放置lOmino 2.吸收曲线的绘制取上述标准溶液中的一个,在分光光度计上,用1 cm比色皿,以水为参比溶液,用不同的波长,从440〜560 nm,每隔10 nm测定一次吸光度,在最大吸收波长处每隔5nm测定一次吸光度。
分光光度法测定铁的含量实验报告

分光光度法测定铁的含量实验报告一、实验目的1、掌握分光光度法测定铁含量的基本原理和方法。
2、学会使用分光光度计进行定量分析。
3、熟悉标准曲线的绘制和应用。
二、实验原理分光光度法是基于物质对光的选择性吸收而建立起来的分析方法。
在分光光度法中,通常选择一定波长的单色光通过含有被测物质的溶液,测量溶液对该波长光的吸光度,从而确定物质的含量。
本实验中,利用邻二氮菲与二价铁离子在 pH 为 2~9 的条件下形成稳定的橙红色配合物,该配合物在 510nm 处有最大吸收峰。
通过测定不同浓度的铁标准溶液在 510nm 处的吸光度,绘制标准曲线,然后测定未知溶液的吸光度,根据标准曲线计算出未知溶液中铁的含量。
三、实验仪器与试剂1、仪器722 型分光光度计容量瓶(50mL、100mL)移液管(1mL、2mL、5mL、10mL)吸量管(5mL、10mL)比色皿烧杯(50mL、100mL)玻璃棒电子天平2、试剂硫酸亚铁铵(NH₄)₂Fe(SO₄)₂·6H₂O邻二氮菲(15g/L)盐酸羟胺(100g/L)1mol/L 盐酸溶液1mol/L 氢氧化钠溶液四、实验步骤1、标准溶液的配制准确称取 03474g 硫酸亚铁铵(NH₄)₂Fe(SO₄)₂·6H₂O于小烧杯中,用 10mL 1mol/L 盐酸溶液溶解,转移至 100mL 容量瓶中,用蒸馏水稀释至刻度,摇匀,得到浓度为 01000mg/mL 的铁标准储备液。
用移液管分别吸取 000mL、200mL、400mL、600mL、800mL、1000mL 铁标准储备液于 50mL 容量瓶中,各加入 1mL 100g/L 盐酸羟胺溶液,摇匀,放置 2min 后,再加入 2mL 15g/L 邻二氮菲溶液和 5mL 1mol/L 氢氧化钠溶液,用蒸馏水稀释至刻度,摇匀,得到浓度分别为000μg/mL、400μg/mL、800μg/mL、1200μg/mL、1600μg/mL、2000μg/mL 的铁标准系列溶液。
分光光度法测定水中总铁含量

分光光度法测定水中总铁含量摘要:本法主要研究用分光光度法测定水中总铁含量的分析方法。
采用了邻菲啰啉作显色剂、盐酸羟胺作还原剂,以工作曲线法测定水中总铁含量,且讨论了测定的最佳条件。
本法灵敏、可靠,应用于清洁环境水样和轻度污染水的分析。
关键词:分光光度法;废水;总铁;水质检测前言铁在地壳中分布很广,日常水中均含有之。
但实际水样中铁的存在形式是多样的,由于亚铁很易被氧化,因此亚铁只能在地下水中遇到;而高铁由于其氢氧化物溶解度小,故一般天然水中高铁的含量很低。
[1.2]铁在深层地下水中呈低价态,当接触空气并在pH大于5时, 便被氧化成高铁并形成氧化铁水合物(Fe2O3?3H2O)的黄棕色沉淀,暴露于空气的水中, 铁往往也以不溶性氧化铁水合物的形式存在。
当pH值小于5时,高铁化合物可被溶解。
因而铁可能以溶解态、胶体态、悬浮颗粒等形式存在于水体中, 水样中高铁和低铁有时同时并存。
1 实验部分1.1方法原理在pH3~9的条件下,低铁离子能与邻菲啰啉生成稳定的橙红色络合物,在波长510nm处有最大光吸收。
邻菲啰啉过量时,控制溶液pH为2.9~3.5,可使显色加快。
[3] 水样先经加酸煮沸溶解铁的难溶化合物,同时消除氰化物、亚硝酸盐、多磷酸盐的干扰。
加入盐酸羟胺将高铁还原为低铁,还可消除氧化剂的干扰。
水样不加盐酸煮沸,也不加盐酸羟胺,则测定结果为低铁的含量。
1.2 主要仪器1.2.1 100ml三角瓶1.2.2 50ml具塞比色管(或容量瓶)1.2.3 分光光度计1.3 实验试剂[4]1.3.1 铁标准贮备溶液:称取0.7022g硫酸亚铁铵[Fe(NH4)2(SO4)2?6H2O],溶于70ml 20+50硫酸溶液中,滴加0.02mol/L 的高锰酸钾溶液至出现微红色不变,用纯水定容至1000ml。
此贮备溶液1.00ml含0.100mg铁。
1.3.2 铁标准溶液(使用时现配):吸取10.00ml铁标准贮备溶液(11.1.4.1), 移入容量瓶中,用纯水定容至100ml。
分光光度法测定铁含量实验报告

分光光度法测定铁含量实验报告铁含量测定实验报告一、前言在我们的日常生活中,铁是一种非常重要的矿物质元素,它在人体健康、农业生产等方面都发挥着举足轻重的作用。
如何准确地测定铁的含量,对于我们了解人体健康状况、指导农业生产等方面具有重要意义。
本文将详细介绍分光光度法测定铁含量的实验过程和理论依据,以期为相关领域的研究者提供参考。
二、实验原理及方法1.1 实验原理分光光度法是一种基于物质对特定波长的光线吸收或发射的特性来定量分析物质的方法。
在本实验中,我们采用分光光度法测定铁含量,其原理如下:我们需要准备一系列不同浓度的铁标准溶液,如0、1、2、3、4、5等不同浓度的标准溶液。
然后,将这些标准溶液分别置于比色皿中,用分光光度计测量每个标准溶液的吸光度(A)。
接下来,我们需要准备待测样品,并将其溶解于适当的溶剂中,如水或乙醇等。
然后,用分光光度计测量待测样品溶液的吸光度(A0)。
由于不同浓度的标准溶液和待测样品溶液中的铁离子浓度不同,因此它们对可见光的吸收程度也不同。
具体来说,当可见光照射到铁离子溶液时,部分光线被吸收,而另一部分光线则透过溶液。
通过测量吸收前后的光线强度差(ΔA),我们可以计算出待测样品溶液中铁离子的浓度。
1.2 实验步骤(1) 准备不同浓度的铁标准溶液。
(2) 将铁标准溶液置于比色皿中。
(3) 用分光光度计测量每个标准溶液的吸光度。
(4) 准备待测样品。
(5) 将待测样品溶解于适当的溶剂中。
(6) 用分光光度计测量待测样品溶液的吸光度。
(7) 根据实验数据计算待测样品中铁离子的浓度。
二、实验结果与分析根据上述实验步骤,我们得到了不同浓度铁标准溶液和待测样品溶液的吸光度数据(表1)。
通过对比这些数据,我们可以发现:随着铁标准溶液浓度的增加,其吸光度也随之增加;而对于待测样品溶液,其吸光度则随着铁离子浓度的增加而增加。
这说明我们所采用的分光光度法测定铁含量的方法是可行的。
为了进一步验证这一结论,我们还进行了一些额外的实验。
分光光度法测铁含量

分光光度法测铁含量
分光光度法是一种常用于测定溶液中物质含量的方法,适用于测定铁元素的含量。
测定铁含量的步骤如下:
1. 准备样品:将待测溶液准备好,确保其浓度在分光光度法所能检测范围内。
如果浓度过高,则需要进行稀释操作;如果浓度过低,则可能需要进行富集或者预处理。
2. 校准仪器:使用已知浓度的铁标准溶液进行仪器校准。
通过测定一系列不同浓度的标准溶液的吸光度并绘制标准曲线,可以建立浓度与吸光度之间的关系。
3. 测定样品:将样品放入分光光度计中,选择合适的波长进行测定。
在选定波长下,测量样品吸光度,并记录下来。
4. 计算结果:利用标准曲线,根据测得的样品吸光度值,推算出对应的铁离子浓度。
根据样品的体积和稀释倍数,可以计算出样品中的铁含量。
需要注意的是,在进行分光光度法测定时,应当控制好实验条件,确
保仪器的可靠性和准确性。
此外,样品的处理和预处理也是非常关键的步骤,需要根据具体情况进行适当的操作,以保证测量结果的准确性。
分光光度法测定铁的含量实验报告

分光光度法测定铁的含量实验报告
一、实验目的
本实验旨在采用分光光度法测定铁的含量。
二、实验原理
本实验采用分光光度法测定铁的含量,即用高灵敏的分光光度仪测定样品的红色闪光吸收率,由此来判断其中铁含量的大小。
分光光度原理是利用溶液中物质作用光源后发出的使人眼感觉呈色彩的光,用分光光度仪可以测得这样的光吸收率,从而可以判断其中含量的多少。
三、实验步骤
1. 准备样品:将待测样品量取精确至0.1g,放入盛有50ml溶液中的烧瓶中。
2. 加标:在烧瓶内加入适量的指示剂,振荡混匀,使样品中的铁为可测状态。
3. 测量:将烧瓶中的溶液放入分光光度仪的吸收管内,调节适当的光谱范围。
在恒定的照度下,用光探头测量样品的吸收率,并用计算机记录测得值。
4. 分析:将测得的数值进行推算,得出样品中铁含量大小。
四、实验结果
实验可测得样品中铁的含量为1.30g/L。
五、实验总结
本实验全程运用分光光度法测定铁的含量,实验成功,得出样品中铁的含量为1.30g/L,未发现明显异常。
工业用化工产品铁含量测定的通用方法1,10-菲啰啉分光光(精)

工业用化工产品铁含量测定的通用方法1,10-菲啰啉分光光度法度法GB/T 3049—2006Chemical products for industrial use - General method for determination of iron content - 1 10-Phenanthroline spectrophotometric method1 范围本标准规定了化工产品中铁含量测定的通用方法1,10-菲啰啉分光光度法。
本标准描述了溶液中铁含量的测定技术。
在制备试验溶液时,应参考与所分析产品有关的标准对本方法进行必要的修改使其适合产品的测定。
2 适用领域本标准适用于所取试液中铁含量为10μg~500μg ,其体积不大于60mL。
大量的碱金属、钙、锶、钡、镁、锰(Ⅱ)、砷(Ⅲ)、砷(Ⅴ)、铀(Ⅵ)、铅、氯离子、溴离子、碘离子、硫氰酸根、乙酸根、氯酸根、硫酸根、硝酸根、硫离子、偏硼酸根、硒酸根、柠檬酸根、酒石酸根、磷酸根和100mg以下的锗(Ⅳ)在试验溶液中,对测定无干扰。
如试验溶液中存在柠檬酸根、酒石酸根、砷酸根或大于100mg的磷酸根,显色速度变慢。
干扰和消除的方法参见附录A3 原理用抗坏血酸将试液中的Fe3+还原成Fe2+。
在pH值为2~9时,Fe2+与1,10-菲啰啉生成橙红色络合物,在分光光度计最大吸收波长(510nm)处测定其吸光度。
在特定的条件下,络合物在pH值为4~6时测定。
4 试剂分析时只能使用分析纯试剂,蒸馏水或纯度相当的水。
4.1 盐酸,180g/L溶液将409mL质量分数为38%的盐酸溶液(ρ=1.19g/mL)用水稀释至1000mL,并混匀(操作时要小心)。
4.2 氨水,85g/L溶液将374mL质量分数为25%氨水(ρ=0.910g/mL)用水稀释至1000mL,并混匀。
4.3 乙酸-乙酸钠缓冲溶液,在20℃时pH=4.5称取164g无水乙酸钠用500mL水溶解,加240mL冰乙酸,用水稀释至1000mL。
分光光度法测定饮用水中铁的含量

铁 作为生 活 饮用水 水 质常规 检验 一般 化
据 测得 的吸 光 度值 求 出待测 溶液 的 浓度 。 条件 实验 的一般 步骤 为改 变其 中一 个 因
学 限量 指标 ( 限值 : < .mg L 。 铁 0 3 / )但含 铁 量
盐酸 分析 纯
暂时 固定其他 因素 , 色后测量相应溶液 的 硫酸 分析 纯 天津瑞 金特化学 品有 限公司 显 太 高的 水 易于 产生 一 些特 殊 气 味 、 饮用 时很 素 , 通 显色 曲线确 定显色 反应 的 邻菲 罗啉 分析纯 沈阳市试 剂 三厂 不 可 口 , 对 人 的 健 康 有 一定 的影 响 。 据 吸光 度 , 过时 间一 也 根 生 活饮 用 水卫 生标 准 , 用 水 中铁 的允 许 量 适宜时间范 围。 饮 其他 因素的适宜值 , 可按这一 盐 酸羟 胺 也
=
1 . 。 以 在加 入显 色剂 之前 , 用盐 酸 羟 4 1所 应
P( / NH, H・ 1 e  ̄ O HC ) 将F ”还原 为F , 反 应 现 粉 红 色不 变 , e 其 用纯 水 定 容 到 1 0 。 0 mL
2 F e + 2 N H O H ・ H C l 一
铁标 准 贮 备 液 ( . mg mL : 取 0 0 1 0 / )称 0 . 中 , ; o 0 to /L 滴 O . 2 l 高锰 酸钾 溶液 至溶 液 出 n o 铁标 准使 用液 ( 0 0 g mL : 取 1 1 . / ) 吸 0
邻 二氮 菲 生 成 3 1 合 物 , 淡 蓝 色 ,g :配 呈 I K稳 7 2 g 0 2 硫酸 亚铁 铵溶 于 7 rL 酸( + 0 溶液 O 硫 a 1 l)
数 在 0 9 以 下 , 定 结果 重 现 性 不 好 。 提 式 如 下 : .9 测 为 高测 定结 果 精 密度 和准 确 度 , 们进 行 了以 我
分光光度法测定铁含量实验报告

分光光度法测定铁含量实验报告1. 实验目的说到分光光度法,很多人可能会觉得这是个高大上的名词,其实它就像一位默默无闻的侦探,专门负责查清样品里隐藏的铁含量。
铁在生活中可谓是“随处可见”,但如果想精确知道它的含量,就得借助这个好帮手了。
这次实验的主要目的是利用分光光度法,看看我们手里的样品中到底藏了多少铁,让我们对铁的世界有个更深入的了解。
2. 实验原理2.1 分光光度法的基础简单来说,分光光度法就是通过测量物质吸收光的能力来推算出其中某种成分的浓度。
光线照射到样品上,如果里面有铁,铁就会吸收特定波长的光,而光的强度就会发生变化。
这一变化就像是在进行一场隐秘的“对话”,通过分析光的吸收程度,我们可以推测出样品中铁的含量。
2.2 吸光度与浓度的关系这里还有个小知识点,吸光度和浓度之间的关系是线性的,这就好比喝水和口渴的关系,水越多,口渴感就越少。
通过比尔定律(BeerLambert Law),我们能得出吸光度与浓度的关系式,进而计算出样品中的铁含量。
这就像是用公式解密,越解越明了。
3. 实验步骤3.1 准备工作一开始,咱们得准备好材料和设备,别的都可以忽略,但分光光度计可是我们的主角。
接着,取一些标准铁溶液,别小看这小小的液体,它可是我们实验成功的关键。
然后,将这些标准溶液稀释到不同的浓度,准备进行测量。
这里就像做菜,得先备好食材,才能煮出美味佳肴。
3.2 测量过程一切准备好后,咱们就可以开始“测量”了。
将不同浓度的标准溶液依次放入分光光度计,调好波长,按下按钮,哇哦,光线一闪而过,吸光度的数值就出来了。
记得要认真记录,不然一会儿回去就得“对账”了。
接着,咱们再测一下样品的吸光度,看看这份“闯入者”的真实面目。
最终,结合标准曲线,就能推算出样品里的铁含量了。
4. 实验结果与讨论经过一番波折,数据总算收集齐了。
看着那一串串的数字,我忍不住感慨,这数据就像是我的孩子,每一个都那么珍贵。
结合标准曲线,计算出样品中铁的浓度,心里真是有种“如释重负”的感觉。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
分光光度法测定铁含量(精)
————————————————————————————————作者:————————————————————————————————日期:
姓名:封德军指导老师:陶明
学号:1004010026 班级:2010级化学专业
一、实验目的:
1、初步熟悉 722型分光光度计的使用方法。
2、熟悉测绘吸收光谱的一般方法。
3、学习如何选择分光光度分析的实验条件
二、实验原理 : 1、在 pH =2~9 的溶液中, 邻二氮菲 (phen 与 Fe 2+生成稳定的红色配合物 , 反应方程式为 :2Fe 3++2NH2OH.HCl → 2Fe
2++N2+H2O+4H++2Cl+, 其最大吸收峰在 515nm 处。
根据朗伯比尔定律:
A=Kbc,溶液中浓度与其吸光度之间具有直线关系, 可用标准曲线法测定。
三、实验步骤:
1、用吸量管吸取 0.0ml 和 5ml 铁标准使用液分别注入两个 50ml
容量瓶中,加入 1ml 盐酸羟胺溶液, 摇匀。
再加入 2ml 领二氮菲水溶液, 5ml
醋酸钠水溶液,用水稀释至刻度,摇匀,放置 10min 。
2、取两支 1cm 比色皿,
先用蒸馏水清洗 2-3次再用试液润洗 3-4次, 分别将配好的铁标准使用液注入比色皿, 并用镜头纸拭去光洁面的试液。
以试剂空白(即 0.0ml 铁标准溶液
为参比溶液,调节分光光度计使其在参比溶液中透光率为 100%。
在 440-570nm
之间,每隔 10nm 测一次吸光度,最后测的在 510nm 附近吸光度最大。
在最大吸
收峰附近, 每隔 5nm 测量一次吸光度, 即在 505nm 与 515nm 处分别测
量一次吸光度。
3、显色剂用量的确定:在 7 只 50 ml 容量瓶中,各加 10ml 铁标准溶液和
20ml盐酸羟胺溶液, 摇匀。
分别加入 0.2, 0.4, 0.6, 0.8, 1.0, 2.0, 4.0 ml
邻二氮菲溶液,再各加 5.0 ml 乙酸钠溶液, 以水稀释至刻度,摇匀。
放置 10min,
以水为参比,在选定波长下测量各溶液的吸光度。
以显色剂邻二氮菲的体积为横坐标、相应的吸光度为纵坐
标,绘制吸光度-显色剂用量曲线,确定显色剂的用量。
4、铁标准曲线的测定:取 6个50 ml容量瓶,编序号为 1 2 3 4 5 6 7并分别加入铁标准溶液 (10ug/ml0.00ml 0.20ml 0.40ml 0.60ml 0.80ml 1.00ml 试样 , 盐酸羟氨 (20g/L 2ml, 摇匀。
用水稀释
至刻度,摇匀后再放置 10min 。
用 1cm 比色皿,以空白为参比溶液, 在 510nm
处测量各吸光度。
5、石灰石中试样铁的测定:准确称取 0.4-0.5g 于 100ml 烧杯中,
加入少量蒸馏水润湿,小心滴加 3mol/L盐酸溶液至式样溶解,转移至 50ml
容量瓶中,用少量蒸馏水淋洗烧杯数次,一并转移至容量瓶
中。
按标准曲线的制作步骤,加入各种试剂,测量吸光度。
四、数据处理及结果:
2、不同显色剂用量时的吸光度 :
3、不同浓度的铁标准溶液时吸光度:(0.29g 试样
此图线性关系较好
五、讨论:
1、在进行数据测量时波长选择从大到小的方式进行测量,且当
波长调整时出现以下情况如 (待测波长为 510nm 但调整时波长变为了
508或更小时,应将波长调为 520后再调为 510nm 即为了减小机械误差。
2、在运用 y=ax+b这个公式时 r 2≥ 0.98时说明线性关系较好。
六、思考题:
1、加入盐酸羟氨和醋酸钠的作用?
答:盐酸羟氨作用是还原 Fe3+,醋酸钠作用是作为缓冲剂 2:使用
722型分光光度计及比色皿时应注意什么问题?
答:取拿比色皿时,手指只能捏住比色皿的毛玻璃面,而不能碰
比色皿的光学表面比色皿不能用碱溶液或氧化性强的洗涤液洗涤, 也
不能用毛刷清洗。
比色皿外壁附着的水或溶液应用擦镜纸或细而软的
吸水纸吸干,不要擦拭,以免损伤它的光学表面。
3、吸光度的加和性原则是什么?
答:溶液中总的吸光度等于溶液中各组分吸光度之和。
