分析化学期中考试考试题答案
分析化学期中考试题答案

分析化学(一)期中考试题答案一、选择题 ( 共10题 20分 )1. D2. B3. A4. D5. A6. D7. B8. C9. D 10. C二、填空题 ( 共15题 30分 )1. 1.B;2.D;3.C;4.A2. 橙红至黄,黄至橙3. 取样、 试样分解、 干扰组分的掩蔽和分离、 测定、 计算结果。
4. 第二 , 35. 溶解、 熔融、 干灰化6. c /K a 1= 0.010/(1.2×10-3) < 500[]()()L mol 1092201001021410211021H 33233/.....----+⨯=⨯⨯⨯+⨯+⨯-= pH = 2.547. (1)[][][][][][]3342443NH PO 2HPO OH PO H H +++=+---+(2)[][][]-+=+OH HAc H8. 5;9. 100 ; 10. [][]622200100lg 922P H HP lg p pH 2a 1....K =+=+=- 11. 1,0.1;12. 1.8×10-4, 2.4×10-8 (10-3.75, 10-7.62) ;13. NH 4Cl-NH 3·H 2O ;14. -0.02 %,-1.5 %;15. [][][][][]--++++=++F OH CaF Ca 2H 2三、计算题 ( 共 3题 30分 )[]()[]()62.11,38.2,/102.410100.0cK 2 87.2/1035.110100.0cK 1.1375.31374.4==⨯=⨯===⨯=⨯==-----+pH pOH L m ol OH pH L m ol H b a )()(2.0.1000×24.25×500×80.04w (NH 4NO 3) = ───────────────── ×100% = 97.1%25×4.000×100097.1换算成干试样时, w '(NH 4NO 3) = ────── = 99.2%(1-2.20%)3. (20.01+20.04+20.04+20.05+20.06)平均值x = ──────────────── %5= 20.04%s x x i =-=∑()/.240019查表得置信度为95%的t 值为2.78所以 μ=±=±t s n (...)%2004%27800195= (20.04 ± 0.024)% ≈ (20.04 ± 0.02)%四、问答题 ( 共 4题 20分 )1. 进行对照试验,回收试验,空白试验,校准仪器和用适当的方法对分析结果校正。
分析化学期中考试考试题答案

分析化学考试题(化工专业)一、填空题每填空1分,共32分)1.根据测量原理分类,分析方法有(化学分析)和(仪器分析)。
2.定量分析过程通常包括(取样);(试样的分解);(待测组分测定);(结果计算)。
3.用沉淀法测定纯NaCl中氯的质量分数,得到下列结果:0.5982,0.6000,0.6046,0.5986,0.6024。
则平均结果为(0.6009 );平均结果的绝对误差为(-5.7x10-3 );相对误差为(-0.94% );中位数为(0.6006 );平均偏差为(2.1x10-3 );相对平均偏差为(0.35% )。
4.按照有效数字的运算规则,下列计算式的结果各应包括几位有效数字:(1)213.64+4.402+0.3244 (五)位;(2)0.1000 x (25.00-1.52)x 246.47/(1.000x1000)(四)位;(3)pH=0.03求H+浓度(两)位。
5. 在分析过程中,下列情况各造成何种(系统、随机)误差。
(1)称量过程中天平零点略有变动(随机误差);(2)分析用试剂中含有微量待测组分(系统误差);6. 标定HCl溶液的浓度时,可用Na2CO3或硼砂(Na2B4O7 10H2O)为基准物质,若Na2CO3吸水,则测定结果(偏高):若硼砂结晶水部分失水,则测定结果(偏低);(以上两项填无影响、偏高、偏低)。
若两者均保存妥当,不存在上述问题,则选(硼砂)作为基准物质更好,原因为(HCL与两者均按1:2计量比进行反应,硼砂摩尔质量大,称量时相对误差小)。
7. 从质量保证和质量控制的角度出发,为了使分析数据能够准确地反映实际情况。
要求分析数据具有(代表性)、(准确性)、(精密性)、(可比性)和(完整性)。
这些反映了分析结果的(可靠性)。
8. 浓度为c(mol/L)H2C2O4溶液的电荷平衡方程:([H+]=[OH-]+[ HC2O4-]+2[C2O42-])9. 根据酸碱质子理论,OH-的共轭酸是(H2O ),HAc的共轭酸是(H2Ac+)。
【免费下载】分析化学2期中试卷 答案

云南大学2011至2012学年上学期化学科学与工程学院《分析化学(2)》期中考试(闭卷)试卷A满分:100分考试时间:120分钟任课教师:_________专业学号姓名题号一二三四五总分得分一、选择题(每小题1分,共25分。
请把答案填写在下表中)题号12345678910111213答案B B D A C B A A D C B D C 题号141516171819202122232425答案B B C C A A D B D D C B1.光谱分析法通常可以获得其它分析方法不能获得的__________。
A.组成信息B.原子或分子的结构信息C. 化合物的存在形态信息D.化合物的极性大小信息2.原子发射光谱的产生是由于________。
A.原子次外层电子在不同能级间的跃迁B.原子外层电子在不同能级间的跃迁C.原子内层电子在不同能级间的跃迁D.原子外层电子的振动和转动3.原子发射光谱中,激发光源的作用是______。
A. 使样品干燥和蒸发B.使样品原子化C.使气态的基态原子激发D.包括A、B、C三种作用4. 在原子发射光谱的光源中,激发温度最高的光源是_______。
A. 高压火花B.直流电弧 C. 交流电弧D.ICP5.ICP光源高温的产生是由于________。
A. 气体燃烧B.电极放电C.气体放电D.电火花6.采用摄谱法进行原子发射光谱的定性分析时通常使用的标准光谱是_________。
A. 铜谱B.铁谱 C. 碳谱D.氢谱7.原子吸收光谱法中,原子化器的作用是。
A:使样品中待测元素转化为气态的基态原子;B:使样品中待测元素转化为激发态原子;C:使样品中待测元素转化为中性分子;D:使样品中待测元素转化为离子。
8.关于多普勒变宽的影响因素,以下说法正确的是_________。
A. 随温度升高而增加B.随温度升高而下降C.随待测原子的摩尔质量增大而增大D.随压力增大而减小9.空心阴极灯中对发射线半宽度影响最大的因素是_________。
沪教版九年级化学(上册)期中质量分析卷及答案

沪教版九年级化学(上册)期中质量分析卷及答案(时间:60分钟 分数:100分) 班级: 姓名: 分数:一、选择题(每小题只有1个选项符合题意。
共20小题,每题2分,共40分)1、过氧化钠(Na2O2)可作呼吸面具中氧气的来源,它与二氧化碳反应后的生成物为( )A .Na 2CO 3和H 2B .Na 2O 和O 2C .NaOH 和O 2D .Na 2CO 3和O 2 2、科学家合成了核电荷数为114的原子,该原子的相对原子质量为289,则该原子的中子数与电子数之差是( )A .114B .61C .175D .2893、南京理工大学胡丙成团队用新方法制得了 NaN5·3H2O ,该化合物中含有等微粒,下列有关说法正确的是( )A .5N -是一种单质B .一个5N -带一个单位的正电荷C .一个5N -中共有36个质子D .一个5N -中共有36个电子4、考古学家通过测定碳14的含量等方法将人类生活在黄土高原的历史推前至距今212万年。
碳14原子的核电荷数为6,相对原子质量为14,则该原子核外电子数为( )A .6B .8C .14D .20 5、下列实验设计不能达到其对应实验目的的是( )A .测定空气里氧气的含量B .检查装置的气密性C .验证质量守恒定律D .证明CO 2密度比空气的大6、某同学在量取10mL 水时,视线仰视,则他量取的水的实际体积( )A.等10mL B.小于10mL C.大于10mL D.无法判断7、如图表示治理汽车尾气所涉及反应的微观过程。
下列说法不正确的是()A.图中单质的化学式为NB.生成物不属于空气质量标准监控对象2C.该反应属于置换反应 D.生成单质与化合物的质量比为7:228、地壳中含量最多的非金属元素是()A.Si B.Fe C.Al D.O9、生活中常接触到的“加铁酱油”“含氟牙膏”中的铁、氟是指()A.单质B.元素C.原子D.分子10、下列关于金属材料的说法中,不正确的是()A.常温下,铝能与空气中的氧气反应,在其表面生成致密的氧化铝薄膜B.铁在干燥的空气中容易生锈C.硬铝(铝合金)的硬度大于纯铝D.金属资源的回收利用既保护了环境,又节约了金属资源11、实验室用高锰酸钾制氧气的实验中,不需要使用的一组仪器是A.烧杯、玻璃棒 B.大试管、集气瓶C.酒精灯、铁架台 D.导管、单孔塞12、将金属M的粉末放入盛有硝酸铜溶液的烧杯中,充分反应后,溶液呈无色,继续向烧杯中加入一定量的硝酸银溶液,充分反应后过滤,得到滤渣和蓝色滤液。
分析化学期中试卷-2(含答案)

化学与环境学院院、系2010 /2011 学年(下)学期期中考试试卷《分析化学》专业年级班级姓名学号一:选择题(20×2分)1、已知某溶液的氢离子浓度为0.0063,该溶液的pH值是:()A) 2.20;B) 2.201;C) 2.2007 ;D) 2.22、已知硼砂(Na2B4O7·10H2O)的摩尔质量为381.4 g/mol,用它来标定0.1 mol/L HCl溶液,宜称取硼砂为:( )A) 0.45g左右;B) 0.9 g左右;C) 2.25 g左右;D) 4.5g左右3、四人同时分析一矿物中的含硫量,每次取样3.5 g,分析结果表示合理的是:()A) 0.0419%;B) 0.04190%;C) 0.04%;D) 0.042%4、下列说法正确的是( )A)准确度高精密度一定高;B)精密度高准确度一定高;C)准确度高低与精密度无关;D)上述说法均不正确5、下列表述中,最能说明偶然误差小的是:()A) 高精密度;B) 与已知含量的试样多次分析结果的平均值一致;C) 误差小;D) 仔细校正所用砝码和容量仪器等6、常采用标准品对照来检验方法的准确度,采用()方法检验测定结果与标准值之间是否存在系统误差A) F检验;B) t检验;C) F检验后,进行t检验;D) G检验7、测定(NH4)2SO4中的氮时,不能用NaOH直接滴定的原因是:()A) NH3的Kb太小;B) (NH4)2SO4不是酸;C) NH4+的Ka太小;D) (NH4)2SO4中含有游离的H2SO48、用NaOH滴定等浓度的某弱酸HA,当滴定至50%时,溶液的pH=5.00;滴定至100%时,溶液的pH=8.00;滴定至200%时,溶液的pH=12.00,则该弱酸的pKa 为:()A) 5.00;B) 8.00;C) 12.00;D) 6.509、有关酸碱指示剂的描述,正确的是:()A) 能指示溶液的确切pH值;B) 能在pH值一定的变化范围内呈现不同颜色;C) 显酸色时溶液为酸性,显碱色时溶液为碱性;D) 都是有机弱酸10、在滴定分析中,所使用的锥形瓶中沾有少量蒸馏水,使用前:( )A) 需用滤纸擦干;B) 必须烘干;C) 不必处理;D) 必须用标准溶液润洗2~3次11、滴定突跃范围一定在偏碱区域的是:()A) 强酸滴定强碱;B) 强碱滴定一元弱酸;C) 强酸滴定一元弱碱;D) 强碱滴定多元酸12、如果NaOH标准溶液吸收了空气中的CO2,当用其测定米醋中的醋酸含量时,所得结果将:()A) 偏高;B) 偏低;C) 不受影响;D) 不确定13、用HCl标准溶液滴定一元弱碱时,一定能使滴定突跃增大的情况是:()A) K b不变,c弱碱减小;B) pK b减小,c弱碱增大;C) K b减小,c弱碱增大;D) K b增大,c弱碱减小14、配制NaOH标准溶液时,正确的操作方法是:()A) 在托盘天平上迅速称取一定质量的NaOH,溶解后用容量瓶定容;B) 在托盘天平上迅速称取一定质量的NaOH,溶解后稀释至一定体积,再标定;C) 在分析天平上准确称取一定质量的NaOH,溶解后用量瓶定容;D) 在分析天平上准确称取一定质量的NaOH,溶解后用量筒定容15、在水溶液中共轭酸碱对Ka与Kb的关系是:( )A) Ka•Kb=1;B) Ka•Kb=Kw;C) Ka/Kb=Kw;D) Kb/Ka=Kw16、以下溶液用纯水稀释10倍时pH改变最小的是:( )A) 1 mol/L NaAc-1 mol/L HAc溶液;B) 0.1 mol/L HCl溶液;C) 0.1 mol/L HAc溶液;D) 1 mol/L NH3·H2O溶液17、用邻苯二甲酸氢钾标定NaOH溶液浓度时会造成系统误差的是()A) 用甲基橙作指示剂;B) NaOH溶液吸收了空气中的CO2;C) 每份邻苯二甲酸氢钾质量不同;D) 每份加入的指示剂量不同18、已知H3AsO4的pKa1= 2.2, pKa2= 6.9, pKa3= 11.5,则在pH=7.0时,溶液中[H3AsO4]/[AsO43-]等于:( )A) 100.4;B) 10-0.4;C) 10-5.2;D) 10-4.819、以甲基红指示剂,能用NaOH 标准溶液准确滴定的酸是()A) 甲酸(pKa=3.75);B) 硫酸(pKa2=1.99);C) 乙酸(pKa=4.75);D) 硼酸(pKa=9.24)20、下列酸碱溶液的浓度均为0.1000 mol/L,其中可按二元酸碱被分步滴定的是()A) 乙二胺(pK b1=4.07,pK b2=7.15);B) 邻苯二甲酸(pK a1=2.95,pK a2=5.41);C) 亚磷酸(pK a1=1.30,pK a2=6.60);D) 联胺(pK b1=5.52,pK b2=14.12)二:填空题(40分)1、对某一试样进行平行测定时,若几份试样的分析结果精密度很高,但准确度不好,则可能是由下列原因引起的(答案不止一种)a. 操作过程中发现某份试液有溅失现象;b. 所使用的分析方法会产生正误差;c. 使用未校正过的砝码和容量仪器;d. 读取滴定管读数时,体积有±0.01 mL的误差;e. 使用不纯的试剂;f. 称样不均匀;g. 称样前,试样吸水。
分析化学题库+参考答案

分析化学题库+参考答案一、单选题(共100题,每题1分,共100分)1.一般情况下,EDTA与金属离子形成的配位化合物的配位比是A、1∶1B、2∶1C、3∶1D、1∶2正确答案:A2.明矾中铝含量的测定应选用()A、EDTA滴定法B、沉淀滴定法C、两者均可用D、两者均不可用正确答案:A3.不属于仪器分析法的特点是()A、灵敏B、快速C、准确D、适合于常量分析E、适用于微量分析正确答案:D4.下列是四位有效数字的是()A、1.00B、1.005C、1.1050D、pH=12.00E、2.1000正确答案:B5.物质的量浓度相同,体积也相同的一元酸和一元碱恰好中和时,溶液A、显酸性B、显碱性C、显中性D、无法确定E、以上均不是正确答案:D6.直接碘量法不能在下列条件下测定()A、中性B、酸性C、弱碱性D、加热正确答案:D7.钙、锌等离子含量的测定应选用()A、EDTA滴定法B、沉淀滴定法C、两者均可用D、两者均不可用正确答案:A8.溴甲酚绿-甲基红指示剂与酚酞指示剂比较具有的特点()A、变色敏锐B、变色范围窄C、两者均是D、两者均不是正确答案:C9.能够用于沉淀滴定的沉淀反应不需要符合的条件是()A、沉淀反应必须能迅速定量完成B、生成的沉淀溶解度必须足够小C、必须有沉淀生成D、必须有适当的指示化学计量点的方法E、必须用AgNO3作滴定液正确答案:E10.用于准确移取一定体积溶液的量器()A、移液管B、滴定管C、量瓶D、锥形瓶E、试剂瓶正确答案:A11.下列哪一种酸只能用非水酸碱滴定A、HCOOH(Ka=1.77×10-4)B、HAc(Ka=1.76×10-5)C、H3BO3(Ka=7.3×10-10)D、苯甲酸(Ka=6.46×10-5)正确答案:C12.下列哪种误差属于操作误差()A、操作人员看错砝面值B、操作者对终点颜色的变化辨别不够敏锐C、加错试剂D、溶液溅失E、用银量法测定氯化物时,滴定时没有充分振摇使终点提前正确答案:B13.减小偶然误差在方法A、多次测量取平均值B、回收实验C、空白试验D、对照试验正确答案:A14.在用HCl滴定液滴定NaOH溶液时,记录消耗HCl溶液的体积正确的是()A、24.100mIB、24.1mlC、24.1000mlD、24.10mlE、24ml正确答案:D15.间接碘量法中用基准物质标定Na2S2O3溶液时,要加入过量的KI,对KI的作用理解不正确的是()A、增大析出I2的溶解度B、作为还原性C、防止I2的挥发D、使反应快速、完全E、作为氧化剂正确答案:E16.下列物质中,可以用氧化还原滴定法测定含量的物质是()A、醋酸B、盐酸C、硫酸D、草酸正确答案:D17.在银量法中要用到的基准物质是()A、Na2CO3B、邻苯二甲酸氢钾C、NaClD、硼砂E、ZnO正确答案:C18.将4克氢氧化钠溶于水中,制成1升溶液,其物质的量为A、4克B、0.1摩尔C、0.1摩尔/升D、1摩尔正确答案:B19.直接碘量法适宜的酸碱度条件是A、弱酸性B、中性C、弱碱性D、强碱性E、A+B+C正确答案:E20.在滴定分析中,对滴定液的要求有:A、准确的浓度B、无色C、性质稳定D、无氧化性E、A+C正确答案:E21.在标定HCL溶液浓度时,某同学4次测定结果分别为0.1018mol/L.0.1017mol/L.0.1018mol/L.0.1019mol/L,而准确浓度为0.1036mol/L,该同学的测量结果为()A、准确度较好,但精确度较差B、准确度较好,精确度也好C、准确度较差,但精确度较好D、准确度较差,精确度较差正确答案:C22.用ZnO标定EDTA溶液浓度时,以EBT作指示剂调解溶液酸度应用()A、六次甲基四安B、氨水C、NH3-NH4ClD、A+BE、B+C正确答案:E23.间接碘量法滴定时的酸度条件为()A、中性或弱酸性B、强碱性C、弱碱性D、强酸性E、弱酸性正确答案:A24.可用来标定NaOH滴定液的基准物是A、邻苯二甲酸氢钾B、硼砂C、无水碳酸钠D、草酸钠E、甲酸正确答案:A25.影响氧化还原反应平衡常数的因素是A、反应物浓度B、温度C、催化剂D、反应产物浓度E、以上均不是正确答案:B26.用 Na2C2O4(A)标定 KMnO4(B)时,其反应系数之间的关系为:A、nA = 5/2 nBB、nA = 2/5 nBC、nA = 1/2 nBD、nA = 1/5 nBE、以上均不是正确答案:A27.影响消耗滴定液的量()A、溶液的浓度B、沉淀的溶解度C、两者都有关D、两者都无关正确答案:A28.用酸碱滴定法测定醋酸的含量()A、超微量分析B、常量分析C、半微量分析D、微量分析E、电位分析正确答案:B29.间接碘量法中,滴定至终点的溶液放置后(5min内)又变为蓝色的原因是()A、空气中氧的作用B、溶液中淀粉过C、KI加量太少D、反应速度太慢E、待测物与KI反应不完全正确答案:E30.在定性化学分析中一般采用()A、常量分析B、仪器分析C、化学分析D、微量分析E、半微量分析正确答案:A31.酸,碱的强度越大()A、ka小于或等于10-7B、间接法配制C、cka³10-8D、Ka>10-7E、突越范围越大正确答案:E32.对直接碘量法与间接碘量法的不同之处描述错误有()A、指示剂不同B、终点的颜色不相同C、加入指示剂的时间不同D、滴定液不同正确答案:A33.AgNO3应储存在A、棕色试剂瓶B、白色容量瓶C、白色试剂瓶D、棕色滴定管正确答案:A34.用基准物质邻苯二甲酸氢钾标定NaOH溶液的浓度,选用的指示剂()A、甲基橙B、酚酞C、两者均可D、两者均不可正确答案:B35.用0.1000mol/LHCl溶液滴定25.00mlNaOH,终点消耗20.00ml,则NaOH溶液的浓度为()A、0.1000mol/LB、0.1250mol/LC、0.08000mol/LD、1.000mol/LE、0.08mol/L正确答案:C36.非水碱量法常用的溶剂是A、醋酐B、稀醋酸C、水D、无水乙醇E、冰醋酸正确答案:E37.提高分析结果准确度的主要方法不包括()A、增加平行测定次数B、减小测量误差C、消除偶然误差D、消除系统误差E、增加有效数字的位数正确答案:E38.下列属于碱性溶剂的是()A、乙二胺B、乙醇C、水D、苯E、乙酸正确答案:A39.提高氧化还原反应的速度可采取()措施。
2022分析化学期中测验(含答案)

2022分析化学期中测验(含答案)一、选择题(单项选择题,每小题2分,共30分)1、分析天平上称取样品7.00某10-2g,其有效数字为:()A、3B、4C、5D、62、某溶液的pH=11.20,其有效数字为:()A、2B、3C、4D、53、用0.1000mol·L-1NaOH溶液滴定0.1000mol·/LHAC溶液时,指示剂应选:()A、甲基橙B、甲基红C、酚酞D、EDTA4、Na2CO3水溶液的质子条件为:()A、[H+]+[H2CO3-]=[OH-]+[CO32-];B、[H+]+[HCO3-]+2[H2CO3]=[OH-]C、[H+]+[HCO3-]+[H2CO3]=[OH-];D、[H+]+2[Na+]+[HCO3-]=[OH-]5、某酸碱指示剂的KHIn为1某10-4,理论上其pH变色范围应为:()A、5—6;B、6—7C、3—5D、2—46、酸碱滴定中选择指示剂的原则是:()A、Ka=KbB、指示剂的变色点pH与化学计量点pH完全符合C、指示剂变色范围处于或部分处于滴定突跃范围内D、指示剂应在pH=7.00时变色7、下列物质均为“分析纯”,何种可用直接法配制标准溶液:()A、固体NaOH;B、液体盐酸;C、固体K2Cr2O7;D、固体Na2S2O38、浓度相同的下列物质水溶液的pH最高的是:()A、NaCl;B、NaHCO3;C、NH4Cl;D、Na2CO33+9、在实验室用EDTA滴定Al,应该采用那种滴定方式比较合适:()A、直接滴定;B、返滴定法;C、置换滴定;D、间接滴定10、根据酸碱质子理论,下列物质中既是酸、又是碱的是:()A、HAcB、COC、HPOD、NH11、下列各组物质中,不能用来制备缓冲溶液的是:()A、HCl和NH3·H2O;B、NaOH和HAc;C、Na2H2PO4和Na2HPO4;;D、NaOH和Na2CO312、某酸碱滴定pH突跃为7.7~9.7,适宜用的指示剂是:()A、苯胺黄(pH变色范围为1.3~3.2)B、甲基橙;C、甲基红D、酚酞13、0.2000mol/LEDTA溶液的TFe2O3/EDTA是()(注:Fe2o3的相对分子质量为159.7)A、0.007985g/ml;B、0.07985g/ml;C、0.1597g/ml;D、0.01597g/ml14、影响EDTA配合物稳定性的因素之一是酸效应,酸效应是指:()A、酸能使EDTA配位能力降低的现象B、酸能使某些电解质溶解度增大或减小现象C、酸能使金属离子M配位能力降低的现象D、酸能抑制金属离子M水解的现象15、下列措施中,与改变吸光光度分析的灵敏度无关的(A)A、改变被测溶液的浓度B、改变被测溶液的温度C、改变入射光波长D、采用不同的显色剂16、某学生在用Na2C2O4标定KMnO4溶液浓度时,所得结果偏高,原因可能是(A)A、将Na2C2O4溶解加H2SO4后,加热至沸,稍冷即用KMnO4溶液滴定,B、在滴定的开始阶段,KMnO4溶液滴加过快,C、终点时溶液呈较深的红色;D、无法判断17、用K2Cr2O7滴定Fe2+时,常用H2SO4-H3PO4混合酸作介质,加入H3PO4的主要作用是(B)A、增大溶液酸度B、增大滴定的突跃范围C、保护Fe2+免受空气氧化D、可以形成缓冲体系18、摩尔吸光系数的单位为(A)A、L/mol·cmB、mol/L·cmC、g/mol·cmD、cm/mol·L119、已知TK2Cr2O7/Fe=0.003284g/ml,且MFe=55.85g/mol,则C(K2Cr2O7)=(A)mol/l6A、0.05880B、0.3528C、0.5880D、0.00588020、待测组分为MgO(相对分子量40.304),沉淀形式为MgNH4PO4·6H2O(相对分子量245.41),称量形式为Mg2P2O7(相对分子量222.55),换算因数F等于(A)(A)0.362(B)0.724(C)1.105(D)2.210二、填空题(每空1分,共20分):1、准确度是描述测定值与()相符合的程度,而()是描述平行测定值之间相一致的程度,两者间,()是保证()的先决条件。
(完整版)分析化学考试题库有答案

分析化学题库第一、二章绪论、误差一、判断题:1.按照测定原理,分析化学常分为化学分析和仪器分析两大类。
( √) 2.分析化学的任务包括定性分析、定量分析、结构分析和形态分析。
(×)3.用高锰酸钾法测定双氧水中过氧化氢的含量是属于滴定分析。
( √) 4.偶然误差是定量分析中误差的主要来源,它影响分析结果的精密度。
( √) 5.只要是可疑值(或逸出值)一定要舍去。
(×)6.被分析的物质称为样品,与样品发生化学反应的物质称为试剂,以化学反应为基础的分析方法称为化学分析法。
( √)7、偏差是测量值与平均值之差。
(×)8、绝对误差是测量值与真实值之差。
( √)9、增加平行测定次数,可以减少系统误差。
(×)10、当偶然误差消除后,分析结果的精密度越高,准确度越高。
(×)11、在滴定分析中,测定结果的精密度越高,其准确度也越高。
(×)12、相对平均偏差、样本标准偏差、总体标准偏差都可用来表示测定值的分散程度。
(×)13.增加测定次数可以提高分析结果的准确度。
(×)14.用20ml移液管移取NaOH溶液,体积数记为20ml。
(×)15.按照测定原理,分析化学常分为化学分析和仪器分析两大类。
( √) 16.用酸碱滴定法测定醋酸的含量,属于化学分析。
( √)17.化学分析是分析化学的基础,仪器分析是分析化学发展的方向。
( √)18.在一定称量范围内,被称样品的质量越大,称量的相对误差就越小。
( √) 19.滴定管的初读数必须是“0.00ml”。
(×)20.测定0.8ml 样品溶液的含量,属于常量分析。
(×)21.测定值与真实值相接近的程度称为准确度。
( √)二、填空题1.配制用的蒸馏水中含有少量被测组分,此情况属于系统误差。
2.用50ml移液管移取NaOH溶液,体积数记为50.00 ml。
3.称量太慢,使试样吸湿,此情况属于系统误差。
分析化学期中考试答案

2011-2012第1学期《分析化学》期中考试答案一、选择题(本大题共10小题,每小题2分,共20分)二、填空题(本大题共10小题,每小题2分,共20分) 1、 Ba 2+, Ca 2+, Mg 2+, K +, Na +, NH 4+。
2、黑, Zn 2+。
3、 38.60% ± 0.63% 。
4、[H 2A] = [HA -]:2.0 ;[H 2A] = [A 2-]:3.5 。
5、 直接法 , 间接法 。
6、_ 5 _, 4 ~ 6 。
7、 C K a1≥10-8, C K a2≥10-8, K a1/ K a2 ≥105 。
8、 [H +]+[HCO 3-]+2[H 2CO 3] = [NH 3]+[OH - ] 9、 0.005055 (g/mL) 。
10、 β= 2.3C δHA δA , 0.58 mol.L -1.pH -1。
三、问答题(本大题共3小题,共20分)1、答:因为称取的Na 2CO 3实际质量m 偏低,所以标定时消耗的HC1溶液体积V 偏小,根据HCl 溶液浓度的计算式:C = (2m/M) / V 可知,V 偏小,HC1溶液浓度C 偏高。
用此HCl 溶液测定某有机碱的摩尔质量时,根据有机碱的摩尔质量的计算式:M = m / (CV) ,C 的数值偏高,有机碱的摩尔质量M 偏低。
2、答:酸碱指示剂本身是一种有机弱酸碱,也会参加质子的转移反应,其酸式体和碱式体结构不同,颜色也不同。
根据酸碱指示剂的解离平衡:HIn(颜色1) = H + + In -(颜色2)可知,在计量点附近时,当溶液酸度发生变化时,酸碱指示剂结构发生变化,酸式体和碱式体的浓度比发生变化,其颜色也将发生变化。
3、答:反应方程式:(1)CaCO 3 +2HCl(已知过量) = CaCl 2 + CO 2↑+ H 2O (2)HCl(剩余) + NaOH = NaCl + H 2O主要试剂:标准HCl 溶液,标准NaOH 溶液,酚酞指示剂 主要仪器:碱式滴定管,锥形瓶,移液管,称量瓶含量计算式:%100210)(%333⨯⨯⨯-=-sCaCO NaOH NaOH HCl HCl CaCO m M V C V C w四、计算题(本大题共4小题,每小题10分,共40分)1、解:)(0479.01069.159100.02613/32722--•=⨯⨯⨯=mL g T O Fe O Cr K )(0463.01055.231100.03613/43722--•=⨯⨯⨯=mL g T O Fe O Cr K 2、解:方法一: (1)L mol C V C PO H NaOH PO H /04110.0;04120.0,04110.0,04100.0;00.251000.0214343=⨯⨯=(2)%2.0%10004110.030001.00000.00001.0=⨯⨯++=r d(3)0001.0130001.00000.00001.0222=-++=S%2.0%10004110.00001.0%100=⨯=⨯=xS S r方法二 (1)20.5020.5520.6020.55()3VmLL mol C PO H /04110.000.2555.201000.02143=⨯⨯=(2)%16.0%10055.20305.000.005.0=⨯⨯++=r d(3)2220.050.000.050.0531S%2.0%10055.2005.0%100=⨯=⨯=xS S r3、解:(1)化学计量点:444[]11()(1.00014.00 4.74) 5.1322W NH NH bWb NHK H C KaC K pHpC pK pK(2)滴定突跃范围:-0.1%:340.1%lg14.00 4.74lg6.2699.9%NH aNHC pHpK C+0.1%: []00.4)2200.0%1.0lg(2%1.003=⨯-=⇒⨯=+pH C HNH4、解:V 1=10.50mL,V 2=20.50mL ,∵V 2>V 1∴试样由Na 2CO 3和NaHCO 3组成=⨯⨯⨯⨯=-%100000.199.1051050.101000.0%332CO Na 11.13%=⨯⨯⨯-⨯=-%100000.101.8410)50.1050.20(1000.0%33NaHCO 8.40%。
分析化学期中考试试题

分析化学期中考试试题一、单项选择题。
(每题2分,共40分)1误差是衡量 .............................................................. ( )A. 精密度B.置信度C.准确度D.精确度2、........................................... 分析测定中论述偶然误差正确的是( )A. 大小误差出现的几率相等B.正误差出现几率大于负误差C.负误差出现几率大于正误差D.正负误差出现的几率相等3、计算x=11.25+1.3153+1.225+25.0678,答案x 应为....................... ( )A.38.66B.38.6581C.38.86D.38.674、有两组分析数据,要比较它们的精密度有无显著差异,则应用 ......... ( )A. t检验B. F检验C. Q检验D. u检验5、在置信度为95%时,测得Al 2O3的平均值的置信区间为35.21 ± 0.10,其意是( )A. 在所测定的数据中有95%的数据在此区间内B. 若再进行测定系列数据,将有95%落入此区间C. 总体平均值卩落入此区间的概率为95%D. 在此区间内包括总体平均值□的把握有95%6、二乙三胺五乙酸(H5L)的pKa1~pKa5分别为1.94, 2.87, 4.37, 8.69, 10.56。
其溶液中的Na2H3L组分浓渡最大的pH值是....................................... ( )A.3.62B.5.00C.9.62D. 2.877、浓度为cmol/L的H2SO4和HCOOH混合液的质子条件是 .................... ( )- 2 -A. [H +]=[OH ]+[HSO 4 ]+[SO 4 ]+[HCOO ]B. [H +]=[OH ] +[SO 4 ]+[HCOO ]—2 -C. [H+]=[OH ]+[HSO 4 ]+2[SO 4 ]+[HCOO ]+ - 2D. [H ]=[OH ]+[HSO 4 ]+2[SO 4 ]8、用NaOH 滴定H3PO4 (pKa1~ pKa3 分别为2.12, 7.20, 12.36)至第二计量点,pH 值为..................................................................... ( )A.10.70B.9.78C.8.74D.7.789、在pH=10.0 的氨性溶液中,已计算出Zn(NH3) =104.7, zn(oH) 卩2" , y(H) 卩0",则在此条件下,lgK MY为(已知IgK MY =16.5) ............................... ( )A.8.9B.11.8C.14.3D.11.310、铬黑T (EBT )与Ca2+的络合物的稳定常数K ca-EBT=105.4,已知EBT的逐级质子化常数K H1=1011.6,K H2= 106。
分析化学期中考试题(答案)

16、已知用0.1000 mol·L-1NaOH滴定0.1000 mol·L-1HAc(pKa=4.74)时的pH突跃范围是7.74-9.70,可以推断用1.000 mol·L-1NaOH滴定等浓度的某一元弱酸HB(pKa=2.74)时的pH突跃范围是……………………………………………(E);
A 11.00;B 9.00;C 8.50;D 9.50
19、下列溶液能用酸碱滴定法直接准确滴定的是………………………………(E)。
(1) 0.10mol/L (CH2)6N4·HClpKb[(CH2)6N4] = 8.85
(2) 0.10mol/L NH4ClpKb(NH3) = 4.74
(3)0.10 mol/L HCNpKa(HCN)= 9.21
g·mol-1)的滴定度 (单位:g·mL-1)为………………………………(B)。
A0.01001;B0.005004;C0.002502;D10.01;E 5.004;F 2.502
6、在分析工作中要减小测定的随机误差可采取的方法为………………………(C)。
A对照试验;B空白试验;C多次平行试验;D校准仪器;E回收试验。
学院班级姓名学号
…………………密……………封……………线……………密……………封………………………………
嘉应学院化学与环境学院2016-2017学年第二学期期中考试试卷
《分析化学》试题
(考试形式:闭卷,考试时间:120分钟)1605-1607班
题号
一
二
三
四
五
六
七
总分
复核人
得分
评卷人
一、选择题(每个选项1.5分,共30分)
大学分析化学期中试题

分析化学(一)期中考试试卷学号班级姓名分数一、选择题( 共10题20分)1. 2 分表示一组数据离散特性的最好标志是------------------------------------------( )(A)全距(B)偏差(C)平均偏差(D)标准差2. 2 分已知H3PO4的p K a1 = 2.12, p K a2 = 7.20, p K a3 = 12.36。
今有一磷酸盐溶液的pH = 4.66, 则其主要存在形式是-------------------------------------------------------------( )(A) HPO42-(B) H2PO4-(C) HPO42- + H2PO4(D) H2PO4-+ H3PO43. 2 分用0.10 mol/LNaOH溶液滴定0.10 mol/L HA(K a=5.0×10-5), 若终点的pH为9.0, 则终点误差为----------------------------------------------------------------------------( )(A) +0.02% (B) +0.01%(C) -0.02% (D) -0.01%4. 2 分磷以MgNH4PO4·6H2O形式沉淀,经过滤、洗涤后用适量HCl标准溶液溶解,而后以NaOH标准溶液返滴定,选甲基橙为指示剂,这时磷与HCl的物质的量比n(P):n(HCl)为---------------------------------------------------------------------------( )(A) 1:3 (B) 3:1 (C) 1:1 (D) 1:25. 2 分将PO43-以MgNH4PO4·6H2O形式沉淀,经过滤、洗涤后先用过量HCl标准溶液溶解, 而后以NaOH标准溶液返滴定,此时应选的指示剂是------------------( )(A) 甲基橙(B) 石蕊(C) 酚酞(D) 百里酚酞6. 2 分以下溶液稀释10倍时,pH改变最大的是--------------------------------------( )(A) 0.1mol/L NH4Ac (B) 0.1mol/L NaAc(C) 0.1mol/L HAc (D) 0.1mol/L HCl7. 2 分下面四种表述中,正确的是--------------------------------------------------------( )(1) 置信水平定得越高越好(2) 置信水平太高,对总体平均值的估计往往失去意义(3) 置信水平越高置信区间越宽(4) 置信水平越高置信区间越窄(A)1,2 (B)2,3 (C)3,4 (D)4,18. 2 分今有1L含0.1mol H3PO4和0.3mol Na2HPO4的溶液,其pH应当是--------( )(H3PO4的p K a1~p K a3分别为2.12、7.20、12.36)(A) 2.12 (B) (2.12+7.20)/2 (C) 7.20 (D) (7.20+12.36)/29. 2 分将13.5g六次甲基四胺加到4.0mL 12mol/L HCl中,稀释至100mL,其pH为( ) {p K b[(CH2)6N4] = 8.85, M r[(CH2)6N4] = 140.0}(A) 0.32 (B) 2.57 (C) 4.43 (D) 5.1510. 2 分c(NaCl) = 0.1mol/L的NaCl水溶液的质子平衡式是-------------------------( )(A) [Na+] = [Cl-] = 0.1mol/L (B) [Na+]+[Cl-] = 0.1 mol/L(C) [H+] = [OH-] (D) [H+]+[Na+] = [OH-]+[Cl-]二、填空题( 共15题30分)1. 2 分以下测定和标定各应采用的滴定方式分别是:(填A,B,C,D)(1) 用酸碱滴定法测定CaCO3试剂的纯度____(2) 以K2NaCo(NO2)6形式沉淀,再用KMnO4滴定以测定K+ ____(3) 用K2Cr2O7标定Na2S2O3____(4) 用H2C2O4标定KMnO4____(A)直接法(B)回滴法(C)置换法(D)间接法2. 2 分以甲基橙为指示剂,用NaOH滴定HCl时,终点颜色变化是___________________,用HCl滴定NaOH时,终点颜色变化是__________________________________。
分析化学期中考试试题(答案)
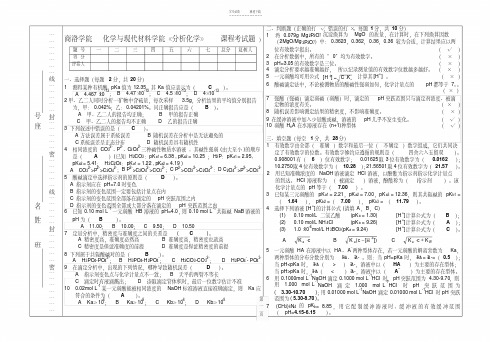
K 2Cr2O7 溶液的物质的量浓度;(2)K 2Cr2O7 对 Fe2+的滴定度(T
)和 K 2Cr2O7
K 2 Cr 2 O 7 / Fe
T 对 Fe2O3 的滴定度(
)(9 分)
K 2 Cr 2 O 7 / Fe 2 O3
解: (1) C m / M
V
2.4515 / 294.18 500.0 10 3
号…
座
密 …
…
…
…
…
线
…
…
…
…
名…
封
姓…
…
…
班…
…
密
…
…
…
…
…
…
…
4. 下列酸碱溶液浓度均为 0.10 mol·L-1,能否采用等浓度的滴定剂直接准确进行滴
定? (共 5 分)
(1)H3BO3 (2 分)
(3)(CH 2)6N4·HCl
( 3 分)
解:( 1) CSP?Ka=0.050 × 5.8 ×-101<010-8 ( 1 分)
=0.007986g m·L-1
(2 分)
或: T = T · K 2Cr2O7 / Fe2O3
K 2 Cr2 O7 / Fe
M Fe2 O3
=0.005586×
159.69
=0.007986g·
-1
mL
2M Fe
2 55.85
第 二 页
(1 分) (1 分 )
学习必备
欢迎下载
…
…
…
…
…
封
…
…
…
…
[H +] 计算公式为(
B ); A ); C )。
《分析化学》期中考试

《分析化学》期中考试1、徐寿:考质求数之学,乃格物之大端,而为化学之极致也”。
这句话中考质”、求数”分别表示()革选题]*A、定性分析、定量分析正确答案)B、定量分析、定性分析C、定性分析、结构分析D、定量分析、结构分析2、下列各项定义中不正确的是()革选题]*A、绝对误差是测定值和真值之差B、相对误差是绝对误差在真值中所占的百分率C、绝对偏差是指测定值与平均值之差D、准确度是反映数据的分散程度正确答案)3、定量分析中,精密度与准确度之间的关系是()单选题]*A、精密度高,准确度必然高B、准确度高,精密度也就高C、精密度是保证准确度的前提(正确答案)D、准确度是保证精密度的前提4、偶然误差具有()单选题]*A、可测性B、重复性C、不确定性(正确答案)D、可校正性5、下列哪种方法可以减小分析测试定中的偶然误差()革选题]*A、对照试验B、空白试验C、仪器校正D、增加平行试验的次数正确答案)6、在进行样品称量时,由于汽车经过天平室附近引起天平震动是属于()单选题]*A、系统误差B、偶然误差正确答案)C、过失误差D、操作误差7、可用下列何种方法减免分析测试中的系统误差()革选题]*A、进行仪器校正正确答案)B、增加测定次数C、认真细心操作D、测定时保证环境的湿度一致8、分析工作中实际能够测量到的数字称为()革选题]*A、精密数字B、准确数字C、可靠数字D、有效数字正确答案)9、下面数值中,有效数字为四位的是()单选题]*A、0. 060pH=11.50Pka = 1.380D、0.6正确答案)10、按有效数字运算规则,213.64+3.8+0.38 =)革选题]*A、217.82B、217C、217.正确答案)D、217.82011、在不加样品的情况下,用测定样品同样的方法、步骤,对空白样品进行定量分析,称之为()革选题]*A、对照试验B、空白试验正确答案)C、平行试验D、预试验12、滴定分析中,对化学反应的主要要求是()单选题]*A、滴定剂必须是基准物B、反应必须有颜色变化C、滴定剂与被测物必须是1:1的计量关系D、反应必须定量完全反应正确答案)13、直接法配制标准溶液必须使用()革选题]*A、基准试剂正确答案)B、化学纯试剂C、分析纯试剂D、优级纯试剂14、滴定管可估读到±).01mL,若要求滴定的相对误差小于0.1%,至少应耗用体积()mL [单选题]*A、10(正确答案)B、20C、30D、4015、欲配制10mL 0.1mol/L HCl溶液,应取浓盐酸12mol/L HCl()mL。
分析化学期中考试试题(含答案)

分析化学期中考试试题(含答案)一、选择题1. 下列哪种物质在水溶液中会发生水解反应?A. NaClB. NaOHC. CH3COONaD. Na2CO3答案: C、D:水解反应是指盐类在水中与水分子反应生成弱电解质的过程。
选项中,CH3COONa(醋酸钠)和Na2CO3(碳酸钠)都是弱酸的盐,因此在水中会发生水解反应,生成对应的弱酸和碱。
而NaCl(氯化钠)是强酸强碱盐,不会发生水解反应;NaOH(氢氧化钠)是强碱,也不会发生水解反应。
二、填空题2. 填写下列反应的化学方程式:(1)铁与稀硫酸反应生成硫酸亚铁和氢气。
(2)氢氧化钠与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠。
答案:(1)Fe + H2SO4 → FeSO4 + H2↑(2)2NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4:(1)铁与稀硫酸反应,铁作为还原剂,将硫酸中的氢离子还原成氢气,生成硫酸亚铁。
化学方程式为:Fe + H2SO4 → FeSO4 + H2↑。
(2)氢氧化钠与硫酸铜溶液反应,氢氧化钠中的氢氧根离子与硫酸铜中的铜离子结合,生成氢氧化铜沉淀,同时生成硫酸钠。
化学方程式为:2NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4。
三、计算题3. 20g的氢氧化钠溶液中,含有5g的氢氧化钠,计算该溶液的质量分数。
答案: 25%:质量分数是指溶质的质量与溶液总质量的比值,通常用百分比表示。
计算公式为:质量分数 = (溶质质量 / 溶液总质量) × 100%。
因此,该溶液的质量分数为:(5g / 20g) × 100% = 25%。
四、问答题4. 请解释什么是氧化还原反应,并举例说明。
答案:氧化还原反应是指化学反应中,原子或离子失去或获得电子的过程。
在氧化还原反应中,氧化剂会接受电子,被还原;还原剂会失去电子,被氧化。
:举例说明:- 反应方程式:Zn + CuSO4 → ZnSO4 + Cu在这个反应中,锌(Zn)失去电子,被氧化,生成锌离子(Zn^2+),因此锌是还原剂。
分析化学期中考试题(答案)

13、0.02mol·L-1某一元弱酸能被相同浓度的NaOH标准溶液直接准确滴定,则Ka应符合的条件为…………………………………………………………………(A)。
AKa≥10-6;BKa≥10-8;CKb≥10-6;DKb≥10-8
14、下列物质属于两性物质的是………………………………………………(D)。
(1)NH4Ac(2)NH4H2PO4
解:(1)MBE: [NH3]+[NH4+]=C(1分)
[HAc]+[Ac-]=C(1分)
PBE: [H+]+[HAc]=[OH-]+[NH3](1分)
(2)MBE: [NH3]+[NH4+]=C(1分)
[H3PO4]+ [H2PO4-]+ [HPO42-]+ [PO43-]=C(1分)
故 (2分)
pH=2.64(0.5分)
(3) SP时,溶液的pH由A-解离所决定:
(1分)
(1分)
∵ (0.5分)
∴[OH-]SP= (2分)
pOHSP=5.57 pHSP=8.43(0.5分)
1、根据有效数字的运算规则进行计算:(每小题2分,共4分)
(1)0.0325×5.108×60.05÷139.8=?
解:原式= 0.0325 ×5.11×60.0 ÷140= 0.0712
(2)25.0123+23.75+3.40874=?
解:原式=25.01+ 23.75 + 3.41=52.17
A化学计量点;B滴定误差;C滴定终点;D滴定分析
二、填空题(每空1分,共31分)
分析化学期中考试题(答案)

分析化学期中考试题(答案)分析化学期中考试题(答案)1. 选择题1) 在一次质量为2.5 g的样品中,有1.2 g的氧元素,其氧的质量分数为多少?解答:氧的质量分数 = (氧的质量) / (样品质量) × 100% = (1.2 g) / (2.5 g) × 100% = 48%2) 下列物质中,酸性最强的是:A. Na2SO4B. FeCl3C. H2SO3D. NH3解答:酸性由酸根离子的酸性强弱决定,硫酸根离子(SO4^2-)比氯离子(Cl^-)酸性更强,因此酸性最强的物质是A. Na2SO4。
3) 某元素M的原子量为48,恰好能与氧元素结合成化合物M2O3,求M的化合价。
解答:化合物M2O3表明元素M的化合价为3,因为氧的化合价为-2,而化合物的总电荷为零。
2. 简答题1) 什么是稀释法?解答:稀释法是在已知浓度的溶液中加入溶剂,使其溶液浓度降低的方法。
通过稀释法可以调节溶液的浓度,用以满足实验要求或分析测定的需要。
2) 请简述草酸定量分析法的原理。
解答:草酸定量分析法是基于草酸与高锰酸钾反应的滴定分析方法。
高锰酸钾溶液是一种强氧化剂,草酸是还原剂。
在酸性条件下,草酸与高锰酸钾反应生成无色的四氧化二锰和二氧化碳。
通过滴定的方法,可以确定高锰酸钾溶液中草酸的含量。
3. 计算题1) 某个研究人员称在一种果汁中发现了超过预定值的维生素C含量。
已知该果汁中维生素C的摩尔浓度为0.025 mol/L,某瓶果汁体积为500 mL,求该瓶果汁中维生素C的质量。
解答:维生素C的摩尔质量为176.12 g/mol。
由摩尔浓度可知,该瓶果汁中维生素C的摩尔数为0.025 mol/L × 0.5 L = 0.0125 mol。
维生素C的质量为0.0125 mol × 176.12 g/mol = 2.20 g。
2) 一份未知样品中含有硫酸铜 (CuSO4) 和甲状腺素 (TH)。
分析化学期中考试题(答案)

A 1010.0000;B pH=11.42;C 1000;D π=3.142。
2、甲、乙二人同时分析一矿物中含硫量,每次采样3.500g,分析结果的平均值分别报告为,甲:0.042%;乙:0.04201%。问正确报告应是…………………………(B)。
学院班级姓名学号
…………………密……………封……………线……………密……………封………………………………
嘉应学院化学与环境学院2015-2016学年第二学期期中考试试卷
《分析化学》试题答案
(考试形式:闭卷,考试时间:120分钟)1505-1507班
题号
一
二
三
四
五
六
七
总分
复核人
得分
评卷人
一、选择题(每题1.5分,共30分)
4、分析结果的有效数字位数与待测组分在试样中的相对含量有关。一般具体要求如下:对于高含量组分(>10%)的测定结果应保留(4)位有效数字;对于中含量组分(1%~10%)的测定结果应保留(3)位有效数字;对于微量组分(<1%)的测定结果常取(2)位有效数字。
5、一元弱酸HA在溶液中以HA、A-两种型体存在,若此一元弱酸的解离常数为Ka,两种型体的分布分数分别为δHA、δA-。此一元弱酸的δi-pH曲线中有1个交点,在此交点上pH=(pKa),δHA=δA- =(0.5)。可通过控制溶液的(pH)以得到所需要的某种型体,欲使溶液中以HA为主要的存在型体,则要求pH(<)pKa;欲使溶液中以A-为主要的存在型体,则要求pH(>)pKa。
(1)0.0121×26.54×1.0275=?
解:原式=0.0121×26.5×1.03=0.330(2分)
《分析化学》期中测试题

《分析化学》期中测试题总分100分单选题(只有一个最佳选项) 多选题(答案为两个或两个以上)姓名: [填空题] *_________________________________1.用移液管移取溶液后,调节液面高度到标线时,移液管应怎样操作( ) [单选题] *A.悬空在液面上B.置容器外C.管口浸在液面下D.管口紧贴容器内壁(正确答案)2.下列哪种滴定液不能装于酸式滴定管( ) [单选题] *A.盐酸滴定液B.高锰酸钾滴定液C.氢氧化钠滴定液(正确答案)D.硫代硫酸钠滴定液E.HAc滴定液3.可以配制准确配制浓度的量器为( ) [单选题] *A.滴定管B.移液管C.容量瓶(正确答案)D.锥形瓶E.吸量管4.下列有关偶然误差的叙述中不正确的是( ) [单选题] *A.偶然误差在分析中可消除(正确答案)B.偶然误差正负误差出现的机会相等C.偶然误差由一些不确定的偶然因素造成D.偶然误差不可消除,但可降低5.用25ml移液管移出的溶液体积应记录为 [单选题] *A. 25mlB.25. 0mlC.25.00ml(正确答案)D.25.000mlE.25.0000ml6.根据滴定突跃范围,用氢氧化钠滴定液滴定盐酸时,可选用下列哪种指示剂 [单选题] *A.甲基黄B.酚酞(正确答案)C.两者均可D.两者均不可7.用0.1mo/L的盐酸滴定0.1mol/L的氢氧化钠溶液,当滴定至化学计量点时,溶液的pH为 [单选题] *A.7.0(正确答案)B.4.3C.9.7D.138.下列叙述中结论错误的是 [单选题] *A. EDTA-2Na的酸效应使配合物的稳定性降低B金属离子的水解效应使配合物的稳定性降低C辅助配位效应使配合物的稳定性降低D.各种副反应均使配合物的稳定性降低(正确答案)9.使用铬黑T指示剂的酸度范围是 [单选题] *A. pH<6.3B. pH6.3~11.6(正确答案)C pH>Il.6D pH 6.3±110.用EDTA滴定金属离子,终点所呈现的颜色是 [单选题] *A.EDTA-金属离子配合物的颜色B.指示剂一金属离子配合物的颜色C.游离指示剂自身的颜色(正确答案)D.EDTA的混合色11.在EDTA-2Na的各种存在形式中,能直接与金属离子配合的是 [单选题] *A.Y⁴⁻(正确答案)B.HY³⁻C.H₄YD.H₆Y²⁺12.化学计量点时,指示剂不变色,使得无法判断滴定终点,是因为 [单选题] *A.指示剂封闭现象(正确答案)B.指示剂僵化想象C.发生沉淀反应D.发生氧化反应13.0.1mol/LNaOH滴定20.00ml 0.1mol/L HAc溶液滴定突跃范围在7.76-9.70 可选用什么指示剂? [单选题] *A.甲基红 pH变色范围4.4-6.2B.酚酞 pH8.0-9.8(正确答案)C.甲基橙pH3.1-4.4D.溴百里酚蓝pH6.0-7.614.间接碘法中若酸度过高,,将会发生什么? [单选题] *A.反应不定量易挥发B.I₂易挥发C.终点不明显D.I⁻被氧化,Na₂S₂O₃被分解(正确答案)15.高锰酸钾法测定H₂O₂含量时,调节酸度时应选用 [单选题] *A.HACB.HCLC.HNO₃D.H₂SO₄(正确答案)16.滴定法中,不用另外加指示剂的是 [单选题] *A.重铬酸钾法B.碘量法C.高锰酸钾法(正确答案)D.福尔哈德法17.对高锰酸钾滴定法,下列说法错误的是 [单选题] *A. 可在盐酸介质中进行滴定(正确答案)B.直接法可测定还原性物质C.标准滴定溶液用标定法制备D.在硫酸介质中进行滴定E.可使用自身指示剂18.莫尔法滴定条件应在 [单选题] *A强酸性B.强碱性C.中性或弱碱性(正确答案)D.中性19.碘量法常用的淀粉指示剂属于 [单选题] *A.自身指示剂B.专属指示剂(正确答案)C.氧化还原指示剂D.金属指示剂20.高锰酸钾法用的指示剂属于 [单选题] *A.自身指示剂(正确答案)B.特殊指示剂C.氧化还原指示剂D.金属指示剂21.在EDTA滴定中,要求金属指示剂与待测金属离子形成配合物的条件稳定常数K′(MIn)值应( )。
定量分析化学期中试卷

定量分析化学期中试卷一、填空题(1)EDTA与金属离子形成的络合物具有_____、______、_______和_______等特性。
(2)已知HCN的pKa=9.14,在pH=5.0时,氰化物的酸效应系数为___________。
(3)pH为7.20的磷酸盐溶液(H3PO4的p K a1 = 2.12, p K a2 = 7.20, p K a3 = 12.36), 磷酸盐存在的主要形式为__________和____________; 其浓度比为___________________。
(4)0.1mol/L NaCl溶液的电荷平衡式是_____________________________________。
(5)用甲醛法测定工业(NH4)2SO4{M r [(NH4)2SO4]=132}中氨的质量分数w(NH3), 把试样溶解后用250 mL容量瓶定容,移取25 mL,用0.2 mol/L NaOH标准溶液滴定, 则应称取试样约_________ g。
二、选择题(1)称取钢样2.000 g,充分燃烧后产生的SO2通入50.00 mol 0.01000 mol/L NaOH溶液中吸收,过量的NaOH 用0.01000 mol/L HCl溶液返滴定至酚酞终点,消耗30.00 mL,则钢样中硫的质量分数为( ) [Ar(S)=32.06, H2SO3的pKa1=1.89,pKa2=7.20](A) 0.16 (B) 0.32 (C) 0.08 (D) 0.64(2)以下物质必须采用间接法配制标准溶液的是 ( )(A) K2Cr2O7 (B) Na2S2O3 (C) Zn (D) H2C2O4·2H2O(3)使用碱式滴定管进行滴定的正确操作是 ( )A 用左手捏稍低于玻璃珠的近旁 B用左手捏稍高于玻璃珠的近旁C 用左手捏玻璃珠上面的橡皮管 D用右手捏稍低于玻璃珠的近旁(4)用基准邻苯二甲酸氢钾标定NaOH溶液时,下列情况对标定结果产生负误差的是A 标定完成后,最终读数时,发现滴定管挂水珠B 规定溶解邻苯二甲酸氢钾的蒸馏水为50ml,实际用量约为60mlC 读数时,终点颜色偏深D 锥形瓶中有少量去离子水,使邻苯二甲酸氢钾稀释(5) HPO42-的共轭碱是 ( )(A) H2PO4-(B) H3PO4(C) PO43- (D) OH-(6)用NaOH标准溶液滴定0.1mol/LHCl-0.1mol/L H3PO4混合液,在滴定曲线上出现几个突跃 ( )(A) 1 (B) 2 (C) 3 (D) 4(7)下列溶液用酸碱滴定法能准确滴定的是 ( )(A) 0.1 mol/L HF (p K a = 3.18)(B) 0.1 mol/L HCN (p K a = 9.21)(C) 0.1 mol/L NaAc [p K a(HAc) = 4.74](D) 0.1 mol/L NH4Cl [p K b(NH3) = 4.75](8)EDTA的酸效应曲线是指 ( )(A) a Y(H)-pH 曲线 (B) pM-pH 曲线(C) lg K'(MY)-pH 曲线 (D) lg a Y(H)-pH 曲线(9)用EDTA直接滴定有色金属离子,终点所呈现的颜色是 ( )(A) 指示剂-金属离子络合物的颜色(B) 游离指示剂的颜色(C) EDTA-金属离子络合物的颜色(D) 上述 B 与 C 的混合颜色(10)在络合滴定中, 用回滴法测定Al3+时, 若在pH=5~6时以某金属离子标准溶液回滴过量的EDTA, 金属离子标准溶液应选 ( )(A) Mg2+ (B) Zn2+ (C) Ag+ (D) Bi3+(11)今有A、B浓度相同的Zn2+-EDTA溶液两份:A为pH = 10.0的NaOH溶液;B为pH = 10.0的氨性缓冲溶液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
分析化学考试题(化工专业)一、填空题每填空1分,共32分)1.根据测量原理分类,分析方法有(化学分析)和(仪器分析)。
2.定量分析过程通常包括(取样);(试样的分解);(待测组分测定);(结果计算)。
3.用沉淀法测定纯NaCl中氯的质量分数,得到下列结果:0.5982,0.6000,0.6046,0.5986,0.6024。
则平均结果为(0.6009 );平均结果的绝对误差为(-5.7x10-3 );相对误差为(-0.94% );中位数为(0.6006 );平均偏差为(2.1x10-3 );相对平均偏差为(0.35% )。
4.按照有效数字的运算规则,下列计算式的结果各应包括几位有效数字:(1)213.64+4.402+0.3244 (五)位;(2)0.1000 x (25.00-1.52)x 246.47/(1.000x1000)(四)位;(3)pH=0.03求H+浓度(两)位。
5. 在分析过程中,下列情况各造成何种(系统、随机)误差。
(1)称量过程中天平零点略有变动(随机误差);(2)分析用试剂中含有微量待测组分(系统误差);6. 标定HCl溶液的浓度时,可用Na2CO3或硼砂(Na2B4O710H2O)为基准物质,若Na2CO3吸水,则测定结果(偏高):若硼砂结晶水部分失水,则测定结果(偏低);(以上两项填无影响、偏高、偏低)。
若两者均保存妥当,不存在上述问题,则选(硼砂)作为基准物质更好,原因为(HCL与两者均按1:2计量比进行反应,硼砂摩尔质量大,称量时相对误差小)。
7. 从质量保证和质量控制的角度出发,为了使分析数据能够准确地反映实际情况。
要求分析数据具有(代表性)、(准确性)、(精密性)、(可比性)和(完整性)。
这些反映了分析结果的(可靠性)。
8. 浓度为c(mol/L)H2C2O4溶液的电荷平衡方程:([H+]=[OH-]+[ HC2O4-]+2[C2O42-])9. 根据酸碱质子理论,OH-的共轭酸是(H2O ),HAc的共轭酸是(H2Ac+)。
10.某溶液含有M和N离子,且KMY »KNY。
lgK`MY先随溶液pH增加而增大,这是由于(αY(H)减小)。
然后当pH增加时,lgK`MY保持在某一定值(N在此条件下不水解),这是因为(αY(N)>αY(H),lgK`MY的大小由αY(N)决定,与αY(H)无关)。
11. 一般分析实验室对日常生产流程中的产品质量指标进行检查控制的分析方法为(例行)分析。
不同企业部门对产品质量和分析结果有争议时,请权威的分析测试部门进行裁判的分析称为(仲裁)分析。
12. 在滴定中指示剂颜色的那一点成为(滴定终点)。
(滴定终点)与化学计量点不一定恰好吻合,由此造成的分析误差成为(终点误差)。
13. 试样的采集是指大批物料中采取(少量)样本作为原始试样。
原始试样在经加工处理后用于分析,其分析结果被视作反映原始物料的实际情况。
因此所采集试样应具有高度的(代表性)。
二、选择题(每题2分,共20分)1. 从精密度好就可以判断分析结果可靠的前提是(B)A.随机误差小;B.系统误差小;C.平均偏差小;D.相对误差小。
2. 下列各项定义中不正确的是(D)A.绝对误差是测定值与真值之差;B.相对误差是绝对误差在真值中所占的百分率;C.偏差是指测定值与平均值之差;D.总体平均值就是真值。
3.下列哪种方法可以减小分析测定中的偶然误差(D)A.对照试验;B.空白试验;C.仪器校正;D.增加平行试验次数。
4. 共轭酸碱对的Ka 与Kb的关系是(B)A. Ka Kb=1;B. KaKb= Kw;C. Ka/Kb= Kw;D. Kb/Ka=Kw。
5. H2PO4-的共轭碱是(B)A. H3PO4;B. HPO42-;C. O43-;D. OH-。
6. 按质子理论,Na2HPO4是(D)A.中性物质;B.酸性物质;C.碱性物质;D.两性物质。
7.将酚酞指示剂加到无色溶液中,溶液呈无色,该溶液的酸碱性为(D)。
A.中性;B.酸性;C.碱性;D.不定。
8. Ca2+、Mg2+共存时,在(C)条件下,不加掩蔽剂可用EDTA滴定Ca2+。
A.pH=5;B. pH=10;C. pH=12;D. pH=2。
9. 一般情况下,EDTA与金属离子形成络合物的络合比是(A)。
A.1:1;B. 2:1;C. 1:3;D. 1:2。
10.EDTA滴定金属离子,准确滴定(Et<0.1%)的条件( D )A. lgKMY ≥6;B. lgK`MY≥6; C. lgcMsp KMY≥6; D.lgcMsp K`MY≥6三、简答题(每题3分,共18分)1.常用的手工缩分方法是四分法。
四分法?答:将已粉碎的试样充分混匀后堆成圆锥形,然后将它压成圆饼状,再通过圆饼状中心按十字形将其分为四等分,弃去任意对角两份,将留下的一半试样收集在一起混匀。
这样试样便缩减了一半,成为缩分一次。
经过多次缩分后,剩余试样可减少至所需量。
2.测定锌合金中Fe、Ni、Mg的含量,应采用什么溶剂溶解试样?答:用NaOH溶解试样,Fe,Ni,Mg形成氢氧化物沉淀,与Zn基体分离。
3.“四舍六入五成双”规则?答:尾数≤4时舍; 尾数≥6时入尾数=5时, 若后面数为0, 舍5成双;若5后面还有不是0的任何数皆入4.镍币中含有少量铜、银。
欲测定其中铜、银的含量,有人将镍币的表层擦洁后,直接用稀HNO3溶解部分镍币制备试液。
根据称量镍币在溶解前后的质量差,确定试样的质量。
然后用不同的方法测定试液中铜、银的含量。
试问这样做对不对?为什么?答:不对。
应将镍币全部溶解,因为镍币中铜银分布不一定均匀,这样做取样无代表性。
5.有人试图用酸碱滴定法来测定NaAc的含量,先加入一定量过量标准HCl溶液,然后用NaOH标准溶液返滴定过量的HCl。
上述操作是否正确?试述其理由。
答:上述操作不正确。
因为NaOH返滴定过量的HCl时,NaAc的中和产物HAc 也能与NaOH作用。
6. 何种情况下可用反滴定法?试举例说明。
答:如下情况下可用反滴定法:封闭指示剂;被测M与Y络合反应慢;易水解例 Al3+的测定四、计算题(每题15分,共30分)1.某混合溶液含有0.10 mol·L -lHCl 、2.0×10-4mol·L -lNaHSO 4和2.0×10-6mol·L -l HAc 。
a .计算此混合溶液的pH 。
b .加入等体积0.10 mol·L -l NaOH 溶液后,溶液的pH 。
解:a. HSO 4- K a2=1.0×10-2 HAc K a =1.8×10-5均为弱酸,且浓度远低于HCl 的浓度,所以此体系中的HSO 4-和HAc 在计算pH 值时刻忽略。
故pH=1.00。
b.加入等体积0.1mol/LNaOH 溶液,HCl 被中和,体系变为HSO 4-和HAc 的混酸体系,H +⎡⎤=⎣⎦ 忽略K W 及K HA [HA],[H + ]2=4HSO K -(C HSO4--[H + ])解得[H + ]=9.90×10-5 故pH=4.002. 在pH =10的氨性缓冲溶液中,[NH3]=0.2 mol/L, 用0.02mol/L EDTA 滴定0.02mol/L Cu2+,计算化学计量点时的pCu ',若滴定的是0.02mol/L Mg2+, 化学计量点时的pMg '又为多少?(β1=104.31;β1=107.89;β1=1011.02;β1=1013.32;β1=1012.86;pH=10时,lg αCu (OH )=101.7、lg αY (H )=0.45)答:sp : Ccusp = 0.01 mol/L, [NH3] = 0.1 mol/Lα Cu(NH3) = 1+β1[NH3]+ ⋅ ⋅ ⋅ + β5[NH3]5 =109.36α Cu(OH) = 101.7α Cu = α Cu(NH3) + α Cu(OH) -1 = 109.36 pH =10, lg α Y(H) = 0.45 lg K 'CuY = lg K CuY - lg αY(H) - αCu= 18.80 - 0.45 -9.36 =8.99 pCu ' =1/2 (pCCusp + lg K 'CuY )= 1/2 (2.00 + 8.99) =5.50 对于Mg2+, lg α Mg =0lg K 'MgY =lg K MgY -lg αY(H)= 8.70 - 0.45 =8.25 pMg ' =1/2(pCMgsp + lg K 'MgY )= 1/2(2.00 + 8.25) =5.13。
