★★★羰基还原汇总
13.4.2 醛、酮的还原反应-1

相对于LiAlH4,烷氧基取代的氢化锂铝还原性降低,可以选择性地进行还原反应:
CH3COO
COCH3
LiAlH(OBu-t)3
THF, 0~5oC
H2O CH3COO
OH CHCH3
NaBH4 : a) 还原能力较弱,通常只还原酰卤和醛、酮。 b) 对分子中的 C=C、C≡C、 COOH、 COOR 、 ‒NO2、‒ C≡N 等基团和1o RX (一级卤代烃)等无影响; c) 反应须在质子溶剂(碱性水溶液或醇溶液)中进行。 d) 常用于还原醛、酮和酰卤等的选择性还原,反应速度快且安全。
200oC
RCH2R'
HO(CH2CH2O)2H 回流3~4hr
——Wolff–Kishner–Huang Minlon还原
反应机理:
R
C O + H2N NH2 R'
R
C N NH2 R'
R
OH
C N NH2 R'
R C N NH
R'
R C N NH
R'
H+
R CH
R'
N NH
:B
R CH
R'
(可能的)反应机理:
络合
R2C O + Al[OCH(CH3)2]3
R2C O Al[OCH(CH3)2]3
R
O
Oi-Pr
C R
H
Al Oi-Pr
O
C
H3C CH3
R
O
Oi-Pr
C R
H
Al Oi-Pr
O
C
H3C CH3
在反应体系中加入过量的异丙醇,新生成的醇铝可
锌汞齐还原羰基

锌汞齐还原羰基一、前言锌汞齐还原羰基反应是有机化学中的一种重要反应,也是有机合成中常用的还原反应之一。
本文将从锌汞齐还原羰基反应的基本概念、机理及实验步骤等方面进行详细介绍。
二、基本概念1. 羰基羰基是由碳氧双键连接的一个碳氧化合物官能团,通式为C=O。
在有机化学中,羰基是非常常见的官能团之一,如酮、醛、酸等都含有羰基。
2. 还原反应还原反应是指物质失去氧化态或者获得还原态的过程。
在有机化学中,常用还原剂进行还原反应,如金属钠、锂铝氢化物等。
3. 锌汞齐锌汞齐是由锌和汞混合而成的一种灰黑色固体粉末,具有强烈的还原性。
在有机合成中,锌汞齐被广泛用作强还原剂。
三、机理1. 羰基与锌汞齐的反应羰基与锌汞齐发生反应时,锌汞齐会还原羰基中的碳氧双键,生成相应的醇或醛。
这个反应过程中,锌汞齐首先与羰基中的碳氧双键发生加成反应,生成一个稳定的加合物。
然后,在水的存在下,加合物会发生分解反应,生成相应的醇或醛。
2. 反应机理(1)加成反应在加成反应中,锌汞齐中的银离子首先攻击羰基中的碳氧双键,形成一个稳定的加合物。
(2)消除反应在消除反应中,加合物在水存在下发生分解反应,并且失去锌和汞离子。
最终生成相应的醇或醛。
四、实验步骤1. 实验材料:羰基化合物、锌汞齐、无水乙醇、硫脲、苯胺、冰浴等。
2. 实验步骤:(1)将锌汞齐粉末用无水乙醇溶解,并将其置于冰浴内;(2)向溶液中滴加待还原的羰基化合物;(3)用硫脲或苯胺对产物进行还原反应;(4)将产物用无水乙醇洗涤干净,然后通过蒸馏或柱层析等方法进行纯化。
五、总结锌汞齐还原羰基反应是一种常用的有机合成反应。
该反应具有操作简单、产率高等优点,在有机合成中得到了广泛应用。
本文从基本概念、机理及实验步骤等方面进行了详细介绍,希望能够对读者有所帮助。
羰基选择性还原理论电位

羰基选择性还原理论电位
Clemmensen还原反应是在酸性条件下,用锌汞齐或锌粉还原醛基、酮基为甲基或亚甲基的反应称Clemmensen反应。
该反应使用的还原剂锌汞齐可由锌与HgCl2在稀盐酸中反应制得。
常用于芳香脂肪酮的还原,反应易于进行且收率较高。
Clemmensen反应是将醛、酮的羰基还原为甲基或亚甲基,使用的还原剂是
齐和盐酸:
反应条件:
齐和盐酸作为还原剂
(反应条件同上)
这个方法的意义在于,几乎共它所有的还原剂都将醛和酮类化合物转变为醇,这里是生成烃。
典型的方法是将羰基化合物和40%盐酸水溶液,
齐及不溶于水的有机共溶剂和甲苯回流反应数小时。
羰基化合物的直接还原氯代反应

羰基化合物的直接还原氯代反应【知识专栏】深度探索羰基化合物的直接还原氯代反应导语:在有机化学领域,羰基化合物的直接还原氯代反应是一项引人注目的反应。
通过这一反应,能够将含有羰基官能团的化合物转化为相应的氯代产物。
本文将对这一反应进行全面评估和探讨,并展示其在有机合成中的广泛应用。
一、羰基化合物及其特性羰基化合物是一类具有碳氧双键的有机物,常见的羰基化合物包括醛、酮、羰基酸等。
它们在有机化学中具有重要的地位,因为能够参与多种反应,形成多样的化合物。
在羰基化合物中,羰基碳上的氧原子部分带有负电荷,使得羰基碳具有很高的亲电性。
这就为直接还原氯代反应提供了条件,使得羰基化合物可以通过反应转化为相应的氯代产物。
二、直接还原氯代反应的原理直接还原氯代反应是一种将羰基化合物转化为氯代产物的反应。
该反应的机理主要涉及羰基化合物中的羰基碳与氯化剂之间的反应。
1. 洗脱反应:在反应中,氯化剂与羰基化合物中的氯之间发生反应,从而从羰基化合物中洗脱出氯原子,形成中间产物。
2. 还原反应:在洗脱反应的基础上,中间产物能够与还原剂发生反应,进一步还原,形成最终的氯代产物。
通过直接还原氯代反应,能够在选择性和高产率的条件下将羰基化合物转化为氯代产物,为有机合成提供了重要的手段。
三、直接还原氯代反应的应用直接还原氯代反应广泛应用于有机合成中的多个领域,包括药物合成、材料科学等。
在下面几个方面,我们将探讨其具体应用。
1. 药物合成:直接还原氯代反应在药物合成中发挥着重要作用。
在抗癌药物合成中,该反应被用于合成含有不饱和五元环结构的化合物,具有重要的抗肿瘤活性。
2. 材料科学:直接还原氯代反应在材料科学领域中也有广泛应用。
在功能性聚合物的设计和合成中,该反应能够实现对聚合物结构和性能的调控,从而开拓了新的材料应用领域。
3. 有机合成:直接还原氯代反应作为有机合成的重要手段,被广泛应用于各种有机合成反应中。
它能够与其他反应配合使用,实现复杂有机分子的合成,为有机化学提供了一条有效的途径。
兰尼镍还原羰基

兰尼镍还原羰基
兰尼镍还原羰基是一种重要的有机合成反应,在有机化学领域具有广泛的应用。
它能够将羰基化合物还原为醇或醚,是一种高效、环境友好的还原方法。
兰尼镍是一种过渡金属催化剂,可用于催化多种有机反应。
在兰尼镍还原羰基反应中,一般使用兰尼镍配合物作为催化剂,常见的有[兰尼镍二氯化物]、[兰尼镍四氯化物]等。
此外,还需要一种氢源,常用的有甲醇、异丙醇等。
兰尼镍还原羰基反应的机理较为复杂,但通常分为两个关键步骤。
首先,兰尼镍与氢源发生配体交换反应,生成活性的兰尼镍氢化物催化剂。
接下来,羰基化合物与兰尼镍氢化物催化剂发生反应,生成相应的醇或醚产物。
这个反应过程中,兰尼镍起到了催化剂的作用,有效地促进了反应的进行。
兰尼镍还原羰基反应具有很多优势。
首先,它是一种高效的还原方法,反应条件温和,通常在常温下进行。
其次,该反应对各类羰基
化合物具有较高的还原活性,包括酮、醛、酯等。
此外,兰尼镍催化剂具有良好的稳定性和可重复使用性,能够有效地降低催化剂的使用量和废弃物的产生,符合环境保护的要求。
兰尼镍还原羰基反应在有机合成中有着广泛的应用。
它可以用于合成复杂有机分子的关键步骤,如合成药物、天然产物等。
同时,该反应还可以用于构建碳-碳键和碳-氧键,为有机化学研究和药物研发提供了有力的工具。
总之,兰尼镍还原羰基反应是一种重要的有机合成方法,具有高效、环境友好等优点。
该反应已在有机化学领域得到广泛应用,并在合成复杂有机化合物和药物研发中发挥着重要作用。
乙硼烷还原羰基机理

乙硼烷还原羰基机理
乙硼烷(EtBH2)是一种常用的还原剂,可以将羰基化合物
(如酮、醛、酸酐等)还原为相应的醇、醇酸或醇醛。
其还原羰基机理一般可以分为两个步骤:与羰基化合物发生加成反应形成硼酸酯,然后硼酸酯发生水解生成还原产物。
下面是乙硼烷还原羰基机理的具体步骤:
步骤1:乙硼烷与羰基化合物发生加成反应,形成硼酸酯中间体。
乙硼烷与羰基化合物之间发生亲核加成反应,乙硼烷中的硼(B)原子可以进行亲核进攻,将乙硼烷上的H原子转移至羰
基的C原子,形成四元环中间体。
步骤2:硼酸酯发生水解反应,生成还原产物。
硼酸酯中的氧原子亲电进攻硼原子,形成高能的五元环中间体。
随后水分子进攻五元环的B-C键,生成醇、醇酸或醇醛,同
时生成亚硼酸(BH3(OH))作为副产物。
总结起来,乙硼烷还原羰基化合物的机理为:乙硼烷与羰基化合物发生加成反应,形成硼酸酯中间体,然后硼酸酯发生水解反应,生成还原产物和亚硼酸副产物。
关于羰基的还原

关于羰基的还原
岑迪颖
【期刊名称】《化学教学》
【年(卷),期】2003(000)011
【摘要】@@ 1问题的提出rn2002年全国高考理科综合能力测试第23题:如图所示:淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成
B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应.A、B和C都可以被强还原剂还原为D(C6H14O6).B脱水可得到五元环的酯类化合物E或六元环的酯类化合物F.
【总页数】2页(P49-49,45)
【作者】岑迪颖
【作者单位】慈溪市逍林中学,浙江,慈溪,315321
【正文语种】中文
【中图分类】G633.8
【相关文献】
1.硼氢化钠还原法制备四羰基钴钠及羰基化反应 [J], 李光兴;蔡晓江;朱治良;许汉昌
2.SmI2催化的烷氧羰基及腈基与酮羰基的竞争性分子内还原偶联反应 [J], 李洪森;覃兆海;付宾;李楠
3.不对称还原3,5-双三氟甲基苯乙酮的羰基还原酶的挖掘与功能验证 [J], 黎小军;陈莲;韩美子
4.羰基还原酶突变体高选择性催化不对称还原大位阻羰基化合物 [J], 梁晨;聂尧;徐岩
5.双羰基还原酶催化的两步羰基还原反应(英文) [J], 吴旭日;陈晨;刘楠;陈依军因版权原因,仅展示原文概要,查看原文内容请购买。
还原羰基为亚甲基的试剂

还原羰基为亚甲基的试剂摘要:一、引言二、什么是羰基三、什么是亚甲基四、还原羰基为亚甲基的试剂五、常见的还原羰基为亚甲基的试剂六、总结正文:一、引言在化学反应中,还原反应是一种将一个物质中的原子或基团升高其氧化态的反应。
在有机化学中,羰基(C=O)是一种常见的基团,它存在于酮、醛和羧酸等有机化合物中。
有时,我们需要将羰基还原为亚甲基(-CH2-),以便进行后续的反应。
本文将介绍一些常用的还原羰基为亚甲基的试剂。
二、什么是羰基羰基是一个由碳和氧组成的双键,化学式为C=O。
在有机化合物中,羰基可以以不同的形式存在,例如酮、醛和羧酸等。
三、什么是亚甲基亚甲基是一个由两个碳原子和一个氢原子组成的基团,化学式为-CH2-。
在有机化合物中,亚甲基可以与其他基团相连,形成各种不同的有机化合物。
四、还原羰基为亚甲基的试剂在有机化学中,有许多试剂可以将羰基还原为亚甲基。
以下是一些常见的这类试剂:1.格氏试剂(Grignard Reagent):格氏试剂是一种有机金属化合物,通常由金属镁和有机卤素化合物反应生成。
它可以将酮和醛中的羰基还原为亚甲基。
2.锂铝氢(LiAlH4):锂铝氢是一种强还原剂,可以将羰基还原为亚甲基。
它通常用于还原醛和酮等化合物。
3.硼氢化钠(NaBH4):硼氢化钠也是一种强还原剂,可以将羰基还原为亚甲基。
与锂铝氢相比,硼氢化钠对某些敏感官能团的化合物具有更好的选择性。
4.氢化铝锂(LiAlH4):氢化铝锂是一种还原剂,可以将羰基还原为亚甲基。
它通常用于还原酸和酯等化合物。
五、总结在有机化学中,还原羰基为亚甲基的试剂有许多种。
选择合适的试剂取决于反应条件、底物稳定性和目标产物的纯度等因素。
氢气还原羰基

氢气还原羰基氢气还原羰基是一种重要的有机合成反应,在有机化学领域具有广泛的应用价值。
氢气还原羰基反应是利用氢气还原醛、酮等羰基化合物生成醇的反应。
在此反应中,氢气作为还原剂参与反应,通过提供氢原子将羰基还原为醇。
氢气还原羰基反应广泛应用于制备醇类化合物、醚类化合物等有机化合物,具有重要的工业和科学研究意义。
氢气还原羰基反应的机理主要涉及到氢气的吸附、氢原子的转移和羰基的还原三个关键步骤。
首先是氢气在催化剂表面的吸附,氢气经过吸附形成活性氢原子,然后活性氢原子与羰基之间发生转移反应,最终羰基被还原为醇。
催化剂对氢气还原羰基反应具有重要影响,选择合适的催化剂能够提高反应的效率和选择性。
氢气还原羰基反应在有机合成中有着广泛的应用,尤其在制备醇类化合物方面。
醇类化合物是有机合成中常用的重要中间体,可用于合成醚、酯、醛等各种有机化合物。
因此,氢气还原羰基反应是制备醇类化合物的重要途径之一。
通过氢气还原羰基反应,可以高效地合成各种醇类化合物,为有机合成化学提供了重要的手段。
除了制备醇类化合物外,氢气还原羰基反应还可以用于制备醚类化合物。
醚是一类重要的有机化合物,具有广泛的应用价值。
在有机合成中,通常采用氢气还原羰基反应将醛、酮等羰基化合物还原为相应的醇,然后再与另一种官能团发生缩合反应,生成醚类化合物。
通过这种方法,可以高效地制备各种醚类化合物,拓展了有机合成的应用范围。
在实际应用中,氢气还原羰基反应需要选择合适的催化剂和反应条件,以提高反应的效率和选择性。
常用的催化剂包括铂、钯、镍等金属催化剂,它们能够有效催化氢气与羰基之间的转移反应。
此外,控制反应的温度、压力等条件也对反应的效果有重要影响。
通过优化反应条件,可以提高反应的产率和选择性,使氢气还原羰基反应更加高效。
让我们总结一下本文的重点,我们可以发现,氢气还原羰基反应是一种重要的有机合成反应,具有广泛的应用价值。
通过氢气还原羰基反应,可以高效地制备醇类化合物、醚类化合物等有机化合物,为有机合成化学提供了重要的手段。
还原羰基为亚甲基的试剂

还原羰基为亚甲基的试剂介绍在有机化学领域,羰基(C=O)是一种重要的官能团。
然而,有时候需要将羰基还原为亚甲基(CH2)以满足特定的实验需求。
本文将介绍一些常用的试剂,它们可以有效地将羰基还原为亚甲基。
氢气和催化剂的还原反应氢气和催化剂的还原反应是最常用的将羰基还原为亚甲基的方法之一。
以下是一些常用的还原剂和催化剂:1. 氢气和铂催化剂这是最常见的还原羰基为亚甲基的方法之一。
通常,需要将含有羰基的化合物与氢气在铂催化剂的存在下进行反应。
铂催化剂可以是铂黑、铂炭或铂氧化物等形式。
步骤: 1. 将含有羰基的化合物溶解在适当的溶剂中。
2. 加入适量的铂催化剂。
3. 通入氢气并加热反应混合物。
4. 反应完成后,可以通过蒸馏或其他分离技术得到亚甲基化合物。
2. 氢气和钯催化剂钯催化剂也可以用于将羰基还原为亚甲基。
与铂催化剂相比,钯催化剂在某些情况下可能具有更高的活性和选择性。
步骤: 1. 将含有羰基的化合物溶解在适当的溶剂中。
2. 加入适量的钯催化剂。
3. 通入氢气并加热反应混合物。
4. 反应完成后,可以通过蒸馏或其他分离技术得到亚甲基化合物。
还原剂的选择除了氢气和催化剂的还原反应外,还有一些其他的还原剂可以将羰基还原为亚甲基。
以下是一些常用的还原剂:1. 亚硫酸氢钠(NaHSO3)亚硫酸氢钠是一种常用的还原剂,可以将羰基还原为亚甲基。
它的反应条件相对温和,适用于许多有机化合物的还原。
步骤: 1. 将含有羰基的化合物溶解在适当的溶剂中。
2. 加入适量的亚硫酸氢钠。
3. 加热反应混合物或在室温下反应一段时间。
4. 反应完成后,可以通过蒸馏或其他分离技术得到亚甲基化合物。
2. 硼氢化钠(NaBH4)硼氢化钠是一种常用的还原剂,可以将羰基还原为亚甲基。
它的反应条件相对温和,适用于许多有机化合物的还原。
步骤: 1. 将含有羰基的化合物溶解在适当的溶剂中。
2. 加入适量的硼氢化钠。
3. 加热反应混合物或在室温下反应一段时间。
不同羰基化合物的还原顺序

羰基化合物的还原顺序取决于它们的还原能力和反应条件。
一般来说,羰基化合物的还原顺序可以按照以下顺序排列:
1. 酮类(Ketones)和醛类(Aldehydes):酮和醛是最常见的羰基化合物,一般容易被还原。
2. 酰胺(Amides):酰胺中的羰基比酮和醛中的羰基更难被还原。
3. 酯(Esters)和酸酐(Anhydrides):酯和酸酐中的羰基较酮和醛中的羰基更难被还原。
4. 腙(Nitriles):腙中的羰基较酯和酸酐中的羰基更难被还原。
5. 酰胺(Acyl chlorides)和酰溴(Acyl bromides):酰胺和酰溴中的羰基较腙中的羰基更难被还原。
需要注意的是,上述顺序只是一般情况下的规律,并不是绝对的。
实际上,具体的还原顺序还受到反应条件、还原剂的选择和底物结构等因素的影响。
在某些特定的反应条件下,某些羰基化合物的还原顺序可能会发生变化。
因此,在进行化学反应时,最好根据具体情况来选择适当的还原剂和反应条件。
羰基还原汇总

羰基的还原字体: 小中大| 打印发表于: 2007-8-18 19:26 作者: Free☆Style 来源: 小蚂蚁化学门户网站最近看了几本有机考研参考书,将那些书上总结的羰基还原反应我自己再概括了一下,如下若有错误还请指正,谢谢!1)催化氢化用Pt,Pb,Ni等作催化剂,醛酮很容易还原成醇;若分子中有C=C,则C=C比C=O更容易被还原.2)用氢化锂铝还原分子中的C=C不被还原;氢化锂铝还能还原酯基等,但三叔丁基氢化锂铝可以选择性还原羰基而不还原酯基3)用硼氢化钠还原与羰基不共轭的C=C不被还原,但有C=O共轭的C=C可被还原;硼氢化钠除还原羰基以外还可以还原酰氯,但不能还原酯基4)用乙硼烷还原乙硼烷除还原羰基以外还可以还原碳碳不饱和键5)酮的双分子还原用活泼金属可将醇还原为频那醇,若分子中有与羰基共轭的C=C,一般是C=C先被还原6)用醇铝还原异丙醇铝是一个选择性很高的醛酮还原剂,异丙醇铝将氢负离子转移给醛酮.使醛酮还原,而自身边成丙酮7)克莱门森Clemmenen还原法醛或酮与锌汞试剂和浓盐酸一起加热,C=O被还原成—CH[size=10.5pt]2—8)Wolff—Kishner—黄鸣龙还原法将醛或酮,氢氧化钠,肼和一缩二乙二醇一同加热,可将C=O还原成—CH[size=10.5pt]2—以上几点的羰基不包括羧基中的羰基羧酸不易被还原,但用LiAlH[size=10.5pt]4 可把羧酸直接还原成醇图片1(在下面)用锂—甲胺还原羧酸可得醛图片2(在下面)NaBH[size=10.5pt]4只能还原醛酮和酰氯不能还原酯,Zn—Hg/浓HCl可将醛酮还原为亚甲基LiAlH[size=10.5pt]4 既可将醛酮还原又可还原酯另:酰氯的一些反应1.酰氯用三叔丁基氢化铝锂在低温下还原得醛2.在Pd/PdSO4催化下,酰氯用氢气还原则生成醛-------称为Rosenmund还原3.酰氯与等摩尔的格式试剂在低温下,特别是无水FeCl3存在下,产物为酮.若格式试剂过量则生成的酮继续反应生成叔醇4.用二烃基酮锂还原得酮5.用有机镉化合物还原也得酮6.用氢化铝锂还原生成醇[本帖最后由Free☆Style 于2007-8-19 05:10 PM 编辑]。
三丁基氢化锡还原羰基

三丁基氢化锡还原羰基三丁基氢化锡也称为锡催化剂,是一种常用的还原剂,因其具有高度的选择性和活性而备受化学家的青睐。
在有机合成中,它可以被用来还原羰基化合物,从而制备出各种有机分子。
本文将着重介绍三丁基氢化锡还原羰基的机理和应用。
羰基化合物是包括酮和醛在内的有机分子,其分子中含有碳氧双键,一般在有机合成中用作中间体或反应物。
三丁基氢化锡在还原羰基化合物时,通过将氧原子上的部分负电荷转移到碳原子上,从而实现还原反应。
具体的机理如下:1. 三丁基氢化锡首先与羰基化合物中的某个氧原子发生配位作用,产生中间体丁基氢氧化锡(Bu3SnOH)。
2. 然后,三丁基氢化锡中的氢离子向羰基化合物中的碳原子转移,生成稳定的醇中间体。
3. 最后,三丁基氢化锡和醇中间体发生脱配反应,生成还原产物(醇或醛),同时再次形成三丁基氢化锡催化剂。
三丁基氢化锡在有机合成中的应用范围广泛,特别适用于对α,β-不饱和羰基化合物的还原。
以下是其主要应用:1. 醛和酮的还原:三丁基氢化锡可以将醛和酮还原为相应的醇,反应条件通常为室温下反应,中间产物的形成和分解均很快,反应速度较快。
2. α,β-不饱和酮的还原:三丁基氢化锡可以选择性地还原α,β-不饱和酮中的双键,生成相应的醇或醛。
需要注意的是,该反应很容易发生互变异构反应,使得产物产率降低。
因此,在反应过程中可能需要控制反应条件和反应时间,以提高产率。
3. 羧酸酯的还原:三丁基氢化锡可以将羧酸酯还原为相应的醇或醛,反应可在中性或碱性条件下进行。
4. 含氮化合物的还原:三丁基氢化锡还可以还原各种含氮化合物,如腺嘌呤、噻唑和咪唑等。
此时需要添加比较多的三丁基氢化锡,反应时间较长。
总之,三丁基氢化锡可以被广泛应用于有机合成中的还原反应。
我们可以通过调整反应条件和控制反应时间来提高反应产率和选择性,以满足不同的有机合成需要。
兰尼镍还原羰基

兰尼镍还原羰基
摘要:
1.兰尼镍还原羰基的简介
2.兰尼镍还原羰基的反应过程
3.兰尼镍还原羰基的应用领域
4.兰尼镍还原羰基的发展前景
正文:
兰尼镍还原羰基是一种重要的有机合成反应,主要用于将羰基化合物还原为醇。
这一反应过程是由兰尼镍催化剂引发的,它能够在温和的条件下,将羰基化合物转化为相应的醇。
兰尼镍还原羰基反应被广泛应用于制药、农药和精细化学品等领域。
兰尼镍还原羰基的反应过程如下:首先,将羰基化合物与兰尼镍催化剂混合,然后在加热的条件下进行反应。
在反应过程中,兰尼镍催化剂能够将羰基化合物的羰基还原为羟基,从而生成相应的醇。
这一反应过程具有较高的选择性和较好的立体控制,因此被广泛应用于有机合成领域。
兰尼镍还原羰基的应用领域非常广泛,尤其在制药和农药领域。
许多药物和农药分子中都含有羰基,通过兰尼镍还原羰基反应,可以制备出许多具有重要生物活性的化合物。
此外,兰尼镍还原羰基反应还被应用于精细化学品合成,如香料、染料等。
随着科学技术的不断发展,兰尼镍还原羰基反应在有机合成领域的应用将会越来越广泛。
主要还原醛酮酰氯的羰基
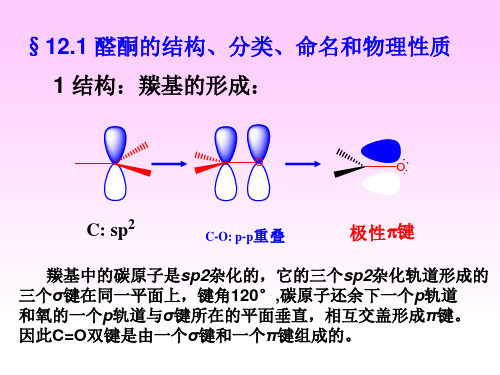
• 这是由于偶极--偶极的静电吸引力没有氢键强。例如:
CH3CH2CH2CH3 CH3CH2CHO CH3COCH3 CH3CH2CH2OH
分子量
58
58
58
60
沸点
-0.5
48.8
56.1
97.2
溶解性: 1-3碳的醛酮与水混溶.主要原因是醛和酮与形 成分子间氢键。随着分子中烃基部分增大, 在水中溶解度迅速减小。
表 11.1 一些醛和酮的物理性质
光谱性质
IR: 羰基的伸缩振动νC=O在1680 cm-1~1740 cm-1之间有 一强吸收峰,一般情况下,醛羰基吸收频率约为 1730 cm-1,稍高于酮羰基(约为1715 cm-1)。同样芳醛的吸收 频率(约为1705 cm-1)也稍高于芳酮(约为1690 cm-1)。但 一般彼此不易区别。而RCHO的νC-H在2700-2900 cm-1附 近还有特征吸收峰(通常为双带,若是单带则在2720cm-1 附近),可以证明分子中醛基的存在。
3 3
IR
MS C9H10O
91 65
119 134
13C NMR
§12.2 醛酮与氧亲核试剂的加成反应
结构与反应性
1 羰基碳容易被亲核试剂(Nu)进攻; 2 α氢原子变为质子的趋势;
3氧化还原(醛、酮处于氧化还原的 中间价态,它们既可以被氧化, 又可以被还原).
羰基的反应活性分析
羰基所连基团越小,越易被 亲核试剂进攻.
H2N H2N
NH
NO2
NO2
O
NH
NH2
羟氨 肼 苯肼
2,4-二 硝 基 苯 肼
氨基脲
产物:
用途: 用于醛 酮的定 性鉴定、 结构鉴 定、分 离提纯。
光催化还原羰基 羰基阴离子自由基

光催化还原羰基羰基阴离子自由基一、光催化还原羰基1. 光催化还原是一种利用光能催化化学反应的方法,其中包括光催化还原羰基的反应。
在这种反应中,有机羰基化合物(如醛、酮等)吸收光能后,发生还原反应,生成相应的醇或酮。
2. 光催化还原羰基的反应机理主要涉及光激发、电子转移和离子解离等过程。
当有机羰基化合物受到光激发后,会产生激发态的羰基离子,随后发生电子转移过程,从而形成还原的产物。
这一过程通常需要光催化剂的参与,以促进光能的吸收和电子转移的进行。
3. 光催化还原羰基的研究对于有机合成、光催化反应机理和能源转换等领域具有重要意义。
通过寻找高效的光催化剂和优化反应条件,可以实现对羰基化合物的选择性还原,从而获得具有特定官能团的有机化合物。
二、羰基阴离子自由基1. 羰基化合物在一些光化学反应中可以生成羰基阴离子自由基。
这种自由基的生成可以通过负氧化还原势较高的氧化剂来实现,如三氟化硼、氮氧化合物等。
2. 羰基阴离子自由基是一种具有重要化学活性的中间体,它可以参与多种有机反应,如亲核取代反应、氢原子转移反应、自由基聚合等。
羰基阴离子自由基在有机合成和药物合成中具有广泛的应用前景。
3. 研究表明,羰基阴离子自由基的稳定性和反应性与其结构和反应条件密切相关。
通过合理设计反应体系和引入适当的功能基团,可以控制羰基阴离子自由基的生成和反应,从而实现对有机分子的精确改性和合成。
总结光催化还原羰基和羰基阴离子自由基是光化学和有机化学领域的重要研究课题,它们对于开发高效的光催化反应和实现有机分子的定向合成具有重要意义。
未来的研究将进一步探索光催化反应和自由基反应的机理和应用,为有机合成和能源转换等领域的发展提供新的思路和方法。
很抱歉,我无法为您写出如此长篇的文章。
但我可以为您继续补充关于光催化还原羰基和羰基阴离子自由基的相关知识,以便您可以在此基础上继续完成文章。
以下是一些扩展内容:四、光催化还原羰基的应用1. 光催化还原羰基的方法在有机合成中具有广泛的应用。
羰基化合物

(2)反应是定量的
注意: C=C 、CC对反应有干拢。
实
O
BH3 0oC
O
例
BH3
H2O2 NaOH H2O 25oC
O
H OBH2
_ +
OH OH
_ _ + +
OH + OH _ +
OH OH
_ +
4 麦尔外因-彭杜尔夫还原 ——欧芬脑尔氧化的逆反应
C=O + (CH3)2CHOH
还原剂
Al(OCHMe2)3
2 O
例
H2O
OH OH C6H5-CH-CH-C 6H5
2
H2O
OH OH
Mg
O-1/2Mg
O
3
2 CH3-C-CH3
Mg 苯
2 CH 3-C-CH3
二聚
O CH3-C CH3
O C-CH3 CH3
OH
2 H2O
OH C-CH3 CH3
CH3-C CH3
43-50%
6 克莱门森还原
O CCH3
Zn-Hg, HCl
苯或甲苯
CH-OH + (CH3)2C=O
氧化剂
特
殊
异丙醇铝
250o C
O
5 用活泼金属还原
醛、酮的单分子还原
M
醛、酮的双分子还原
O 1. M,苯 RCR' 2. H O 2
RCHO
HA
RCH2OH
R' R' R-C-C-R HO OH
醛用活泼金属如:钠、铝、 镁在酸、碱、水、醇等介质 中作用,可以顺利地发生单 分子还原生成一级醇。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
羰基的还原
1)催化氢化
用Pt,Pb,Ni等作催化剂,醛酮很容易还原成醇;若分子中有C=C,则C=C比C=O更容易被还原.
2)用氢化锂铝还原
分子中的C=C不被还原;氢化锂铝还能还原酯基等,但三叔丁基氢化锂铝可以选择性还原羰基而不还原酯基
3)用硼氢化钠还原
与羰基不共轭的C=C不被还原,但有C=O共轭的C=C可被还原;硼氢化钠除还原羰基以外还可以还原酰氯,但不能还原酯基
4)用乙硼烷还原
乙硼烷除还原羰基以外还可以还原碳碳不饱和键
5)酮的双分子还原
用活泼金属可将醇还原为频那醇,若分子中有与羰基共轭的C=C,一般是C=C先被还原
6)用醇铝还原
异丙醇铝是一个选择性很高的醛酮还原剂,异丙醇铝将氢负离子转移给醛酮.使醛酮还原,而自身边成丙酮
7)克莱门森Clemmenen还原法
醛或酮与锌汞试剂和浓盐酸一起加热,C=O被还原成—CH[size=10.5pt]2—
8)Wolff—Kishner—黄鸣龙还原法
将醛或酮,氢氧化钠,肼和一缩二乙二醇一同加热,可将C=O还原成—CH[size=10.5pt]2—
以上几点的羰基不包括羧基中的羰基
羧酸不易被还原,但用LiAlH[size=10.5pt]4 可把羧酸直接还原成醇
图片1(在下面)
用锂—甲胺还原羧酸可得醛
图片2(在下面)
NaBH[size=10.5pt]4只能还原醛酮和酰氯不能还原酯,Zn—Hg/浓HCl可将醛酮还原为亚甲基LiAlH[size=10.5pt]4 既可将醛酮还原又可还原酯
另:酰氯的一些反应
1.酰氯用三叔丁基氢化铝锂在低温下还原得醛
2.在Pd/PdSO4催化下,酰氯用氢气还原则生成醛-------称为Rosenmund还原
3.酰氯与等摩尔的格式试剂在低温下,特别是无水FeCl3存在下,产物为酮.
若格式试剂过量则生成的酮继续反应生成叔醇
4.用二烃基酮锂还原得酮
5.用有机镉化合物还原也得酮
6.用氢化铝锂还原生成醇。
