过渡金属元素解析
元素周期表中的过渡金属元素

元素周期表中的过渡金属元素元素周期表是一张记录了所有已知元素的表格,它按照一定规律排列了元素的原子序数和化学性质。
其中,过渡金属元素是周期表中的一类重要元素。
本文将介绍过渡金属元素的定义、特性以及在各个领域的应用。
一、过渡金属元素的定义过渡金属元素是指元素周期表中第4至第11族的元素,它们的电子配置在填充d轨道时出现了不规则的变化。
这类元素包括钛(Ti)、铬(Cr)、铁(Fe)、镍(Ni)等,共有38个元素。
过渡金属元素以其独特的物理和化学特性而备受关注。
二、过渡金属元素的特性过渡金属元素具有一系列独特的特性,使其在化学、材料科学以及生物学等领域具有重要应用价值。
1. 变价性:过渡金属元素的最外层电子数较少,因此它们容易失去或吸收电子,表现出多样的化合价态。
例如,铁在+2和+3价之间变化,形成不同的化合物。
2. 高熔点和良好的热导性:过渡金属元素由于其复杂的电子结构和强大的金属键,具有相对较高的熔点和良好的热导性。
因此,它们常被用于高温环境下的合金制备和热传导材料。
3. 催化性能:过渡金属元素在催化反应中起到重要作用。
它们能够改变反应的速率和方向,提高反应的效率。
例如,铂是许多重要催化剂的组成部分,广泛应用于汽车排放控制和化学工业中。
4. 彩色化合物的形成:过渡金属元素形成的化合物常常具有鲜艳的颜色。
这是由于它们d轨道电子的能级结构引起的。
例如,铜(II)离子形成的化合物呈现出蓝色,铬(III)离子形成的化合物呈现出绿色。
三、过渡金属元素的应用由于其独特的化学性质和物理特性,过渡金属元素在许多领域有着广泛的应用。
1. 工业领域:过渡金属元素被广泛应用于材料工程、电子工业和制药工业等领域。
例如,钢中的铁是由铁和碳以及其他过渡金属元素组成的合金,具有高强度和抗腐蚀性。
2. 能源产业:某些过渡金属元素在能源领域具有重要的作用。
铂、钴等元素被用作燃料电池的催化剂,提高其效率和稳定性。
铬和钒等元素则广泛应用于储能材料中。
元素周期表中的过渡金属元素

元素周期表中的过渡金属元素元素周期表是化学家们用来分类和组织元素的一张表格。
其中,过渡金属元素是周期表中的一个重要类别。
它们具有独特的化学性质和广泛的应用。
本文将对元素周期表中的过渡金属元素进行介绍。
过渡金属元素是指周期表中的d区元素,它们位于主族元素之后,但又并不属于稀土元素。
过渡金属元素的共同特点是其原子的d轨道变化较为复杂,容易形成不同的氧化态。
它们具有良好的电子传导性和热传导性,因此在金属工业和电子工业中有着重要的地位。
在元素周期表中,过渡金属元素的原子序数(也称为核电荷数)从21到30、39到48、57到80和89到112。
这个范围内的元素包括钒(V)、铬(Cr)、锰(Mn)、铁(Fe)、钴(Co)、镍(Ni)、铜(Cu)、锌(Zn)等等。
这些元素在化学反应中表现出了各种各样的性质,使它们在工业和生活中有着广泛的应用。
首先,过渡金属元素具有良好的催化性能。
钯(Pd)和铂(Pt)是广泛应用于催化剂领域的元素。
它们的原子结构使它们能够吸附其他物质并参与化学反应,促进反应速度。
以钯为催化剂的氢化反应、以铂为催化剂的汽车尾气净化反应等都是重要的例子。
其次,过渡金属元素也在颜料和染料工业中得到了应用。
铬酸盐是一种常见的绿色颜料,它被广泛用于涂料、油墨和塑料等产品中。
铁离子的不同氧化态也导致了不同的颜色,比如二价的铁离子会使物质呈现出黄色。
此外,过渡金属元素还在电池和电子器件中扮演着重要的角色。
锂电池中的正极材料常常使用过渡金属氧化物,如锰酸锂(LiMn2O4)。
这些氧化物能够发生可逆的氧化还原反应,从而储存和释放电能。
钨(W)和铌(Nb)等过渡金属元素也常被用于制造电子器件和导线,因为它们具有较高的熔点和良好的导电性。
最后,过渡金属元素在生物体内也起着重要的作用。
比如铁(Fe)是血红蛋白的组成部分,负责氧气的输送。
锌(Zn)是多种酶的辅助因子,参与体内的代谢过程。
总之,元素周期表中的过渡金属元素具有丰富的化学性质和广泛的应用价值。
元素周期表中的过渡金属

元素周期表中的过渡金属元素周期表是化学家们总结出来的一种整体呈现化学元素的方式。
它按一定的规律排列了所有已知的化学元素,并将它们分组和分类。
其中,过渡金属是元素周期表中的一类重要元素。
本文将竭尽全力探讨过渡金属的特性、应用以及对人类社会的影响。
一、过渡金属的特性过渡金属是位于元素周期表中d区的一组元素。
它们共同具有许多独特的特性,使得它们成为化学反应和物质变化中不可或缺的一部分。
首先,过渡金属的原子结构中有未填满的d轨道电子,这使得它们在化学反应中表现出较高的活性。
这些未填满的电子能级使过渡金属能够容易地失去或获得电子,从而形成不同的化合物和离子态。
其次,过渡金属具有多种氧化态。
它们的d轨道电子能级的填充方式使它们能够在不同的氧化态之间转变,进而发挥多种不同的化学活性。
这也是过渡金属与许多生物分子相互作用的基础,如血红蛋白中的铁离子。
此外,过渡金属还表现出较高的熔点和沸点,使得它们在制备高温合金、电子材料和催化剂等领域具有重要应用价值。
二、过渡金属的应用过渡金属由于其独特的性质,在许多领域得到了广泛应用。
首先,在材料科学领域,过渡金属可用于制备高强度和轻质的合金材料。
例如,钛合金以其优异的强度和耐腐蚀性广泛应用于航空航天和汽车制造业。
其次,过渡金属也被广泛运用于电子器件中。
铜、铝等过渡金属的导电性良好,可用于制造电线和电路板。
许多过渡金属的氧化物还具有半导体性质,使它们成为电子元件的重要材料。
此外,过渡金属还被用作催化剂。
许多化学反应需要催化剂的参与才能顺利进行,而过渡金属离子或化合物往往具有良好的催化活性。
催化剂的应用范围涵盖了化工、环境保护和能源等领域。
三、过渡金属对人类社会的影响过渡金属的广泛应用对人类社会产生了深远的影响。
首先,过渡金属的应用推动了科学技术的发展。
它们作为新材料和催化剂的研究推动了材料科学和化学工程学科的发展。
通过深入研究过渡金属的特性和应用,我们能够更好地理解和利用这些元素,从而推动相关学科不断进步。
元素周期表中的过渡金属元素及其性质研究

地壳中过渡金属元素的种类和分布
地壳中过渡金属元素的开采难度和成本
地壳中过渡金属元素的应用领域和价值
地壳中过渡金属元素的丰度排名
过渡金属元素在自然界中的分布:主要存在于地壳中,如铁、铜、锌等
开采方法:根据元素性质和矿床类型选择合适的开采方法,如露天开采、地下开采等
镍的化合物:硫酸镍、氯化镍、硝酸镍等
Hale Waihona Puke 铜元素:原子序数29,位于元素周期表第四周期
铜的物理性质:红色金属,具有良好的导电性和导热性
铜的化学性质:在空气中稳定,不易氧化,但在高温下可与氧气反应生成氧化铜
铜的化合物:包括氧化铜(CuO)、硫酸铜(CuSO4)、氯化铜(CuCl2)等,具有不同的物理和化学性质
汇报人:
元素周期表中的过渡金属元素及其性质研究
目录
添加目录标题
过渡金属元素概述
过渡金属元素的物理性质
过渡金属元素的化学性质
常见过渡金属元素及其化合物
过渡金属元素在自然界中的存在和开采
添加章节标题
过渡金属元素概述
过渡金属元素位于周期表的第4、5、6周期
过渡金属元素包括铁、钴、镍、铜、锌、钼、钨、钽、铌、钌、铑、钯、银、金、铂、汞等
过渡金属元素在工业上广泛应用,如铁、铜、铝等
过渡金属元素在生物体内具有重要作用,如铁、锌等
过渡金属元素在环保领域也有广泛应用,如铬、锰等
过渡金属元素在化学实验中常用作催化剂,如镍、铂等
过渡金属元素的物理性质
过渡金属元素的原子结构:原子半径、电离能、电子亲和能等
电子排布:过渡金属元素的电子排布规律和特点
原子结构对物理性质的影响:如熔点、沸点、导电性等
元素周期表中的过渡金属与稀有金属

元素周期表中的过渡金属与稀有金属元素周期表是化学领域中最重要的工具之一,它将元素按照一定规律排列,让我们可以更好地理解和研究化学元素及其性质。
在元素周期表中,过渡金属和稀有金属是其中两个重要的类别。
本文将深入探讨过渡金属和稀有金属的特点、性质和应用。
一、过渡金属过渡金属是指元素周期表中d区的元素,它们的原子结构有一个或多个不满的d电子壳层。
过渡金属具有以下几个显著特点:1. 高熔点和沸点:过渡金属具有较高的熔点和沸点,这是由于它们之间存在较强的金属键和金属间的相互作用力。
2. 变价性:过渡金属的化合物中,过渡金属离子可出现不同的氧化态,显示出较强的变价性。
这使得过渡金属离子在催化反应、光谱分析等领域具有广泛的应用。
3. 裂变性:过渡金属化合物常常可以通过赋予能量使其电子跃迁,从而发生裂变。
这种特性使得过渡金属化合物在荧光材料、激光器件等领域得到应用。
4. 色彩多样性:过渡金属化合物常常表现出丰富多样的颜色,这是由于不同氧化态的过渡金属离子吸收和发射不同波长的光。
这使得过渡金属化合物在颜料、染料等领域有广泛的应用。
常见的过渡金属包括铁、铜、银、钼、铂等,它们在工业和生活中扮演着重要的角色。
比如铁在建筑、交通工具和机械制造等领域有广泛应用;铜在电子、通讯和建筑等方面发挥着重要作用;银在导电材料、反射材料和摄影等领域具有重要地位。
二、稀有金属稀有金属是指元素周期表中f区的元素,它们的原子结构有一个或多个不满的f电子壳层。
稀有金属具有以下几个主要特点:1. 稀有度高:稀有金属在地壳中的含量较低,因此得名稀有金属。
这使得稀有金属具有较高的经济价值和战略地位。
2. 耐腐蚀性好:稀有金属具有较好的耐腐蚀性,可以抵抗氧化、腐蚀等外界环境的侵蚀。
这使得稀有金属在航空、化工和核工业等领域有广泛应用。
3. 罕见金属:稀有金属的存在形式多为分散态或矿石,因此开采和提炼稀有金属的成本较高,加之其用途广泛,使得稀有金属价格较高。
元素周期表中的过渡金属特点与应用

元素周期表中的过渡金属特点与应用过渡金属是指位于d区的元素,它们在原子内外电子的排布上具有特殊性质,呈现出独特的化学性质和广泛的应用价值。
下面将从元素周期表的角度出发,详细介绍过渡金属的特点和应用。
一、元素周期表中的过渡金属特点过渡金属具有以下特点:1. 化合价多变性:过渡金属能够在化合物中以不同的化合价存在。
这一特点使得它们可以形成多种不同的化合物,从而拓展了它们的应用领域。
2. 原子尺寸和离子半径变化规律:过渡金属的原子尺寸和离子半径在周期表中呈现出规律性的变化。
随着元素周期数的增加,原子半径逐渐减小,而离子半径则呈现复杂的变化规律。
3. 异常磁性:过渡金属具有较强的磁性,其中铁、镍和钴是常见的磁性过渡金属。
这一特点使得它们在制造电磁设备、磁性材料等方面具有重要的应用。
4. 催化性能:过渡金属具有优良的催化性能,尤其是在工业生产过程中的应用广泛。
比如,钯金属催化剂常用于化学合成中的氢化反应和氧化反应。
5. 彩色离子:过渡金属的化合物往往呈现出丰富多彩的颜色。
这是由于过渡金属能够吸收和发射可见光范围内的电磁波,使物质呈现不同的颜色。
二、过渡金属的应用1. 催化剂应用:过渡金属常被用作催化剂,广泛应用于各个行业。
铂金属催化剂在汽车尾气净化中起到催化还原的作用,使有害气体转化为无害物质;钯金属催化剂在有机合成中能够加速氢化和氧化反应,提高反应速率。
2. 电池材料:过渡金属氧化物常被用作电池材料。
锰酸锂是一种常用的正极材料,在锂离子电池中具有高能量密度和长循环寿命的特点。
3. 金属合金:过渡金属是制备金属合金的重要成分。
例如,钢中加入适量的铬、钼等过渡金属可以提高钢的硬度和耐腐蚀性,使其具备更广泛的应用领域。
4. 光电器件:过渡金属氧化物和硫化物是光电器件的重要组成部分。
如氧化铟锡(ITO)透明导电薄膜广泛应用于显示器和太阳能电池等领域。
5. 颜料和染料:过渡金属化合物常被用作颜料和染料,给产品带来丰富的颜色。
元素周期表中的过渡金属

医学应用
01
02
03
药物合成
过渡金属在药物合成中发 挥重要作用,如铂、钴、 镍等金属的配合物用于治 疗癌症的药物研发。
诊断试剂
某些过渡金属离子如铁、 铜、锌等参与生物体内的 代谢过程,可作为生物标 记物用于诊断疾病。
医疗器械
一些具有特殊物理和化学 性质的过渡金属及其合金 用于制造医疗器械,如手 术刀具、植入物等。
环境治理
污水处理
过渡金属化合物在污水处理中具有重要作用 ,能够有效去除水中的重金属离子和有害物 质,保障水质安全。
大气治理
利用过渡金属化合物去除大气中的有害气体 ,如二氧化硫、氮氧化物等,有助于改善空
气质量。
谢谢您的聆听
THANKS
元素周期表中的过渡金属
CONTENTS
• 过渡金属的概述 • 过渡金属的化学性质 • 过渡金属的物理性质 • 过渡金属的应用 • 过渡金属的发现与开采 • 过渡金属的未来发展
01
过渡金属的概述
定义与特性
定义
过渡金属是元素周期表中d区和ds区 的金属元素,它们具有未填满的d电 子壳层。
特性
过渡金属具有多种氧化态,可以形成 多种复杂的化合物,具有丰富的化学 性质和物理性质。
功能材料
过渡金属化合物在磁性、光学、电学 等方面具有优异性能,可用于信息存 储、光电器件、传感器等领域。
新能源开发
燃料电池催化剂
过渡金属(如铂、钯等)具有良好的催化性能,是燃料电池中重要的催化剂,有助于提 高燃料电池的效率和稳定性。
太阳能电池
过渡金属化合物在太阳能转换方面具有潜在应用价值,能够提高太阳能电池的光电转换 效率和稳定性。
详细描述
过渡金属具有多种氧化态,这是因为它们的d电子可以轻易地参与成键,形成不 同的价态。此外,由于d电子的存在,使得相邻氧化态间的电离能差较小,这使 得过渡金属在化学反应中容易发生氧化还原反应。
元素周期表中的过渡金属

元素周期表中的过渡金属元素周期表是化学中的重要工具,它按照原子序数将化学元素分类,并提供了有关元素性质的重要信息。
在周期表中,过渡金属是一组独特的元素,它们在化学和物理性质上与其他元素有所不同。
本文将介绍元素周期表中的过渡金属,并探讨它们的特点、应用和重要性。
1. 过渡金属的定义过渡金属是周期表中位于d区的元素,它们的电子结构具有特殊的特点。
这些元素的外层电子结构通常包含一个或多个d电子,因此它们被称为“过渡元素”。
过渡金属的一些典型代表包括铁、铜、铬和钼等。
2. 过渡金属的特性过渡金属具有许多独特的化学和物理性质,使其在许多应用领域中非常重要。
以下是一些过渡金属的典型特性:2.1 变价性:过渡金属的不同价态具有不同的电子配置,这使它们在化学反应中能够转移电子,从而形成不同的化合物。
2.2 良好的导电性和导热性:过渡金属通常具有良好的导电性和导热性,使其在电子工业和热传导领域得到广泛应用。
2.3 高熔点和高沸点:大多数过渡金属具有较高的熔点和沸点,这使其在高温环境下稳定性较好。
2.4 形成彩色化合物:过渡金属离子可以吸收和发射可见光,因此它们在形成彩色化合物和催化剂中具有重要作用。
3. 过渡金属的应用由于过渡金属的特殊性质,它们在许多不同的领域中得到广泛应用。
以下是一些常见的应用领域:3.1 电子工业:过渡金属的良好导电性使其成为电子器件中常用的材料,如导线、接插件和电路板等。
3.2 催化剂:许多过渡金属离子具有良好的催化活性,因此它们广泛应用于化工工业中的反应催化剂。
3.3 金属合金:过渡金属与其他元素的合金形成具有特殊性能的金属材料,如钢铁、铜合金和镍基合金等。
3.4 医学应用:一些过渡金属离子在医学领域具有抗菌、止血和治疗特定疾病的作用,如铁离子在贫血治疗中的应用。
4. 过渡金属的重要性过渡金属在化学和材料科学中的重要性不可忽视。
它们的独特性质为我们提供了研究和开发新材料、催化剂和技术的基础。
过渡金属名词解释

过渡金属名词解释过渡金属是元素周期表中的一个独特的家族,它们可是化学世界里的一群“超级明星”呢。
首先呢,从原子结构的角度来看,过渡金属原子的最外层电子数一般为1 - 2个,次外层电子却未填满。
这一特殊的电子结构使得过渡金属具有许多独特的化学性质。
比如说铁,它的原子结构就让它能够参与各种各样的化学反应。
在我们的日常生活中,铁生锈这个现象就和它的原子结构息息相关。
铁原子容易失去电子与氧气结合,形成铁锈,这看似简单的氧化过程,背后却是过渡金属原子结构特性的体现。
过渡金属在化合物中的化合价往往有多种。
以锰为例,锰可以有+2、+4、+6、+7等多种化合价。
这种多变的化合价是因为过渡金属原子的d轨道电子可以在不同的反应条件下参与成键。
在高锰酸钾(KMnO₄)中,锰是+7价,它具有很强的氧化性,可以用来消毒、做化学分析中的氧化剂等。
而在氯化锰(MnCl₂)中,锰是+2价,它更多地表现出金属离子的一些基本性质,像在溶液中可以和碱发生反应生成氢氧化锰沉淀。
过渡金属还具有很强的催化性能。
铂、钯等过渡金属在汽车尾气净化的催化剂中发挥着不可替代的作用。
汽车尾气中含有一氧化碳、氮氧化物等有害气体,在有过渡金属催化剂存在的情况下,这些有害气体能够在较低的温度下发生化学反应,转化为无害的二氧化碳、氮气等。
这是因为过渡金属能够提供合适的反应活性位点,降低反应的活化能,就像给化学反应开了一条“捷径”。
再比如合成氨工业中的铁触媒,它以铁为主要成分,能够加快氮气和氢气合成氨的反应速度。
如果没有铁触媒,这个反应需要在非常高的温度和压力下才能进行,有了铁触媒,反应条件就可以温和许多。
过渡金属的配合物也是化学研究中的一个热门领域。
过渡金属离子可以和许多有机或无机的配体形成配合物。
像铜离子可以和氨分子形成铜氨配合物。
这种配合物的形成会改变过渡金属离子的性质,颜色就是一个很明显的变化。
例如,氯化钴(CoCl₂)在没有和配体结合时是蓝色的,当它和水形成配合物后就变成了粉红色。
元素周期表中的过渡元素

元素周期表中的过渡元素元素周期表是描述化学元素的分类和属性的重要工具。
其中,过渡元素是周期表中的一类特殊元素,具有许多独特的化学和物理性质。
本文将介绍过渡元素的定义、特点、应用以及对人类社会的重要意义。
一、过渡元素的定义和特点过渡元素是周期表中d区的元素,它们的原子结构中有不满的d电子壳层。
根据IUPAC的定义,从原子序数21(钪,Sc)到原子序数30(锌,Zn)以及从原子序数39(钇,Y)到原子序数48(银,Ag)的元素属于过渡元素。
过渡元素具有以下几个特点:1. 多种氧化态:过渡元素的d电子壳层不是完全填满的,因此它们可以容易地失去或获得电子,形成多种氧化态。
这使得过渡元素在化学反应中具有多样性和灵活性。
2. 良好的催化性能:由于其电子结构的特殊性质,过渡元素常常表现出良好的催化活性。
它们可作为催化剂参与许多重要的化学反应,促进反应速率和选择性。
3. 彩色化合物:过渡元素离子在溶液中或固体中具有吸收和发射特定波长光谱的能力,因此它们通常形成彩色的化合物。
这也是过渡元素被应用于颜料、染料和激光材料等领域的原因之一。
4. 高熔点和密度:大多数过渡元素具有较高的熔点和相对密度。
这与它们的原子结构和离子半径有关,使得过渡元素在高温和高压条件下具有许多特殊的物理性质。
5. 磁性: 过渡金属元素中的许多具有未配对的d电子,这使得它们具有磁性。
这些元素在物理和材料科学中的磁学研究中非常重要。
二、过渡元素的应用过渡元素在许多领域都有广泛的应用,下面是一些重要的应用领域:1. 工业催化剂:过渡金属催化剂在化学工业中广泛应用,用于促进氢气合成、石油加工、氨的合成和环保领域。
2. 电子材料:许多过渡金属元素具有优异的电导率、热导率和磁性。
它们被广泛应用于电子、计算机、通信和数据存储等领域。
3. 生物学:过渡金属离子在生物学过程中发挥关键作用。
例如,铁在血红蛋白和细胞色素中起到氧气运输的重要作用。
4. 颜料和染料:由于过渡元素形成彩色的化合物,它们被广泛用于颜料、染料和陶瓷等领域,为我们的生活增添了色彩。
元素周期表中的过渡金属

元素周期表中的过渡金属元素周期表是描述元素的分类和性质的重要工具。
其中,过渡金属是指在周期表中位于主族元素和稀土金属之间的一组元素。
它们具有一系列独特的性质和应用,对我们的日常生活和科学领域都有重要影响。
过渡金属的定义在元素周期表中,过渡金属通常被定义为具有部分填充的d轨道的元素。
它们的原子结构特点是d电子层不是满电子层,即d轨道中存在未配对或未填满的电子。
这使得过渡金属具有许多独特的性质,例如可变的氧化态、良好的导电性和热导性等。
典型的过渡金属元素过渡金属包括铬(Cr)、锰(Mn)、铁(Fe)、钴(Co)、镍(Ni)、铜(Cu)、锌(Zn)等。
它们具有共同的特征,如高熔点、高密度、良好的导电性和热导性等。
这些元素在自然界中广泛存在,且大多数用途广泛。
性质和应用过渡金属具有许多重要的物理和化学性质,为它们带来了广泛的应用。
以下是一些常见的例子:1. 催化剂:过渡金属广泛用于催化反应,例如铂(Pt)催化剂在汽车尾气净化和氢气燃料电池中起着重要作用。
2. 磁性材料:铁、钴和镍等过渡金属是制造磁性材料的重要成分。
它们被广泛应用于电子设备、电动机和磁存储介质等领域。
3. 合金:过渡金属在合金制备中起着关键作用。
例如,钢是由铁和碳以及其他过渡金属组成的合金,拥有优异的强度和耐腐蚀性能。
4. 荧光材料:某些过渡金属离子在激发条件下能够发出明亮的荧光,例如钐(Sm)和铕(Eu)等离子常用于荧光显示器和照明装置中。
5. 生物学应用:许多过渡金属离子在生物体内具有重要的生理功能,如铁在血红蛋白中的运输氧气。
过渡金属的周期性和趋势过渡金属元素在元素周期表中按照原子序数的增加排列。
它们的性质和趋势在一定程度上与原子序数的变化相吻合,但也存在一些异常现象。
1. 电子结构:过渡金属的电子结构具有一定的规律性。
它们的原子结构中的d电子数目逐渐增加,从Sc(21)到Cu(29)的元素具有各自特定的电子组态。
2. 原子半径:在过渡金属族中,原子半径从左到右逐渐减小。
元素周期表中的过渡金属元素特性

元素周期表中的过渡金属元素特性元素周期表是现代化学学科的基本工具之一,它将所有已知的化学元素组织成特定的顺序。
在这个表中,过渡金属元素占据了一整个区域,包括3d系列和4d系列的元素,它们具有特殊的化学和物理性质,对于我们理解和应用元素周期表是非常重要的。
本文将重点探讨过渡金属元素的特性。
一、原子结构过渡金属元素的共同特点是它们的原子结构中有一个或多个未填满的d轨道。
这意味着过渡金属元素的电子结构在外层电子的填充上有一些特殊规律。
以铁(Fe)为例,其电子结构为1s² 2s² 2p⁶ 3s² 3p⁶ 4s²3d⁶,其中未填满的3d轨道成为其特征。
二、物理性质过渡金属元素常常具有良好的导电性和热导率。
这是由于它们的原子结构中的未填满d轨道,能够容纳更多的电子和形成更复杂的电子结构,从而增强导电性能。
此外,过渡金属元素的硬度通常较高,且具有高熔点和高密度。
这些物理性质使得过渡金属元素在工业和科学研究中有广泛的应用。
三、化学性质1. 变价性:过渡金属元素通常具有多种变价态。
由于其未填满的d轨道,过渡金属元素可以通过失去或获得d轨道中的电子来形成不同的化合物。
这种多变价性使得过渡金属元素在催化剂、电池等领域有着重要的应用。
2. 形成配合物的能力:过渡金属元素具有形成配合物的能力,这是由于它们的d轨道可以接受配体的电子对并与之形成稳定的配合物。
这种能力使得过渡金属元素在生物学、医药化学和材料科学等领域具有广泛的应用。
3. 催化活性:由于其特殊的电子结构和变价性,过渡金属元素经常作为催化剂在化学反应中发挥着重要的作用。
例如,铂(Pt)常用来催化氢气和氧气的结合以产生水,铁(Fe)则在哈伯-博什过程中用作氨的合成催化剂。
四、应用领域过渡金属元素在许多领域都有着广泛的应用。
例如,铁、钴(Co)和镍(Ni)被广泛建筑和汽车制造业用作钢铁的合金成分。
铜(Cu)是一种重要的导电金属,广泛应用于电子、电力和通信行业。
化学元素周期表基础知识点清单过渡金属

化学元素周期表基础知识点清单过渡金属化学元素周期表基础知识点清单-过渡金属过渡金属是元素周期表中的一类元素,它们的特点是位于周期表的B区,外层电子数为d的1至10个电子。
过渡金属具有许多独特的性质和重要的应用,本文将为您介绍一些过渡金属的基础知识点。
1. 过渡金属的定义过渡金属是指周期表中第4至第11族的元素,包括铬、锰、铁、钴、镍、铜、锌等。
它们在化学性质上通常表现为多价态和显著的配位能力,可形成复杂的络合物。
2. 过渡金属的电子结构过渡金属的电子结构特点是在外层能级中含有不满的d电子。
举个例子,铁的电子结构是[Ar] 3d^6 4s^2,其中3d轨道的电子数为6个,处于不满的状态,因此具有很强的反应活性。
3. 过渡金属的物理性质过渡金属通常是固态,具有较高的密度和熔点。
它们的硬度较高,具有良好的导电性和导热性。
此外,过渡金属还具有良好的延展性和塑性,可轻松制成细丝或薄片。
4. 过渡金属的化学性质过渡金属的化学性质独特且多样。
它们能够与其他元素形成氧化物或化合物,产生丰富的配位化合物。
过渡金属也可以发生氧化还原反应,并在不同价态之间转变。
5. 过渡金属的催化性质过渡金属在许多化学反应中起到重要的催化作用。
催化剂能够降低化学反应的活化能,提高反应速率。
过渡金属的多价态和丰富的配位能力使其成为优秀的催化剂,广泛应用于工业生产和环境保护等领域。
6. 过渡金属的重要应用过渡金属及其化合物在许多领域都有重要的应用。
铁和钢是构建基础设施和制造机械的关键材料;铜被广泛用于电气工程和通信技术;钴广泛用于电池制造和催化剂领域。
此外,许多药物和颜料也包含过渡金属元素。
总结:过渡金属作为元素周期表的重要一部分,具有独特的物理和化学性质。
了解过渡金属的基础知识对于深入研究和应用化学非常重要。
通过掌握过渡金属的电子结构、物理和化学性质,我们可以更好地理解和利用这些元素在催化、材料科学、医药和环境等领域中的重要性。
元素周期表中的过渡元素

元素周期表中的过渡元素元素周期表是化学中最为重要的工具之一,它按照元素的原子序数排列,将各种元素分类并展示其基本性质。
其中,过渡元素是元素周期表中的一个重要分类。
本文将对过渡元素进行详细的介绍和解析。
一、什么是过渡元素过渡元素,又称过渡金属元素,是指元素周期表中位于d区的元素。
具体来说,它们位于周期表的第4至7周期,并且填充d轨道的电子数量从1至10,即d1至d10。
过渡元素具有一些特殊的性质,使得它们在化学反应和催化过程中起到重要的作用。
二、过渡元素的特性和性质1. 原子结构和电子配置过渡元素的原子结构是它们特殊性质的基础。
由于过渡元素具有填充d轨道的电子,其电子配置比较复杂。
以铁(Fe)为例,其电子配置为 [Ar] 3d^6 4s^2。
可以看出,过渡元素的电子配置中包含了未填满的d轨道和填满的s轨道。
2. 多种化合价和化合物形成过渡元素常常能够形成多种化合价和化合物。
这是因为过渡元素的d轨道中的电子容易发生配位反应,形成不同化合物的结构。
以铜(Cu)为例,它可以形成Cu+和Cu2+两种离子,分别与不同的配体形成多种不同的配合物。
3. 颜色和催化性能过渡元素及其化合物常常具有鲜艳的颜色,这是由于它们的d轨道电子发生跃迁所致。
这种特性使得过渡元素被广泛应用在染料、颜料和催化剂等领域。
例如,钛(Ti)被广泛用于催化剂制备中,而铬(Cr)则用于制造不锈钢。
4. 磁性和电导性由于过渡元素具有未填充的d轨道电子,它们常常表现出良好的磁性和电导性。
例如,铁(Fe)和钴(Co)是常见的磁性材料,可以用于制造磁铁和磁带。
铜(Cu)和银(Ag)则是良好的电导体,广泛用于导线和电路中。
三、过渡元素的应用1. 催化剂过渡元素及其化合物在催化剂制备中具有重要的应用。
催化剂可以加速化学反应速率,降低反应温度和能源消耗。
铂(Pt)和钯(Pd)常被用作催化剂,例如在汽车尾气净化中,它们能将有害气体转化为无害物质。
2. 电池和电子器件过渡元素在电池和电子器件中也发挥着重要的作用。
过渡金属元素定义

过渡金属元素定义过渡金属元素定义是指周期表中位于d区的元素。
这些元素有着一些独特的特征和性质,使它们在化学、物理和生物领域中表现出色。
以下是更详细的有关过渡金属元素的定义和特征的分解:1. 定义过渡金属元素是指在周期表中从第3到第12组的元素。
它们都拥有不同数量的d电子,在它们的外层离子殼中,它们还具有可变的氧化数。
它们的原子结构与物理性质具有一些相似之处,这些性质在大的类别中可以归纳为金属的特征。
2. 特征过渡金属元素具有以下特征:a. 常见离子的颜色较为复杂这是由于它们的d电子处于相对较低的能量状态,这使它们的电子吸收和发射能量的方式与其他元素不同。
b. 构成化合物的能力较强由于过渡金属元素的d电子数量有所不同,因此它们可以参与不同类型的键合,这使它们可以形成广泛的化合物。
c. 具有良好的热和电导性由于它们的原子结构具有多个构建电子能带的有用d电子,因此它们的热和电导性能比其他元素高。
d. 化学反应稳定由于它们具有多个价态,因此它们可以形成复杂稳定的化合物,这使它们在化学反应中表现出色。
3. 应用由于它们的特性和独特的原子结构,过渡金属元素在许多领域中都具有广泛的应用,例如:a. 产业过渡金属元素广泛应用于材料加工、制造和修复,这些过程需要导电性和不容易腐蚀,并且通常需要特殊的颜色。
b. 医学由于它们的化学反应和稳定性能力,过渡金属元素广泛应用于医学,作为诊断和治疗工具。
c. 环保过渡金属元素还可以广泛应用于污染控制和环保,例如过渡金属元素可以用来去除烟气中的污染物。
总结:过渡金属元素的定义、特点和应用说明了它们在许多领域的很多优点。
它们的化学反应稳定,因此在许多应用中具有广泛的适用性。
这些元素的特殊性质和应用使得它们在现代科技和生产中有着广泛而关键的作用。
元素周期表中的过渡金属元素性质分析

元素周期表中的过渡金属元素性质分析元素周期表是化学领域中最重要的工具之一,它将所有已知的化学元素按照一定的规律排列在一起。
其中,过渡金属元素是周期表中的一个重要类别,它们具有独特的性质和广泛的应用。
本文将对过渡金属元素的性质进行分析和探讨。
过渡金属元素是指周期表中3至12族元素,它们的电子排布在d轨道中。
这使得过渡金属元素具有一系列特殊的性质。
首先,过渡金属元素常常具有多种氧化态。
这是因为它们的d轨道能级相对较低,容易失去或获得电子,形成不同的氧化态。
例如,铁元素可以呈现2+、3+、4+等多种氧化态,这使得它在生物体内起着重要的作用,如参与氧气的运输和储存。
其次,过渡金属元素具有良好的催化性能。
由于它们的d轨道能级接近反应物和产物的能级,过渡金属元素能够提供活化能,促进化学反应的进行。
铂金、钯等过渡金属元素常被用作催化剂,广泛应用于化学工业、环境保护和能源领域。
例如,铂金催化剂可用于汽车尾气净化,将有害气体转化为无害物质。
此外,过渡金属元素还具有良好的磁性和导电性。
这是因为它们的d轨道中存在未填充的电子,这些电子能够自由移动,形成电流。
铁、钴、镍等过渡金属元素是常见的磁性材料,它们在电子学和材料科学中有着重要的应用。
例如,硬盘驱动器中的磁性材料就是由过渡金属元素构成的,它们能够存储和读取大量的数据。
过渡金属元素还表现出丰富的颜色。
这是由于它们的d轨道能级与可见光的能级相近,能够吸收或散射特定波长的光。
铬元素的化合物常常呈现绿色,铜元素的化合物呈现蓝色。
这些颜色不仅赋予了过渡金属元素化合物独特的外观,还在颜料、染料等领域中得到广泛应用。
最后,过渡金属元素在生物体内发挥着重要的生理功能。
铁元素是血红蛋白的组成部分,它能够与氧气结合并在体内进行氧气的运输。
锌元素是许多酶的辅助因子,参与多种生化反应。
这些生理功能使得过渡金属元素在医学和生物学研究中具有重要的地位。
综上所述,过渡金属元素具有多种独特的性质和广泛的应用。
元素周期表中的过渡金属元素

元素周期表中的过渡金属元素元素周期表是化学领域中最为基础的工具之一,它将所有已知的化学元素按照一定的规律排列起来。
其中过渡金属元素是周期表中的一类重要元素,它们的性质和应用广泛而深入。
本文将探讨元素周期表中的过渡金属元素及其在生活中的重要性。
一、什么是过渡金属元素过渡金属元素是指周期表中的d区元素,它们的电子结构特点是在最外层电子壳中含有d电子。
这些元素包括铁、铜、锌、铬、钴等,它们在化学反应中具有独特的性质,如高反应活性、多种氧化态等。
过渡金属元素的化学性质使得它们在许多重要的应用中发挥着重要的作用。
二、过渡金属元素的物理性质过渡金属元素的物理性质与其电子结构密切相关。
由于d电子的存在,过渡金属元素具有较高的熔点和沸点,以及较高的硬度和密度。
这些特性使得过渡金属元素在材料科学中的应用广泛,如用于制造高强度的合金和耐高温材料。
三、过渡金属元素的化学性质过渡金属元素的化学性质多样且丰富。
它们通常具有多种氧化态,可以与其他元素形成多种化合物。
这些化合物在催化剂、电池、磁性材料等方面有着广泛的应用。
例如,铁是最常见的过渡金属元素之一,它在生活中的应用非常广泛,如用于制造钢铁、电器、建筑材料等。
四、过渡金属元素的生物学意义过渡金属元素在生物学中也扮演着重要的角色。
例如,铁是血红蛋白中的关键成分,它在输送氧气和维持身体正常功能方面起着至关重要的作用。
锌是许多酶的重要成分,它参与了许多生物化学反应。
过渡金属元素的生物学功能对于人类的健康和生命至关重要。
五、过渡金属元素的应用过渡金属元素在各个领域都有广泛的应用。
在工业上,铁、铜、锌等过渡金属元素用于制造汽车、航空器、电子设备等。
在能源领域,钴、镍等过渡金属元素被用于制造电池和催化剂。
在医学领域,铂等过渡金属元素被用于制造抗癌药物。
过渡金属元素的应用范围广阔,对于人类社会的发展起着重要的推动作用。
六、过渡金属元素的环境影响尽管过渡金属元素在许多领域有重要的应用,但它们的排放和使用也会对环境造成一定的影响。
过渡金属元素解析
族
周期
IIIB IVB VB VIB VIIB
第一过渡系 Sc Ti V Cr Mn
VIIIB Fe Co Ni
IB IIB Cu Zn
第二过渡系 Y Zr Nb Mo Tc Ru Rh Pd Ag Cd
离子中未配对的电子数
离子在水溶液中的颜色
0
Ag+、Zn2+、Cd2+、Hg2+、Sc3+、Ti4+(无色)
1
Cu2+(蓝色)、Ti3+(紫色)
2
Ni2Co2+(桃红色)
4
Fe2+(淡绿色)
5
Mn2+(淡红色)、 Fe3+ (浅紫色)①
① Fe3+在溶液中由于水解等原因,水溶液常呈现黄色或褐色。
族
周期
IIIB IVB VB VIB VIIB
第一过渡系 Sc Ti V Cr Mn
VIIIB Fe Co Ni
IB IIB Cu Zn
第二过渡系 Y Zr Nb Mo Tc Ru Rh Pd Ag Cd
第三过渡系 La Hf Ta W Re Os Ir Pt Au Hg
原子结构特点:
➢随核电荷的递增,电子依次填充在次外层的d轨道上, 最外层有1~2个电子; ➢其价层电子构型为(n-1)d1~10ns1~2(Pd为4d105s0)
第三过渡系 La Hf Ta W Re Os Ir Pt Au Hg
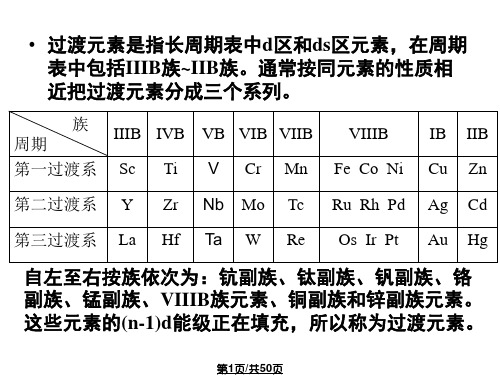
自左至右按族依次为:钪副族、钛副族、钒副族、铬 副族、锰副族、VIIIB族元素、铜副族和锌副族元素。 这些元素的(n-1)d能级正在填充,所以称为过渡元素。
过渡元素的名词解释

过渡元素的名词解释过渡元素,也称为过渡金属,是化学元素周期表中的一部分。
它们位于周期表的中间,处于主族元素和稀有气体之间。
过渡元素的特征是具有多种化学价态,并且具有良好的热和电导性能。
本文将通过对过渡元素的性质和应用的介绍,来深入解释这一概念。
1. 过渡元素的性质过渡元素具有许多独特的性质,使它们在化学和物理领域中具有广泛的应用。
首先,过渡元素的电子配置具有特殊性。
它们的电子填充在d轨道中,因此能够容纳更多的电子。
这也是为什么过渡金属能够形成多个氧化态的原因之一。
正因为这种电子配置的特殊性,过渡元素之间的相互作用和混杂非常复杂,导致它们具有丰富的化学性质。
其次,过渡元素的离子半径逐渐减小。
在周期表中,随着元素的原子序数的增加,过渡金属离子的半径逐渐减小。
这一性质使得过渡元素可以形成复杂的配合物,与其他离子或分子进行配位反应。
这也是过渡金属在催化剂和生物学中广泛应用的原因之一。
另外,由于过渡元素在周期表中的位置接近稀有气体,因此具有稳定的电子云分布和较高的原子核电荷。
这使得过渡元素具有良好的热和电导性能,并且能够形成稳定的化合物。
例如,许多过渡金属是良好的催化剂,它们能够加速化学反应的速率,提高产率和选择性。
2. 过渡元素的应用过渡元素在各个领域具有广泛的应用。
以下将介绍几个重要的领域。
首先是催化剂领域。
过渡金属催化剂被广泛应用于化学反应中。
在催化剂作用下,化学反应的速率可以被显著提高,反应条件也变得更加温和。
许多工业生产中的重要反应都依赖于过渡金属催化剂,如加氢反应、氧化反应和聚合反应等。
其次是生物学领域。
许多生物体内的重要酶活性中心含有过渡金属。
例如,血红蛋白中的铁离子能够与氧气结合,用于氧气的运输;叶绿素中的镁离子参与光合作用过程。
这些过渡金属离子在生物学中起着关键的作用,保证了生物体正常的新陈代谢和生命活动。
此外,过渡元素还被广泛应用于材料科学和电子工程领域。
过渡金属的合金和化合物具有良好的热和电导性能,使它们成为制造高温材料和半导体器件的重要原料。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
+4 +5 +6 +4 +3
+2
+6
+7
第二过渡系 Y Zr Nb Mo Tc Ru Rh Pd Ag Cd
氧化数 +3 +4 +5 +6 +7 +4 +3 +2 +1 +2
第三过渡系 La Hf Ta W Re Os Ir Pt Au Hg
氧化数
+3 +4 +5 +6 +7 +8 +3 +2 +1 +1 +4 +4 +3 +2
(2)多种氧化数
族
元素
3dn 主 要 氧 化 数
ⅢB ⅣB ⅤB ⅥB ⅦB
Ⅷ
ⅠB ⅡB
Sc Ti V Cr Mn Fe Co Ni Cu Zn
3d1 3d2 3d3 3d5 3d5 3d6 3d7 3d8 3d9 3d10
+2
+2 +2 +2 +2 +2 +1 +2
+3 +3 +3 +3 +3 +3 +3 +3 +2
第6章 过渡金属元素
6.1 过渡元素的通性 6.2 ⅣB~ⅥB族金属元素及其化合物 6.3 ⅦB~ⅧB族金属元素及其化合物 6.4 稀土金属及其应用
• 过渡元素是指长周期表中d区和ds区元素,在周期 表中包括IIIB族~IIB族。通常按同元素的性质相 近把过渡元素分成三个系列。
族
周期
IIIB IVB VB VIB VIIB
• 过渡元素是指长周期表中d区和ds区元素,在周期 表中包括IIIB族~IIB族。通常按同元素的性质相 近把过渡元素分成三个系列。
族
周期
IIIB IVB VB VIB VIIB
第一过渡系 Sc Ti V Cr Mn
VIIIB Fe Co Ni
IB IIB Cu Zn
第二过渡系 Y Zr Nb Mo Tc Ru Rh Pd Ag Cd
第一过渡系 第二过渡系 第三过渡系
ⅡB E (M2+/M)/V Ⅷ Zn -0.7626 Ni Cd -0.403 Pd Hg +0.8535 Pt
E (M2+/M)/V -0.257 +0.92 +1.2
第二、第三过渡系金属都不活泼,与氧化性酸在 加热时才能发生反应。
Mo只能与浓硝酸和热浓硫酸反应,铌、铑、钽、 锇、铱与王水都很难反应
Zn -0.7626
稀HCl H2SO4等
值同I其。I一IB可活第族周溶泼一是期于性过过迅元非减渡渡速素氧元弱氧系从素化化金左中,性属到最与稀除活右水酸C泼作总u置的用外趋换金释,势出E属放E,氢出(MS(氢气Mc2+、气。/2M+Y/M、)均L)增为a 能大负
同族元素(除Sc分族外)自上往下金属活泼性降低
• 如果离子中的电子都已配对,如d0、d10等就比较稳 定,不易激发,这些离子一般无色,如Sc3+、Ag+、 Zn2+等。
6.1.2 化学性质
• (1)金属活泼性 • (2)多种氧化数 • (3)易形成配合物
(1)金属活泼性
元素
E (M2+/M)/V 可溶该金 属的酸
Sc
— 各种
酸
Ti
-1.63 热HF HCl
+4 +4
+4
+5
+6 +6 +7
稳定氧化数 不稳定氧化数
1.从左到右, 元素最高氧化数升高, ⅦB后又降低
(2)多种氧化数
族 ⅢB ⅣB ⅤB ⅥB ⅦB Ⅷ ⅠB ⅡB
第一过渡系 Sc Ti V Cr Mn Fe Co Ni Cu Zn
氧化数Байду номын сангаас
+3 +3 +4 +3 +2 +2 +2 +2 +1 +2
第一过渡系 Sc Ti V Cr Mn
VIIIB Fe Co Ni
IB IIB Cu Zn
第二过渡系 Y Zr Nb Mo Tc Ru Rh Pd Ag Cd
第三过渡系 La Hf Ta W Re Os Ir Pt Au Hg
自左至右按族依次为:钪副族、钛副族、钒副族、铬 副族、锰副族、VIIIB族元素、铜副族和锌副族元素。 这些元素的(n-1)d能级正在填充,所以称为过渡元素。
IVB~VIIB族元素的单质具有高熔、沸点、高硬度的原 因,主要是它们的原子半径较小,有效核电荷较大, 价电子层有较多的未成对d电子(铬有5个),这些d电 子也参与成键,因而增强了金属的强度和晶格能。
(2)水合离子的颜色
• 过渡金属的水合离子、含氧酸根离子和配离子常 是有颜色的,与此相反,主族金属的相应离子是 无色的。
2
Ni2+(绿色)
3
Cr3+(蓝紫色)、Co2+(桃红色)
4
Fe2+(淡绿色)
5
Mn2+(淡红色)、 Fe3+ (浅紫色)①
① Fe3+在溶液中由于水解等原因,水溶液常呈现黄色或褐色。
• 通常,基态和激发态的能量差越小,电子吸收光的 波长越长,物质呈现的颜色就越深;反之,电子吸 收光的波长越短,则物质呈现的颜色就越浅。
(1)熔点、沸点及硬度
• 过渡金属大多熔点、沸点高,硬度大,强 度高,密度也大(如Os、Ir 的密度为 22.6×103kg·m-3),属重金属。
熔点、沸点最高的金属主要集中在d区,尤其是 IVB、VB、VIB、VIIB族的金属,其中钨的熔点、 沸点最高(熔点3683K,沸点6200K)。
过渡元素熔点、沸点的递变规律是自IIIB至VIB依次升 高,VIB族金属的熔点、沸点最高,VIIB族以后逐渐 降低,IIB族已是低熔点金属,汞的熔点(234.13K) 最低。VIB族的铬硬度最大(9)。
• 过渡元素的离子通常在d轨道上有未成对电子,这 些电子的基态和激发态的能量比较接近,一般只 要是可见光中的某些波长的光就可使电子激发, 这些离子大都具有颜色。
离子中未配对的电子数
离子在水溶液中的颜色
0
Ag+、Zn2+、Cd2+、Hg2+、Sc3+、Ti4+(无色)
1
Cu2+(蓝色)、Ti3+(紫色)
第三过渡系 La Hf Ta W Re Os Ir Pt Au Hg
原子结构特点:
➢随核电荷的递增,电子依次填充在次外层的d轨道上, 最外层有1~2个电子; ➢其价层电子构型为(n-1)d1~10ns1~2(Pd为4d105s0)
6.1.1 物理性质
• 过渡元素的单质显示典型的金属性质,有 金属光泽,延展性,是热和电的良导体等。
V
Cr
-1.13 -0.90
浓H2SO4 稀HCl HNO3、HF H2SO4
Mn -1.18 稀H2SO4 HCl等
元素
Fe Co
Ni
E (M2+/M)/V -0.44 -0.277 -0.257
可溶该金 属的酸
稀HCl 稀HCl H2SO4 等
等 (缓慢)
稀H2SO4 HCl等
Cu
0.34
浓 H2SO4
