第九章 乙烯及其衍生物
高等有机第九章 周环反应(协同反应)

第九章周环反应(协同反应)协同反应——(1)此类反应中无产生离子或自由基等中间活性体(2)不受催化剂或溶剂的影响(3)键的生成和断裂在一步中完成(4)可在热和光照下反应(5)立体专一性反应由于反应的过渡态是一环状结构,所以也称为周环反应。
周环反应是以轨道对称守恒原理为基础的,由Woodward提出。
第一节分子轨道对称守恒定律1、术语:以乙烯分子为例:21反键轨道成键轨道分子轨道用波函数来表示:对乙烯分子π轨道来说,它有一个对称因素:为面对称(成键轨道S),而对反键轨道来说是反对称(A)C1对称:Symmetry波函数的数学符号相同,S 面:对映关系轴:转180°反对称:Antisymmetry波函数的数学符号相反,A轴C1:二个碳原子的连线轴C2:两个平面乙烯面与m平面的交线节点:将符号相同的波函数相连与C1轴的交点乙烯的π型分子轨道、节点数和对称性总结为:反键轨道成键轨道轨道节点数对称性21m C2A SS A 节面节点的物理意义:(1)节点越多,说明该轨道的能级越高不安定因素(2)节点处的电子密度等于零对Ψ1来说:是π电子的最高占有分子轨道(HOMO)high occupied molecule orbit *不是说满轨道,只要有一个也是占有最高占有轨道的电子束缚得最松弛,具有给电子的性质,最易激发到最低空轨道,因此这二个轨道为Ψ2是最低的空分子轨道(LUMO)low unoccupied molecule orbit 前线轨道(前沿轨道)对电子的亲和力较强,具有接受电子的性质丁二烯的分子轨道及其对称性:节点数 对称性 m C 23210A S S A A S S A21己三烯的分子轨道及其对称性321节点数 对称性 m C 2543210A S S A A S S A A S S A当最高轨道HOMO 的电子受到光的吸收光子的能量发生跃迁,到最低空轨道时,那时该轨道就变成HOMO 了基态:未激发的HOMO激发态:激发的HOMO ,相当于LUMO第二节 电子反应中的轨道对称守恒原理电环反应中的两种反应形式:1、热化学:是反应物分子处于基态所发生的反应 HOMO2、光化学: 激发态所发生的反应 LUMO 一、丁二烯和环丁烯的电环反应hγγLUMOHOMOCH3CH3H H 175。
第九章 聚合物的化学反应(2012)

丙烯腈、聚丙烯酰胺经水解,最终均能形成聚丙烯酸。
CH 2 CH CO OC H 3 OH CH 2 CH C OO H
聚丙烯酸或部分水解的聚丙烯酰胺可用于锅炉水的
防垢和水处理的絮凝剂,水中有铝离子时,聚丙烯酸成
絮状,与杂质一起沉降除去。
9 聚合物的化学反应
22
9.2
聚合物的基团反应
9.2.5 苯环侧基的取代反应
聚乙烯醇缩醛化反应可得到重要的高分子产品。
CH 2 C H CH 2 C H OH OH + RCH O H CH O CH CH O
缩甲醛:维尼纶 缩丁醛:良好的玻璃粘合剂 9 聚合物的化学反应
R
21
9.2
聚合物的基团反应
9.2.4 聚丙烯酸酯类的基团反应
与丙烯腈、丙烯酰胺的水解相似,聚丙烯酸甲酯、聚
9 聚合物的化学反应
23
9.2.5 苯环侧基的取代反应
H 2 C CH + H 2 C CH 悬浮共聚合 体型共聚物小珠
H 2C C H 浓硫酸磺化 (阳离子交换树脂) SO 3 H
+
NR 3 氯甲基化
+
(阴离子交换树脂) C H 2 Cl CH 2 N R 3 Cl
-
P
SO 3 H
-
+
Na 交 换 P H C l, 再 生
聚苯乙烯及其共聚物,带有苯环侧基,苯环上的氢原子
容易进行取代反应。几乎可进行芳烃的一切反应。
如:以苯乙烯-二乙烯苯共聚物为母体制备离子交换树脂。 离子交换树脂由三部分组成:不溶不熔的三维网状骨架 、固定在骨架上的官能团和官能团所带的可交换离子。 如PS类的是由苯乙烯与二乙烯基苯的悬浮共聚得到体型
第九章 乙烯及其衍生物..

工业生产方法
乙炔水合法
催化剂:HgSO4 1916年工业化,技术成熟,产品纯度高 催化剂有毒,耗能,被取代
乙醇制乙醛
吸热脱氢
催化剂:金属铜 操作温度:260~290 度,副产氢
放热氧化脱氢
催化剂:金属银 550度下反应,容易深度氧化
C3/C4烷烃氧化制乙醛
丙烷/丁烷混合物气相氧化制乙醛 1943年在美国工业化 425度,1MPa下反应 产物分离困难
乙烯直接氧化法
又称瓦克法,是HESS(赫斯)公司开发 原料便宜,成本低,副反应少,收率高 全世界广泛使用
乙烯液相氧化法生产乙醛
反应原理
催化剂:氯化钯、氯化铜的盐酸水溶液 三步
工艺过程
一步法工艺,也称氧气法
125度,0.3MPa 加压精馏塔 催化剂再生
O2,盐酸 CuCl氧化为CuCl2
二步法制乙醛
也称空气法 105~110度,1.0~1.2MPa 反应器一
羰基化反应
反应器二
氯化亚铜的氧化反应
醋酸
醋酸的性质
乙酸,CH3COOH 特殊刺激性气味的无色液体 冰醋酸
醋酸乙烯
性质和用途
CH3COOCHCH2,醋酸乙烯酯 合成维尼纶
过氧化物 醋酸乙烯 聚合 聚醋酸乙烯 醇解 NaOH-CH3OH 聚乙烯醇
维尼纶
醋酸乙烯的生产方法
乙炔法
/ 硫酸锌 C2H2 CH3COOH 硫酸汞 CH3COOCHCH 2 H2
乙烯气相催化氧化法
反应机理
二氯乙烷生成
二氯乙烷裂解原理
高二化学烃的衍生物课件

3
分离和提取
烃衍生物在化学分离和提取技术中被广 泛应用,如蒸馏和萃取。
应用案例:石油化工
汽油 合成橡胶
塑料
石油提炼中的主要产品,广泛用于汽车燃料。
通过合成工艺,利用烃衍生物生产出耐磨橡胶材 料。
烃衍生物作为塑料的重要组成部分,被广泛应用 于包装和制造业。
总结
烃的衍生物提供了广泛的应用领域,从日常生活到化学实验室,都有其重要地位。深入了解烃衍生物的种类和 应用,将帮助我们更好地理解有机化学领域的奥秘。
高二化学烃的衍生物课件
欢迎来到本次课件,我们将探索烃及其衍生物的世界!从基本概念到日常应 用,带您一起探索不一样的化学领域。
烃的基本概念
烃是由碳和氢元素组成的有机化合物。它们以碳-碳键为主要结构,并分为饱和和不饱和烃两种类型。
衍生物的定义
烃的衍生物是通过将其他元素或基团与烃分子中的一个或多个氢原子替换而 形成的新化合物。
2 燃料和能源
烃衍生物如汽油和天然气 被广泛用作燃料和能源来 源。
3 化妆品和个人护理产
品
许多化妆品和个人护理产 品,如香水和洗发水,都 使用了烃衍生物。
化学实验室中的烃衍生物应用
1பைடு நூலகம்
溶剂
某些烃衍生物可用作溶剂,在化学实验
反应活性
2
室中起到重要作用。
烃衍生物是许多有机合成和催化反应的
重要反应活性体。
烃的衍生物种类
饱和烃的衍生物
通过取代烷烃中的一个或多个氢原子,形成如卤代烷和醇等衍生物。
不饱和烃的衍生物
通过替换烯烃或炔烃中的氢原子,形成如醛、酮和酯等衍生物。
环烷烃的衍生物
通过在环烷烃分子上引入不同的基团,形成如芳香化合物等衍生物。
2013高考总复习化学:第九章第1节

栏目 导引
第九章
重要的有机化合物
思考感悟 3.你能区分分馏、蒸馏、干馏三个概念吗? 【提示】 分馏和蒸馏都属于物理变化,而干
馏是化学变化。分馏和蒸馏的区别在于分馏是 运用蒸馏原理,将多组分混合物通过控制不同 的沸点范围,使它们逐步分开的方法。
栏目 导引
第九章
重要的有机化合物
考点串讲深度剖析
几种典型烃的比较及烃 燃烧的规律
教材高频考点
例1
下列对有机物结构或性质的描 )
述,错误的是(
A.一定条件下,Cl2可在甲苯的苯环或 侧链要的有机化合物
B.苯酚钠溶液中通入CO2 生成苯酚, 则碳酸的酸性比苯酚弱 C.乙烷和丙烯的物质的量共1 mol,完 全燃烧生成3 mol H2O D.光照下2,2二甲基丙烷与Br2 反应, 其一溴取代物只有一种
)
栏目 导引
第九章
重要的有机化合物
A.①② C.①③
B.③④ D.②④
栏目 导引
第九章
重要的有机化合物
【解析】
抓住“取代反应”的关键
点:(1)有机物分子中的一个原子或原 子团被另一物质中的原子或原子团所 代替的反应; (2)反应物两种,产物一定是两种化合 物。显然③④属于取代反应。
栏目 导引
第九章
第九章
重要的有机化合物
易错易误剖析
例3
下列各组有机物的结构表达式中 )
互为同分异构体的是(
栏目 导引
第九章
重要的有机化合物
栏目 导引
第九章
重要的有机化合物
栏目 导引
第九章
重要的有机化合物
【常见错误】 【错因分析】
A或D (1)常见错误分析
本题极易误选A和D,选项A中的苯环用凯库 勒式表示,易误认为是一种单双键交替的结 构,但我们应明确苯分子中不存在单双键交 替的结构,而是一种特殊的化学键,因此A 中两种结构简式表示的是同一种物质。
第九章_氧化反应-课件

R CO2Et
69%~98%
CH2OH
O CH
RO OO
O
Ph
O
RO OO
IBX, DMSO, r.t.
O
Ph
O
NH2 O
NHAC
NH2 O
NHAC
AcO
OAc OAc
AcO
OAc OAc
BF4-
NO Re PPh3 R
R HO
IBX, DMSO, 20 oC, 3-4h
BF4NO Re PPh3 R
O OH OH
Ag2CO3, 硅藻土
O
HO O
80%
(4)亚硝酸钠-醋酸酐氧化法
2000年,Babasaheb P B等发现NaNO2-Ac2O新氧化体系 在无溶剂和温和条件下能够对各种伯醇、苄醇、烯丙醇进行快 速和选择性氧化,得到相应的醛类化合物,产率60~97%。
RC 2O HHN 25a℃ 2 N -,<A 1m O 2O iC n
9.1 醇羟基和酚羟基的氧化反应
9. 1. 1 醇羟基的氧化反应
醇羟基氧化方法很多,本节只介绍一些具有选择性的实用 氧化方法。
①.氧化剂直接氧化法
(1)三氧化铬—吡啶络合物氧化法
将三氧化铬加入吡啶中可以得到该络合物,性质温和、 易吸湿。制备时不能将吡啶加到三氧化铬上,易着火。
2
N+ Cr3O
(
_ O
8 0 %
C3H
C3H
HO
Al(OC4H9-n)3 C3H CO3CH
O
机理:烷氧基铝使醇成为醇铝,醇铝再与过量丙酮作用,通过 形成环状过渡态被氧化。
◆ 四醋酸铅Pb(OAc)4氧化法:用四醋酸铅在吡啶溶液中能将 伯醇、仲醇和烯丙醇氧化为相应的羰基化合物。
2024秋季人教版高一化学必修第二册第七章有机化合物《第二节乙烯与有机高分子材料:乙烯》

教学设计:2024秋季人教版高一化学必修第二册第七章有机化合物《第二节乙烯与有机高分子材料:乙烯》一、教学目标(核心素养)1.知识与技能:学生能够掌握乙烯的分子结构、物理性质及主要化学性质(加成反应、氧化反应);理解乙烯作为重要化工原料在工业生产中的应用;初步认识乙烯与有机高分子材料的关系。
2.过程与方法:通过实验观察、小组讨论、案例分析等方法,培养学生观察分析、逻辑推理和解决问题的能力;引导学生运用结构决定性质的观点,探究乙烯的性质。
3.情感态度与价值观:激发学生对化学的兴趣,培养科学探究精神;增强学生对化学与日常生活、工业生产联系的认识,树立可持续发展的观念。
二、教学重点与难点•教学重点:乙烯的分子结构、主要化学性质(加成反应)及其在工业上的重要应用。
•教学难点:理解乙烯加成反应的实质,能够将乙烯的性质与其结构联系起来进行解释。
三、教学资源•教材及配套实验手册•乙烯分子模型、多媒体教学课件•实验器材:乙烯气体、溴水、高锰酸钾溶液、试管、酒精灯等•工业生产乙烯的视频资料四、教学方法•讲授法:介绍乙烯的基础知识。
•实验探究法:通过实验观察乙烯与溴水、高锰酸钾的反应,加深理解。
•小组讨论法:针对乙烯的性质及应用进行小组讨论,促进思维碰撞。
•案例分析法:分析乙烯在工业上的应用案例,增强理论联系实际的能力。
五、教学过程1. 导入新课•情境导入:播放一段关于塑料、聚乙烯纤维等高分子材料在日常生活中广泛应用的视频,引导学生思考这些材料是如何制得的,引出乙烯这一重要原料。
•设疑激趣:提问:“乙烯是如何从石油等化石燃料中获得的?它有哪些独特的性质使得它成为有机高分子材料的基础?”2. 新课教学•乙烯的分子结构与物理性质•展示乙烯分子模型,讲解其分子结构特点(含碳碳双键)。
•介绍乙烯的物理性质,如无色气体、难溶于水、密度略小于空气等。
•乙烯的化学性质•加成反应:•演示实验:乙烯通入溴水中,观察溴水褪色现象,引导学生分析原因。
2014年高考一轮化学(人教版):第9章 有机化合物 第1节

基础知识回扣
热点考向聚焦
归纳总结探究
巩固提升训练
活 页 作 业
(2)取代反应
①硝化反应:苯在浓硫酸作用下,在 50~60℃ 还 可 以 与
浓硝酸发生取代反应,反应的化学方程式为: 。 ②卤代反应:苯与液溴在溴化铁作催化剂的条件下生成的
溴苯是 无 色 液 体,密度比水 大 ,反应的化学方程式为:
。
新课标高考总复习· 化学(配RJ版)
碱及强氧化剂反应,但在一定条件下可燃烧,可发生取代反应 和分解反应。 ①烷烃(CnH2n+2)的燃烧通式为: 3n+1 点燃 CnH2n+2+ O2――→nCO2+(n+1)H2O 。 2 ②乙烷与Cl2发生取代反应生成一氯代物的化学方程式为:
光照 CH3CH3+Cl2――→CH3CH2Cl+HCl 。
基础知识回扣
热点考向聚焦
归纳总结探究
巩固提升训练
活 页 作 业
(3)加成反应
苯在 Ni 作催化剂的条件下,可以与氢气发生加成反应,反应的化学方程式为 Nhomakorabea。
新课标高考总复习· 化学(配RJ版)
基础知识回扣
热点考向聚焦
归纳总结探究
巩固提升训练
活 页 作 业
三、烷烃的组成、结构与性质 3.(1)分子组成相差 n个CH2原子团的两种有机物一定是同系 物吗? (2)制备CH3CH2Cl用乙烷与Cl2取代可以吗? [提示](1)同系物首先要结构相似,组成上相差 n个 CH2原子
(2)烷烃分子中碳原子在一条直线上吗? (3)苯分子中是碳碳单键与双键交替出现吗?
新课标高考总复习· 化学(配RJ版)
基础知识回扣
热点考向聚焦
归纳总结探究
巩固提升训练
活 页 作 业
亚洲乙烯及衍生物生产商纷纷削减产量

总部位 于美 国休斯敦 的咨 询公 司 T w sn o me o nedPl r y
Sri s I o t n的最新研 究报 告显 示 , ev e & n r i c f mao 受新兴 市场 特别是中国市场需求强劲增长的刺激 , 未来 3年全球塑料 添加 剂市场需求有 望以年均 4 5 . %的速度 快速增长 。这
B PD O 、B ) B 、 n P D P 用于玩具和儿童护理品。因为研究 已表
是市场需求疲软 以及装置检 修。台湾东 联化学公 司 自今
年 7月份起已将位于台湾林园的一套 2 0k/ 5 ta的 E G装兰 的开工率削减至低 于 5 % , 0 主要原 因是赢 利低下 和市场
需求疲软 。中国石 化上海 石化分公 司旗下一 套 4 0k a 5 t / 的聚乙烯 ( E 装置在 整个 1 P) 0月份将维持 6 % 的低开工 0 率水平 。此外公司的一套 2 0k aE 3 t G装 置因赢利疲软而 /
d i 20 al 0 8一O y. 9—2 5
来已同意与色母料生产商沙特 At sa聚合物公 司组建合 资 r
中国引领全球塑料添加剂市场需求快速增长
公司向中东地 区的树脂生产商出售客户特定的抗氧化剂产 品。该公司计划在 20 09年底前开始向客户供应产品 。
近来全球 塑料添加剂工业 主要的投资包括 雅宝公 司
中心位 于韩 国丽水 的 3套裂解装 置的开工率将从 当前 的
精
5 8
细
油
化
工
进
展
第 9卷第 l 0期
ADVA E N F N E OC MI L NC S I I E P TR HE CA S
乙二醇是化学工业重要的中间体。例如 , 在塑料工 业 中, 它为生产聚酯纤维和树脂所需 ; 在汽车:业 中, 亡 它可用
【创新设计】(江西版)2015届高考化学总复习 第九章 重要的烃 煤 石油和天然气的综合应用课件第1课时

是溴水。但鉴别甲烷和乙烯时两者均可。
2.证明苯分子中不存在单双键交替排列的事实? _________________________________________________
_________________________________________________
答案 ①苯中碳碳键完全相同,为平面正六边形结构。
【示例2】 (2013· 新课标Ⅱ,8)下列叙述中,错误的是 B.苯乙烯在合适条件下催化加氢可生成乙基环己烷
(
)。
A.苯与浓硝酸、浓硫酸共热并保持55~60 ℃反应生成硝基苯
C.乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 解析 苯与浓硝酸、浓硫酸在55~60 ℃反应生成硝基苯,A正 确;苯乙烯催化加氢可生成乙基环己烷,B正确;乙烯与溴的 四氯化碳溶液发生加成反应,生成1,2-二溴乙烷,C正确; 甲苯与氯气在光照下主要发生侧链上的取代反应,生成
同的化合物不一定是同分异构体。
②同分异构体的最简式相同。但最简式相同的化合物不 一定是同分异构体,如C2H4与C3H6(环丙烷)。 ③结构不同,即分子中原子的连接方式不同。同分异构 体可以是同一类物质,也可以是不同类物质。
(3)类型
探究思考 1.如图所示是几种烷烃的球棍模型,试回答下列问题:
(1)A、B、C三者的关系是________。
Hale Waihona Puke 【示例4】 (2012· 海南化学,5)分子式为C10H14的单取代芳烃, 其可能的结构有 A.2种 解析 B.3种 C.4种 D.5种 ( )。
单取代芳烃即苯环上只有一个取代基。根据分子式
C10H14可确定其连接方式为C6H5—C4H9,—C4H9(丁基)有四 种结构:CH3CH2CH2CH2—、CH3CH(CH3)CH2—、 CH3CH2CH(CH3)—、C(CH3)3—,所以选C。
乙烯及衍生物工业全貌

乙烯及衍生物工业全貌
乙烯是世界上产量最大的化学产品之一,乙烯产品占石化产品的70%以上,是石油化工产业的核心,乙烯工业在国民经济中占有重要地位,其生产规模和水平已经成为衡量一个国家石油化工发展水平的重要标准之一。
乙烯是以石油加工过程中产生的石脑油、轻质柴油、加氢裂化尾油作为原料,经裂解、分离而制取的。
由于乙烯具有能自己聚合能与其他物质结合的特性,通过乙烯的聚合、氧化、卤化(包括氧氯化)、烷基化、水合、羰基化、齐聚等系列反应,可以获得大量多种极其重要的化工原材料,因此乙烯有“石油化工之母”的美誉。
在现代工业中,乙烯主要用于发展当代“三大合成”材料,即合成纤维、合成树脂、合成橡胶。
合成纤维如腈纶、涤纶、绵纶等是纺织工业的原料;合成树脂是塑料工业的原料;合成橡胶是橡胶制品工业的原料,因此乙烯及其下游衍生物或制品对整个国民经济的发展起着至关重要的作用。
为便于朋友们充分了解乙烯及其衍生物家族,《石油石化行业资讯》特绘制了乙烯工业及其衍生物的家族谱图,供大家参阅。
乙烯及衍生物的生产与管理

河北化工医药职业技术学院毕业论文氨噻肟酸的合成工艺及发展前景姓名马亚洋学号1201130423专业应用化工技术班级应化1304班指导教师孙娜完成时间2016年1月10日化学与环境工程系摘要近年来,全世界的工业高速发展,其中大部分是基于石油烃的,石油烃最重要的中间体则是乙烯。
上世纪70年代美国、日本和西欧的乙烯总产量达11,000,000吨以上,这表明在十年里的增长率近4倍,在二十年里增长率达10倍以上。
大规模的乙烯生产也已经扩展到其他国家,这些国家1970年的乙烯总生产量至少1,500,000吨。
本文详细的讨论了乙烯的性质和用途、、乙烯生产工艺、乙烯的衍生物及生产方法等方面问题。
乙烯作为石油化工基础原料之一,乙烯的产量是衡量一个国家石油化工发展水平的重要标志。
中国乙烯工业经过三十多年的发展,已经具备一定的生产能力,积累了丰富的经验,培养了一批人才,并研究和开发了一批技术成果。
关键词;石油烃乙烯合成方法发展趋势目录第一章绪论第二章乙烯的性质及用途 (1)第一节乙烯 (1)第二节乙烯的性质 (5)第三节乙烯的用途 (6)第三章乙烯的生产方法第一节焦炉气制乙烯 (9)第二节蒸汽裂解法 (10)第三节石油烃高温裂解法 (11)第四节乙醇催化脱水法 (13)第四章乙烯三废处理技术第一节废水处理技术第二节废气处理技术第三节废物处理技术第五章乙烯相关产品情况第一节乙烯及其下游产品的开发和生产情况第二节乙烯及其衍生物第三节与乙烯相似的化工产品第六章乙烯及其衍生物的发展第一节乙烯的市场情况第二节国内外乙烯的发展情况第三节乙烯的发展进展第四节存在的问题及建议参考文献 (37)致谢..................................................... .38第一章绪论第一节乙烯的历史发展17世纪中叶比歇尔首先观察到了加热酒精和浓硫酸的混合物生成一种可燃气体这一事实。
在他1667年首次出版的《地下物理学》一书中就指的是此种气体或所生成的。
高二化学烃的衍生物知识总结
例3、 某同学做银镜实验反应时, 在一洁净的试管中加入2mL 2%的 稀氨水,然后边摇动边逐滴加入几 滴2%的AgNO3溶液,然后再加入 几滴乙醛,在水浴中加热,试管内 壁无光亮的银镜出现,其失败的原 因是什么?
例4、 A和B两种物质的分子式都是 C7H8O,它们都能跟金属反应放出氢气。 A不溶于NaOH溶液,而B能溶于NaOH 溶液。B能使适量溴水褪色,并产生白色 沉淀,A不能。B的一溴代物有两种结构。 写出A和B的结构简式和名称。
例1. 阿司匹林的结构简式为: CH3-C-O- -C-OH
O A. 水解反应
C. 加成反应
O
)
它不可能发生的反应是 (
B. 酯化反应
D. 消去反应
A、B、C、D、E是中学化学中常见的有机物, 他们之间的反应关系如下图所示(图中部分反应 条件和无机物已经略去):
A
B +C
浓硫酸,加热
C D NaOH溶液
烃的衍生物知识总结
烃的衍生物
卤代烃 通式 代表物 醇类 通式 代表物 醛类 羧酸 酯(油脂) 酚
通式
代表物
通式
代表物
通式
代表物
通式
代表物
烃的衍生物知识总结
烃的衍生物
卤代烃 醇类为CnH2n+1X
卤代 烃
代表物
CH3CH2B r
化性:①强碱溶液中发生水解生成醇(取代反 应) ②在强碱的醇溶液里发生消去反应生成 乙烯 制法:①乙烯加HBr ② CH3—CH3取代 ③C2H5OH、NaBr、H2SO4混合加热
狼马他们.九天寒龟道:"他们还需要呆在这里十年,你们先行出去锻炼吧,不过闪电鸟小强倒是可以跟着你们走,这里面装了大量の火龙果,是老夫培育出来の,你们用它喂小强就行了."
第九章 氧化反应

(5)有机五价碘氧化剂 ◆ 1-羟基碘酰苯(简称IBX)及其衍生物—高价碘化物作为一
种性能温和、选择性高及环境友好的醇氧化剂在有机合成中得 到了广泛的应用。
◆其显著特点是对底物的化学选择性极高,即一般仅氧化醇羟 基为羰基,而不会氧化其它易被氧化的官能团如氨基、巯基等, 所以它在合成一些药物和天然产物方面具有独特的优势。
86
85 82 92 85 90
*TNCB用硝酸铈铵和溴酸钠作用得到。
◆ Fe(NO3)3-FeBr3氧化体系:催化空气氧化仲醇、苄醇得到相应 的羰基化合物(乙腈,25℃;不氧化伯醇)。
OH OOH ຫໍສະໝຸດ HO OH 74%78%
CH2OH
CHO
OH
O
80%
OH O
80%
NH2 85%
NH2
NBS aq, 二噁烷
H3C OH H3C
Ag2CO3 C6H6
H3C O H3C
H3C
CH 3 OH
H3C
CH 3 OH
H3C H3C
OH H3C
H3C
Ag2CO3 CH3COCH3
OH
HO
O
反应活性:苄醇(烯丙醇)>仲醇>伯醇;高位阻羟基难氧化。
◆碳酸银可以将二元醇(1,4-丁二醇、1,5-戊二醇、1,6-己二 醇)中的一个羟基氧化成羧酸,进而转变为相应的内酯,这是 其他方法不易得到的。
9. 1. 2 酚羟基的氧化反应
◆ 酚环对单电子氧化剂非常敏感,去掉一个质子后给出离域 的芳基氧自由基。
OH
H+
O
O
O
O
◆ 例如,2-萘酚在碱性条件下用K3Fe(CN)6氧化得到联二萘酚。
OH
第九章共轭烯键的化学
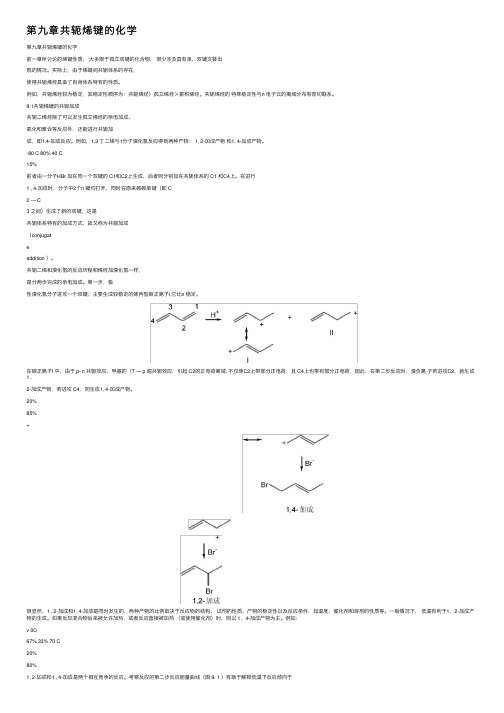
第九章共轭烯键的化学第九章共轭烯键的化学前⼀章所讨论的烯键性质,⼤多限于孤⽴双键的化合物,很少涉及具有单、双键交替出现的情况。
实际上,由于烯键间共轭体系的存在,使得共轭烯烃具备了⾃⾝体系特有的性质。
例如,共轭烯烃较为稳定,其稳定性顺序为:共轭烯烃〉孤⽴烯烃>累积烯烃。
共轭烯烃的特殊稳定性与n 电⼦云的离域分布有密切联系。
9.1共轭烯键的共轭加成共轭⼆烯烃除了可以发⽣孤⽴烯烃的亲电加成、氧化和聚合等反应外,还能进⾏共轭加成,即1,4-加成反应。
例如,1,3 丁⼆烯与1分⼦溴化氢反应得到两种产物: 1, 2-加成产物和1, 4-加成产物。
-80 C 80% 40 C15%前者由⼀分⼦HBr 加在同⼀个双键的 C1和C2上⽣成,后者则分别加在共轭体系的 C1 和C4上。
在进⾏1 , 4-加成时,分⼦中2个n 键均打开,同时在原来碳碳单键(即 C2 — C3 之间)⽣成了新的双键,这是共轭体系特有的加成⽅式,故⼜称为共轭加成(conjugateaddition )。
共轭⼆烯和溴化氢的反应历程和烯烃加溴化氢⼀样,是分两步完成的亲电加成。
第⼀步,极性溴化氢分⼦进攻⼀个双键,主要⽣成较稳定的烯丙型碳正离⼦I,它⽐n 稳定。
在碳正离⼦I 中,由于 p- n 共轭效应、甲基的(T — p 超共轭效应,引起 C2的正电荷离域, 不仅使C2上带部分正电荷,且 C4上也带有部分正电荷,因此,在第⼆步反应时,溴负离⼦若进攻C2,就⽣成1 ,2-加成产物,若进攻 C4,则⽣成1, 4-加成产物。
20%85%+很显然,1 , 2-加成和1, 4-加成是同时发⽣的,两种产物的⽐例取决于反应物的结构、试剂的性质、产物的稳定性以及反应条件,如温度、催化剂和溶剂的性质等。
⼀般情况下,低温有利于1,2-加成产物的⽣成。
如果反应混合物后来被允许加热,或者反应直接被加热(或使⽤催化剂)时,则以 1,4-加成产物为主。
例如:v 0C67% 33% 70 C20%80%1, 2-加成和1 , 4-加成是两个相互竞争的反应。
烃 的 衍 生 物知识要点

高二化学烃的衍生物(乙烯烯烃)教材:全日制普通高级中学教科书必修加选修人民教育出版社第三节乙烯烯烃江宁高级中学化学组马明祥教学目标:知识目标:1、了解乙烯的结构、通式和物理性质2、掌握乙烯的实验室制取方法3、了解乙烯的物理性质4、掌握乙烯的重要化学性质5、了解乙烯的重要用途能力目标:培养学生的分析推理能力、知识迁移和应用的能力科学思想和方法:培养科学的探索精神,养成严谨的科学品质教学重点难点:乙烯的实验室制取方法乙烯的结构乙烯的加成反应教学构想:新知识的教学是建立对旧知识的掌握基础上进行的,新旧知识间的这种联系如能够加以善用,则不但可以起到复习的作用,而且还能够将新知识的构建上升为一种对知识的整合,从而将知识进行一些恰当的串联,以利于学生形成知识体系。
发现式的探究可以帮助学生更好地认识事物。
本节课中,乙烷的结构、烃基、原子核外电子排布等的知识是学生已经掌握的知识点。
那么从乙烷入手,构建乙烯的结构也就将成为一种可以尝试的方法,实际上,这种方法在一些习题的解法中也是非常有用的。
同样,关于气体的实验室制取方法,在以往的教学中已经学过了氢气、氧气、二氧化碳、氨气、氯气等,并且也对这些气体的实验室制取方法进行过总结和归纳。
从这一角度来说,乙烯的实验室制取方法不算是一个新的知识点。
但是,乙烯的实验室制取方法相对于上述即使是相似的方法也存在着极大的差异,而这些差异也正是导致在乙烯的实验室制取方法中要采取一些特殊措施的重要原因。
从这些问题的分析与阐述中,学生也可以学到一些正确分析问题的方法,学到一些如何解决实际问题的能力。
本节的重点在于乙烯的结构、乙烯的实验室制取方法和乙烯的加成反应,拟采用讨论探究的方法开展教学活动,通过预设的一些大的方向性问题的学生间的互助式学习,让学生在探究与讨论中逐步形成对上述问题的正确认识,培养学生的分析推理能力、知识迁移和应用的能力和科学的探索精神,培养严谨的科学品质。
教学方式:问题探究、小组讨论、实验演示教学器材:球棍模型、比例模型、乙烯制备及性质实验的仪器一套教学设计:展示球棍模型引入: 乙烷的结构模型乙烯的结构模型乙烷 乙烯思考与讨论1、根据上述结构模型写出乙烯的电子式、结构式、结构简式、分子式。
《基础化学》第9章 羧酸及羧酸衍生物---课程思政

《基础化学》
第九章 羧酸及衍生物
一、羧酸衍生物的结构和命名 1. 羧酸衍生物的结构
O RC L
L: 卤原子(X), O 酰氧基( OCR),
烷氧基(-OR),
酰卤 酸酐 酯
氨基(-NH2, -NHR, -NR2)
酰胺
《基础化学》
第九章 羧酸及衍生物
O
RC X
酰卤
OO
R C 酸O酐பைடு நூலகம் R
RCH2COOH + Br2
PBr3 -HBr
RCHCOOH Br
思政元素
(1)培养刻苦钻研的学习态度 (2)树立正确的人生观和世界观
《基础化学》
第九章 羧酸及衍生物
3、 羧 基上羟基的取代反 应
取代羟基生成羧酸衍生物
O R C OH
羧酸
O RC X
O
O
R C O CR
O R C OR'
O R C NH2(R)
《基础化学》
第九章 羧酸及衍生物
通过羧酸钠盐脱羧
O R C OH
(1) NaOH
(2)
R H + CO2 产率一般较低
其他直链羧酸盐与碱石灰热熔的产物复杂,无制备意义。
CH3CH2COONa + NaOH(CaO)
热熔 CH3CH2CH3 + CH4 + 烯及混合物
17%
20%
《基础化学》
第九章 羧酸及衍生物
《基础化学》
第九章 羧酸及衍生物
2. 还原反应
(1) 用氢化铝锂还原
O
C15H31CCl
①LiAlH4, Et2O ② H2O,98%
第九章助剂

第九章助剂橡塑助剂橡塑助剂是指在橡胶、塑料成型加工进程中能改善加工工艺或增进产品品质并组成产品组分的辅助化学品。
按功能分类:抗老化作用的稳固化助剂:抗氧剂、光稳固剂、热稳固剂、防霉剂改善机械性能的助剂:硫化剂、硫化增进剂、填充剂、偶联剂改善加工性能的助剂:润滑剂和脱膜剂柔软化和轻质化的助剂:增塑剂和发泡剂改良表面性能和外观的助剂:抗静电剂、防雾滴剂、着色剂阻燃添加剂:阻燃剂、抑烟剂9.1.1 增塑剂一、概念增塑剂是能使聚合物增加塑性、变软并降低脆性的物质。
举例PVC二、增塑机理增塑剂的作用机理是当增塑剂添加到聚合物中,或增塑剂分子插入到聚合物分子链之间,减弱了聚合物分子链间的引力,结果增加了聚合物分子链的移动性,降低了聚合物分子链的结晶度,从而使聚合物的塑性增加。
聚合物的结晶度:是指空间有规结构的聚合物分子链在适当的条件下,一部份高分子链能够从卷绕杂乱的状态变成紧密折叠成行的有规那么排列状态。
聚合物分子链的排列是由结晶区分散于无定形区的,而增塑剂分子插入结晶区要比插入无定型区困难的多。
若是增塑剂的分子既能插入聚合物的无定型区同时又能插入结晶区域,那么此增塑剂即是溶剂型增塑剂,即所谓主增塑剂。
若是增塑剂的分子仅能插入部份结晶的聚合物的无定型区域,那么此溶剂即是非溶剂型增塑剂,即助增塑剂。
举例:邻苯二甲酸二丁酯(DBP)塑化聚氯乙稀当温度升高时,PVC分子链间的距离由于热运动而增大,DBP插入到PVC的分子链间,DBP的酯型偶极与PVC的偶极(因为含氯原子)彼此作用而使DBP 的苯环极化,如此DBP与PVC就结合在一路。
由于DBP非极性部份的亚甲基链不极化,它夹在PVC的分子链间,减弱了PVC分子间力,使PVC分子链的移动容易了。
由此可见,一样增塑剂分子内部必需含有能与极性聚合物彼此作用的极性部份和不与聚合物作用的非极性部份。
三、增塑剂的化学结构与增塑的关系一、增塑剂与聚合物化学结构上的类似性二者结构类似,增塑成效就越好。
乙烯基摩尔质量

乙烯基摩尔质量
乙烯基的摩尔质量为28.05 g/mol。
一、什么是乙烯基?
乙烯基是一种有机化合物,化学式为C2H3,由一个碳原子和一个双键连接的氢原子组成。
乙烯基是乙烯的衍生物,也被称为乙烯的基团。
二、乙烯基的摩尔质量如何计算?
计算乙烯基的摩尔质量需要先计算出其分子量。
乙烯基的分子量计算公式如下:
分子量= 每个原子的相对原子质量之和
C2H3 的分子量= 2 ×相对原子质量(碳)+ 3 ×相对原子质量(氢)
根据化学元素周期表,相对原子质量(碳)为12.01,相对原子质量(氢)为1.01,则:
C2H3 的分子量= 2 × 12.01 + 3 × 1.01 = 28.05 g/mol
因此,乙烯基的摩尔质量为28.05 g/mol。
三、乙烯基在化学中的应用
乙烯基在化学中具有广泛的应用。
它是许多有机化合物和高分子材料的重要的基础结构单元。
乙烯基可以通过不同反应制备出丙烯酸乙烯酯、乙烯基乙烯酸甲酯和聚乙烯等化合物。
此外,乙烯基也可以用来制备其他有机化合物,如硬脂酸乙烯酯、聚酰胺等。
在工业生产中,乙烯基可以作为隧道工业中的表面处理剂和增塑剂。
【结语】
乙烯基是一种重要的有机化合物,具有广泛的应用。
通过简单的计算,我们可以得到乙烯基的摩尔质量是28.05 g/mol。
在化学研究和工业生产中,乙烯基扮演着重要的角色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
反应机理
二氯乙烷生成
二氯乙烷裂解原理
二氯乙烷裂解工艺条件
反应温度控制在500~550度
二氯乙烷裂解是吸热反应 太低,转化率很低 太高,深度裂解、聚合等副反应加剧
反应压力控制在0.6~1.5MPa
分子数增大的反应 压力太大,容易生炭
停留时间
10s 太长,转化率提高,副反应增加
催化剂碘化钴,250度,60~70MPa
1960s,美国孟山都公司开发新合成工艺
采用Rh催化剂,175度,3MPa
甲醇羰基化法
Celanese公司开发了其专有的AO Plus工艺,通过添加高浓度 的无机碘化物(主要是碘化锂),来增加铑催化剂的稳定性
1996年BP公司声称开发出一种名为“Cati—va”工艺的铱基改 进催化剂,并已安装在先前的基于铑的装置上。Cativa工艺以 金属铱为主催化剂,加入了一部分铼、钌和锇等作为助催化剂, 反应在190℃和2.8MPa下进行,反应速率和产品选择性均较 高 日本千代田公司开发了一种称为“Acetica”的甲醇羰化法醋酸 生产工艺。该工艺采用(铑基)负载型非均相催化剂体系和泡罩 塔反应器。Acetica工艺于1999年通过中试验证,现已与我国 贵州水品有机化学集团公司签订了36kt/a醋酸装置首次工业 化应用的转让合同
乙烯及其衍生物
乙烯
乙烯
乙烯的制备与利用
最早,乙醇脱水 石油烃裂解制乙烯
裂解气 催化裂化 热裂化 C2馏分 8-12% 焦炉气 3%
乙烯是国民经济的基 础原料,有石油化工 原料之母的美称。目 前约有75%的石油化 工产品由乙烯生产, 乙烯产量已成为衡量 一个国家石油化工工 业发展水平的标志
C2H3Cl 常温常压下,无色有乙醚香味的气体 易自燃 对人体有毒 双键加成和聚合 光作用下也容易发生聚合 聚氯乙烯是目前塑料最大的品种之一
氯乙烯合成方法
乙炔法合成氯乙烯
催化剂:活性炭负载的HgCl2 能耗大,催化剂有毒,被取代
乙烯法
也称二氯乙烷法
以石油乙烯为原料经氯化制得中间产物二氯乙烷,然后 二氯乙烷裂解脱氯化氢而获得氯乙烯
乙烯氧化
乙烯部分氧化,生产环氧乙烷
主要用途生产乙二醇 其他用途
生产表面活性剂 医药中间体 油品添加剂 抗氧化剂 农药乳剂 杀虫剂
环氧乙烷
乙烯直接氧化制环氧乙烷
乙烯氧化法制环氧乙烷
环氧乙烷的储存
环氧乙烷容易自聚,特别在铁、酸、碱、醛 等杂质存在和高温条件下更容易自聚 自聚时放出热量,引起温度上升,压力增大, 甚至引起爆炸
氧化:醋酸 氢氰酸反应,可得丙烯腈 醇醛缩合:正丁醇等
工业生产方法
乙炔水合法
催化剂:HgSO4 1916年工业化,技术成熟,产品纯度高 催化剂有毒,耗能,被取代
乙醇制乙醛
吸热脱氢
催化剂:金属铜 操作温度:260~290 度,副产氢
放热氧化脱氢
催化剂:金属银 550度下反应,容易深度氧化
直接水合法
C2H4 H2O CH3CH2OH
固体酸
H3PO4/SiO2催化剂 295度,7MPa
作业
为什么乙烯产量是衡量国家石油化工发展水 平的标志?
C3/C4烷烃氧化制乙醛
丙烷/丁烷混合物气相氧化制乙醛 1943年在美国工业化 425度,1MPa下反应 产物分离困难
乙烯直接氧化法
又称瓦克法,是HESS(赫斯)公司开发 原料便宜,成本低,副反应少,收率高 全世界广泛使用
乙烯液相氧化法生产乙醛
反应原理
催化剂:氯化钯、氯化铜的盐酸水溶液 三步
储存必须清洁,而且保持0度以下
乙二醇
环氧乙烷水合法制乙二醇
主要副反应为乙二醇继续与环氧乙烷反应生 成一缩乙二醇,二缩乙二醇,多缩乙二醇 酸催化剂作用下,常压,50~70度下进行 没有催化剂作用下,2~3MPa,140~230 度下进行
环氧乙烷合成乙二醇工艺流程
氯乙烯
氯乙烯
催化剂:含Co、Mn等金属的醋酸盐或环烷酸盐 15~225度 4~8MPa
乙烯直接氧化法
日本昭和电工公司于1997年开发成功的工艺技术,在日本千叶建 成的首套产能为100kt/a的工业装置
该工艺采用负载钯的催化剂,由乙烯不经乙醛直接氧化为醋酸, 反应在固定床反应器内进行,反应温度约150-160℃,压力约 0.9MPa,乙烯单程转化率为7.4%,醋酸、乙醛和二氧化碳的选 择性分别为86.4%、8.1%和5.1% 日本昭和电工公司采用自主开发的乙烯直接氧化工艺生产醋酸, 计划用新型高效催化剂配备现有装置,从而使产能增加30%,在 2006年的上半年定期维修期间将其大部分醋酸产能提高30kt/a, 达到130kt/a,同时醋酸乙烯产能提高55kt/a,达到175kt/a。 该公司还计划在亚洲建醋酸乙酯生产中心,从而成为亚洲最大的 乙酰基产品生产商。
乙醛液相氧化法
乙醛氧化制醋酸属于催化自氧化范畴,是一 强放热反应 CH3CHO +1/2O2——CH3COOH 中间产物为CH3COOOH
催化剂存在下,分解速度加快
催化剂是可变价的Mn,Co,Ni等金属的醋 酸盐,醋酸锰最好
乙烷直接氧化法
SABIC公司开发的乙烷催化气相氧化制醋酸新工艺, 已于2005年第二季度在沙特Yanbu地区的一套34kt /a醋酸新装置上首次工业应用。 基于乙烷氧化路线的该技术具有以下优点:(1)符合 环保和安全标准;(2)竞争能力得到增强;(3)醋酸产 品质量得到改善;(4)生产成本降低。SABIC公司完 全拥有该技术的专利权,并有权将该技术用于生产并 可向第三方颁发许可证。 在乙烷制乙烯或醋酸过程中,人们认为乙烷先在催化 剂表面生成一种乙氧化物中间体,乙氧化物中间体进 一步被氧化生成表面醋酸盐,最后表面醋酸盐与水进 行水解反应生成醋酸。
纯醋空气中爆炸 醋酸蒸汽对眼睛粘膜有刺激作用
醋酸的用途
最重要的有机合成中间体之一 醋酸乙烯酯是制造合成纤维维尼纶的主要原 料 醋酸纤维素是合成人造纤维、塑料和电影胶 片的原料 用途广泛
工业生产方法
丁烷或轻馏分油氧化法
甲醇羰基化法
甲醇羰基合成法是目前最主要的醋酸生产方 法,其中较为典型的工艺有Monsanto/BP 和Hal—con/Eatsman两种。近年来又出 现了三种新工艺,即Celanese的“AOPlus” 工艺、BP的“Cativa”工艺以及千代田的 “Acetica”工艺。
1930年BASF建成第一套装置
平衡氧氯化法制氯乙烯
催化剂:CuCl2/Al2O3,5%Cu 反应温度:220~230度 压力:<10MPa 反应原理
平衡氧氯化法制氯乙烯的组合工艺过程
乙醛
乙醛的性质和用途
CH3CHO,常温下,无色透明液体,具有特殊气 味 溶于水 易燃,与空气爆炸 有毒 运输:聚合为三聚乙醛,再分解 很宝贵的有机合成中间体
1 C2H4 CH3COOH O2 Pd / Pd 合金 CH3COOCHCH2 H2O 2
循环气
乙醇
乙醇的性质和用途
CH3CH2OH 用作溶剂,合成醋酸 乙酯 工业生产方法
乙烯水合制乙醇 间接水合法,硫酸法
水解 乙烯+硫酸 烷基硫酸酯 水解 乙醇
醋酸乙烯
性质和用途
CH3COOCHCH2,醋酸乙烯酯 合成维尼纶
过氧化物 醋酸乙烯 聚合 聚醋酸乙烯 醇解 NaOH-CH3OH 聚乙烯醇
维尼纶
醋酸乙烯的生产方法
乙炔法
C2H2 CH3COOH 硫酸汞 / 硫酸锌 CH3COOCHCH2 H2
乙烯气相催化氧化法
工艺过程
一步法工艺,也称氧气法
125度,0.3MPa 加压精馏塔 催化剂再生
O2,盐酸 CuCl氧化为CuCl2
二步法制乙醛
也称空气法 105~110度,1.0~1.2MPa 反应器一
羰基化反应
反应器二
氯化亚铜的氧化反应
醋酸
醋酸的性质
乙酸,CH3COOH 特殊刺激性气味的无色液体 冰醋酸
