各种元素周期表PPT课件
合集下载
《元素性质的周期性变化规律》元素周期律PPT课件

(2)试从原子结构角度解释同周期元素性质存在周期性变化的原 因。 提示:核外电子层数相同,随着原子序数(核电荷数)的递增,原子 核对核外电子的引力逐渐增强,原子半径逐渐减小,元素原子的 得电子能力逐渐增强,失电子能力逐渐减弱,最终导致元素的非 金属性逐渐增强,金属性逐渐减弱。
【案例示范】 【典例】(2017·全国卷Ⅱ)a、b、c、d为原子序数依 次增大的短周期主族元素,a原子核外电子总数与b原子 次外层的电子数相同;c所在周期数与族数相同;d与a同 族,下列叙述正确的是 ( )
第二节 元素周期律 第1课时 元素性质的周期性变化规律
-.
一、原子结构的周期性变化
结合图1、图2、图3完成下表:
原子 电子 最外层 序数 层数 电子数
1~2 1
3~ 10
_2_
1~2
_1_~__8_
原子半径的 变化(稀有气 体元素除外)
—
由_大__到_小__
最高或最 低化合价 的变化
+1→0
变化。 核外电子排
2.实质:元素性质的周期性变化是原子的___________ 布 ___的周期性变化的必然结果。
知识点一 元素周期表中主族元素的周期性变化规律
【重点释疑】
项目
同周期(左→右)
原 核电荷数 逐渐增大 子 电子层数 相同 结 构 原子半径 逐渐减小
同主族(上→下) 逐渐增大 逐渐增多
③Al向(OAHl)(3O+H3)H3+沉=淀==中= 加Al入3++盐3H酸2O,发生反应的离子方程式: _________________________。
3.钠、镁、铝的最高价氧化物对应水化物的碱性
NaOH 分类 强碱 碱性强弱 结论
优秀课件——元素周期律(共45张PPT)

化学反应中不稳定结构总是通过各种方式(得失电子、
共用电子对)趋向达到稳定结构
(2)核外电子排布与元素性质的关系
质子数、电子层数 决定 元素的原子半径由________________
最外层电子数 决定 元素的化学性质主要由________________
最外层电子数 决定 元素的化合价主要由_________________ 金属元素的原子最外层电子数一般少于4,易失电子
N +5
-3
O
F
Ne 0
最低价
元素符号 最高价 Na +1 Mg +2 Al +3
-2
-1
Si +4
-4
P +5
-3
S +6
-2
Cl +7
-1
Ar 0
最低价
最高正价= 最外层电子数(F、O除外) 负价 = 最外层电子数-8
随着原子序数的递增
引起了
课堂总结
核外电子排布呈周期性变化 最外层电子数 1→8
• 【回顾】
• 1、碱金属元素的性质递变,其本质原因? • 2、卤素性质递变,其本质原因?
•【思考与交流】 元素的性质随着原子序数的递增而呈怎 样变化呢?
从今天开始,我们就通过来学习认清这些问题
一. 原子核外电子的排布
1. 电子层-表示运动着的电子离核远近及能量高低
含多个电子的原子中, 电子是分层排布的。能量较 低的电子运动在离核较近的 区域,能量较高的电子运动 在离核较远的区域。
深入探讨
原子半径受哪些因素制约?为什么随原子序数 的递增,原子半径出现从大到小的周期性变化?
①电子层数:电子层数越多,原子半径越大 最主要因素 影响原 子半径 大小的 因素 ②核电荷数: 核电荷数增多,使原子半径有减小的趋向
共用电子对)趋向达到稳定结构
(2)核外电子排布与元素性质的关系
质子数、电子层数 决定 元素的原子半径由________________
最外层电子数 决定 元素的化学性质主要由________________
最外层电子数 决定 元素的化合价主要由_________________ 金属元素的原子最外层电子数一般少于4,易失电子
N +5
-3
O
F
Ne 0
最低价
元素符号 最高价 Na +1 Mg +2 Al +3
-2
-1
Si +4
-4
P +5
-3
S +6
-2
Cl +7
-1
Ar 0
最低价
最高正价= 最外层电子数(F、O除外) 负价 = 最外层电子数-8
随着原子序数的递增
引起了
课堂总结
核外电子排布呈周期性变化 最外层电子数 1→8
• 【回顾】
• 1、碱金属元素的性质递变,其本质原因? • 2、卤素性质递变,其本质原因?
•【思考与交流】 元素的性质随着原子序数的递增而呈怎 样变化呢?
从今天开始,我们就通过来学习认清这些问题
一. 原子核外电子的排布
1. 电子层-表示运动着的电子离核远近及能量高低
含多个电子的原子中, 电子是分层排布的。能量较 低的电子运动在离核较近的 区域,能量较高的电子运动 在离核较远的区域。
深入探讨
原子半径受哪些因素制约?为什么随原子序数 的递增,原子半径出现从大到小的周期性变化?
①电子层数:电子层数越多,原子半径越大 最主要因素 影响原 子半径 大小的 因素 ②核电荷数: 核电荷数增多,使原子半径有减小的趋向
元素周期表优质课公开课一等奖课件省赛课获奖课件

+7 +6 +5 +4 +3 +2 +1
-1 H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar
-2 -3 -4
2、元素化合价与元素在周期表中位置的关系
①价电子:元素的最外层中的电子(主族元素) ②主族族序数=价电子数=最外层电子数=主族 元素的最高正价数
③最高正价+ |最低负价| =8
得电子能力依次增大 原子半径依次减小
原子半径依次增大 失电子能力依次增大
金属性依次增强
非金属性依次增强 得电子能力依次增大
原子半径依次减小
原子半径依次增大 失电子能力依次增大
金属性依次增强
课堂练习:
1、下列递变规律中对的的是( C ) A、Na、Mg、Al 的还原性依次增强 B、Cl、Br、I 的非金属性依次增强 C、Si、P、S、Cl 的最高价氧化物的水化物的酸性依次增强 D、C、N、O、F 的原子半径依次增大
思考:在同一周期、同一主族最高价氧化物的水化物的酸 碱性,气态氢化物的稳定性如何变化?
同一周期最高价氧化物对应的水化物的酸性依次增强, 碱性依次削弱。
同一主族最高价氧化物对应的水化物的酸性依次削弱, 碱性依次增强。
同一周期气态氢化物的稳定性依次增强, 同一主族气态氢化物的稳定性依次削弱。
元素化合价周期性递变图
周期数=最外电子层数
练习
推算原子序数为 13,34,53,88,82的元素在周期表中的位置。
原子 序数
核外电子排布
周 期 族序 数数
6 2,4 13 2,8,3 34 2,8,18,6
2 ⅣA 3 ⅢA
4 ⅥA
53 2,8,18,18,7
-1 H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar
-2 -3 -4
2、元素化合价与元素在周期表中位置的关系
①价电子:元素的最外层中的电子(主族元素) ②主族族序数=价电子数=最外层电子数=主族 元素的最高正价数
③最高正价+ |最低负价| =8
得电子能力依次增大 原子半径依次减小
原子半径依次增大 失电子能力依次增大
金属性依次增强
非金属性依次增强 得电子能力依次增大
原子半径依次减小
原子半径依次增大 失电子能力依次增大
金属性依次增强
课堂练习:
1、下列递变规律中对的的是( C ) A、Na、Mg、Al 的还原性依次增强 B、Cl、Br、I 的非金属性依次增强 C、Si、P、S、Cl 的最高价氧化物的水化物的酸性依次增强 D、C、N、O、F 的原子半径依次增大
思考:在同一周期、同一主族最高价氧化物的水化物的酸 碱性,气态氢化物的稳定性如何变化?
同一周期最高价氧化物对应的水化物的酸性依次增强, 碱性依次削弱。
同一主族最高价氧化物对应的水化物的酸性依次削弱, 碱性依次增强。
同一周期气态氢化物的稳定性依次增强, 同一主族气态氢化物的稳定性依次削弱。
元素化合价周期性递变图
周期数=最外电子层数
练习
推算原子序数为 13,34,53,88,82的元素在周期表中的位置。
原子 序数
核外电子排布
周 期 族序 数数
6 2,4 13 2,8,3 34 2,8,18,6
2 ⅣA 3 ⅢA
4 ⅥA
53 2,8,18,18,7
初中化学元素周期表 PPT课件 图文

返回
锂
元素名称锂 元素符号Li 原子序数3 相对原子质量(12C = 12.0000)6.941 英文名称Lithium 物理性质:状态:软的银白色金属,是最轻的金属。
返回
铍
元素名称铍
返回
元素符号Be
原子序数4
相对原子质量(12C = 12.0000)9.012182
返回
氯
元素名称氯 元素符号Cl 原子序数17 相对原子质量(12C = 12.0000) 35.4527 英文名称Chlorine 物理性质:状态:黄绿色卤气。
返回
氩
元素名称氩 元素符号Ar 原子序数18 相对原子质量(12C = 12.0000)39.948 英文名称Argon 物理性质:状态:无色、无臭、无味的惰性气体。
返回
铝
元素名称铝 元素符号Al 原子序数13 相对原子质量(12C = 12.0000)26.981539 英文名称Aluminum 物理性质:状态:银色,轻质,非磁性的可锻金属。
返回
硅
元素名称硅 元素符号Si 原子序数14 相对原子质量(12C = 12.0000)28.0855 英文名称Silicon 物理性质:状态:硬的深灰色非金属。
返回
氮
元素名称氮 元素符号N 原子序数7 相对原子质量(12C =12.0000) 14.00674 英文名称Nitrogen 物理性质:状态:无色、无味、无臭的气体。
返回
氧
元素名称氧 元素符号O 原子序数8 相对原子质量(12C = 12.0000)15.9994 英文名称Oxygen 物理性质:状态:无色、无臭、无味的气体。
第一节元素周期表(共40张PPT)
第ⅦA 族
与水缓慢反应
(2)原子结构特点 Cl2+H2O=HCl+HClO
静置后,液体分为两层。
通一过个以 12上C相质比量较同×,1点/思12考:钠和钾最的外性质层有 7个电子
静置后,液体分为两层。
和递变性。 (氧化性:Cl2 >I2)
核电荷数依次增多
不同点: 电子层数依次增多 上层无色,下层分别呈橙红色、紫红色
第一章 物质结构、元素周期律
第一节 元素周期表 一、元素周期表的结构
原子序数:依原子核电荷数由小到大的顺序给元素编号,这种
编号叫原子序数。
原子序数=核电荷数=质子数=核外电子数 (一)元素周期表的编排原则
1、横行: 把电子层数相同的各种元素按原子序数递增顺序
从左到右排列。
2、纵行: 把最外层电子数相同的各种元素按电子层数递增顺序 从上而下排成。
性逐渐增强,非金属性逐渐减弱。
2. 元素性质与原子结构有有密切的关系,主要与原子
核外的排布,特别是最外层电子数有关。原子结构
相似的一族元素,它们在化学性质上表现出相似性 和递变性。
1、砹(At)原子序数85,与F、Cl、Br、I同族,推测砹或
砹的化合物不可能具有的性质是( B)
A、砹易溶于某些有机溶剂 B、砹能与水剧烈反应
应越来越
,剧生烈成的氧化物越来越
。
最高复价杂氧化物对应水化物的碱性越来越 。
强
讨论1:Li与K 应如何保存? Li封存于固体石蜡中, 少量K保存于煤油中。
讨论2:碱金属与盐酸: 2R+2H+= 2R++H2 ↑ 讨论3:碱金属与盐溶液: 先与水反应
讨论4:Li+、Na+、K+、Rb+、Cs+也具有强还原性吗? 没有。 有较弱的氧化性。 氧化性: Li+ > Na+ > K+ > Rb+ > Cs+
51元素周期表(精品课件 ppt--高中化学

o (3)表中能形成两性 氧化物的元素是 ________(填名称),分 写出 元素的 氧化物与⑥、⑨最高价氧化物的水化物反 的 化学方程式: _______________________
o (4) 一个 方案,比 ⑦、⑩ 氧化性的强弱:
o ____________________________
o (2) 跟水起 烈反 ,放出________色 气体,同 使滴有紫色石蕊 液的溶液 ________色,因 ____________________________ ___________(写出离子方程式)。
o (3)碳酸 的水溶液使酚 液 ________色,因 ____________________________ ____________________________ ________________(用离子方程式表示 )。
o 三、核素 o 1.原子 o (1)原子 构:
o (2)有关粒子 的关系 o ① 量数(A)=________+________; o ②中性原子: 子数=________=
________;
o ③阳离子: 子数=核外 子数+ ________;
o ④阴离子: 子数=核外 子数- ________。
o A. 子数、中子数 o B. 子数、最外 子数 o C.中子数、最外 子数 o D.最外 子数、 量数 o 答案:B
o 2.(2008·四· 川高考)下列叙述中正确的是 o ()
o A.除零族元素外,短周期元素的最高化合价 在数 上都等于 元素所属的族序数
o B.除短周期外,其他周期均有18种元素 o C.副族元素中没有非金属元素 o D.碱金属元素是指第ⅠA族的所有元素 o 答案:C
o ③元素:具有相同________的同一 ________的 称。
o (4) 一个 方案,比 ⑦、⑩ 氧化性的强弱:
o ____________________________
o (2) 跟水起 烈反 ,放出________色 气体,同 使滴有紫色石蕊 液的溶液 ________色,因 ____________________________ ___________(写出离子方程式)。
o (3)碳酸 的水溶液使酚 液 ________色,因 ____________________________ ____________________________ ________________(用离子方程式表示 )。
o 三、核素 o 1.原子 o (1)原子 构:
o (2)有关粒子 的关系 o ① 量数(A)=________+________; o ②中性原子: 子数=________=
________;
o ③阳离子: 子数=核外 子数+ ________;
o ④阴离子: 子数=核外 子数- ________。
o A. 子数、中子数 o B. 子数、最外 子数 o C.中子数、最外 子数 o D.最外 子数、 量数 o 答案:B
o 2.(2008·四· 川高考)下列叙述中正确的是 o ()
o A.除零族元素外,短周期元素的最高化合价 在数 上都等于 元素所属的族序数
o B.除短周期外,其他周期均有18种元素 o C.副族元素中没有非金属元素 o D.碱金属元素是指第ⅠA族的所有元素 o 答案:C
o ③元素:具有相同________的同一 ________的 称。
元素周期表_课件PPT

人类在长期的生产活动和科学实践中,逐步认识了元 素间的内在联系和元素性质变化的规律性。那么同族元素 间有哪些规律存在呢?让我们一起走进丰富多彩的物质世 界,共同探讨元素的性质与原子结构的关系。
●梳理导引 1.碱金属元素原子的最外层都有______________个 电子,都是活泼的金属;且随核电荷数增加,电子层数逐 渐______________,原子半径逐渐______________,金属 性逐渐____________。 2.碱金属单质的物理性质:都有______________的 金属光泽,质______________,密度______________,熔 点____________,导电性和导热性都____________;随着 核电荷数增加,碱金属单质的熔、沸点逐渐____________, 密度逐渐____________[特殊的ρ(K)<ρ(Na)]。
4.比较元素金属性强弱的方法 (1)根据金属活动性顺序表判断。自左至右金属性减弱, 即失电子能力减弱,如:Zn>Cu。 (2)根据元素周期表判断。同周期,从左至右金属性减 弱 。 同 主 族 , 自 上 而 下 金 属 性 增 强 。 如 : Na>Mg>Al , Na<K。 (3)根据元素的单质与水(或酸)反应置换出氢的难易程 度判断。置换反应越易发生的元素金属性越强。如钾与水 比钠与水反应剧烈,则K>Na(金属性)。
溶液分上 下两层,下层呈 红棕色
Cl2+ 2NaBr===2NaCl+Br2
b.将少量新制的饱 和氯水加入盛有KI溶液 的试管,振荡后加CCl4, 振荡,静置
溶液分上 下两层,下层呈 紫红色
+I2
Cl2+2KI===2KCl
实验
c.将少量溴水加 入盛有KI溶液的试管, 振荡后加CCl4,振荡,
元素周期表ppt课件

元素周期表揭示了元素在生物地球化学循环中的作用,有助于理解 生态系统的物质循环和能量流动。
05
元素周期表的未来发展
新的元素发现与合成
合成新元素
随着科学技术的不断进步,科学家们 可能会合成更多超重元素,进一步丰 富元素周期表。
探索新元素特性
新元素的发现将有助于深入了解元素 的性质和行为,为科学研究和技术创 新提供更多可能性。
元素周期表的完善与修正
修正元素性质
随着新元素的合成和性质研究,元素周期表中的元素性质可能会得到修正和完 善。
调整周期表结构
根据新发现和研究成果,元素周期表的排列和分类可能会进行相应的调整和优 化。
元素周期表在未来的应用前景
科学研究
元素周期表在化学、物理、材料科学等领域的研究中发挥着重要作用,未来仍将 是科学家们的重要工具。
技术创新
元素周期表中的元素是许多技术和产品的关键组成部分,随着新元素的发现和应 用,将有助于推动技术创新和产业发展。
THANKS
感谢观看
材料分类与鉴别
元素周期表为材料分类和鉴别提 供了依据,有助于对不同材料进
行科学分类和鉴别。
在生命科学领域的应用
生物分子结构研究
元素周期表在解析生物分子结构中发挥了重要作用,例如蛋白质 和核酸的结构研究。
药物设计与研发
通过元素周期表,可以预测药物分子的性质和行为,有助于新药的 研发和优化。
生物地球化学循环
通过元素周期表,科学家可以了解材料的物理和 化学性质,从而在材料科学和工程领域进行有效 的应用。
促进化学和其他学科的发展
元素周期表为化学学科提供了基础框架,同时也 为其他学科提供了重要的参考和借鉴。
02
元素周期表中的元素
05
元素周期表的未来发展
新的元素发现与合成
合成新元素
随着科学技术的不断进步,科学家们 可能会合成更多超重元素,进一步丰 富元素周期表。
探索新元素特性
新元素的发现将有助于深入了解元素 的性质和行为,为科学研究和技术创 新提供更多可能性。
元素周期表的完善与修正
修正元素性质
随着新元素的合成和性质研究,元素周期表中的元素性质可能会得到修正和完 善。
调整周期表结构
根据新发现和研究成果,元素周期表的排列和分类可能会进行相应的调整和优 化。
元素周期表在未来的应用前景
科学研究
元素周期表在化学、物理、材料科学等领域的研究中发挥着重要作用,未来仍将 是科学家们的重要工具。
技术创新
元素周期表中的元素是许多技术和产品的关键组成部分,随着新元素的发现和应 用,将有助于推动技术创新和产业发展。
THANKS
感谢观看
材料分类与鉴别
元素周期表为材料分类和鉴别提 供了依据,有助于对不同材料进
行科学分类和鉴别。
在生命科学领域的应用
生物分子结构研究
元素周期表在解析生物分子结构中发挥了重要作用,例如蛋白质 和核酸的结构研究。
药物设计与研发
通过元素周期表,可以预测药物分子的性质和行为,有助于新药的 研发和优化。
生物地球化学循环
通过元素周期表,科学家可以了解材料的物理和 化学性质,从而在材料科学和工程领域进行有效 的应用。
促进化学和其他学科的发展
元素周期表为化学学科提供了基础框架,同时也 为其他学科提供了重要的参考和借鉴。
02
元素周期表中的元素
人教版高中化学必修二第一章第一节 《元素周期表 》课件(共15张PPT)

B.原子的核外电子数
C.原子核内的质子数
√D.原子的中子数
1.原子序数为 x 的元素位于第IA族,那么原子序 数为 x+2 的元素肯定不会在( )
√ A.第 IA 族 B.第ⅢB族 C.第ⅢA族 D.0族
【提示】若x为氢元素,则A正确;若x为锂或钠, 则C正确;若x在第4、5、6、7周期,则B项正确。 故答案为D。
3.第ⅠA族和0族元素的原子序数
4.每周期元素的种数
一、元素周期表的结构 “三短”“四长”;“七主”“七副”“0族和Ⅷ族” 二、元素原子结构与其在周期表中位置的关系.
周期序数=电子层数 主族序数=最外层电子数
原子序数
核外电子排布
周期表中位置
1.不能作为元素周期表中元素排列顺序的依据是
A.原子的核电荷数
螺旋式元素周期表
金字塔式元素周期表
1869年,俄国化学家门捷列夫将 元素按照相对原子质量由小到大 依次排列,制出了第一张元素周 期表,这就是现代元素周期表的 雏形。
第一章 物质结构 元素周期律
第一节 元素周期表
【思考与交流】
周期表的结构
阅读教材P4、5页并结合周期表,讨论以下问题
1.元素周期表的编排原则是什么?周期表有多 少横行,多少纵行,多少族?
A.若X是氢,则Y是氦
√C.若X是氟,则W是硫
B.若Y是氦,则Z是钠 D.若Y是氟,则Z是铝
例.已知某主族元素的原子结构示意图如下,判断 其位于第几周期,第几族?
【提示】X为第4周期,第ⅠA族;Y为第5周期,第 ⅦA族。
【记一记】
周期表的结构
1.原子序数=核电荷数=质子数=核外电子数
2.周期序数=电子层数 主族序数=最外层电子数
元素ppt课件

磷元素及其性质
磷元素的物理性质:磷是一种 白色或浅黄色固体,具有微弱 的毒性。
磷元素的化学性质:磷在常温 下能与氧气反应生成五氧化二 磷,同时也能与酸反应。
磷的重要化合物:磷酸、磷酸 盐等。
氯元素及其性质
氯元素的物理性质
氯是一种黄绿色气体,具有强烈的刺激性气味。
氯元素的化学性质
氯气具有强氧化性,能与多种金属和非金属反应 生成氯化物。
描述铁在自然界中的存在形式,以及铁在工 业和日常生活中的用途。
05
CHAPTER
非金属元素及其性质
硫元素及其性质
硫元素的物理性质
硫是一种淡黄色固体,具有刺激 性气味。
硫元素的化学性质
硫在常温下不易与氧气反应,但 在加热条件下能与氧气反应生成
二氧化硫。
硫的重要化合物
硫化氢、二氧化硫、三氧化硫等 。
氢气是已知的最轻的元素,也 是宇宙中最丰富的元素。
物理性质:无色、无味、透明 的气体。
化学性质:非常活泼,可以与 几乎所有其他元素形成化合物
。
氢气的用途:用于生产氨、盐 酸、甲醇等化工产品;作为火 箭推进剂;用于核聚变研究等
。
氧元素及其性质
原子序数:8 元素符号:O
原子质量:15.9994
氧元素及其性质
中的表现。
镁的存在和用途
描述镁在自然界中的存在形式 ,以及镁在工业和日常生活中
的用途。
铝元素及其性质
铝的原子结构
详描述铝的原子结构,包括 质子数、中子数和电子数等。
铝的物理性质
描述铝的外观、状态、密度、 硬度等物理特性。
铝的化学性质
分析铝与其他元素之间的化学 反应,以及铝在各种化学环境 中的表现。
元素周期表完整(33张)ppt课件

短周期元素中,族序数等于周期序数的元素有 ___H__、__B_e_、__A_l__,族序数等于周期序数2倍的元素有 ___C__、__S_,周期序数等于族序数2倍的元素有__L_i___。
ppt精选版
28
4.判断正误
× (1)最外层电子数为2的元素一定在第ⅡA族。( )
2He
如:氦
10Ne
√ (2)若发现了115号元素,则该元素肯定位于第7周期第ⅤA族。( 18Ar)
6个横行 6个周期
第Ⅷ族
18个纵行,16个族 ppt精选版
金属与 非金属 分界线
26
2.下列各图为元素周期表的一部分,表中的数字为原子序数, 其中M为37的是( C )
35 36
35
×
×
37 38
√
ppt精选版
27 45
×
27
3.第3周期第ⅣA族的元素是__S_i_____;Na元素的原子 序数为11,其相邻的同族元素的原子序数是__3_、__1_9__;
6
ppt精选版
螺
旋
时
钟
式
元
素
周
期
表
7
ppt精选版
塔 式 元 素 周 期 表
8
棱
台
型
元
素
周
期
ppt精选版
表
9
ppt精选版
层 式 元 素 周 期 表
10
ppt精选版
螺 旋 式 元 素 周 期 表
11
ppt精选版
透 视 式 元 素 周 期 表
12
ppt精选版
螺 旋 式 元 素 周 期 表
13
Mn= 55 Rh=104.4 Pt= 197.4
ppt精选版
28
4.判断正误
× (1)最外层电子数为2的元素一定在第ⅡA族。( )
2He
如:氦
10Ne
√ (2)若发现了115号元素,则该元素肯定位于第7周期第ⅤA族。( 18Ar)
6个横行 6个周期
第Ⅷ族
18个纵行,16个族 ppt精选版
金属与 非金属 分界线
26
2.下列各图为元素周期表的一部分,表中的数字为原子序数, 其中M为37的是( C )
35 36
35
×
×
37 38
√
ppt精选版
27 45
×
27
3.第3周期第ⅣA族的元素是__S_i_____;Na元素的原子 序数为11,其相邻的同族元素的原子序数是__3_、__1_9__;
6
ppt精选版
螺
旋
时
钟
式
元
素
周
期
表
7
ppt精选版
塔 式 元 素 周 期 表
8
棱
台
型
元
素
周
期
ppt精选版
表
9
ppt精选版
层 式 元 素 周 期 表
10
ppt精选版
螺 旋 式 元 素 周 期 表
11
ppt精选版
透 视 式 元 素 周 期 表
12
ppt精选版
螺 旋 式 元 素 周 期 表
13
Mn= 55 Rh=104.4 Pt= 197.4
原子结构和元素周期表ppt课件

(2)最外层电子数是次外层电子数的一半元素:Li、Si (3)最外层电子数等于次外层电子数的元素:Be、Ar (4)最外层电子数是次外层电子数2倍的元素:C (5)最外层电子数是次外层电子数3倍的元素:O (6)最外层电子数是次外层电子数4倍的元素:Ne (7)最外层电子数等于电子层数的元素:H、Be、Al 1至20号元素中,
族 序 数
ⅠⅡ ⅢⅣⅤ Ⅵ A A BBB B
Ⅶ B
Ⅷ
ⅠⅡⅢⅣⅤⅥⅦ BBAAAAA
0
常见族的别名:
第ⅠA族(除氢外):碱金属元素 第ⅦA族: 卤族元素 0族:稀有气体元素
(2)族的分类 18个纵行16个族
主族:由短周期元素和长周期元素共同构成(7个)
表示方法:ⅠA 、ⅡA 、ⅢA 、ⅣA 、ⅤA、 ⅥA、 ⅦA
原子结构与元素周期表
原子结构:
质子
电子
中子
质子 带正电荷
{ { 原子
原子核
(带正电荷)中子
不带电
(不带电) 核外电子 (带负电荷)
核电荷数=质子数=核外电子数=原子序数
构成原子 的粒子
质量/kg
电子 9.109×10-31
质子 1.673×10-27
中子 1.675×10-27
相对质量
1/1836 (电子与质子质量之比)
与氩原子电子层结构相同的阳离子是:K+、Ca 2+ 与氩原子电子层结构相同的阴离子是:S2- 、Cl-
元素周期表:
门捷列夫 相对原子质量
相对原子质量
核电荷数
原子序数=核电荷数=质子数=核外电子数
每一横行电子层数相同;每一纵行最外层电子数相同(除稀有气体元素) 编排原则:(1)按原子序数递增的顺序从左到右排列。 (2)将电子层数相同的元素排列成一个横行,即周期。 (3)把最外层电子数相同的元素按电子层数递增的顺序从上到下排成纵行, 即族。
族 序 数
ⅠⅡ ⅢⅣⅤ Ⅵ A A BBB B
Ⅶ B
Ⅷ
ⅠⅡⅢⅣⅤⅥⅦ BBAAAAA
0
常见族的别名:
第ⅠA族(除氢外):碱金属元素 第ⅦA族: 卤族元素 0族:稀有气体元素
(2)族的分类 18个纵行16个族
主族:由短周期元素和长周期元素共同构成(7个)
表示方法:ⅠA 、ⅡA 、ⅢA 、ⅣA 、ⅤA、 ⅥA、 ⅦA
原子结构与元素周期表
原子结构:
质子
电子
中子
质子 带正电荷
{ { 原子
原子核
(带正电荷)中子
不带电
(不带电) 核外电子 (带负电荷)
核电荷数=质子数=核外电子数=原子序数
构成原子 的粒子
质量/kg
电子 9.109×10-31
质子 1.673×10-27
中子 1.675×10-27
相对质量
1/1836 (电子与质子质量之比)
与氩原子电子层结构相同的阳离子是:K+、Ca 2+ 与氩原子电子层结构相同的阴离子是:S2- 、Cl-
元素周期表:
门捷列夫 相对原子质量
相对原子质量
核电荷数
原子序数=核电荷数=质子数=核外电子数
每一横行电子层数相同;每一纵行最外层电子数相同(除稀有气体元素) 编排原则:(1)按原子序数递增的顺序从左到右排列。 (2)将电子层数相同的元素排列成一个横行,即周期。 (3)把最外层电子数相同的元素按电子层数递增的顺序从上到下排成纵行, 即族。
元素周期表ppt课件

通过元素周期表,可以了 解不同元素之间的组合规 律,指导新型材料的合成 。
分析材料组成
利用元素周期表,可以对 材料进行定性和定量分析 ,确定其组成元素及其比 例。
在能源科学研究中的应用
能源转换与储存
元素周期表中的元素可以用于能 源转换和储存,如利用过渡金属 元素制备催化剂,提高能源利用
效率。
能源材料研究
元素周期表的结构与特点
结构
元素周期表主要包括多个周期和多个族,每个周期和每个族都有特定的元素组 成和性质特征。
特点
元素周期表具有周期性和重复性,元素的性质随着原子序数的增加呈现出规律 性的变化。
02
元素周期表中的元素分类
金属元素
定义
金属元素是指在周期表中的具有金属特性的元素 。
特点
金属元素通常具有较高的原子序数和相对较大的 原子质量,具有导电和导热性。
稀有气体元素的化学反应性能变化规律
• 稀有气体元素:稀有气体元素位于元素周期表零族,其化学反 应性能非常不活泼,几乎不与任何其他元素发生化学反应。
05
元素周期表在科学研究中的应用
在材料科学研究中的应用
预测材料性质
元素周期表可以用于预测 材料的物理、化学性质, 如硬度、熔点、电导率等 。
指导材料合成
化合物结构研究
通过元素周期表,可以研究化合物的结构,预测 化合物的性质,为合成和设计新的化合物提供理 论支持。
化学史教育
元素周期表的发展历程也是化学史的重要内容, 有助于学生了解化学学科的发展历程。
在研究生化学教学中的应用
科研实践应用
在研究生阶段,元素周期表是科研实践的重要工具,通过元素周期 表可以研究新型材料、新药物等。
同一周期内,从左到右,电负性逐渐 增大
分析材料组成
利用元素周期表,可以对 材料进行定性和定量分析 ,确定其组成元素及其比 例。
在能源科学研究中的应用
能源转换与储存
元素周期表中的元素可以用于能 源转换和储存,如利用过渡金属 元素制备催化剂,提高能源利用
效率。
能源材料研究
元素周期表的结构与特点
结构
元素周期表主要包括多个周期和多个族,每个周期和每个族都有特定的元素组 成和性质特征。
特点
元素周期表具有周期性和重复性,元素的性质随着原子序数的增加呈现出规律 性的变化。
02
元素周期表中的元素分类
金属元素
定义
金属元素是指在周期表中的具有金属特性的元素 。
特点
金属元素通常具有较高的原子序数和相对较大的 原子质量,具有导电和导热性。
稀有气体元素的化学反应性能变化规律
• 稀有气体元素:稀有气体元素位于元素周期表零族,其化学反 应性能非常不活泼,几乎不与任何其他元素发生化学反应。
05
元素周期表在科学研究中的应用
在材料科学研究中的应用
预测材料性质
元素周期表可以用于预测 材料的物理、化学性质, 如硬度、熔点、电导率等 。
指导材料合成
化合物结构研究
通过元素周期表,可以研究化合物的结构,预测 化合物的性质,为合成和设计新的化合物提供理 论支持。
化学史教育
元素周期表的发展历程也是化学史的重要内容, 有助于学生了解化学学科的发展历程。
在研究生化学教学中的应用
科研实践应用
在研究生阶段,元素周期表是科研实践的重要工具,通过元素周期 表可以研究新型材料、新药物等。
同一周期内,从左到右,电负性逐渐 增大
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
11 Na
12 Mg
13 Al
14 Si
15 P
16 S
17 Cl
18 Ar
19 K
20 Ca
21 Sc
22 Ti
23 V
24 Cr
25 Mn
26 Fe
27 Co
28 Ni
29 Cu
30 Zn
31 Ga
32 Ge
33 As
34 Se
35 Br
36 Kr
Hydrogen Helium Lithium Beryllium Boron Carbon Nitrogen Oxygen Fluorine Neon Sodium Magnesium Aluminum Silicon Phosphorous Sulfur Chlorine Argon Potassium Calcium Scandium Titanium Vanadium Chromium Manganese Iron Cobalt Nickel Copper Zinc Gallium Germanium Arsenic Selenium Bromine Krypton
U n1n8ilh e xiu m
Unnilseptium
v 1A
1 H
2A
34 Li Be
11 12 Na Mg
19 20 K Ca
Row
2 He
1
3A 4A 5A 6A 7A
5 B
6 C
7 N
8 O
9 F
10 Ne
2
13 Al
14 Si
15 P
16 S
17 Cl
18 Ar
3
21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36
Hafnium Tantalum Tungsten Rhenium O sm ium Iridium Platinum Gold Mercury Thallium Lead Bismuth Polonium Astatine Radon Francium Radium Actinium Thorium Protactinium Uranium Neptunium Plutonium Americium Curium Berkelium Californium Einsteinium Ferm ium Mendelevium Nobelium Lawrencium Unnilquadium Unnilpentium
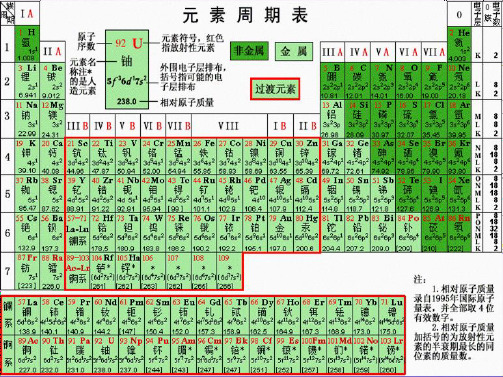
各种元素周期表
.
1
.
2
1829年,德国耶那大学的化学教授德贝莱纳(D Obereiner) 根据元素性质的相似性,提出了“三素组”学说。
按照这种分类方法,可以找到一些规律。如每组里中
间元素的原子量大约等于其他两种元素原子量的平均值。
但是,在当时已发现的54种元素中却只能把15种元素
归入“三素组”。
71 L. u
Rubidium Strontium Yttrium Zirconium Niobium Molybdenum Technetium Ruthium Rhodium Paladium Silver Cadmium Indium Tin Antimony Tellurium Iodine Xenon Cesium Barium Lanthanum Cerium Praseodymium Neodymium Promethium Samarium Europium Gadolinium Terbium Dysprosium H olm ium Erbium Thulium Ytterbium Lutetium
.
8.Biblioteka 9.10.
11
.
12
目前我们最常使用的元素周期表
.
13
立体的元素周期表
.
14
.
15
我国早期的元. 素周期表
16
.
17
THE NAMES, ATOMIC NUMBERS, AND SYMBOLS OF THE ELEMENTS
1
H
2
He
3
Li
4
Be
5
B
6
C
7
N
8
O
9
F
10 Ne
素周期表,1870年. 发表
5
.
6
1865年,英国人纽兰兹(Newlands)把当时已知的元素按原子量 由小到大的顺序排列,发现每8种元素之后,会重复出现相似的性 质。他把他的发现称为“八音律”,就象音乐里的八度音程一样。 但是,纽兰兹按“八音律”排的元素表在很多地方是混乱的。但 是他没有充分估计到测定原子量.会有错误,又未考虑到还有未7发 现的元素而留出空白。
Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 4
37 Rb 38 Sr 39 Y 40 Zr 41 Nb 42 Mo 43 Tc 44 Ru 45 Rh 46 Pd 47 Ag 48 Cd 49 In 50 Sn 51 Sb 52 Te 53 I 54 Xe 55 Cs 56 Ba 57 La 58 Ce 59 Pr 60 Nd 61 Pm 62 Sm 63 Eu 64 Gd 65 Tb 66 Dy 67 Ho 68 Er 69 Tm 70 Yb
72 Hf 73 Ta 74 Tu 75 Re 76 Os 77 Ir 78 Pt 79 Au 80 Hg 81 Ti 82 Pb 83 Bi 84 Po 85 At 86 Rn 87 Fr 88 Ra 89 Ac 90 Th 91 Pa 92 U 93 Np 94 Pu 95 Am 96 Cm 97 Bk 98 Cf 99 Es 100 Fm 101 Mv 102 No 103 Lw 104 Unq 105 Unp 106 Unh 107 Uns
但是由于元素的性质呈周期
性变化并不完全是由原子量
决定的,所以螺旋图并没有
真正反映元素的性质呈周期
性变化。
.
4
J.L.迈尔的《六元素表》
(1864年)
Li (Be)
C N O F Na Mg
Si P S Cl K Ca
As Se Br Rb Sr
Sn Sb Te I Cs Ba
Pb Bi
(Tl)
迈尔在1869年10月制作了元
.
3
1862年法国化学家A.E.B德尚
库托提出了元素的性质随原
子量而变创立了“螺旋图”。
他将当时已知的62种元素按
其原子量的大小循序标记在
圆柱上的螺旋线上。这样就
能清楚地看出那些性质相似
的元素基本上处于圆柱的同
一母线上,如Li---Na----K;S-
---Se-----Te;Cl----Br----I等等。
