《二烯烃和共轭体系》习题及答案
第四章 二烯烃和共轭体系共13页文档

第四章二烯烃共轭体系共振论分子中含有两个碳—碳双键的碳氢化合物称为二烯烃。
通式:C n H2n-2可见,二烯烃与炔烃互为官能团异构。
4.1 二烯烃的分类和命名4.1.1 二烯烃的分类根据分子中两个C=C的相对位置,二烯烃可分为三类。
(1) 孤立二烯烃两双键之间相隔两个或两个以上单键的二烯烃。
例:CH2=CH-CH2-CH=CH2CH2=CH-CH2- CH2-CH=CH21,4-戊二烯1,5-己二烯单双键交替的体系,为共轭体系!由于两个双键共轭,相互影响,其性质特殊,是本章的重点之一。
4.1.2 二烯烃的命名与烯烃相似。
用阿拉伯数字标明两个双键的位次,用“Z/E”或“顺/反”表明双键的构型。
例:4.2 二烯烃的结构4.2.1 丙二烯的结构丙二烯是典型的累积二烯。
仪器测得,丙二烯是线型非平面分子:由于中心碳为sp杂化,两个双键相互⊥(动画),所以丙二烯及累积二烯烃不稳定。
4.2.2 1,3-丁二烯的结构仪器测得,1,3-丁二烯分子中的10个原子共平面:1,3-丁二烯分子中存在着明显的键长平均化趋向!⑴价键理论的解释1,3-丁二烯中的碳原子是sp2杂化态(因为只有sp2杂化才能是平面构型,轨道夹角约120°):四个sp2杂化碳搭起平面构型的1,3-丁二烯的σ骨架:四个P轨道肩并肩地重叠形成大π键:(动画,π-π共轭)除了C1-C2和C3-C4间的P轨道可肩并肩地重叠外,C2-C3间也能肩并肩重叠。
但由键长数据表明,C2-C3间的重叠比C1-C2或C3-C4间的重叠要小。
⑵分子轨道理论的解释(主要用来处理p电子或π电子)丁二烯分子中四个碳原子上的未参加sp2杂化的p轨道,通过线性组合形成四个分子轨道:4.3 电子离域与共轭体系电子离域——共轭体系中,成键原子的电子云运动范围扩大的现象。
电子离域亦称为键的离域。
电子离域使共轭体系能量降低。
共轭体系——三个或三个以上互相平行的p轨道形成的大π键。
有机化学(第四版)习题解答

高鸿宾(主编)有机化学(第四版)习题解答化学科学学院罗尧晶编写高鸿宾主编《有机化学》(第四版)作业与练习第二章饱和烃:烷烃和环烷烃练习(P60—62):(一的1,3,5,7,9,11小题)、(五)、(六)、(十三)第三章不饱和烃:烯烃和炔烃作业:(P112—117):(二)、(四)、(七)、(十一)、(十五的2,3小题)、(十六的2~5小题)、(二十一)第四章二烯烃共轭体系练习:(P147—149):(三)、(十)、(十一)、(十三)第五章芳烃芳香性作业:(P198—202):(二)、(三)、(九)、(十)、(十六)、(十七)、(十八的2、5~10小题)、(二十四)第六章立体化学练习:(P229—230):(五)、(六)、(七)、(十二)第七章卤代烃作业:(P263);(P290-295):(P263):(习题7.17)、(习题7.18)、(习题7.19)。
(P290-295):(六)、(七)、(八)、(十的1、2、5小题)、(十三的1、2小题)、(十四的1、2小题)第九章醇和酚作业:(P360—362):(二)、(三的2、4小题)、(五)、(九的1、3小题)第十一章醛、酮和醌作业:(P419—421):(一)、(三)、(七题的1—9小题)、(十三)、(十四)第十二章羧酸练习:(P443—444):(一)、(三)、(五)、(七)第十三章羧酸衍生物练习:(P461—464):(一)、(四)、(六)、(七)(八题的1、3小题)、第十四章β-二羰基化合物作业:(P478—480):(一)、(五)、(七)第十五章有机含氮化合物作业:(P526—530):(三)、(四)、(八)、(十一)第二章 烷烃和环烷烃 习题解答(一)题答案:(1) 3-甲基-3-乙基庚烷 (2)2,3 -二甲基-3-乙基戊烷 (3)2,5-二甲基-3,4 -二乙基己烷 (4)1,1-二甲基-4-异丙基环癸烷 (5)乙基环丙烷 (6)2-环丙基丁烷 (7)1,5-二甲基-8-异丙基二环[4.4.0]癸烷(8)2-甲基螺[3.5]壬烷 (9)5-异丁基螺[2.4]庚烷 (10)新戊基 (11)2′-甲基环丙基 (12)1′-甲基正戊基(四)题答案:(1)的透视式: (2)的透视式: (3)的透视式:Cl HCH 3H 3C ClHCH 3CH 3ClHHCH 3Cl ClCH 3H H(4)的投影式: (5)的投影式:BrBr CH 3HH H 3CBrBr CH 3CH 3HH(五)题解答:都是CH 3-CFCl 2的三种不同构象式; 对应的投影式依次分别如下:ClClClClClClFFFHH H H H H H H ( )( )( )123验证如下:把投影式(1)的甲基固定原有构象位置不变,将C-C 键按顺时针方向分别旋转前面第一碳0°、60°、120°、180°、240°得相应投影式如下:ClCl ClClClClClCl ClFF FF F H HH H H HHH H H H H HH H ( )( )( )( )( )ab c de各投影式对应的能量曲线位置如下:由于(a )、(c )、(e )则为(1)、(2)、(3)的构象,而从能量曲线上,其对应能量位置是一样的,所以前面三个透视式只是CH 3-CFCl 2的三种不同构象式。
高鸿宾四版有机化学答案 第四章 二烯烃和共轭体系

第四章 二烯烃和共轭体系习题(P147)(一) 用系统命名法命名下列化合物:(1) CH 2=CHCH=C(CH 3)2(2) CH 3CH=C=C(CH 3)24-甲基-1,3-戊二烯2-甲基-2,3-戊二烯(3)CH 2=CHCH=CHC=CH 3CH 3(4)C=CCH=CH 2CH 3H H2-甲基-1,3,5-己三烯 (3Z)-1,3-戊二烯(二) 下列化合物有无顺反异构现象:若有,写出其顺反异构体并用Z,E-命名法命名。
解:(1) 无;(2) 有;(3E)-1,3-戊二烯, (3Z)-1,3-戊二烯;(3) 有;(3Z,5Z)-3,5-辛二烯, (3Z,5E) -3,5-辛二烯,(3E,5E) -3,5-辛二烯; (4) 有;(3E)-1,3,5-己三烯, (3Z)-1,3,5-己三烯; (5) 无 (三) 完成下列反应式:解:红色括号中为各小题所要求填充的内容。
(1)+ HOOCCH=CHCOOH(2)CHCH +(3)33H+COOCH 3COOCH 3HH(4)33HH+HCOOCH 3HCH 3OOC(5)+ RMgX MgX+ RH(6)O+3(7)CHO+(8)CH 2Cl+CH 2Cl KMnO +HOOCCH 2CHCH 2CH 2COOHCH 2Cl(A)(B)(9)CH 33h33(10) CHCH 3CH 3H CH 3CH 3CH 3H(四) 给出下列化合物或离子的极限结构式,并指出哪个贡献最大?(1) CH 3CN (2)(CH 3)2C=CH C(CH 3)2 (3) CH 2=CH CH 2(4) (5)CH 2C CH 3O(6)CH 3C CH=CH 2O解: (1) CH 3C N CH 3CNCH 3CN贡献最大(非电荷分离)(2) (CH 3)2C=CH C(CH 3)2(CH 3)2C CH=C(CH 3)2结构相似,二者贡献一样大(3) CH 2=CH CH 2CH 2CH=CH 2结构相似,二者贡献一样大(4)... ...各共振结构式结构相似,能量相同,对真实结构的贡献相同。
第四章 二烯烃与共轭体系

光照 顺旋
CH3 H CH3 H
(Z,Z,E)-2,4,6-辛三烯
对旋
光照 顺旋
H H CH3 CH3
顺-5,6-二甲基环己二烯
CH3 H H CH3
加热 对旋 (E,Z,E)-2,4,6-辛三烯
4.5.4 双烯合成:Diels-Alder 反应
•含环己烯环的化合物的制备方法
CH2
+
BrCH2CH
CHCH2Br
Br
(37%) (63%)
结论
1,4加成产物更稳定; 1,2加成产物和1,4加成产物是可逆的; 1,2加成产物的活化能低,反应速度快。
练习题: 由丁二烯合成重要的药物前体及 材料合成中间体3-羟甲基戊二酸
HO2C
OH CO2H
HO2C
OH CO2H
第四章 二烯烃与共轭体系
分子中含有两个碳–碳双键的不饱和烃称为二烯 烃, 包括链状二烯烃和环状二烯烃.
链状二烯烃
环状二烯烃
4.1 二烯烃的分类和命名
•隔离二烯烃 •共轭二烯烃
C
•累积二烯烃
4.2 二烯烃的结构
(1) 丙二烯的结构 (2) 1,3–丁二烯的结构
4.2 二烯烃的结构
4.2.1 丙二烯的结构
C +
+
+ C -
C + C +
p *3
C -
C
p2
成 键 轨 道
+ C + C -
+ C + C -
C + + C -
C + + C -
+ C + C C C C C
《有机化学》第四版[1]._高鸿宾版_课后练习答案(新)
![《有机化学》第四版[1]._高鸿宾版_课后练习答案(新)](https://img.taocdn.com/s3/m/2e51507deefdc8d376ee32b9.png)
第二章饱和烃习题(P60)(一) 用系统命名法命名下列各化合物,并指出这些化合物中的伯、仲、叔、季碳原子。
(1) (2)3-甲基-3-乙基庚烷2,3-二甲基-3-乙基戊烷(3) (4)2,5-二甲基-3,4-二乙基己烷1,1-二甲基-4-异丙基环癸烷(5) (6)乙基环丙烷2-环丙基丁烷(7) (8)1,7-二甲基-4-异丙基双环[4.4.0]癸2-甲基螺[]壬烷烷(9) (10)5-异丁基螺[]庚烷新戊基(11) (12)2-甲基环丙基2-己基 or (1-甲基)戊基(二) 写出相当于下列名称的各化合物的构造式,如其名称与系统命名原则不符,予以改正。
(1) 2,3-二甲基-2-乙基丁(2) 1,5,5-三甲基-3-乙基己(3) 2-叔丁基-4,5-二甲基己烷烷烷2,3,3-三甲基戊烷2,2-二甲基-4-乙基庚烷2,2,3,5,6-五甲基庚烷(4) 甲基乙基异丙基甲烷(5) 丁基环丙烷(6) 1-丁基-3-甲基环己烷2,3-二甲基戊烷1-环丙基丁烷1-甲基-3-丁基环己烷(三) 以C2与C3的σ键为旋转轴,试分别画出2,3-二甲基丁烷和2,2,3,3-四甲基丁烷的典型构象式,并指出哪一个为其最稳定的构象式。
解:2,3-二甲基丁烷的典型构象式共有四种:2,2,3,3-四甲基丁烷的典型构象式共有两种:(四) 将下列的投影式改为透视式,透视式改为投影式。
(1)(2)(3)(4)(5)(五)解:它们是CH3-CFCl2的同一种构象——交叉式构象!从下列Newman投影式可以看出:将(I)整体按顺时针方向旋转60º可得到(II),旋转120º可得到(III)。
同理,将(II)整体旋转也可得到(I)、(III),将(III)整体旋转也可得到(I)、(II)。
(六) 解:⑴、⑵、⑶、⑷、⑸是同一化合物:2,3-二甲基-2-氯丁烷;⑹是另一种化合物:2,2-二甲基-3-氯丁烷。
(七) 解:按照题意,甲基环己烷共有6个构象异构体:(A)(B)(C)(D)(E)(F)其中最稳定的是(A)。
共轭二烯烃练习题答案

共轭二烯烃练习题答案共轭二烯烃练习题答案解析共轭二烯烃是有机化学中一类重要的化合物,具有特殊的结构和性质。
在本篇文章中,我们将对共轭二烯烃练习题的答案进行解析,帮助读者更好地理解这一化合物的性质和反应。
首先,我们需要了解什么是共轭二烯烃。
共轭二烯烃是指分子中存在两个相邻的双键,而且这两个双键之间还存在一个或多个单键的有机化合物。
典型的共轭二烯烃有丁二烯、己二烯等。
接下来,我们来看一道共轭二烯烃的练习题:题目:请画出以下共轭二烯烃的结构式,并给出它的IUPAC命名。
1. 1,3-丁二烯2. 2,4-己二烯3. 1,3,5-庚三烯解析:1. 1,3-丁二烯的结构式如下所示:H2C=CH-CH=CH2它的IUPAC命名为:buta-1,3-二烯2. 2,4-己二烯的结构式如下所示:H2C=CH-CH2-CH=CH2它的IUPAC命名为:hexa-2,4-二烯3. 1,3,5-庚三烯的结构式如下所示:H2C=CH-CH2-CH=CH-CH2-CH=CH2它的IUPAC命名为:hepta-1,3,5-三烯通过以上解析,我们可以看出,共轭二烯烃的结构式可以通过在相邻的双键之间添加一个或多个单键来构建。
而IUPAC命名则是根据双键和单键的位置来进行命名的。
除了结构式和IUPAC命名,共轭二烯烃还具有一些特殊的性质和反应。
由于共轭结构的存在,共轭二烯烃具有较好的稳定性和共轭效应,可以参与多种有机反应,如加成反应、环加成反应等。
此外,共轭二烯烃还具有一定的共振稳定性,使其具有较低的能量和较高的反应活性。
综上所述,共轭二烯烃是有机化学中一类重要的化合物,具有特殊的结构和性质。
通过对共轭二烯烃练习题的解析,我们可以更好地理解这一化合物的结构和命名规则,为进一步学习有机化学打下坚实的基础。
高鸿宾《有机化学》(第4版)章节题库题-二烯烃 共轭体系 共振论 (圣才出品)

第4章二烯烃共轭体系共振论1.下列化合物有无顺反异构体?若有,写出其构型式并命名。
(1)1,3-戊二烯(2)2,4,6-辛三烯解:(1)双键C3和C4连有不同的基团,因此存在两种顺反异构体:(2)双键C2和C3、C4和C5、C6和C7连有不同的基团,因此存在八种顺反异构体:2.完成反应。
解:3.4-甲基环己烯在环氧化反应中不显示立体选择性,得到环氧化物,反式稍占优势(反:顺=54:46)。
另一方面,顺-4,5-二甲基环己烯优先地生成反,反-4,5-二甲基环氧化环己烯(反:顺=87:13),试解释之。
解:4-甲基环己烯反应情况如下:整个平衡倾向于左边。
因此反式与顺式产物的比例接近,而反式物略多于顺式产物。
其中.注:(t)代表反式,(c)代表顺式,(a)代表直立键,(e)代表平伏键。
顺-4,5-二甲基环己烯反应情况如下:甲基阻止了环氧化的进行,使大大减小,(反式环氧烷87%),(顺式环氧烷13%),因此优先生成反,反-4,5-二甲基环氧化环己烯。
4.二烯酮A辐射产生三个异构的饱和酮,它们都有环丁烷的环。
请给出合理的结构。
解:5.试述如何从下列亲双烯体或双烯体通过狄-阿(Diels-Alder)反应制得最后合成目标的前体。
再设计一系列反应转化狄-阿加成物至最后产物。
(a)用α-溴化丙烯醛作为亲双烯体制4-亚甲基环己烯。
(b)用α-氯代丙烯腈作亲双烯体制双环酮。
(c)用1-甲氧基-3-三甲基硅氧基丁二烯作为双烯体制4-乙酰基环己-3-烯酮。
(d)用四苯基环戊二烯酮作为双烯体,制2,2′,3,3′,4,4′,5,5′-八苯基联苯。
解:6.下列反应均为周环反应,若反应能发生,请完成反应式,并注明反应类型及反应方式。
解:7.2,5-二甲基-2,4-己二烯的低温光氧化生成一种不稳定加成物,后者在温度比室温稍高的条件下分解至丙酮和4-甲基-2-戊烯醛问此产物的结构。
是否从二烯一般能得到这一类型产物?如果不是,为什么本化合物是不寻常的?解:一般要有烷基取代的烯才能得到这一类产物。
二烯烃和共轭体系习题

第四章 二烯烃和共轭体系 例题例一 写出下列化合物、离子或自由基的共振结构式,并指出其中哪一个极限结构式贡献最大。
答:(1)为正离子,电子离域的方向是向着碳正离子方向,而且是π电子转移,即三个极限结构式的贡献基本相同。
(2)是负离子,电子离域的方向是有带负电荷的碳原子转向其它原子,即最后一个极限结构的贡献最大,因为它的负电荷在氧原子上,遵循了电负性原则且具有完整的芳香性苯环。
(3)是自由基,其共振结构如下:三个极限结构的贡献相同。
(4)是化合物,其共振结构如下:第一个极限结构的共价键最多,且没有电荷分离,因此最稳定,对共振杂化体的贡献最大。
例二 解释下列现象,下列现象说明什么问题?(1)不同的1-取代的1,3-丁二烯与顺丁烯二酸酐反应的相对活性不同:(2)反-1,3-戊二烯与四氰基乙烯的反应活性比4-甲基-1,3-戊二烯大103倍。
(3)2-叔丁基-1,3-丁二烯与顺丁烯二酸酐反应的速率比反应活性比1,3-丁二烯大快27倍。
答:(1)1,3-丁二烯的1位有烷基时,由于烷基供电的结果,一般使反应速率略有增加。
但当烷基时叔丁基时,由于叔丁基体积较大,阻碍了它与顺丁烯二酸酐的接近,使反应不易进行。
即叔丁基空间效应的影响远大于其电子效应的影响。
(2)已知双烯体在进行反应时需要采取s-顺式构象,两个化合物的s-顺式构象如下:在4-甲基-1,3-戊二烯分子的s-顺式构象中,处于内侧的4位甲基与1位氢原子之间的非键张力不利于该分子采取s-顺式构象,因此反应活性降低。
(3) 在2-叔丁基-1,3-丁二烯分子中,2位叔丁基的存在使s-顺式构象比s-反式构象更稳定而更容易形成,因此有利于反应的进行。
以上事实说明,立体效应对双烯合成也具有重要影响,其影响表现在两方面:①在双烯端位有取代基时,阻碍双烯体与亲双烯体相互接近,使反应速率减慢;②双烯体分子内的取代基,由于空间效应的影响,若不利于过渡态采取s-顺式构象时,则反应较难进行,甚至不能发生。
2020全国高中生化学竞赛—有机化学—二烯烃和共轭体系4007_共轭二烯烃的1,4-加成反应[共7页]
![2020全国高中生化学竞赛—有机化学—二烯烃和共轭体系4007_共轭二烯烃的1,4-加成反应[共7页]](https://img.taocdn.com/s3/m/e52df3ac5ef7ba0d4b733b04.png)
H
δ+
δ+
CH2 CH CH CH2
碳正离子(I)为仲碳正离子,且是烯丙位正离子;(II) 为伯碳正离子。 (I)比(II)稳定。
第二步
H
δ+
δ+
CH2 CH CH CH2
H CH2 CH CH CH2
Br–
Br H
CH2 CH CH CH2
1,2–加成
H
Br– Br
H
CH2 CH CH CH2
CH2 CH CH CH2
1,4–加成
1,2−加成与1,4−加成势能图
反应活化能 产物稳定性
能量
ΔG1,2
ΔG1,4
δ+
δ+ H
CH2 CH CH2 CH2
CH2 CH CH CH2
1,4 1,2
Br-
H Br
反应进程
ΔG1,2 逆
Br H
CH2 CH CH CH2
Br
H
CH2 CH CH CH2
CH2 CH CH CH2 + CH2 CH CH CH2
Br Br Br
Br
正己烷
62%
38%
氯仿
37%
63%
温度的影响
CH2 CH CH CH2 Cl2
CH2 CH CH CH2 + CH2 CH CH CH2
Cl Cl Cl
Cl
~25°C
60%
40%
~200°C
30%
70%
一般低温有利于 1,2-加成, 温度升高有利于 1,4-加成
CH2 CH CH CH2
HBr CH2 CH CH CH2 + CH2 CH CH CH2
共轭二烯烃练习题答案

共轭二烯烃练习题答案共轭二烯烃练习题答案共轭二烯烃是有机化学中的一个重要概念,它指的是分子中存在着两个或多个相邻的双键,这些双键通过共轭系统相连。
共轭二烯烃具有许多特殊的性质和反应,因此在有机化学的学习中占据着重要的地位。
下面将针对一些常见的共轭二烯烃练习题进行解答,帮助大家更好地理解和掌握这一知识点。
1. 以下哪个分子是共轭二烯烃?A. 乙烯B. 丙烯C. 丁二烯D. 丁烯答案:C. 丁二烯解析:共轭二烯烃要求分子中存在相邻的双键,并且这些双键通过共轭系统相连。
在选项中,只有丁二烯符合这一要求,因此答案为C。
2. 以下哪个分子不是共轭二烯烃?A. 戊二烯B. 己二烯C. 辛二烯D. 丙烯答案:D. 丙烯解析:共轭二烯烃要求分子中存在相邻的双键,并且这些双键通过共轭系统相连。
在选项中,只有丙烯不满足这一要求,因为丙烯只有一个双键,而且没有其他的双键与之相连。
3. 共轭二烯烃的π电子数是多少?A. nB. 2nC. 4nD. 6n答案:C. 4n解析:共轭二烯烃的π电子数等于每个双键上的π电子数之和。
对于每个双键来说,有两个π电子,因此共轭二烯烃的π电子数是双键数的两倍,即4n。
4. 下列哪个分子具有最强的共轭效应?A. 丁二烯B. 戊二烯C. 己二烯D. 辛二烯答案:D. 辛二烯解析:共轭效应是指共轭系统中π电子的扩散和共享,从而使分子具有特殊的稳定性和反应性。
共轭效应的强弱取决于共轭系统的长度和结构。
在选项中,辛二烯具有最长的共轭系统,因此共轭效应最强。
5. 以下哪个分子是共轭二烯烃的异构体?A. 丁二烯B. 戊二烯C. 戊烯D. 辛二烯答案:C. 戊烯解析:异构体是指分子具有相同的分子式但结构不同的化合物。
在选项中,戊烯和戊二烯具有相同的分子式C5H8,但结构不同。
戊烯只有一个双键,不满足共轭二烯烃的要求,因此是共轭二烯烃的异构体。
通过以上练习题的解答,我们对共轭二烯烃的概念、性质和特点有了更深入的了解。
二烯烃与共轭体系
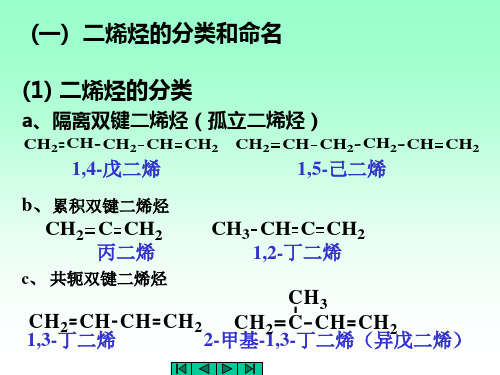
O
O
100 oC
+
O 苯
O
95%
O
O
顺丁烯二酸酐 顺 - 4- 四氢化邻苯二甲酸酐
CHO 115 oC, 2~4 h
+
甲苯
丙炔醛
双烯体 亲双烯体
CHO 82%
1,4 - 环己二烯甲醛
双烯体含有供电基和亲双烯体具有吸电基时利于反应。
双烯体均以 s-顺式参加反应,如不能形成 s-顺式,
则反应不能进行。
(2)二烯烃的命名(标明每个双键位置和顺反关系)
CH3 CH CH CH2 CH CH2 1,4-己二烯
CH2 C CH CH2 CH3 1,2-戊二烯
CH3CH3 CH2 C C CH2
2,3-二甲基-1,3-丁二烯
H
CH3
C
CC
H
H
H
C CH3
顺,顺-2,4-己二烯 或(Z,Z)-2,4-己二烯
(20%)
(20%)
CH2 CH CH CH3 Br
(80%)
25 oC
(60%)
(40%)
CH2 CH CH CH2 + Cl2
200oC
(2) 电环化反应
CH2 CH CH CH2 + CH2 CH CH CH2
Cl Cl Cl
Cl
(30%)
(70%)
光(或热)
1,3-丁二烯
环状过渡态
环丁烯
(3)双烯合成, 亦称 Diels-Alder 反应
这个能量差值是共轭效应的具体表现,通称离域能 或共轭能。
由π电子离域所体现的共轭效应,称为π,π-共 轭效应。
共轭效应产生的条件: (1)构成共轭体系的原子必须在同一平面内。 (2)p轨道的对称轴垂直与该平面。
二烯烃,共轭体系

一二烯烃分子中含有不止一个双键的开链烃,按照双键数目的多少,分别叫做二烯烃,三烯烃.....至多烯烃等。
其中以二烯烃最为重要。
而根据二烯烃中双键位置的不同,又可以分为三类:a 累积二烯烃:两个双键连接在同一个碳原子上。
B 共轭二烯烃:两个双键之间,有一个单键相隔。
C 隔离二烯烃:两个双键之间,有两个或以上的单键相隔。
在这里主要介绍共轭二烯烃的性质。
1共轭二烯烃的结构以及共轭效应:1,3—丁二烯是最简单的共轭二烯烃,下面就以它为例来说明共轭二烯烃的结构。
在丁二烯分子中,四个碳原子和六个氢原子都处在同一个平面上。
其每一个碳原子都是sp2杂化,它们以sp2杂化轨道与相邻的碳原子相互交盖形成碳碳单键,与氢原子的1S轨道形成碳氢单键。
分子中一共形成了三个碳碳单键和六个碳氢单键,sp2杂化碳原子的三个σ键指向三角形的三个顶点,三个σ键相互之间的夹角都接近120°。
由于每一个碳原子的σ键都排列在一个平面上,所以就形成了分子中所有σ键都在一个平面的结构,此外,每一个碳原子都有一个未参与杂化的p轨道,它们都和丁二烯分子所在的平面垂直,因此这四个p轨道互相平行,在四个碳原子之间都有电子云交盖,从而电子也并不固定在两个原子之间,从而发生离域。
也就是说四个电子在四个原子轨道形成的共轭体系中流动,并不固定在某一位置。
2 共轭二烯烃的性质A 1,2—加成和1,4—加成共轭二烯烃和卤素,氢卤酸等都容易发生亲电加成,但可产生两种加成产物,如下所示:(1,2—加成产物和1,4—加成产物的键线式)1,2—加成产物是一分子试剂在同一个双键的两个碳原子上的加成,而1,4—加成产物则是一分子试剂加载共轭双键的两端碳原子上,同时原来的双键变为单键,而双键之间的单间变为双键。
1,3—丁二烯之所以有这两种加成方式,与其共轭结构有密切关系。
下面以溴化氢与丁二烯的加成来说明这一原理。
丁二烯与溴化氢的加成第一步也是H+的进攻,加成反应可能发生在C(1)或者C(2)上,然后生成相应的碳正离子(I)和(II)对于这两种碳正离子来说,双键上的碳原子,以及带有正电荷(在键线式中所表达出来的)的碳原子都是sp2杂化,而在(I)碳正离子中,三个碳原子剩余的p轨道均平行于三个碳原子锁组成的平面,因此它们之间存在共轭效应,从而正电荷并不只是单纯的聚集在同一个碳原子上,电荷因共轭效应而被分配到三个碳原子上,并且在C(2)和C(4)上的正电荷相对较多,从而分子比较稳定,生成(I)碳正离子所需要的活化能相对更低,而(II)碳正离子则没有共轭效应,因此反应总是向着(I)碳正离子的方向进行。
第四章 二烯烃和共轭体系

有机化学
主讲教师:
佟拉嘎
北京石油化工学院
第四章 二烯烃和共轭体系 (4学时)
Ⅱ Ⅰ为仲碳正离子,Ⅱ为伯碳正离子。 Ⅰ中存在 如下p-π共轭效应, Ⅱ中不存在。故Ⅰ比Ⅱ稳 定。
1,2-加 成 + H 2C C H + C CH3 H Br1,4-加 成 H 2C C H Br H 2C C H
H C
CH3
Br C CH3 H
1,2-加成为动力学控制产物; 1,4-加成为热力学控制产物;
★p,π-共轭
• π轨道与相邻原子的 p轨道组成的共轭体系;
H2C C CH2 H
H2C
C H
CH2
存在p,π-共轭的分子举例:
H2C C CH2 H H2C C CH2+ H H2C C CH2H
H 2C
C Cl H
H 2C
C O R H
★超共轭
• 超共轭效应:涉及到C-Hσ键与相邻π键参 与的电子离域效应。也称σ,π-共轭效应。 存在这种效应的体系称为超共轭体系。 *超共轭效应比π,π-共轭效应和p,π-共轭效 应弱得多。
氯菌酸酐
+ COOCH3
H COOCH3
二环[2,2,1]-5-庚烯-2-羧酸甲酯
+
二环[2,2,1]-2,5-庚二烯
(2)加氢
+ H2
Pd-Ti 50 ℃
(3)α-氢原子反应
3.3-二烯烃和共轭体系

17
18
6. 共振论
共振论代表价键理论的一种引伸,它用来处 理能画出不止一个刘易斯结构的分子。 • 当用一个经典的结构式不能反映分子的真实 结构时,可采用含几个相关经典结构的共振 杂化体来描述。共振杂化体中每一个经典结 构式叫共振式(极限式, 共振结构)。
19
• Pauling指出:这些共振结构本身可能是不 存在的,共振论是用假设的价键结构去近 似地描绘真实物质结构的理论。
共振规则
• 共振杂化体是关于含有非定域键的分子的真实结 构的一种表示法,是画出数个可能结构,并假定 真实分子为它们的共振杂化体。 • 这些极限式是不存在的仅存在于纸面上,它们是 人们的设想。分子不是在它们之间的迅速转变, 也不是某些分子具有一个极限式,而另外一些分 子具有另一个极限式。
• 物质的全部分子具有相同的结构,这个结构在所 有时间都是一样的,并且为所有极限式的加权平 均值。
2. 二烯烃的命名 a. 选含两个双键的最长碳链为主链;
b. 从靠近双键的一端开始编号,双键位置和最小;
c. 写出名称,每个双键的位置都需要标明; d. 有顺反异构者,需标明。
2
H3C
CH CH3
CH
C
CH2
H2C
CH
CH2
C CH3
CH
CH3
CH2CH3
4-甲基-2-乙基-1,3-戊二烯
H3C H H CH3 H H
叫做超共轭。还有丙炔、甲苯等。 CH3C H2 超共轭体系 σ-P共轭体系:CH3C H2 σ ,π - 和σ , p -超共轭体系的共同特点是:参与超 共轭的C―H σ越多,超共轭效应越强。
14
5.2 共轭效应
由于形成共轭π键而引起的分子性质的改变。
第四章_二烯烃和共轭体系

在1,3-丁二烯分子中,两个双键还可以在碳碳(C2和 C3 之 间 ) 单 键 的 同 侧 和 异 侧 存 在 两 种 不 同 的 空 间 排 布 , 但 由 于 C2 和 C3 之 间 的 单 键 在 室 温 仍 可 以 自 由 旋 转 。 因此,这两种不同的空间排布,只是两种不同的构象,而
不 是 构 型 的 不 同 , 分 别 称 为 s- 顺 式 和 s- 反 式 [ s 指 单 键 (singlebond)],或以s-(Z)和s-(E)表示。
极性溶剂有利于1,4-加成
反应温度的影响也是明显的,一般低温有
利于1,2-加成,温度升高有利于1,4-加成。 例如:
4.4.2 共轭二烯烃1,4-加成的理论解释
共轭二烯烃能够进行1,4-加成可利用共轭效应进行 解释。例如,1,3-丁二烯与极性试剂溴化氢的亲电加成 反应,当溴化氢进攻1,3-丁二烯的一端时,1,3-丁二 烯不仅一个双键发生极化,而且整个共轭体系的电子云 发生变形,形成交替偶极。
第四章 二烯烃 共轭体系
主要内容
4.1 二烯烃的分类与命名 4.2 二烯烃的结构 4.3 电子离域与共轭体系 4.4 共轭二烯烃的化学性质
本章重点
共轭二烯烃 共轭体系与共轭效应
电子离域 1,4加成 电环化反应 周环反应 Diels-Alder反应 (双烯加成)
本章难点
1,3丁二烯分子轨道 共轭体系与共轭效应
H2C=CH CH=CH2
在共轭分子中,任何一个原子受到外界的影 响,由于π电子在整个体系中的离域,均会影响 到分子的其余部分,这种电子通过共轭体系传递 的现象,称为共轭效应。 由π电子离域所体现的共轭效应,称为π,π-共轭效应。
4个π电子扩展到四个碳原子之间:电子的离域
《有机化学》(第四版)第四章 二烯烃和共轭体系(习题答案)

第四章二烯烃和共轭体系思考题习题4.1 下列化合物有无顺反异构体?若有,写出其构型式并命名。
(P119)(1) 1,3-戊二烯解:有2个顺反异构体!(Z)- 1,3-戊二烯 (E)- 1,3-戊二烯(2) 2,4,6-辛三烯解:有6个顺反异构体!(Z,Z,Z)- 2,4,6-辛三烯(Z,Z,E)- 2,4,6-辛三烯(E,Z,E)- 2,4,6-辛三烯(E,E,E)- 2,4,6-辛三烯(E,E,Z)- 2,4,6-辛三烯 (Z,E,Z)- 2,4,6-辛三烯习题4.2 下列各组化合物或碳正离子或自由基哪个较稳定?为什么?(P126)(1) 3-甲基-2,5-庚二烯和 5-甲基-2,4-庚二烯√(2)(3)(4) (5)(6)习题4.3 解释下列事实:(P126)(1)(2)(3)习题4.4 什么是极限结构?什么是共振杂化体?一个化合物可以写出的极限结构式增多标志着什么?(P130)解:极限结构——对真实结构有贡献,但不能完全代表真实结构的经典结构式;共振杂化体——由若干个极限结构式表示的该化合物的真实结构。
一个化合物可以写出的极限结构式增多标志着该化合物稳定性增加。
习题4.5 写出下列化合物或离子可能的极限结构式,并指出哪个贡献最大。
(P130)(1)(2)(3)习题4.6 指出下列各对化合物或离子是否互为极限结构。
(P130)(1) (原子核有位移,不符合共振条件)(2) (原子核有位移,不符合共振条件)(3) (原子核有位移,不符合共振条件)(4)(原子核无位移,只是电子发生转移,符合共振条件)习题4.7 完成下列反应式,并说明理由。
(P132)(1)(低温下,动力学产物为主要产物,即以1,2-加成为主。
)(2)(较高温度下,以1,4-加成为主,形成更加稳定的热力学产物。
)(3)(较高温度下,形成更加稳定的热力学产物。
而1,6-加成的产物共轭程度更高,更加稳定。
)习题4.8 试判断下列反应的结果,并说明原因。
《二烯烃和共轭体系》习题及答案

《二烯烃和共轭体系》习题及答案(一)用系统命名法命名下列化合物:CH 2CHCH C(CH 3)2(1)(2)CH 3CH CC(CH 3)2(3)H 2CCHCH CHCCH 2CH 3(4)C CHCH 3CHCH 2【解答】(1)4-甲基-1,3-戊二烯 (2)2-甲基-2,3-戊二烯(3)2-甲基-1,3,5-己三烯 (4)顺 (或3Z )-1,3-戊二烯(二)下列化合物有无顺反异构现象?若有,写出其顺反异构体并用Z, E-标记法命名。
(1)2-甲基-1, 3-丁二烯 (2)1, 3-戊二烯 (3)3, 5-辛二烯 (4)1, 3, 5-己三烯 (5)2, 3-戊二烯 【解答】(1)和(5)无顺反异构;(2)有;(3E)-1,3-戊二烯,(3Z)-1,3-戊二烯; (3)(3Z, 5Z)-3,5-辛二烯,(3E, 5E)-3,5-辛二烯,(3Z, 5E)-3,5-辛二烯; (4)有,(3E)- 1,3,5-己三烯,(3Z)- 1,3,5-己三烯(三)完成下列反应式:HO 2CCH CHCO2H(1)(2)HCHC(3)CO 2CH 3CO 2CH3HH(4)CO 2CH 3HHH 3CO 2C(5)(6)(7)(8)+RMgX++CHO (A)Br 2(B)+CH 2Cl (B)(9)(10)【解答】COOHCOOH(1 )(2 )(3 )3333(4 )(5) ,(6),(7)(A )(B )(8)(A )(B )(9),(10)(四)给出下列化合物或离子的极限结构式,并指出哪个贡献大。
(1),(2),(3),(4)(5),(6)【解答】(1),第一个贡献大。
CH 3CH 3hvH 3H 333O CHOBrBr CH 2ClHO 2CCH 2CHCH 2CH 2COOHCH 2ClH CH 3H3HCH 3CH 3H 3C H 3CH+(CH 3)2C=CH-C(CH 3)2CH 2=CH-CH 3--(2),两者贡献相同。
《有机化学》(第四版)第四章-二烯烃和共轭体系(习题答案)

第四章 二烯烃和共轭体系思考题习题4.1 下列化合物有无顺反异构体?若有,写出其构型式并命名。
(P119)(1) 1,3-戊二烯 CH 2=CH CH=CHCH 3解:有2个顺反异构体!C=CCH 3HCH 2=CHHC=CH CH 3CH 2=CHH(Z)- 1,3-戊二烯 (E)- 1,3-戊二烯(2) 2,4,6-辛三烯 CH 3CH=CH CH=CH CH=CHCH 3 解:有6个顺反异构体!C=C C=CHC=C HH CH 3H H CH 3HC=C C=CHC=C HCH 3HH H CH 3HC=CC=C H C=CHCH 3HCH 3H HH(Z,Z,Z)- 2,4,6-辛三烯 (Z,Z,E)- 2,4,6-辛三烯 (E,Z,E)- 2,4,6-辛三烯C=CC=C C=C HHHH CH 3CH 3H HC=CC=CC=C H HCH 3HHH HCH 3C=CC=C C=C HHCH 3H HCH 3H H(E,E,E)- 2,4,6-辛三烯 (E,E,Z)- 2,4,6-辛三烯 (Z,E,Z)- 2,4,6-辛三烯习题4.2 下列各组化合物或碳正离子或自由基哪个较稳定?为什么?(P126)(1) 3-甲基-2,5-庚二烯 和 5-甲基-2,4-庚二烯√CH 3CH=CCH 2CH=CHCH 3CH 3CH 3CH=CHCH=CCH 2CH 3CH 3π-π共轭无π-π共轭有(2)(CH 3)2C=CHCH 2CH 3CH=CHCH 2CH 2=CHCH 2、和(CH 3)2C=CHCH 2CH 3CH=CHCH 2CH 2=CHCH 26个超共轭σ-H 3个超共轭σ-H 0个超共轭σ-H 稳定性:>>(3)(CH 3)2CHCHCH=CH 2(CH 3)2CCH 2CH=CH 2(CH 3)2CCH 2CH 3、和(CH 3)2CHCHCH=CH 2(CH 3)2CCH 2CH=CH 2(CH 3)2CCH 2CH 3稳定性:>>有p -π共轭p -π共轭无p -π共轭无给电子性:CH 3CH=CH 2>(4)、和CH 2CH=CHCH=CH 2CH 2CH=CHCH 2CH 3CH 3CHCH 2CH=CH 2稳定性:>>有π-π共轭CH 2CH=CHCH=CH 2CH 2CH=CHCH 2CH 3CH 3CHCH 2CH=CH 2p -π有共轭π-π无共轭π-π无共轭p -π有共轭p -π共轭无 (5)CH 3 , (CH 3)2CHCH 2 , CH 3CHCH 2CH 3 和 (CH 3)3C甲基自由基 一级自由基 二级自由基 三级自由基(6)(CH 2CH=CH)2CH , CH 2=CHCH 2 和 CH 3CH=CH5个sp 2杂化碳共轭 3个sp 2杂化碳共轭 成单电子不在p 轨道上,不参与共轭共轭程度更大共轭程度相对较小习题4.3 解释下列事实:(P126)(1)CH 3CH 2CH=CHCH 3CH 3CH 2CH 2CHCH 3Cl CH 3CH 2CHCH 2CH 3ClHCl+(主)(次)稳定性:>CH 3CH 2CHCH 2CH 3CH 3CH 2CH 2CHCH 3(2)CH 3CH=CCH 3CH 3CH 3CH 2CCH 3CH 3ClCH 3CHCHCH 3CH 3Cl+HCl(主)(次)稳定性:>CH 3CH 2CCH 3CH 3CH 3CHCHCH 3CH 3(3)+HBr , 过氧化苯甲酰-78 Co(96%)(4%)CH 3CH=CH 2CH 3CH 2CH 2Br CH 3CHCH 3Br>稳定性:CH 3CHCH 2Br CH 3CHCH 2BrCH 3CH=CH 2CH 3CHCH 2Br CH 3CHCH 2BrPhCOOH + BrPhCOOBr+(过氧化苯甲酰)2PhCOOPhCO OCPh O O机理:... ...习题4.4 什么是极限结构?什么是共振杂化体?一个化合物可以写出的极限结构式增多标志着什么?(P130)解:极限结构——对真实结构有贡献,但不能完全代表真实结构的经典结构式;共振杂化体——由若干个极限结构式表示的该化合物的真实结构。
4第四章__二烯烃_共轭体系_共振论(3学时)

杂化体
虚线表示负电荷离域,虚线、实线共同表示 键键长。 虚线表示负电荷离域,虚线、实线共同表示C-O键键长。 键键长
25
4.4 共振论
每个极限结构代表电子离域的限度。 每个极限结构代表电子离域的限度。一个分子的极限结构式 越多,电子离域的可能性越大,体系的能量也越低, 越多,电子离域的可能性越大,体系的能量也越低,分子越 稳定。 稳定。 能量最低的极限结构与共振杂化体之间的能量差,称为共振 能量最低的极限结构与共振杂化体之间的能量差,称为共振 能,其等于离域能或共轭能
19
H
C
C H
CH2
4.3.3 超共轭
4.3 电子离域与共轭体系
电子离域不仅存在于单双键交替的π 共轭体系, 键与π 电子离域不仅存在于单双键交替的π,π-共轭体系, 在σ 键与π 共轭体系 键相连的体系中,也存在类似的电子离域现象。 键相连的体系中,也存在类似的电子离域现象。
H
R H C
C
+
H H
预计与实测数值相差不大, 预计与实测数值相差不大,说明孤立烯烃与一般 烯烃的稳定性相差不大。 烯烃的稳定性相差不大。
10
4.2 1,3-丁二烯的结构 丁二烯的结构
CH3CH2CH CH2 CH2 CH CH CH2
1 -丁烯 1 ,3 -丁二烯
氢化热:126 .8 kJ /mol 氢化热: 预计:126 .8×2=253.6 kJ/mol 实测:238.9 kJ/mol
15
4.3.1 π,π-共轭 共轭
1,3-丁二烯单双键交替排列形成共轭体系 丁二烯单双键交替排列形成共轭体系 丁二烯单双键交替排列形成 四个碳原子均为sp 四个碳原子均为 2杂化
4.3 电子离域与共轭体系
第4章 二烯烃和共轭体系

CH2
极性分子
以 1,3- 丁二烯与极性试剂溴化氢的亲电加成反应为例。
δ CH2
+
δ CH
δ CH
+
+ δ δ CH2 + H
δ Br
第一步:
CH2 CH CH CH2 H
+
CH2
CH2
CH
CH
CH
+
CH3
+
(Ⅰ)
(Ⅱ)
CH2 CH2
仲碳正离子(Ⅰ)比伯碳正离子 (Ⅱ)稳定, 因此 反应通常按生成碳正离子(Ⅰ)的途径进行。
当一个分子、离子或自由基的结构可用一个以上不同电子排
列的经典结构式(共振式)表达时,就存在着共振。这些共振式
均不是这一分子、离子或自由基的真实结构,其真实结构为所有 共振式的杂化体。
提示: 共振式之间只是电 子排列不同
共振杂化体不是共 振式混合物
共振杂化体也不是 互变平衡体系
关于共振论的几点说明:
如: 1,3-丁二烯,丙烯醛, 丙烯腈 超共轭( , π):甲基被视为部分失去一个质子, 可以和一个相邻的π键共轭 p, π 共轭: 一个π键和一个碳的P轨道紧邻, 中间无
饱和碳隔开.
, p共轭:CH3CH2+ , CH3CH2·
1
2
3 4
1. π, π 共轭;
2,3. p, π 共轭;
4. 超共轭
(20%)
(80%)
25 C CH2 CH CH CH2 + Cl2 200oC
o
(60%)
(40%)
CH2 CH CH CH2 + CH2 CH CH CH2 Cl Cl Cl Cl
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
矿产资源开发利用方案编写内容要求及审查大纲
矿产资源开发利用方案编写内容要求及《矿产资源开发利用方案》审查大纲一、概述
㈠矿区位置、隶属关系和企业性质。
如为改扩建矿山, 应说明矿山现状、
特点及存在的主要问题。
㈡编制依据
(1简述项目前期工作进展情况及与有关方面对项目的意向性协议情况。
(2 列出开发利用方案编制所依据的主要基础性资料的名称。
如经储量管理部门认定的矿区地质勘探报告、选矿试验报告、加工利用试验报告、工程地质初评资料、矿区水文资料和供水资料等。
对改、扩建矿山应有生产实际资料, 如矿山总平面现状图、矿床开拓系统图、采场现状图和主要采选设备清单等。
二、矿产品需求现状和预测
㈠该矿产在国内需求情况和市场供应情况
1、矿产品现状及加工利用趋向。
2、国内近、远期的需求量及主要销向预测。
㈡产品价格分析
1、国内矿产品价格现状。
2、矿产品价格稳定性及变化趋势。
三、矿产资源概况
㈠矿区总体概况
1、矿区总体规划情况。
2、矿区矿产资源概况。
3、该设计与矿区总体开发的关系。
㈡该设计项目的资源概况
1、矿床地质及构造特征。
2、矿床开采技术条件及水文地质条件。
