硫化物的溶解性归纳
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
硫化物的溶解性归纳
氢硫酸可形成正盐和酸式盐,酸式盐均易溶于水,而正盐中除碱金属(包
括NH4+)的硫化物和BaS易溶于水外,碱土金属硫化物微溶于水(BeS 难溶),其它硫化物大多难溶于水,并具有特征的颜色。大多数金属硫化物难溶于水。从结构方面来看,S2-的半径比较大,因此变形性较大,在与重金属离子结合时,由于离子相互极化作用,使这些金属硫化
物中的M—S键显共价性,造成此类硫化物难溶于水。显然,金属离子的极化作用越强,其硫化物溶解度越小。根据硫化物在酸中的溶解情况,将其分为四类。
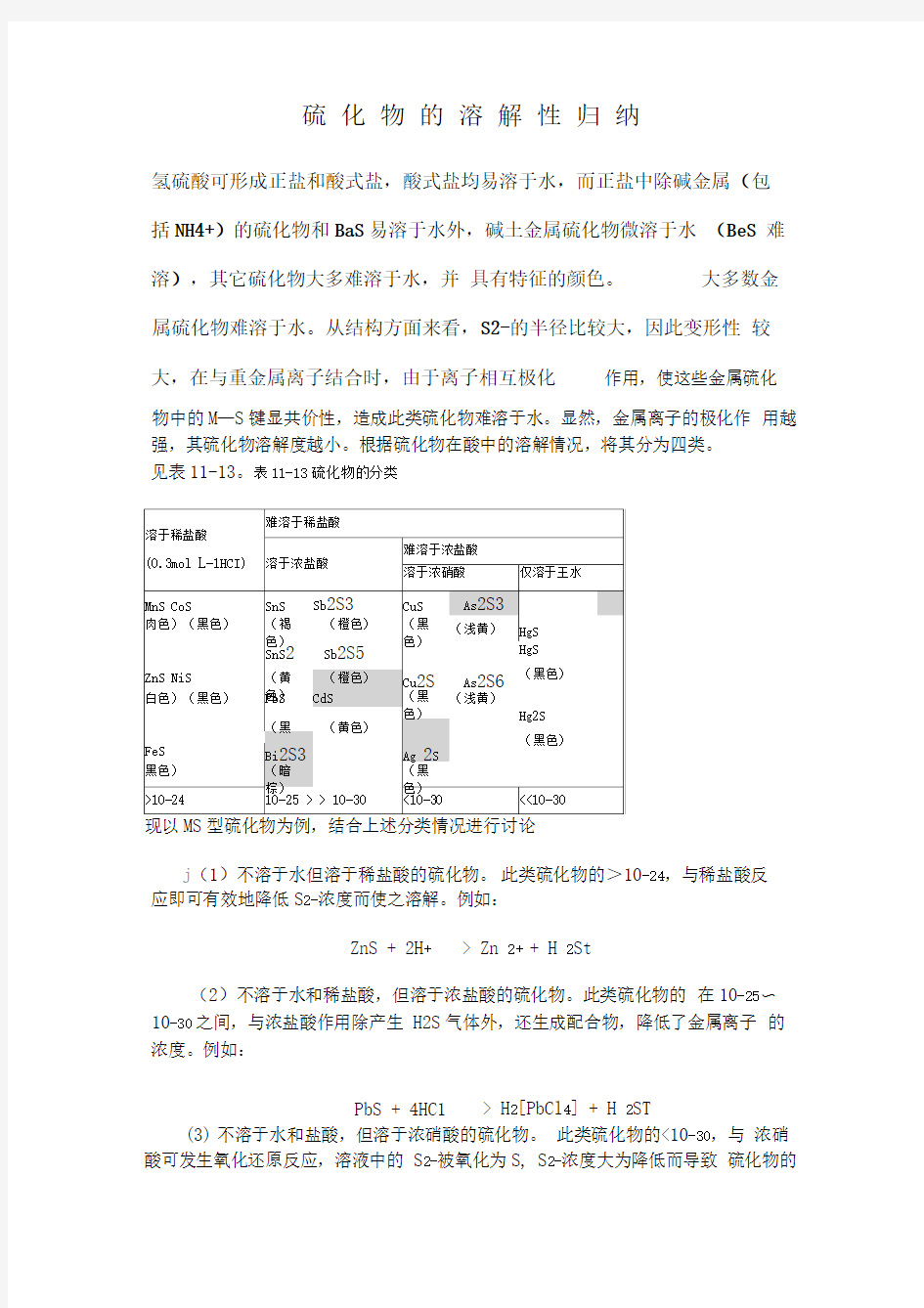
见表11-13。表11-13硫化物的分类
现以MS型硫化物为例,结合上述分类情况进行讨论
j(1)不溶于水但溶于稀盐酸的硫化物。此类硫化物的>10-24,与稀盐酸反
应即可有效地降低S2-浓度而使之溶解。例如:
ZnS + 2H+ > Zn 2+ + H 2S t
(2)不溶于水和稀盐酸,但溶于浓盐酸的硫化物。此类硫化物的在10-25〜10-30之间,与浓盐酸作用除产生H2S气体外,还生成配合物,降低了金属离子的浓度。例如:
PbS + 4HC1 > H2[PbCl4] + H 2S T
(3)不溶于水和盐酸,但溶于浓硝酸的硫化物。此类硫化物的<10-30,与浓硝酸可发生氧化还原反应,溶液中的S2-被氧化为S, S2-浓度大为降低而导致硫化物的
溶解。例如:
3CuS + 8HN(3 > 3Cu(NO3) 2 + 3S ;+ 2NOT + 4H 2O
(4)仅溶于王水的硫化物。对于更小的硫化物如HgS来说,必须用王水才能溶解。因为王水不仅能使S2-氧化,还能使Hg2+与Cl-结合,从而使硫化物溶解。反应如下:
3HgS + 2HNO + 12HC1 > 3H2[HgCl4] + 3S J + 2NOT +
4H2O
由于氢硫酸是弱酸,故硫化物都有不同程度的水解性。碱金属硫化物,例如Na2S溶于水,因水解而使溶液呈碱性。工业上常用价格便宜的Na2S代替NaOH 作为碱使用,故硫化钠俗称“硫化碱”。其水解反应式如下:
S2- + H 2O HS + OH-
碱土金属硫化物遇水也会发生水解,例如:
2CaS + 2H2O Ca(HS)2 + Ca(OH) 2
某些氧化数较高金属的硫化物如AI2S3、Cr2S3等遇水发生完全水解:
Al 2S3 + 6H 2O > 2AI(OH) 3;+ 3H 2S t
Cr2S3 + 6H 2O > 2Cr(OH) 3;+ 3H 2S t
因此这些金属硫化物在水溶液中是不存在的。制备这些硫化物必须用干法,如用
金属铝粉和硫粉直接化合生成AI2S3。
可溶性硫化物可用作还原剂,制造硫化染料、脱毛剂、农药和鞣革,也用于制荧光粉。
判断金属硫化物的溶解性
(1) 3 Na的金属硫化物易溶于水。
(2)Mg^Al的金属硫化物易水解,在水中不存在。
(3)Zn^ Pb的金属硫化物均不溶于水。
16判断金属硫化物的颜色
(1) 3Zn的金属硫化物为无色或白色。
(2) Fe以后的金属硫化物均为黑色。
