直肠癌诊疗指南
NCCN指南解读:直肠癌NCCN指南

NCCN指南解读:直肠癌NCCN指南NCCN指南解读:直肠癌NCCN指南在临床医学领域,NCCN(National Comprehensive Cancer Network)指南发挥着至关重要的作用,为医生和患者提供了有关各种癌症诊断和治疗的一致、全面的信息。
其中,直肠癌NCCN指南为医生和患者提供了有关该疾病的最新治疗信息和指导。
本文将对NCCN直肠癌指南进行解读,探讨其在直肠癌诊疗中的应用及其对患者治疗的指导意义。
NCCN指南是一个针对各种癌症的全面指南,包括直肠癌、乳腺癌、肺癌等多种类型。
该指南旨在提供医生在治疗各种癌症时所需的信息和指导,以便为患者提供最佳的治疗方案。
直肠癌NCCN指南包括多种治疗选项,如手术、放疗、化疗和免疫治疗等,根据患者的具体情况提供相应的推荐。
直肠癌NCCN指南在直肠癌的诊疗中具有重要指导意义。
首先,该指南为医生提供了基于最新证据的治疗选择,以确保患者接受最佳的治疗方案。
其次,指南还考虑到了患者的个人情况,包括年龄、健康状况、偏好等因素,为医生制定个性化的治疗计划提供了参考。
此外,NCCN指南还为患者提供了关于疾病管理、生活质量等方面的信息,帮助他们更好地应对疾病。
为了进一步说明NCCN指南在直肠癌诊疗中的应用,我们来看几个具体的案例。
例如,在一个案例中,一位年轻女性被诊断为早期直肠癌。
在接受了NCCN指南推荐的手术后,她很快恢复了健康,并按照指南的建议进行了后续的放疗和化疗。
由于遵循了NCCN指南的建议,她的治疗效果得到了保证,并且她在治疗过程中获得了良好的生活质量。
另一个案例是一位老年患者,他在被诊断为晚期直肠癌后,接受了NCCN指南推荐的化疗和免疫治疗。
尽管他的病情较为复杂,但由于遵循了指南的建议,他获得了显著的临床缓解,并且生活质量也得到了显著改善。
通过这些案例,我们可以看到NCCN直肠癌指南在临床实践中的实际应用及其效果。
它为医生和患者提供了清晰、实用的治疗指导,有助于确保患者获得最佳的治疗效果和生活质量。
直肠癌规范化诊疗指南

直肠癌规范化诊疗指南(试行)1 范围本指南规定了直肠癌的规范化诊治流程、诊断依据、诊断和鉴别诊断、治疗原则及治疗方案。
本指南适用于农村重大疾病医疗保障工作定点医院对直肠癌的诊断和治疗。
2 术语和定义下列术语和定义适用于本指南。
直肠系膜:指的是在中下段直肠的后方和两侧包裹着的,形成半圆,厚1.5~2.0cm的结缔组织,内含有动脉、静脉、淋巴组织及大量脂肪组织,上自第3骶椎前方,下达盆膈。
3 缩略语下列缩略语适用于本指南。
3.1 TME:(total mesorectal excision)全直肠系膜切除术3.2 CEA:(carcinoembryonic antigen)癌胚抗原4 诊治流程图5 诊断依据5.1 病因直肠癌的发病原因尚未完全阐明,导致发生的原因可归纳为:5.1.1 环境因素饮食习惯、肠道细菌、化学致癌物质、土壤中缺钼和硒。
5.1.2 内在因素基因变异、腺瘤、血吸虫性结肠炎、慢性溃疡性结肠炎。
5.2 高危人群5.2.1 有便血、便频、大便带粘液、腹痛等肠道症状的人。
5.2.2 大肠癌高发区的中、老年人。
5.2.3 大肠腺瘤患者。
5.2.4 有大肠癌病史者。
5.2.5 大肠癌患者的家庭成员。
5.2.6 家族性大肠腺瘤病患者。
5.2.7 溃疡性结肠炎患者。
5.2.8 Crohn病患者。
5.2.9 有盆腔放射治疗史者。
5.3 临床表现及体征5.3.1 症状主要表现为直肠刺激症状:便频、里急后重、肛门下坠、便不尽感、肛门痛等。
大便表面带血和/或粘液,严重时有脓血便。
根据临床表现出现的频度,直肠癌临床表现依次以便血、便频及大便变形多见。
5.3.2 直肠指诊凡遇到患者有便血、直肠刺激症状、大便变形等症状均应行直肠指诊。
检查时动作要轻柔,切忌粗暴,要注意有无肿物触及,肿瘤距肛门距离、大小、硬度、活动度、粘膜是否光滑、有无压痛及与周围组织关系、是否侵犯骶前组织。
如果肿瘤位于前壁,男性必须明确与前列腺关系,女性患者需做阴道指诊,查明是否侵犯阴道后壁。
CSCO结直肠癌诊疗指南(2019word版)
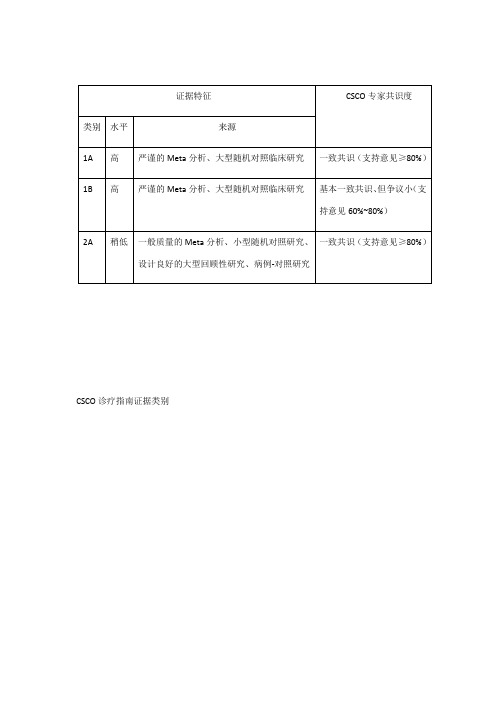
CSCO诊疗指南证据类别CSCO诊疗指南推荐等级1、结直肠癌诊疗总则结直肠癌的MDT诊疗模式注释:A.结直肠癌的诊治应重视多学科团队(multidisciplinary team,MDT)的作用,推荐有条件的单位将尽可能多的结直肠癌患者,尤其是转移性结直肠癌患者的诊疗纳入MDT的管理。
的实施过程中由多个学科的专家共同分析患者的临床表现、影像、病理和分子生物学资料,对患者的一般状况、疾病的诊断、分期/侵犯范围、发展趋向和预后作出全面的评估,并根据当前的国内外治疗规范/指南或循证医学依据,结合现有的治疗手段,为患者制定最适合的整体治疗策略。
原则应该贯穿每一位患者的治疗全程。
团队应根据治疗过程中患者机体状况的变化、肿瘤的反应而适时调整治疗方案,以期最大幅度地延长患者的生存期、提高治愈率和改善生活质量。
2、结直肠的诊断原则无症状健康人群的结直肠癌筛查结肠癌的诊断注释:影像学诊断的更多具体内容详见“影像学检查附录”A.患者存在临床显性肠梗阻,鉴于结肠镜检查前肠道准备会加剧梗阻或造成穿孔,原则上禁止行结肠镜检查。
临床疑似或诊断肠梗阻患者不建议钡剂灌肠检查。
B.患者不具备条件,或拒绝全结肠镜检查,或结肠镜不能检查全部结肠,建议清洁肠道后腹部/盆腔增强CT行结肠检查。
C.鉴于颈胸部淋巴结等诊断与鉴别诊断需要,推荐增强胸部CT;强调高空间分辨率重建图像诊断和鉴别诊断结肠癌肺转移瘤。
D.患者存在静脉造影的禁忌证,建议腹/盆腔增强MRI 加非增强胸部CT。
不能确诊肝转移瘤时,或肝转移瘤存在手术切除机会时,建议行腹部MRI,且包含T2 加权,DWI 加权以及多期T1 加权增强成像序列,用于确定肝转移瘤数目、大小及分布;有条件者可行肝脏细胞特异性造影剂增强MRI,该方法有助于检出1cm 以下病灶。
F.有条件者可行肝脏超声造影或术中超声造影,进一步明确诊断肝脏转移瘤。
G.临床怀疑转移但其他影像检查无法确诊、或重大治疗决策前,PET/CT可用于发现可能存在的转移灶,从而避免过度治疗;但不推荐PET/CT 作为结肠癌诊断的常规检查。
CSCO结直肠癌诊疗指南(2019年度整编)

CSCO诊疗指南证据类别CSCO诊疗指南推荐等级1、结直肠癌诊疗总则结直肠癌的MDT诊疗模式注释:A.结直肠癌的诊治应重视多学科团队(multidisciplinary team,MDT)的作用,推荐有条件的单位将尽可能多的结直肠癌患者,尤其是转移性结直肠癌患者的诊疗纳入MDT 的管理。
B.MDT的实施过程中由多个学科的专家共同分析患者的临床表现、影像、病理和分子生物学资料,对患者的一般状况、疾病的诊断、分期/侵犯范围、发展趋向和预后作出全面的评估,并根据当前的国内外治疗规范/指南或循证医学依据,结合现有的治疗手段,为患者制定最适合的整体治疗策略。
C.MDT 原则应该贯穿每一位患者的治疗全程。
D.MDT 团队应根据治疗过程中患者机体状况的变化、肿瘤的反应而适时调整治疗方案,以期最大幅度地延长患者的生存期、提高治愈率和改善生活质量。
2、结直肠的诊断原则2.1无症状健康人群的结直肠癌筛查2.2.1结肠癌的诊断注释:影像学诊断的更多具体内容详见“影像学检查附录”A.患者存在临床显性肠梗阻,鉴于结肠镜检查前肠道准备会加剧梗阻或造成穿孔,原则上禁止行结肠镜检查。
临床疑似或诊断肠梗阻患者不建议钡剂灌肠检查。
B.患者不具备条件,或拒绝全结肠镜检查,或结肠镜不能检查全部结肠,建议清洁肠道后腹部/盆腔增强CT行结肠检查。
C.鉴于颈胸部淋巴结等诊断与鉴别诊断需要,推荐增强胸部CT;强调高空间分辨率重建图像诊断和鉴别诊断结肠癌肺转移瘤。
D.患者存在静脉造影的禁忌证,建议腹/盆腔增强MRI 加非增强胸部CT。
E.CT不能确诊肝转移瘤时,或肝转移瘤存在手术切除机会时,建议行腹部MRI,且包含T2 加权,DWI 加权以及多期T1 加权增强成像序列,用于确定肝转移瘤数目、大小及分布;有条件者可行肝脏细胞特异性造影剂增强MRI,该方法有助于检出1cm 以下病灶。
F.有条件者可行肝脏超声造影或术中超声造影,进一步明确诊断肝脏转移瘤。
《2023版CSCO结直肠癌诊疗指南》解读PPT课件

关键知识点总结回顾
结直肠癌流行病学特征
包括发病率、死亡率、危险因素等。
诊断方法与技术进展
如内镜检查、影像学检查、实验室检查等 。
治疗手段及效果评估
包括手术、放疗、化疗、免疫治疗等。
随访监测与康复管理
针对患者康复过程中的问题进行指导和干预 。
新型诊疗技术发展趋势预测
精准医疗与基因检测
利用基因检测技术指导个体化治疗。
个体化治疗策略制定及调整时机
个体化治疗策略
根据患者病情、身体状况、经济情况等因素,制定个体化的治疗方案。
调整时机
在治疗过程中,根据患者病情变化和不良反应情况,及时调整治疗方案。
04 药物选择及耐药问题应对策略
常用药物介绍及作用机制阐述
化疗药物
如5-氟尿嘧啶、卡培他滨等,通 过干扰DNA合成和细胞增殖来杀
05 并发症预防与处理建议
手术后并发症类型及危险因素分析
手术后并发症类型
包括感染、吻合口瘘、肠梗阻、出血等。
危险因素分析
高龄、营养不良、免疫功能低下、手术时间长、术中出血多等是手术后并发症发生的危险因素。
放化疗相关毒性反应预防措施
放疗相关毒性反应
放射性肠炎、膀胱炎等是放疗常见的毒性反应。
化疗相关毒性反应
放疗
针对局部进展期患者,放疗可缩小肿瘤、缓解症状、提高手术切除率。
化疗
与放疗联合应用,可增强放疗效果,提高患者生存率。
转移性结直肠癌全身治疗原则和方法探讨
治疗原则
以全身化疗为主,根据患者病情及基 因检测结果,选择合适的靶向药物和 免疫治疗方案。
治疗方法
包括化疗、靶向治疗、免疫治疗等, 可单独或联合应用。
结直肠癌发病率
CSCO结直肠癌诊疗指南(2019word版)

CSCO诊疗指南证据类别注释:A.结直肠癌的诊治应重视多学科团队(multidisciplinary team,MDT)的作用,推荐有条件的单位将尽可能多的结直肠癌患者,尤其是转移性结直肠癌患者的诊疗纳入MDT的管理。
B.MDT的实施过程中由多个学科的专家共同分析患者的临床表现、影像、病理和分子生物学资料,对患者的一般状况、疾病的诊断、分期/侵犯范围、发展趋向和预后作出全面的评估,并根据当前的国内外治疗规范/指南或循证医学依据,结合现有的治疗手段,为患者制定最适合的整体治疗策略。
C.MDT 原则应该贯穿每一位患者的治疗全程。
D.MDT 团队应根据治疗过程中患者机体状况的变化、肿瘤的反应而适时调整治疗方案,以期最大幅度地延长患者的生存期、提高治愈率和改善生活质量。
影像学诊断的更多具体内容详见“影像学检查附录”A.患者存在临床显性肠梗阻,鉴于结肠镜检查前肠道准备会加剧梗阻或造成穿孔,原则上禁止行结肠镜检查。
临床疑似或诊断肠梗阻患者不建议钡剂灌肠检查。
B.患者不具备条件,或拒绝全结肠镜检查,或结肠镜不能检查全部结肠,建议清洁肠道后腹部/盆腔增强CT行结肠检查。
C.鉴于颈胸部淋巴结等诊断与鉴别诊断需要,推荐增强胸部CT;强调高空间分辨率重建图像诊断和鉴别诊断结肠癌肺转移瘤。
D.患者存在静脉造影的禁忌证,建议腹/盆腔增强MRI 加非增强胸部CT。
E.CT不能确诊肝转移瘤时,或肝转移瘤存在手术切除机会时,建议行腹部MRI,且包含T2 加权,DWI 加权以及多期T1 加权增强成像序列,用于确定肝转移瘤数目、大小及分布;有条件者可行肝脏细胞特异性造影剂增强MRI,该方法有助于检出1cm 以下病灶。
F.有条件者可行肝脏超声造影或术中超声造影,进一步明确诊断肝脏转移瘤。
G.临床怀疑转移但其他影像检查无法确诊、或重大治疗决策前,PET/CT可用于发现可能存在的转移灶,从而避免过度治疗;但不推荐PET/CT 作为结肠癌诊断的常规检查。
直肠癌诊疗规范

直肠癌诊疗规范
【诊断标准】
1.临床表现
(1)肠刺激症状排便习惯改变,大便次数增多或便秘。
(2)感染破溃症状大便性状改变,大便带血或粘液血便,脓血便,有大便后不净感,大便变细。
(3)慢性低位肠梗阻症状。
(4)肿物局部侵犯和远处转移症状;直肠内或骶部剧痛,向下腹腰部和下肢放射;尿频尿痛、肝肿大、黄疸等表现。
2.辅助检查
(1)直肠指诊:约90%的直肠癌经仔细的直肠指诊能触及直肠肿块,形状不规则、高低不平、质硬,指套可染脓血。
可发现肿块位置、范围、固定程度。
(2)直肠镜和结肠镜直视肿瘤形态,并可取组织活检确定性质。
(3)X线钡剂灌肠能显示充盈缺损、粘膜破坏、肠腔狭窄,僵硬或局部梗阻等征象。
(4)盆腔CT,直肠腔内超声检查,CEA等对诊断起辅助价值。
【治疗原则】
直肠癌一旦诊断,手术是唯一根治的手段,术前术后可给予放疗、化疗、免疫和中药西药等辅助性治疗。
1.手术治疗
(1)根治性手术:①腹会阴联合切除术,Miles术,适合于距肛门齿状线4cm以内直肠癌;②直肠前切除:Dixon手术,适合于直肠癌下缘距肛门齿状线4cm以上。
(2)如已有远处转移的直肠癌,局部有可能切除应作姑息性切除术加放疗、化疗等综合性治疗。
(3)直肠癌局部侵犯严重与周围组织固定,已不能作局部切除时,可行乙状结肠单腔造瘘术,以解除梗阻。
2.放射治疗直肠癌患者术前、术后可行放射治疗,降低复发率。
3.化学药物治疗预防复发,杀死残存肿瘤细胞。
4.免疫治疗包括肿瘤疫苗的制备,生物修饰剂的应用。
2023 CSCO结直肠癌指南

2023 CSCO结直肠癌指南
根据2023年中国临床肿瘤学会(CSCO)的最新指南,以下是针对结直肠癌的一些重要指导原则和建议:
筛查和早期诊断
- 对于高风险人群,建议进行定期筛查,包括肠镜检查和粪便DNA检测。
- 结直肠镜检查是最常用的筛查方法,能够直接观察肠道粘膜的病变情况。
- 对于早期诊断,应充分利用影像学技术(如CT扫描)和肿瘤标志物检测。
分期和治疗选择
- 结直肠癌的分期是治疗决策的关键因素之一,需要准确评估肿瘤的深浸病变和淋巴结转移情况。
- 手术切除仍然是根治结直肠癌的主要手段,但需要考虑术前辅助治疗(如放疗或化疗)的可行性。
- 对于晚期或转移性结直肠癌,靶向治疗和免疫治疗是重要的治疗选择。
- 进行个体化治疗时需要综合考虑患者的肿瘤特征、身体状况以及治疗风险和益处。
近期发展和研究方向
- 新的药物、治疗方法和策略的研究仍在不断进行中,其中包括靶向药物的精准匹配和新型免疫治疗的应用。
- 早期诊断技术的改进和精准医学的发展有望进一步提高结直肠癌的治疗效果和生存率。
- 结直肠癌的预防和个性化治疗将成为未来研究的重要方向。
以上是2023年CSCO结直肠癌指南的一些要点和建议,旨在为医生和患者提供指导和参考,帮助提高结直肠癌的筛查、诊断和治疗水平。
参考文献:。
2023版CSCO结直肠癌诊疗指南更新解读(早期疾病部分)

2023版CSCO指南:MRD获更多关注
首个基于ctDNA (MRD)指导下的II期结肠癌术后辅助化疗研究
Adjuvant Treatment Delivery
Recurrence-Free Survival
MRD领域面临的临床困境及前景
MRD领域面临的临床困境及前景
近期有硏究显示,动态ctDNA监测有助于提前预警木后复发转移,但其是否应该被常规用于 术后随访并指导治疗仍存在争议,[2] REINERT T, HENRIKSEN TV, CHRISTENSEN E, et aL Analysis of plasma cel I-free DNA by ultradeep sequencing in pattents with stages ! to III colorectal cancer. JAMA Oncology, 2019, 5 (8) :1124-1131.[3] TIE J, COHEN JD, WANG Y, et al. Circulating Tumor DNA Analyses as Markers of Recurrence Risk and Benefit of Adjuvant Therapy for Stage 1H Colon Cancer. JAMA Oncol', 2019, 5:1710-1717,[4] CHEN G, PENG J, XIAO Q, et aL Postoperative circulating tumor DNA as markers of recurrence risk in stages II to III colorectal cancer. J Hematol Oncol, 2021 r 14: 80.
2023 CSCO结直肠癌指南更新(全文)

2023 CSCO结直肠癌指南更新(全文)2023 CSCO结直肠癌指南更新要点——影像诊断结直肠癌肝脏转移瘤-影像诊断1. 结直肠癌诊断方法中,“肝脏细胞特异性造影剂增强肝脏MRI”名词更新。
直肠癌的诊断2. 结直肠癌TNM分期更新。
下段直肠癌的T4a/b分期统一。
直肠癌的T分期增加【注释c】,直肠癌cT4a 期:直肠癌侵犯脏层腹膜而未侵犯MRF,诊断为T4aMRF-;直肠癌侵犯脏层腹膜且在无脏层腹膜覆盖的区域同时侵犯MRF,诊断为T4a 伴MRF+。
增加【注释d】,直肠癌cT4b 期:直肠癌侵犯盆腔脏器及结构,包括盆腔脏器(输尿管膀胱尿道、前列腺精囊腺、子宫宫颈阴道卵巢、小肠及结肠等)、直接侵犯而非血行转移盆腔骨骼、盆底肌肉(坐骨尾骨肌、梨状肌、闭孔肌、肛提肌、耻骨直肠肌、外括约肌等)、盆底神经、骶棘或骶结节韧带、直肠系膜外血管、脂肪等结构。
3. 直肠癌N分期更新,增加侧方淋巴结概念,引入TD概念,定义MRF。
直肠癌的N分期增加【注释e】,直肠癌cN分期:临床诊断的淋巴结转移依据,包括短径≥5mm,形态不规则、边界不清楚、信号/回声不均匀;区域淋巴结包括直肠系膜、乙状结肠系膜远端、直肠上动静脉旁、闭孔、髂内淋巴结,报告为cN 分期;非区域淋巴结包括髂外淋巴结、髂总淋巴结及腹股沟淋巴结,报告为cM分期;如为直肠癌向下侵犯肛管达齿线(耻骨直肠肌)以下,腹股沟淋巴结考虑为区域淋巴结,报告为cN 分期;推荐放射科医师标注淋巴结位置。
增加【注释f】,侧方淋巴结:下段直肠癌或cT3-4可等可被考虑为侧方淋巴结转移的高风险因素;新辅助治疗后,侧方淋巴结显著缩小或消失,则肿瘤残留概率低。
增加【注释g】,癌结节( tumor deposit,TD ):有研究提出TD 影像诊断依据可包括形态不规则、棘状突、信号或回声不均匀位于血管走行区域、与直肠癌原发灶无直接连接。
TD 与直肠癌患者生存预后存在关联性,需密切关注但是TD 与完全被肿瘤侵犯的淋巴结存在影像学鉴别诊断困难。
直肠癌诊治指南

直肠癌诊治指南简介·直肠癌(carcinoma of rectum)是乙状结肠直肠交界处至齿状线之间的癌,是消化道常见的恶性肿瘤。
·随着人民生活水平的不断提高,饮食习惯和饮食结构的改变以及人口老龄化,我国结直肠癌的发病率和死亡率均保持上升趋势。
·早期直肠癌的临床特征主要为便血和排便习惯改变,常被误诊为痔疮。
·直肠癌的诊断,通常要应用直肠指检、直肠镜或乙状结肠镜等检查方法。
·直肠癌的治疗目前仍以外科手术为主,化疗为辅,放射治疗有一定的作用。
定义直肠癌(carcinoma of rectum)是乙状结肠直肠交界处至齿状线之间的癌,是消化道常见的恶性肿瘤。
流行病学2012年,美国估计共有40,290例新发的直肠癌(其中男性23,500例,女性16,790例)。
同年,估计美国将有51,690名患者死于结直肠癌。
直肠癌是西方国家最常见的恶性肿瘤之一,约占成年恶性肿瘤患者的5%,其发病率位于恶性肿瘤的第5位。
欧洲每年约有140 000直肠癌新发病例,全球发病率增加最快的是东欧和日本。
近年来,我国结直肠癌的发病率和死亡率亦处于上升趋势,估计每年直肠癌的新发病例不少于10 万。
中国人直肠癌与西方人比较,有三个流行病学特点:①直肠癌比结肠癌发生率高,约1. 5:1;最近的资料显示结直肠癌发生率逐渐靠近,有些地区已接近1:1,主要是结肠癌发生率增高所致;②低位直肠癌所占的比例高,约占直肠癌的 60%~75%;绝大多数癌肿可在直肠指诊时触及;③青年人(G30岁)直肠癌比例高,约10%一15%。
直肠癌根治性切除术后总的5年生存率在60%左右,早期直肠癌术后的5年生存率为80%-90%。
病因直肠癌的病因目前仍不十分清楚,其发病与社会环境、饮食习惯、遗传因素等有关。
直肠息肉也是直肠癌的高危因素。
目前基本公认的是动物脂肪和蛋白质摄入过高,食物纤维摄入不足是直肠癌发生的高危因素。
2019版:直肠癌规范化诊疗指南(完整版)

2019版:直肠癌规范化诊疗指南(完整版) The 2019 XXX (Complete n)1.ScopeThis guideline specifies the standardized diagnosis and treatment process。
diagnostic criteria。
diagnosis and differential diagnosis。
treatment principles。
XXX.XXX.2.XXX and nsXXX.Rectal mesentery: XXX wraps around and forms a semi-circle behind and on both sides of the middle and lower rectum。
with a thickness of 1.5-2.0 cm。
containing arteries。
veins。
lymphatic tissue。
and a large amount of fat tissue。
It extends from the frontof the third sacral vertebra to the pelvic diaphragm.3.nsXXX.3.1 XXX: XXX3.2 CEA: Carcinoembryonic Antigen4.Diagnosis and XXX Flowchart5.Diagnostic Criteria5.1 logyXXX not fully understood。
but the XXX:5.1.1 Environmental factors: dietary habits。
intestinal bacteria。
chemical carcinogens。
XXX.5.1.2 Intrinsic factors: ic ns。
adenomas。
XXX。
《2023 CSCO结直肠癌诊疗指南》解读PPT课件

05
靶向治疗和免疫治疗进展及挑战
靶向治疗药物及适应证
1 2
抗EGFR单抗
适用于KRAS/NRAS/BRAF野生型左半结肠癌, 联合化疗可延长生存期。
抗VEGF/VEGFR药物
贝伐珠单抗联合化疗可用于各线治疗,瑞戈非尼 和呋喹替尼是晚期肠癌三线治疗标准药物。
3
PARP抑制剂
奥拉帕利可用于dMMR/MSI-H/TMB-H肠癌后 线治疗,帕米帕利和氟唑帕利已获批用于铂类敏 感肠癌维持治疗。
《2023 CSCO结直肠癌诊疗指南》 解读
汇报人:xxx 2023-12-11
ቤተ መጻሕፍቲ ባይዱ
目录
• 引言 • 结直肠癌流行病学及危险因素 • 临床分期与治疗策略选择 • 手术、放疗、化疗联合应用及进展 • 靶向治疗和免疫治疗进展及挑战 • 随访管理与生活质量保障 • 总结与展望
01
引言
CSCO结直肠癌诊疗指南背景
免疫治疗在结直肠癌中应用前景
MSI-H/dMMR肠癌
PD-1抑制剂帕博利珠单抗和纳武利尤单抗已获批用于MSI-H/dMMR肠癌二线及以上治疗,不受肿瘤部位限制。
MSS型肠癌
免疫联合化疗在MSS型肠癌新辅助治疗中具有应用前景,PD-1抑制剂联合CTLA-4抑制剂可提高MSS型肠癌的客 观缓解率。
多学科协作提高治疗效果
个体化治疗方案制定
综合评估
考虑患者年龄、体能状态、合并 症、肿瘤分期和分子分型等因素
,制定个体化治疗方案。
多学科协作
外科医生、肿瘤内科医生、放疗 科医生、病理科医生等多学科团
队共同参与治疗方案制定。
动态调整
根据患者病情变化和治疗效果, 及时调整治疗方案,以达到最佳
2019版:直肠癌规范化诊疗指南(完整版)

2019版:直肠癌规范化诊疗指南(完整版)1 范围本指南规定了直肠癌的规范化诊治流程、诊断依据、诊断和鉴别诊断、治疗原则及治疗方案。
本指南适用于农村重大疾病医疗保障工作定点医院对直肠癌的诊断和治疗。
2 术语和定义下列术语和定义适用于本指南。
直肠系膜:指的是在中下段直肠的后方和两侧包裹着的,形成半圆,厚1.5~2.0cm的结缔组织,内含有动脉、静脉、淋巴组织及大量脂肪组织,上自第3骶椎前方,下达盆膈。
3 缩略语下列缩略语适用于本指南。
3.1 TME:(total mesorectal excision)全直肠系膜切除术3.2 CEA:(carcinoembryonic antigen)癌胚抗原4 诊治流程图5 诊断依据5.1 病因直肠癌的发病原因尚未完全阐明,导致发生的原因可归纳为:5.1.1 环境因素饮食习惯、肠道细菌、化学致癌物质、土壤中缺钼和硒。
5.1.2 内在因素基因变异、腺瘤、血吸虫性结肠炎、慢性溃疡性结肠炎。
5.2 高危人群5.2.1 有便血、便频、大便带粘液、腹痛等肠道症状的人。
5.2.2 大肠癌高发区的中、老年人。
5.2.3 大肠腺瘤患者。
5.2.4 有大肠癌病史者。
5.2.5 大肠癌患者的家庭成员。
5.2.6 家族性大肠腺瘤病患者。
5.2.7 溃疡性结肠炎患者。
5.2.8 Crohn病患者。
5.2.9 有盆腔放射治疗史者。
5.3 临床表现及体征5.3.1 症状主要表现为直肠刺激症状:便频、里急后重、肛门下坠、便不尽感、肛门痛等。
大便表面带血和/或粘液,严重时有脓血便。
根据临床表现出现的频度,直肠癌临床表现依次以便血、便频及大便变形多见。
5.3.2 直肠指诊凡遇到患者有便血、直肠刺激症状、大便变形等症状均应行直肠指诊。
检查时动作要轻柔,切忌粗暴,要注意有无肿物触及,肿瘤距肛门距离、大小、硬度、活动度、粘膜是否光滑、有无压痛及与周围组织关系、是否侵犯骶前组织。
如果肿瘤位于前壁,男性必须明确与前列腺关系,女性患者需做阴道指诊,查明是否侵犯阴道后壁。
直肠癌临床实践指南要点解读(完整版)

直肠癌临床实践指南要点解读(完整版)2024年1月,美国结直肠外科医生协会(the American Society of Colon and Rectal Surgeon,ASCRS)对2020年发布的直肠癌临床实践指南进行了中期增补,纳入了近年涌现的高影响力数据,以对直肠癌的诊疗提供最新的建议[1-2]。
本文将从上段直肠癌治疗、全程新辅助治疗、临床完全缓解(clinical complete response,cCR)患者的等待观察、经肛全直肠系膜切除术(transanal total mesorectal excision,taTME)的安全性等4个方面,对该指南增补的要点进行概括和解读。
一、上段直肠肿瘤优先手术切除增补要点:“上段直肠”是位于腹膜反折之上直肠的最近端部分,与中下段直肠癌相比,上段直肠癌局部复发率较低[3-5]。
腹膜反折通常距肛缘11~15 cm,根据患者的个体解剖而有所不同,可由核磁共振成像、硬性或软性内镜将肿瘤定位于上段直肠[6-7]。
新辅助放化疗(neoadjuvant chemoradiotherapy,NCRT)的主要目的是减少直肠切除术后的局部复发,然而上段直肠肿瘤通常不能从NCRT中获益。
瑞典一项纳入243例肿瘤距离肛缘>11 cm直肠癌患者的研究中,接受短程放疗与直接手术者局部复发率差异无统计学意义(8%比12%,P=0.3)[8]。
荷兰TME研究同样发现,在上段直肠癌患者中,与直接手术相比,短程放疗没有减少局部复发率(3.7%比6.2%,P=0.122)[9]。
2009年MRC CR07和NCIC-CTG C016研究对上段直肠癌患者的亚组分析显示,接受NCRT和直接手术者的3年局部复发率差异无统计学意义(1.2%比6.2%,P=0.19)[10]。
解读:与中下段直肠癌相比,上段直肠癌局部复发率较低,与左侧结肠癌类似。
NCRT并未显著减少上段直肠癌患者的局部复发率,且与盆底功能损害、放射性肠炎、吻合口漏等并发症相关[8-10]。
中国临床肿瘤学会 (CSCO)结直肠癌诊疗指南2020版

针对患有某器官或系统疾病的病人进行讨论 形成该病人的诊断、治疗决策 并由相应学科MDT成员执行
结直肠癌的MDT诊治原则
结直肠癌的MDT诊治原则
• 推荐有条件的单位将尽可能多的结直肠癌患者,尤其是转 移性的结直肠癌患者的诊疗纳入MDT的管理
证据级别
证据级别
注意事项
I级 1A类证据:
2A类证据:
• 可及性好
专家推荐 基于高水平证据,如严谨的 基于稍低水平证据,如一般质量 • 适应症明确
Meta分析或大型随机对照 的meta分析、小型随机对照研 • 基本为国家医保所收
临床研究结果,专家组取得 究(II期)、设计良好的大型回
录
一致共识(支持意见≥80%) 顾性研究、病例-对照研究,专 • 不因商业医疗保险改
• 阳性者进入高危人群
管理流程 • 阴性者进入后续筛查
后续筛查
FIT 每年1次
阴性
下一年继续FIT
无症状健康人群的筛查:一般人群 (I 级专家推荐)
• 多项研究一致证实,免疫法大便隐血检测(FIT)在不降低特异性情况下,筛 检的敏感性较化学法大便隐血检测有显著提升。
• 免疫法大便隐血检测(FIT):建议进行2次间隔1周的检测。经一项1020人 的全人群结肠镜金标准对照筛查试验,与1次检测相比,2次间隔1周的大便
• FAP患者会出现先天性视网膜色素上皮肥大(CHRPE),在典型的FAP中发生率可达80%。 • 1/3-1/4的FAP患者无家族遗传史,为该个体胚系新发肿瘤。家族史并不是诊断FAP的必要条件。
FAP遗传基因筛检
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
直肠癌规范化诊疗指南(试行)1 范围本指南规定了直肠癌的规范化诊治流程、诊断依据、诊断和鉴别诊断、治疗原则及治疗方案。
本指南适用于农村重大疾病医疗保障工作定点医院对直肠癌的诊断和治疗。
2 术语和定义下列术语和定义适用于本指南。
直肠系膜:指的是在中下段直肠的后方和两侧包裹着的,形成半圆,厚1.5~2.0cm的结缔组织,内含有动脉、静脉、淋巴组织及大量脂肪组织,上自第3骶椎前方,下达盆膈。
3 缩略语下列缩略语适用于本指南。
3.1 TME:(total mesorectal excision)全直肠系膜切除术3.2 CEA:(carcinoembryonic antigen)癌胚抗原4 诊治流程图5 诊断依据5.1 病因直肠癌的发病原因尚未完全阐明,导致发生的原因可归纳为:5.1.1 环境因素饮食习惯、肠道细菌、化学致癌物质、土壤中缺钼和硒。
5.1.2 内在因素基因变异、腺瘤、血吸虫性结肠炎、慢性溃疡性结肠炎。
5.2 高危人群5.2.1 有便血、便频、大便带粘液、腹痛等肠道症状的人。
5.2.2 大肠癌高发区的中、老年人。
5.2.3 大肠腺瘤患者。
5.2.4 有大肠癌病史者。
5.2.5 大肠癌患者的家庭成员。
5.2.6 家族性大肠腺瘤病患者。
5.2.7 溃疡性结肠炎患者。
5.2.8 Crohn病患者。
5.2.9 有盆腔放射治疗史者。
5.3 临床表现及体征5.3.1 症状主要表现为直肠刺激症状:便频、里急后重、肛门下坠、便不尽感、肛门痛等。
大便表面带血和/或粘液,严重时有脓血便。
根据临床表现出现的频度,直肠癌临床表现依次以便血、便频及大便变形多见。
5.3.2 直肠指诊凡遇到患者有便血、直肠刺激症状、大便变形等症状均应行直肠指诊。
检查时动作要轻柔,切忌粗暴,要注意有无肿物触及,肿瘤距肛门距离、大小、硬度、活动度、粘膜是否光滑、有无压痛及与周围组织关系、是否侵犯骶前组织。
如果肿瘤位于前壁,男性必须明确与前列腺关系,女性患者需做阴道指诊,查明是否侵犯阴道后壁。
指诊检查完毕应观察指套有无血迹。
5.4 辅助检查5.4.1 内镜检查内镜检查是诊断直肠癌最安全、有效的检查方法。
内镜检查可直接观察病灶,并取活体组织做病理诊断。
取活检时需注意取材部位,做多点取材。
如果活检阴性且临床考虑为肿瘤的患者,应重复取材以免漏诊。
5.4.2 X线检查气钡双重对比造影X线摄片检查表现有:①结节状充盈缺损,多在直肠的内侧壁,圆形光滑或轻度分叶,局部肠壁僵硬,凹入;②菜花状肿块,较大,表面不平,分叶明显,其底宽,肠壁僵硬;③不规则的环状狭窄,管壁僵硬,粘膜中断,分界截然;④不规则的腔内龛影,呈三角形、长条形等,较浅,周围环堤宽窄不均;⑤完全性肠梗阻,或肠套叠征象,阻塞近段有时难以显示。
应注意,钡灌肠的X线检查有时无法显示直肠病变,易让人产生无病变的错觉。
5.4.3 B型超声波检查腹部B型超声扫描对判断肝脏有无转移有一定价值,应列为术前常规检查内容。
5.4.4 CT扫描检查腹盆腔增强CT检查应为常规检查项目,对于术前了解肝内有无转移,腹主动脉旁淋巴结是否肿大,癌肿对周围结构或器官有无浸润,判断手术切除的可能性和危险性等,指导术前选择合理的治疗方案提供可靠依据。
5.4.5 胸部X射线摄影检查应包括胸部正位和侧位片,排除肺转移。
对于胸部X线检查异常者行胸部CT检查除外转移。
5.4.6 盆腔MRI检查MRI具有较高的对比分辨率,可清楚显示盆腔内软组织结构和脏器毗邻关系,对直肠癌的术前分期和指导手术方案选择有重要作用。
5.4.7 实验室检查血常规、尿常规、大便常规+大便潜血试验,血型,肝功能、肾功能,凝血功能,血糖,电解质,血清病毒指标检测,肿瘤标志物检查(CEA和CA19-9)。
5.4.8 心电图检查6 直肠癌的分类和分期6.1 直肠肿瘤的组织学分类表1 WHO直肠肿瘤组织学分类(2010)上皮性肿瘤癌前病变腺瘤8140/0管状8211/0绒毛状8261/0管状绒毛状8263/0锯齿状8213/0不典型增生(上皮内肿瘤),低级别8148/0不典型增生(上皮内肿瘤),高级别8148/2锯齿状病变增生性息肉广基锯齿状腺瘤/息肉8213/0经典锯齿状腺瘤8213/0错构瘤Cowden相关性息肉幼年性息肉Peutz-Jeghers息肉癌腺癌8140/3 筛状粉刺型腺癌8201/3 髓样癌8510/3 微乳头状癌8265/3 黏液腺癌8480/3 锯齿状腺癌8213/3 印戒细胞癌8490/3 腺鳞癌8560/3 梭形细胞癌8032/3 鳞状细胞癌8070/3 未分化癌8020/3神经内分泌肿瘤神经内分泌肿瘤(NET)NET 1级(类癌) 8240/3 NET 2级8249/3 神经内分泌癌(NEC)8246/3大细胞神经内分泌癌8013/3小细胞神经内分泌癌8041/3混合性腺神经内分泌癌8244/3EC细胞,5-羟色胺生成性神经内分泌肿瘤8241/3L细胞,胰高血糖素样肽和PP/PYY生成性神经内分泌肿瘤8152/1间叶性肿瘤平滑肌瘤8890/0脂肪瘤8850/3血管肉瘤9120/3胃肠道间质瘤8936/3Kaposi肉瘤9140/3平滑肌肉瘤8890/3淋巴瘤继发性肿瘤6.2 直肠癌的分期6.2.1 Dukes分期由于1932年Dukes提出的直肠癌分期简单易行,且对预后有一定的指导意义,因此,目前仍被应用。
直肠癌Dukes分期Dukes A期:肿瘤局限于肠壁内;Dukes B期:肿瘤侵犯至肠壁外;Dukes C期:有区域淋巴结转移,无论侵犯深度。
6.2.2 TNM分期美国癌症联合协会(AJCC)提出的TNM分期系统对直肠癌的预后有更好的指导意义。
表2 TNM分期(AJCC, 2009 第七版)T-原发瘤分期Tx 原发肿瘤不能评估T0 无原发肿瘤证据Tis 原位癌:上皮内或粘膜固有层T1 肿瘤侵犯粘膜下层T2 肿瘤侵犯固有肌层T3 肿瘤侵犯浆膜下或无腹膜被覆的结肠或直肠旁组织T4 肿瘤侵透脏层腹膜和/或直接侵犯其他器官或结构T4a 肿瘤穿透脏层腹膜表面T4b 肿瘤直接侵犯其他器官或结构N –区域淋巴结Nx 区域淋巴结不能评价N0 无区域淋巴结转移N1 1-3个区域淋巴结转移-N1a 1个区域淋巴结转移-N1b 2-3个区域淋巴结转移-N1c 无区域淋巴结转移,但在浆膜下或无腹膜被覆的结肠或直肠旁组织存在单个(或多个)癌结节(卫星灶)-N2 ≥4个区域淋巴结转移-N2a 4-6个区域淋巴结转移-N2b ≥7个区域淋巴结转移M- 远处转移M0 无远处转移M1 有远处转移-M1a 单个器官或部位发生转移(如肝、肺、卵巢、非区域淋巴结,如髂外和髂总淋巴结)-M1b 多个器官或部位发生转移或腹膜转移TNM分期及Dukes分期stage T N M Dukes MAC0 Tis N0 M0 - -I T1 N0 M0 A AT2 N0 M0 A B1IIA T3 N0 M0 B B2IIB T4a N0 M0 B B2IIC III T4b任何TN0N1,N2M0M0BCB3IIIA T1-T2 N1/N1c M0 C C1 T1 N2a M0 C C1 IIIB T3-T4a N1/N1c M0 C C2 T2-T3 N2a M0 C C1/C2T1-T2 N2b M0 C C1 IIIC T4a N2a M0 C C2 T3-T4a N2b M0 C C2T4b N1-N2 M0 C C3IV A 任何T 任何N M1a - -IVB 任何T 任何N M1b - -前缀p:为术后病理分期7 诊断和鉴别诊断7.1 诊断年龄在40岁以上,有以下任一表现者应列为高危人群:①Ⅰ级亲属有直肠癌病史者;②有癌症史或肠道腺瘤或息肉史者;③大便隐血试验阳性者;④以下五种表现中具有2项以上者:粘液血便、慢性腹泻、慢性便秘、慢性阑尾炎史及精神创伤史。
对此高危人群行肠镜检查或气钡双重对比灌肠造影X线摄片检查可明确诊断。
7.2 鉴别诊断对有便血、便频、便细、粘液便等症状的患者予以高度警惕,必须进一步检查,排除直肠癌的可能性。
通过直肠指诊、内镜检查及病理检查明确诊断。
在临床中对于拟诊内痔、息肉、肠炎及慢性痢疾的患者,应常规行直肠指诊,除外直肠癌后,方可按以上疾病治疗。
8 治疗8.1 治疗原则临床上一般应采取以手术为主的综合治疗。
根据病人的全身状况和各个脏器功能状况、肿瘤的位置、肿瘤的临床分期、病理类型及生物学行为等决定治疗措施。
合理地利用现有治疗手段,以期最大程度地根治肿瘤、最大程度地保护脏器功能和改善病人的生活质量。
直肠癌的治疗主要有手术治疗、放射治疗和化学治疗及靶向治疗。
8.2 手术治疗8.2.1 手术治疗适应证8.2.1.1 全身状态和各脏器功能可耐受手术。
8.2.1.2 肿瘤局限于肠壁或侵犯周围脏器,但可整块切除,区域淋巴结能完整清扫。
8.2.1.3 已有远处转移(如肝转移、卵巢转移、肺转移等),但可全部切除,酌情同期或分期切除转移灶。
8.2.1.4 广泛侵袭或远处转移,但伴有梗阻、大出血、穿孔等症状应选择姑息性手术,为下一步治疗创造条件。
8.2.2 手术治疗禁忌证8.2.2.1 全身状态和各脏器功能不能耐受手术和麻醉。
8.2.2.2 广泛远处转移和外侵,无法完整切除,无梗阻、穿孔、大出血等严重并发症。
8.2.3 手术治疗方法的选择8.2.3.1 直肠癌局部切除手术需严格把握以下手术指征①肿瘤侵犯肠周径<30%;②肿瘤大小<3cm;③切缘阴性(距离肿瘤>3mm);④肿瘤活动,不固定;⑤肿瘤距肛缘8cm 以内;⑥仅适用于T1N0M0肿瘤;⑦内镜下切除的息肉,伴癌浸润,或病理学不确定;⑧无血管淋巴管浸润(LVI)或神经浸润;⑨高-中分化;⑩治疗前影像学检查无淋巴结肿大的证据。
注:局部切除标本必须由手术医师展平、固定,标记方位后送病理检查。
术后病理如果为T2或者T1伴有切缘阳性、血管淋巴管侵润、分化差的高危患者则应行经腹切除术。
拒绝手术患者考虑放射治疗。
8.2.3.2 经腹直肠癌根治性切除术全直肠系膜切除术(TME)为中低位直肠癌手术的标准术式,是指在直视下锐性解剖盆筋膜脏层和壁层间的特定间隙,完整切除脏层筋膜内的全部组织,包括直肠系膜内的血管淋巴管结构、脂肪组织和直肠系膜筋膜,保留自主神经功能。
切除肿瘤下缘以下4~5cm的直肠系膜或达盆膈,下段直肠癌(距离肛缘小于5cm)切除肿瘤远端肠管至少2cm。
8.2.4 手术方式直肠癌低位前切除术、经腹会阴联合切除术、Hartmann手术等。
8.2.5 转移灶的处理8.2.5.1 肝转移完整切除必需考虑肿瘤范围和解剖学上的可行性。
切除后剩余肝脏必须能够维持足够功能。
达不到R0切除的减瘤手术不做推荐,无肝外不可切除病灶。
