实验二十一甲基橙的制备
制备甲基橙实验报告

实验名称:甲基橙的制备实验日期:2022年10月15日实验地点:化学实验室一、实验目的1. 学习重氮化反应和偶联反应的实验操作;2. 掌握甲基橙的制备方法及原理;3. 了解甲基橙的性质和应用。
二、实验原理甲基橙是一种常用的酸碱指示剂,具有C6H5-NN-N-C6H5结构。
在酸性溶液中呈红色,在碱性溶液中呈黄色。
本实验采用重氮化-偶联反应法制备甲基橙。
三、实验仪器与试剂1. 仪器:烧杯、试管、玻璃棒、抽滤瓶、冰水浴、温度计、天平、电子秤、滴管、滤纸等。
2. 试剂:对氨基苯磺酸、NaNO2、N,N-二甲基苯胺、冰醋酸、NaOH、浓盐酸、饱和氯化钠溶液、乙醇等。
四、实验步骤1. 准备溶液:(1)称取2.00g对氨基苯磺酸晶体,加入100ml烧杯中,再加入10ml 5%氢氧化钠水溶液,热水浴湿热溶解。
(2)溶液冷却至室温,一边搅拌一边加入0.8g NaNO2,将其溶解。
2. 制备重氮盐:(1)将13ml水和0.25ml浓盐酸加入250ml烧杯中,搅拌均匀。
(2)将上述溶液分批滴入步骤1中制备的溶液中,边滴边搅拌。
(3)用碘化钾淀粉试纸检验以确定亚硝酸钠是否不足。
保持液体温度在0-5℃以下,反应结束后将烧杯放在冰水浴中,放置15min。
3. 偶联反应:(1)在一支试管中加入1.3ml N,N-二甲基苯胺和1ml冰醋酸,振荡混合。
(2)在搅拌下将上述溶液缓慢加入步骤2中的冷却重氮液中,搅拌10min左右。
4. 结晶与纯化:(1)烧杯一直浸在冰水中,一边慢慢加入15ml 10% NaOH,一边搅拌。
(2)以上2-6步骤总体系温度不应超过5℃,以免发生冒料危险。
(3)反应后,将烧杯加热,沸腾,烧杯内物质溶解,浓缩。
(4)冷却至室温后,置于冰水浴中,使甲基橙结晶沉淀。
(5)抽滤,收集晶体。
抽滤时用饱和氯化钠溶液冲洗烧杯两次,每次10ml左右。
5. 干燥与称量:将收集到的晶体用干燥器干燥,称量并计算产率。
五、实验结果与分析1. 甲基橙的制备:通过重氮化-偶联反应,成功制备了甲基橙。
实验二十一甲基橙的制备

实验二十一甲基橙的制备 Revised by BLUE on the afternoon of December 12,2020.实验二十一甲基橙的制备Experiment 21 Preparation of methyl orange[实验目的]1、熟悉重氮化反应和偶合反应的原理。
2、掌握甲基橙的制备方法。
[实验内容]一、实验原理1、重氮化反应芳香族伯胺在低温和强酸溶液中与亚硝酸钠作用,生成重氮盐的反应称为重氮化反应(diazotization)。
由于芳香族伯胺在结构上的差异,重氮化方法也不尽相同。
苯胺、联苯胺及含有给电子基的芳胺,其无机酸盐稳定又溶于水,一般采用顺重氮法,即先把1mol胺溶于 mol 的无机酸,于0-5℃加入亚硝酸钠。
含有吸电子基(-SO3H、-COOH)的芳胺,由于本身形成内盐而难溶于无机酸,较难重氮化,一般采用逆重氮化法,即先溶于碳酸钠溶液,再加入亚硝酸钠,最后加酸。
本次实验,甲基橙的制备即采用该方法。
含有一个-NO2、-Cl等吸电子的芳胺,由于碱性弱,难成无机盐,且铵盐难溶于水,易水解,生成的重氮盐又容易与未反应的胺生成重氮氨基化合物(-ArN=N-NHAr),因此多采用先将胺溶于热的盐酸,冷却后再重氮化。
2、偶合反应在弱碱或弱酸性条件下,重氮盐和酚、芳胺类化合物作用,生成偶氮基(-N=N-)将两分子中的芳环偶联起来的反应称为偶联反应(coupling reaction偶合反应)。
偶联反应的实质是芳香环上的亲电取代反应,偶氮基为弱的亲电基,它只能与芳环上具有较大电子云密度的酚类、芳胺类化合物反应。
由于空间位阻的影响,反应一般在对位发生。
若对位已经有取代基,则偶联反应发生在邻位。
重氮盐和酚的反应是在若碱性的介质中进行。
而重氮盐与芳胺的反应是在弱酸环境下进行的。
对于本实验,甲基橙的制备,由于为重氮盐与芳胺的反应,故以冰醋酸为溶剂。
该反应的方程式为:NH 2SO 3H NaOHH 2ONH 2SO 3-Na +++NH 2SO 3-Na +N +HO 3SNCl -C 6H 5N(CH 3)2HOAcN HO 3SNNH(CH 3)2+OAc -NaOHN NaO 3SNN(CH 3)2NaAc++H 2O二、实验所需试剂及仪器药品:对氨基苯磺酸、5%氢氧化钠溶液、 亚硝酸钠、 浓盐酸、 冰醋酸 、N, N -二甲基苯胺、乙醇、乙醚、淀粉-碘化钾试纸 仪器:烧杯、温度计、表面皿、布氏漏斗 三、实验具体操作步骤 1、重氮盐的制备在50 mL 烧杯中、加入1 g 对氨基苯磺酸结晶和5 mL 5%氢氧化钠溶液,温热使结晶溶解,用冰盐浴冷却至0℃以下。
甲基橙(实验室酸碱指示剂)的制备-学生用

甲基橙(实验室酸碱指示剂)的制备一、训练要求1、学习和掌握甲基橙(实验室酸碱指示剂)制备原理和方法,清楚反应的影响因素,进行制备方案的查询和选择。
2、根据所确定的方案查阅并记录原料、中间产物、副产物、产品的常规物性和毒理性质。
做实验环境的评估、选择和安全预案。
3、理解反应过程中出现的副反应,且在合成操作后,有逻辑的明确提纯方案。
4、根据实施路线和数量要求,合理选择适合的玻璃仪器,辅助装置,并能够正确、熟练的搭建实验装置。
5、能够熟练的操作仪器,控制反应进程,对粗品进行纯化处理,进行基本的性质检测。
6、实验训练中,能够仔细观察现象,正确分析现象的原因,进行对应的正确操作与处理。
7、实验过程中,及时、准确、正确的记录实验数据和现象。
实验结束后进行数据的归纳、整理、计算。
8、本实验要求熟练掌握:试剂的称量、低温合成、洗涤与抽滤操作、干燥、以及熔点仪的使用。
二、教学重点和难点重点:偶氮化合物的制备原理和方法,反应设备的搭建,减压抽滤的原理和方法。
难点:通过减压抽滤去除固液混合组分中非产品成分的方法。
甲基橙(实验室酸碱指示剂)粗品的重结晶提纯。
本制备过程的粗产物是固液非均相体系,并含有副产物,使用减压抽滤和重结晶的处理方式,获得纯度较高的产品是典型的固液混合相产物处理方法,在有机合成操作中具有代表意义。
三、试验原理中文别名:金莲橙D英文名称::Methyl Orange结构式:外观与性状:橙黄色鳞状晶体或粉末。
分子量:327.24甲基橙的变色范围是pH<3.1 变红,pH>4.4变黄,3.1~4.4呈橙色。
相对密度:1.28溶解性: 微溶于冷水,易溶于热水,几乎不溶于乙醇; 最大吸收波长:505nm在酸碱滴定中主要用作酸碱指示剂,在氧化还原滴定法中可以用作氧化还原指示剂,在催化动力光度分析和氧化还原光度分析中主要用作还原剂,在配合物水相光度分析中主要用作配位剂。
主反应:甲基橙是指示剂,它是由对氨基苯磺酸重氮盐与N ,N —二甲基苯胺的醋酸盐,在弱酸性介质中偶合,首先得到亮黄色的酸式甲基橙称为酸性黄,在碱中酸性黄转变为橙黄色的钠盐,即甲基橙。
实验二十一 甲基橙的制备

实验二十一甲基橙的制备Experiment 21 Preparation of methyl orange[实验目的]1、熟悉重氮化反应和偶合反应的原理。
2、掌握甲基橙的制备方法。
[实验内容]一、实验原理1、重氮化反应芳香族伯胺在低温和强酸溶液中与亚硝酸钠作用,生成重氮盐的反应称为重氮化反应(diazotization)。
由于芳香族伯胺在结构上的差异,重氮化方法也不尽相同。
苯胺、联苯胺及含有给电子基的芳胺,其无机酸盐稳定又溶于水,一般采用顺重氮法,即先把1mol胺溶于2.5-3 mol 的无机酸,于0-5℃加入亚硝酸钠。
含有吸电子基(-SO3H、-COOH)的芳胺,由于本身形成内盐而难溶于无机酸,较难重氮化,一般采用逆重氮化法,即先溶于碳酸钠溶液,再加入亚硝酸钠,最后加酸。
本次实验,甲基橙的制备即采用该方法。
含有一个-NO2、-Cl等吸电子的芳胺,由于碱性弱,难成无机盐,且铵盐难溶于水,易水解,生成的重氮盐又容易与未反应的胺生成重氮氨基化合物(-ArN=N-NHAr),因此多采用先将胺溶于热的盐酸,冷却后再重氮化。
2、偶合反应在弱碱或弱酸性条件下,重氮盐和酚、芳胺类化合物作用,生成偶氮基(-N=N-)将两分子中的芳环偶联起来的反应称为偶联反应(coupling reaction偶合反应)。
偶联反应的实质是芳香环上的亲电取代反应,偶氮基为弱的亲电基,它只能与芳环上具有较大电子云密度的酚类、芳胺类化合物反应。
由于空间位阻的影响,反应一般在对位发生。
若对位已经有取代基,则偶联反应发生在邻位。
重氮盐和酚的反应是在若碱性的介质中进行。
而重氮盐与芳胺的反应是在弱酸环境下进行的。
对于本实验,甲基橙的制备,由于为重氮盐与芳胺的反应,故以冰醋酸为溶剂。
该反应的方程式为:NH 2SO 3H NaOHH 2ONH 2SO 3-Na +++NH 2SO 3-Na +N +HO 3SNCl -C 6H 5N(CH 3)2N HO 3SNNH(CH 3)2+OAc -NaOHN NaO 3SNN(CH 3)2NaAc++H 2O二、实验所需试剂及仪器药品:对氨基苯磺酸、 5%氢氧化钠溶液、 亚硝酸钠、 浓盐酸 、 冰醋酸 、N, N -二甲基苯胺、乙醇、乙醚、淀粉-碘化钾试纸 仪器:烧杯、温度计、表面皿、布氏漏斗 三、实验具体操作步骤 1、重氮盐的制备在50 mL 烧杯中、加入1 g 对氨基苯磺酸结晶和5 mL 5%氢氧化钠溶液,温热使结晶溶解,用冰盐浴冷却至0℃以下。
甲基橙制备实验报告

一、实验目的1. 熟悉有机合成实验的基本操作,提高实验技能。
2. 学习甲基橙的制备方法,掌握重氮化反应和偶合反应的实验操作。
3. 了解甲基橙的性质及其在化学分析中的应用。
二、实验原理甲基橙是一种常用的酸碱指示剂,具有酸碱变色范围广、颜色变化明显等特点。
本实验采用重氮化反应和偶合反应制备甲基橙。
重氮化反应:对氨基苯磺酸与亚硝酸钠在酸性条件下反应,生成重氮盐。
偶合反应:重氮盐与N,N-二甲基苯胺在碱性条件下反应,生成甲基橙。
三、实验仪器与试剂1. 仪器:烧杯、试管、玻璃棒、滴管、冰水浴、水浴锅、抽滤装置、蒸发皿、烘箱等。
2. 试剂:对氨基苯磺酸、亚硝酸钠、浓盐酸、N,N-二甲基苯胺、冰乙酸、10%氢氧化钠溶液、饱和氯化钠溶液、无水乙醇等。
四、实验步骤1. 对氨基苯磺酸的制备将2.00g对氨基苯磺酸晶体倒入100ml烧杯中,加入10ml 5%氢氧化钠溶液,热水浴加热至溶解。
冷却至室温。
2. 重氮化反应将冷却后的溶液中加入0.8g亚硝酸钠,搅拌溶解。
将13ml水和0.25ml浓盐酸加入250ml烧杯中,搅拌。
将上述溶液分批滴入烧杯中,同时用碘化钾淀粉试纸检验亚硝酸钠是否不足。
保持液体温度在0~5℃。
3. 偶合反应在一支试管中加入1.3ml N,N-二甲基苯胺和1ml冰乙酸,振荡混合。
在搅拌下将此溶液缓慢加入上述冷却重氮液中,搅拌10min左右。
4. 结晶与抽滤将烧杯浸入冰水浴中,一边慢慢加入15ml 10%氢氧化钠溶液,一边搅拌。
以上2~4步骤总体系温度不应超过5℃,以免发生冒料危险。
反应后,将烧杯加热,沸腾,使物质溶解,浓缩。
冷却至室温后,置于冰水浴中,使甲基橙结晶沉淀。
5. 收集与干燥抽滤,收集晶体。
抽滤时用饱和氯化钠溶液冲洗烧杯两次,每次10ml左右。
将收集到的晶体移至蒸发皿中,置于烘箱中干燥,得到甲基橙产品。
五、实验结果与分析1. 实验结果通过实验,成功制备了甲基橙产品,其外观为橙红色晶体。
2. 结果分析实验过程中,重氮化反应和偶合反应顺利进行,甲基橙产品产量较高。
甲基橙的制备

甲基橙的制备一.实验目的1.掌握重氮化反应和耦合反应的原理和实验操作。
2.巩固盐析和重结晶的原理和操作。
二.常规制备方法的改进现行制备甲基橙的一般方法都需要在低温下进行重氮盐的制备。
制备步骤是:首先将对氨基苯磺酸碱化成水溶性较好的盐,然后在低温强酸性环境中进行重氮化反应,制得重氮盐,再于醋酸环境中与N,N-二甲基苯胺偶联、碱化中和制得。
这种制备方法在进行重氮化时没有充分利用对氨基苯磺酸本身的酸性在重氮化反应中的作用,而且该方法操作复杂,反应条件不易控制,不利于偶联反应,且粗产品容易变质,尤其是加热溶解时容易变成黑色物质。
故对常规方法进行了改良,改进的关键是在常温时充分利用对氨基苯磺酸自身的酸性来完成重氮化,由于没有外加酸,亚硝酸是由亚硝酸钠与对氨基苯胺酸反应而来,这就避免了因过量亚硝酸而引起的一些副反应,因此也就不需用淀粉碘化钾试纸检验亚硝酸是否过量,使制备过程更简单,而且此方法还降低了试剂损耗,条件易于控制,实验时间缩短。
以下是该方法的实验原理。
三.实验原理甲基橙学名“对二甲基偶氮苯磺酸钠”。
甲基橙广泛应用于生产和科学实验中,常用作酸碱指示计和生物染料,在中性或碱性介质中呈黄色,在酸性介质中(PH<3.0)呈红色。
制备的主要反应方程式如下:四.实验仪器和试剂五.实验步骤●粗甲基橙的合成在干燥的100mL三口瓶上安装电动搅拌机(也可人工搅拌)、滴液漏斗,回流冷凝管,在三口烧瓶中加入2.5g对氨基苯磺酸、1.0g亚硝酸钠和30mL水,搅拌使固体溶解,生成重氮盐。
用移液管量取1.8mLN-N二甲基苯胺和2倍体积的乙醇(同一移量管),加入滴液漏斗中,一边搅拌,一边用滴液漏斗滴加混合液,滴加完毕后还需搅拌30min,再在三口烧瓶中加入3mL1.0mol/L NaOH溶液继续搅拌2min,将该混合液冷却,静置,待片状结晶出现后过滤,得到甲基橙粗品。
●粗产品的纯化将滤饼连同滤纸转移到有10ml热水的烧瓶中,微微加热并且不断地搅拌,滤饼几乎完全溶解后,取出滤纸,溶液冷却至室温,然后在冰水浴中再冷却,使甲基橙晶体析出完全。
甲基橙的制备

甲基橙的制备一、 实验目的:1. 通过甲基橙的制备,学习重氮化反应和偶合反应的实验操作;2. 掌握盐析和重结晶的原理和操作。
二、实验原理:1、重氮化反应2、偶合反应甲基橙可通过对氨基苯磺酸的重氮化反应以及重氮盐与N, N-二甲苯胺的醋 酸盐,在弱酸性介质中进行偶联来合成。
化学反应过程如下:三 试剂与规格亚硝酸钠(C.P.) 浓盐酸(C.P.) 冰醋酸(C.P.) 乙醚(C.P.)对氨基苯磺酸(C.P.) N,N-二甲苯胺(C.P.) 95%乙醇(C.P.) 5%氢氧化钠 四 实验流程五、实验步骤:1、重氮盐的制备在100ml烧杯中、加入2g对氨基苯磺酸结晶和10ml 5%氢氧化钠溶液,温 热使结晶溶解 [1] ,用冰盐浴冷却至0℃以下。
另在一试管中配制0.8g亚硝酸钠和 6ml水的溶液。
将此配制液也加入烧杯中【若不能全溶,可加入适量水】 。
维持 温度0-5℃ [2] ,在搅拌 [3] 下,慢慢用滴管滴入 3ml浓盐酸和10ml水溶液,直至,继续在冰盐浴 用淀粉-碘化钾试纸检测呈现蓝色为止 [4] 【8~10秒显蓝色正好】中放置15分钟,使反应完全,这时往往有白色细小晶体析出 [5] 。
2、偶合反应在试管中加入1.3ml N,N-二甲基苯胺和1ml 冰醋酸,并混匀。
在搅拌下将 此混合液缓慢加到上述冷却的重氮盐溶液中,加完后继续搅拌10min【充分搅 。
此时有红色的酸性黄沉淀,然后在冷却下搅拌,缓缓加入约15ml 5%氢氧 拌】化钠溶液,直至反应物变为橙色(此时反应液为碱性 [6] )。
甲基橙粗品呈细粒状 沉淀析出 [7] 。
将反应物置沸水浴中加热5分钟,冷却后,再放置冰浴中冷却,使甲基橙晶 体析出完全 [8] 。
抽滤搜集晶体,依次用10ml饱和食盐水冲洗烧杯两次、并用这 些冲洗液洗涤产品。
再依次用少量水、乙醇和乙醚洗涤,压紧抽干。
干燥后得粗 品约3g。
粗产品用1%氢氧化钠进行重结晶。
待结晶析出完全,抽滤,依次用少量水、乙醇和乙醚洗涤,压紧抽干,得片状结晶。
实验二十一-甲基橙的制备

实验二十一甲基橙的制备Experiment 21 Preparation of methyl orange[实验目的]1、熟悉重氮化反应和偶合反应的原理。
2、掌握甲基橙的制备方法。
[实验内容]一、实验原理1、重氮化反应芳香族伯胺在低温和强酸溶液中与亚硝酸钠作用,生成重氮盐的反应称为重氮化反应(diazotization)。
由于芳香族伯胺在结构上的差异,重氮化方法也不尽相同。
苯胺、联苯胺及含有给电子基的芳胺,其无机酸盐稳定又溶于水,一般采用顺重氮法,即先把1mol胺溶于2.5-3 mol 的无机酸,于0-5℃加入亚硝酸钠。
含有吸电子基(-SO3H、-COOH)的芳胺,由于本身形成内盐而难溶于无机酸,较难重氮化,一般采用逆重氮化法,即先溶于碳酸钠溶液,再加入亚硝酸钠,最后加酸。
本次实验,甲基橙的制备即采用该方法。
含有一个-NO2、-Cl等吸电子的芳胺,由于碱性弱,难成无机盐,且铵盐难溶于水,易水解,生成的重氮盐又容易与未反应的胺生成重氮氨基化合物(-ArN=N-NHAr),因此多采用先将胺溶于热的盐酸,冷却后再重氮化。
2、偶合反应在弱碱或弱酸性条件下,重氮盐和酚、芳胺类化合物作用,生成偶氮基(-N=N-)将两分子中的芳环偶联起来的反应称为偶联反应(coupling reaction偶合反应)。
偶联反应的实质是芳香环上的亲电取代反应,偶氮基为弱的亲电基,它只能与芳环上具有较大电子云密度的酚类、芳胺类化合物反应。
由于空间位阻的影响,反应一般在对位发生。
若对位已经有取代基,则偶联反应发生在邻位。
重氮盐和酚的反应是在若碱性的介质中进行。
而重氮盐与芳胺的反应是在弱酸环境下进行的。
对于本实验,甲基橙的制备,由于为重氮盐与芳胺的反应,故以冰醋酸为溶剂。
该反应的方程式为:二、实验所需试剂及仪器药品:对氨基苯磺酸、 5%氢氧化钠溶液、亚硝酸钠、浓盐酸、冰醋酸、N, N-二甲基苯胺、乙醇、乙醚、淀粉-碘化钾试纸仪器:烧杯、温度计、表面皿、布氏漏斗三、实验具体操作步骤1、重氮盐的制备在50 mL烧杯中、加入1 g对氨基苯磺酸结晶和5 mL 5%氢氧化钠溶液,温热使结晶溶解,用冰盐浴冷却至0℃以下。
甲基橙的制备

甲基橙的制备一、实验目的1、学习重氮盐制备技术,了解重氮盐的控制条件。
2、掌握和了解重氮盐偶联反应的条件,掌握甲基橙制备的原理及实验方法。
3、进一步练习抽滤,洗涤,搅拌等基本操作。
二、实验原理1、芳香族伯胺在酸性介质中和亚硝酸钠作用下生成重氮盐,重氮盐与芳香叔胺偶联,生成偶氮染料。
将对氨基苯磺酸与氢氧化钠作用生成易溶于水的盐,再重氮化,然后再与N,N—二甲基苯胺偶联得到粗产品甲基橙。
与HNO22、甲基橙制备相关的反应方程式:三、主要试剂及物理性质、浓盐酸、10%NaOH、1、主要药品:对氨基苯磺酸、5%NaOH、N,N-二甲基苯胺、NaNO2饱和氯化钠溶液、95%乙醇、冰乙酸、碘化钾淀粉试纸、pH试纸。
2、主要化合物的物理性质对氨基苯磺酸:一种白色至灰白色粉末,在空气中吸收水分后变为白色结晶体,带有一个分子的结晶水,温度达100℃时失去结晶水,在300℃时开始分解碳化,在冷水中微溶,溶于沸水,微溶于乙醇、乙醚和苯,有明显的酸性,能溶于氢氧化钠溶液和碳酸钠溶液。
用于制造偶氮染料等,也可用作防治麦锈病的农药。
N,N-二甲基苯胺:淡黄色油状,有特殊气味液体,熔点2.5℃,沸点193℃,不溶于水,易溶于醇、醚、苯和酸溶液。
本品剧毒,能使人呼吸短促而致死,车间内气体最高容许浓度为5mg/m3。
:微带淡黄色的白色结晶,密度2.17(20℃),熔点为217℃,易溶于水,微NaNO2溶于乙醇和乙醚,在空气中易潮解。
在320℃时分解生成氧、氮、氧化氮和氧化钠。
与有机物接触易发生燃烧和爆炸,燃烧时放出有毒的氧化氮气体。
能从空气中吸收氧逐渐化为硝酸钠。
亚硝本钠是剧毒品。
四、试剂用量规格1、称取2.00g对氨基苯磺酸;2、量取5%NaOH10ml;3、称取0.8g NaNO2;4、准备冰冷水13ml,实际水80ml;5、吸取1.3ml N,N-二甲基苯胺,冰醋酸1.0ml;6、量取10%NaOH15ml;7、准备饱和氯化钠溶液20ml;8、准备乙醇5ml;五、实验装置1、主要仪器: 100mL烧杯、抽滤瓶、布氏漏斗、刻度吸管、温度计、玻璃棒、台称、试管、pH试纸、10ml量筒、100ml量筒、电炉。
甲基橙的制备实验报告

甲基橙的制备实验报告甲基橙的制备实验报告橙色是一种充满活力和温暖的颜色,它常常让人联想到太阳和快乐。
而甲基橙,作为一种常用的染料,不仅在纺织、印刷和制药等行业得到广泛应用,还在科学实验中扮演着重要的角色。
本文将介绍甲基橙的制备实验,探索其合成原理和实验步骤。
一、实验背景甲基橙,化学式为C14H14N3NaO3S,是一种有机染料,常用于酸碱指示剂、细胞染色和细菌培养基中。
它的制备方法多种多样,其中一种常用的方法是通过苯胺和二甲基亚硝基胺的反应得到。
二、实验原理甲基橙的合成原理基于亲电取代反应。
在反应中,苯胺与亚硝酸钠反应生成二甲基亚硝基胺,然后与苯胺进一步反应生成甲基橙。
这个过程中,亚硝基胺起到了氧化剂的作用,将苯胺氧化为甲基橙。
三、实验材料和仪器1. 苯胺2. 亚硝酸钠3. 硫酸4. 氢氧化钠5. 乙醇6. 锥形瓶7. 滴定管8. 显微镜四、实验步骤1. 在一个锥形瓶中加入15毫升苯胺和15毫升浓硫酸,搅拌均匀。
2. 将锥形瓶置于冰水混合物中冷却15分钟,控制温度在5-10摄氏度。
3. 将10毫升亚硝酸钠溶液滴加到冷却的苯胺硫酸溶液中,同时搅拌。
4. 将反应混合物放置在室温下静置30分钟,观察溶液颜色的变化。
5. 加入适量的氢氧化钠溶液,使溶液呈碱性。
6. 将反应混合物转移到一个锥形瓶中,用乙醇洗涤,直至洗涤液呈淡黄色。
7. 用乙醇溶解甲基橙并过滤,收集纯净的甲基橙晶体。
8. 在显微镜下观察甲基橙晶体的形态和颜色。
五、实验结果与讨论根据实验步骤,我们成功合成了甲基橙。
在实验过程中,我们观察到溶液从无色逐渐变为橙色,这是由于苯胺被氧化生成甲基橙所致。
通过乙醇洗涤和过滤,我们得到了纯净的甲基橙晶体。
甲基橙晶体呈现出橙色,具有良好的溶解性和稳定性。
在显微镜下观察,我们可以看到晶体呈现出规则的结构,这与其分子的有序排列有关。
甲基橙的染色性能优良,可以用于染色细胞和组织,帮助科学家观察和研究细胞结构和功能。
甲基橙的制备试验

一、实验目的
1.通过甲基橙的制备掌握重氮化反应和偶联反应的反应原理和操 作。
2.进一步巩固过滤、洗涤和重结晶等基本操作。
3
当前您浏览的位置是第三页,共九页。
二、实验原理
➢甲基橙是一种酸碱指示剂,pH<3.1,呈红色; pH>4.4,呈红
色;介于两者之间则呈橙色。
SO3Na
HO3S
HCl
C6H5N(CH3)2 HOAC
HO3S
NaOH
NaO3S
NN NN
+ N
N Cl-
+ N(CH3)2 OA
cH
N(CH3)2
当前您浏览的位置是第五页,共九页。
三、仪器和药品
仪器:150 mL烧杯(或锥形瓶) 、抽滤瓶、布氏漏斗、酒精灯、
石棉网、滤纸、玻棒、表面皿、量筒等。
对氨基苯磺酸
+10ml,5%氢氧 化钠
① 温热,溶解
② 加入0.8g亚硝酸 钠溶于6ml水的溶 液,并冰水冷却
①加入3ml盐酸与 10ml水的溶液至酸 性,淀粉KI测试
② 冷却15min
重氮盐
重氮盐
①滴加1.3mlN,N-二甲 基苯胺和1ml醋酸混合 液
②搅拌10min
偶联产物
加入25ml,5%氢氧 化钠至橙色
HO3S
H NN
+
酸式(红色) N(CH3)2 OAc -
NaO3S
NN
N(CH3)2
碱式(黄色)பைடு நூலகம்
4
当前您浏览的位置是第四页,共九页。
➢ 芳香族伯胺在酸性介质中和亚硝酸钠作用下生成重氮盐,重氮盐与芳香 叔胺偶联,生成偶氮染料。
有机化学报告甲基橙制备图文

一、实验目的
• 掌握重氮化反应和耦合反应的原理和实验操作。 巩固盐析和重结晶的原理和操作。
• 学习如何控制温度及该条件下制备甲基橙和在实 验过程中注意的实验事项。
二、实验原理
• 由于制备甲基橙的一般方法需要在低温下进行重 氮盐制备。甲基橙常用作酸碱指示剂,在中性或 碱性介质中呈黄色,在酸性介质中(PH<3.0) 呈红色,制备的主要反映方程式如下:
3、取0.6gN,N—二甲 基苯胺和0.5mL冰醋酸 好,不断搅拌下加入 上述溶液中。继续搅 拌后慢慢加入 12.5mL5%氢氧化钠溶 液。
• 实验现象: • 反应物变为橙色。
五、实验步骤及现象记录
4、将反应物在沸水浴上加热 5min,冷却室温后,再在 冰水浴中冷却。最后抽虑
实验现象:表面不断有气泡 冒出,冷却有晶体析出, 抽滤后得到红棕色晶体和 滤液。
• 实验现象: • 固体溶解
五、实验步骤及现象记录
2、溶0.4g亚硝酸钠于3mL水 中,加入上述烧杯内,用 冰盐浴冷却并不断搅拌。 搅拌期间将1.5mL浓盐酸 与5mL配成的溶液缓缓加 入混合溶液中,用淀粉— 碘化钾试纸检验。
• 实验现象:
• 溶液颜色为无色。
• 淀粉—碘化钾试纸呈紫 色。
五、实验步骤及现象记录
七、实验结果分析与讨论
结果分析: 产率=0.74÷1×100%=74%
讨论:得到的甲基橙产品产率较低。实验过程中,在用冰盐 浴冷却时,不能控制好温度。检验甲基橙时,颜色的反应 ,明确为甲基橙无误,但是未精制,所得到的甲基橙产品 纯度应该不高。
指导老师:熊兵
谢谢观赏!
2020/11/5
13
五、实验步骤及现象记录
甲基橙的制备实验报告

甲基橙的制备实验报告甲基橙是一种常用的有机合成试剂,广泛应用于生物化学实验和工业生产中。
本实验旨在通过苯甲醛和N,N-二甲基苯胺的反应制备甲基橙,并对其制备过程进行详细记录和分析。
实验步骤:1. 实验前准备,取一定量的苯甲醛和N,N-二甲基苯胺,准备好硫酸和氢氧化钠溶液。
2. 将苯甲醛溶解于乙醇中,加入少量氢氧化钠溶液进行中和。
3. 将N,N-二甲基苯胺溶解于乙醇中,加入硫酸溶液进行中和。
4. 将步骤2和步骤3中的溶液缓慢混合,观察反应过程并记录。
5. 过滤得到沉淀物,用乙醇洗涤并干燥,得到甲基橙产物。
实验结果:经过实验操作,成功合成了甲基橙产物。
产物为橙色粉末状固体,纯度较高。
通过红外光谱和质谱分析,确认了产物的结构和纯度。
实验讨论:甲基橙的制备过程中,苯甲醛和N,N-二甲基苯胺发生了偶联反应,生成了目标产物。
在反应过程中,硫酸和氢氧化钠起到了催化剂和中和剂的作用,促进了反应的进行。
通过实验操作,我们验证了甲基橙的制备方法,并对产物的性质进行了初步分析。
实验结论:本实验成功合成了甲基橙,并对其进行了初步表征。
实验结果表明,所得产物的纯度较高,符合预期要求。
通过本实验,我们进一步了解了甲基橙的制备方法和相关性质,为今后的实验和应用奠定了基础。
总结:甲基橙是一种重要的有机合成试剂,其制备方法简单,产物纯度高。
本实验通过详细的操作记录和结果分析,验证了甲基橙的制备方法,并对产物进行了初步表征。
通过实验,我们对甲基橙的制备过程有了更深入的了解,为今后的实验和应用提供了参考。
以上为甲基橙的制备实验报告,希望对相关研究和实验工作有所帮助。
甲基橙的制备
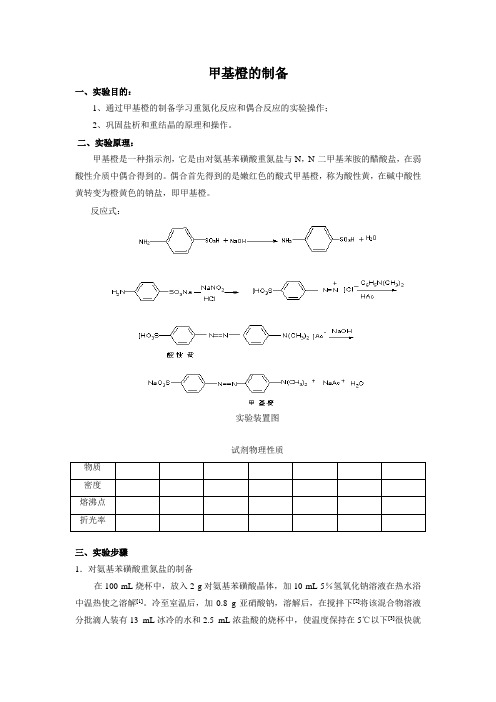
甲基橙的制备一、实验目的:1、通过甲基橙的制备学习重氮化反应和偶合反应的实验操作;2、巩固盐析和重结晶的原理和操作。
二、实验原理:甲基橙是一种指示剂,它是由对氨基苯磺酸重氮盐与N,N-二甲基苯胺的醋酸盐,在弱酸性介质中偶合得到的。
偶合首先得到的是嫩红色的酸式甲基橙,称为酸性黄,在碱中酸性黄转变为橙黄色的钠盐,即甲基橙。
反应式:实验装置图试剂物理性质三、实验步骤1.对氨基苯磺酸重氮盐的制备在100 mL烧杯中,放入2 g对氨基苯磺酸晶体,加10 mL 5%氢氧化钠溶液在热水浴中温热使之溶解[1]。
冷至室温后,加0.8 g亚硝酸钠,溶解后,在搅拌下[2]将该混合物溶液分批滴人装有13 mL冰冷的水和2.5 mL浓盐酸的烧杯中,使温度保持在5℃以下[3]很快就有对氨基苯磺酸重氮盐的细粒状白色沉淀[4],为了保证反应完全,继续在冰浴中放置15 min。
2.偶合在一支试管中加入1.3 mL N,N—二甲基苯胺和1 mL冰醋酸,振荡使之混合。
在搅拌下将此溶液慢慢加到上述冷却的对氨基苯磺酸重氮盐溶液中,加完后,继续搅拌10 min,此时有红色的酸性黄沉淀,然后在冷却下搅拌,慢慢加入15 mL 10%氢氧化钠溶液。
反应物变为橙色,粗的甲基橙细粒状沉淀析出。
将反应物加热至沸腾,使粗的甲基橙溶解后,稍冷,置于冰浴中冷却,待甲基橙全部重新结晶析出后,抽滤收集结晶。
用饱和氯化钠水溶液冲洗烧杯两次,每次用10 mL,并用这些冲洗液洗涤产品[5]。
若要得到较纯的产品,可将滤饼连同滤纸移到装有75 mL热水的烧瓶中,微微加热并且不断搅拌,滤饼几乎全溶后,取出滤纸让溶液冷却至室温,然后在冰浴中再冷却,待甲基橙结晶全析出后,抽滤。
依次用少量乙醇、乙醚洗涤产品[6]。
产品干燥后,称重,产量2.5 g (产率75%)。
产品没有明确的熔点,因此不必测定其熔点。
溶解少许产品于水中,加几滴稀盐酸,然后用稀氢氧化钠溶液中和,观察溶液的颜色有何变化[7]。
甲基橙的制备实验报告

有机化学实验报告实验名称:甲基橙的制备学院:化学工程学院专业:化学工程与工艺班级:化工xx班姓名:xxx 学号xxx指导教师:日期:2013年xx月18日一、 实验目的1. 通过甲基橙的制备学习重氮化反应和偶合反应的实验操作;2. 巩固盐析和重结晶的原理和操作。
二、实验原理NH 2SO 3HNaOH NH 2SO 3Na NaNO 2HClNSO 3H N ClN CH 3CH 3HAcNSO 3H NNH(CH 3)2AcNaOHN NN(CH 3)2NaO 3S三、 主要试剂及用量四、 仪器装置烧杯,量筒,玻璃棒,滴管,电磁炉,抽虑装置,表面皿实验 试剂对氨基苯磺酸5%NaOHNaNO 2浓盐酸N,N-二甲基苯胺冰醋酸10%NaOH饱和NaCl乙醇乙醚试剂用量2.00g10.00 ml0.80 g2.50 ml1.30 ml1.00 ml15.00 ml20.00ml少量五、实验步骤及现象理论上2.00g的对氨基苯磺酸可得到甲基橙的质量:=(2.00g×327.33g/mol)÷173.83g/mol=3.77g;m1实验的产率:ω=(2.7g÷3.77g)×100%=71.6%。
七、实验讨论1、本次的实验产率可能有一点偏低。
2、没有控制好实验温度,会降低产率。
3、冷却时间不够长,导致晶体未完全析出。
甲基橙的制备

H2N
SO3H + NaOH
H2N
SO3Na + H2O
合 成 路 线
NaNO2 HCl
HO3S
N N Cl
CH3 N
CH3
HOAc
CH3
NaOH
O3S
NN
N
H
CH3
ቤተ መጻሕፍቲ ባይዱ
酸性黄(红色)
NaO3S
NN
CH3 N
甲基橙
CH3
实验试剂和仪器
仪器: 50mL 烧杯 抽滤瓶
锥形瓶、 砂芯漏斗
试剂: 对氨基苯磺酸(2.1g) 亚硝酸钠(0.8g) N,N-二甲基苯胺(1.3ml) 浓盐酸; 氢氧化钠(5%) 淀粉-碘化钾试纸等.
主要试剂及产品的物理常数
名称
分子量
对氨基苯磺酸 173.2
N, N-二甲苯 胺
121.18
甲基橙
327.33
性状
白色 晶体 无色 液体 橙色 晶体
折光率 比重
熔点℃
280 开始碳 化
溶解度:克/100 mL溶
沸点℃
剂
水
醇醚
0.8/10℃ 不溶 不溶
1.5582 0.9563
193 不溶 ∞ ∞
300
4、N,N-二甲基苯胺与重氮盐偶合为什么总是在氨基的
对位上发生?
5、重结晶操作应迅速,否则由于产物呈碱性, 在温度高时易使产物变质,颜色变深。用乙醇、 乙醚洗涤的目的是使其迅速干燥。
思考题
1、什么叫偶联反应?试结合本实验讨论一下偶联反应的 条件。
2、试解释甲基橙在酸碱介质中的变色原因,并用反应式 表示。
3、在本实验中,重氮盐的制备为什么要控制在0-5℃中 进行?偶合反应为什么在弱酸性介质中进行?
甲基橙的合成实验报告

甲基橙的合成实验报告甲基橙的合成实验报告橙色是一个充满活力和温暖的颜色,它代表着阳光和希望。
而甲基橙,则是一种常见的有机染料,其鲜艳的橙色常被用于染料工业和生物学实验中。
本实验旨在通过合成甲基橙,了解有机合成的基本原理和实验操作技巧。
一、实验原理甲基橙的化学结构为C14H14N3NaO3S,它是一种偶氮染料。
合成甲基橙的方法主要有两种:一种是通过苯胺和亚硝酸钠反应生成偶氮化合物,再与萘胺发生偶联反应得到甲基橙;另一种是通过苯胺和甲酸反应生成偶氮化合物,再与N-甲基苯胺发生偶联反应得到甲基橙。
本实验采用第一种方法进行合成。
二、实验步骤1. 实验前准备:准备好所需的试剂和仪器设备,包括苯胺、亚硝酸钠、萘胺、稀盐酸、氢氧化钠、醋酸等。
2. 反应制备:将苯胺溶解在稀盐酸中,加入亚硝酸钠溶液搅拌,反应生成偶氮化合物。
3. 偶联反应:将萘胺溶解在稀盐酸中,缓慢滴加偶氮化合物溶液,搅拌反应,生成甲基橙。
4. 结晶和过滤:将反应混合物加热浓缩,使甲基橙结晶,然后用冷水洗涤结晶物质,最后用滤纸过滤。
5. 纯化和干燥:将过滤得到的甲基橙溶解在少量醋酸中,加热浓缩,得到纯净的甲基橙溶液。
将溶液倒入干燥皿中,放置于通风处晾干,得到干燥的甲基橙。
三、实验结果与讨论通过上述实验步骤,我们成功合成了甲基橙。
合成的甲基橙呈现出明亮的橙色,符合预期的颜色。
在实验过程中,我们需要注意控制反应的温度和反应时间,以避免产生副产物或产率下降。
甲基橙是一种有机染料,在染料工业中有广泛的应用。
它可以用于染色纺织品、皮革和纸张等材料,赋予它们鲜艳的颜色。
此外,甲基橙还常被用于生物学实验中,作为染色剂用于细胞和组织的显微镜观察。
在实验中,我们还可以对甲基橙进行一些性质测试和分析。
例如,可以通过紫外-可见光谱分析甲基橙的吸收峰,从而确定其化学结构和纯度。
同时,也可以通过溶解度测试、熔点测定等方法对甲基橙进行进一步的表征。
四、实验总结通过本次实验,我们了解了甲基橙的合成原理和实验操作技巧。
甲基橙的制备

NaNO2 HCl
+
NH2
SO 3Na
SO 3H
N
N
Cl
-
2.偶联 2.偶联
①在一支试管中加入1.3mLN,N-二甲基苯胺和 在一支试管中加入 , 二甲基苯胺和1mL冰 冰 二甲基苯胺和 醋酸,振荡混合。 醋酸,振荡混合。 ②在搅拌下,将此液慢慢加到上述冷却的重氮盐中(此 在搅拌下,将此液慢慢加到上述冷却的重氮盐中( 间应始终保持低温操作),搅拌10min。 ),搅拌 间应始终保持低温操作),搅拌 。 至为橙色, ③继续搅拌,慢慢加入25mL10%NaOH至为橙色,粗甲 继续搅拌,慢慢加入 至为橙色 基橙呈细粒状沉淀析出。 基橙呈细粒状沉淀析出。
பைடு நூலகம்
4.重结晶 4.重结晶 将滤饼连同滤纸移到装有75mL热水中微热搅拌, 热水中微热搅拌 ①将滤饼连同滤纸移到装有 热水中微热搅拌, 全溶后,冷却至室温, 全溶后,冷却至室温,冰浴冷却至甲基橙结晶全部 析出,抽滤。 析出,抽滤。 滤饼依次用少量无水乙醇、乙醚洗涤产品。 ②滤饼依次用少量无水乙醇、乙醚洗涤产品。压 紧抽干。 紧抽干。 产品转移至表面皿上, ③产品转移至表面皿上,于50℃以下自然晾干, ℃以下自然晾干, 称重,计算产率。 称重,计算产率。
NH2 SO 3H
+
NaOH
NH2
SO 3Na
+ H2O
亚硝酸钠溶于6mL水中,加到上述烧杯 水中, ②另取0.8g亚硝酸钠溶于 另取 亚硝酸钠溶于 水中 用冰盐水浴冷却至0~ ℃ 中,用冰盐水浴冷却至 ~5℃。
亚硝酸钠易溶于水。 亚硝酸钠易溶于水。
二、实验步骤
1.对氨基苯磺酸重氮盐的制备 1.对氨基苯磺酸重氮盐的制备 在搅拌下, 浓盐酸与10mL水配制成的溶 ③在搅拌下,将3mL浓盐酸与 浓盐酸与 水配制成的溶 缓慢滴加到上述混合液中。 液缓慢滴加到上述混合液中。此间应注意控制反应液 温度在5℃以下(可用温度计间歇测温)。滴加完毕, )。滴加完毕 温度在 ℃以下(可用温度计间歇测温)。滴加完毕, 用淀粉-碘化钾试纸检验反应终点 碘化钾试纸检验反应终点。 用淀粉 碘化钾试纸检验反应终点。然后在冰盐水浴 中继续搅拌15min,以保证反应完全。 中继续搅拌 ,以保证反应完全。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验二十一甲基橙的制备
Experiment 21 Preparation of methyl orange
[实验目的]
1、熟悉重氮化反应和偶合反应的原理。
2、掌握甲基橙的制备方法。
[实验内容]
一、实验原理
1、重氮化反应
芳香族伯胺在低温和强酸溶液中与亚硝酸钠作用,生成重氮盐的反应称为重氮化反应(diazotization)。
由于芳香族伯胺在结构上的差异,重氮化方法也不尽相同。
苯胺、联苯胺及含有给电子基的芳胺,其无机酸盐稳定又溶于水,一般采用顺重氮法,即先把1mol胺溶于 mol 的无机酸,于0-5℃加入亚硝酸钠。
含有吸电子基(-SO3H、-COOH)的芳胺,由于本身形成内盐而难溶于无机酸,较难重氮化,一般采用逆重氮化法,即先溶于碳酸钠溶液,再加入亚硝酸钠,最后加酸。
本次实验,甲基橙的制备即采用该方法。
含有一个-NO2、-Cl等吸电子的芳胺,由于碱性弱,难成无机盐,且铵盐难溶于水,易水解,生成的重氮盐又容易与未反应的胺生成重氮氨基化合物(-ArN=N-NHAr),因此多采用先将胺溶于热的盐酸,冷却后再重氮化。
2、偶合反应
在弱碱或弱酸性条件下,重氮盐和酚、芳胺类化合物作用,生成偶氮基(-N=N-)将两分子中的芳环偶联起来的反应称为偶联反应(coupling reaction偶合反应)。
偶联反应的实质是芳香环上的亲电取代反应,偶氮基为弱的亲电基,它只能与芳环上具有较大电子云密度的酚类、芳胺类化合物反应。
由于空间位阻的影响,反应一般在对位发生。
若对位已经有取代基,则偶联反应发生在邻位。
重氮盐和酚的反应是在若碱性的介质中进行。
而重氮盐与芳胺的反应是在弱酸环境下进行的。
对于本实验,甲基橙的制备,由于为重氮盐与芳胺的反应,故以冰醋酸为溶剂。
该反应的方程式为: NH 2
SO 3H NaOH
H 2O
NH 2
SO 3-Na +
++
NH 2
SO 3-Na +
N +HO 3S
N
Cl -
C 6H 5N(CH 3)2
N HO 3S
N
NH(CH 3)2
+
OAc -
NaOH
N NaO 3S
N
N(CH 3)2
NaAc
++
H 2O
二、实验所需试剂及仪器
药品:对氨基苯磺酸、?5%氢氧化钠溶液、? 亚硝酸钠、? 浓盐酸?、 冰醋酸 、N, N -二甲基苯胺、乙醇、乙醚、淀粉-碘化钾试纸 仪器:烧杯、温度计、表面皿、布氏漏斗 三、实验具体操作步骤 1、重氮盐的制备
在50 mL 烧杯中、加入1 g 对氨基苯磺酸结晶和5 mL 5%氢氧化钠溶液,温热使结晶溶解,用冰盐浴冷却至0℃以下。
另在一试管中配制 g 亚硝酸钠和3 mL 水配成的溶液。
将此配制液也加入烧杯中。
维持温度0-5℃,在搅拌下,慢慢用滴管滴入 mL 浓盐酸和5 mL 水配成的溶液,直至用淀粉-碘化钾试纸检测呈现蓝色为止,继续在冰盐浴中放置15 min ,使反应完全,这时往往有白色细小晶体析出。
2、偶合反应
在试管中加入 mL N, N -二甲基苯胺和 mL 冰醋酸,并混匀。
在搅拌下将此混合液缓慢加到上述冷却的重氮盐溶液中,加完后继续搅拌10 min 。
缓缓加入约15 mL 5%氢氧化钠溶液,直至反应物变为橙色(此时反应液为碱性)。
甲基橙粗品呈细粒状沉淀析出。
将反应物置沸水浴中加热5 min ,冷却后,再放置冰浴中冷却,使甲基橙晶体析出完全。
抽滤,依次用少量水、乙醇和乙醚洗涤,压紧抽干。
干燥后得粗品。
3、纯化
粗产品用1% 氢氧化钠进行重结晶。
待结晶析出完全,抽滤,依次用少量水、乙醇和乙醚洗涤,压紧抽干,得片状甲基橙结晶。
称重并计算产率。
4、将少许甲基橙溶于水中,加几滴稀盐酸,然后再用稀碱中和,观察并记录颜色变化。
四、实验关键及注意事项
1、对氨基苯磺酸为两性化合物,酸性强于碱性,它能与碱作用成盐而不能与酸作用成盐。
2、重氮化过程中,应严格控制温度,反应温度若高于5℃,生成的重氨盐易水解为酚,降低产率。
3、若试纸不显色,需补充亚硝酸钠溶液。
4、重结晶操作要迅速,否则由于产物呈碱性,在温度高时易变质,颜色变深。
用乙醇和乙醚洗涤的目的是使其迅速干燥。
五、思考题
1、在重氮盐制备前为什么还要加入氢氧化钠如果直接将对氨基苯磺酸与盐酸混合后,再加入亚硝酸钠溶液进行重氮化操作行吗为什么???
2、制备重氮盐为什么要维持0-5℃的低温,温度高有何不良影响
3、重氮化为什么要在强酸条件下进行偶合反应为什么要在弱酸条件下进行
4、试解释甲基橙在酸碱介质中的变色原因,并用反应式表示。
5、预习下次实验并做好预习报告
附:主要试剂及产品的物理常数(文献值)。
