化学1:第一单元 丰富多彩的化学物质复习课0
苏教版高一化学必修一专题一第一单元 丰富多彩的化学物质 课件(共23张PPT)

⑴按物质的组成分类
混合物: 空气、碘酒、食盐水
单质: 铜、碘、氧气、石墨
乙醇 化合物:
水、硫酸铵
(有机化合物)
(无机化合物)
空气、乙醇(C2H5OH)、水、硫酸铵、铜、碘酒、 碘(I2)、氧气、石墨、食盐水。
⑵按物质的状态(常温下)分类
固态: 硫酸铵、铜、碘、石墨 液态: 乙醇、水 、碘酒、食盐水 气态: 空气、氧气
专题1 化学家眼中的物质世界
第一单元 丰富多彩的化学物质
第一节 物质的分类与转化
交流与讨论
将下列物质进行分类,并说明分类的依据。
空气、乙醇(C2H50H)、水、 硫酸铵、 铜、 碘酒、 碘(I2)、 氧气、 石墨、 食盐水
空气、乙醇(C2H5OH)、水、硫酸铵、铜、 碘酒、碘(I2)、氧气、石墨、食盐水。
空气、乙醇(C2H5OH)、水、硫酸铵、铜、碘酒、 碘(I2)、氧气、石墨、食盐水。
⑶按物质的导电性分类 导体: 铜、石墨、食盐水、 绝缘体: 空气、乙醇、水、碘酒、碘、氧气
硫酸铵晶体不导电,其水溶液能导电。
空气、乙醇(C2H5OH)、水、硫酸铵、铜、碘酒、 碘(I2)、氧气、石墨、食盐水。 ⑷按物质在水中的溶解能力分类 易溶: 乙醇、 硫酸铵、食盐水、水、碘酒 微溶: 碘、氧气 难溶: 空气、铜、石墨
强碱 NaOH、KOH、Ca(OH) 2、Ba(OH)2
碱
从碱性强
弱分
弱碱
NH3·H2O 、Cu(OH)2、 Mg(OH)2、Fe(OH) 3
……
物质的分类
从是否溶 于水分
按组成 离子分 盐
可溶盐
难溶盐 钠盐 钾盐 氨盐
NaCl、AgNO3、CuSO4
CaCO3、BaSO4、ZnS
1.1《丰富多彩的化学物质》教案1(苏教版必修1)

高中化学—苏教版(必修1)第一章—化学家眼中的物质世界第一单元丰富多彩的化学世界【课标内容】1. 知道化学是在分子层次上认识物质和合成新物质的一门科学;了解物质的组成、结构和性质的关系;认识化学变化的本质。
2. 认识摩尔是物质的量的基本单位,能用于进行简单的化学计算,体会定量研究的方法和学习化学的重要作用。
3.认识并欣赏化学科学对提高人类生活质量和促进社会发展的重要作用。
4.能根据物质的组成和性质对物质进行分类。
尝试按不同的方法对物质进行分类。
5.知道胶体是一种常见的分散系。
6.知道酸、碱、盐在溶液中能发生电离。
7.正确认识科学、技术与社会的相互作用,能运用所学知识解释生产、生活中的化学现象,解决与化学有关的一些实际问题。
赞赏化学科学对个人生活和社会发展的贡献,关注与化学有关的社会热点问题。
初步树立社会可持续发展的思想。
【课标解读】从不同角度研究物质的分类和转化,是化学家研究物质及其变化的重要内容。
通过本单元的学习,既可以让学生了解研究化学物质的一般方法,又可以让学生从分子层次上对化学物质有一个大致的了解。
本单元教材以“物质的分类及转化”、“物质的量”、“物质的聚集状态”、“物质的分散系”等化学物质的一般属性为主线进行编写的。
物质的分类和转化实质是分子等微观粒子的变化;物质的量是将微观粒子与宏观质量相联系的基本物理量,帮助实现物质转化过程中的定量研究;物质聚集状态的变化实质是分子等微观粒子间相互作用的变化和分子间距离的变化,同时很自然地引出了“气体摩尔体积”的基本概念;物质的分散系也涉及分子等微观粒子。
所以本单元内容实质上是在引导学生以化学的眼光、从微观的角度去认识丰富多彩的物质世界,使学生认识到宏观和微观的相互转化是研究化学的科学方法之一。
这样编写一方面可以与初中化学进行合理衔接,另一方面又为高中化学后续内容的学习准备必要的基础知识。
在初中化学的学习中,学生已掌握了一些化学反应,知道化学反应的四种基本类型和物质转化的一些实例,但初中化学中没有系统学习和研究有关酸、碱、盐、氧化物等物质之间的转化规律,没有对这些物质的转化反应进行整理总结。
化学必修1专题1第一单元丰富多彩的化学物质(共15张PPT)

昨日的明天是今天。明天的昨日是今天。为什么要计较于过去呢(先别急着纠正我的错误,你确实可以在评判过去中学到许多)。但是我发现有的人过分地瞻前顾后了。为 何不想想“现在”呢?为何不及时行乐呢?如果你的回答是“不”,那么是时候该重新考虑一下了。成功的最大障碍是惧怕失败。这些句子都教育我们:不要惧怕失败。如 果你失败了他不会坐下来说:“靠,我真失败,我放弃。”并且不是一个婴儿会如此做,他们都会反反复复,一次一次地尝试。如果一条路走不通,那就走走其他途径,不 断尝试。惧怕失败仅仅是社会导致的一种品质,没有人生来害怕失败,记住这一点。宁愿做事而犯错,也不要为了不犯错而什么都不做。不一定要等到时机完全成熟才动手。 开头也许艰难,但是随着时间的流逝,你会渐渐熟悉你的事业。世上往往没有完美的时机,所以当你觉得做某事还不是时候,先做起来再说吧。喜欢追梦的人,切记不要被 梦想主宰;善于谋划的人,切记空想达不到目标;拥有实干精神的人,切记选对方向比努力做事重要。太阳不会因为你的失意,明天不再升起;月亮不会因为你的抱怨,今 晚不再降落。蒙住自己的眼睛,不等于世界就漆黑一团;蒙住别人的眼睛,不等于光明就属于自己!鱼搅不浑大海,雾压不倒高山,雷声叫不倒山岗,扇子驱不散大雾。鹿 的脖子再长,总高不过它的脑袋。人的脚指头再长,也长不过他的脚板。人的行动再快也快不过思想!以前认为水不可能倒流,那是还没有找到发明抽水机的方法;现在认 为太阳不可能从西边出来,这是还没住到太阳从西边出来的星球上。这个世界只有想不到的,没有做不到的!不是井里没有水,而是挖的不够深;不是成功来的慢,而是放 弃速度快。得到一件东西需要智慧,放弃一样东西则需要勇气!终而复始,日月是也。死而复生,四时是也。奇正相生,循环无端,涨跌相生,循环无端,涨跌相生,循环 无穷。机遇孕育着挑战,挑战中孕育着机遇,这是千古验证了的定律!种子放在水泥地板上会被晒死,种子放在水里会被淹死,种子放到肥沃的土壤里就生根发芽结果。选
苏教版高中化学必修一复习资料

重结晶 混合物中各组分在溶剂中的溶解度随温度变化不同 烧杯及过滤仪器 从氯化钠和硝酸钾的混合物中提纯硝酸钾 ①一般先配制较高温度的饱和溶液,然后降温结晶
(3) 从物质的状态分类:气体物质、液体物质和固态物质。
(4) 从物质在水中的溶解能力分类:可将物资分为可溶、难溶。
另外,还可以从物质的用途、物质的来源等其他角度对它们进行分类。
二、 物质的转化
1. 物质的性质及其变化
(1) 物质的性质
物理性质 物质不需要经过化学反应直接表现出来的性质。如:颜色、状态、气味、熔点、沸点、密度、硬度等 化学性质 物质在发生化学反应时表现出来的性质。如:酸性、碱性、氧化性、还原性、可燃性、稳定性等 (2) 物质的变化
(二) 配制一定物质的量浓度的溶液
1. 配制物质的量浓度溶液主要配制仪器
托盘天平(以固体、容量瓶、
胶头滴管
2. 配制物质的量浓度溶液步骤如下:
杂变沉:加入一种试剂将要除去的杂质变成沉淀,最后用过滤的方法除去沉淀。
化为气:加热或加入一种试剂使杂质变为气体逸出。如食盐水中混有Na2CO3,则可加盐酸使CO32-变CO2逸出。
溶剂分:加入一种试剂将杂质或被提纯物质萃取出来。如用CCl4可将碘从水中萃取出来。
(3) 物质分离和提纯的常用方法
和分离的主要区别在于除掉后的杂质可以不进行恢复。
①物质提纯的原则:不增、不变、易分。
所谓不增,是指在提纯过程中不增加新物质,不变指被提纯的物质性质不能改变,易分是指使杂质与被提纯物质容易分开。
苏教化学必修1专题1第一单元丰富多彩的化学物质(共18张PPT)

CO2+H2O====H2CO3
NaOH +HCl====NaCl+H2O
点燃
2KClO3====2KCl+3O2 Fe +CuSO4====FeSO4+Cu
碳酸钙生成氧化钙 二氧化碳生成葡萄糖
(2)按反应类型研究物质的转化
结论
化合反应
分解反应
氧化还原反应
置换反应
复分解反应
钠、氯气、氯化铁溶液、硫酸、碳酸钙、氧化钙、 氢氧化钠 葡萄糖
答案: 混合物:
氯化铁溶液
单质:
钠、氯气
氧化物:
氧化钙
酸: 碱: 盐: 有机化合物:
硫酸 氢氧化钠 碳酸钙 葡萄糖
交流与讨论:
在我们的日常生活中,常会接触到下列物质,请你按一定的依据 对上述物质进行分类:
空气、铜、酒精、硫酸铵、碘酒、碘、氢气、石墨、食盐水、
物质的分类
从是否溶 于水分
从组成离 子分
盐
从酸根是 否含氧分
……
可溶盐 难溶盐 钠盐 钾盐
氨盐
NaCl、AgNO3、CuSO4
CaCO3、BaSO4、ZnS
硫酸盐 碳酸盐
……
硝酸盐
含氧酸盐 无氧酸盐
KNO3、KMnO4、FeSO4 NaCl、ZnS、CaCl2
练习:
根据物质的组成对下列物质进行分类:
酸
从酸性
强弱分
中强酸
Hale Waihona Puke H3PO4……弱酸
H2CO3
物质的分类
从是否溶 于水分
专题一第一单元丰富多彩的化学物质期末复习

专题一 第一单元 丰富多彩的化学物质一 物质的分类及转化1、物质的分类(1) 单质 金属:钠、镁、铝、铁 非金属:碳、硫(2)氧化物酸性(酸酐):SO 2 CO 2 碱性:Na 2O Fe 2O 3 两性:Al 2O 3 不成盐氧化物:CO NO(3)酸按是否含氧分(含氧酸:H 2SO 4 不含氧酸:HCl )按挥发性分(难挥发性酸:如H 2SO 4 易挥发性酸:如浓HCl 浓HNO 3)(4)碱溶解性(可溶性碱:如NH 3·H 2O NaOH Ba(OH)2 难溶性碱:如Mg(OH)2 Fe(OH)3 Al(OH)3)(5)盐正盐:如Na 2CO 3 NH 4NO 3 酸式盐:如NaHSO 4 KHSO 3 NaHCO 3 碱式盐:如Cu 2(OH)2CO 3)2、物质的转化规律3四种基本反应类型:化合、分解、置换、复分解。
课堂练习一1、下列叙述正确的是( )。
(写出正确答案,并将每个选项错误的原因改写在后面)A. 碱性氧化物一定是金属氧化物B. 凡酸性氧化物都能直接与水反应生成对应的酸C. 酸分子中有几个H 原子即为几元酸D. 盐电离时,只生成一种阳离子,一种阴离子E. 金属氧化物都是碱性氧化物F. 凡非金属氧化物都是酸性氧化物3 ( )4、某药品说明书中标明:本品每克含碘150mg ,镁65mg ,锌1.5mg ,锰1mg,这里的碘、镁、锌、锰是指 ( )A.分子B.原子C.元素D.物质5、下列反应中,不属于氧化还原反应的是 ( )A .Na 2O+CO 2=Na 2CO 3B .CH 4 + 2O 2CO 2+ 2H 2O C .Na 2O 2+SO 2=Na 2SO 4 D .Fe + SFeS二物质的量及其应用1、物质的量(1)定义:科学上用来研究一定数目微粒集体的一个物理量。
符号:n. 单位:摩尔(mol)。
(2)基准:以0.012kg 126c 中所含的碳原子数为基准,即阿伏加德罗常数。
苏教版高一化学必修一专题一第一单元 丰富多彩的化学物质 课件(共21张PPT)

(5)稀盐酸 (6)HNO3 (8)Na2SO4 (9)CH3COOH
电解质与非电解质
常见的电解质 酸、碱、盐属于电解质
常见的非电解质
葡萄糖、淀粉、油脂等大部分有机物, 非金属氧化物属于非电解质
重点深化
电解质的电离通常用电离方程式表示 根据示意图你能写出NaCl在水中电离的方 程式吗?
电解质溶于水后生 成水合离子,但为 了书写方便,常写 成简单离子的形式
概念理解
盐酸能导电,盐酸是电解质吗? 金属铜能导电,铜是电解质吗? CO2溶于水所得溶液能导电,它是电 解质吗? NaCl是电解质,NaCl固体能导电吗?
电离需要通电吗?
练习
指出下列哪些物质是电解质,哪些物质是非电
解质
(1)NaOH (2) HCl (3) Fe
(4)酒精 (7)食盐水
(10)CO2
1nm = 10-9m
问题解决 怎样用实验鉴别分散系是溶液还是胶体? 当光束通过胶体时,在垂直于光线的方向可以 看到一条光亮的通路 —— 丁达尔效应
实验室中利用丁达尔效应区别溶液和胶体。
美丽的大自然 自然界的丁达尔现象—— 雾也是一种胶体
实验2
在两只试管中分别加入相同量的含有悬浮颗粒物 的浑浊的水,再向其中一只试管中加入适量氢氧 化铁胶体,搅拌后静置片刻,比较两只烧杯中液 体的浊度。
2ml 黄色浑浊
是否均匀混合物 均匀
均匀
不均匀
分散质颗粒大小 很小
很小
比较大
分散系种类
溶液
溶液?
浊液
激光笔照射 透过无光柱 透过有光柱 不透无光柱
不同光照效果的 原因
本质区别: 分散质粒子直径由小到大,量变引起质变
分散系
高一化学第一单元 丰富多彩的化学物质 复习学案
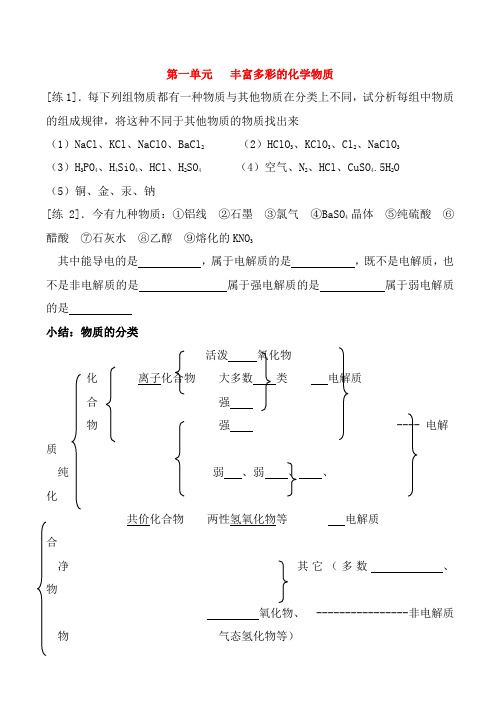
第一单元丰富多彩的化学物质[练1].每下列组物质都有一种物质与其他物质在分类上不同,试分析每组中物质的组成规律,将这种不同于其他物质的物质找出来(1)NaCl、KCl、NaClO、BaCl2(2)HClO3、KClO3、Cl2、NaClO3(3)H3PO4、H4SiO4、HCl、H2SO4(4)空气、N2、HCl、CuSO4.5H2O(5)铜、金、汞、钠[练2].今有九种物质:①铝线②石墨③氯气④BaSO4晶体⑤纯硫酸⑥醋酸⑦石灰水⑧乙醇⑨熔化的KNO3其中能导电的是,属于电解质的是,既不是电解质,也不是非电解质的是属于强电解质的是属于弱电解质的是小结:物质的分类化离子化合物电解质合物强 ---- 电解质纯弱、弱、、化共价化合物两性氢氧化物等电解质合净其它(多数、物氧化物、 ----------------非电解质物气态氢化物等)单金属质 ----- 既不是电解质也不是非电解质非金属混非均匀混合物 ----浊液合溶液物均匀混合物胶体[ ][变1-1] 下列各物质的分类、名称(或俗名)、化学式都正确的是A.碱性氧化物氧化铁 FeO B.酸性氧化物碳酸气 C0C.酸硫酸 H2S D.盐纯碱 Na2CO3[变1-2]从H、O、S、K四种元素中选择适当的元素,组成与表中第一栏物质类别相同的物质,将其化学式填在表中相应空格内。
[ ][练3].Na2O、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为同一类物质,下列分类标准正确的是①钠的化合物②能与硝酸反应的物质;③可溶于水的物质;④电解质;⑤钠盐;⑥钠的含氧化合物A.①③④ B.①②⑤⑥ C.②⑤⑥ D.①②④⑤小结:二、单质、氧化物酸、碱、盐等物质之间的相互转化关系注意:复分解反应的条件:金属与盐溶液的置换条件:[ ][练4].以NA为阿伏加德罗常数的值,下列说法正确的是A.NA 个N2分子与NA个CO分子的质量比为1∶1B.水的摩尔质量等于NA个水分子的相对分子质量之和C.1 mol O2的质量等于NA个氧原子的质量D.分别由NA个水分子组成的冰、水、水蒸气的质量各不相同小结:三、有关物质的量、阿伏加德罗常数、摩尔质量、气体摩尔体积等概念注意:(1)物质的量度量的对象是微粒集体,微粒可以是分子、原子、离子、电子、中子、质子等。
苏教化学必修1专题1第一单元丰富多彩的化学物质(共15张PPT)

★
26. 如果你为自己定的所有目标都已达到,那么说明你定的目标还不够远大。 32. 人一定要想清三个问题,第一你有什么,第二你要什么,第三你能放弃什么。 33. 你要记得:在你的人生舞台上,你是自己的主角,不需要去做谁的配角。 5、积极向上的心态,是成功者的最基本要素。 30、我们这个世界,从不会给一个伤心的落伍者颁发奖牌。 41、梯子的梯阶从来不是用来搁脚的,它只是让人们的脚放上一段时间,以便让别一只脚能够再往上登。 83、松软的沙滩上最容易留下脚印。钽也最容易被潮水抹去。 1. 不要被教条所限,不要活在别人的观念里。 16、给别人开启一扇窗,也就让自已看到了更完整的天空。 38、永不言败是追究者的最佳品格。 79、事业的大厦如缺乏毅力的支柱,只能是空中楼阁。 20. "路"必须去走方能到达."苦"必须去受才可消除 19. 亲情是一种深度,友情是一种广度,而爱情是一种纯度。亲情是没有条件、不求回报的阳光沐浴,友情是浩荡巨大、可以随时安然栖息的 堤岸;而爱情则是神秘无边、可以使歌至到忘情泪至潇洒的心灵照射。人生一世,亲情、友情、爱情;三者缺一,已为遗憾,三者缺二,实为可 怜;三者皆缺,活而如亡。 17、只有坚定的自信心,才能产生实现目标的伟大力量。 7、上帝制造人类的时候就把我们制造成不完美的人,我们一辈子努力的过程就是使自己变得更加完美的过程,我们的一切美德都来自于克服 自身缺点的奋斗。
(5) 1molNa+质量是 23 克
(6) 1molNaCl质量 58.5 克
粒子数目固定 定值
二、摩尔质量
化学上,我们把 1 mol 物质所 具有的质量叫做 摩尔质量。
★ 符号: M
单位:g·mol-1 或 g/mol 数值:等于物质或粒子的相对原子或 相对分子质量
化学:专题 第一单元 丰富多彩的化学物质 教案多课时苏教版必修

专题1第一单元丰富多彩的化学物质第1课时物质的分类与转化一、物质的分类1.物质的分类依据为了更好地认识和研究物质,人们常根据物质的________、________、________等对物质进行分类。
根据物质的存在状态,将物质分为__________、__________和__________;根据物质的导电性,将物质分为________、__________和__________;根据物质在水中的溶解性,将物质分为____________、________________和______________。
2.物质分类方法(1)按组成结构分类(2)根据物质的性质分类如氧化物的分类1酸性氧化物A.概念:能够与碱反应生成________的氧化物。
B.举例:写出CO2和NaOH溶液反应的化学方程式:___________。
2碱性氧化物A.概念:能够与酸反应生成________的氧化物。
B.举例:写出CaO和盐酸反应的化学方程式:____________________________。
二、物质的转化1.常见物质之间的转化类型物质的转化化学方程式举例单质―→化合物化合物―→单质碱性氧化物―→碱酸性氧化物―→酸酸―→盐碱―→盐盐+盐―→两种新盐单质+化合物―→单质+化合物2.钙及其化合物之间的转化写出上述反应的化学方程式:1________________________________________________________________________2________________________________________________________________________3________________________________________________________________________4________________________________________________________________________5________________________________________________________________________三、化学反应的几种类型1.以反应物和生成物的类别、反应前后物质的种类为分类依据,化学反应可分为:____________、____________、__________和____________。
苏教版高中化学必修一专题1第一单元丰富多彩的物质世界(期末复习一).docx

高中化学学习材料唐玲出品第一单元 丰富多彩的物质世界 班级 姓名考点一:能根据物质的组成和性质对物质进行分类(C )物质⎩⎪⎪⎨⎪⎪⎧混合物⎩⎪⎨⎪⎧溶液胶体浊液纯净物⎩⎪⎨⎪⎧化合物⎩⎪⎨⎪⎧有机化合物⎩⎪⎨⎪⎧烃烃的衍生物无机化合物:酸、碱、盐、氧化物单质⎩⎪⎨⎪⎧非金属金属氧化物分为酸性氧化物、碱性氧化物和两性氧化物。
与碱反应生成盐和水的氧化物叫酸性氧化物,如CO 2、SO 2;与酸反应生成盐和水的氧化物叫碱性氧化物,如CaO 、Na 2O 。
酸可以从两个不同的角度进行分类:一是依据酸分子电离生成的H +个数分为一元酸、二元酸、 多元酸等;二是依据酸的组成元素中是否含氧元素分为含氧酸和无氧酸。
碱一般根据溶解性可分为可溶性碱和难溶性碱;盐可分为正盐、酸式盐、碱式盐。
考点二:了解物质常见变化的分类方法(B )1. 四种基本反应类型:化合反应、分解反应、置换反应、复分解反应。
2. 根据反应中是否有电子转移可将反应分为氧化还原反应和非氧化还原反应。
3. 根据反应中是否有离子参加可将反应分为离子反应和非离子反应。
4. 根据反应程度大小分为可逆反应和不可逆反应。
5. 四种基本反应类型与氧化还原反应的关系:置换反应一定是氧化还原反应,复分解反应一定不是氧化还原反应,化合反应、分解反应可能是氧化还原反应。
考点三:认识物质的量是描述微观粒子集体的一个物理量,摩尔是物质的量的基本单位;了解阿伏加德罗常数的涵义(B)1. 物质的量(n):表示物质含指定微观粒子多少的物理量。
微观粒子—分子、原子、离子、质子、中子、电子及其组合。
单位:摩尔(mol),简称为摩。
规定0.012_kg12C中所含碳原子数为1_mol。
2. 阿伏加德罗常数:N A≈6.02×1023_mol-1。
计算公式:n=N/N A。
考点四:了解摩尔质量的涵义(B)摩尔质量(M):单位物质的量的物质所具有的质量。
单位:g·mol-1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一单元丰富多彩的化学物质(一)
知识回顾一
1.同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
(1)生石灰属于哪种类别的物质?
(2)生石灰可做干燥剂的理由是什么?(用化学方程式表示)
(3)生石灰还可以跟哪些类别的物质发生化学反应?列举两例,并写出化学方程式
(4)小纸袋中的物质能否长期持续地做干燥剂?为什么?
(5)在你所认识的化学物质中,还有哪些可以用作干燥剂?列举一例。
2.经测定,一瓶气体中只含有C、H两种元素,通常情况下这瓶气体不可能是()A.一种化合物B.一种单质和一种化合物的混合物
C.两种化合物D.两种单质
3.据报道,2003年12月26日,重庆开县发生了天然气矿井“井喷”事件,喷出的气体主要成分是甲烷,还含有硫化氢(H2S),氰化氢(HCN)等多种有毒气体,造成290多人中毒死亡。
你认为喷出的气体是()A.一种纯净物B.全部由无机化合物组成的混合物
C.全部由有机化合物组成的混合物D.由无机化合物和有机化合物组成的混合物知识整理一
请你根据物质的组成对物质进行分类
知识回顾二
4.以石灰石、水、纯碱为原料,如何制取烧碱?写出有关反应的化学方程式,并说明基本反应类型。
(1)__________________________________________,属于_____________反应。
(2)__________________________________________,属于_____________反应。
(3)__________________________________________,属于_____________反应。
5.按下列要求各写出一个化学反应方程式:
(1)有水生成的化合反应______________________________________________________ (2)生成一种碱性氧化物和一种酸性氧化物的分解反应____________________________ (3)有硝酸银参加反应生成硝酸铜的置换反应____________________________________ (4)生成两种沉淀的复分解反应________________________________________________
知识整理二
(一)化学反应的基本类型
(二)单质、氧化物、酸、碱、盐之间的转化关系
知识回顾三
6.现在有下列物质:
①氧气②硫酸铜③氢氧化钠的水溶液④铜⑤氯化氢⑥蔗糖⑦酒精⑧三氧化硫⑨水
在以上物质中,属于电解质的是----------------------------------------------------------;
属于非电解质的是---------------------------------------------------------
知识整理三
强电解质和弱电解质
巩固练习
1. 将下列物质按酸、碱、盐分类,依次排列正确的是( ) A.硫酸、纯碱、石灰石B.氢硫酸、烧碱、胆矾
C.碳酸、生石灰、石灰石D.磷酸、乙醇钠、苛性钾
2.下列关于化学反应类型的叙述中,正确的是()
A.凡是生成盐和水的反应都是中和反应
B.复分解反应一定没有单质参加
C.生成一种单质和一种化合物的反应一定是置换反应
D.分解反应的生成物一定有单质
3.在下列溶液中分别放入铁棒,过一会儿再把铁棒取出后(1)能使铁棒质量增加的溶液是();(2)溶液质量不变的是();(3)溶液质量增加的是()A. 稀硫酸 B. 食盐水 C. 硫酸铜溶液 D. 盐酸
4.A是废铁屑表面上红色固体的主要成分,B、C、F都是单质,D、F都是无色无味的气体,它们之间的相互转化关系如下图:
试写出下列各物质的化学式:A______________ B______________________-
C________________D__________________E________________ F_________________ 5.(1)沈括《梦溪笔谈》中提到信州(今江西省)铅山县有一苦泉,将苦泉水煎熬,得到一种蓝色晶体.此晶体常用作游泳池或浴池杀菌消毒剂.试回答:
①此晶体的化学式为_________________;
②煎熬苦泉水的铁锅用久了就会在其表面析出一层红色物质,其原因为(用化学方程式表示)___________________________________________。
(2)下列物质在潮湿空气中发生的变化,主要与哪些气体有关,请将其填写在相应的空格处(写化学式):
①钢铁生锈_____________;②氢氧化钠固体潮解变质_______________;③铜器生锈_______________;④二氧化硫形成酸雨________________。
6.某同学从一种未知的无色溶液中检验出Ba2+、Ag+,同时溶液的酸性很强,他还准备继
续检验溶液中是否含有Cu2+、Cl-、CO32-、K+、Al3+、SO42-、NO3-等离子,很显然,有些
离子还必须检验,你认为必须检验的离子是
7.一学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物
填空和回答下列问题
(1)B物质是(写化学式)
(2)按此实验方案分离得到的NaCl,经分析含有杂质,是因为上述方案中某一步设计有
毛病,这一步的正确设计方案应是。
(3)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,
这种物质是。
8.若从H2SO4、Na2SO4、Na2CO3、NaCl、NaOH、Cu(NO3)2、HNO37种溶液中取出其中的2种,进行混合及有关实验,所观察到的现象已记录在下表中。
试据各步实验及其现象先进行分步推断(即实验进行到该步所能作出的某物质肯定存在、否定存在或可能存在的
①和;②和;③和;
④和;⑤和;⑥和;。
