植物25羟基维生素D325OHD3酶联免疫分析
25-羟基维生素D3测定试剂盒(酶联免疫法)产品技术要求meikang
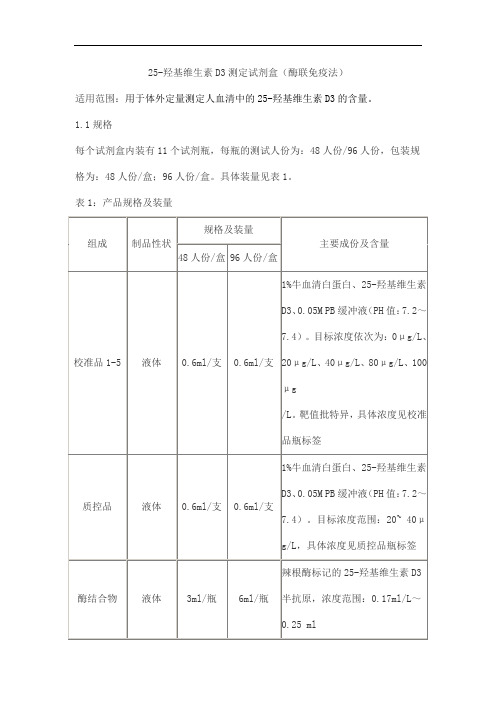
25-羟基维生素D3测定试剂盒(酶联免疫法)
适用范围:用于体外定量测定人血清中的25-羟基维生素D3的含量。
1.1规格
每个试剂盒内装有11个试剂瓶,每瓶的测试人份为:48人份/96人份,包装规格为:48人份/盒;96人份/盒。
具体装量见表1。
表1:产品规格及装量
2.1 外观
试剂盒各组份应齐全、完整、液体无渗漏;包装完好,标签清晰,准确,牢固。
2.2 净含量:液体试剂的净含量应不少于标示值。
2.3 空白限:用校准品1(0μg/L)测试本产品,OD值不低于1.50。
2.4 定量限:测定5.0μg/L(定量限),变异系数CV≤20%。
2.5 线性:在[5,100.0]μg/L的线性范围内,线性相关系数r≥0.9900;
2.6 准确度:回收率介于85%~115%。
2.7 精密度
2.7.1 批内差:同一批号产品测量结果的变异系数CV≤15%。
2.7.2 批间差:3个不同批号产品测量结果的极差≤15%。
2.8 分析特异性:检测浓度为100μg/L的维生素D3,结果应≤
3.0μg/L。
2.9 稳定性:取2℃~8℃保存至效期后三个月内的产品,分别检测2.3~2.6、2.7.1、2.8项,其结果应符合各项要求。
25羟基维生素d(25-oh-vd)的原理

25羟基维生素d(25-oh-vd)的原理是固相夹心法酶联免疫吸附实验(ELISA)。
已知待测物质浓度的标准品、未知浓度的样品加入微孔酶标板内进行检测。
先将待测物质和生物素标记的抗体同时温育。
洗涤后,加入与标记抗体特异结合的酶,再与底物一起温育。
底物经酶的催化变为有色产物,通过颜色变化对待测物质进行定量测定。
25羟维生素D是维生素D在体内的主要存在形式。
维生素D为类固醇衍生物,属脂溶性维生素,为环戊烷多氢菲类化合物。
维生素D主要由人体皮肤经紫外线照射后合成,少部分从食物或补充品中摄入。
维生素D不仅仅影响钙磷代谢,而且具有广泛的生理作用,是维持人体健康、细胞生长和发育的必不可少的物质,与多种疾病密切相关。
25羟基维生素D检测方法及参考值说明(2)

25羟基维生素D (25OHD)检测方法及参考值说明一、液相串联质谱法的特点1、特异性强,可同时检测25OHD2和25OHD3含量,方法准确度高。
首先前处理过程中,通过蛋白沉淀、液液萃取、色谱柱分离将目标类固醇化合物从数百种化合物中有效分离出来,再通过质谱特异性的检测目标化合物分子,并进行定量,通过同系物内标进行结果的矫正;通过美国NIST校准品检测和BIO-RAD质控品检测,确保结果的准确性。
2、有效祛除杂质干扰,使结果更精准。
血清内存在大量的高亲和蛋白,严重影响维生素D 的准确检测。
此方法通过蛋白沉淀、液液萃取、液相色谱分离等步骤将目标类固醇有效的与数百种干扰物分离,并通过质谱法特异性的检测目标化合物分子,从而使方法对25羟基维生素D检测有着高度的特异性和专一性。
因此溶血、黄疸血样对检测结果的影响不大。
3、液相色谱串联质谱法得到标准化。
目前25OHD检测的唯一标准物质是美国国家技术和标准委员会给出的SRM972校准品,该校准品的检测值是由液相色谱串联质谱法检出的,所以液相色谱串联质谱法使得维生素D检测标准化成为可能,并且是未来维生素D检测的“金标准”。
因此,液相色谱串联质谱法检测维生素D是高端科研的首选方法。
4、液相色谱串联质谱法可为检测提供更高的灵敏度和稳定性。
检测系统可实现半自动化,在一些重要研究中也使用该方法,再现性更好。
二、25OHD参考值情况目前就25OHD的最佳参考范围仍未达成广泛共识,25OHD水平受到许多因素影响:例饮食、日晒、季节、地域、年龄、肤色等影响,所以对健康人群取样检测并不是建立参考范围的理想途径。
我中心参考值参考:中华医学会儿科学分会儿童保健组、《中华儿科杂志》编辑委员会:儿童微量营养素缺乏防治建议. 中华儿科杂志 2010年7月,第48卷,第7期.儿童参考值范围:< 5ng/mL 维生素D严重缺乏5-15ng/mL 维生素D缺乏16-20ng/mL 维生素D不足20-100ng/mL 维生素D正常> 100ng/mL 维生素D过量三、25OHD检测项目基本信息标本类型:血清,需尽快分离标本量:1ml,最少0.5ml报告时间:每周一、三、五检测注:由于25OHD的C-3同分异构体的干扰,该方法对于一岁以下儿童结果有影响。
维生素d2论文维生素d3论文25-羟基维生素d2论文25-羟基维生素d3论文

维生素d2论文维生素d3论文25-羟基维生素d2论文 25-羟基维生素d3论文维生素D补充与药物选择摘要近10多年来,液相色谱-质谱法(lc-ms)已能精确区分且定量测定血清25-羟基维生素d2(25(oh)d2)和25-羟基维生素d3(25(oh)d3)水平,由此发现维生素d3的营养能力优于维生素d2。
本文介绍用25-羟基维生素d水平评估维生素d营养状况的理由及定量测定25(oh)d2和25(oh)d3方法的演变过程,综述比较维生素d2和维生素d3提高血清25(oh)d2和25(oh)d3水平能力的临床数据,并得到如下结论:为了预防和治疗维生素d不足或缺乏,临床医师应该首选维生素d3补充剂。
关键词:维生素d2 维生素d3 25-羟基维生素d2 25-羟基维生素d3vitamin d supplementation and its supplements selection zhou jian-lie1*,christopher yang2(1. “vitamin d today” website,shanghai,200234;2. department of chemistry,university of southern california,los angeles,ca90007)abstractlc-ms has been able to accurately distinguish and quantify serum levels of 25(oh)d2 and 25(oh)d3 over the last decade. it is found that the nutritional effects of vitamin d3 are better than those of vitamin d2. this article describes the reasons for using 25(oh)d as assessment for nutritionalstatus of vitamin d and an evolution of quantitative determination of 25(oh)d2 and 25(oh)d3 levels,and reviews clinical research data on improvement of 25(oh)d2 and25(oh)d3 levels in serum by supplementation of vitamin d2 and vitamin d3. therefore,clinicians should prefer vitamin d3 supplements in order to prevent and treat vitamin d insufficiency and deficiency.key wordsvitamin d2;vitamin d3;25(oh)d2;25(oh)d3世界各地有近10亿人维生素d不足,需要补充维生素d[1]。
25-羟基维生素D3(25(OH)D3)定量测定试剂盒(酶联免疫吸附法)产品技术要求zd

25-羟基维生素D3(25(OH)D3)定量测定试剂盒(酶联免疫吸附法)
适用范围:产品供临床机构测量成人心率、脉搏体积记录、肢体无创血压指标,并根据以上指标计算出脉搏波传导速度(PWV)、踝臂指数(ABI)、臂踝指数(BAI)、趾臂指数(TBI)。
用于体外定量测定人体血清样本中25-羟基维生素D3的含量。
1. 产品型号/规
格
本产品包装规格为48人份/盒和96人份/盒。
表1 25-羟基维生素D3试剂盒组成
2. 性能指标
2.1 外观
2.1.1标识应清晰,易识别;
2.1.2试剂盒各组分应齐全、完整,液体无渗漏;
2.1.3铝箔袋应无破损漏气现象。
2.2 装量
试剂盒组成内,液体试剂成分的装量应不少于标示值。
2.3准确度
其回收率应在90%~110%范围内。
2.4空白限
试剂盒空白限应不大于2ng/ml 。
2.5 线性
在[4ng/ml,160ng/ml]范围内,相关系数(r)应不低于0.9900。
2.6 重复性
重复测定2个不同浓度的样本,变异系数(CV)应不高于12.0%。
2.7批间差
用三个批号试剂盒检测同一份样本,三个批号试剂盒之间的批间变异系数(CV)应不高于15.0%。
2.8溯源性
根据GB/T21415及有关规定提供校准品的来源、赋值过程以及不确定度等内容,校准品溯源至企业校准品,与已上市产品比对赋值,详见附录A。
2.9稳定性
试剂盒在2~8℃放置有效期(有效期为12个月)后两个月内进行检测,测定结果应符合2.1~2.6各项要求。
人1,25二羟基维生素D3(1,25-(OH)2D3)酶联免疫分析
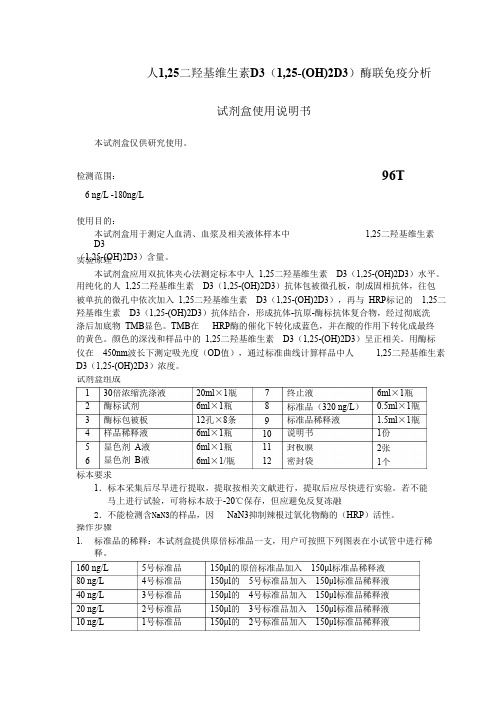
人1,25二羟基维生素D3(1,25-(OH)2D3)酶联免疫分析试剂盒使用说明书本试剂盒仅供研究使用。
检测范围:96T6 ng/L -180ng/L使用目的:本试剂盒用于测定人血清、血浆及相关液体样本中1,25二羟基维生素D3 (1,25-(OH)2D3)含量。
实验原理本试剂盒应用双抗体夹心法测定标本中人1,25二羟基维生素D3(1,25-(OH)2D3)水平。
用纯化的人1,25二羟基维生素D3(1,25-(OH)2D3)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入1,25二羟基维生素D3(1,25-(OH)2D3),再与HRP标记的1,25二羟基维生素D3(1,25-(OH)2D3)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的1,25二羟基维生素D3(1,25-(OH)2D3)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中人1,25二羟基维生素D3(1,25-(OH)2D3)浓度。
试剂盒组成1 2 3 4 5 6 30倍浓缩洗涤液酶标试剂20ml×1瓶6ml×1瓶12孔×8条6ml×1瓶6ml×1瓶6ml×1/瓶78终止液6ml×1瓶0.5ml×1瓶1.5ml×1瓶1份标准品(320 ng/L)标准品稀释液说明书酶标包被板样品稀释液显色剂A液显色剂B液9101112封板膜2张密封袋1个标本要求1.标本采集后尽早进行提取,提取按相关文献进行,提取后应尽快进行实验。
若不能马上进行试验,可将标本放于-20℃保存,但应避免反复冻融2.不能检测含NaN3的样品,因NaN3抑制辣根过氧化物酶的(HRP)活性。
操作步骤1. 标准品的稀释:本试剂盒提供原倍标准品一支,用户可按照下列图表在小试管中进行稀释。
25-羟基维生素D3测定试剂盒(酶联免疫吸附法)产品技术要求meikang
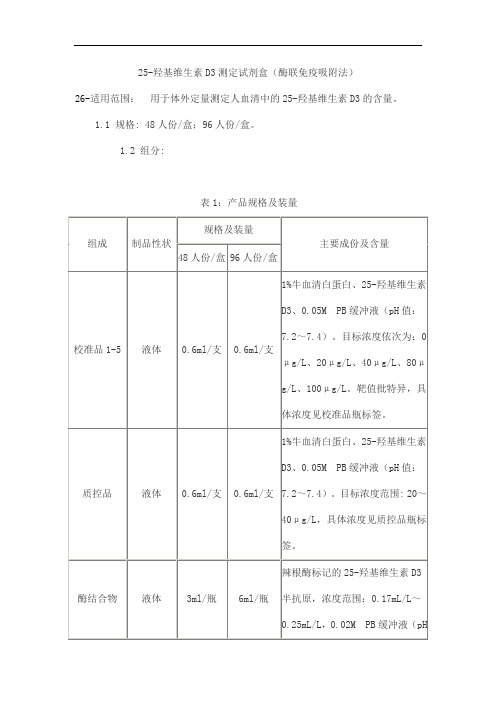
25-羟基维生素D3测定试剂盒(酶联免疫吸附法)
26-适用范围:用于体外定量测定人血清中的25-羟基维生素D3的含量。
1.1 规格: 48人份/盒;96人份/盒。
1.2 组分:
表1:产品规格及装量
2.1 外观
试剂盒各组份应齐全、完整、液体无渗漏;包装完好,标签清晰,准确,牢固。
2.2 净含量:液体试剂的净含量应不少于标示值。
2.3 空白限:浓度不高于1.50μg/L。
2.4 定量限:测定5.0μg/L(定量限),变异系数CV≤20%。
2.5 线性:在[5,100.0]μg/L的线性范围内,线性相关系数r≥0.9900;
2.6 准确度:回收率介于85%~115%。
2.7 精密度
2.7.1 批内差:同一批号产品测量结果的变异系数CV≤15%。
2.7.2 批间差:3个不同批号产品测量结果的极差≤15%。
2.8 分析特异性:检测浓度为100μg/L的维生素D3,结果应≤
3.0μg/L。
2.9 量值溯源:
试剂盒校准曲线按照GB/T 21415-2008 《体外诊断医疗器械生物样品中量的
测量校准品和控制物质赋值的计量学溯源性》的要求,溯源至公司内部工作校准品,并与已上市产品比对赋值。
2.10 稳定性:
取2℃~8℃保存至效期后三个月内的产品,分别检测2.3~2.6、2.7.1、2.8
项,其结果应符合各项要求。
人125二羟基维生素D3125OH2D3酶联免疫分析
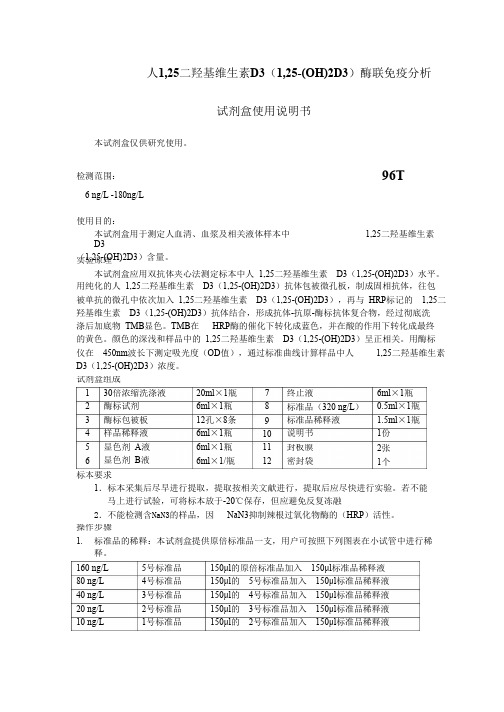
人1,25二羟基维生素D3(1,25-(OH)2D3)酶联免疫分析试剂盒使用说明书本试剂盒仅供研究使用。
检测范围:96T6 ng/L -180ng/L使用目的:本试剂盒用于测定人血清、血浆及相关液体样本中1,25二羟基维生素D3 (1,25-(OH)2D3)含量。
实验原理本试剂盒应用双抗体夹心法测定标本中人1,25二羟基维生素D3(1,25-(OH)2D3)水平。
用纯化的人1,25二羟基维生素D3(1,25-(OH)2D3)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入1,25二羟基维生素D3(1,25-(OH)2D3),再与HRP标记的1,25二羟基维生素D3(1,25-(OH)2D3)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的1,25二羟基维生素D3(1,25-(OH)2D3)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中人1,25二羟基维生素D3(1,25-(OH)2D3)浓度。
试剂盒组成1 2 3 4 5 6 30倍浓缩洗涤液酶标试剂20ml×1瓶6ml×1瓶12孔×8条6ml×1瓶6ml×1瓶6ml×1/瓶78终止液6ml×1瓶0.5ml×1瓶1.5ml×1瓶1份标准品(320 ng/L)标准品稀释液说明书酶标包被板样品稀释液显色剂A液显色剂B液9101112封板膜2张密封袋1个标本要求1.标本采集后尽早进行提取,提取按相关文献进行,提取后应尽快进行实验。
若不能马上进行试验,可将标本放于-20℃保存,但应避免反复冻融2.不能检测含NaN3的样品,因NaN3抑制辣根过氧化物酶的(HRP)活性。
操作步骤1. 标准品的稀释:本试剂盒提供原倍标准品一支,用户可按照下列图表在小试管中进行稀释。
秦皇岛地区儿童25-羟基维生素D3检测结果分析

秦皇岛地区儿童25-羟基维生素D3检测结果分析刘冬妹;吴红丽;李兰;刘雅琪【期刊名称】《国际检验医学杂志》【年(卷),期】2017(038)024【摘要】目的检测并分析秦皇岛地区儿童血清25-羟基维生素D3[25-(OH)D3]的水平,指导秦皇岛地区儿童合理进行维生素D补充.方法选取2016年1月至2016年12月于该院保健部进行健康体检的1246例0~6岁儿童作为调查对象,采用酶联免疫吸附法(ELISA)检测血清25-(OH)D3水平,并对检测结果进行分析.结果对秦皇岛地区0~6岁儿童的血清25-(OH)D3检测结果进行分析发现,该地区儿童血清25-(OH)D3平均水平为(25.398 ± 7.765)μg/L,维生素D缺乏率为25.12%.不同性别儿童之间血清25-(OH)D3水平对比差异无统计学意义(P>0.05);不同年龄段儿童的血清25-(OH)D3水平对比差异有统计学意义(P<0.05),新生儿、婴儿以及3~6岁学龄前儿童维生素D缺乏率较高.结论秦皇岛地区0~6岁儿童的血清25-(OH)D3缺乏率较高,应针对不同年龄段儿童的个体差异和发育特点,有针对性地进行维生素D3的监测和补充.【总页数】2页(P3480-3481)【作者】刘冬妹;吴红丽;李兰;刘雅琪【作者单位】河北省秦皇岛市妇幼保健院检验科,河北秦皇岛 066000;河北省秦皇岛市妇幼保健院检验科,河北秦皇岛 066000;河北省秦皇岛市妇幼保健院检验科,河北秦皇岛 066000;河北省秦皇岛市妇幼保健院检验科,河北秦皇岛 066000【正文语种】中文【相关文献】1.广州番禺地区儿童总钙和25-羟基维生素 D检测结果分析 [J], 肖钘;何金花;黎毓光;韩泽平;胡淑芬;黄惠2.我院6275例0~6岁儿童血清25-羟基维生素D检测结果分析 [J], 邝炎波;曾丽;周永贤;麦荣嘉;姚叶珊3.绍兴地区14岁以下儿童25-羟基维生素D检测结果分析 [J], 陈晓霞;吴长划;余红4.身材矮小儿童25-羟基维生素D、25-羟基维生素D3与骨密度的关系 [J], 徐其忠;黄响高;朱行美5.6958例儿童血清25-羟基维生素D检测结果分析 [J], 田仁义因版权原因,仅展示原文概要,查看原文内容请购买。
25-羟基维生素D测定试剂盒(酶联免疫吸附法)产品技术要求bohui

25-羟基维生素D测定试剂盒(酶联免疫吸附法)适用范围:该产品与中性电极共同作用为高频电刀的附件,在外科手术中进行切割和凝血。
用于体外定量测定人血清、血浆或耳指末梢全血中25-羟基维生素D的含量。
1.1产品规格96人份/盒、48人份×2/盒、48人份/盒。
1.2主要组成成分2.1 外观试剂盒外观应整洁,文字符号标识清晰;液体组分应澄清透明,无沉淀、无渗漏;包被的检测板密封完好,不得有破损。
2.2 装量实际装量不得低于标称量,且偏差不大于标称量的3%。
2.3 检测限不高于5μg/L。
2.4 线性在[5,120]μg/L内,线性相关系数(r)应≥0.990。
2.5 准确度与高效液相色谱法做对比试验,用线性回归方法计算两组结果的相关系数(r)及每个浓度点的相对偏差,其线性相关系数(r)≥0.975,且相对偏差≤15%。
2.6 重复性用质控品1、质控品2两个浓度水平的质控品各重复检测10次,变异系数(CV)应≤10%。
2.7 特异性测定浓度为100μg/L的维生素D,交叉反应率应≤10%。
32.8 微量全血处理液的pH值pH:7.4±0.03。
2.9 溯源性根据GB/T 21415-2008及有关规定提供所用校准品的来源赋值过程等内容,溯源至25-羟基维生素D标准品(美国NIST,SRM2972)。
2.10 质控品赋值有效性质控品测值,应在质控范围内。
2.11 批间差用三个批次的试剂盒检测同一份样品,三个批次之间的变异系数(CV)应≤15%。
2.12 效期稳定性2℃~8℃保存,有效期为12个月。
到期后三个月内应符合2.3、2.4、2.5、2.6的要求。
植物25羟基维生素D325OHD3酶联免疫分析
植物25羟基维生素D3(25(OH)D3)酶联免疫分析试剂盒使用说明书本试剂盒仅供研究使用。
检测范围:96T60ng/L -2500 ng/L使用目的:本试剂盒用于测定植物组织,细胞及其它相关样本中25羟基维生素D3(25(OH)D3)含量。
实验原理本试剂盒应用双抗体夹心法测定标本中植物25羟基维生素D3(25(OH)D3)水平。
用纯化的植物25羟基维生素D3(25(OH)D3)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入植物25羟基维生素D3(25(OH)D3),再与HRP标记的25羟基维生素D3(25(OH)D3)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB 显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的植物25羟基维生素D3(25(OH)D3)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中植物25羟基维生素D3(25(OH)D3)浓度。
试剂盒组成标本要求1.标本采集后尽早进行提取,提取按相关文献进行,提取后应尽快进行实验。
若不能马上进行试验,可将标本放于-20℃保存,但应避免反复冻融2.不能检测含NaN3的样品,因NaN3抑制辣根过氧化物酶的(HRP)活性。
操作步骤1.标准品的稀释:本试剂盒提供原倍标准品一支,用户可按照下列图表在小试管中进行稀待测样品孔。
在酶标包被板上标准品准确加样50μl,待测样品孔中先加样品稀释液40μl,然后再加待测样品10μl(样品最终稀释度为5倍)。
加样将样品加于酶标板孔底部,尽量不触及孔壁,轻轻晃动混匀。
3.温育:用封板膜封板后置37℃温育30分钟。
4.配液:将30倍浓缩洗涤液用蒸馏水30倍稀释后备用5.洗涤:小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置30秒后弃去,如此重复5次,拍干。
6.加酶:每孔加入酶标试剂50μl,空白孔除外。
7.温育:操作同3。
25二羟基维生素D3(1

人1,25二羟基维生素D3(1,25-(OH)2D3/DVD/DHVD 3)酶联免疫分析试剂盒使用说明书本试剂盒仅供研究使用产品编号:CSB-E05120h检测范围:1.56 pg/ml - 100 pg/ml最低检测限:0.39 pg/ml特异性:本试剂盒可同时检测天然或重组的人1,25-(OH)2D3,且与其他相关蛋白无交叉反应。
有效期:6个月预期应用:ELISA法定量测定人血清、血浆、细胞培养上清或其它相关生物液体中1,25-(OH)2D3含量。
说明1.试剂盒保存:-20℃(较长时间不用时);2-8℃(频繁使用时)。
2.浓洗涤液低温保存会有盐析出,稀释时可在水浴中加温助溶。
3.中、英文说明书可能会有不一致之处,请以英文说明书为准。
4.刚开启的酶联板孔中可能会含有少许水样物质,此为正常现象,不会对实验结果造成任何影响。
概述1966年狄路卡等证明维生素D是一个前体激素,其活性型为1,25-二羟基维生素D3(1,25-(OH)2D3)。
1,25-(OH)2D3的作用原理与经典类固醇激素一样,涉及遗传信息的表达。
关于存在1,25-(OH)2D3受体/结合蛋白的靶组织除传统的小肠、骨和肾脏外,还有胰、脑垂体、甲状旁腺、乳腺、胎盘,甚至还可存在于性腺、子宫、结肠、皮肤成纤维细胞、胸腺和腮腺等多种组织。
近来,发现1,25-(OH)2D3可抑制增生并降低白血病细胞分化,它可将白血病细胞分化为单核细胞/巨嗜细胞。
另外,它还可抑制一系列其它恶性细胞增生,包括胸腺、前列腺和结肠癌细胞。
1,25-(OH)2D3还影响激素分泌。
除了影响甲状旁腺和垂体腺激素分泌,还报道有增加胰岛素分泌。
此外,它还影响免疫系统,抑制T-细胞增生和细胞分裂表达。
实验原理用纯化的抗体包被微孔板,制成固相载体,往包被抗1,25-(OH)2D3抗体的微孔中依次加入标本或标准品、生物素化的抗1,25-(OH)2D3抗体、HRP标记的亲和素,经过彻底洗涤后用底物TMB显色。
人25羟基维生素D3(25-OH-D3)说明书-1
人25羟基维生素D3(25-OH-D3)酶联免疫分析(ELISA)试剂盒使用说明书本试剂仅供研究使用目的:本试剂盒用于测定人血清,血浆及相关液体样本中25羟基维生素D3(25-OH-D3)的含量。
实验原理:本试剂盒应用双抗体夹心法测定标本中人25羟基维生素D3(25-OH-D3)水平。
用纯化的抗D3(25-OH-D3)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入人25羟基维生素D3(25-OH-D3),再与HRP标记的D3(25-OH-D3)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的25羟基维生素D3(25-OH-D3)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中人25羟基维生素D3(25-OH-D3)浓度。
样本处理及要求:1. 血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如出现沉淀,应再次离心。
2. 血浆:应根据标本的要求选择EDTA或柠檬酸钠作为抗凝剂,混合10-20分钟后,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如有沉淀形成,应该再次离心。
3. 尿液:用无菌管收集,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如有沉淀形成,应再次离心。
胸腹水、脑脊液参照实行。
4. 细胞培养上清:检测分泌性的成份时,用无菌管收集。
离心20分钟左右(2000-3000转/分)。
仔细收集上清。
检测细胞内的成份时,用PBS(PH7.2-7.4)稀释细胞悬液,细胞浓度达到100万/ml左右。
通过反复冻融,以使细胞破坏并放出细胞内成份。
离心20分钟左右(2000-3000转/分)。
仔细收集上清。
保存过程中如有沉淀形成,应再次离心。
5. 组织标本:切割标本后,称取重量。
25-羟基维生素d荧光免疫层析法

25-羟基维生素d荧光免疫层析法
25-羟基维生素D检测是用来评估体内维生素D水平的方法之一。
荧光免疫层析法(Fluorescence Immunoassay)是一种常
用的检测方法。
该方法基于维生素D与特定的抗体结合形成复合物的原理。
首先,样本中的25-羟基维生素D被提取出来,并与特异性的
抗体结合。
然后,添加荧光标记的二抗来与这个复合物结合。
在加入荧光素测定试剂后,荧光素会与荧光标记的复合物结合,并且发出荧光信号。
最后,通过荧光测量仪器来检测荧光信号的强度,从而确定样品中25-羟基维生素D的浓度。
荧光免疫层析法具有灵敏度高、检测速度快、操作简单等优点。
它被广泛应用于临床医学中,用于评估维生素D缺乏症和骨
骼相关疾病的风险,以及监测维生素D补充治疗的效果。
慢性肾脏病患者25-羟基维生素D3检测结果分析

慢性肾脏病患者25-羟基维生素D3检测结果分析发表时间:2014-08-01T16:23:38.500Z 来源:《医药前沿》2014年第7期供稿作者:汪明星文锋彭卫平杨益枫付小国[导读] 慢性肾脏病患者多伴有矿物质和骨代谢紊乱,且为慢性肾脏病患者高病死率的危险因素。
汪明星文锋彭卫平杨益枫付小国(广东省连州市人民医院 513404)【摘要】目的分析研究慢性肾脏病患者的25-羟基维生素D3患者的水平,研究慢性肾脏病患者25-羟基维生素D3(25(OH)D3)水平与矿物质和骨代谢紊乱的关系。
方法以2011年7月~2013年9月我院收治的糖尿病肾病作为慢性肾脏病代表,其中包括糖尿病组、早期糖尿病肾病组、临床糖尿病肾病、终末期肾病组、健康组各25例作为临床研究对象,对所有患者均测定25(OH)D3。
结果各组患者中以终末期肾病组的25(OH)D3浓度最低,健康组最高,终末期肾病组与其它组对比差异有统计学意义(P<0.05);各组患者中,GFR以健康组最高,终末期肾病组最低,终末期肾病组与其它组对比有显著性差异(P<0.05);各组患者中,终末期肾病组血钙最低、血磷最高,终末期肾病组与其它组对比差异有统计学意义(P<0.05)。
结论终末期慢性肾脏病患者的25(OH)D3有明显的降低,可以反映患者的矿物质和骨代谢紊乱。
【关键词】慢性肾脏病糖尿病肾病 25-羟基维生素D3(25(OH)D3) 矿物质和骨代谢紊乱【中图分类号】R446 【文献标识码】A 【文章编号】2095-1752(2014)07-0205-02慢性肾脏病患者多伴有矿物质和骨代谢紊乱,且为慢性肾脏病患者高病死率的危险因素。
在慢性肾脏病患者的终末期,患者会有心血管疾病的危险,其中氧化应激、CKD-MBD及炎症等均会加重患者发生心血管疾病。
且临床研究还发现,维生素D缺乏与慢性肾病患者心血管疾病升高、矿物质和骨代谢紊乱密切相关。
本文研究分析了慢性肾脏病患者的25-羟基维生素D3患者的水平,报告如下:1.资料与方法1.1一般资料以2011年7月~2013年9月我院收治的2型糖尿病肾病作为慢性肾脏病代表,其中包括健康组(1组)、糖尿病组(2组)、早期糖尿病肾病组(3组)、临床糖尿病肾病(4组)、终末期肾病组(5组)各25例作为临床研究对象。
25-羟基维生素D3测定试剂盒(酶联免疫法)产品技术要求bohui

25-羟基维生素D3测定试剂盒(酶联免疫法)
适用范围:用于体外定量测定人血清、血浆或耳指末梢全血中25-羟基维生素D3的含量。
1.1产品规格
96人份/盒(A型)、96人份/盒(B型)、48人份/盒
1.2产品组成:
见表1。
表1:产品组成
2.1溯源性
根据GB/T 21415-2008及有关规定提供所用25-羟基维生素D
定标品的来源、赋
3
标准品(美国NIST,SRM2972)。
值过程等内容,溯源至25-羟基维生素D
3
2.2外观
试剂盒外观应整洁,文字符号标识清晰;液体组分应澄清透明,无沉淀、无渗漏;包被的检测板密封完好,不得有破损。
2.3装量
实际装量不得低于标称量。
2.4空白限
不高于5μg/L。
2.5线性
在[5,100]μg/L内,线性相关系数(r)应≥0.990。
2.6准确度
与高效液相色谱法做对比试验,用线性回归方法计算两组结果的相关系数(r)及每个浓度点的相对偏差,其相关系数(r)≥0.975,且相对偏差≤15%。
2.7重复性
CV值应≤10%。
2.8批间差
CV值应≤15%。
2.9特异性
测定浓度为100μg/L的维生素D3,交叉反应率应≤10%。
2.10微量全血处理液的pH值
pH:7.4±0.03。
2.11效期稳定性
25-羟基维生素D3测定试剂盒在2℃~8℃贮存条件下,有效期为12个月。
到期后三个月内应符合2.4、2.5、2.6、2.7的要求。
反复呼吸道感染患儿血清25羟基维生素D3、免疫球蛋白的变化

反复呼吸道感染患儿血清25羟基维生素D3、免疫球蛋白的变化目的:探讨反复呼吸道感染患儿血清25羟基维生素D3[25-hydroxyvitaminD3,25-(OH)D3]、免疫球蛋白的变化。
方法:选择200例诊断为反复肺部感染的患儿作为病例组,采用随机数字表法均分为常规组与观察组,常规组给予常规抗炎治疗,观察组在常规治疗基础上补充维生素D,于治疗前、治疗后3个月检测25-(OH)D3、免疫球蛋白水平;选择100例健康儿童作为健康组,检测25-(OH)D3、免疫球蛋白水平作为参照值,分析其与肺部感染的相关性。
结果:病例组治疗前25-(OH)D3、IgG、IgA均明显低于健康组,差异均有统计学意义(P<0.05);治疗后25-(OH)D3、IgG、IgA均较治疗前明显升高,差异均有统计学意义(P<0.05);但25-(OH)D3、IgA均低于健康组,差异均有统计学意义(P <0.05)。
治疗后常规组与观察组患儿25-(OH)D3、IgG、IgA均较治疗前升高,差异均有统计学意义(P<0.05);且治疗后观察组25-(OH)D3、IgG、IgA则较常规组升高更明显,差异均有统计学意义(P<0.05)。
随访1年观察组复发例数、需住院治疗人次及症状持续平均天数均明显低于常规组,差异均有统计学意义(P<0.05)。
结论:反复呼吸道感染患儿多存在血清25-(OH)D3、IgG、IgA 水平低下,在积极抗感染治疗基础上,给予患儿补充维生素D可更好地提高机体免疫功能。
临床上由于小儿机体发育不成熟、免疫功能低下、喂养不当等因素影响,小儿容易发生呼吸道感染,其中20.0%患儿出现反复呼吸道感染,甚至哮喘、心肌炎等,严重影响小儿的正常生长发育[1]。
血清25羟基维生素D3[25-(OH)D3]是维生素D代谢产物,其参与了细胞的增殖、分化、调节过程,对生长发育期小儿机体免疫系统有积极作用[2]。
免疫球蛋白可以反映机体的免疫功能情况。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
植物25羟基维生素D3(25(OH)D3)酶联免疫分析
试剂盒使用说明书
本试剂盒仅供研究使用。
检测范围:96T
60ng/L -2500 ng/L
使用目的:
本试剂盒用于测定植物组织,细胞及其它相关样本中25羟基维生素D3(25(OH)D3)含量。
实验原理
本试剂盒应用双抗体夹心法测定标本中植物25羟基维生素D3(25(OH)D3)水平。
用纯化的植物25羟基维生素D3(25(OH)D3)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入植物25羟基维生素D3(25(OH)D3),再与HRP标记的25羟基维生素D3(25(OH)D3)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB 显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的植物25羟基维生素D3(25(OH)D3)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中植物25羟基维生素D3(25(OH)D3)浓度。
试剂盒组成
1.标本采集后尽早进行提取,提取按相关文献进行,提取后应尽快进行实验。
若不能马上进行试验,可将标本放于-20℃保存,但应避免反复冻融
2.不能检测含NaN3的样品,因NaN3抑制辣根过氧化物酶的(HRP)活性。
操作步骤
1.标准品的稀释:本试剂盒提供原倍标准品一支,用户可按照下列图表在小试管中进行稀
2.加样:分别设空白孔(空白对照孔不加样品及酶标试剂,其余各步操作相同)、标准孔、
待测样品孔。
在酶标包被板上标准品准确加样50μl,待测样品孔中先加样品稀释液40μl,然后再加待测样品10μl(样品最终稀释度为5倍)。
加样将样品加于酶标板孔底部,尽量不触及孔壁,轻轻晃动混匀。
3.温育:用封板膜封板后置37℃温育30分钟。
4.配液:将30倍浓缩洗涤液用蒸馏水30倍稀释后备用
5.洗涤:小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置30秒后弃去,如此
重复5次,拍干。
6.加酶:每孔加入酶标试剂50μl,空白孔除外。
7.温育:操作同3。
8.洗涤:操作同5。
9.显色:每孔先加入显色剂A50μl,再加入显色剂B50μl,轻轻震荡混匀,37℃避光显色
10分钟.
10.终止:每孔加终止液50μl,终止反应(此时蓝色立转黄色)。
11.测定:以空白空调零,450nm波长依序测量各孔的吸光度(OD值)。
测定应在加终止
液后15分钟以内进行。
操作程序总结:
计算
以标准物的浓度为横坐标,OD值为纵坐标,在坐标纸上绘出标准曲线,根据样品的
OD值由标准曲线查出相应的浓度;再乘以稀释倍数;或用标准物的浓度与OD值计算出标准曲线的直线回归方程式,将样品的OD值代入方程式,计算出样品浓度,再乘以稀释倍数,即为样品的实际浓度。
注意事项
1.试剂盒从冷藏环境中取出应在室温平衡15-30分钟后方可使用,酶标包被板开封后如未用完,板条应装入密封袋中保存。
2.浓洗涤液可能会有结晶析出,稀释时可在水浴中加温助溶,洗涤时不影响结果。
3.各步加样均应使用加样器,并经常校对其准确性,以避免试验误差。
一次加样时间最好控制在5分钟内,如标本数量多,推荐使用排枪加样。
4.请每次测定的同时做标准曲线,最好做复孔。
如标本中待测物质含量过高(样本OD值大于标准品孔第一孔的OD值),请先用样品稀释液稀释一定倍数(n倍)后再测定,计算时请最后乘以总稀释倍数(×n×5)。
5.封板膜只限一次性使用,以避免交叉污染。
6.底物请避光保存。
7.严格按照说明书的操作进行,试验结果判定必须以酶标仪读数为准.
8.所有样品,洗涤液和各种废弃物都应按传染物处理。
9.本试剂不同批号组分不得混用。
保存条件及有效期
1.试剂盒保存:;2-8℃。
2.有效期:6个月。
