15.烃
化学工艺学复习资料

15.烃类氧化反应采用最为普遍的氧化剂是空气、纯氧16.化学工艺即化学生产技术,指将原料物质主要经过化学反应转变为产品的方法和过程,包括实现这种转变的全部化学的和物理的总和。
解: RC 1mol乙烯
产物
11mol乙烯
反应器分离器产物
FF MF RPKmol乙烯EO,水
设反应器中初始含有5kg乙烯,由乙烯单程转化率为25%,则可知反应掉的乙烯的量为5
5-(5-1.25-x)=1.25+x,由环氧乙烷的选择性为75%,则可设每次反应生成环氧乙烷为ykg。则:
所以环循环比应该为11.
A.①>③>②>④B.③>②>①>④C.②>①>③>④D.④>②>③>①5.脱甲烷塔的关键组分是:A. 与 B. C. D.
6.管式炉裂解石脑油所得裂解气含 很少,脱硫大多采用:A.碱洗法B.乙醇胺溶液吸收法C.N-甲基吡咯烷酮吸收法D.先乙醇胺法后碱洗法
7.冷箱在脱甲烷塔之前为:A.前加氢B.前冷C.后冷D.后加氢8.裂解气深冷分离过程中造成-100 低温一般采用的冷凝剂是:A.丙烯B.氨C.乙烯D.乙烷
7.反应达到平衡转化率所需要的反应时间为无限长。()8.反应过程中,某反应的-△ 值越大,达到平衡的转化率就越高,在相同的反应条件下,所达到的转化率要高。()
9.有机反应中,加氢反应一般是吸热反应。(×)10.可逆吸热反应的温度控制,通常是在最优温度线附近。(√)11.煤的高温干馏温度一般为900 1100 。(√)
四、、判断题
烃的计算

练习
常温常压下,a毫升两种气态烃混合物与足量 氧气混合点燃爆炸后,恢复到原来的状态体 积缩小2a毫升,则两种烃可能是( ) (A) CH4 C2H4 (B) C2H6 C3H6 (C) CH4 C2H6 (D) C2H2 C3H8
做在练习本上
在标准状况下10ml某气态烃在80ml氧气中充 分燃烧后,恢复到标准状况,所得气体的体 积为60ml,该烃是 A、乙烷 B、丙烷 C、丙烯 D、丁烯
烃完全燃烧时耗氧量规律
①物质的量相同的烃,(x+y/4)越大,耗氧 量越大 ②质量相同的烃,y/x越大(相当于含氢量大), 则耗氧量越多, 此时就把CxHy改写成CHy/x,y/x越大耗氧量越 大。 ③质量相同的烃, x/y越大(相当于含碳量大), 则生成的二氧化碳越多,
④ 质量相同的烃, ____越大,则生成的水 越多。 ⑤质量相同的烃, ______相等,则生成的 水和CO2相等。
练习
在常温常压下,取下列四种气态烃各1mol, 分别在足量的氧气中燃烧,消耗氧气最多 的是( )
A、CH4 C、C3H8 B、C2H6 D、C4H10
练习
等质量的下列物质, A、CH4 B、C2H2 C、C2H4 D、C6H6 耗氧量由大到小的是______________. 生成CO2的量有小到大的是_________.
练习
若1mol某气态烃完全燃烧,需用3mol氧气, 则其分子式为_________.
烃的计算
一、烃的燃烧规律
烃的通式:CxHy, 烃燃烧的通式: CxHy + (x+y/4)O2 xCO2+y/2H2O 1、当温度大于100℃时,若物质均是气体, 则有△V=V前-V后 =1- y/4, ①当y=4时,△V=0,体积不变。 ②当y<4时,△V>0,体积减小。 ③当y>4时,△V<0,体积增大。
烃的结构与性质

第28页/共35页
2、煤的相关知识 (1)煤的组成: 煤是由许多有机物和无机物组成的复杂的混合物 煤中主要含有C、H、O、N、S等元素,以C元素为主 (2)燃烧煤的污染 形成酸雨 (3) 煤的综合利用 ①煤的干馏②煤的气化③煤的液化
第29页/共35页
考考你:下列说法正确的是( AB)
A.石油中含有C5一C11的烷烃,可以通过石油的 分馏得到汽油 B.已C18以的烷烃的重油经过催化裂化可以得到 汽油 C.煤是由有机物和无机物组成的复杂的化合物 D.煤中含有苯和甲苯,可以先用干馏后用分馏 的方法把它们分离出来
(1)、甲烷的存在 沼气、坑气(瓦斯) 、天然气(80%) (2)、甲烷的物理性质 无色、无味、极难溶于水密度为0.717g/L(标况) 甲烷是有机物中分子量最小、含氢量最高的物质
第10页/共35页
(3)、甲烷的结构
分子式 电子式
结构式 结构示意图
H
H
CH4 H ··C······H H C H H
H
H
H
CH H
第11页/共35页
练习:下列关于甲烷的叙述,正确的是( D )
A.甲烷是一种无色无味易溶于水的气体 B.甲烷能使酸性高锰酸钾溶液褪色 C.将甲烷通入氯水中能使氯水褪色 D.甲烷可用作家庭燃料
第12页/共35页
(4)甲烷的化学性质 :由于甲烷分子结构稳定,所以通 常不与强酸、强碱及强氧化剂(如酸性高锰酸钾)反应。
系物
结构特点 碳碳单键 碳碳双键 碳碳叁键 含有一
呈链状
呈链状 呈链状 个苯环
主要反应 取代反应 加成反应、加聚反 取代反应、
应、氧化反应
加成反应
通入溴水 气态烃无现象,
现象
液态烃能萃取
高考化学知识点复习《烃》十年真题汇总含答案

高考化学知识点复习《烃》十年真题汇总含答案1.【2022年辽宁卷】下列关于苯乙炔()的说法正确的是KMnO溶液褪色B.分子中最多有5个原子共直线A.不能使酸性4C.能发生加成反应和取代反应D.可溶于水【答案】C【解析】根据苯环的性质判断可以发生氧化、加成、取代反应;根据碳碳叁键的特点判断可发生加成反应,能被酸性高锰酸钾钾氧化,对于共线可根据有机碳原子的杂化及官能团KMnO溶液褪色,A 的空间结构进行判断;A.苯乙炔分子中含有碳碳三键,能使酸性4错误;B.如图所示,,苯乙炔分子中最多有6个原子共直线,B错误;C.苯乙炔分子中含有苯环和碳碳三键,能发生加成反应,苯环上的氢原子能被取代,可发生取代反应,C正确;D.苯乙炔属于烃,难溶于水,D错误;故选答案C;2.(2021.1·浙江真题)下列说法不正确...的是A.联苯()属于芳香烃,其一溴代物有2种B.甲烷与氯气在光照下发生自由基型链反应C.沥青来自于石油经减压分馏后的剩余物质D.煤的气化产物中含有CO、H2和CH4等【答案】A【解析】A.由联苯()的分子结构可知,其分子由2个苯基直接相连,故其属于芳香烃;根据对称分析法可知,其一溴代物共有3种,A说法不正确;B.甲烷与氯气在光照下发生反应,氯气分子先吸收光能转化为自由基氯原子,然后由氯原子引发自由基型链反应,B说法正确;C.石油经常压分馏后可以得到的未被蒸发的剩余物叫重油,重油经经减压分馏可以得到重柴油、石蜡、燃料油等,最后未被气化的剩余物叫沥青,C说法正确;D.煤的气化是指煤与水蒸气在高温下所发生的反应,其产物中含有CO、H2和CH4等,D说法正确。
综上所述,本题选A。
3.(2020·天津高考真题)关于的说法正确的是A.分子中有3种杂化轨道类型的碳原子B.分子中共平面的原子数目最多为14C.分子中的苯环由单双键交替组成D.与Cl2发生取代反应生成两种产物【答案】A【解析】A.—CH3的碳原子有4个σ键,无孤对电子,是sp3杂化,苯环上的碳原子有3个σ键,无孤对电子,是sp2杂化,—C≡CH的碳原子有2个σ键,无孤对电子,是sp 杂化,因此分子中有3种杂化轨道类型的碳原子,正确;B.根据苯中12个原子共平面,乙炔中四个原子共直线,甲烷中三个原子共平面,因此分子中共平面的原子数目最多为15个(甲基中碳原子和其中一个氢原子与其他原子共面),错误;C.分子中的苯环中碳碳键是介于碳碳单键和双键之间独特的键,错误;D.与Cl2发生取代反应,取代甲基上的氢有一种产物,取代苯环上的氢有四种产物,因此取代反应生成五种产物,错误。
新教材2023版高中化学课时作业15烃及有机高分子材料新人教版必修第二册

课时作业15 烃及有机高分子材料[学业达标]1.下列关于烃的说法正确的是( )A.烃是指仅含有碳和氢两种元素的有机物B.烃是指分子里含碳元素的化合物C.烃是指发生燃烧反应后生成二氧化碳和水的有机物D.烃是指含有碳和氢两种元素的化合物2.下列关于有机高分子化合物的说法不正确的是( )A.有机高分子化合物称为聚合物,是因为它们大部分是由小分子通过聚合反应制得的B.有机高分子化合物的相对分子质量很大,但其结构是若干链节的重复C.对于一种高分子材料,n是一个整数值,因而它的相对分子质量是确定的D.高分子材料可分为天然高分子材料和合成高分子材料两大类3.PVC是聚氯乙烯的英文缩写,为保证PVC塑料制品的性能,通常需要加入多种有机助剂。
下列选项中的事实均能支持“PVC保鲜膜对人体健康带来危害”的是( )①PVC塑料属于高分子材料②使用的有机助剂有毒③含氯的化合物不一定有毒④在高温下会分解出有害物质A.①② B.③④C.②④ D.①③4.(双选)科学家对探测器发回的数据进行了分析,发现土卫六的大气层中含有95%的氮气,剩余的气体为甲烷和其他碳氢化合物。
下列关于碳氢化合物的叙述正确的是( ) A.碳氢化合物的通式为C n H2n+2B.燃烧产物为二氧化碳和水的化合物可能是碳氢化合物C.有些烷烃在光照下不能与氯气发生取代反应D.碳氢化合物分子的相对分子质量一定是偶数5.烃在自然界中广泛存在。
下列对烃的分类不正确的是( )A.CH4、CH2===CH2、CH2===CHCH===CH2均属于饱和烃B.CH3CH2CH3、CH3CH===CH2、CH3CH===CHCH2CH===CH2均属于链状烃C.CH3CH3、、C18H38均属于饱和烃D.均属于芳香烃6.(双选)物质的构成有很多奥秘,人们用不同的化学用语来表示物质的构成。
下列化学用语错误的是( )A.四氯化碳的电子式:B.丙炔的分子式:C3H4C.乙烯的结构简式:CH2===CH2D.丙烷分子的充填模型:7.有关“苯宝宝”的表情包非常流行,如图:下列有关苯的说法错误的是( )A.苯分子结构中对位上的4个原子在一条直线上B.苯的结构简式可用表示,说明含有3个碳碳双键C.苯的一氯代物有1种D.苯是一种碳原子的价键远没有饱和的烃8.某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1∶2,则( ) A.分子中C、H、O原子的个数比为1∶2∶3B.分子中C、H原子的个数比为1∶2C.分子中可能含有氧原子D.此有机物的最简式为CH49.(双选)有机高分子材料在现实生活中有广泛应用。
第15章烯烃Alkene

第15章烯烃Alkene15.1烯烃(Alkene)烯烃是不饱和的碳氢化合物。
它们仅由碳和氢原子组成,并具有一个或多个碳-碳双键。
这意味着烯烃的氢原子数比最大可能数少。
碳-碳双键使烯烃的反应性比烷烃更强。
乙烯(最简单的烯烃)是合成多种聚合物产品的起始原料,例如聚乙烯、PVC、聚苯乙、涤纶纤维以及抗冻剂和油漆等。
当原油进行热裂解时,可产出大量乙烯。
■通式(The general formula)具有一个双键的烯烃通式为C n H2n。
如何命名烯烃(How to name alkene)如分子中只有一个碳原子,则不能形成碳-碳双键。
因此最简单的烯烃是乙烯CH2=CH2,接下来是丙烯CH3CH=CH2。
■结构(Structure)烯烃的形状(The shape of alkene)乙烯是一个平面(平的)分子。
这使得每个键之间的角度大约为1200。
与烷烃中的C-C键不同,双键不能旋转。
这是由于双键的构成决定的。
任何乙烯分子中的氢原子被另一个原子或基团取代,该分子将围绕碳-碳双键呈现相同的平面形状。
■应用和科学探索(Application and How Science Work)为什么双键不能旋转(Why a double bond can not rotate)与正常的C-C键一样,碳-碳双键的每个碳原子也有一个P轨道(含有一个电子)。
这两个轨道重合,形成一个单轨道,其上的电子云密度大于一个单轨道,而小于两个单轨道,见图1和图2。
这样的一个轨道称为π(发音pi)轨道,存在这样一个轨道意味着化学键不能旋转。
有时也将其称为旋转受限。
■异构体(Isomers)具有三个碳原子以上的烯烃可形成不同类型的异构体,我们将按照IUPAC系统来对其命名,见5.2节,使用一个后缀ene来显示其有一个双键。
与烷烃中发现的碳链异构体相似,烯烃可形成两种类型的异构体(包含一个双键):■位置异构体■几何异构体位置异构体(Position isomers)这些异构体的双键处于不同的位置上,即,在碳链不同位置上的一对相邻碳原子之间。
15号白油成分

15号白油成分
15号白油是一种精制矿物油,主要成分是饱和烃类化合物,具有较高的纯度和化学稳定性。
以下是15号白油的主
要成分和特点:
1.饱和烃类化合物:15号白油的主要成分是饱和烃类化合物,包括直链和支链的烷烃、环烷烃等。
这些化合物在常温下呈液态,具有较高的化学稳定性,不易氧化和变质。
2.不饱和烃类化合物:15号白油中还含有一定量的不饱和烃类化合物,如烯烃和炔烃。
这些化合物的含量较低,对白油的整体性质影响较小。
3.芳香烃类化合物:在一些15号白油中,还含有一定量的芳香烃类化合物,如甲苯、乙苯等。
这些化合物的存在可以提高白油的溶解性能和抗氧化性。
4.其他添加剂:为了提高15号白油的性能,往往会在基础油中添加一些添加剂,如抗氧化剂、清洁剂、润滑剂等。
这些添加剂可以改善白油的使用性能,延长其使用寿命。
5.微量杂质:由于15号白油的精制过程不可能完全去除所有杂质,因此往往会在产品中残留一些微量杂质,如水分、硫化物、氮化物等。
这些杂质对白油的整体性能影响不大。
总之,15号白油是一种高纯度、化学稳定性好的矿物油。
其成分主要包括饱和烃类化合物、不饱和烃类化合物、芳香烃类化合物以及其他添加剂和微量杂质。
这些成分共同作用,
使15号白油具有优良的物理性能和化学性能,被广泛应用于工业、医药、化妆品等领域。
实验十五 卤代烃的性质

实验十五卤代烃的性质一、实验目的掌握卤代烃的化学性质和鉴别方法。
二、实验原理取代反应和消除反应是卤代烃的主要化学性质。
其化学活性取决于卤原子的种类和烃基的结构。
叔碳原子上的卤素活泼性比仲碳和伯碳原子上的要大。
在烷基结构相同时,不同的卤素表现出不同的活泼性,其活泼性次序为:RI>RBr>RCl>RF。
乙烯型的卤原子都很稳定,即使加热也不与硝酸银醇的溶液作用。
烯丙型卤代烃非常活泼,室温下与硝酸银的醇溶液作用。
隔离型卤代烃需要加热才与硝酸银的醇溶液作用。
卤代烷与碱的醇溶液共热,分子中脱去卤化氢等小分子形成双键的反应叫消除反应。
三、主要药品1-溴丁烷1-氯丁烷1-碘丁烷溴化苄溴苯硝酸银乙醇5%氢氧化钠四、实验操作⑴与硝酸银的乙醇反应[1]①不同烃基结构的反应取三支干燥试管并编号,在管1中加入10滴1-溴丁烷,管2中加入10滴溴化苄(溴苯甲烷)管3中加入10滴溴苯,然后各加入4滴2%硝酸银的乙醇溶液,摇动试管观察有无沉淀析出。
如10min后仍无沉淀析出,可在水浴上加热煮沸后再观察。
写出它们活泼性次序。
②不同卤原子的反应取三支干燥试管并编号,各加入4滴2%硝酸银的乙醇溶液,然后分别加入10滴1-氯丁烷、1-溴丁烷及1-碘丁烷。
按上述方法观察沉淀生成的速度,写出它们活泼性的次序。
⑵卤代烃的水解[2]①不同烃基结构的反应取三支试管,分别加入10~15滴1-氯丁烷、2-氯丁烷及2-氯-2-甲基丙烷,然后在各管中加入1~2ml 5%氢氧化钠,充分振荡后静置。
小心取水层数滴,加入同体积稀硝酸酸化,用2%硝酸银检查有无沉淀。
若无沉淀,可在水浴上小心加热,再检查。
比较三种氯代烃的活泼性次序。
②不同卤原子的反应取三支试管分别加入10~15滴1-氯丁烷、1-溴丁烷及1-碘丁烷,然后各加入1~2ml 5%氢氧化钠,振荡,静置。
小心取水层数滴,按上述方法用稀硝酸酸化后,再用2%硝酸银检查,记录活泼性次序。
③β-消除反应实验在一试管中加入1g氢氧化钾固体和乙醇4~5 ml,微微加热,当KOH全部溶解后,再加入溴乙烷1mL振摇混匀,塞上带有导管和塞子,导管另一端插入盛有溴水或酸性高锰酸钾溶液的试管中。
第二章《烃》测试题20212022学年高二人教版2019化学选择性必修3

第二章《烃》测试题一、单选题(共15题) 1.下列物质能确定其为丙烯的是 A .B .36C HC .D .23CH CH CH —2.某气态烃0.5mol 能与0.5molCl 2完全加成,加成产物又可被3molCl 2完全取代,则此气态烃可能是 A .CH 2=CH 2 B .CH 3—CH=CH 2 C .CH 2=CHCH 2CH 3D .CH 2=CH—CH=CH 23.2,2,4 - 三甲基戊烷俗称异辛烷(),常加入汽油中来减震,下列各烃与氢气加成能得到异辛烷的是 A .2,2,4 -三甲基-1-戊烯 B .2,4,4 - 三甲基-1-戊烯 C .2,4,4 - 三甲基-2-戊炔D .3,4,4 - 三甲基-1-戊炔 4.设A N 为阿伏加德罗常数的值,下列说法正确的是 A .标准状况下,11.2L 己烷所含的分子数为A 0.5N B .30g 乙烷分子中含有的共用电子对数为A 6NC .标准状况下,11.2L 丙炔和乙烯混合物中含氢原子数目为A 2ND .常温常压下,1mol 苯中含有A 3N 碳碳双键和A 3N 碳碳单键 5.除去相关物质中的杂质,所选试剂正确的是A.A B.B C.C D.D6.下列化学用语表示错误的是A.甲醛的电子式:B.苯的球棍模型:CH CH=CH D.1,2-二溴乙烷的键线式:C.丙烯的结构简式:327.甲、乙、丙三种有机化合物的键线式如图所示。
下列说法不正确的是C HA.甲、乙的化学式均为814B.甲、乙、丙均能使酸性高锰酸钾溶液褪色C.乙的一氯代物共有2种(不考虑立体异构)D.丙的名称为乙苯,其分子中所有碳原子可能共平面8.下列用系统命名法命名的有机物名称正确的是A.2—甲基—4—乙基戊烷B.3,4,4—三甲基己烷C.2,3—二甲基戊烷D.1,2—二甲基丙烷9.某单烯烃加氢后产物的键线式为,考虑顺反异构,则该烯烃有A.3种B.5种C.6种D.7种10.下列实验操作对应的现象符合事实的是A.图1:用饱和碳酸钠溶液除去CO中含有的CO2,有沉淀析出B.图2:向铜片中加浓硫酸加热,铜片表面有气泡逸出,溶液逐渐变蓝色C.图3:向试管中加入2mL苯,再加入0.5mL酸性KMnO4溶液,振荡、静置,下层液体呈无色D .图4:用洁净的玻璃棒蘸取某溶液,在酒精灯火焰上灼烧,火焰呈黄色,说明溶液中含Na +11.下列说法不正确的是A .乙炔与分子式为C 4H 6的烃一定互为同系物B .乙炔和乙烯都能发生加成反应和加聚反应C .乙炔分子中含有极性键和非极性键D .乙炔是直线形分子,碳原子都是sp 杂化12.设A N 为阿伏加德罗常数的值,下列说法不正确的是 A .44g 丙烷中含有的共价键总数为A 10NB .28g 由乙烯和丙烯()36C H 组成的混合物完全燃烧生成的2CO 分子的数目为A 2N C .标准状况下,32.24LCH Cl 分子中含C H -键的数目为A 0.3ND .11mol L -⋅的醋酸溶液中所含3CH COOH 分子的数目一定小于A N13.用如图装置可探究部分物质的性质,用下列各选项的药品不能得出相应结论的是A .AB .BC .CD .D14.设N A为阿伏加德罗常数的值。
苏教版高二化学选修5专题三《常见的烃》测试题(含答案解析)

苏教版⾼⼆化学选修5专题三《常见的烃》测试题(含答案解析)绝密★启⽤前苏教版⾼⼆化学选修5专题三《常见的烃》测试题本试卷分第Ⅰ卷和第Ⅱ卷两部分,共100分,考试时间150分钟。
第Ⅰ卷⼀、单选题(共15⼩题,每⼩题3.0分,共45分)1.下列性质中,属于烷烃特征的是()A.完全燃烧产物只有⼆氧化碳和⽔B.它们⼏乎不溶于⽔C.分⼦的通式为,与氯⽓发⽣取代反应D.它们是⾮电解质2.下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中⼀定不存在同分异构体的反应是()A.异戊⼆烯()与等物质的量的Br2发⽣加成反应B. 2-氯丁烷与NaOH⼄醇溶液共热发⽣消去HCl分⼦的反应C.甲苯在⼀定条件下发⽣硝化反应⽣成⼀硝基甲苯的反应D.邻羟基苯甲酸与NaHCO3溶液反应3.下列现象因为发⽣加成反应⽽产⽣的是()A.⼄烯使酸性KMnO4溶液褪⾊B.将苯滴⼊溴⽔中,振荡后⽔层接近⽆⾊C.⼄烯使溴的四氯化碳溶液褪⾊D.甲烷与氯⽓混合,光照⼀段时间后黄绿⾊消失4.苯的结构简式可⽤来表⽰,下列关于苯的叙述中正确的是()A.苯分⼦中6个碳碳化学键完全相同B.苯中含有碳碳双键,所以苯属于烯烃C.苯主要是以⽯油为原料⽽获得的⼀种重要化⼯原料D.苯可以与溴⽔、⾼锰酸钾溶液反应⽽使它们褪⾊5.下列化合物中既易发⽣取代反应,也可发⽣加成反应,还能使酸性溶液褪⾊的是 () A.⼄烷B.⼄醇C.丙烯D.苯6.下图表⽰4-溴环⼰烯所发⽣的4个不同反应。
其中,产物只含有⼀种官能团的反应是()A.①②B.②③C.③④D.①④7.下列有关简单的烷烃的叙述中正确的是()①都是易燃物②特征反应是取代反应③相邻两个烷烃在分⼦组成上相差⼀个甲基A.①和③B.②和③C.只有①D.①和②8.下列物质属于芳⾹烃,但不是苯的同系物的是()A.③④B.②⑤C.①②⑤⑥D.②③④⑤⑥9.⽤下图所⽰装置检验⼄烯时不需要除杂的是 ()10.下列关于油和脂肪的⽐较错误的是()A.油的熔点低,脂肪的熔点⾼B.油含不饱和烃基的相对量⽐脂肪少C.油和脂肪都不易溶于⽔,易溶于汽油、酒精、苯等有机溶剂D.油经过氢化可以转化为脂肪,通常⼜叫做硬化油11.下列各对物质中,互为同系物的是()12.已知:,如果要合成,所⽤的起始原料可以是()①2-甲基-1,3-丁⼆烯和2-丁炔②1,3-戊⼆烯和2-丁炔③2,3-⼆甲基-1,3-戊⼆烯和⼄炔④2,3-⼆甲基-1,3-丁⼆烯和丙炔A.①④ B.②③ C.①③ D.②④13.分⼦式为C5H11Cl,在NaOH溶液中加热反应,⽣成的有机物在Cu的催化作⽤下加热反应,氧化产物能发⽣银镜反应的有(不考虑⽴体异构)()A. 2种B. 4种C. 6种D. 8种14.⼄烷在光照条件下与氯⽓发⽣取代反应,理论上得到的氯代物最多有⼏种()A. 5种B. 6种C. 8种D. 9种15.烯烃不可能具有的性质有()A.能使溴⽔褪⾊B.加成反应C.取代反应D.能使酸性KMnO4溶液褪⾊第Ⅱ卷⼆、⾮选择题(共5⼩题,每⼩题11.0分,共55分)16.烃A是合成⾷品包装袋的原料,A的⼀系列反应如下(部分反应条件略去):回答下列问题:(1)A的化学名称是________,E的结构简式是_______________;(2)E与C的关系:________;(3)反应⑥的化学⽅程式为____________________,其反应类型为___________;(4)与F互为同分异构体且不与Na反应的有机物的结构简式为________。
有机化学推导题
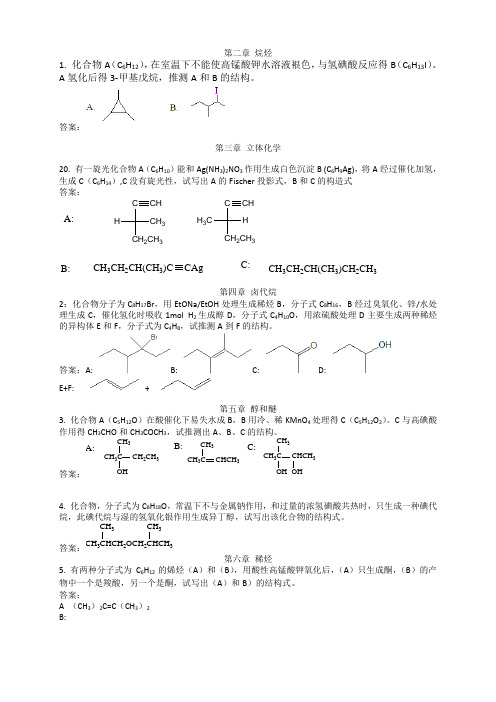
第二章 烷烃1. 化合物A (C 6H 12),在室温下不能使高锰酸钾水溶液裉色,与氢碘酸反应得B (C 6H 13I )。
A 氢化后得3-甲基戊烷,推测A 和B 的结构。
答案:第三章 立体化学20. 有一旋光化合物A (C 6H 10)能和Ag(NH 3)2NO 3作用生成白色沉淀B (C 6H 9Ag),将A 经过催化加氢,生成C (C 6H 14),C 没有旋光性,试写出A 的Fischer 投影式,B 和C 的构造式 答案:CCH 2CH 3CH 3HCH CCH 2CH 3H H 3CCH A:B:CH 3CH 2CH(CH 3)CCAgCH 3CH 2CH(CH 3)CH 2CH 3C:第四章 卤代烷2:化合物分子为C 8H 17Br ,用EtONa/EtOH 处理生成稀烃B ,分子式C 8H 16,B 经过臭氧化、锌/水处理生成C ,催化氢化时吸收1mol H 2生成醇D ,分子式C 4H 10O ,用浓硫酸处理D 主要生成两种稀烃的异构体E 和F ,分子式为C 4H 8,试推测A 到F 的结构。
答案:A: B:C: D:E+F: +第五章 醇和醚3. 化合物A (C 5H 12O )在酸催化下易失水成B ,B 用冷、稀KMnO 4处理得C (C 5H 12O 2)。
C 与高碘酸作用得CH 3CHO 和CH 3COCH 3,试推测出A 、B 、C 的结构。
答案:A:CH 3CCH 3CH 2CH 3CH 3CCH 3CHCH 3CH 3C CH 3CHCH 3B:C:4. 化合物,分子式为C 8H 18O ,常温下不与金属钠作用,和过量的浓氢碘酸共热时,只生成一种碘代烷,此碘代烷与湿的氢氧化银作用生成异丁醇,试写出该化合物的结构式。
答案:CH 32OCH 23CH 3CH 3第六章 稀烃5. 有两种分子式为C 6H 12的烯烃(A )和(B ),用酸性高锰酸钾氧化后,(A )只生成酮,(B )的产物中一个是羧酸,另一个是酮,试写出(A )和B )的结构式。
多环芳烃物质15项

多环芳烃物质15项
多环芳烃(PAHs)是一类有机化合物,具有两个或两个以上的苯环。
国际癌研究中心(IARC)在1976年列出的94种对实验动物致癌的化合物中,有15种属于多环芳烃。
这类化合物是原油的天然成分,也是炼油过程中常见的残留物。
这15种多环芳烃包括萘、苊烯、苊、芴、菲、蒽、荧蒽、芘、苯并(a)蒽、屈、苯并(b)荧蒽、苯并(k)荧蒽、苯并(a)芘、茚苯(1,2,3-cd)芘和二苯并(a,n)蒽。
其中,苯并芘是第一个被发现的环境化学致癌物,而且致癌性很强,因此常作为多环芳烃的代表。
此外,在PAHs的检测种类中,还常见包括苊、芴、菲、荧蒽、芘等化合物。
这些物质有一种类似于汽车轮胎或沥青的特有气味,含有多环芳烃的油渣作为软化剂或增量剂添加到橡胶和塑料中。
儿童玩具中可能含有多环芳烃等有害物质,这些物质来源于其原料本身或是生产过程中使用的辅料。
如果这些物质超标,儿童皮肤长期接触此类玩具,容易通过舔食、吮吸、皮肤吸收等行为将有害物质摄入体内,危及儿童健康。
因此,建议在日常生活中注意防范多环芳烃等有害物质的危害。
人教版初中高中化学选修三第二章《烃》知识点(含答案解析)

一、选择题1.下列关于的说法正确的是A.所有原子可能都在同一平面上B.最多只可能有9个碳原子在同一平面C.有7个碳原子可能在同一直线D.只可能有5个碳原子在同一直线答案:D解析:A.分子中有甲基,具有甲烷的正四面体结构,所有原子不可能在同一平面上,故A错误;B.甲基碳位于碳碳双键平面内,碳碳三键的直线结构位于苯环的平面内,碳碳双键平面和苯环平面,可以通过碳碳单键的旋转使两个平面重合,所以最多有11个碳原子共面,最少有9个碳原子共面,故B错误;C.苯环是平面图形,两个基团位于苯环的对位位置,碳碳三键为直线型结构,连接苯环的碳碳双键的碳原子处于苯中氢原子的位置,此碳原子、苯环上相连的碳原子和苯环对位的碳原子以及碳碳三键上的碳原子,一共5个碳原子共直线,故C错误;D.苯环是平面图形,两个基团位于苯环的对位位置,碳碳三键为直线型结构,连接苯环的碳碳双键的碳原子处于苯中氢原子的位置,此碳原子、苯环上相连的碳原子和苯环对位的碳原子以及碳碳三键上的碳原子,一共5个碳原子共直线,故D正确;故答案为:D。
2.下列说法正确的是A.C240和C340互为同素异形体B.氕、氘、氚是氢元素的三种核素,其中子数相同C.CH3COOH与HCOOCH2CH3互为同系物D.C3H8的一氯取代物有3种答案:A解析:A.C240和C340都是由碳元素形成的单质,但二者组成和结构都不同,所以互为同素异形体,A正确;B.氕、氘、氚是氢元素的三种核素,其质子数相同,但中子数不同,B不正确;C.CH3COOH属于羧酸,而HCOOCH2CH3属于酯,所以二者不互为同系物,C不正确;D.C3H8分子中只有2种不同性质的氢原子,所以其一氯取代物有2种,D不正确;故选A。
3.下列说法错误的是A.乙酸乙酯在NaOH溶液中水解完全后静置分层,混合液上层为有机层B.乙酸的分子式可表示为C2H4O2C.石油分馏是物理变化,可得到汽油、煤油和柴油等产品D.相同物质的量的C3H6和C3H8O,充分燃烧,消耗氧气量相同答案:A解析:A.乙酸乙酯在NaOH溶液中水解完全后产生CH3COONa、CH3CH2OH,两种物质都易溶解在水中,因此静置后液体不分层,A错误;B.乙酸结构简式是CH3COOH,分子式为C2H4O2,B正确;C.石油是多种烃的混合物,根据物质沸点的不同,采用分馏的方法分离。
烃的知识总结

填空题甲烷是和的主要成分,甲烷的分子式是,电子式,结构式实验证明甲烷分子中的五个原子不在同一个上,而是构成一个四个C—H键强度,键角。
甲烷的物理性质:颜色,状态,气味,密度(与空气相比),水溶性。
甲烷的化学性质:强酸强碱发生反应。
甲烷与氧气反应方程:实验现象甲烷点燃之前要,怎样证明甲烷燃烧产物是水与二氧化碳。
取代反应:有机分子中的或被其他或所替代的反应。
甲烷与氯气的取代反应方程:方程 1 生成物状态方程2 生成物状态方程3 生成物状态方程4 生成物状态取代反应的得到的产物是(混合物或纯净物)并写出出三氯甲烷与四氯甲烷的俗称与结构式电子式,,,,,。
取代反应要求卤素单质必须是(混合物或纯净物)反应条件是。
实验现象为:。
一个氯气分子一次取代个氢原子,1 mol 甲烷完全被取代需要mol 氯气,生成mol HCl。
甲烷(能或不能)氯水发生反应。
甲烷的氯的取代物密度比水。
写出下列物质的结构简式:乙烷,丙烷,丁烷,异丁烷,戊烷异戊烷新戊烷碳碳之间以键结合成状,剩余的价键均与结合,使每一个碳都达到这样的烃叫烃也称烷烃,烷烃的通式是,烷烃的燃烧方程烃的燃烧方程。
结构组成上相差的物质成为同系物。
同系物物理性质化学性质。
烷烃的习惯命名法用表示碳原子数目,碳原子数相同时用区分。
相同不同的有机物称为同分异构现象,具有的化合物互称同分异构体。
同分异构体的化学性质物理性质相同(不一定或一定)。
烷烃的物理性质:碳原子数为气态为液态为固态,碳原子数越多熔沸点碳原子数相同支链越多熔沸点。
能够说明甲烷是正四面体结构的依据是。
烃基是烃分子失去后剩余的部分,写出甲基,乙基的结构式,写出庚烷所有的同分异构体的结构简式:1 ,2 ,3 ,4 ,56 ,7 ,8 ,9并指出那种结构庚烷一氯取代物有三种同分异构体。
电子数为42的烷烃是。
密度是1.16g/L 的烷烃混合物中一定有,等物质的量的气态烷烃完全燃烧耗氧量最大的是,等质量烷烃完全燃烧耗氧量与有关。
高中化学必修二考点知识讲解与同步练习17---烃 有机高分子材料

高中化学必修二考点知识讲解与同步练习烃有机高分子材料[核心素养发展目标]1.了解烃的概念及分类,了解常见烃的组成及结构,培养“证据推理与模型认知”能力。
2.初步认识有机高分子材料的组成、性能,了解塑料、合成橡胶、合成纤维的性能及在生活生产中的应用,培养“宏观辨识与微观探析”的学科素养。
一、烃1.烃的概念仅含碳和氢两种元素的有机化合物称为碳氢化合物,也称为烃。
2.烃的分类依据:烃分子中碳原子间成键方式的不同及碳骨架的不同。
3.常见烃分子结构探究目的:通过学习甲烷、乙烯、乙炔的分子结构,理解常见烃的分子结构特点。
活动记录:烃甲烷乙烯乙炔电子式化学键C—H共价单键C—H共价单键和共价键C—H共价单键和—C≡C—键球棍模型分子结构特点碳原子4个单电子完全和4个氢原子形成4个共价单键,形成以碳原子为中心的正四面体结构碳和碳形成碳碳双键,剩余价键完全和氢原子形成C—H单键,键和键夹角为120°,2个碳原子和4个氢原子在同一平面内碳和碳形成碳碳三键,剩余价键和氢原子形成C—H单键,键和键夹角为180°,2个氢和2个碳原子成直线结构(1)含有碳和氢两元素的有机化合物就属于烃( ×)提示烃是分子中只含C和H两元素的有机化合物。
(2)属于烃的有机化合物分子中氢原子个数可以为奇数( ×)提示根据碳原子的4价键理论,烃分子中的氢原子一定为偶数。
(3)甲烷、乙烯和乙炔分子中都只含有碳和氢两元素,故它们是同系物( ×)提示三者的结构不同,甲烷分子中全部为单键,乙烯分子中含有碳碳双键,乙炔分子中含有碳碳三键,而且分子组成上也不相差一个或若干个CH2原子团,故不为同系物。
(4)乙烯的分子式为C2H4,故分子组成为C6H12的烃一定属于烯烃( ×)提示分子组成为C6H12的烃,可以是烯烃,也可能属于环烷烃,如环己烷。
(5)苯的分子式为C6H6,结构简式为,分子高度不饱和,故苯分子中一定含有碳碳双键,属于烯烃( ×)提示苯分子中含有,结构简式是一种习惯写法,分子中不含有,属于芳香烃。
实验15 芳烃的性质

实验15 芳烃的性质一、实验目的1. 掌握芳烃的品质鉴定方法,确定某些未知物质是否为芳烃。
2. 通过芳烃的性质实验,了解芳烃的燃烧性、溶解度、氧化还原性和取代反应等基本特性。
二、实验原理1. 芳烃的品质鉴定方法物质是芳烃有以下特点:(1)有苯环,即C6H5结构为母体结构。
(2)具有芳香味。
(3)较难与其他有机物发生反应。
(4)加热容易发生热解或裂解,产生芳烃或芳香烃。
(5)在硫酸、硝酸等强酸剂中不容易被铜或铁还原,但容易被氢氧化钠或氢氧化钾还原。
(6)芳烃的热稳定性较高,即能承受较高的温度而不分解。
(1)芳烃的燃烧性:芳烃燃烧时释放出大量的热能,并产生CO2和H2O,因此燃烧产生的热值较高。
(2)芳烃的溶解度:芳烃具有不良的溶解度,与水的溶解度很小,而与有机溶剂的溶解度较大。
(3)芳烃的氧化还原性:芳烃中的苯环与其他原子发生反应时,多数发生电子云共享的碳碳键加成反应。
(4)芳烃的取代反应:由于苯环的稳定性较高,是很难发生加成反应的,但是芳烃中的氢原子与一些取代试剂反应,可以发生取代反应。
三、实验操作将待鉴定物质溶解在水中,加入过量的氢氧化钾,观察是否有悬浮在溶液中的黄色物质出现,若出现,则为芳香酮或芳香烃。
2. 燃烧性实验将几滴苯加入蒸馏水中,并用玻璃杯盖住,将其倒置,用火机将水中的苯点燃,观察燃烧现象。
3. 溶解度实验取一定量的苯和甲醇,分别倒入两个试管中,观察两者是否能充分混合。
4. 氧化还原性实验将几滴溶有铁离子的盐酸滴入苯溶液中,观察反应现象。
5. 取代反应实验向苯溶液中加入利什曼试剂,观察反应现象。
四、实验结果及分析实验时发现苯能够燃烧,并产生明亮的火焰,燃烧结束后产生CO2和H2O。
经实验可知,苯与甲醇不能充分混合。
实验时,在苯溶液中加入少量的铁离子溶液,发现溶液颜色由无色变为了深紫色,说明芳烃具有较高的电子云稳定性,难于发生氧化还原反应。
实验时,将貌似白色结晶的利什曼试剂溶解在苯溶液中,观察到溶液由无色变为棕色,说明在利什曼试剂的作用下,苯中的氢原子被取代。
单元15 烃的衍生物

单元15 烃的衍生物班级________姓名________学号________1. 根据右面乙酸分子的化学键断键立置的示意图,回答下列问题:(1)乙酸与乙醇生成CH 3COOC 2H 5时断键的位置是_________________;当乙酸表现出酸的通性时,断键的位置是____________________。
(2)请用化学方程式和必要的文字来说明乙酸的酸性。
2. 工业上可用乙醛制乙酸。
(1)在制备过程中,证明已有乙醛被氧化为乙酸的方法是:取反应后的混合物并配成溶液,在溶液中加入__________,当观察到__________时,即可证明有乙酸生成。
(2)有同学认为,证明乙醛已被完全氧化的方法是:向反应后的溶液加入新制氢氧化铜,加热,若无红色沉淀生成,说明已被完全氧化。
请你评价这种方法是否存在问题,并说出理由。
________________________________________________________________________________ 写出乙醛与新制氢氧化铜反应的化学方程式:________________________________________。
3. 已知有机物M 的结构如右图示。
关于M 的描述正确的是A.分子式为C 11H 7O 2ClB.1mol M 与H 2发生加成反应时,最多消耗5mol H 2C.1mol M 与Br 2发生加成反应时,最多消耗4mol Br 2D.1mol M 与NaOH 溶液发生反应时,最多消耗2mol NaOH异戊二烯是重要的有机化工原料,其结构简式为:。
异戊二烯的一种制备方法如下图所示:(1)A 中含氧官能团能发生的反应有______________________________。
(填反应类型)(2)B 的结构简式为____________________。
B 的同分异构体Y 能发生银镜反应,则Y 可能的结构有__________种。
烃的复习

烃的复习一、学习目标1、以烷、烯、炔和芳香烃的代表物为例,比较他们在组成、结构、性质上的差异。
2、了解天然气、液化石油气和汽油的主要成分和用途。
3、举例说明烃类物质在有机合成和有机化工中的重要作用。
二、学习内容1、以烷、烯、炔和芳香烃的代表物为例,比较他们在组成、结构、性质上的差异。
(1)各类烃组成、结构、性质上的差异(是否能反应,条件是什么,产物是什么。
)(2)、方程式书写甲烷和氯气反应:反应类型:。
乙烯使溴水褪色:反应类型:。
工业制备乙醇:反应类型:。
制备聚苯乙烯:反应类型:。
乙炔制备聚氯乙烯:反应类型:。
2-甲基-1,3-丁二烯:反应类型:。
苯和液溴反应:反应类型:。
苯和浓硝酸、浓硫酸混合加热:反应类型:。
甲苯和浓硝酸制备TNT:反应类型:。
2、了解天然气、液化石油气和汽油的主要成分和用途。
(1)判断下列过程是化学变化还是物理变化。
煤的干馏、煤的气化、煤的液化、分馏(蒸馏)、裂化、裂解。
(2)天然气、液化石油气、汽油的主要成分。
3、与烃有关的几个实验分析。
(1)甲烷取代把1体积甲烷和4体积氯气组成的混合气体充入大试管中,将此试管倒立在盛有硅酸钠溶液的水槽中,放在光亮处,一段时间后出现的现象为?(2)乙烯的制备及性质(圆底烧瓶中有浓硫酸和乙醇的混合物)①实验室制备乙烯的原理是?(方程式表示),在140℃产生副产品乙醚的原理?各自的反应类型为?②加热一段时间后,圆底烧瓶中有黑色物质生成,请解释原因?③洗气瓶中装有的液体是?作用是?试管中液体可以是什么?3、溴苯的制备(1)反应开始前已向仪器A中加入的是药品是?装在左侧分液漏斗中的药品是?装有碱石灰的C的作用是?(2)将左侧分液漏斗的旋纽打开后,在A中可观察到的现象是?(3)冷凝管B有上、下两口,冷却水应从口进入。
(4)反应结束后加入NaOH其作用是?最终如何获得溴苯?(5)要证明该反应是取代反应,方便的实验方法有哪些?【思维含量题】:由两种气态烃组成的混合物20mL与过量的氧气混合后进行燃烧,当燃烧产物通过浓硫酸后,体积减小了30mL,再通过碱石灰,体积又减少40mL。
烃的概述烷烃的化学性质

第1章第3节第1课时烃的概述烷烃的化学性质班级:高二( )班姓名:座号:【目标导航】1.了解烃的分类。
2.了解烷烃、烯烃、炔烃、苯及其同系物的物理性质。
3.掌握烯烃、炔烃的命名规则(含一个双键或叁键)。
(重点) 4.掌握烷烃的结构和化学性质。
(重点) 知识点1 烃的概述微体验(1)烷烃属于饱和烃,也属于链烃。
() (2)不饱和烃分子中一定含有碳碳双键或碳碳叁键。
()(3)含有苯环的有机物属于芳香烃。
()题组1烃的分类及物理性质1.下列关于芳香族化合物的叙述中正确的是()A.其分子组成的通式是C n H2n-6B.分子里含有苯环的烃C.分子里含有苯环的有机物D.苯及其同系物的总称2.已知①丁烷;②2-甲基丙烷;③正戊烷;④2-甲基丁烷;⑤2,2-二甲基丙烷,下列关于它们的沸点的排列顺序正确的是()A.①>②>③>④>⑤B.⑤>④>③>②>①C.③>④>⑤>①>②D.②>①>⑤>④>③3.下列各烃属于苯的同系物的是()4.按照要求对下列物质进行分类(将序号填在横线上)。
(1)属于链烃的为________。
(2)属于环烃的为________。
(3)属于脂环烃的为________。
(4)属于芳香烃的为________。
题组2烃的命名5.下列有机物命名正确的是()6.下列四种命名正确的是()A.2-甲基-2-丁炔B.2-乙基丙烷C.3-甲基-2-丁烯D.2-甲基-2-丁烯7.分子式为C8H10的芳香烃,苯环上的一硝基取代物只有一种,该芳香烃的名称是() A.乙苯B.邻二甲苯C.间二甲苯D.对二甲苯8.(1)用系统命名法命名下列物质:(2)根据下列名称写出各物质的结构简式:知识点2 烷烃的化学性质微体验(1)烷烃能使酸性KMnO4溶液退色。
()(2)常温下,烷烃均为气体,易燃烧。
()(3)烷烃在一定条件下与卤素单质反应生成卤代烃。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
浓硫酸
O2N
NO2
• 三硝基甲苯是淡黄色针状晶体,不溶于水。不稳定, 易爆炸 —CH3对苯环的影响使取代反应更易进行
7、CxHy 燃烧
点燃 CxHy+(x+y/4)O2
__________________________.
xCO2+y/2H2O
CxHyOz燃烧:
点燃
CxHyOZ+(x+y/4-z/2)O2
5、化学性质(1)可燃性 现象:火焰明亮并带有浓烟
2C6H6 + 15O2
点燃
12CO2 + 6H2O
注意:苯易燃烧,但不能被酸性KMnO4溶液氧化
2. 苯的硝化反应
注: 1.100℃以下,均可采 用水浴加热。 2.温度计悬挂在水浴中。
(2)取代反应(硝化反应)
_____________________________________ 催化剂 吸水剂 a、浓硫酸的作用:______________________ 水浴 b、根据温度可采用___________方式加热。
_______________________.
xCO2+y/2H2O
8、CxHy耗氧量最多的计算问题: (1)等物质的量时 (x+y/4)越大,耗氧量越大 _____________________________________ (2) 等质量时 (y/x)越大,耗氧量越大 ____________________________________. 1、2、3 9、满足CxH4的x值可以是____________,它们在 温度高于100度时,反应前后气体物质的量不变.
( 2 ) 物理性质: 天然气、沼气、坑道气、瓦斯的主要 甲烷 成分都是____________.甲烷是摩尔质量最小的有机 难 物, ______溶于水,无色,无味的气体 。
( 3) 化学性质: 点燃 ①可燃性 CH4+2O2 CO2+2H2O A 、燃烧方程式:_____________________ 淡蓝 B 、现象:火焰呈______色,放出大量热,产 变浑浊 生的气体能使澄清的石灰水_______ C、用作理想的清洁燃料原因: 产物是CO2和H2O,无污染;相同体积的气体CH4放热量高。 _________________________________ ② 取代反应: A、取代反应的特点:取而代之,有上有下。 B 、甲烷与氯气的取代反应: (四个方程式) 下一页 ___________________________.
主要用途
气体燃料,化工原料 氮肥
粗氨 水 粗苯 煤焦油
苯 甲苯 二甲苯 苯 甲苯 二甲苯 酚类 萘 沥青 碳
炸药,染料,医药, 农药,合成材料 医药,染料,农药, 合成材料 电极,筑路材料 冶金,燃料,合成氨
焦碳
3、苯的结构特点
简写为
结构简式(凯库勒式):___________________.
单、双键交替 其中6个键完全相同,不存_____________________,
是介于______________________________________. 12个原子处于同一平面。
碳碳单键和碳碳双键之间的一种独特的键
球棍模型
比例模型
4、物性
有 无色,有特殊气味,_____毒的液体, 不 小 密度比水________,__________溶于水。常 用作有机溶剂。易挥发。低于5.5℃,会凝结 成晶体.
加热
C8H18+C8H16
7、乙烯
(1)结构特点: H H CH2=CH2 C=C H H 结构式:_________结构简式:______ 平面结构 CH2 空间构型:_________最简式:___. 不 无 (2)物性:__色,稍有特殊气味气体。___溶 接近 于水,密度与空气____,可用作果实催熟剂. 乙烯的产量作为衡量国家石油化工发展水平 的标志。
光照下甲烷与氯气发生取代反应
CH4 + Cl2
光照
CH3Cl + HCl
CH3Cl + Cl2 光照 CH2Cl2 + HCl CH2Cl2 + Cl2 光照 CHCl3 + HCl CHCl3 + Cl2
光照
CCl4 + HCl
a 、无论比例如何产物通常都是混合物 光照 、 纯的卤素单质 b、条件:______________________ CH3CI c 、产物中只有______是气体,其余都是液体。 CHCI3 CCI4 ________被称为氯仿,_________可用于 火;__________常用做有机溶剂。 CCI4、CHCI3 1 d 、参加反应的1摩尔氯气,其中_____摩尔氯 原子存在有机物中。 f 、反应用箭头连接。 1 1 g 、甲烷一氯代物有___种,二氯代物有___种, 1 三氯代物有___种。
思考:甲烷气体中混有乙烯应如何鉴别、除杂。
通入高锰酸钾溶液中,溶液褪色; 或通入溴水中,溴水颜色褪去。 鉴别:_________________________________
除杂:________________________________
通入溴水中进行洗气。 (不可通入到高锰酸钾溶液中)
(四)煤---工业的粮食
正丁烷
异丁烷 CH3CHCH3
CH3CH2CH2CH3 CH3 __________________________ ; • 戊烷的同分异构体数目有_____种,名称与结构 3 简式为:
正戊烷 CH3CH2CH2CH2CH3 异戊烷 CH3CHCH2CH3 新戊烷 C(CH3)3
CH3 __________________________________. • 丙基的结构有_____________种;丁烷的一氯代 2 4 物共有______种,丁基的结构有______种;戊烷 4 的一氯代物共有______种。 8
一些常见烷基的名称: -CH3: 甲基 -CH2CH3: 乙基 -CH(CH3)2:异丙基 -CH2CH2CH3:正丙基
-CH2CH2CH2CH3:丁基
-CH2CH(CH3)2: -C(CH3)3 : 异丁基 第三丁基(特丁基)
CH2 CH3 -HC CH3
: 第二丁基(另丁基)
4、甲烷
(1)组成:
(3)化学性质: C2H4 +3O2
点燃
①与氧气反应 __________________________. 明亮 现象:火焰______,同时伴有_____. 黑烟 原因: 乙烯中含碳量高 _________________________. ②通入酸性高锰酸钾溶液中现象: 溶液紫红色退去 ______________________________.
重要的有机化合物必修2部分
一、有机物的通性
1、大多数含有碳元素的化合物是有机物,
CO2、 H2CO3 、NaHCO3 但_____________________除外。 2、大多有机物沸点低、难溶于水、可以燃烧。
碳 氢 3、烃中仅含有____和_______两种元素组成。
二、烷烃 (烷烃性质同甲烷)
2CO2+2H2O
③加成反应
有上无下 类似化合 • 定义:由不饱和键生成相对饱和键的反应。 注意:由碳碳三键生成双键或单键的反应、 双键生成单键的反应都属于加成反应。 Br Br A、与溴水加成方程式: CH2=CH2+Br2 CH2-CH2 ________________ 溴水褪色,溶液分层,下层呈油状物 现象:_________________. B、练习乙烯分别与加成 一定条件 (1)氢气_________________________ (2)水____________________________ (3)氯化氢__________________________
5、石油的裂化 (1)目的:提高轻质燃料的产量。 (2)课本举例:(十六烷裂化)
催化剂
C16H34
_________________________________. ( 3) 得到的汽油(裂化汽油)是否存在不饱和键? 存在 _________. 深度裂化 6、石油的裂解即———————————,得 到乙烯、丙烯等小分子烃。
苯Hale Waihona Puke • 1、煤中 除含有碳氢元素外,还含有少量的 碳、氢、硅、铝、硫、铁等 ___________________________元素,是 有机物和无机物的混合物。
• 2、 煤的干馏是将煤_______加强热使其分 解的过程,是_____变化。 化学
隔绝空气
干馏产物
炉 煤 气 焦炉 气
主要成分
氢气 甲烷 乙烯 一氧化碳 氨气 氨盐
苦杏仁 有 c、硝基苯的物性:________味,____________毒, 大 密度比水______ d、混合时,要将浓硫酸缓缓注入浓硝酸中,并不断振荡。 (3)苯与酸性高锰酸钾不反应,与溴水发生萃取(上 层呈_________色,下层几乎无色)。 橙红
6、TNT的制备:
CH3
CH3
+ 3HNO3 + 3H2O NO △ __________________________________.
碳碳单键 1、结构特点:除碳氢键外,都是_________ 键。烷烃是相同数目碳原子烃中结合氢原 子数目最多的烃。 CnH2n+2 2、通式:_________ (n≥1) 分子式 3、 同分异构体:具有相同_______而 结构 _________不同的化合物
• 丁烷的同分异构体数目有_____种,名称与结构 2 简式为:
C、甲烷不与酸、碱、酸性高锰酸钾反应。
甲烷不能使高锰酸钾溶液褪色,所以一 定不能发生氧化反应?
能在氧气中燃烧,可发生可发生氧化反应
三、石油--工业的血液
•
烯烃
