板蓝根质量标准及检验操作规程
112板蓝根注射液成品内控质量标准

天津市中升挑战生物科技有限公司GMP管理文件一、目的:制定板蓝根注射液成品的内控质量标准,确保板蓝根注射液成品的质量。
二、依据:《兽药规范》1978版。
三、适用范围:适用于板蓝根注射液成品的生产和检验。
四、责任者:QC五、正文:板蓝根注射液本品为板蓝根经提取制成的灭菌水溶液。
【制法】取板蓝根500g,加水煎煮二次,第一次2小时,第二次1小时,合并煎液,滤过,滤液浓缩至约750ml,冷却,加乙醇使含醇量达70%,搅匀,静置24小时,滤过,滤液回收乙醇至350~500ml,冷藏,滤过,滤液用氨试液调节pH值为8.0~8.5,搅匀,冷藏48小时,加热除去氨,加注射用水至900ml,冷藏,滤过,滤液用1%氢氧化钠溶液调节pH值为7.0~7.5,冷藏,滤过,滤液加甘露醇10g.并加注射用水调整总量至1000ml,滤过,灌封,灭菌,即得。
【性状】本品为棕黄色至棕色的澄明液体。
【鉴别】取本品作为供试品溶液。
另取板蓝根对照药材1g,加乙醇30ml,超声处理15分钟,滤过,滤液浓缩至约0.5ml,作为对照药材溶液。
再取L-脯氨酸对照品,加80%乙醇制成每1ml含2mg的溶液,作为对照品溶液,照薄层色谱法(附录Ⅵ B)试验,吸取上述三种溶液各2μl,分别点于同一硅胶G薄层板上,以正丁醇-水-冰醋酸(4:1:1)为展开剂,展开,取出,晾干,喷以0.2%茚三酮乙醇溶液,在105℃加热至斑点显色清晰。
供试品色谱中,分别在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的斑点。
【检查】pH值应为5.0~6.5(附录Ⅶ G)。
炽灼残渣取本品5ml,置已炽灼至恒重的坩埚中,置水浴上蒸干后,依法检查(附录Ⅸ J),遗留残渣不得过1.0%。
重金属取炽灼残渣项下遗留的残渣,依法检查(附录Ⅸ E第一法),含重金属不得过百万分之十。
其他应符合注射剂项下有关的各项规定(附录Ⅰ U)。
【含量测定】取本品,用适宜的氨基酸分析仪进行分离测定,另取L-脯氨酸、L-精氨酸、L-缬氨酸、L-γ-氨基丁酸、L-丙氨酸、L-亮氨酸、L-异亮氨酸、L-苯丙氨酸、L-丝氨酸、L-苏氨酸、L-酪氨酸对照品,制成相应浓度的对照品溶液,同法测定,按外标法的峰面积计算各种氨基酸的含量,并计算出总氨基酸的含量。
板蓝根颗粒质量标准及检验操作规程
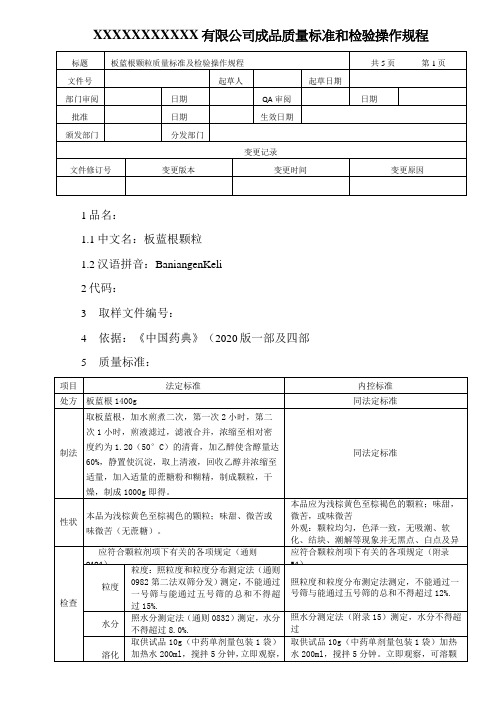
XXXXXXXXXXX 有限公司成品质量标准和检验操作规程1品名:1.1中文名:板蓝根颗粒 1.2汉语拼音:BaniangenKeli 2代码:3 取样文件编号:4依据:《中国药典》(2020版一部及四部 5 质量标准:6检验操作规程:6.1试药与试剂:十八烷基硅烷键合硅胶、甲醇、正丁醇、冰醋酸、水、茚三酮试液、板蓝根对照药材、L-脯氨酸对照品、精氨酸对照品、亮氨酸对照品、尿苷对照品、鸟苷对照品及腺苷对照品。
6.2仪器与用具:电子天平、水浴锅、干燥箱、超声波清洗器、硅胶G薄层板。
6.3性状:取本品适量,在自然光下目测形态和色泽,尝味,并记录结果。
6.4鉴别:(1)取本品适量2g(相当于饮片2.8g),研细,加乙醇10ml,超声处理30分钟,滤过,滤液浓缩至2ml,作为供试品溶液。
另取板蓝根对照药材0.5g,加乙醉20ml,同法制成对照药材溶液,再取L-脯氨酸对照品、精氨酸对照品、亮氨酸对照品,分别加乙醇制成每lml各含1mg的溶液,作为对照品溶液。
照薄层色谱法(通则0502)试验,吸取上述五种溶液各2〜5u l,分别点于同一硅胶G薄层板上,以正丁醇一冰醋酸一水(19:5:5)为展开剂,展开,取出,晾干,喷以茚三酮试液,在105r加热至斑点显色清晰,置日光下检视。
供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的斑点。
(2)取尿苷对照品、鸟苷对照品、(R,S)-告依春对照品及腺苷对照品,加5%甲醇制成每1ml含尿苷、鸟苷、(R,S)-告依春各20u g及腺苷25u g的混合溶液,作为对照品溶液,照<含量测定>项下的方法试验,吸取上述对照品溶液及<含量测定〉项下的供试品溶液各5-10u l,注入液相色谱仪,记录色谱图。
供试品色谱中,应呈现与对照品色谱峰保留时间相对应的色谱峰。
6.5检查:应符合颗粒剂项下有关的各项规定(附录54)。
6.6含量测定:6.6.1对照品溶液的制备取尿苷对照品、鸟苷对照品及腺苷对照品适量,精密称定,加5%甲醇制成每1ml含尿苷20u g,鸟苷20u g及腺苷25u g的混合溶液,即得。
板蓝根颗粒执行标准

板蓝根颗粒执行标准板蓝根颗粒是一种常见的中药材,具有清热解毒、抗病毒、抗炎等功效,被广泛应用于临床治疗。
为了保证板蓝根颗粒的质量和安全性,制定了相应的执行标准,以规范其生产过程和质量要求。
一、原料要求。
1. 板蓝根颗粒的原料应选用新鲜、无霉变、无虫蛀、无霉斑、无异物的板蓝根为原料。
2. 原料应符合《中华人民共和国药典》规定的品质标准。
二、生产工艺。
1. 原料处理,应将板蓝根进行清洗、除杂、晾干等处理,确保原料的干净和安全。
2. 提取工艺,采用适当的提取剂和工艺条件,进行板蓝根的提取工艺,确保有效成分的提取率和质量。
3. 干燥工艺,采用适当的干燥工艺,确保板蓝根颗粒的水分符合要求,且不影响有效成分的稳定性。
三、质量指标。
1. 外观,板蓝根颗粒应呈现均匀的颗粒状,无结块、异物和霉变现象。
2. 含量测定,板蓝根颗粒中有效成分的含量应符合国家标准规定的范围。
3. 溶出度,板蓝根颗粒在规定条件下的溶出度应符合国家标准规定的范围。
4. 微生物限度,板蓝根颗粒中细菌总数、霉菌和酵母菌数、大肠杆菌和沙门氏菌均应符合国家标准规定的限度要求。
5. 重金属、有害元素限量,板蓝根颗粒中重金属和有害元素的含量应符合国家标准规定的限量要求。
四、包装和储存。
1. 包装,板蓝根颗粒应采用符合食品包装卫生标准的包装材料,包装应牢固、密封良好,防潮、防污染。
2. 标签,包装上应标注产品名称、规格、生产日期、保质期、生产企业名称、生产许可证编号等信息。
3. 储存,板蓝根颗粒应储存在阴凉、干燥、通风、无异味的环境中,远离有害气体和阳光直射。
五、执行标准依据。
1. 《中华人民共和国药典》。
2. 国家药品监督管理局颁布的相关法规和标准。
3. 国家食品药品监督管理局颁布的相关法规和标准。
六、结论。
板蓝根颗粒执行标准的制定,对于保障板蓝根颗粒的质量和安全性具有重要意义。
各生产企业应严格按照执行标准的要求进行生产,确保产品质量稳定、安全可靠,为广大患者提供优质的药品保障。
112板蓝根注射液成品内控质量标准

天津市中升挑战生物科技有限公司GMP管理文件题目板蓝根注射液成品内控质量标准编码 B.ZL.CP.02.112制定审核批准制定日期审核日期批准日期颁发部门GMP办颁发数量2份执行日期分发部门生产部、质量部共1页第 1 页一、目的:制定板蓝根注射液成品的内控质量标准,确保板蓝根注射液成品的质量。
二、依据:《兽药国家标准》化学药品、中药卷第一册(农业部公告第1960号)。
三、适用范围:适用于板蓝根注射液成品的生产和检验。
四、责任者:QC五、正文:板蓝根注射液本品为十字花科植物菘蓝的干燥根。
经水煮提取制成的灭菌水溶液,每2ml相当于原生药1g。
【制法】取板蓝根500g(以干燥品计算),水煎二次,第一次1小时30分钟,第二次1小时,药汁滤过,澄清,70℃以下减压浓缩至650~700g。
冷却至60℃以下,在搅拌下缓缓加入95%乙醇,至溶液含醇量达60%,静置沉淀,滤过,滤液减压浓缩300~350g,冷藏静置沉淀。
滤过,滤液加浓氨水调节pH值至8.0左右,冷藏静置沉淀。
滤过,滤液加热去氨(pH值至5.5~6.0),冷藏静置沉淀。
滤液加注射用水至500ml,滤过,加注射用水至约950ml,加10g聚山梨酯80,苯甲酸10g,调节pH值,加注射用水至1000ml。
用4号垂熔漏斗滤过,灌封,灭菌,即得。
【性状】本品为棕色澄明灭菌溶液。
【检查】pH值应为5.0~6.5(附录49页)。
可见异物应符合规定。
无菌应符合规定。
装量按最低装量检查法(附录67页)检查,应符合规定。
【含量测定】精密量取本品2ml,加0.05mol/L硫酸溶液20ml,置水浴中加热15分钟,放冷,加0.1mol/L氢氧化钠溶液20ml中和后,精密加入碘滴定液(0.05mol/L)20ml和0.1mol/L氢氧化钠溶液40ml,放置10分钟,加稀硫酸溶液3ml,用硫代硫酸钠滴定液(0.1mol/L)滴定,至近终点时,加淀粉指示剂2ml,继续滴定至蓝色消失。
板蓝根质量标准及检验操作规程

XXXXXXX有限公司原料质量标准及检验操作规程1 品名:1.1 中文名:板蓝根1.2 汉语拼音:Banlangen2 代码:3 取样文件编号:4 检验方法文件编号:5 依据:《中国药典》(2020年版一部)。
6 质量标准:7 检验操作规程:7.1试药与试剂:稀乙醇、板蓝根对照药材、(R-S)-告依春对照品、甲醇、石油醚(60~90℃)、乙酸乙酯、盐酸、精氨酸对照品、羧甲基纤维素钠、正丁醇、冰醋酸、茚三酮试液、水。
7.2仪器与用具:显微镜、电子天平、三用紫外分析仪、恒温鼓风干燥箱、超声波清洗器、水浴锅、硅胶G薄层板、硅胶GF254薄层板。
7.3性状:取本品适量,自然光下目测色泽,嗅闻气味。
7.4鉴别:7.4.1取本品横切面制片显微镜(10×10)观察组织结构特征。
7.4.2取本品粉末0.5g,加稀乙醇20ml,超声处理20分钟,滤过,滤液蒸干,残渣加稀乙醇1ml使溶解,作为供试品溶液。
另取板蓝根对照药材0.5g 同法制成对照药材溶液。
再取精氨酸对照品,加稀乙醇制成每1ml含0.5mg 的溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述三种溶液各1~2μl,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(19:5:5)为展开剂,展开,取出,热风吹干,喷以茚三酮试液,在105℃加热至斑点显色清晰。
供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的斑点。
7.4.3取本品粉末1g,加80%甲醇20ml,超声处理30分钟,滤过,滤液蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。
另取板蓝根对照药材1g同法制成对照药材溶液。
再取(R-S)-告依春对照品,加甲醇制成每1ml含0.5mg的溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述三种溶液各5~10μl,分别点于同一硅胶GF254薄层板上,以石油醚(60~90℃)-乙酸乙酯(1:1)为展开剂,展开,取出,晾干,置紫外光灯(254nm)下检视。
南板蓝根质量标准及检验操作规程
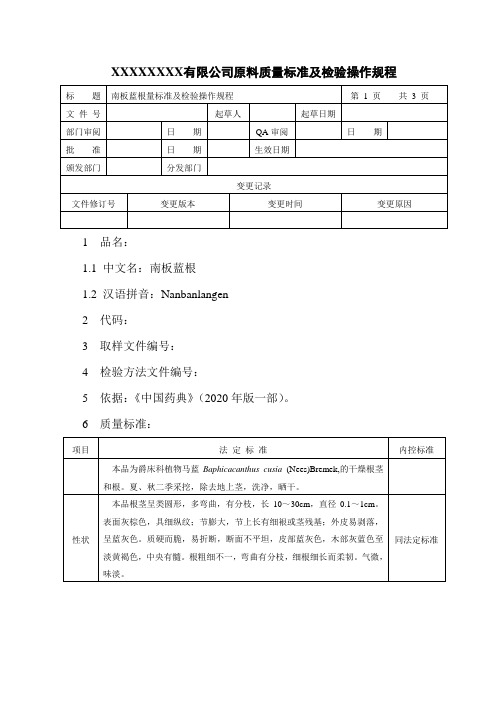
XXXXXXXX有限公司原料质量标准及检验操作规程
1 品名:
1.1 中文名:南板蓝根
1.2 汉语拼音:Nanbanlangen
2 代码:
3 取样文件编号:
4 检验方法文件编号:
5 依据:《中国药典》(2020年版一部)。
6 质量标准:
7 检验操作规程:
7.1 试药与试剂:三氯甲烷、靛蓝对照品、靛玉红对照品、石油醚、乙酸乙酯、乙醇。
7.2 仪器与用具:显微镜、硅胶G板、烘箱、马弗炉。
7.3 性状:取本品适量,自然光下目测色泽,嗅闻气味。
7.4 鉴别:
7.4.1取本品制片置10×10显微镜下做显微观察。
7.4.2取本品粉末2g,加三氯甲烷20ml,加热回流1小时,滤过,滤液浓縮至2ml,作为供试品溶液。
另取靛蓝对照品、靛玉红对照品,加三氯甲烷制成每lml各含0.lmg的混合溶液,作为对照品溶液。
照薄层色谱法(附录7)
试验,吸取上述两种溶液各20µl,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)三氯甲烷-乙酸乙酯(1 :8 :1)为展开剂,展开,取出,晾干,立即检视。
供试品色谱中,在与对照品色谱相应的位置上,显相同的蓝色和紫红色斑点。
7.5 检查:
7.5.1 水分不得过12.0%(附录15第二法)。
7.5.2总灰分不得过10.0%(附录17)。
7.5.3二氧化硫残留量照二氧化硫残留量测定法(附录58)测定,不得过150mg/kg。
7.6 浸出物:照醇溶性浸出物测定法(附录19 ) 项下的热浸法测定,用稀乙醇作溶剂,不得少于13.0%。
板蓝根检验操作规程

范围:板蓝根检验。
责任:质检员、QA监控员、质检科长、质保科长、质量总监。
内容:[性状]板蓝根呈圆柱形,稍扭曲,长10~20cm,直径0.5~1cm,表面淡灰色或淡棕黄色,有纵皱纹及支根痕,皮孔横长,根头略膨大,可见暗绿色或暗棕色较大排列的叶柄残其和密集的的疣状突起。
体实,质略软,断面皮部黄白色,木部黄色。
气微,味微甜后带苦涩。
[鉴别]1仪器设备:载玻片、盖玻片、酒精灯、显微镜、烧杯、紫外分析暗箱、量筒、具塞锥形瓶、超声波处理器,漏斗、电子天平、毛细管、羧甲基纤维素钠为黏合剂的硅胶G薄层板,展开缸、热风机、显色喷瓶、烘箱。
2试剂溶液:水合氯醛、甘油、稀乙醇、精氨酸对照品,正丁醇-冰醋酸-水(19:5:5)茚三酮试液。
3操作方法:3.1取本品制片置显微镜下观察:木栓层为数列细胞。
皮层狭。
韧皮部宽广,射线明显,形成层成环。
木质部导管黄色,类圆形,直径约至8μm;有木纤维束。
薄壁细胞含淀粉粒。
3.2取本品水煎液,置紫外光灯(365nm)观察,显蓝色荧光。
3.3取本品粉末0.5g,加稀乙醇20ml,超声处理20分钟,滤过,滤液蒸干,残渣加稀乙醇1ml使溶解,作为供试品溶液。
另取精氨酸对照品,加稀乙醇制成每1ml含0.5mg的溶液,作为对照品溶液。
照薄层色谱法试验,吸取上述两种溶液各1~2μl,分别点于同一羧甲基纤维素钠为黏合剂的硅胶G薄板上,以正丁醇-冰醋酸-水(19:5:5)为展开剂,展开,取出,热风吹干,喷以茚三酮试液,在105℃加热至斑点,显色清晰。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
[检查]水分:照“水分测定法操作规程”第一法测定,除另有规定外,不得过15.0%。
W2-W0公式:――――――×100%W1-W0W0-称量瓶的重量W2-干燥后的总重量W1-供试品和瓶的总重量[浸出物]1仪器设备:电子天平、锥形瓶、移液管、回流冷凝管、水浴锅、干燥滤器、蒸发皿、干燥器。
ZL-JB-001-2014 南板蓝根冲剂检验操作规程 2

GMP管理文件1、名称:南板蓝根冲剂Nanbanlangen Chongji2、代号或编号:C—0013、引用标准:部颁药品标准中药成方制剂第九册(WS3-B-1774-94)。
4、检验操作规程(本规程所用试剂,除另有规定外,均为分析纯)。
4.1性状:本品为黄褐色颗粒,或长方形块状冲剂;味甘、微苦。
4.1.1操作方法:取本品,置亮处观察其颜色。
4.1.2记录:记录所观察到的现象。
4.1.3结果判定:若本品符合上述“4.1性状”的描述,则可判为符合规定。
4.2.检查4.2.1水分4.2.1.1仪器与设备:电子天平、恒温干燥箱、称量瓶4.2.1.2操作方法:取本品2~5g,照《水分测定法标准操作规程(附录ⅨH)》测定。
4.2.1.3记录与计算:记录并按《水分测定法标准操作规程》(文件编号:ZG-JB-041-2011)计算。
4.2.1.4结果判定:若含水分不超过6.0%,则判为符合规定4.2.2粒度:4.2.2.1仪器与设备: 标准药筛(一号筛、五号筛)、电子天平。
4.2.2.2操作方法:取一号筛置于五号筛之上,并于五号筛下配以密合的接受容器,保持水平壮态过筛,左右往返,约3分钟,取不能通过一号筛和能通过五号筛的颗粒,精密称定重量。
4.2.2.3计算公式:不能通过一号筛和能通过五号筛的颗粒的重量,除以供试品的取用量,计算百分率。
4.2.2.4结果判定:不得过13%。
则可判为符合规定。
4.2.3溶化性4.2.3.1仪器与设备:电炉、烧杯4.2.3.2操作方法:取本品1袋,加热水200ml,搅拌5分钟,立即观察。
4.2.3.3记录:记录观察到的现象。
4.2.3.4结果判定:,应全部溶化,允许有轻微浑浊。
则判为符合规定。
4.2.4装量差异4.2.4.1 仪器与用具:电子天平。
4.2.4.2 操作方法:取本品10袋,照《装量差异检查法标准操作规程》(文件编号:ZL-J B-080-2014)检查。
4.2.4.3记录:记录检查结果。
板蓝根质量标准

1.目的:通过制定板蓝根质量标准,为采购和检验提供依据,以确保板蓝根的质量。
2.范围:适用于板蓝根药材、饮片的质量控制。
3.责任:质量管理部、生产技术部、储运部、采购部。
4.内容:4.1基本信息4.1.1物料名称品名:板蓝根汉语拼音:Banlangen拉丁名:ISATIDIS RADIX4.1.2物料代码:Z074.1.3质量标准依据:《中国药典》2015年版一部(第205页)及四部通则0502、2301、0832、2302、2331、2201、05124.1.4批准供应商:见质量管理部批准的供应商清单4.2取样及检验操作规程编号物料、中间产品(待包装产品)、成品取样标准操作程序 2S-307703板蓝根检验标准操作规程2S-3121064.3定性和定量的限度要求4.3.1法定质量标准【来源】本品为十字花科植物菘蓝Isatis indigotica Fort.的干燥根。
秋季采挖,除去泥沙,晒干。
【性状】本品呈圆柱形,稍扭曲,长10~20cm,直径0.5~1cm。
表面淡灰黄色或淡棕黄色,有纵皱纹、横长皮孔样突起及支根痕。
根头略膨大,可见暗绿色或暗棕色轮状排列的叶柄残基和密集的疣状突起。
体实,质略软,断面皮部黄白色,木部黄色。
气微,味微甜后苦涩。
【鉴别】(1)本品横切面:木栓层为数列细胞。
栓内层狭。
韧皮部宽广,射线明显。
形成层成环。
木质部导管黄色,类圆形,直径约至80μm;有木纤维束。
薄壁细胞含淀粉粒。
(2)取本品粉末0.5g,加稀乙醇20ml,超声处理20分钟,滤过,滤液蒸干,残渣加稀乙醇1ml使溶解,作为供试品溶液。
另取板蓝根对照药材0.5g,同法制成对照药材溶液。
再取精氨酸对照品,加稀乙醇制成每1ml 含0.5mg的溶液,作为对照品溶液。
照薄层色谱法(见文件“薄层色谱法标准操作规程”)试验,吸取上述三种溶液各1~2μl,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(19∶5∶5)为展开剂,展开,取出,热风吹干,喷以茚三酮试液,在105℃加热至斑点显色清晰。
板蓝根种子质量标准

宁夏隆德县六盘山中药资源开发有限公司
管理类别—通用管理文件文件编码第1页/共2页
板蓝根种子质量标准
颁发部门资料档案室生效日期年月日分发部门质量管理部
制定人审核人批准人
制定日期年月日审核日期年月日批准日期年月日版本号第01版变更原因新文件
板蓝根种子质量标准
1.目的
控制板蓝根种子生产及采购时质量状况的规范,确保板蓝根产品质量。
2.适用范围
本文件适用于板蓝根种子质量管理的规范.
3.责任
质检部、采购及生产部门应严格按照标准本文件规定标准执行。
4.内容
4.1种子的外观性状:板蓝根种子长椭圆形,长3.2~3.8mm,宽1.0~1.2mm,表面黄褐色,基部具有一小尖突状种柄,两侧各具一较明显的纵沟:肧弯曲,黄色,肧根圆柱状,子叶2枚,背倚于肧根。
4.2种子要选择饱满,颜色呈紫蓝色,发光发亮的。
4.3种子出芽率要大于等于80%以上。
4.4 种子纯度要大于等于95%以上。
4.5 种子水分要小于等于9%
5.记录
文件编码记录表
6.变更历史
新文件,无变更记录
X。
板蓝根颗粒中间体质量标准及检验操作规程
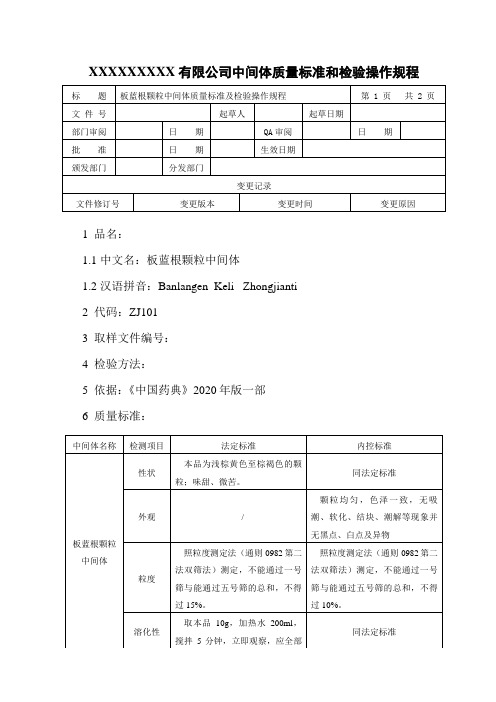
XXXXXXXXX有限公司中间体质量标准和检验操作规程1 品名:1.1 中文名:板蓝根颗粒中间体1.2 汉语拼音:Banlangen Keli Zhongjianti2 代码:ZJ1013 取样文件编号:4 检验方法:5 依据:《中国药典》2020年版一部6 质量标准:7 检验操作规程7.1仪器与用具:一号筛、五号筛、电子天平、烘箱、称量瓶。
7.2检查:7.2.1板蓝根颗粒中间体:7.2.1.1性状:取本品,在自然光下目测颜色及形态、尝味,并记录结果。
7.2.1.2 外观:颗粒均匀,色泽一致,无吸潮、软化、结块、潮解等现象并无黑点、白点及异物。
7.2.1.2粒度:照粒度测定法(附录52)第二法,双筛分法测定,不能通过一号筛与能通过五号筛的总和,不得过10%。
7.2.1.3溶化性:取本品10g,加热水200ml,搅拌5分钟,立即观察,应全部溶化或轻微浑浊。
(附录54)7.2.1.4水分:照水分测定法(附录15)测定,不得过5.0%。
7.3 含量测定:7.3.1 对照品溶液的制备取尿苷对照品、鸟苷对照品及腺苷对照品适量,精密称定,加5%甲醇制成每1ml含尿苷20μg,鸟苷20μg及腺苷25μg的混合溶液,即得。
7.3.2 供试品溶液的制备取装量差异项下的本品,研细,取适量(约相当于饮片1.4g),精密称定,置具塞锥形瓶中,精密加入5%甲醇10ml,密塞,称定重量,超声处理(功率500W,频率40kHz)5分钟,放冷,再称定重量,用5%甲醇溶液补足减失的重量,摇匀,滤过,取续滤液,即得。
7.3.3 测定法分别精密吸取对照品溶液与供试品溶液各5~10μl,注入液相色谱仪,测定,即得。
本品每袋含板蓝根以尿苷(C9H12N2O6)、鸟苷(C10H13N5O5)、腺苷(C10H13N5O4)总量计不得少于0.80mg。
南板蓝根质量标准及检验操作规程

甘肃亚兰药业有限公司成品质量标准及检验操作规程
1 品名:
1.1 中文名:南板蓝根
1.2 汉语拼音:Nanbanlangen
2 代码:
3 取样文件编号:
4 检验方法文件编号:
5 依据:《中国药典》(2020年版一部)。
6 质量标准:
7 检验操作规程:
7.1 试药与试剂:三氯甲烷、靛蓝对照品、靛玉红对照品、石油醚、乙酸乙酯、乙醇、氢氧化钠滴定液、甲基红乙醇溶液指示剂。
7.2 仪器与用具:显微镜、硅胶G板、烘箱、马弗炉、中药二氧化硫测定仪。
7.3 性状:取本品适量,自然光下目测色泽,嗅闻气味。
7.4 鉴别:
7.4.1取本品制片置10×10显微镜下,做显微观察。
7.4.2取本品粉末2g,加三氯甲烷20ml,加热回流1小时,滤过,滤液浓縮至2ml,作为供试品溶液。
另取靛蓝对照品、靛玉红对照品,加三氯甲烷制成每lml各含0.lmg的混合溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述两种溶液各20µl,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)三氯甲烷-乙酸乙酯(1:8:1)为展开剂,展开,取出,晾干,立即检视。
供试品色谱中,在与对照品色谱相应的位置上,显相同的蓝色和
紫红色斑点。
7.5 检查:
7.5.1水分:不得过12.0%(附录15第二法)。
7.5.2总灰分:不得过10.0%(附录17)。
7.5.3二氧化硫残留量:照二氧化硫残留量测定法(附录58)测定,不得过150mg/kg。
7.6 浸出物:照醇溶性浸出物测定法(附录19)项下的热浸法测定,用稀乙醇作溶剂,不得少于13.0%。
板蓝根质量标准及检验操作规程

XXXXXXX有限公司原料质量标准及检验操作规程1品名:1.1中文名:板蓝根1.2 汉语拼音:Baniangen2代码:3取样文件编号:4检验方法文件编号:5依据:《中国药典》(2020年版一部)6质量标准:7检验操作规程:7.1试药与试剂:稀乙醇、板蓝根对照药材、(R-S)-告依春对照品、甲醇、石油醚(60〜90C)、乙酸乙酯、盐酸、精氨酸对照品、羧甲基纤维素钠、正丁醇、冰醋酸、茚三酮试液、水。
7.2仪器与用具:显微镜、电子天平、三用紫外分析仪、恒温鼓风干燥箱、超声波清洗器、水浴锅、硅胶G薄层板、硅胶GF254薄层板。
7.3性状:取本品适量,自然光下目测色泽,嗅闻气味。
7.4鉴别:7.4.1取本品横切面制片显微镜(10X10)观察组织结构特征。
7.4.2取本品粉末0.5g,加稀乙醇20ml,超声处理20分钟,滤过,滤液蒸干,残渣加稀乙醇1ml使溶解,作为供试品溶液。
另取板蓝根对照药材0.5g 同法制成对照药材溶液。
再取精氨酸对照品,加稀乙醇制成每1ml含0.5mg 的溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述三种溶液各1〜2门分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(19:5:5)为展开剂,展开,取出,热风吹干,喷以茚三酮试液,在105 C加热至斑点显色清晰。
供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的斑点。
7.4.3取本品粉末1g,加80%甲醇20ml,超声处理30分钟,滤过,滤液蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。
另取板蓝根对照药材1g同法制成对照药材溶液。
再取(R-S)-告依春对照品,加甲醇制成每1ml含0.5mg 的溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述三种溶液各5~10卩」分别点于同一硅胶GF254薄层板上,以石油醚(60~90C)-乙酸乙酯(1:1 )为展开剂,展开,取出,晾干,置紫外光灯(254nm)下检视。
GC-YL-10710板蓝根检验操作规程

f-------------------------稀释体积。
W样
式中:
W0 ----------- 坩埚重量(g)。
W1----------- 坩埚与灰分的重量(g)。
W样----------- 样品的重量(g)。
二氧化硫残留量:照二氧化硫残留量测定法(通则2331)测定,不得过150mg/kg
仪器与试剂:电热套、竖式回流冷凝管、磁力搅拌器、分析天平、甲基红乙醇溶液指示剂、氢氧化钠滴定液滴、盐酸溶液(6mol/L)等
计算公式:
二氧化硫残留量(mg/kg)=(V供-V空)×C×0.032×106
W供
式中V供为供试品溶液消耗氢氧化钠滴定液的体积,ml;
V空为空白消耗氢氧化钠滴定液的体积,ml;
c 为氢氧化钠滴定液摩尔浓度,mol/L;
W供为供试品的重量,g。
0.032为lm l氢氧化钠滴定液(lmol/L)相当的二氧化硫的质量,g;
仪器:粉碎机、药筛、分析天平、坩埚、箱式电阻炉等。
方法:取供试品2~3g,过二号筛混合均匀后,置炽灼至恒重的坩埚中称定重量,缓缓炽热,注意避免燃烧,至完全炭化时,逐渐升高温度至500~600℃,使完全灰化至恒重。根据残渣重量,计算供试品中总灰分的含量(%)。
计算公式:
W1-W0
总灰分% =×100%
计算公式:
酸不溶性灰分% =
W样
式中:
W0----------- 坩埚重量(g)。
W1-----------酸不溶性灰分与坩埚的重量(g)。
W样----------- 样品的重量(g)。
【浸出物】照水溶性浸出物测定法(通则2201)项下的冷浸法测定,不得少于25.0%。
板蓝根

【来源】本品为十字花科植物菘蓝Isatis in,digotica Fort.的干燥根。
秋季采挖,除去泥沙,晒干。
【性状】本品呈圆形的厚片。
外表皮淡灰黄色至淡棕黄色,有纵皱纹。
切面皮部黄白色,木部黄色。
气微,味微甜后苦涩。
【鉴别】(1)取本品粉末0.5g,加稀乙醇20ml,超声处理20分钟,滤过,滤液蒸于,残渣加稀乙醇1ml使溶解,作为供试品溶液。
另取板蓝根对照药材0.5g,同法制成对照药材溶液。
再取精氨酸对照品,加稀乙醇制成每1ml含0.5mg的溶液,作为对照品溶液。
照薄层色谱法(附录ⅥB)试验,吸取上述三种溶液各1~2μl,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(19:5:5)为展开剂,展开,取出,热风吹于,喷以茚三酮试液,在105℃加热至斑点显色清晰。
供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的斑点。
(2)取本品粉末lg,加80%甲醇20ml,超声处理30分钟,滤过,滤液蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。
另取板蓝根对照药材lg,同法制成对照药材溶液。
再取(R,S)-告依春对照品,加甲醇制成每1ml含0.5mg的溶液,作为对照品的溶液。
照薄层色谱法(附录ⅥB)试验,吸取上述三种溶液各5~lOμl,分别点于同一硅胶GF254薄层板上,以石油醚(60~90℃)-乙酸乙酯(1:1)为展开剂,展开,取出,晾干,置紫外光灯(254nm)下检视。
供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的斑点。
【检查】水分同药材,不得过13.0%。
总灰分同药材,不得过8.0%。
酸不溶性灰分不得过2.0%(附录ⅨK)。
【炮制】除去杂质,洗净,润透,切厚片,干燥。
【性味与归经】苦,寒。
归心、胃经。
【功能与主治】清热解毒,凉血消斑。
用于温疫时毒,发热咽痛,温毒发斑,丹毒。
【用法与用量】 9~15g。
【贮藏】置干燥处,防霉,防蛀。
板蓝根茶中间产品控质量标准

依据:《板蓝根茶质量标准》,产品质量的稳定性考察。
内容:
1稠膏
1.1性状:本品为棕褐色稠膏。
1.2检查
1.2.1 相对密度:应为1.25~1.30 (60℃±5℃测定,用比重计)。
1.2.2 溶化性:搅拌5分钟,应全部溶化,且不得有焦屑等异物。
2 块状物
2.1性状:本品为棕色至棕褐色的块状物;味甜、微苦。
2.2检查
2.2.1水分:不得过2.8%(快速水分测定法)。
2.2.2溶化性:搅拌5分钟,应全部溶化,允许有轻微浑浊。
不得有焦屑等异物。
2.2.3重量差异:(10g)±4.5%,(15g)±4.5%。
3 包装:装量准确,每件数量应为:10克×10块×100盒或15克×10块×100盒;
封口严密、牢固;产品批号、生产日期、有效期印字清晰,内外一致;打包端正(打
包带上下偏差不得过1㎝),松紧适度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
XXXXX药业有限公司成品质量标准及检验操作规程
1 品名:
1.1 中文名:板蓝根
1.2 汉语拼音:Banlangen
2 代码:
3 取样文件编号:
4 检验方法文件编号:
5 依据:《中国药典》(2015年版一部)。
6 质量标准:
7 检验操作规程:
7.1 试药与试剂:稀乙醇、板蓝根对照药材、(R-S)-告依春对照品、甲醇、石油醚(60~90℃)、乙酸乙酯、盐酸、精氨酸对照品、羧甲基纤维素钠、正丁醇、冰醋酸、茚三酮试液、水、氢氧化钠滴定液、甲基红乙醇溶液指示剂。
7.2 仪器与用具:显微镜、电子天平、紫外光灯、超声波清洗器、水浴锅、硅胶G薄层板、硅胶GF254薄层板、烘箱、二氧化硫测定仪。
7.3 性状:取本品适量,自然光下目测色泽,嗅闻气味。
7.4 鉴别:
7.4.1取本品粉末0.5g,加稀乙醇20ml,超声处理20分钟,滤过,滤液蒸干,残渣加稀乙醇1ml使溶解,作为供试品溶液。
另取板蓝根对照药材0.5g 同法制成对照药材溶液。
再取精氨酸对照品,加稀乙醇制成每1ml含0.5mg 的溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述三种溶液各1~2μl,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(19:5:5)为展开剂,展开,取出,热风吹干,喷以茚三酮试液,在105℃加热至斑点显色清晰。
供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的斑点。
7.4.2取本品粉末1g,加80%甲醇20ml,超声处理30分钟,滤过,滤液蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。
另取板蓝根对照药材1g同
法制成对照药材溶液。
再取(R-S)-告依春对照品,加甲醇制成每1ml含0.5mg 的溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述三种溶液各5~10μl,分别点于同一硅胶GF254薄层板上,以石油醚(60~90℃)-乙酸乙酯(1:1)为展开剂,展开,取出,晾干,置紫外光灯(254nm)下检视。
供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的斑点。
7.5 检查:
7.5.1水分:不得过13.0%(附录15第二法)测定。
7.5.2总灰分:不得过8.0%(附录17)。
7.5.3酸不溶性灰分:不得过2.0%(附录17)。
7.5.4二氧化硫残留量照二氧化硫残留量测定法(附录58)测定,不得过150mg/kg。
7.6浸出物:照醇溶性浸出物测定法(附录19)项下的热浸法测定,用45%乙醇作溶剂,不得少于25.0%。
7.7含量测定:照高效液相色谱法(附录8)测定。
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以甲醇-0.02%磷酸溶液(7:93)为流动相;检测波长为245nm。
理论板数按(R,S)-告依春峰计算应不低于5000。
对照品溶液的制备取(R,S)-告依春对照品适量,精密称定,加甲醇制成每1ml含40μg溶液,即得。
供试品溶液的制备取本品粉末(过四号筛)约1g,精密称定,置圆底瓶中,精密加入水50ml,称定重量,煎煮2小时,放冷,再称定重量,用水补足减失的重量,摇匀,滤过,取续滤液,即得。
测定法分别精密吸取对照品溶液与供试品溶液各10~20μl,注入液相色谱仪,测定,即得。
本品按干燥品计算,含(R,S)-告依春(C5H7NOS)的总量不得少于0.030%。
