高中化学选修三《第三章 晶体结构与性质》全套教案分解
人教版-选修3-第三章 晶体结构和性质全章教案

金太阳教育网 第一节 晶体的常识教材分析:本节内容是安排在原子结构、分子结构以及结构决定性质的内容之后来学习,对于学生的学习有一定的理论基础。
本节内容主要是通过介绍各种各样的固体为出发点来过渡到本堂课的主题——晶体和非晶体。
而晶体和非晶体的学习是以各自的自范性和微观结构比较为切入点,进而得出得到晶体的一般途径以及晶体的常见性质和区分晶体的方法。
[学习目标][知识梳理]一、晶体与非晶体1.晶体的自范性即______________________________________________________.晶体呈自范性的条件之一是____________________________________________________.2.得到晶体一般有三条途径:(1)____________,(2)___________________________,(3)_________________________4. 晶体的熔点较__________,而非晶体的熔点_______________,区分晶体与非晶体最可靠的科学方法是______________________________________________.金太阳教育网 二、晶胞5._________________________________ _________________是晶胞。
[方法导引]晶胞中粒子数的计算方法:晶体结构类习题最常见的题型就是已知晶胞的结构而求晶体的化学式。
解答这类习题首先要明确一个概念:由晶胞构成的晶体,其化学式不一定是表示一个分子中含有多少个原子,而是表示每个晶胞中平均含有各类原子的个数,即各类原子的最简个数比。
解答这类习题,通常采用分摊法。
在一个晶胞结构中出现的多个原子,这些原子并不是只为这个晶胞所独立占有,而是为多个晶胞所共有,那么,在一个晶胞结构中出现的每个原子,这个晶体能分摊到多少比例呢。
这就是分摊法。
高中化学 第三章 晶体结构与性质 章末整合教案 新人教版选修3-新人教版高二选修3化学教案

晶体结构与性质章末整合热点专题突破REDIANZHUANTITUPO专题一四种晶体的基本类型与性质专题二物质熔点高低的规律比较判断晶体熔点的高低时,首先分析物质所属的晶体类型,其次抓住决定同一类晶体熔点高低的因素。
1.不同类晶体:一般情况下,原子晶体>离子晶体>分子晶体;金属晶体(除少数外)>分子晶体。
金属晶体的熔点有的很高,如钨、铂等,有的则很低,如汞、铯、镓等。
2.同种类型晶体:构成晶体粒子间的作用力大,则熔点高,反之则低。
(1)离子晶体:离子所带的电荷数越高,离子半径越小,则其熔点就越高。
例如:NaCl>CsCl;MgO>MgCl2。
(2)分子晶体:①组成和结构相似的分子晶体,一般相对分子质量越大,分子间作用力越强,则熔点越高。
如I2>Br2>Cl2>F2。
②其他方面相同时,分子的极性越大,熔点越高。
③同分异构体之间一般支链越多,熔点越低。
④若分子间有氢键,晶体熔点较高。
(3)原子晶体:一般半径越小,键长越短,键能越大,则熔点越高。
例如:金刚石>碳化硅>晶体硅。
(4)金属晶体:金属阳离子所带电荷数越多,离子半径越小,则金属键越强,熔点越高。
例如:Al>Mg>Na 。
第三章 晶体结构与性质专题三 晶体结构中的有关计算(1)根据晶体晶胞的结构特点确定晶体的化学式及晶胞中粒子数目的计算(均摊法)注意:①当晶胞为正六棱柱时,其顶点上的粒子被6个晶胞共用,每个粒子属于该晶胞的部分为16,而不是18。
②审题时一定要注意是“分子结构”还是“晶体结构”,若是分子结构,其化学式由图中所有实际存在的原子个数决定,且原子个数可以不互质(即原子个数比可以不约简)。
(2)根据晶体晶胞的结构特点和有关数据,求算晶体的密度或晶体晶胞的体积或晶胞参数a (晶胞边长)对于立方晶胞,可建立如下求算途径:得关系式:ρ=n ×M a 3×N A(a 表示晶胞边长,ρ表示密度,N A 表示阿伏加德罗常数的数值,n 表示1个晶胞所含基本粒子数,M 表示摩尔质量)。
高中化学选修三晶体结构与性质全套教案定稿版

高中化学选修三晶体结构与性质全套教案 HUA system office room 【HUA16H-TTMS2A-HUAS8Q8-第三章晶体结构与性质第一节晶体常识第一课时教学目标设定:1、通过实验探究理解晶体与非晶体的差异。
2、学会分析、理解、归纳和总结的逻辑思维方法,提高发现问题、分析问题和解决问题的能力。
3、了解区别晶体与非晶体的方法,认识化学的实用价值,增强学习化学的兴趣。
教学重难点:1、晶体与非晶体的区别2、晶体的特征教学方法建议:探究法教学过程设计:[新课引入]:前面我们讨论过原子结构、分子结构,对于化学键的形成也有了初步的了解,同时也知道组成千万种物质的质点可以是离子、原子或分子。
又根据物质在不同温度和压强下,物质主要分为三态:气态、液态和固态,下面我们观察一些固态物质的图片。
[投影]:1、蜡状白磷; 2、黄色的硫磺; 3、紫黑色的碘; 4、高锰酸钾[讲述]:像上面这一类固体,有着自己有序的排列,我们把它们称为晶体;而像玻璃这一类固体,本身原子排列杂乱无章,称它为非晶体,今天我们的课题就是一起来探究晶体与非晶体的有关知识。
[板书]:一、晶体与非晶体[板书]:1、晶体与非晶体的本质差异[提问]:在初中化学中,大家已学过晶体与非晶体,你知道它们之间有没有差异?[回答]:学生:晶体有固定熔点,而非晶体无固定熔点。
[讲解]:晶体有固定熔点,而非晶体无固定熔点,这只是晶体与非晶体的表观现象,那么他们在本质上有哪些差异呢?[投影]晶体与非晶体的本质差异[板书]:自范性:晶体能自发性地呈现多面体外形的性质。
[解释]:所谓自范性即“自发”进行,但这里得注意,“自发”过程的实现仍需一定的条件。
例如:水能自发地从高处流向低处,但不打开拦截水流的闸门,水库里的水不能下泻。
[板书]:注意:自范性需要一定的条件,其中最重要的条件是晶体的生长速率适当。
[投影]:通过影片播放出,同样是熔融态的二氧化硅,快速的冷却得到玛瑙,而缓慢冷却得到水晶过程。
2019-2020年高中化学 第三章 晶体结构与性质复习教案 人教版选修3

2019-2020年高中化学第三章晶体结构与性质复习教案人教版选修3教学目标1.巩固有关晶体粒子、粒子间作用力、晶体结构和晶体性质的基本知识。
2.掌握有关晶体的简单计算。
教学重点1.四种晶体类型的基本知识及应用;2.有关晶体的简单计算。
教学难点提高归纳和应用知识的能力,训练学生思维的敏捷性和严密性。
教学过程【引入】在这一章里我们学习了五种不同类型的晶体,这节课我们对这些晶体的性质来进行比较和总结。
【板书】单元复习一、晶体结构及粒子间相互作用【师】由离子化合物形成的晶体一定是离子晶体;由共价化合物构成的晶体一般是分子晶体,少数为原子晶体;由金属单质构成的晶体一般是金属晶体(Hg除外);由非金属单质构成的晶体一般是分子晶体,少数为原子晶体。
【板书】二、晶体熔沸点的比较1.相同条件下不同状态固态 > 液态 > 气态2.不同晶型多数情况:原子晶体 > 离子晶体 > 分子晶体3.相同晶型⑴分子晶体:相对分子质量、氢键、分子的极性⑵原子晶体:共价键强弱——原子半径大小⑶金属晶体:金属键强弱——金属离子半径和离子所带电荷数⑷离子晶体:离子键强弱——离子半径和离子所带电荷数【例1】下列物质的熔沸点记低顺序正确的是( B )A.金刚石 > 晶体硅 > 二氧化硅 > 碳化硅 B.CI4 > CBr4 > CCl4 > CF4 C.MgO > H2 > O2 > N2 D.金刚石 > 生铁 > 纯铁 > 钠【例2】下列各组物质的沸点,按由低到高的顺序排列的是( C )A.NH3、CH4、NaCl、Na B.H2O、H2S、MgSO4、SO2C.CH4、H2O、NaCl、SiO2D.Li、Na、K、Rb、Cs【板书】三、典型晶体结构1.干冰、金刚石、二氧化硅、NaCl、CsCl、石墨2.有关晶胞的计算【板书】四、判断晶体类型的方法【师】主要根据各类晶体物理性质的差异:熔沸点、导电性、机械性能、硬度等。
(新人教版)高中化学选修3 《物质构造与性质》全册教案

(新人教版)高中化学选修3 《物质构造与性质》全册教案第一章物质的结构特征及其性质1.1 结晶态与非晶态1.1.1 结晶态的特征及其产生条件课时安排- 课时一:结晶态的形成及特征- 课时二:结晶体的分类及特征中心思想结晶态是物质在一定条件下排列成具有规则空间排列的微观结构. 结晶态和非晶态都是物质存在的两种形态.1.1.2 非晶态物质的特征及其产生条件课时安排- 课时一:非晶态物质的形成及特征- 课时二:非晶态物质的分类及特征中心思想非晶态是物质在一定条件下呈现出无规则排列的微观结构. 非晶态物质具有良好的光学和力学性质.1.2 共价键理论1.2.1 原子轨道与分子轨道的混合课时安排- 课时一:原子轨道与分子轨道的概念及特点- 课时二:分子轨道的构成与性质中心思想通过混合原子轨道,可以产生更多的分子轨道. 分子轨道中的电子云分布可以反映化学反应过程中电子的变化.1.2.2 共价键的构成及其分类课时安排- 课时一:共价键的概念及其特点- 课时二:共价键的分类及其特点中心思想共价键包含单键、双键、三键和π键. 共价键的构成方式影响着物质的性质.第二章功能性材料的结构与性能2.1 材料的基本结构与性质2.1.1 材料的结构特征课时安排- 课时一:晶体材料的结构特征- 课时二:非晶态材料的结构特征中心思想材料的结构特征对其性质具有极大的影响. 晶体材料和非晶态材料在微观结构上存在很大的区别.2.1.2 材料的力学性质课时安排- 课时一:静态力学性质的基本概念- 课时二:动态力学性质的基本概念中心思想材料的力学性质是用于描述材料承受外力时的变形程度和破坏形式的. 材料的力学性质可以反映出材料的稳定性.2.2 功能性材料的设计与合成2.2.1 功能性材料的发展概况课时安排- 课时一:功能性材料的定义和分类- 课时二:功能性材料的应用现状中心思想功能性材料是指通过材料的化学合成,物理改性和微结构设计等手段得到的具有特定功能的新型材料.2.2.2 功能性材料的设计及合成方法课时安排- 课时一:功能性材料的设计原则- 课时二:功能性材料的合成方法中心思想功能性材料的设计需要考虑材料的特定功能,包括电学、磁学、光学和感知等方面的要求. 合适的合成方法可以有效提高功能性材料的合成效率和产品质量.。
高中化学选修3 第三章晶体结构与性质 讲义及习题.含答案解析

高中化学选修三第三章晶体结构与性质一、晶体常识1、晶体与非晶体比较自范性:晶体的适宜的条件下能自发的呈现封闭的,规则的多面体外形。
对称性:晶面、顶点、晶棱等有规律的重复各向异性:沿晶格的不同方向,原子排列的周期性和疏密程度不尽相同,因此导致的在不同方向的物理化学特性也不尽相同。
2、获得晶体的三条途径①熔融态物质凝固。
②气态物质冷却不经液态直接凝固(凝华)。
③溶质从溶液中析出。
3、晶胞晶胞是描述晶体结构的基本单元。
晶胞在晶体中的排列呈“无隙并置”。
4、晶胞中微粒数的计算方法——均摊法某粒子为n个晶胞所共有,则该粒子有1/n属于这个晶胞。
中学常见的晶胞为立方晶胞。
立方晶胞中微粒数的计算方法如下:①晶胞顶角粒子为8个晶胞共用,每个晶胞占1/8②晶胞棱上粒子为4个晶胞共用,每个晶胞占1/4③晶胞面上粒子为2个晶胞共用,每个晶胞占1/2④晶胞内部粒子为1个晶胞独自占有,即为1注意:在使用“均摊法”计算晶胞中粒子个数时要注意晶胞的形状。
二、构成物质的四种晶体1、四种晶体的比较(1)不同类型晶体的熔、沸点高低一般规律:原子晶体>离子晶体>分子晶体。
金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低。
(2)原子晶体由共价键形成的原子晶体中,原子半径小的键长短,键能大,晶体的熔、沸点高。
如熔点:金刚石>碳化硅>硅(3)离子晶体一般地说,阴阳离子的电荷数越多,离子半径越小,则离子间的作用力就越强,相应的晶格能大,其晶体的熔、沸点就越高。
晶格能:1mol气态阳离子和1mol气态阴离子结合生成1mol离子晶体释放出的能量。
(4)分子晶体①分子间作用力越大,物质熔、沸点越高;具有氢键的分子晶体熔、沸点反常的高。
②组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高。
③组成和结构不相似的物质(相对分子质量接近),分子的极性越大,熔、沸点越高。
④同分异构体,支链越多,熔、沸点越低。
(5)金属晶体金属离子半径越小,离子电荷数越多,其金属键越强,金属熔、沸点就越高。
高中化学选修三《第三章--晶体结构与性质》全套教案分解

第三章晶体结构与性质第一节晶体常识第一课时教学目标设定:1、通过实验探究理解晶体与非晶体的差异。
2、学会分析、理解、归纳和总结的逻辑思维方法,提高发现问题、分析问题和解决问题的能力。
3、了解区别晶体与非晶体的方法,认识化学的实用价值,增强学习化学的兴趣。
教学重难点:1、晶体与非晶体的区别2、晶体的特征教学方法建议:探究法教学过程设计:[新课引入]:前面我们讨论过原子结构、分子结构,对于化学键的形成也有了初步的了解,同时也知道组成千万种物质的质点可以是离子、原子或分子。
又根据物质在不同温度和压强下,物质主要分为三态:气态、液态和固态,下面我们观察一些固态物质的图片。
[投影]:1、蜡状白磷;2、黄色的硫磺;3、紫黑色的碘;4、高锰酸钾[讲述]:像上面这一类固体,有着自己有序的排列,我们把它们称为晶体;而像玻璃这一类固体,本身原子排列杂乱无章,称它为非晶体,今天我们的课题就是一起来探究晶体与非晶体的有关知识。
[板书]:一、晶体与非晶体[板书]:1、晶体与非晶体的本质差异[提问]:在初中化学中,大家已学过晶体与非晶体,你知道它们之间有没有差异?[回答]:学生:晶体有固定熔点,而非晶体无固定熔点。
[讲解]:晶体有固定熔点,而非晶体无固定熔点,这只是晶体与非晶体的表观现象,那么他们在本质上有哪些差异呢?[投影]晶体与非晶体的本质差异[板书]:自范性:晶体能自发性地呈现多面体外形的性质。
[解释]:所谓自范性即“自发”进行,但这里得注意,“自发”过程的实现仍需一定的条件。
例如:水能自发地从高处流向低处,但不打开拦截水流的闸门,水库里的水不能下泻。
[板书]:注意:自范性需要一定的条件,其中最重要的条件是晶体的生长速率适当。
[投影]:通过影片播放出,同样是熔融态的二氧化硅,快速的冷却得到玛瑙,而缓慢冷却得到水晶过程。
[设问]:那么得到晶体的途径,除了用上述的冷却的方法,还有没有其它途径呢?你能列举哪些?[板书]:2、晶体形成的一段途径:(1)熔融态物质凝固;(2)气态物质冷却不经液态直接凝固(凝华);(3)溶质从溶液中析出。
高中化学第三章 晶体结构与性质优秀教案

第三节金属晶体【教学目标】:1、知识技能目标:⑴了解金属晶体内原子在二维空间的两种排列方式,⑵掌握金属晶体四种堆积模型的结构特点2 、过程方法目标:⑴通过对金属晶体结构的学习与研究,培养学生观察能力,空间想像能力等⑵通过制作模型训练学生的动手能力和空间想象能力。
3、情感态度价值观:以小组讨论交流、实践活动制作模型的方式培养学生的合作意识和严谨的科学态度【重点和难点】:1、教学重点:金属晶体的4种根本堆积模型2、教学难点:金属晶体的4种根本堆积模型【教学方法】:1、科学探究:质疑----实验----分析----解决---归纳---比拟2、多媒体课件与自制教具相结合的互动探究式课堂教学模式3、师生探究模式和生生探究模式【思考】:1、原子晶体和金属晶体的性质差异有哪些?2、为何原子晶体和金属晶体的微粒间作用都是化学键,但物理性质会有很大的差异?第二课时金属晶体的堆积方式一、有关原子堆积模型的重要概念:1、_____________________:假设金属原子为等径实心刚性〔直径恒定〕圆球。
假设相邻金属圆球之间是相切的关系。
2、_____________:微粒间的作用力使微粒尽可能的相互接近,使它们占有最小的空间。
3、_____________:空间被晶格质点占据的百分数,用来表示紧密堆积的程度。
公式:4、_____________:在紧密堆积中,一个原子或离子周围距离最近且相等的原子或离子数目。
二、金属原子在平面上〔即二维空间〕的堆积模型学生活动〔摆一摆、画一画〕:1、金属原子在平面里的紧密排列有哪些方式?2、这些不同的排列方式有什么特点?三、金属原子在三维空间的堆积模型1、由非密置层在三维空间的堆积方式学生活动〔摆一摆、画一画〕:⑴将非密置层一层一层的在三维空间堆积起来,使相邻层的球紧密接触,有几种方式?⑵这些不同的排列方式有什么特点?⑶画出这些堆积方式的模型。
【练习】:1、1、金属晶体堆积密度大,原子配位数高,能充分利用空间的原因是〔〕A、金属原子的价电子数极少B、金属晶体中存在自由移动的电子C、金属原子的原子半径较大D、金属键不具有方向性和饱和性2、金属原子在二维空间里的放置有如以下图所示的两种方式,以下说法中正确的是〔〕A、〔a〕为非密置层,配位数为6B、〔b〕为密置层,配位数为4C、〔a〕在三维空间里堆积可得体心立方堆积D、〔b〕在三维空间里堆积可得简单立方堆积3、如图甲、乙所示为二维平面晶体示意图。
人教版高中化学选修三教案 第三章 晶体的结构与性质

Y 位于立方体的中心,晶体中距离最近的两个 X 与一个 Y
形成的夹角∠XYX 的角度为:( )
A. 90° B. 60° C. 120° D. 109°28′
3、右面图形是石墨晶体的层面结构图,
试分析图形推测层面上每个正六边型拥有的
共价键数和碳原子数是分别:( )
A、6,6 B、2,4 C、2,3 D、3,2
4、图是超导化合物一钙钛矿晶体中最小重复单元(晶胞)的结构.请回答:
(1)该化合物的化学式为_______. (2)在该化 合物 晶体 中,与某 个钛 离子距 离最近且 相等 的其他 钛离子共有 __________个. (3)设该化合物的摩尔质量为 M,密度为 ag / cm3 ,阿伏加德罗常数为 N A ,则晶 体中钙离子与钛离子之间的最短距离为_______.
(4) 投影 氢键的表示 如:冰一个水分子能和周围 4 个水分子从氢键相结
合组成一个正四面体 见图 3-11 教师诱导:在分子晶体中,分子内的原子以共价键相结合,而相邻分子通过
分子间作用力相互吸引。分子晶体有哪些特性呢?学生回答
4.分子晶体的物理特性:熔沸点较低、易升华、硬度小。固态和熔融状态
下都不导电。教师诱导:大多数分子晶体结构有如下特征:如果分子间作用力只
一、分子晶体 1.定义:含分子的晶体称为分子晶体 也就是说:分子间以分子间作用力相结合的晶体叫做分子晶体 看图 3-9,如:碘晶体中只含有 I2 分子,就属于分子晶体 问:还有哪些属于分 子晶体? 2.较典型的分子晶体有非金属氢化物,部分非金属单质,部分非金属氧化物, 几乎所有的酸,绝大多数有机物的晶体。
投影小结完成表格
晶体类型
分子晶体
结构
构成晶体的粒子 粒子间的相互作用力
选修3第三章《晶体结构与性质》全章教学设计

选修3第三章《晶体结构与性质》章教学设计东莞市第一中学刘国强一、本章教材体现的课标内容1、主题:第一节晶体的常识了解晶胞的概念,会计算晶胞中原子占有个数,并由此推导出晶体的化学式。
2、主题:第二节分子晶体与原子晶体知道分子晶体与原子晶体的结构微粒、微粒间作用力的区别。
了解原子晶体的特征,能描述金刚石、二氧化硅等原子晶体的结构与性质的关系。
3、主题:第三节金属晶体知道金属键的涵义,能用金属键理论解释金属的一些物理性质。
能列举金属晶体的基本堆积模型。
知道金属晶体的结构微粒、微粒间作用力与分子晶体、原子晶体的区别。
4、主题:第四节离子晶体能说明离子键的形成,能根据离子化合物的结构特征解释其物理性质。
知道离子晶体的结构微粒、微粒间作用力与分子晶体。
原子晶体、金属晶体的区别。
了解晶格能的应用,知道晶格能的大小可以衡量离子晶体中离子键的强弱。
二、本章教材整体分析(一)教材地位本单元知识是在原子结构和元素周期律以及化学键等知识的基础上介绍的,是原子结构和化学键知识的延伸和提高;本单元知识围绕晶体作了详尽的介绍,晶体与玻璃体的不同,分子晶体、原子晶体、金属晶体、离子晶体,从构成晶体的微粒、晶胞、微粒间的作用力,熔沸点比较等物理性质做了比较,结合许多彩图及详尽的事例,对四大晶体做了阐述;同时,本单元结合数学立体几何知识,充分认识和挖掘典型晶胞的结构,去形象、直观地认识四种晶体,在学习本单元知识时,应多联系生活中的晶体化学,去感受生活中的晶体美,去感受环境生命科学、材料中的晶体知识。
“本章比较全面而系统地介绍了晶体结构和性质,作为本书的结尾章,与前两章一起构成“原子结构与性质、分子结构与性质、晶体结构与性质”三位一体的“物质结构与性质”模块的基本内容。
”“通过本章的学习,结合前两章已学过的有关物质结构知识,学生能够比较全面地认识物质的结构及结构对物质性质的影响,提高分析问题和解决问题的能力。
”(二)内容体系本单元知识内容分为两大部分,第一节简单介绍晶体的常识,区别晶体与非晶体,认识什么是晶胞:第二部分分为三节内容,第二节“分子晶体和原子晶体”分别介绍了分子晶体和原子晶体的结构特征及晶体特性,在陈述分子晶体的结构特征时,以干冰为例,介绍了如果分子晶体中分子问作用力只是范德华力时,分子晶体具有分子密堆积特征;同时,教科书以冰为例,介绍了冰晶体里由于存在氢键而使冰晶体的结构具有其特殊性。
高中化学选修三第三章教案
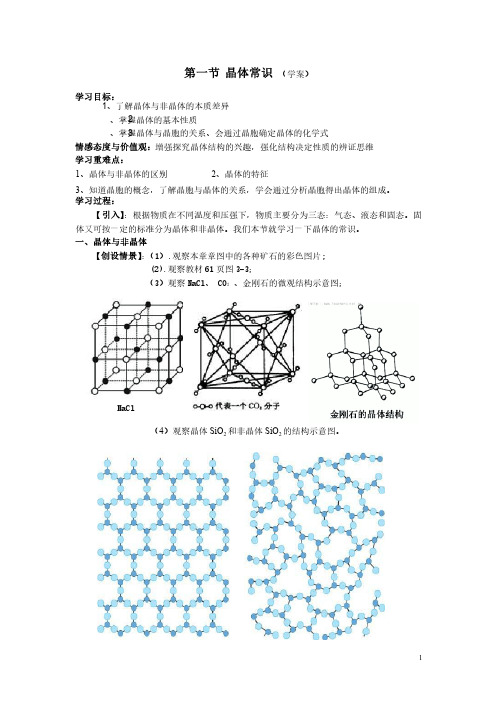
第一节 晶体常识(学案)学习目标:1、了解晶体与非晶体的本质差异、了解晶体与非晶体的本质差异 2、掌握晶体的基本性质、掌握晶体的基本性质 3、掌握晶体与晶胞的关系、会通过晶胞确定晶体的化学式、掌握晶体与晶胞的关系、会通过晶胞确定晶体的化学式情感态度与价值观:增强探究晶体结构的兴趣,强化结构决定性质的辨证思维增强探究晶体结构的兴趣,强化结构决定性质的辨证思维 学习重难点:1、晶体与非晶体的区别、晶体与非晶体的区别2、晶体的特征、晶体的特征3、知道晶胞的概念,了解晶胞与晶体的关系,学会通过分析晶胞得出晶体的组成。
、知道晶胞的概念,了解晶胞与晶体的关系,学会通过分析晶胞得出晶体的组成。
学习过程:【引入】:根据物质在不同温度和压强下,物质主要分为三态:气态、液态和固态。
固体又可按一定的标准分为晶体和非晶体。
我们本节就学习一下晶体的常识。
一、晶体与非晶体【创设情景】:(1).观察本章章图中的各种矿石的彩色图片观察本章章图中的各种矿石的彩色图片; ;(2).(2).观察教材观察教材61页图3-33-3;;(3)观察NaCl NaCl、、 CO 2 、金刚石的微观结构示意图;、金刚石的微观结构示意图;(4)观察晶体SiO 2和非晶体SiO 2的结构示意图。
的结构示意图。
NaCl NaCl【提出问题】:结合教材P 60-P 62,思考下列问题,思考下列问题 (1). (1).晶体有什么特点和性质?晶体有什么特点和性质?晶体有什么特点和性质? ((2)晶体和非晶体的本质区别是什么?)晶体和非晶体的本质区别是什么? ((3)如何区别晶体和非晶体?)如何区别晶体和非晶体? (4)晶体形成的一般途径有哪些?)晶体形成的一般途径有哪些? (5)你能否根据所学的知识,给晶体下一个定义?)你能否根据所学的知识,给晶体下一个定义?【问题解决】:通过学生的观察、思考、分析,结合学生已有的经验和知识,以解决问题为主线,引导学生积极,主动的参与问题的解决。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章晶体结构与性质第一节晶体常识第一课时教学目标设定:1、通过实验探究理解晶体与非晶体的差异。
2、学会分析、理解、归纳和总结的逻辑思维方法,提高发现问题、分析问题和解决问题的能力。
3、了解区别晶体与非晶体的方法,认识化学的实用价值,增强学习化学的兴趣。
教学重难点:1、晶体与非晶体的区别2、晶体的特征教学方法建议:探究法教学过程设计:[新课引入]:前面我们讨论过原子结构、分子结构,对于化学键的形成也有了初步的了解,同时也知道组成千万种物质的质点可以是离子、原子或分子。
又根据物质在不同温度和压强下,物质主要分为三态:气态、液态和固态,下面我们观察一些固态物质的图片。
[投影]:1、蜡状白磷;2、黄色的硫磺;3、紫黑色的碘;4、高锰酸钾[讲述]:像上面这一类固体,有着自己有序的排列,我们把它们称为晶体;而像玻璃这一类固体,本身原子排列杂乱无章,称它为非晶体,今天我们的课题就是一起来探究晶体与非晶体的有关知识。
[板书]:一、晶体与非晶体[板书]:1、晶体与非晶体的本质差异[提问]:在初中化学中,大家已学过晶体与非晶体,你知道它们之间有没有差异?[回答]:学生:晶体有固定熔点,而非晶体无固定熔点。
[讲解]:晶体有固定熔点,而非晶体无固定熔点,这只是晶体与非晶体的表观现象,那么他们在本质上有哪些差异呢?[投影]晶体与非晶体的本质差异[板书]:自范性:晶体能自发性地呈现多面体外形的性质。
[解释]:所谓自范性即“自发”进行,但这里得注意,“自发”过程的实现仍需一定的条件。
例如:水能自发地从高处流向低处,但不打开拦截水流的闸门,水库里的水不能下泻。
[板书]:注意:自范性需要一定的条件,其中最重要的条件是晶体的生长速率适当。
[投影]:通过影片播放出,同样是熔融态的二氧化硅,快速的冷却得到玛瑙,而缓慢冷却得到水晶过程。
[设问]:那么得到晶体的途径,除了用上述的冷却的方法,还有没有其它途径呢?你能列举哪些?[板书]:2、晶体形成的一段途径:(1)熔融态物质凝固;(2)气态物质冷却不经液态直接凝固(凝华);(3)溶质从溶液中析出。
[投影图片]:1、从熔融态结晶出来的硫晶体;2、凝华得到的碘晶体;3、从硫酸铜饱和溶液中析出的硫酸铜晶体。
[探究实验]:完成教材实验3-1,请同学们认真观察,并提问同学观察到什么现象。
[回答]:首先碘升华,然后在表面皿下面出现碘的固体。
[讲解]:事实上,这里提到的固体就是凝华得到的碘晶体。
[过渡]:许多固体的粉末用肉眼是看不见晶体的,但我们可以借助于显微镜观察,这也证明固体粉末仍是晶体,只不过晶粒太小了![投影]:晶体二氧化硅和非晶体二氧化硅的示意图[提问]:小组讨论,通过比较,可以得出什么样结论。
[回答]:晶体的原子排列有序,而非晶体则不是。
[讲述]:从本质上来说,晶体的自范性是晶体中粒子在微观空间里所呈的现周期性。
[讲述]:通过前面对晶体与非晶体的讨论,现在我们来总结一下,晶体有哪些特点:[板书]:3、晶体的特点:(1)有固定的几何外形;(2)有固定的熔点;(3)有各向异性。
[解析]:对于同一幅图案来说,从不同的方向审视,也会产生不同的感受,那么对于晶体来说,许多物理性质:如硬度、导热性、光学性质等,因研究角度不同而产生差异,即为各向异性。
例如:蓝晶石(Al2O3·SiO2)在不同方向上的硬度不同;石墨在与层垂直的方向上的导电率与层平行的方向上的导电率1∕104。
[小结]:可以根据晶体特点区别某一固体属于晶体还是非晶体。
然而,得出区别晶体与非晶体最可靠的方法是利用x-射线衍射实验。
[提问]:通过这节课的学习,现在请你用一句话来定义晶体,应该怎么说?[回答]:学生1、内部原子有规律的排列的物质;学生2、内部原子有规律的排列,且外观为多面体的固体物质。
[板书]:4、晶体的定义:质点(分子、离子、原子)在空间有规则地排列成的,具有整齐外型,以多面体出现的固体物质。
练习:1、下列关于晶体与非晶体的说法正确的是:A、晶体一定比非晶体的熔点高B、晶体有自范性但排列无序C、非晶体无自范性而且排列无序D、固体SiO2一定是晶体2、区别晶体与非晶体最可靠的科学方法是:A、熔沸点B、硬度C、颜色D、x-射线衍射实验3、在我们的生活中遇到许多固体,通过今天这节课的学习,我们知道固体可以分为晶体与非晶体。
请你举出常见的晶体与非晶体的实例。
答案:1、C;2、D;3、晶体:玛瑙、水晶、硫晶体等等;非晶体玻璃、水泥等等。
4、下列不属于晶体的特点是:A、一定有固定的几何外形B、一定有各向异性C、一定有固定的熔点D、一定是无色透明的固体5、下列过程可以得到晶体的有:A、对NaCl饱和溶液降温,所得到的固体B、气态H2O冷却为液态,然后再冷却成的固态C、熔融的KNO3冷却后所得的固体D、将液态的玻璃冷却成所得到的固体6、晶体具有各向异性。
如蓝晶石(Al2O3·SiO2)在不同方向上的硬度不同;又如石墨在与层垂直的方向上的导电率与层平行的方向上的导电率1∕104。
晶体的各向异性主要表现在是:①硬度②导热性③导电性④光学性质A、①③B、②④C、①②③D、①②③④7、一些不法商人制造假宝石来牟取暴利,你能否根据晶体物理性质的各向异性的特点,列举出一些可能有效鉴别假宝石的方法?第二课时一、晶胞定义:晶体结构中的基本单元叫晶胞二、晶胞中原子个数的计算方法:位于晶胞顶点的微粒,实际提供给晶胞的只有1/8;位于晶胞棱边的微粒,实际提供给晶胞的只有1/4;位于晶胞面心的微粒,实际提供给晶胞的只有1/2;位于晶胞中心的微粒,实际提供给晶胞的只有1。
练习:1、现有甲、乙、丙、丁四种晶胞(如图2-8所示),可推知:甲晶体中A与B的离子个数比为;乙晶体的化学式为;丙晶体的化学式为______;丁晶体的化学式为______。
2、钙-钛矿晶胞结构如图2-9所示。
观察钙-钛矿晶胞结构,求该晶体中,钙、钛、氧的微粒个数比为多少?3、晶体硼的基本结构单元都是由硼原子组成的正二十面体,其中含有20个等边三角形的面和一定数目的顶角,每个顶角各有一个硼原子。
如图2-10所示,回答:(1)键角____;(2)晶体硼中的硼原子数____个;B—B 键____条?4、在碳单质的成员中还有一种混合型晶体——石墨,如图2-11所示。
它是层状结构,层与层之间依靠作用力相结合。
每层内部碳原子与碳原子之间靠作用力相结合,其键角。
分析图中每个六边形含有个碳原子。
教学反思:本节内容是安排在原子结构、分子结构以及结构决定性质的内容之后来学习,对于学生的学习有一定的理论基础。
本节内容主要是通过介绍各种各样的固体为出发点来过渡到本堂课的主题——晶体和非晶体。
而晶体和非晶体的学习是以各自的自范性和微观结构比较为切入点,进而得出得到晶体的一般途径以及晶体的常见性质和区分晶体的方法。
第二节分子晶体与原子晶体第一课时分子晶体教学目标设定:1、使学生了解分子晶体的组成粒子、结构模型和结构特点及其性质的一般特点。
2、使学生了解晶体类型与性质的关系。
3、使学生理解分子间作用力和氢键对物质物理性质的影响。
4、知道一些常见的属于分子晶体的物质类别。
5、使学生主动参与科学探究,体验研究过程,激发他们的学习兴趣。
教学重点难点:重点掌握分子晶体的结构特点和性质特点难点是氢键的方向性和氢键对物体物理性质的影响从三维空间结构认识晶胞的组成结构教学方法建议:运用模型和类比方法诱导分析归纳教学过程设计:复问:什么是离子晶体?哪几类物质属于离子晶体?(离子化合物为固态时均属于离子晶体,如大部分盐、碱、金属氧化物属于离子晶体)投影展示实物:冰、干冰、碘晶体教师诱导:这些物质属于离子晶体吗?构成它们的基本粒子是什么?这些粒子间通过什么作用结合而成的?学生分组讨论回答板书:分子通过分子间作用力形成分子晶体一、分子晶体1、定义:含分子的晶体称为分子晶体也就是说:分子间以分子间作用力相结合的晶体叫做分子晶体看图3-9,如:碘晶体中只含有I2分子,就属于分子晶体问:还有哪些属于分子晶体?2、较典型的分子晶体有非金属氢化物,部分非金属单质,部分非金属氧化物,几乎所有的酸,绝大多数有机物的晶体。
3、分子间作用力和氢键过度:首先让我们回忆一下分子间作用力的有关知识阅读必修2 P22科学视眼教师诱导:分子间存在着一种把分子聚集在一起的作用力叫做分子间作用力,也叫范徳华力。
分子间作用力对物质的性质有怎么样的影响。
学生回答:一般来说,对与组成和结构相似的物质,相对分子量越大分子间作用力越大,物质的熔沸点也越高。
教师诱导:但是有些氢化物的熔点和沸点的递变却与此不完全符合,如:NH3,H2O和HF的沸点就出现反常。
指导学生自学:教材中有些氢键形成的条件,氢键的定义,氢键对物质物理性质的影响。
多媒体动画片氢键形成的过程:①氢键形成的条件:半径小,吸引电子能力强的原子(N,O,F)与H核②氢键的定义:半径小、吸引电子能力强的原子与H核之间的静电吸引作用。
氢键可看作是一种比较强的分子间作用力。
③氢键对物质性质的影响:氢键使物质的熔沸点升高。
④投影氢键的表示如:冰一个水分子能和周围4个水分子从氢键相结合组成一个正四面体见图3-11教师诱导:在分子晶体中,分子内的原子以共价键相结合,而相邻分子通过分子间作用力相互吸引。
分子晶体有哪些特性呢?学生回答4.分子晶体的物理特性:熔沸点较低、易升华、硬度小。
固态和熔融状态下都不导电。
教师诱导:大多数分子晶体结构有如下特征:如果分子间作用力只是范德华力。
以一个分子为中心,其周围通常可以有几个紧邻的分子。
如图3-10的O2,C60,我们把这一特征叫做分子紧密堆积。
如果分子间除范德华力外还有其他作用力(如氢键),如果分子间存在着氢键,分子就不会采取紧密堆积的方式学生讨论回答:在冰的晶体中,每个水分子周围只有4个紧邻的水分子,形成正四面体。
氢键不是化学键,比共价键弱得多却跟共价键一样具有方向性,而氢键的存在迫使四面体中心的每个水分子与四面体顶角方向的4个相邻水分子的相互吸引,这一排列使冰晶体中空间利用率不高,皆有相当大的空隙使得冰的密度减小。
教师诱导,还有一种晶体叫做干冰,它是固体的CO2的晶体。
干冰外观像冰,干冰不是冰。
其熔点比冰低的多,易升华。
出示干冰的晶体结构晶胞模型。
教师讲解:干冰晶体中CO2分子之间只存在分子间力不存在氢键,因此干冰中CO2分子紧密堆积,每个CO2分子周围,最近且等距离的CO2分子数目有几个?一个CO2分子处于三个相互垂直的面的中心,在每个面上,处于四个对角线上各有一个CO2分子周围,所以每个CO2分子周围最近且等距离的CO2分子数目是12个。
投影小结完成表格课堂巩固练习1、下列属于分子晶体的一组物质是A 、CaO、NO、CO B、CCl4、H2O2、HeC、CO2、SO2、NaCl D 、CH4、O2、Na2O2、下列性质符合分子晶体的是A、熔点1070℃,易熔于水,水溶液能导电B、熔点是10.31℃,液体不导电,水溶液能导电C、熔点97.81℃,质软,能导电,密度是0.97g/cm3D、熔点,熔化时能导电,水溶液也能导电3、下列物质的液体中,不存在分子是A 二氧化硅B 二氧化硫C 二氧化碳D二硫化碳4、下列说法正确的是A、离子化合物中可能含有共价键B、分子晶体中的分子内不含有共价键C、分子晶体中一定有非极性共价键D、分子晶体中分子一定紧密堆积5、干冰汽化时,下列所述内容发生变化的是A、分子内共价键B、分子间作用力C、分子间距离D、分子间的氢键6、“可燃冰”是深藏在海底的白色晶体,存储量巨大,是人类未来极具潜在优势的洁净能源。
