合成气一步法制二甲醚双功能催化剂中甲醇脱水组分对催化性能的影响
合成气一步法制二甲醚催化剂成胶pH对其结构和性能的影响

16
天然气化工—C1 化学与化工
2019 年第 44 卷
后 , 室 温 下 放 置 24h 后 将 其 倒 入 溶 有 36.24g Cu(NO3)2、22.31g Zn(NO3)2(天津科密欧化学试剂有限 公司,分析纯)和 2.6g 聚乙二醇 600(国药集团)的无 水乙醇溶液中,加入适量的水,在 85℃搅拌均匀后, 向混合溶液中滴加氨水(天津市科密欧化学试剂有 限 公 司 ,分 析 纯 )控 制 成 胶 pH 分 别 为 3、4、6、7、8, 之 后 升 温 至 95℃搅 拌 5 h,再 敞 口 1h,室 温 下 老 化 11d 得到催化剂前驱体。 其中 pH 为 3 时为未添加 氨水的溶液 pH 值。 将前驱体倒入混有 0.5mL span鄄 80 的 300mL 液体石蜡中,在 N2 气氛中缓慢升温至 280℃后,搅拌 8 h,得到浆状催化剂。 根据成胶 pH 大小将催化剂命名为 Cat鄄3、Cat鄄4、Cat鄄6、Cat鄄7、Cat鄄 8。 1.2 催化剂的表征
多,控制不当易造成混浊甚至沉淀,胶体的均匀性 直接影响金属的分散性, 成胶 pH 在胶体形成过程 中扮演重要角色[8]。 李双明等[9]以硝酸铜、柠檬酸为 原料, 利用氨水调节 pH 制备溶胶, 结果表明,当 pH=6~7 时,形成的凝胶均一,可以制得粒径为 50~ 70nm 的球形纳米铜颗粒, 催化剂的催化活性有了 较大的提高。 Alamolhoda 等[10]通过控制成胶 pH 制 备 NeFe2O4 当 pH 为 8 时 为 最 佳 条 件 , 获 得 的 NeFe2O4 均 匀 且 颗 粒 较 小 。 Ilican 等[11]在 制 备 ZnO 薄 膜 的 过 程 中 利 用 冰 乙 酸 和 氨 水 控 制 成 胶 pH,成 胶 pH 对 ZnO 的 结 构 和 形 貌 影 响 显 著 , 当 pH 由 5.05 提 高 到 7 时 ,ZnO 晶 粒 度 和 纯 度 不 断 提 高 ,当 pH 高于 7 时,ZnO 晶粒度减小且有杂质产生。 Qiu W 等 [12]以 TiOSO4 和 SiO2 溶 胶 为 原 料 , 用 氨 水 调 节 pH 值 制 备 TiO2 和 TiO2/SiO2 催 化 剂 ,TiO2 和 TiO2/ SiO2 光催化剂的比表面积随 pH 值升高略有增大, 表面酸量随 pH 值升高而增加。
合成气一步法制备二甲醚核壳结构催化剂的制备及其反应性能

文章编号:0253⁃2409(2013)08⁃1003⁃07 收稿日期:2013⁃05⁃25;修回日期:2013⁃06⁃10㊂ 基金项目:山西省青年科技研究基金(2013021008⁃3);太原市科技项目(120247⁃23)㊂ 联系作者:王琰,Tel :0351⁃6010121,E⁃mail :wangyan @ ㊂合成气一步法制备二甲醚核壳结构催化剂的制备及其反应性能王文丽,王 琰,陈月仙,赵文超,李瑞丰(太原理工大学精细化工研究所,山西太原 030024)摘 要:以生物质(葡萄糖㊁蔗糖㊁淀粉)为模板剂,通过水热合成法制备具有核壳结构的CuO⁃ZnO⁃Al 2O 3@Al 2O 3复合催化剂,该催化剂以甲醇合成催化剂CuO⁃ZnO⁃Al 2O 3为核,甲醇脱水催化剂Al 2O 3为壳㊂SEM⁃EDS 对催化剂核壳结构的表征发现,通过改变水热合成温度和合成时间可以调变催化剂中Al 2O 3壳层的厚度㊂将该复合催化剂用于合成气直接制备二甲醚的反应,在空速1500mL /(h ㊃g cat )㊁温度260℃㊁压力5.0MPa 的条件下,CO 转化率和二甲醚选择性分别达到35.2%和61.1%㊂关键词:核壳双功能催化剂;合成气;二甲醚中图分类号:O 643 文献标识码:APreparation of core⁃shellcatalysts for one⁃step synthesis of dimethyl ether from syngasWANG Wen⁃li ,WANG Yan ,CHEN Yue⁃xian ,ZHAO Wen⁃chao ,LI Rui⁃feng(Institute of Special Chemicals ,Taiyuan University of Technology ,Taiyuan 030024,China )Abstract :A core⁃shell catalyst CuO⁃ZnO⁃Al 2O 3@Al 2O 3for one⁃step synthesis of dimethyl ether from synthesis gas was prepared using glucose ,sucrose or starch as template ,and characterized by scanning electron microscopy (SEM )with energy dispersive spectroscopy (EDS ).The thickness of the Al 2O 3shell in the catalyst was altered by controlling the synthesis condition ,such as temperature and time.The catalytic performance of dimethyl ether (DME )synthesized from CO hydrogenation on the catalysts were investigated.The conversion of CO and the selectivity of DME on CuO⁃ZnO⁃Al 2O 3@Al 2O 3achieved 35.2%and 61.1%at 260℃,5.0MPa and 1500mL /(h ㊃g cat ),respectively.Key words :core⁃shell catalysts ;syngas ;dimethyl ether 目前,工业上二甲醚主要由煤炭或天然气经合成气合成甲醇㊁甲醇再脱水到二甲醚的过程而制得㊂利用中国丰富的煤炭和天然气资源制备二甲醚,对弥补中国石油资源的不足㊁缓解能源利用和环境污染的矛盾都具有重要意义[1,2]㊂二甲醚(Dimethyl ether ),简称DME ,是一种无毒和非腐蚀性化合物,其十六烷值达55~60,具有极为优良的燃烧性能,可分别替代液化石油气和柴油作为民用和车用燃料[3~6],而且在较低温度下可催化重整制取氢气,可用来作为燃料电池的氢源[7,8]㊂相对于传统的含氯氟烃(氟里昂等),二甲醚具有零消耗臭氧潜能值和低全球变暖潜能值的优点,广泛用于对环境友好的气溶胶喷雾和绿色制冷剂[9]㊂此外,在工业上,二甲醚也可作为制备硫酸二甲酯㊁低碳烯烃等许多化学品的原料或中间体[5,10]㊂合成气直接制备二甲醚(Syngas to Dimethyl ether ,简称STD )的反应主要包含甲醇合成和甲醇脱水两个反应㊂两反应方程式分别为:CO +2H ⥫⥬‗2CH 3OH (1)2CH 3⥫⥬‗OH CH 3OCH 3+H 2O (2)同时,式(2)中生成的部分水会发生水汽变换反应(water⁃gas⁃shift reaction ,WGS ):CO +H 2⥫⥬‗O CO 2+H 2(3)总的反应方程式为:3CO +3H ⥫⥬‗2CH 3OCH 3+CO 2(4)通常,合成气直接制备二甲醚双功能催化剂包含甲醇合成催化剂和甲醇脱水催化剂两种活性组分㊂由于催化剂的协同效应,打破了甲醇合成反应的化学反应平衡限制,CO 的单程转化率得以提高,反应工艺流程得以简化,比两步法制取二甲醚具有显著的经济效益[11~16]㊂传统机械混合的双功能催化剂,两活性组分随机分布,不能很好的发挥两组分的协同效应㊂核壳结构的双功能催化剂的限制效应第41卷第8期2013年8月燃 料 化 学 学 报Journal of Fuel Chemistry and Technology Vol.41No.8Aug.2013和协同效应使其在STD反应中和机械混合的催化剂相比具有更高的DME选择性[17]㊂本实验制备了具有核壳结构的双功能催化剂,以甲醇合成催化剂CuO⁃ZnO⁃Al2O3为核,甲醇脱水催化剂Al2O3为壳,提供了一个受限的反应环境㊂合成气先通过晶粒间隙扩散到内核表面,在甲醇合成催化剂活性位上合成甲醇,甲醇在向外扩散经过Al2O3壳层时进行脱水反应㊂1 实验部分1.1 催化剂的制备以葡萄糖㊁蔗糖或淀粉为模板剂,采用一步法制备以工业甲醇合成催化剂CuO⁃ZnO⁃Al2O3(简称CZA)为核和以Al2O3为壳的CZA@Al2O3复合催化剂的制备方法如下:首先,将CZA压片㊁粉碎成20~40目大小的颗粒备用㊂制备浓度为0.5mol/L的葡萄糖(或蔗糖或淀粉)溶液,将2g的铝盐Al(NO3)3加入到40mL的葡萄糖(或蔗糖或淀粉)溶液中,搅拌至其完全溶解,然后加入2g CZA颗粒,装入100mL自压反应釜中,于100~140℃的旋转反应釜(10r/min)中进行反应,反应时间分别为4㊁6和12h,得到核壳结构的复合催化剂样品,该样品用蒸馏水和无水乙醇洗涤,之后在室温下干燥,并经过焙烧过程制成最终的CZA@Al2O3复合催化剂㊂所得复合催化剂标记为CZA@Al2O3⁃Template⁃Temperature⁃Time㊂焙烧过程:样品在管式炉中进行焙烧,首先样品在氮气保护下升温至330℃焙烧3h,然后继续升温至440℃焙烧3h,之后切换至氧气气氛下于550℃焙烧3h,其升温速率为3℃/min㊂1.2 催化剂的表征采用Shimazu XRD⁃6000粉末X射线衍射仪对催化剂的物相进行分析㊂实验条件为:Cu Kα射线(姿=0.154nm),Ni滤波,管电压40kV,管电流30mA,扫描速率8°/min,5°~80°扫描㊂采用配备EDS的HITACHI S⁃4800场发射扫描电子显微镜对催化剂的形貌㊁横截面核壳结构和元素分布进行表征和分析㊂1.3 催化剂的活性评价催化剂的活性评价在高压固定床微型反应装置(NEWFORD)上进行㊂催化剂用量为1g,反应前先将催化剂用还原气(5%H2+95%N2)在280℃还原12h,气体流量为50mL/min,还原后降温至反应温度,以一定空速通入合成气(64%H2+32%CO+4% Ar)进行反应㊂反应进行6h后,反应产物以岛津GC⁃2014C色谱仪在线分析,色谱配备双色谱柱TCD检测器;TDX⁃01色谱柱检测CO和CO2, GDX⁃501色谱柱检测甲醇㊁DME和碳氢化合物㊂反应装置的管路均用加热带加热并保持温度在100℃,以避免产物在管路中冷凝㊂2 结果与讨论2.1 催化剂的结构表征在同样的合成条件下,以葡萄糖㊁蔗糖和淀粉为模板剂制备的核壳结构催化剂以及工业甲醇催化剂CZA的XRD谱图见图1㊂由图1可知,CZA@ Al2O3⁃p⁃120⁃6㊁CZA@Al2O3⁃z⁃120⁃6㊁CZA@Al2O3⁃d⁃120⁃6的出峰位置和CZA的出峰位置一致,主要是CuO的特征衍射峰,没有发现其他新物质的特征峰,表面氧化铝为无定形㊂图1 CZA㊁CZA@Al2O3⁃p⁃120⁃6㊁CZA@Al2O3⁃z⁃120⁃6㊁CZA@Al2O3⁃d⁃120⁃6样品的XRD谱图Figure1 XRD patterns of CZA,CZA@Al2O3⁃p⁃120⁃6, CZA@Al2O3⁃z⁃120⁃6,CZA@Al2O3⁃d⁃120⁃6 图2为甲醇合成催化剂CZA(图2(a)㊁(b))和核壳结构的复合催化剂CZA@Al2O3⁃p⁃120⁃6(图2 (c)㊁(d))的表面扫描电镜照片和EDS分析㊂甲醇催化剂CZA表面较为光滑,CZA中的黑色颗粒为工业催化剂中的石墨,用以增加工业甲醇催化剂CZA的机械强度㊂EDS分析结果表明,CZA的组成元素主要为Cu㊁Zn和Al,且其物质的量比为Cu∶Zn∶Al=60.0∶29.5∶10.5㊂经过水热合成表面涂层后,由图2(c)可以看出,CZA表面包裹着一层粗糙的相对完整的壳层结构㊂从其表面的EDS分析结果看,其表面主要为Al元素,同时有少量的Cu和Zn元素㊂从SEM的表征结果中可以看出,本实验成功的合成出具有核壳结构的CZA@Al2O3复合催4001 燃 料 化 学 学 报第41卷化剂,Al 2O 3壳层完整的包裹在内核CZA 的表面㊂图2 CZA 及CZA @Al 2O 3⁃p⁃120⁃6的SEM 照片和表面EDS 分析Figure 2 SEM images and surface EDS analysis of CZA and CZA @Al 2O 3⁃p⁃120⁃6(a ),(b ):CZA ;(c ),(d ):CZA @Al 2O 3⁃p⁃120⁃6 图3为不同水热温度条件下合成的CZA @Al 2O 3⁃p⁃t ⁃6横截面SEM 照片和线扫描EDS 分析,由图3可知,在100℃(图3(a )㊁(b ))㊁120℃(图3(c )㊁(d ))或140℃(图3(e )㊁(f ))下合成的CZA @Al 2O 3⁃p 均具有明显的核壳结构㊂通过CZA @Al 2O 3⁃p⁃100⁃6的线扫描EDS 分析看到,Al 元素的信号值在49μm 处突然上升之后在76μm 处下降,表明催化剂CZA @Al 2O 3⁃p⁃t ⁃6的壳层是Al 2O 3,其厚度为27μm ㊂同时,Cu 和Zn 的信号值在核壳结合处突然上升,表明核壳结构催化剂CZA @Al 2O 3⁃p⁃t ⁃6中Cu 和Zn 元素主要分布在CZA 内核中㊂从图3(b )㊁(d )和(f )中分别可以看出,CZA @Al 2O 3⁃p⁃100⁃6㊁CZA @Al 2O 3⁃p⁃120⁃6和CZA @Al 2O 3⁃p⁃140⁃6的Al 2O 3壳层厚度依次为27㊁23㊁16μm ,随CZA @Al 2O 3⁃p⁃T⁃6合成温度的提高Al 2O 3壳层厚度逐渐减小㊂ 图4为CZA @Al 2O 3⁃p⁃120⁃t 横截面SEM 照片和线扫描EDS 分析,由图4可知,在4(图4(a )㊁(b ))和12h (图4(c )㊁(d ))下合成的CZA @Al 2O 3⁃p⁃120⁃t 均拥有核壳结构㊂通过线扫描EDS 分析(图4(b )㊁(d ))看出CZA @Al 2O 3⁃p⁃120⁃4和CZA@Al 2O 3⁃p⁃120⁃12的Al 2O 3壳层厚度分别为16㊁23μm ,与CZA @Al 2O 3⁃p⁃120⁃6(图3(c )㊁(d ))相比,可以看出合成时间在4~6h 时,随着时间的延长,Al 2O 3壳层厚度增大,继续增加合成时间时CZA @Al 2O 3⁃p⁃120⁃t 的Al 2O 3壳层厚度基本不变㊂图5为CZA @Al 2O 3⁃z⁃120⁃6和CZA @Al 2O 3⁃d⁃120⁃6横截面SEM 照片和线扫描EDS 分析,由图5可知,模板剂分别为蔗糖(图5(a )㊁(b ))和淀粉(图5(c )㊁(d ))时合成的CZA @Al 2O 3拥有核壳结构㊂通过线扫描EDS 分析(图5(b )㊁(d ))看出,CZA @Al 2O 3⁃z⁃120⁃6和CZA @Al 2O 3⁃d⁃120⁃6的Al 2O 3壳层厚度分别为12㊁17μm ㊂5001第8期王文丽等:合成气一步法制备二甲醚核壳结构催化剂的制备及其反应性能图3 CZA@Al2O3⁃p⁃T⁃6横截面SEM照片和线扫描EDS分析Figure3 Cross⁃section SEM image and line EDS analysis of CZA@Al2O3⁃p⁃T⁃6 (a),(b):CZA@Al2O3⁃p⁃100⁃6;(c),(d):CZA@Al2O3⁃p⁃120⁃6;(e),(f):CZA@Al2O3⁃p⁃140⁃62.2 催化剂反应性能以葡萄糖为模板剂,在合成时间6h㊁合成温度120℃的条件下得到复合催化剂(CZA@Al2O3⁃p⁃120⁃6),其CO的转化率为35.2%,DME的选择性为61.1%,甲醇选择性为5.2%见表1㊂在同等STD反应条件下,CO的转化率高于Yang等[18]报道的具有核壳结构催化剂(CZA@ZSM⁃5),同时CO的转化率和DME的选择性均高于机械混合催化剂(CZA⁃M),而甲醇选择性低于CZA⁃M[17]㊂机械混合催化剂(CZA⁃M)中甲醇合成催化剂和甲醇脱水催化剂随机分布,形成的开放式反应环境使得生成的部分甲醇未发生脱水反应直接从表面逸出,导致二甲醚选择性较低㊂对于核壳催化剂CZA@Al2O3,在水热合成过程中,葡萄糖包裹在CZA表面形成碳层,碳层中的羟基和羧基与溶液中的铝离子相互作用,使得铝离子充分包裹在碳层上,焙烧脱碳后,CZA表面形成一个完整的Al2O3壳层,其反应过程见图6[17]㊂合成气先通过Al2O3壳层扩散到内核表面,在Cu⁃ZnO活性位上生成甲醇,而核壳结构提供的受限反应环境,使在内核生成的6001 燃 料 化 学 学 报第41卷甲醇必须通过壳层向外扩散,从而加大甲醇与壳层上酸性位的碰撞几率,提高二甲醚的选择性㊂图4 CZA @Al 2O 3⁃p⁃120⁃t 横截面SEM 照片和线扫描EDS 分析Figure 4 Cross⁃section SEM image and line EDS analysis of CZA @Al 2O 3⁃p⁃120⁃t(a ),(b ):CZA @Al 2O 3⁃p⁃120⁃4;(c ),(d ):CZA @Al 2O 3⁃p⁃120⁃12表1 CZA @Al 2O 3在STD 反应中的催化反应活性aTable 1 Catalytic performance in the STD reaction over CZA @Al 2O 3SampleCO conversionx mol /%Selectivity s mol /%MeOH DME CO 2HCs b CZA @Al 2O 3⁃p⁃100⁃629.67.350.639.13.0CZA @Al 2O 3⁃p⁃120⁃635.25.261.131.22.5CZA @Al 2O 3⁃p⁃140⁃622.09.159.529.32.1CZA @Al 2O 3⁃p⁃120⁃428.35.856.835.12.3CZA @Al 2O 3⁃p⁃120⁃1232.96.660.330.52.6CZA @Al 2O 3⁃z⁃120⁃619.86.162.530.11.3CZA @Al 2O 3⁃d⁃120⁃634.16.654.635.73.2CZA⁃M [17]28.316.151.630.12.2areaction condition :260℃,5.0MPa ,1500mL /(h ㊃g cat ),TOS =6h ;b HCs mainly include CH 4and C 2hydrocarbons 由表1可知,在较高温度140℃时,合成催化剂在STD 反应中的CO 转化率只有22%㊂由图3可知,CZA @Al 2O 3⁃p⁃100⁃6㊁CZA @Al 2O 3⁃p⁃120⁃6和CZA @Al 2O 3⁃p⁃140⁃6的Al 2O 3壳层厚度依次为27㊁23㊁16μm ㊂壳层的厚度影响着催化剂在STD 反应中的催化效果,较厚的壳层限制原料气和产物的扩散,同时,较薄的壳层厚度导致甲醇不能有效地进行脱水反应,所以CZA @Al 2O 3⁃p⁃100⁃6和CZA @Al 2O 3⁃p⁃140⁃6的CO 转化率和DME 选择性均小于CZA @Al 2O 3⁃p⁃120⁃6㊂合成温度为120℃,合成时间分别为4㊁6㊁12h 时,6h 合成的催化剂的CO 转化率和DME 选择性较大于4h 的,甲醇和二氧化碳选择性也相对较低,与12h 时的基本相同㊂CZA @Al 2O 3⁃p⁃120⁃4㊁CZA @Al 2O 3⁃p⁃120⁃6㊁CZA @Al 2O 3⁃7001第8期王文丽等:合成气一步法制备二甲醚核壳结构催化剂的制备及其反应性能p⁃120⁃12的Al 2O 3壳层厚度分别为16㊁23㊁23μm ,CZA @Al 2O 3⁃p⁃120⁃4的Al 2O 3壳层厚度小于CZA @Al 2O 3⁃p⁃120⁃6,CO 转化率较低,CZA @Al 2O 3⁃p⁃120⁃6和CZA @Al 2O 3⁃p⁃120⁃12的Al 2O 3壳层厚度相同,但由于水热时间较长,可能使得内核CZA 在水热过程中结构破坏,导致CO 转化率降低㊂以蔗糖为模板剂时,CO 转化率相比葡萄糖和可溶性淀粉低大约15%,二甲醚选择性相近㊂葡萄糖和可溶性淀粉的CO 转化率大小相近,但是采用葡萄糖的二甲醚选择性较高,且甲醇和碳氢化合物的选择性也较低,所以选用葡萄糖较为合适㊂图5 CZA @Al 2O 3⁃z⁃120⁃6和CZA @Al 2O 3⁃d⁃120⁃6横截面SEM 照片和线扫描EDS 分析Figure 5 Cross⁃section SEM image and line EDS analysis of CZA @Al 2O 3⁃z⁃120⁃6and CZA @Al 2O 3⁃d⁃120⁃6(a ),(b ):CZA @Al 2O 3⁃z⁃120⁃6;(c ),(d ):CZA @Al 2O 3⁃d⁃120⁃6图6 核壳催化剂CZA @Al 2O 3的反应过程示意图Figure 6 Schematic diagram of the reaction procedure on the CZA @Al 2O 33 结 论 以葡萄糖㊁蔗糖或可溶性淀粉为模板剂,制备出一种具有核壳结构的CZA @Al 2O 3复合催化剂,该复合催化剂以甲醇合成催化剂CuO⁃ZnO⁃Al 2O 3为核,甲醇脱水催化剂Al 2O 3为壳㊂通过改变水热反应温度和时间可以改变Al 2O 3壳层的厚度,同时,也影响了核壳结构复合催化剂CZA @Al 2O 3在STD反应中的催化性能㊂以葡萄糖为模板剂,在合成温度120℃和合成时间6h 的条件下制备出的CZA @Al 2O 3复合催化剂在空速1500mL /(h ㊃g cat )㊁温度260℃㊁压力5.0MPa 的条件下,CO 的转化率可以达到35.2%,DME 的选择性达到61.1%㊂参考文献[1] LV P M ,YUAN Z H ,WU C Z ,MA L L ,CHEN Y ,TSUBAKI N.Bio⁃syngas production from biomass catalytic gasification [J ].EnergyConv Manag ,2007,48(4):1132⁃1139.[2] JIN D F ,ZHU B ,HOU Z Y ,FEI J H ,LOU H ,ZHENG X M.Dimethyl ether synthesis via methanol and syngas over rare earth metals8001 燃 料 化 学 学 报第41卷modified zeolite Y and dual Cu⁃Mn⁃Zn catalysts [J ].Fuel ,2007,86(17):2707⁃2713.[3] ARKHAROV A M ,GLUKHOV S D ,GREKHOV L V ,ZHERDEV A A ,IVASHCHENKO N A ,KALININ D N ,SHARABURIN A V ,ALEKSANDROV A e of dimethyl ether as a motor fuel and a refrigerant [J ].Chem Petrol Eng ,2003,39(5):330⁃336.[4] SEMELSBERGER T A ,BORUP R K ,GREENE H L.Dimethyl ether (DME )as an alternative fuel [J ].J Power Sources ,2006,156(2):497⁃511.[5] CROOKES R J ,BOB⁃MANUEL K D H.RME or DME :A preferred alternative fuel option for future diesel engine operation [J ].EnergyConv Manag ,2007,48(11):2971⁃2977.[6] ARCOUMANIS C ,BAE C ,CROOKES R ,The potential of di⁃methyl ether (DME )as an alternative fuel for compression⁃ignition engines :Areview [J ].Fuel ,2008,87(7):1014⁃1030.[7] LEDESMA C ,LLORCA J.Dimethyl ether steam reforming over Cu⁃Zn⁃Pd /CeO 2⁃ZrO 2catalytic monoliths.The role of Cu species on catalyststability [J ].J Phys Chem C ,2011,115(23):11624⁃11632.[8] XING L H ,GAO Y Z ,WANG Z B ,DU C Y ,YIN G P.Effect of anode diffusion layer fabricated with mesoporous carbon on theperformance of direct dimethyl ether fuel cell [J ].Int J Hydrog Energy ,2011,36(17):11102⁃11107.[9] OMATA K ,WATANABE Y ,UMEGAKI T ,ISHIGURO G ,YAMADA M.Low⁃pressure DME synthesis with Cu⁃based hybrid catalystsusing temperature⁃gradient reactor [J ].Fuel ,2002,81(11):1605⁃1609.[10] MAN J M ,ZHANG Q D ,XIE H J ,PAN J X ,TAN Y S ,HAN Y Z.Effects of reaction atmosphere on dimethyl ether conversion topropylene process over Ca /ZSM⁃5[J ].Journal of Fuel Chemistry and Technology ,2011,39(1):42⁃46.[11] ADACHI Y ,KOMOTO M ,WATANABE I ,OHNO Y ,FUJIMOTO K.Effective utilization of remote coal through dimethyl ether synthesis[J ].Fuel ,2000,79(3):229⁃234.[12] 许庆利,李庭琛,张素平,任铮伟,颜涌捷.分子筛改性对一步法合成二甲醚的影响[J ].燃料化学学报,2008,36(1):74⁃78.(XU Qing⁃li ,LI Ting⁃chen ,ZHANG Su⁃ping ,REN Zheng⁃wei ,YAN Yong⁃jie.Effect of the modified zeolite on one⁃step dimethyl ether synthesis [J ].Journal of Fuel Chemistry and Technology ,2008,36(1):74⁃78.)[13] MAO D S ,YANG W M ,XIA J C ,ZHANG B ,SONG Q Y ,CHEN Q L.Highly effective hybrid catalyst for the direct synthesis of dimethylether from syngas with magnesium oxide⁃modified HZSM⁃5as a dehydration component [J ].J Catal ,2005,230(1):140⁃149.[14] 毛东森,夏建超.分子筛硅铝比及晶粒粒径对CuO⁃ZnO⁃Al 2O 3/HZSM⁃5催化剂直接合成二甲醚反应性能的影响[J ].燃料化学学报,2012,40(2):235⁃240.(MAO Dong⁃sen ,XIA Jian⁃chao.Effects of silicon to aluminum ratio and crystal size of zeolite on catalytic properties of CuO⁃ZnO⁃Al 2O 3/HZSM⁃5for the direct synthesis of dimethyl ether from syngas [J ].Journal of Fuel Chemistry and Technology ,2012,40(2):235⁃240.)[15] WANG D S ,HAN Y Z ,TAN Y S ,TSUBAKI N.Effect of H 2O on Cu⁃based catalyst in one⁃step slurry phase dimethyl ether synthesis [J ].Fuel Process Technol ,2009,90(3):446⁃451.[16] 李超,李琢,李建青,杨成,吴晋沪.一步法合成二甲醚整体式催化剂的制备及反应性能研究[J ].燃料化学学报,2011,39(4):287⁃292.(LI Chao ,LI Zhuo ,LI Jian⁃qing ,YANG Cheng ,WU Jin⁃hu.Preparation and catalytic properties of a monolithic catalyst for one step synthesis of dimethyl ether [J ].Journal of Fuel Chemistry and Technology ,2011,39(4):287⁃292.)[17] WANG Y ,WANG W L ,CHEN Y X ,MA J H ,ZHENG J J ,LI R F.Core⁃shell catalyst CuO⁃ZnO⁃Al 2O 3@Al 2O 3for dimethyl ethersynthesis from syngas [J ].Chem Lett ,2013,42(4):335⁃337.[18] YANG G H ,TSUBAKI N ,SHAMOTO J ,YONEYAMA Y ,ZHANG Y.Confinement effect and synergistic function of H⁃ZSM⁃5/CuO⁃ZnO⁃Al 2O 3capsule catalyst for one⁃step controlled synthesis [J ].J Am Chem Soc ,2010,132(23):8129⁃8136.9001第8期王文丽等:合成气一步法制备二甲醚核壳结构催化剂的制备及其反应性能。
合成气在有机化工生产中的利用方法研究

合成气在有机化工生产中的利用方法研究摘要:在新时期,有机化工企业呈现出积极的发展态势,同时,合成气已成为有机化工生产过程中最重要的原料之一,合成气主要是由乙二醇、乙二醇和甲醇等组合而成,本文主要介绍为在该方法中使用合成气体。
本文详细介绍了合成气体在有机化学品生产中的应用。
关键词:合成气;有机化工;生产;利用方法一、合成气一步法制取二甲醚的生产技术1.一步法合成二甲醚的反应原理合成气一步法适用于制备二甲醚,即在同一容器中进行两步反应,然后将产生的甲醇直接脱水。
用两步法进行了科学合理的比较。
该步骤工艺将合成气中的CO的单向转化率提高了约50%,而且操作非常简单。
同时,鉴于合成气是主要原料,两步法生产的二甲醚的价格会因甲醇的价格而大大降低。
2.慎重选择催化剂在利用合成气一步法制备二甲醚的过程中,针对催化剂需要严格筛选,尽量地抉择组合类催化剂或是双基本功能催化剂(比如甲醇制备与甲醇脱水共同组合的催化剂),只有这样的催化剂,最终的结果是最理想的。
自铜基催化剂开发以来,它们已逐渐发展成为甲醇合成中最广泛使用的催化剂,取代了传统的催化剂(如Zn-Cr催化剂)。
铜基催化剂中最常用的辅酶是Zn和AI,加入Zn,可以进一步增多铝的体积;Al的作用就是框架结构助剂,使铝氧化物均匀分布,而且尺寸一直增大。
在许多在甲醇合成中表现良好的催化剂中,铜芯铝催化剂正成为二甲醚制备中最常见的催化剂。
二、合成气生产甲醇生产技术1.以合成气制甲醇生产技术的主要反应原理主反应包含:CO+2H2=CH3OH。
在制备甲醇的过程中,能触及许多的副反应,分成两种,即平行副反应与连串副反应,副反应的发生,不太单单会消耗大量的原材料,缩合现象不允许准备好的甲烷跟随产品,甲烷对主反应的化学平衡有不同程度的影响,化学反应速度进行循环,在该反应过程中能够更好地控制副反应,一些催化剂可以被添加。
2.催化剂的选择早在20世纪60世纪末左右,便已开发成功了铝.基催化剂,铜基催化剂不但使用性能难,并且活性极低,适宜的反应环境温度为493~543K。
二甲醚的生产方法有一步法和二步法
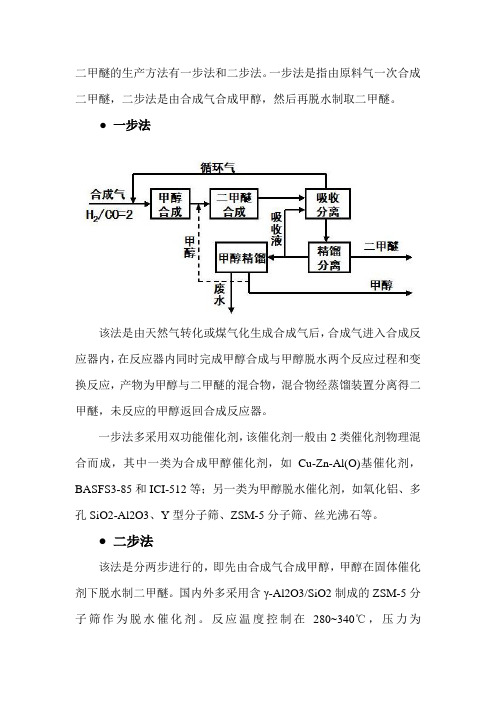
二甲醚的生产方法有一步法和二步法。
一步法是指由原料气一次合成二甲醚,二步法是由合成气合成甲醇,然后再脱水制取二甲醚。
● 一步法该法是由天然气转化或煤气化生成合成气后,合成气进入合成反应器内,在反应器内同时完成甲醇合成与甲醇脱水两个反应过程和变换反应,产物为甲醇与二甲醚的混合物,混合物经蒸馏装置分离得二甲醚,未反应的甲醇返回合成反应器。
一步法多采用双功能催化剂,该催化剂一般由2类催化剂物理混合而成,其中一类为合成甲醇催化剂,如Cu-Zn-Al(O)基催化剂,BASFS3-85和ICI-512等;另一类为甲醇脱水催化剂,如氧化铝、多孔SiO2-Al2O3、Y型分子筛、ZSM-5分子筛、丝光沸石等。
● 二步法该法是分两步进行的,即先由合成气合成甲醇,甲醇在固体催化剂下脱水制二甲醚。
国内外多采用含γ-Al2O3/SiO2制成的ZSM-5分子筛作为脱水催化剂。
反应温度控制在280~340℃,压力为0.5-0.8MPa。
甲醇的单程转化率在70-85%之间,二甲醚的选择性大于98%。
一步法合成二甲醚没有甲醇合成的中间过程,与两步法相比,其工艺流程简单、设备少、投资小、操作费用低,从而使二甲醚生产成本得到降低,经济效益得到提高。
因此,一步法合成二甲醚是国内外开发的热点。
国外开发的有代表性的一步法工艺有:丹麦Topsφe工艺、美国Air Products工艺和日本NKK工艺。
二步法合成二甲醚是目前国内外二甲醚生产的主要工艺,该法以精甲醇为原料,脱水反应副产物少,二甲醚纯度达99.9%,工艺成熟,装置适应性广,后处理简单,可直接建在甲醇生产厂,也可建在其它公用设施好的非甲醇生产厂。
但该法要经过甲醇合成、甲醇精馏、甲醇脱水和二甲醚精馏等工艺,流程较长,因而设备投资较大。
但目前国外公布的大型二甲醚建设项目绝大多数采用两步法工艺技术,说明两步法有较强的综合竞争力。
合成气一步法制二甲醚新型催化剂的研究

合成气一步法制二甲醚新型催化剂的研究随着时代的发展,能源在经济发展和日常生活中发挥的作用愈加显著。
国家未来经济发展的持续性以及人们日常生活质量的提高,对清洁能源的研究不断加深和推广。
二甲醚作为应用不断推广的清洁能源,制作的方式也有好几种,合成气一步法制二甲醚有着不可替代的意义,实际应用中也表现巨大优势,所以应用范围不断推广。
催化剂是实验效果加强的关键,所以要提高制成的二甲醚产品质量,就必须加强新型催化剂的研究。
關键词:合成气一步法二甲醚产品新型催化剂一、前言二甲醚是未来发展中替代柴油等能源的较为重要的清洁能源,所以对二甲醚的研究成为适应发展较为广阔的市场需求以及可持续发展的重要措施,在使用中发挥的巨大经济效益和环境效益等。
文章就当下的二甲醚现状进行分析,就其中的催化剂重要性以及发展进行分析,得出相关的研究成果。
二、合成气一步法二甲醚催化剂的研究进展现状二甲醚不仅是一种重要的化工原料,也是在未来能源领域中可以替代当下应用较为广泛的柴油和天然气等作为清洁能源的燃料。
一方面由于能在对流程中快速溶解,不会对臭氧层造成伤害,另一方也是作为替代能源有许多突出的优势,所以国内外的消费需求都在进一步上升。
二甲醚燃烧之后生成的炭粒较少,允许在较大量的环境中进行废气循环,燃烧时的热量值等效益也较大。
当下已经应用或是正在开发的二甲醚的生产方法主要是由甲醇脱水来制取的二步法和用合成气直接合成的一步法。
应用较为广泛的是二步法,但是一步法发展的速度较为迅速,应用的范围不断推广。
相较于甲醇气相催化脱水二步法支撑的二甲醚,一步法的二甲醚制造技术有流程短以及能耗低等问题,在具体的实验中也有较高的单程转换率。
合成气一步法主要是指采用合成甲醇与甲醇脱水双功能催化剂将合成的甲醇与甲醇脱水二个反应放在一个反应器中进行,减少了步骤转换之间需要浪费的原料和实践,也就是一步法相较之下的优点。
一步法应用是否能够成功的关键便是双功能催化剂的开发成败,因为对社会发展的重要作用,对合成气一步法制二甲醚的催化剂研究重点集中在添加剂种类以及催化剂的改性基础上,在实际应用中也取得较为显著的成就。
合成气一步法合成二甲醚催化剂的研究

合成气一步法合成二甲醚催化剂的研究
近年来,二甲醚(DME)作为新兴能源,在燃料和化工工业中有着重要的地位。
然而,由于不可逆转的化学反应给它的合成带来了挑战,因此,研究开发合成二甲醚催化剂已成为许多科学家研究的重点。
在此背景下,本文旨在研究一种新型的合成二甲醚催化剂以一步法合成二甲醚催化剂。
【催化剂的种类】
催化剂可分为两类:一类是过渡金属催化剂,另一类是非过渡金属催化剂。
过渡金属催化剂通常由铜、铁、钴、钼、银等金属离子组成,具有较高的活性和选择性。
非过渡金属催化剂包括碱金属催化剂和有机催化剂。
由于其应用范围广泛,非过渡金属催化剂在研究二甲醚合成方面具有重要的地位。
【催化剂的制备】
以一步法合成二甲醚催化剂的关键步骤是构建催化剂核心结构。
过渡金属催化剂的构建主要通过采用无机-有机杂化的方法来实现;而非过渡金属催化剂的构建可以通过采用碱金属掺杂、聚合物掺杂和有机掺杂等方法来实现。
在构建催化剂核心结构之后,下一步是表面改性,主要是为了增加催化剂的活性和选择性,以提高催化剂的性能。
【催化剂的测试】
经过上述步骤后,以一步法合成的二甲醚催化剂将进入性能测试阶段。
研究人员将催化剂接种到反应槽中,然后通过调节反应条件,如反应温度、催化剂投加量、气体流量等等,来确定催化剂的活性和
选择性。
如果催化剂的效果达到研究人员的要求,就可以将其投入应用。
【结论】
以一步法合成二甲醚催化剂是一项极具挑战性的研究工作,需要研究者从多个方面全面研究。
在此基础上,此项研究的成果将对燃料和化学工业的发展具有重要的意义。
工艺条件对甲醇脱水制二甲醚反应的影响

2015年2月第23卷第2期 工业催化INDUSTRIALCATALYSIS Feb.2015Vol.23 No.2能源化工与催化收稿日期:2014-10-20作者简介:赵国良,1973年生,男,湖南省华容县人,博士,高级工程师,从事工业催化剂开发工作。
通讯联系人:杨为民,男,教授级高级工程师。
工艺条件对甲醇脱水制二甲醚反应的影响赵国良,滕加伟,金文清,何万仁,徐建军,杨为民(中国石油化工股份有限公司上海石油化工研究院,上海201208)摘 要:以La改性氧化铝为催化剂,在模拟绝热固定床反应器中考察工艺条件对甲醇气相脱水制二甲醚反应的影响。
结果表明,甲醇进料温度210℃时,甲醇脱水反应剧烈,绝热温升约130℃。
催化剂床层热点温度低于380℃时,二甲醚选择性大于98%,过高温度产生大量副产物甲烷。
反应压力对反应影响甚微。
在甲醇进料温度240℃(热点温度370℃)、甲醇进料空速1.5h-1和反应系统压力为50kPa条件下,甲醇转化率大于84%,二甲醚选择性大于98.5%,连续运转2000h,催化剂无明显失活迹象。
关键词:催化剂工程;二甲醚;甲醇;La/Al2O3催化剂;脱水反应doi:10.3969/j.issn.1008 1143.2015.02.013中图分类号:TQ223.2+4;TQ426.94 文献标识码:A 文章编号:1008 1143(2015)02 0143 04InfluenceofprocessconditionsonmethanoldehydrationtodimethyletherZhaoGuoliang,TengJiawei,JinWenqing,HeWanren,XuJianjun,YangWeimin(SinopecShanghaiResearchInstituteofPetrochemicalTechnology,Shanghai201208,China)Abstract:Theprocessconditionsofmethanoldehydrationtodimethylether(DME)onLa/Al2O3catalystwasinvestigatedinasimulatedadiabaticfixed bedreactor.Theresultsindicatedthatmethanoldehydrationreactionwasviolentandtheadiabatictemperaturerisewasabout130℃whenmethanolinlettemperaturewas210℃.TheselectivitytoDMEwasover98%whenthehighestcatalystbedtemperaturewaslessthan380℃.Excessivelyhightemperatureresultedintheformationofalotofbyproductmethane.Reactionpres surehadlittleinfluenceonmethanoldehydrationreaction.Undertheconditionofmethanolinlettemperature240℃(thehighestcatalystbedtemperature370℃),methanolspacevelocity1.5h-1,reactionpressure50kPa,methanolconversionofover84%andtheselectivitytoDMEofmorethan98.5%wereattained.ThecatalyticactivityofLa/Al2O3catalystdidnotexhibitobviouschangeafterrunningfor2000h.Keywords:catalystengineering;dimethylether;methanol;La/Al2O3catalyst;dehydrationreactiondoi:10.3969/j.issn.1008 1143.2015.02.013CLCnumber:TQ223.2+4;TQ426.94 Documentcode:A ArticleID:1008 1143(2015)02 0143 04 二甲醚是柴油机燃料、动力燃料、燃料电池的燃料和石油液化气的替代品,也是合成烯烃、汽油和醋酸等非常合适的化学结构单元[1]。
固定床一步法合成二甲醚的催化剂研究

二 甲醚( i t y E h r 写为 D ) D meh l t e 简 ME 是 剂的活性和选择性 就不同 , 在诸 多种制备 二甲 计算 二 甲醚的 选 择性 和收 率 。 重 要的化 工产品 , 可以做 卤代烃的替 代品用于 醚催化 剂的方 法 中共沉 淀浸 渍法能 有效 的改 催化 剂活性 评价 实验 在气相 色谱 仪 系统 J C一1 4C气相 色谱仪 ) 、热导检 测器( HP一 气雾 剂行业 , 可替 代液化气做分散型 的民用 善 现 有双 功能 催 化 剂 中存 在的 反应 温 度 高 . ( 也 燃料 , 近年来的研究表 明二 甲醚是柴油 的合适 氧 化碳转化率或 二 甲醚选择 性低的 问题 , 具 5 8 A 炼厂 气分 析仪 ) 0 8 检测上 进行 。采用二 替 代品 , 又是 制备低碳 烯烃的 重要原料 , 因此 有反应温 度低 , 一氧 化碳 转化率 高 , 甲醚选 甲醚 合成前后碳 /氢 比恒定 以及碳 平衡计算 二 潜 在市场 的 巨大 需求 使得二 甲醚 合成的研 究 择 性 好 的 优 点 。 ‘ c0 转化率 和产 物选择 性 。
维普资讯
!
: Techn og Inovaton ol y n i Her d ai
固定床 一步法合 成= 甲醚 的催化 剂研 究
王承志 张海燕 ( 大庆石 油学院 1 3 1 ) 3 6 8 摘 要: 通过共沉淀浸渍法, 制备 出合成气一步法制二甲醚 的具有甲醇合成功能和 甲醇脱水功 能的双功 能催化剂 , 加入助剂硼酸对其进行改性, 并在 固定床连续反应器 内进行 实验 。确定 了舍硼量对催化 剂催化效果的影响 , 舍硼量增大 , 转化率。选择性呈先增大后减小的趋势 , 舍硼 0 。
一
本文采用共沉淀浸渍 法制备 DME的催化 剂, 体步骤 如下 : 铜 、锌的硝 酸盐 用去离 具 将 子水将 其配成浓度为 l o/ 地混 合硝酸盐溶 m lL 液; 将此溶液与 I l L碳 酸钠溶液 同时滴加 / mo 到 盛有 Y— , Al 的烧 杯中进行 共沉淀 浸渍 , 0 Y— , Al 的用量 符合催化 剂 中铝的含量 , 0 浸 渍前 被少量去离子水 浸润 ; 共沉淀 在不断搅拌 下进行 , 温度为 7  ̄ p 0 C, H值在 6 之 间 , ~8 由两 种溶液 的相对流速加 以控制 ; 停止加料 后继续 搅拌所 得的沉淀物并保持恒温 以老化 3 分钟 ; 0 过滤 老化 后的沉淀物并 用去离子水 洗涤 ; 将洗 涤后 的沉淀 物放入烘箱 中在 8 ~10C下干燥 0 2 ̄ 1 2小时 ; 再放 人马弗炉 中于 3 0 5 ℃下煅烧 8 小 时; 将获 得 的固体 物 用压 片机 成 型 。还 可 以 在铜 、锌混 合硝 酸盐 中加 入 硼酸 , 其催 化 使 剂 中硼的含 量为 0. % ~2 。 5 % 当制取 其他 硼酸 含量 的催 化剂 的步 骤 同 上 , 改性 二 甲醚 催化 剂 。 得 1 催化剂反应性 能评价 3 采 用流 动 固定床 管式 反应 装置 对催 化剂 进行 评价 , 将催化 剂片剂 粉碎至 2 - 0目, 04 取 5 称 重后 装入反应器 , ml 在常压下用含 H 体积 分数 5 的 H, 混 合气进行还 原 。还 原结束 % N, 后, 切入合成 气 , 缓慢升 压至 4. MPa 调整空 0 , 速至 10 - 0 0 , 别测定 2 03 0 0030h 分 6 -2 ℃时催化 剂的 活性 , 即首 先分析 进 出 口 CO 含量 , 计算 CO转化率 , 同时分析 出 口气中二 甲醚 的含量 ,
甲醇脱水制二甲醚的催化剂研究

2 3因其 具 有独 特 的一 维 孔 道结 构 和 较 强 的 表
作 者 简 介 : 虹 霞 ( 9 8一) 女 , 族 , 程 师 。 东北 石 油 大 关 17 , 满 工
以碱 性硅溶胶 、 铝酸钠 、 氧化钠 和去离子 偏 氢
水为原料 , 异丙 醇 (P 为模 板剂 , 酸调 节 总碱 iA) 硫
度, 动态合成 Z M 一 3分 子筛 。配 比为 : S 2
W S 2 : A2 3 (P : ( H一 : ( i ) W( 1 ): iA) O ) O O
学管理学院硕士研究生。电话 : 5 4 0 9—6 56 。 781 l
第 3期
关 虹霞.甲醇脱水制二 甲醚 的催化剂研究
管的恒温区, 以石英砂填充 , 隙处填 以石英棉 。 两端 间 石英砂预先 用2 N 3 N H O 酸洗 、 焙烧以除杂钝化。 甲醇 的脱 水反应 在 高 压微 反 色谱装 置 上进行 评 价 。装 置主 要 由不锈 钢 固 定 床 反应 器 ( mm X 5 4 0mm) 温 控 系 统 、 量 计 ( 量 流 量 计 和 转 、 流 质
率 为 9 . % , 甲醚 选 择 性 为 9 % 。 76 二 5 关键 词 甲醇 二 甲醚 酸性 催化剂 工 艺条 件
中图分类号 :Q 2 . T 232
文献标识码 : B
文章编号 :0 9—95 ( 00)3— 14—0 10 89 2 1 0 0 9 4
二 甲醚是 一种 用 途广 泛 的化工 产 品 , 可作 气 雾 剂 、 冷 剂 和发 泡剂 , 成低 碳 烯烃 , 是理 想 制 合 也
挤条成型合成气一步法制二甲醚双功能催化剂的研究

挤条成型合成气一步法制二甲醚双功能催化剂的研究王运风;刘宏伟;张海涛;应卫勇;房鼎业【摘要】选择Cu/Zn/Al2O3和拟薄水铝石,同时添加助剂,采用挤条法成型合成气一步法制备二甲醚的双功能催化剂,通过对催化剂进行强度测试、表征和性能评价,确定了最佳的催化剂制备条件为:Cu/Zn/Al2O3与拟薄水铝质量比1∶1,胶溶剂硝酸质量分数为4%,助挤剂质量分数柠檬酸为5%、田菁粉为2.5%,用水量与原料粉体的质量比为0.60。
在此条件下制备的催化剂,其强度可达153N/cm,在250℃、3MPa、2500mL/(g·h)的条件下,催化剂CO转化率为79.8%,二甲醚的选择性为49.1%,甲醇的选择性为15.2%。
%TheCu/Zn/Al2O3 was mixed with pseudo boehmite and extrusion assistants to prepare the shaped bi-functional catalyst for one-step synthesis of dimethyl ether from syngas by extrusion. Through strength measurement, characterization and activity tests of the shaped catalysts, the optimal extrusion shaping conditions were determined as follows: mass ratio of Cu/Zn/Al 2O3 to pseudo boehmite of 1 ∶ 1, peptizer (HNO3) mass fraction of 4%, lubricants citric acid and sesbaria cannabina powder of 5% and2.5%, respectively, and mass ratio of water to solid material of 0.60. The catalyst shaped at the optimized conditions had a strength of about153N/cm, and over it, under 250℃, 3MPa and GHSV of 1500mL/(g·h), CO conversion was 79.8% with a DME selectivity of 49.1%and a methanol selectivity of 15.2%.【期刊名称】《天然气化工》【年(卷),期】2016(041)006【总页数】6页(P1-6)【关键词】合成气;二甲醚;双功能催化剂;挤条成型【作者】王运风;刘宏伟;张海涛;应卫勇;房鼎业【作者单位】华东理工大学化工学院大型工业反应器工程教育部工程中心,化学工程联合国家重点实验室,上海 200237;华东理工大学药学院,上海 200237;华东理工大学化工学院大型工业反应器工程教育部工程中心,化学工程联合国家重点实验室,上海200237;华东理工大学化工学院大型工业反应器工程教育部工程中心,化学工程联合国家重点实验室,上海 200237;华东理工大学化工学院大型工业反应器工程教育部工程中心,化学工程联合国家重点实验室,上海 200237【正文语种】中文【中图分类】TQ426.68;TQ223.24二甲醚(DME)是现代煤化工的重要产品之一[1]。
co2加氢一步法合成二甲醚双功能催化剂

co2加氢一步法合成二甲醚双功能催化剂简介:二甲醚是一种重要的有机合成化合物,它广泛用于工业生产中,如燃料添加剂、溶剂和涂料原料等。
目前,二甲醚的生产主要依赖于甲醇脱水工艺,该工艺对原料纯度和工艺条件有较高要求,从而增加了生产成本。
本文介绍一种基于CO2加氢一步法合成二甲醚双功能催化剂的研究。
背景:CO2加氢一步法是利用CO2为碳源与氢气通过催化加氢反应生成有机化合物的方法。
这种方法具有原料易得、不污染环境和反应条件温和等优点。
内容:1. 合成双功能催化剂研究人员基于金属酸盐的复合物,成功合成了一种表面含酸性位点的纳米金属催化剂。
该催化剂既具有CO2的还原能力,也具有酸性位点的能力。
这种双功能催化剂对CO2与氢气的反应具有高效率和高选择性。
2. 优化反应工艺通过实验,研究人员优化了反应工艺,并选定甲醇和相对应的催化剂作为反应原料。
实验结果表明,当反应温度为180℃,反应压力为1.5 MPa时,反应时间为4小时,可以得到二甲醚的收率达到85%以上。
3. 催化剂的稳定性研究人员还对催化剂的稳定性进行了测试。
实验发现,在反应条件下,催化剂表面的酸性位点会随着反应时间的增加而减少,而后还原性位点的数量会增加。
但总体来说,催化剂的性能仍然较稳定,在5次反应后,仍能保持较高的活性和选择性。
结论:本研究成功合成了一种双功能催化剂,用于CO2加氢一步法合成二甲醚,实验结果表明,在优化的反应工艺下,可以得到高收率的二甲醚产物。
该研究为二甲醚的生产提供了一种新的、成本更低、环境更友好的工艺,具有极大的应用潜力。
合成气在有机化工生产中的利用方法研究

合成气在有机化工生产中的利用方法研究摘要:有机化工工业的发展,使得合成气成为了有机化工生产中不可或缺的原料。
它越来越多地走进了人们的生产及生活中。
笔者就合成气在发展方向上,各种生产技术的使用进行了比较,并结合实际生产经验进行了分析、总结,以说明合成气在未来有机化工生产中的重要作用,并为合成气及产品的深加工提供了重要依据。
关键词:合成气;甲醇;乙二醚引言通常以一氧化碳及氢气为主要成分的气体混合物被称为合成气。
它最先使用煤炭制取,后来又以天然气及重油等气态及液态原料制取。
由于其活性较高,成为了有机化工生产中不可或缺的原料。
很多由合成气生产的有机化工产品在人们的生产生活中得到了普及。
1合成气一步法制取二甲醚生产技术二甲醚(DME)是一种无色、无毒、环境友好的重要清洁能源,被广泛用作制冷剂、气雾剂以及有机化工中间体,另外合成气在制药、农药、燃料等许多行业有重要用途,它具有较高的十六烷值,良好的燃烧性能,含氧量高,作为柴油和无硫排放。
的理想替代燃料在燃烧过程中可实现低NOx1.1一步法合成二甲醚的反应原理合成气一步法制二甲醚生产技术是将两步反应集中在一个反应器中进行,生成的甲醇可直接脱水为二甲醚。
与两步法相比,一步法可使合成气中CO的单程转化率提高50%以上,且操作更方便。
另外,由于原料为合成气,因而避免了两步法中二甲醚价格随甲醇价格的波动而波动。
甲醇合成反应:CO+2H2→CH3OH+90.4kJ/mol (1)甲醇脱水反应:2CH3OH→CH3OCH3+H2O+23.4KJ/mol (2)水气转换反应:CO+H2O→CO2+H2+41.9KJ/mol (3)采用一步法时,反应式(1)中生成的CH3OH可以由反应式(2)立即转化为二甲醚;反应式(2)中生成的H2O又可被反应式(3)消耗;反应式(3)中生成的H2又作为原料参与到反应式(1)中。
三个反应相互促进,从而提高了CO的转化率。
1.2催化剂的选择在合成气一步法制二甲醚生产中,采用由甲醇合成催化剂和甲醇脱水催化剂复合而成的双功能催化剂是现阶段催化效果比较理想的催化剂之一。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
然后将其压片破碎后筛选 20 ~ 40 目的颗粒, 为便
于催化剂成型, 在成型时加入质量分数为 1%的石
墨。
1.2 催化剂表征
1.2.1 X 射线衍射(XRD)表征
X 射 线 衍 射 表 征 在 DX-1000 仪 器 上 进 行 , 以
Cu Kα (λ= 0.15406 nm)为辐射源,管电压 40 kV,管 电流 25 mA,采用石墨单色器滤光。 扫描范围为 10°
(2)
H2O + CO → H2 + CO2
(3)
从以上 3 个反应式可以看出式(1)生成的甲醇是式
收稿日期:2008-07-22;基 金 项 目 :“十 一 五 ”国 家 科 技 支 撑 计 划, 非石油路线制备大宗化学品关键技术开发 (2006BAE02B02);作者简介:李扬(1982-),男 ,工 程 师 ,电 话 028-85964833,电邮 boyliyang@。
TDX-01 填 充 柱 分 析 尾 气 中 的 N2,CO,CH4,CO2; 用 PEG-1540/407 有 机 担 体 填 充 柱 分 析 DME,CH3OH
及烃类产物,反应稳定 3 h 后开始分析。采用外标法
以碳原子的摩尔数计算 CO 转化率和产物选择性,
计算公式如下:
conv(CO)%= (nCO )0 -nCO ×100% (nCO )0
第 5 期 李 扬等:合成气一步法制二甲醚双功能催化剂中甲醇脱水组分对催化性能的影响
45
合成气一步法制二甲醚双功能催化剂中 甲醇脱水组分对催化性能的影响
李 扬,王 莉,艾 珍,吴砚会
(西南化工研究设计院 国家碳一化学工程技术研究中心 工业排放气综合利用国家重点实验室,成都 610225)
摘要:采用并流共沉淀法制备的甲醇合成 CuO-ZnO-Al2O3 催化剂与不同甲醇脱水组分混合制成合成气一步法制二甲醚双
关键词:合成气;二甲醚直接合成;甲醇脱水催化剂;双功能催化剂
中 图 分 类 号 :O643.36
文 献 标 识 Байду номын сангаас :A
文 章 编 号 :1001-9219 (2008 )05-45-05
随着石油资源的日益枯竭, 以合 成 气 (CO +
H2)为原料 合 成 甲 醇 、二 甲 醚 及 其 它 碳 氢 化 合 物 等 燃料越来越受到各国的研究人员的重视[1]。 其中二
表1 Table 1
不同甲醇脱水组分对合成气一步法制二甲醚催 化性能的影响 Effect of different dehydration components on the direct synthesis of DME from syngas
Catalysts
CO conv.
Selectivity /%
功能催化剂,并在高压固定床反应器评价其催化性能。 发现以西南化工研究设计院自主研制的甲醇脱水制二甲醚催化剂(改性
的 γ-Al2O3)为脱水组分时表现出最佳的催化性能。 NH3-TPD 研究表明改性后的 γ-Al2O3 表面酸量和酸强度都有所增加,且在双
功能催化剂表面同时存在着弱酸中心和中等强度的酸中心。
对于甲醇合成催化剂,研究表明催化剂合成过 程中的具有水滑石结构的 Cu-Zn-Al 所形成铜小簇 是合成气制甲醇的关键[9, 12, 13]。 对于甲醇脱水制二甲 醚的研究认为其是一个酸催化反应,目前研究较多 的集中在固体酸催化剂上,如 γ-Al2O3 和 HZSM-5 分 子筛。 Li 等人[11]研究表明,在 550 ℃下焙烧所制得 的 γ-Al2O3 对于甲醇脱水制二甲醚有较高的催化活 性。 而 HZSM-5 分子筛中的强酸中心,可以使产物 进一步脱水生产其它碳氢化合物,从而降低二甲醚 选择性[14]。 本文主要考察了不同甲醇脱水组分,如各 种 γ-Al2O3 和 HZSM-5,在双功能催化剂中对合成气 一步法制二甲醚反应性能的影响,并对催化剂进行 了 XRD 和 NH3-TPD 表征。
~ 80°。
1.2.2 氨程序升温脱附(NH3-TPD)表征
样品的酸性采用氨程序升温脱附法在美国康
塔公司的 ChemBET 3000 化学吸附仪上测定。 首先
将称取 0.15 g 样品,以高纯 He 为载气,按 10℃/min
升温至 550℃,在此温度下处理 60 min。 然后冷却至
120℃下吸附 NH3 至饱和。 再用高纯 He 在 120 ℃吹 扫以除去物理吸附的 NH3 后, 以 10 ℃/min 升温至
×100%
2 结果与讨论
2.1 不同脱水组分对催化性能的影响 首 先 固 定 甲 醇 合 成 组 分 为 CuO-ZnO-Al2O3,考
察不同甲醇脱水组分对反应性能的影响,结果见表 1。 从表 1 中可以看出选用的两种 HZSM-5 作为甲 醇脱水组分时,DME 选择性几乎为零, 产物主要为 CO2 和低碳烃。 这可能和 HZSM-5 自身酸性较强,导 致 DME 进一步脱水生成烃类物质[14]。 同样在以 γAl2O3-g 作为甲醇脱水组分时,主要生成 CO2 和低碳 烃。 而如果改用 γ-Al2O3 原粉为甲醇脱水组分时,在 275 ℃时,CO 的转化率可以达到 77.1%,DME 的选 择性也较以 γ-Al2O3-g 为甲醇脱水组分时有显著提 高。 而用西南化工研究设计院自主研发的甲醇脱水 制二甲醚工业催化剂 γ-Al2O3-c 为双功能催化剂脱 水组分时,DME 选择性可以达到 46.3%, 其在有机 产物中的选择性可以达到 71.1%。 并且相比于其它 4 组催化剂, 产物中低碳烃的含量明显减少, 仅为 3%。 以上结果表明,以 γ-Al2O3-c 为甲醇脱水组分时 催化剂的催化性能最佳。
甲醚 (DME)作 为 一 种 优 质 无 硫 的 燃 料 具 有 低 NOx
排放,燃烧无烟,可以降低发动机噪音等性质,因此
可以替代柴油和液化石油气作为车用燃料和民用
燃料;并且与传统的氟利昂(CFCs)相比,用二甲 醚
作为气溶胶喷射剂和制冷剂更有利于环境保护 。 [1-4]
此外,二甲醚还可以作为非石油路线合成低碳烯烃
77.1 26.8 22.4 41.7 4.5 2.4 2.2
46.0
Cu-Zn-Al/ -Al2O3-g
33.2 0.12 22.1 50.0 10.6 8.8 8.4
0.24
Cu-Zn-Al/ -Al2O3-c
72.6 46.3 15.8 34.8 1.9 1.1 0
71.1
Reaction conditions: T =275℃ ; P =5.0MPa; GHSV =1500 h-1;
Cu-Mn-Zn 等)与甲醇脱水催化剂(如 γ-Al2O3、HZSM5、HY、SAPO 等)按一定方式混合后,可由合成气直
接制取二甲醚[3, 4, 。 8-10] 该过程主要包括甲醇合成,甲醇
脱水以及水煤气变换 3 个反应(见式 1 ~ 3):
2CO + 4H2 → 2CH3OH
(1)
2CH3OH → CH3OCH3 + H2O
后,将沉淀 A 和 B 混合,然后加入甲醇脱水组分,主
要选用 HZSM-5(上海和南开大学生产的,分别记作
HZSM-5-sh 和 HZSM-5-nk),西南化工研究设计院自
主研发的甲醇脱水制二甲醚工业催化剂 γ-Al2O3(记 作 γ-Al2O3-c)、工 业 级 干 燥 剂 γ-Al2O3(记 作 γ-Al2O3g)和 γ-Al2O3 原粉。 混合完毕后继续老化 1 h。 经过 滤、洗涤和干燥后,在 380 ℃空 气 气 氛 中 焙 烧 4 h。
1 实验部分
1.1 催化剂的制备 首先将一定量的 Zn(NO3)2 和 Al(NO3)3 溶于水配
成 Zn-Al 混合溶液,将一定量的 Cu(NO3)2 和 Zn(NO3)2 溶于水配成 Cu-Zn 混合溶液,然后将此两份溶液分
46
天然气化工
2008 年第 33 卷
别与 Na2CO3 溶液在 70 ℃左右并流共沉淀, 得到的 沉淀分别记做沉淀 A 和 沉 淀 B。 沉 淀 老 化 45 min
650 ℃并用 TCD 记录脱附出来的 NH3。 1.3 催化剂反应性能评价
采用高压流动固定床不锈钢反应器评价催化
剂的性能。 催化剂装填量为 4 mL,反应前用 φ(H2)为 3%的 H2-N2 混合气在 240 ℃还原 10 h。 还原完毕后
切 换 成 合 成 气 ( 体 积 组 成 :H2 64% ,CO 28% ,CO2 6%,N2 2%),气体流速通过质量流量计控制。 反应 尾气用 SC-1001 气相色谱仪, 以 TCD 为检测器,用
第 5 期 李 扬等:合成气一步法制二甲醚双功能催化剂中甲醇脱水组分对催化性能的影响
47
增 , 当 温 度 高 于 265℃ 后 ,CO 转 化 率 基 本 维 持 在 70%左右。随着温度升高,产物中甲醇的选择性呈递 减趋势, 说明升高温度有利于甲醇脱水反应的进 行。 随着甲醇选择性降低,相应 DME 和 CO2 选择性 显著增加, 而当温度升高到 285 ℃后,DME 选择性 不再增加,反而有所下降,而此时低碳烃的选择性 增加显著。 因为甲醇脱水生成二甲醚是一个放热反 应,受到热力学的限制,升高温度不利于二甲醚的 生成。 因此,综合考虑 CO 转化率以及 DME 的选择 性,较为适宜反应温度为 265 ℃ ~ 275 ℃之间。
select(DME)%=
2×nDMS
×100%
2×nDMS +nCH3 OH +nCO2 +m×nCm Hn
select(CH3OH)%=
nCH3 OH 2×nDMS +nCH3 OH +nCO2 +m×nCm Hn
×100%
select(CmHn)%=
