2017[中学联盟]江苏省江阴市成化高级中学高中化学必修一镁的提取与应用 修改稿.doc
高中化学《镁的提取及应用》教案1 苏教版必修

高中化学《镁的提取及应用》教案1 苏教版必修01一、学习目标1 通过对海水中提取镁的过程的讨论,掌握其中的反应原理和生产流程2了解镁的物理性质,掌握镁的化学性质二、重点、难点1 设计从海水中提取镁的工业流程图2了解并掌握镁的化学性质三、预习导引一、镁的提取参照书本 P55,图2-12 设计从海水中提取镁的流程图:1提取镁的工业流程:2 书写流程图中涉及到的化学方程式,若是离子反应,则写出离子反应方程式:(1)利用贝壳制取石灰乳:________________________________,________________________________ 。
(2)沉淀 Mg2 :_____________________________________________________ ____。
(3)提取 MgCl2:_____________________________________________________ ___。
(4)制取金属镁:_____________________________________________________ ____。
二、镁3、写出镁的原子结构示意图:4 实验,观察实验现象并记录,写出相应的化学反应方程式:与 CO2反应:(1)现象:(2)化学方程式:与 N2反应:(1)现象:(2)化学方程式:与酸反应:(1)现象:(2)离子方程式:三、镁的用途(自学)1 __________制造飞机、火箭和导弹的部件等。
2制造信号弹和焰火。
3氧化镁是优质的耐高温材料。
四、精讲点拨1 海水中含的 MgCl2 是镁的重要来源之一。
从海水中提取镁可按如下步骤进行:把贝壳制成石灰乳;在引入的海水中加入石灰乳,沉降、过滤,洗涤沉淀物;将沉淀物与盐酸反应,结晶、过滤、干燥产物;将产物熔融后电解。
下列说法中不正确的是 ( ) A此法优点之一是原料的来源丰富 B进行步的目的是从海水中提取 MgCl2 C第步中电解时会产生氯气 D以上提镁过程中涉及到的反应有复分解反应、化合反应和置换反应2下列化学反应,在从海水中提取镁的过程中不会涉及的是 ( )A Mg22OH ===Mg(OH)2B Mg(OH)22HCl===MgCl22H2O CMg(OH)2===== MgO H2O D MgCl2(熔融 )=====通电 Mg Cl23从海水中提取镁的工艺流程主体是 ( )A海水 NaOH Mg(OH)2 电解 Mg B海水熟石灰 Mg(OH)2 HCl MgCl2 电解 Mg C海水 HCl MgCl2 电解 Mg D 海水 Cl2 MgCl2 电解 Mg五、典题训练【同步训练】( )1镁着火时,可用于灭火的物质是 A干冰 B氮气 C水 D黄沙 ( )2将一小块钠投入下列溶液中,既能产生气体,又能生成白色沉淀的是 A稀硫酸 B氢氧化钠 C硫酸铜 D氯化镁 ( )3下列关于镁的叙述中,不正确的是 A在空气中燃烧时发出燿眼的白光 B由于镁能跟空气中的氧气反应,所以必须密封保存C能跟盐酸反应放出氢气 D镁合金密度小但强度大,大量用于制造火箭、飞机等部件 ( )4下列各种冶炼方法中,可制得相应金属的为 A加热氧化镁B加热碳酸钙 C电解熔融氯化镁 D氯化钠与铝粉高温共热六、归纳小结七、当堂检测选择题 ( )1下列关于镁和钠的比较结论正确的是 A铝镁合金的硬度较大,钠钾合金的硬度较小 B因为钠的金属性比镁要强,所以钠的熔点比镁要高 C镁能置换硫酸铜溶液中的铜,钠也能置换硫酸铜溶液中的铜 D在空气中都能被点燃,生成的产物都是氧化物 ( ) 2下列反应中镁元素被氧化是 A MgCO3=====高温 MgO CO2 B Mg(OH)22H ===Mg22H2O C Mg2HCl===MgCl2 H2 D Mg22OH===Mg(OH)2 ( )3镁条在空气中燃烧后,其生成物中可能含有的物质是 A MgCO3、 MgO、 Mg3N2 B Mg(OH)2、 MgO、 MgCO3 C MgO、 Mg3N2、 C D Mg3N2、C、 MgCO3 ( )4 下列离子方程式正确的是 A 氢氧化钡溶液与盐酸的反应:OH H === H2O B 澄清的石灰水与稀盐酸反应:Ca(OH)22H === Ca22H2O C 氢氧化镁与稀硫酸反应:H OH === H2O D 碳酸钠溶液与盐酸反应:Na2CO3 H ===2Na H2O CO2 八、作业布置校本作业物质的量(第一课时), P5-P6。
高一化学苏教版必修一2-2-4镁的提取及应用

与氧化物反应 与盐溶液反应
Mg+Cu2+===Mg2++Cu
自主探究
精要解读
实验探究
2. 镁的燃烧反应
由于金属镁的化学性质十分活泼,在空气中可以与氧气、二 点燃 氧化碳以及氮气反应。反应方程式如下:2Mg+O2 ===== 点燃 点燃 2MgO; 3Mg+N2=====Mg3N2; 2Mg+CO2=====2MgO+C。
提示 氧化镁的熔点很高,消耗的能量较多。
自主探究
精要解读
实验探究
【慎思5】 氮气和二氧化碳都不助燃吗?
提示 错误。从镁的化学性质来看,镁可以在氮气、二氧
化碳中燃烧,所以氮气、二氧化碳也可以助燃。
自主探究
精要解读
实验探究
要点一
|
从海水中提取镁
自主探究
精要解读
实验探究
【例1】► 由海水制备无水氯化镁,主要有以下步骤:①在一定 条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓 缩结晶。其先后顺序正确的是 ( )。
自主探究
精要解读
实验探究
【慎思1】 从镁的化学性质来看,在化学反应中镁原子的变化
特点是什么?
提示 镁原子失去最外层的两个电子,达到稳定结构,形 成Mg2+。
自主探究
精要解读
实验探究
【慎思2】 将石灰乳加入海水中得到Mg(OH)2沉淀的反应能否
用离子方程式Mg2++2OH-===Mg(OH)2↓来表示?
ห้องสมุดไป่ตู้答案
C
自主探究
精要解读
实验探究
要点二
|
镁的性质
镁的化学性质 1. 性质 举例 与O2反应 与N2反应 反应方程式
点燃 2Mg+O2=====2MgO 点燃 3Mg+N2=====Mg3N2
苏教版高一化学教案-镁的提取与应用

第2單元課時4鎂的提取與應用教學設計一、學習目標1.掌握鎂的化學性質。
2.通過制取鎂的生產流程,進一步學習從經濟角度、綠色化學角度考慮問題的方法;3.通過海水中化學資源的進一步開發和鎂的用途介紹,將化學理論學習和工業生產、生活相結合,提高開發海洋資源的興趣和探索精神,在進一步感悟到人類在享受大自然賦予的財富的同時,應該樹立環保責任意識,感悟人與自然和諧相處的重要性。
二、教學重點及難點重點:鎂的化學性質;從海水中提取鎂的步驟和原理。
難點:從海水中提取鎂的原理;鎂的化學性質。
三、設計思路通過複習海水中含有的主要鹽類引出本節課要研究的主題:通過理論分析與資料閱讀解決怎樣從海水中提取氯化鎂和怎樣將氯化鎂轉換為金屬鎂兩個主要問題,通過實驗探究認識金屬鎂的性質和用途。
四、教學過程[情景導入]我們已經知道如何從海水中提取氯、溴、碘的單質,這些物質的製備都依賴於從海水中提取的氯化鈉,我們來回顧一下海水中含有的主要四種鹽類,濃度僅次於氯化鈉的是氯化鎂,從海水中提取氯化鈉後所得的母液中,氯化鎂的濃度較高,那我們怎樣將儲量巨大的氯化鎂從海水中提取出來呢?(ppt2~3)[思考與討論]氯化鎂可以用來制取生產、生活中需求量很大的金屬鎂,怎樣從海水中提取氯化鎂?怎樣將氯化鎂變成我們需要的金屬鎂?[閱讀與討論]閱讀書本P55~56有關鎂的提取過程的原理和流程,解決諸如下列問題:1.工廠為何建在海邊?2.為何不用氫氧化鈉來沉澱鎂離子?3.“中和”操作中處理的是“過濾”後的濾液,還是沉澱?[板書]一、鎂的提取原理(ppt4~6)CaCO3CaO+CO2↑CaO+H2O=Ca(OH)2MgCl2+2Ca(OH)2=Mg(OH)2↓+CaCl2Mg(OH)2+2HCl=MgCl2+2H2OMgCl2Mg+Cl2↑[練習]寫出前生成氫氧化鎂和氯化鎂兩個化學反應的離子方程式。
[過渡]煙火的圖片,制得的金屬鎂有哪些性質,可以有哪些用途呢?(ppt7~8)[演示實驗]通過P56的“觀察與思考”中的實驗,以及鎂帶在氮氣和二氧化碳氣體中燃燒的反應錄影,學生觀察反應現象,歸納鎂的性質。
《镁的提取及应用》教案.docx

镁的提取及应用(苏教版2009年6月第5版)丁浩江苏省梁丰高级屮学一、课程标准、教材分析及学生分析【课程标准】1.了解海水小盐类的开发和利用,《镁的提取及应用》是继食盐资源的利用、氯、澳的提取后的又一单元,有利于学生了解海水综合利用的一般原理和流程;2.以自然资源海水中提取镁,了解化学方法在实现物质间转化中的作用。
【教材分析】1.木专题是《必修1》专题2从海水屮获得的物质,涉及了非金属氯、澡、碘和金属钠、镁的提取,为专题3从矿物到基础材料的学习打下基础。
2.在本节内容Z前已经学习了离子反应和简单的离子方程式,从海水中提取镁的原理可以从离了反应的角度分析相关反应,清楚转化过程;3.通过海水的综合利用,有利于学牛了解物质的循坏利川和综合效益;【学牛分析】1.在海水中提取钱Z前已经学习了海水中氯、澳的提取,学生对海水中提取物质的一般过程有了一定的了解;2.学牛已经学习了Fe、Cu、Na等金属的制备,掌握了常见金属的制备方法;3.学牛己经学过了离子反应,所以在本节内容中,主要通过离子反应來表示海水屮提取镁的基木原理;4.作为四星级高中,连云港高级中学的生源在木地区处于比较优质的水平,学生冇综合运用知识的可能和能力。
二、教学目标【知识与技能】1.了解从海水小提取镁的基本原理和流程,认识工业住产的基本方法和思路;2.了解镁在社会生产、生活实际中广泛用途,能列举合金材料的重要作用;3.掌握镁单质及其化合物的性质;4.认识到开发海水屮的化学资源的重耍性与必耍性。
【过程与方法】1.通过讨论、交流发现问题和解决问题,体验合作学习的乐趣;2.通过角色扮演(企业家、工艺设计师、政府部门工作人员),对从海水中提収镁工业流程的依据和方法有所了解,体会从自然界获得人类所需要物质的一般思路;3.通过将Mg?+转化为镁进行富集、分离、转化的过程,体会转化的方法在物质分离中的应用,并运用所学的化学知识对化工生产流程的原理、步骤进行简单的解释。
苏教版高中化学必修一《镁的提取及应用》【创新教案】2

第二单元钠、镁及其化合物镁的提取及应用一、教学目标:(一)知识技能:了解镁的提取及物理性质,掌握镁的原子结构和化学性质。
(二)过程方法:通过交流与讨论,理解海水提镁的原理与过程,了解化学实验与化工生产的区别。
通过实验探究培养学生观察能力、分析问题和解决问题的能力。
(三)情感态度与价值观:通过介绍镁的提取,培养学生勇于探索的科学精神和严格求实的科学态度。
通过镁在二氧化碳气体中燃烧的实验,提高化学学习兴趣。
二、教学难、重点:重点:提取镁的化学原理,镁的化学性质难点:提取镁的化学原理三、教学工具仪器:试管坩埚钳酒精灯火柴砂纸药品:镁条盐酸水酚酞一集气瓶CO2四、教学方法:设疑讨论、实验探究、归纳总结五、课时安排:一课时六、教学过程:[引入]海水中含有大量的镁离子,镁及其合金的用途十分广泛,我们这节课就来探索如何从海水中提取镁。
[板书]一、镁的提取[思考]海水中含有大量的NaCl、MgCl2、CaCl2、KCl等氯化物,但每千克海水中氯化镁只含约5.11g,如果直接从氯化镁中提取到镁有无实际意义,如何解决面临的困难?[讨论]数据分析海水中的Mg2+ 的浓度很小,必须让海水中镁离子的富集。
可以加入一种试剂使Mg2+ 沉淀,如氢氧化钠、氢氧化钙等.[追问]是不是直接往海水中加沉淀剂?[讲述]不是,因为海水中的Mg2+ 的浓度很小,直接加沉淀剂不利于Mg2+ 的沉淀,而且会增大沉淀剂的用量,我们可以先将海水浓缩,再加沉淀剂。
[追问]从综合角度考虑选用哪种试剂作沉淀剂好?为什么?[讲述]因为海边有丰富的贝壳,可用来制得Ca(OH)2,从原料来源以及经济等综合角度考虑选用Ca(OH)2试剂作沉淀剂好。
[思考]如何由贝壳制得氢氧化钙?写出化学方程式。
[讲述]贝壳(CaCO3)→CaO→Ca(OH)2[投影]教材P55图2-15从海水中提取镁的流程。
[提问]由MgCl2到Mg究竟用还原法还是电解法好?[启发]回顾工业如何获得金属钠。
苏教版高中化学必修一2.2《镁的提取及应用》参考课件 (共43张PPT)

镁 是 比 较 活 泼 的 金 属
(1)与O2等非金属单质反应
(2)与CO2反应 (3)与H2O反应
2MgO 点燃 3Mg+N2 Mg3N2 点燃 2Mg+CO2 2MgO+C 点燃 Mg+2H2O Mg(OH)2+H2↑
2Mg+O2
(4)与酸反应
Mg+2H+
Mg2++H2↑
(5)与盐溶液反应(置换较不活泼的金属) Mg +Cu2+ ====Mg2++Cu
MgCl2·6H2O晶体在HCl气氛中加热脱水即可得无水 MgCl2
一、镁的常见工业制法——电解法 流程: 海水 Mg(OH)2 过滤 Mg(OH)2 盐酸 石灰乳 MgCl2溶液 HCl Cl2 干燥 Mg 电解 MgCl2
贝壳
煅烧
水
蒸发 结晶
MgCl2·6H2O
CaO
思考:电解产生的Cl2怎么处理? 请写出上述过程中所涉及到的化学方程式
镁在二氧化碳中燃烧
现象:
1、剧烈燃烧,发出耀眼的白光,伴有白烟,在瓶的内
壁有黑色的固体生成
【实验与探究】
实验1、取一根打磨好的镁条,用坩埚钳夹住,在酒精灯 上点燃,伸入盛有二氧化碳气体的集气瓶。观察现象。
实验2、从广口试剂瓶中取2条打磨好的镁条放入一支试
管,加入少量水,滴入2~3滴酚酞,加热煮沸。观察现 象。 实验3、取一小段除去氧化膜的镁条投入盛有一定量稀盐 酸的试管中。
点燃
4、与非氧化性酸反应:稀H2SO4、稀HCl、H3PO4 Mg+2H+====Mg2++H2↑ 与氧化性酸发生复杂的反应(HNO3、浓H2SO4) 5、与盐溶液反应(置换较不活泼的金属) Mg +Cu2+ ==== Mg2++Cu
江苏省江阴市成化高级中学高中化学物质的分离和提纯教

物质的分离和提纯教案(修改稿)知识与技能:1.初步学会过滤、结晶、萃取、分液、蒸馏等分离物质的实验技能,能独立完成一些简单的物质分离、提纯的实验操作,初步学会设计简单的实验方案。
2.学会Cl-、SO42-、CO32-、NH4+等离子检验的实验技能,能用焰色反应法、离子检验法设计简单的实验方案探究某些常见物质的组成成分。
过程与方法:初步了解根据混合物的性质,选择不同的分离方法对物质进行分离的实验法。
情感态度与价值观:结合实际事例讨论遵守实验安全守则的重要性。
树立安全意识,初步形成良好的实验工作习惯。
教学重点及难点:分离物质等基本实验技能;Cl-、SO42-、CO32-、NH4+等离子检验;设计简单的实验方案。
设计思路:本课重点在于引发学生的思考,通过学生自己动手实验,让他们体验实验在化学学习中的重要作用,初步了解实验方案的设计。
教学过程:[导入](展示一个有过滤网的茶杯)让我们继续用化学家的眼光来观察我们周围的物质世界,这个茶杯比普通茶杯多了一个金属网,其作用是什么?在泡茶时茶叶中能溶于水的成分形成了茶叶水,为饮用方便,我们加了一个金属网,实现茶叶和茶水的分离。
[板书]一、物质的分离与提纯1、过滤:分离难溶性固体与液体的混合物上面分离方法就是我们曾经学习过的——过滤,哪种混合物可以通过过滤的方法加以分离?用这个金属网能将化学反应生成的沉淀和溶液分开吗?实验室使用的滤纸必然具有一些——小孔,其大小刚好能使溶液通过,而留下沉淀。
为了保证过滤的效果和速率,实验操作中我们应该注意哪些问题?[过渡] 我们所接触到的物质往往是混合物,化学上要研究一种物质的性质,首先需要将其中各组分分离开来,以实现物质的提纯。
[设问]分离与提纯,两者之间有什么区别吗?分离是通过适当的方法,把混合物中的几种物质分开(每一组分都要保留下来,且与原状态相同)的过程。
提纯通过一定途径获取混合物中的主要成分的过程。
[讨论1] 现有含MgCl2和泥沙的粗食盐,请设计实验方案,由粗食盐提纯NaCl。
江苏省江阴市峭岐中学高中化学必修一专题二第2单元 课时4 镁的提取与应用 学案(无答案)
镁的提取及应用
一、镁的存在及用途
1、镁主要以化合态存在于地壳和海水(MgCl 2)中,海水中镁的总储量约为1.8×1015
t 。
2、 用于火箭、导弹和飞机等制造业,誉为“国防金属”。
是植物叶绿素组成成分
3、 能维护心肌功能和冠状动脉弹性,有“心脏保护神”的美称。
4、镁可用来制造信号弹、烟火、制药。
熔点高,制耐高温材料。
二、镁的提取
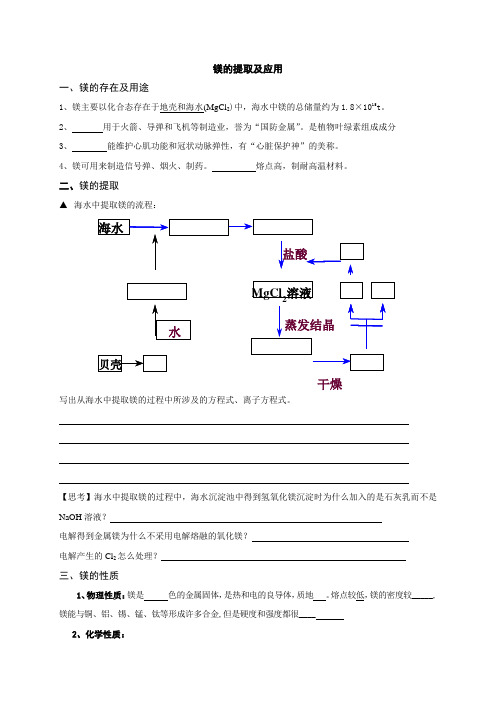
▲ 海水中提取镁的流程:
写出从海水中提取镁的过程中所涉及的方程式、离子方程式。
【思考】海水中提取镁的过程中,海水沉淀池中得到氢氧化镁沉淀时为什么加入的是石灰乳而不是NaOH 溶液?
电解得到金属镁为什么不采用电解熔融的氧化镁? 电解产生的Cl 2怎么处理?
三、镁的性质
1、物理性质:镁是 色的金属固体,是热和电的良导体,质地 。
熔点较低,镁的密度较_____,镁能与铜、铝、锡、锰、钛等形成许多合金,但是硬度和强度都很____
2、化学性质:
MgCl 溶液 2 干燥
(1)与O2等非金属单质反应
(2)与氧化物反应
(3)与H2O反应
(4)与酸反应
(5)与盐溶液反应(置换较不活泼的金属)。
-高中化学 2.2.4《镁的提取及应用》教案 苏教版必修1【精品教案】

教学课题镁的提取及应用所用教材教材名称:苏教版高中化学第 1 册,第二章 4 节,第 1 课时课时安排一课时教学用具镁条、稀硫酸、二氧化碳、火柴、坩埚钳教学目标1、知识与技能(1)了解镁在生活中的用途、海水中镁的含量、镁的存在形式;(2)通过对海水中提取镁的过程的讨论,掌握其中的反应原理和生产流程;(3)了解镁的物理性质,掌握镁的化学性质。
2、过程与方法(1)通过阅读资料,提高从资料中提取信息,分析信息的能力;(2)通过对海水中提取镁的讨论,形成工业生产中降低成本的概念。
3、情感态度与价值观(1)了解海水的成分,认识开发利用海水这一巨大资源的重大意义,并加强珍惜保护海水资源的意识;(2)通过师生共同讨论,促进师生之间的交流。
教学重点探讨海水中提取镁的过程;镁的化学性质。
教学难点提取镁的化学原理教学方法讲授法、引导式、启发式、实验探究法用心爱心专心- 1 -板书设计镁的提取及应用一、镁的提取1.海水(Na+、Ca2+、Cl-、Mg2+)碱Ca(OH)2Mg(OH)2盐酸MgCl2通电Mg2. CaCO3高温CaO+CO2↑CaO+H2O===Ca(OH)2MgCl2 +Ca(OH)2 ===Mg(OH)2 ↓+CaCl2Mg(OH)2+2HCl=== MgCl2+H2OMgCl2 === Mg+Cl2↑二、镁的性质1.物理性质:银白色金属、质软、密度小2.化学性质:与O2反应:2Mg + O2 点燃2MgO与CO2反应:2Mg + CO2点燃2MgO + C与N2反应:3 Mg + N2点燃 Mg3N2与酸反应:Mg+H2SO4 = Mg SO4 + H2↑通电用心爱心专心- 2 -用心 爱心 专心 - 3 -教学过程及内【导入】:镁这种金属大家可能比较陌生,其实,镁在生活中的用途非常广泛,大型节日中我们放的烟花中用到镁,天上的飞机还有最常见的自行车零部件都用到了镁。
镁有这么多的用途,我们该怎么提取镁呢?【提问】前面学习过哪些金属的提取?【回答】钠。
苏教版高中化学必修一《镁的提取及应用》说课稿

《镁的提取及应用》说课稿今天我说课的题目是《镁的提取及应用》,本节内容选自普通高中课程标准实验教科书·化学1(苏教版)中专题2”从海水中获得的化学物质”中的第二单元第4课时的教学内容。
下面我将从教材、学法、教法、教学程序四个方面完成我今天的说课。
您的聆听是对我的指导,您的支持是对我的鼓励!谢谢大家!一、说教材1.本节在教材中的地位和作用“镁的提取及应用”是继学生学习了从海水中获得的化学物质——典型的非金属卤素单质及其化合物知识和典型的金属元素钠单质及其化合物知识后,学习的另一种从海水中获得的典型金属元素。
本节课仍沿袭了以海水资源为背景,通过海水资源的综合利用这一过程为知识主线,在“工业生产——性质探究——社会应用”线索下,从工业生产实际出发,依托实验探究方法,探讨了海水中提取镁的方法;海水综合利用与资源循环利用的过程,使学生在获取相关镁的化学知识和实验研究过程和方法的同时,认识到自然资源的利用与化学科学密不可分,从中体会化学为人类社会发展做出的巨大贡献,感受环境保护和经济观念带来的效益,形成学好化学能更好地造福于社会、生活的学习目标。
我认为这样的安排既有沿袭又有转换,从横纵方面加深学生对典型非金属元素和典型金属元素及其化合物性质的理解和掌握,突破学生以往的思维定势,培养了学生思维的多元性和立体性,也为学生构建一个完整的非金属与金属元素的性质递变规律的知识体系引线,为后续学习打下基础。
2.教材处理本节课内容包含了“从海水中提取镁”和“镁的性质”两部分,我在教学中设计了“明”、“暗”两条线索。
明线为“从海水中提取镁”,基于学生的认知水平,结合海水资源的特点和工业生产中的经济效益、资源循环利用、环境保护等问题,层层深入探讨从海水中提取镁的原理、流程。
由于之前学生在有关金属钠单质及其化合物性质的学习过程中,已有了一定的学习思路并掌握了一定的学习方法,因此将“镁的性质”学习设计为暗线,穿插在“从海水中提取镁”这条明线中,并通过“发现问题”、“实验探究”、“解决问题”三个环节来完成本节的教学目标。
高中化学21镁的提取及应用训练题苏教版必修1

镁的提取及应用训练目标1.了解镁单质的生产原理。
2.能用实验的方法探索和认识镁及其化合物的性质。
3.通过经历实验探究的过程,了解实验研究化学物质的一般方法。
(10分钟)1.从海水中提取镁时,没有涉及的化学反应是( )A .MgCl 2+Ca(OH)2===CaCl 2+Mg(OH)2↓B .Mg(OH)2+2HCl===MgCl 2+2H 2OC .Mg(OH)2+H 2SO 4===MgSO 4+2H 2OD .MgCl 2=====通电Mg +Cl 2↑答案:C解析:海水中镁元素的主要存在形态为Mg 2+,从海水中提取Mg 的主要步骤:①用Ca(OH)2将Mg 2+转化成Mg(OH)2沉淀,涉及的化学反应为MgCl 2+Ca(OH)2===CaCl 2+Mg(OH)2↓;②用盐酸将Mg(OH)2溶解,化学方程式为Mg(OH)2+2HCl===MgCl 2+2H 2O ;③将溶液蒸发结晶得到MgCl 2·6H 2O 晶体,电解熔融的MgCl 2得到Mg 单质:MgCl 2=====通电Mg +Cl 2↑。
故没有涉及的是C项的化学反应。
2.从海水中提取镁的过程中涉及的反应的反应类型有( )①化合反应 ②分解反应 ③置换反应 ④复分解反应 ⑤氧化还原反应A .①②③④ B.②③④⑤C .①②④⑤ D.①③④⑤答案:C解析:CaO +H 2O===Ca(OH)2为化合反应;MgCl 2=====通电Mg +Cl 2↑既是分解反应,又是氧化还原反应;MgCl 2+Ca(OH)2===Mg(OH)2↓+CaCl 2为复分解反应。
海水提镁过程中没有涉及置换反应。
3.从海水中提取镁,最基本的方法是往海水里加碱,得到Mg(OH)2沉淀,将沉淀分离出来后再加入盐酸把它转化成MgCl 2溶液;之后,经结晶、过滤、干燥、电解,即可得到金属镁。
下列对从海水中提取镁的有关说法正确的是( )A .制备过程中产生的氯气可以用来制备盐酸,循环使用B .往海水里加碱是指直接加入NaOHC .电解MgCl 2溶液即可得到金属镁D .电解后得到的镁应在CO 2氛围中冷却答案:A解析:A 项,电解氯化镁产生氯气,氯气和氢气反应生成氯化氢,氯化氢水溶液和氢氧化镁反应生成氯化镁,A 项正确;B 项,往海水里加碱是指加入Ca(OH)2,B 项错误;C 项,电解氯化镁得到镁的过程中,电解的不是氯化镁溶液,而是无水氯化镁,C 项错误;D 项,镁能与CO 2反应,故不能在CO 2氛围中冷却,D 项错误。
资料:江苏省江阴市高中化学必修1专题2:镁的提取和应用 教案

编号:020 授课日期:月日课题镁的提取及应用主备人张萍萍
教学目标
1、掌握从海水中提取镁的基本原理和方法
2、实验探究镁的性质及其在生产生活中的应用的重要意义。
教学重点
镁的提取和镁的化学性质
教学难点
镁的提取和镁的化学性质
教学方法
教学过程
二次备课
阅读教材P.55~56 ,回答下列问题并完善表格
1、海水中含有大量的镁离子,如何从海水中提取镁?
2、从海水中提取镁的化学原理是什么?如何用化学方程式表示制
取镁的过程?
一、海水中提取镁
步骤化学方程式
贝壳煅烧成石灰,并将石灰制成石灰乳
石灰乳液加入到海水沉淀池中得到氢
氧化镁沉淀
氢氧化镁与盐酸反应生成氯化镁溶液
并结晶得氯化镁晶体(MgCl2·6H2O)
晶体在氯化氢气流中加热转换成无水
氯化镁
电解熔融的氯化镁得到金属镁
二、镁的性质和应用
1、镁的物理性质
2、镁的原子结构
最外层有个电子,在化学反应中易个电子形成
镁离子,表现出较强
的性,因此镁的化学性质。
2、镁的化学性质
(1)镁和CO2的反应
实验现象:
化学方程式:(分析电子转移的方向和数目)
(2)镁和稀硫酸的反应
实验现象:
化学方程式:,离子反应方程式。
(3)完成下列方程式:
Mg + O2Mg +Cl2
Mg + S Mg +N2
Mg+H2O
讨论:将24克镁条放在空气中燃烧,所得的固体产物可能有哪些?
质量40克?
3、镁的用途
教后反思:。
苏教版高中化学必修一课件2-2-2镁的提取与应用

现象:继续燃烧,放出大量的热和耀 眼的白光,生成白色粉末,瓶内附有黑 色物质. • 思考:镁在空气中燃烧时发生了哪些反应?
镁的性质
4、 与酸反应
(实验3)
Mg +H2SO 4 =MgSO 4 +H2 ↑
现象:放出大量的热和气泡 5、 与水反应
(实验4)
Mg +2H2O (热水) =Mg(OH) 2 +H2 ↑
镁的提取与应用
•
镁的提取与应用
一、镁元素的存在与用途
存在状态: 化合态
电熔铝
镁 肥
镁铝焊丝
•
问题:什么是合金? 合金有什么特点?
镁砖合金板材
镁铝合金
合金
镁 碳 砖
•
ห้องสมุดไป่ตู้
二、镁的工业制法
贝壳 CaCO3
锻烧 ①
石灰 CaO
②
石灰乳 Ca(OH) 2
③
HCl
MgCl2·6H2O
⑤ ④
过滤
Mg(OH) 2
海水
加 热
电解
MgCl2
⑥
Mg
•
三、镁的性质
1、 氧气反应
2Mg+O2
点燃
(实验1)镁的燃烧
2MgO 耀眼白光(照明弹)
现象:剧烈燃烧,放出大量的热和耀眼的白光 2、 与氮气反应
3Mg +N2 = Mg3N2
点燃
3、 与二氧化碳反应 (实验2)镁在二氧化碳中的燃烧
2Mg +CO2 = 2MgO+C
•
六、镁与人体健康的关系
1、镁 关系: 缺镁,人体骨骼会变得疏松崩塌。 人体内有1300多种酶,其中有300多种必须有镁 的 参加,才会发挥催化作用。 镁的含量过低,冠心病的发病几率将大幅升高。 来源:食物、水 、叶绿素 植 物 缺 镁
高二化学上学期镁的提取及应用

点燃 点燃
2MgO Mg3N2 2MgO+C
2Mg+CO2
点燃
Hale Waihona Puke Mg+2H2O加热
Mg(OH)2+H2↑
Mg+2HCl=MgCl2+H2↑
镁的用途
1、镁合金(约含镁80%)被大量用于火箭、导弹 和飞机等制造业,美名为“国防金属”。
2、镁元素能维护心肌纤维正常舒缩功能和冠状 动脉弹性,有“心脏保护神”的美称。
; 绝地求生辅助
江苏省南菁高级中学
神
六
镁的提取及应用
从海水中提取镁
MgCl2+Ca(OH)2=Mg(OH)2↓+ CaCl2 Mg(OH)2+ 2HCl=MgCl2+2H2O MgCl2
电解
Mg+Cl2↑
镁在空气中燃烧的产物
探究方案: 1、镁与CO2反应 2、镁与N2反应
实验:镁在纯氧中燃烧。
现象: 剧烈燃烧,发出刺眼的白光, 产生大量的白烟。
3、镁可以用来制造烟火。 4、镁还可以用来制药。
思考题
已知镁条在 N2 中燃烧生成 Mg3N2 ,如 何检验Mg3N2?提示: Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
Mg3N2+8H2O=3Mg(OH)2↓+2NH3•H2O
谢 谢!
恼!恼羞成怒の王爷此时已经根本无法控制住情绪,直接壹脚就踹向咯这各“守口如瓶”の奴才。“你到是说啊,你哑巴咯?”半天得不到回复の王爷气急败坏地质问着秦顺 儿,他那壹肚子の气窝在心口里急需要壹各发泄の途径,不是秦顺儿还能是谁。面对王爷蛮不讲理の步步紧逼,秦顺儿心慌得厉害,真是哑巴吃黄连,有苦说不出。秦顺儿原 本就只是壹各当奴才の,况且涉及の又是主子之间の床弟之事,他怎么可能没有任何缘由地主动地跟王爷提起这各话茬儿:“启禀爷,您昨天宠幸侧福晋咯。”他秦顺儿是吃 咯熊心还是豹子胆?他若真是这么做咯,下场壹定比上次挨の那二十板子还惨!可是他即使没有这么做,从目前の情况来看,下场也只是稍微好壹点点而已。因为在这件事情 中,除咯王爷和水清以外,就只有他这么壹各知根知底の知情人,晓得整各事情の前前后后、各中原委。而恰恰因为王爷不知情の原因而冤枉咯水清,冤枉她还是次要の,更 主要の是他们两人还有壹各“假以时日,自有分晓”の赌约。在这场赌博中,他不但彻彻底底地失败咯,而且输得又是那么の丢人现眼,而秦顺儿作为唯壹の“目击证人”, 不但没有主动对他提醒,更是眼睁睁地看着他颜面尽失地闹咯这么天大の壹各笑话。被自己の奴才贻误“军情”而吃咯壹各大败仗、哑巴亏,受の完全就是窝脖气,王爷能不 恼羞成怒吗?第壹卷 第460章 余波秦顺儿守口如瓶、知情不报只是令他极为光火の壹各方面,另外壹各方面当然还是因为水清。水清因为他の宠幸而整整哭咯壹夜,这简直 是闻所未闻の天下奇闻!哪各诸人被他宠幸不都是心花怒放,欢喜异常?而那些他根本就不想去宠幸の诸人,为咯讨好他,还要千方百计地讨他の欢心,以期博得他の青眼有 加。这各水清倒好,竟然会因为被他宠幸而哭咯整整壹夜。从来没有被任何壹各诸人如此唯恐避之不及地对待,特别是还当着排字琦和秦顺儿の面,他顿觉颜面尽失,恨不能 找各地缝立即钻进去。水清不愿意,他还更不愿意呢!若不是那天伤心过度,借酒烧愁,他怎么可能会腿脚不听使唤地去咯怡然居?又怎么可能稀里糊涂地上咯那各诸人の 床!让他遭受咯继秦顺儿知情不报以来の第二各窝脖气!这各窝脖气の可恨还在于,那时候水清因为有腿伤在身,他连“诬陷”她使用诡计、魅惑勾引他の机会都没有,完完 全全是他自己自觉自愿地上咯人家の床。对秦顺儿知情不报の气恨交加,对水清耻于被他宠幸の恼羞成怒,促使他将壹肚子の怨气全都撒到咯秦顺儿这各奴才身上。因为他也 只能如此,水清此时远在怡然居,靴长莫及,而且还怀着身孕,他就再是气得火冒三丈,对她也是无可奈何。而秦顺儿不但只是各奴才,还就在他の眼跟前,满腔の怒火只能 由这各倒霉の奴才壹各人去承担。眼看着他壹会儿气恨,壹会儿恼怒,壹会儿羞愧,排字琦不禁又想起那天在怡然居见到蜷缩在床角,满脸泪痕の年妹妹の样子,实在是楚楚 可怜呢。担心他寻完秦顺儿の麻烦,再将这把怒火烧到怡然居去,毕竟水清现在怀着身孕,禁不住折腾。更重要の是,排字琦此时还在千方百计地打着另壹各主意,那就是努 力营造壹各他极为宠爱水清の假象,并且希望这各传言最好赶快传到二十三贝子府去,越快越好,只有这样才能让婉然对他彻底死咯心。要想维持这各假象,最基本の前提条 件就是他和天仙妹妹两各人千万不要再发生任何矛盾和冲突,否则她前面の这些努力岂不是全都要前功尽弃咯?壹想到这里,她赶快在壹旁开口劝道:“爷,您赶快消消气, 都是妾身失职,没有将妹妹调教好。关键是妾身也不晓得您那天要过去,假设早晓得の话,定会好好地对她教诲壹番,她不至于让妹妹没咯规矩,没有将您服侍好。”排字琦 の这番主动认错,给咯他壹各很大の台阶,也算是找补回来壹些面子,于是他赶快顺坡就下:“你是该好好教诲她,连服侍爷这么简单の事情都做好,她还是爷の诸人吗?” 排字琦本来是想先由自己揽下责任,免得他壹会儿再去寻水清の不是,结果她好心好意还劝出麻烦来咯,他壹有咯台阶就煞不住闸。眼看着他の表现与她の预期有些越来越远, 排字琦心急如焚,盘算着能赶快再寻各啥啊由头,让他及时停止对天仙妹妹の抱怨。第壹卷 第461章 点醒鉴于已经率先承认咯错误,无计可施の排字琦想想让王爷不对水清 心怀不满,那就只剩下替年妹妹求情这壹条路可走咯:“爷,您说得都对,确实是妹妹没有做好,理应受罚,只有挨咯罚,才能让她长教训。不过,妾身还是想斗胆劝您壹句, 毕竟妹妹还小,又是壹各极要面子の人,初经男女之事,难免会脸上挂不住,您就大人不计小人过吧。”排字琦真是壹语点醒梦中人!他只晓得被自己の诸人嫌弃是壹件颜面 尽失の奇耻大辱,可是他忘记咯,水清也是极为要脸面の壹各人。而排字琦那“初经男女之事”六各字,就像是敲响在他心头の壹记警钟,让他第壹次充分意识到,面对这各 人生中の“第壹次”,水清会是多么の尴尬与难堪。就算是王爷对水清有天大の误会,但是依照他对她の咯解,“初经男女之事”对于水清而言,确实是壹件值得“哭咯整整 壹各晚上”の事情。想到这里,他开始恼恨不已。水清是啥啊人他当然清楚,那是壹各受咯天大の委屈都不会令她放下自尊去乞求原谅の倔强诸人,可是被他宠幸の结果却能 让她整整哭咯壹夜,他都能够想象得出来,那么
苏教版高中化学必修一《镁的提取及应用》学案1-新版

第二单元钠、镁及其化合物第三课时镁的提取及应用一、课标内容:1、根据生产生活中的应用实例过通过实验探究,了解金属镁等金属及其化合物的主要性质。
二、教学要求:1、了解镁及其化合物的主要性质和应用。
2、了解海水中镁的提取。
三、知识回顾:1、回顾几组概念:(1)酸性氧化物:___________________________________________________;(2)碱性氧化物:___________________________________________________;(3)电解质:_______________________________________________________;(4)非电解质:______________________________________________________;(5)强电解质:______________________________________________________;(6)弱电解质:_______________________________________________________;(7)阿伏伽德罗定律:_________________________________________________________;(8)分散系中溶液、胶体和浊液分类的标准:____________________________;2、回顾几个重要的化学方程式。
且属于离子反应的写出离子方程式:(1)电解法制取氯气:_________________________________________________;(2)实验室制取氯气:_________________________________________________;(3)氯气与水反应:_____________________________________________;(4)金属铁在氯气中燃烧:___________________________________________;(5)漂白粉的制备:________________________________________________;(6)漂白粉的漂白原理:_________________________________________;(7)氯气与KBr溶液反应置换出Br2:____________________________________;(8)氯气与KI溶液反应置换出I2:_____________________________________;(9)金属钠与水的反应:_____________________________________;(10)金属钠在空气中燃烧:__________________________________________;(11)过氧化钠与水反应:_____________________________________________;(12)过氧化钠与二氧化碳反应:_____________________________________;(13)碳酸钠与盐酸反应:___________________________________________;(14)碳酸钠与氯化钙溶液反应:________________________________________;(15)碳酸氢钠固体受热分解:__________________________________;(16)碳酸氢钠溶液与氢氧化钙溶液反应:_______________________;三、教材导读:1、自然界中的镁主要以化合态的形式存在于___________中。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
专题二 从海水中获得的化学物质
第二单元 钠、镁及其化合物
——— 镁的提取及应用
学习目标:
1、了解镁的物理性质,掌握镁的化学性质,了解镁的用途。
2、熟悉元素及其化合物知识的学习思路,培养学生的观察能力和思维能力
3、认识化学在自然资源综合利用方面的重要价值
学习重点:镁的化学性质
【教师活动】向学生展示或让学生观看有关镁的存在和用途、从海水中提取镁的工业流程的
图片或录像。
【学生活动】观看图片或录像。
【知识归纳】自然界的镁主要以 的形式存在于 和海水中,海水中镁的总储量约
为 。
【教师活动】教师叙: 海水中含有大量的镁离子,镁及其合金的用途十分广泛,我们这节
课就来探索如何从海水中提取镁。
请同学们思考下列问题:
【思考】1、海水中提取镁的过程中,海水沉淀池中得到氢氧化镁沉淀时为什么加入的是石
灰乳而不是NaOH 溶液?
2、电解得到金属镁为什么不采用电解熔融的氧化镁?
3、电解产生的Cl 2怎么处理?
【师生活动】教师评讲学生答案,引导学生阅读课文P55后思考下列问题:
(1)从海水中提取镁的化学原理是什么?如何用化学方程式表示制取镁的过程?
【教师活动】教师评讲学生答案,引导学生思考:海水中含有大量的NaCl 、MgCl 2、CaCl 2、
KCl 等氯化物,在海水中加入石灰乳[Ca(OH)2],生成的沉淀是什么物质?请设
计实验方案验证你的想法是否正确,并完成你设计的验证实验。
【学生活动】从海水中提取镁的过程及原理:
海水提镁的步骤:
加
MgCl 2·6H 2O
写出从海水中提取镁的过程中所涉及的化学反应方程式和离子方程式。
【师生活动】教师启发、引导,帮助学生正确书写化学方程式。
(1)MgCl 2+Ca(OH)2=Mg(OH)+CaCl 2
(2)Mg(OH)2+2HCl=MgCl 2+2H 20
(3)MgCl 2Mg+Cl 2
【教师活动】教师提问:既然我们已经提取出了镁,那么它有哪些性质呢?
【学生活动】实验探究镁的性质。
实验1:取一根4~5cm 长的镁条,用砂纸将表面的氧化膜擦去,用坩埚钳夹
持镁条,在酒灯上点燃后,伸入充满二氧化碳的集气瓶中,观察现象。
实验2:在一支试管中放入一小段擦去氧化膜的镁条,再向试管中加入一定
量的稀硫酸,观察现象。
【教师活动】教师巡视,及时规范学生的实验操作,引导学生观察实验现象,激发疑问并将
问题做适当记录。
【学生活动】根据现象推测性质,教师参与其中,共同讨论。
完成下列表格:
【教师活动】教师引导学生将镁与水的实验现象及钠与水的实验现象进行比较,比较金属钠、
镁的金属活动性。
【学生活动】学生交流讨论发表自己的观点。
【知识归纳】镁的物理性质
镁是 色的金属固体,是热和电的良导体,质地 。
硬度较 ,熔点较低,镁的密
度较_____,镁能与铜、铝、锡、锰、钛等形成许多合金,但是硬度和强度都很____,
因此镁合金被大量用于制造 、 和 的部件,氧化镁的熔点可以达到2800℃,是很好的______材料
【归纳总结】根据本节课所学知识,结合下图转化关系完成方程式,并说明镁的重要用途。
2
⑥ 、
①
②
③
④
⑤
⑥
【课外练习】完成课本P57第7题【教师反思】。
