生物化学实验复习题 2
河南城建学院生物工程系12年-13年生物化学(二)复习题

生物化学(二)复习题一、名词解释1 酵解2 糖异生3 三羧酸循环4 乳酸循环5β-氧化6 酮体7 乙醛酸循环8 一碳单位9 糖异生10 呼吸链11 不对称转录12 转录泡13 复制眼14 半不连续复制15 半保留复制16 柠檬酸穿梭17 痛风18 转录因子19 启动子20终止子21 遗传密码22遗传密码的简并性23 尿素循环24 新陈代谢25 乳酸发酵26 底物水平磷酸化27 酮体28 两用代谢途径29 填补反应30ATP循环31 肝昏迷二、填空1、用整体动物做实验,禁食24小时,大鼠肝中的糖原由7%降低到1%,饲喂乳酸后,发现大鼠肝糖原增加,说明生物体内存在现象。
2、植物细胞中蔗糖合成时需提供糖基,淀粉合成时需,纤维素合成时需和;动物细胞中糖元合成时需。
3、剧烈运动时产生的大量会迅速扩散到血液,PH值下降,该物质随血流流至肝脏,先氧化成,再经过作用转变为葡萄糖,进而补充,也可重新合成肌糖原被贮存起来,防止中毒。
4、糖异生作用关键的步骤是、和5、磷酸戊糖途径的限速酶是6、磷酸戊糖途径的代谢起始物是,返回的代谢终产物和,其重要的中间代谢产物是和NADPH。
该途径包括和两个阶段7、当碘乙酸抑制3-磷酸甘油醛脱氢酶时,有氧与无氧分解均不可进行,生物体内发生另一个能分解糖的途径是。
8、尿黑酸症(alcaptonuria)是代谢中缺乏尿黑酸酶引起的代谢遗传病。
9、酵解途径中,砷酸盐的存在会解除和的偶联作用。
10、糖原的合成场所是____________;糖原合成的关键酶是____________;糖原分解的关键酶是____________。
11、骨骼肌和脑组织中,NADH要进入线粒体经过穿梭系统,共产生ATP。
12、日常生活中利用乳酸发酵的例子有和。
乙醇发酵的应用有和。
13、糖酵解过程中,催化三步不可逆反应的酶分别是、和,其中是限速酶。
14、是心脏的主要能源,若心脏用能减少,则其氧化速率会。
15、糖酵解中催化底物水平磷酸化生成ATP的两个酶是________和_________、16、1个葡萄糖分子经糖酵解可净生成_______个ATP;糖原中有1个葡萄糖残基经糖酵解可净生成__________个ATP。
生物化学试题及答案(2)

生物化学试题及答案(2)生物化学试题及答案(2)第二章核酸的结构与功能一、名词解释1(核酸 2(核苷 3(核苷酸 4(稀有碱基 5(碱基对 6(DNA的一级结构 7(核酸的变性 8(Tm值 9(DNA的复性 10(核酸的杂交二、填空题11(核酸可分为 ____和____两大类,其中____主要存在于____中,而____主要存在于____。
12(核酸完全水解生成的产物有____、____和____,其中糖基有____、____,碱基有____和____两大类。
13(生物体内的嘌呤碱主要有____和____,嘧啶碱主要有____、____和____。
某些RNA分子中还含有微量的其它碱基,称为____。
14(DNA和RNA分子在物质组成上有所不同,主要表现在____和____的不同,DNA分子中存在的是____和____,RNA分子中存在的是____和____。
15(RNA的基本组成单位是____、____、____、____,DNA的基本组成单位是____、____、____、____,它们通过____键相互连接形成多核苷酸链。
16(DNA的二级结构是____结构,其中碱基组成的共同特点是(若按摩尔数计算)____、____、____。
17(测知某一DNA样品中,A=0.53mol、C=0.25mol、那么T= ____mol,G=____mol。
18(嘌呤环上的第____位氮原子与戊糖的第____位碳原子相连形成____键,通过这种键相连而成的化合物叫____。
19(嘧啶环上的第____位氮原子与戊糖的第____位碳原子相连形成____键,通过这种键相连而成的化合物叫____。
20(体内有两个主要的环核苷酸是____、____,它们的主要生理功用是____。
21(写出下列核苷酸符号的中文名称:ATP____、dCDP____。
22(DNA分子中,两条链通过碱基间的____相连,碱基间的配对原则是____对____、____对____。
生化实验试题参考

生化实验试题参考篇一:生物化学实验考试试题(完整版)生物化学实验二、填空题:1. 测定蛋白质含量的方法有(双缩脲法),(紫外吸收法),( Folin-酚试剂法(或Lowry法) )和(考马斯亮蓝G-250染色法)。
2. CAT能把H2O2分解为H2O和O2,其活性大小以(以一定时间内分解的H2O2量)来表示,当CAT与H2O2反应结束,再用(碘量法)测定未分解的H2O2。
3. 聚丙烯酰胺凝胶电泳是以(聚丙烯酰胺凝胶)作为载体的一种区带电泳,这种凝胶是由(Acr)和交联剂(Bis)在催化剂作用下聚合而成。
化学聚合法一般用来制备(分离)胶,其自由基的引发剂是(Ap),催化剂是(TEMED);光聚合法适于制备大孔径的(浓缩)胶,催化剂是(核黄素)。
4.层析技术按分离过程所主要依据的物理化学性质进行分类,可分成以下几种:(吸附层析),(分配层析),(离子交换层析),(凝胶层析)和(亲和层析)。
5. 使用离心机离心样品前,必须使离心管(等重)且对称放入离心机。
6. 米氏常数可近似表示酶和底物亲合力,Km愈小,表示E对S的亲合力愈(大),Km愈大,表示E对S的亲合力愈(小)。
7. 分光光度计在使用之前必须预热,注意预热及样品槽空时必须__(打开)____(打开、合上)样品池翻盖。
8. CAT是植物体内重要的酶促防御系统之一,其活性高低与植物的(抗逆性)密切相关。
9. 纸层析实验中,____________形成固定相,____________流动相。
10. 聚丙烯酰胺凝胶是是由和交联剂在催化剂作用下聚合而成的,在具有自由基团体系时,两者就聚合。
引发产生自由基的方法有两种:(化学法)和(光聚合法)。
11. 层析技术按按固定相的使用形式进行分类,可分成以下几种:(柱层析),(纸层析),(薄层层析)和(薄膜层析)。
参考答案:生物化学实验一、名词解释:1、电泳:指带电粒子在电场中向与其自身所带电荷相反的电极方向移动的现象。
医学检验生物化学历考试复习题(3篇)

医学检验生物化学历考试复习题(3篇)医学检验生物化学历考试复习题(一)一、选择题(每题2分,共40分)1. 下列哪种物质是人体内主要的能量来源?A. 葡萄糖B. 脂肪C. 蛋白质D. 核酸2. 酶的活性中心通常由哪些氨基酸残基组成?A. 疏水性氨基酸B. 极性氨基酸C. 碱性氨基酸D. 酸性氨基酸3. 下列哪种维生素是辅酶A的前体?A. 维生素B1B. 维生素B2C. 维生素B3D. 维生素B54. 糖酵解过程中,ATP的生成主要发生在哪个阶段?A. 糖的活化B. 糖的裂解C. 氧化还原反应D. 底物水平磷酸化5. 下列哪种激素主要调节血糖水平?A. 胰岛素B. 胰高血糖素C. 甲状腺激素D. 生长激素6. 脂肪酸β氧化过程中,每循环一次生成的产物有哪些?A. 乙酰辅酶A、NADH、FADH2B. 丙酮酸、NADH、FADH2C. 乙酰辅酶A、NADPH、FADH2D. 丙酮酸、NADPH、FADH27. 蛋白质的二级结构主要由哪种键维持?A. 氢键B. 离子键C. 疏水键D. 二硫键8. 下列哪种方法常用于蛋白质的定量分析?A. 凯氏定氮法B. 紫外分光光度法C. 比色法D. 以上都是9. DNA复制过程中,引物的主要成分是什么?A. DNAC. 蛋白质D. 脂肪10. 下列哪种酶在DNA复制中起关键作用?A. DNA聚合酶B. RNA聚合酶C. DNA连接酶D. 限制性内切酶11. 下列哪种物质是人体内主要的缓冲系统?A. 碳酸氢盐缓冲系统B. 磷酸盐缓冲系统C. 蛋白质缓冲系统D. 以上都是12. 下列哪种离子在维持细胞膜电位中起重要作用?A. Na+C. Ca2+D. Mg2+13. 下列哪种方法常用于测定血糖浓度?A. 葡萄糖氧化酶法B. 葡萄糖脱氢酶法C. 葡萄糖激酶法D. 以上都是14. 下列哪种物质是胆固醇的前体?A. 乙酰辅酶AB. 丙酮酸C. 脂肪酸D. 磷脂15. 下列哪种维生素是凝血因子合成的必需因子?A. 维生素KC. 维生素DD. 维生素E16. 下列哪种酶在尿素循环中起关键作用?A. 谷氨酸脱氢酶B. 脲酶C. 精氨酸酶D. 赖氨酸酶17. 下列哪种物质是人体内主要的抗氧化剂?A. 维生素CB. 维生素EC. 谷胱甘肽D. 以上都是18. 下列哪种方法常用于测定血清总蛋白浓度?A. 双缩脲法C. 紫外分光光度法D. 以上都是19. 下列哪种物质是人体内主要的电解质?A. 钠B. 钾C. 钙D. 以上都是20. 下列哪种激素主要调节钙磷代谢?A. 甲状旁腺激素B. 降钙素C. 维生素DD. 以上都是二、填空题(每空1分,共20分)1. 糖酵解过程中,葡萄糖首先被转化为_________。
生物化学复习题 (2)

生物化学各章知识要点及复习参考题蛋白质的酶促降解、氨基酸代谢、核苷酸代谢知识要点蛋白质和核酸是生物体中有重要功能的含氮有机化合物,它们共同决定和参与多种多样的生命活动。
在自然界的氮素循环中,大气是氮的主要储库,微生物通过固氮酶的作用将大气中的分子态氮转化成氨,硝酸还原酶和亚硝酸还原酶也可以将硝态氮还原为氨,在生物体中氨通过同化作用和转氨基作用等方式转化成有机氮,进而参与蛋白质和核酸的合成。
(一)蛋白质和氨基酸的酶促降解在蛋白质分解过程中,蛋白质被蛋白酶和肽酶降解成氨基酸。
氨基酸用于合成新的蛋白质或转变成其它含氮化合物(如卟啉、激素等),也有部分氨基酸通过脱氨和脱羧作用产生其它活性物质或为机体提供能量,脱下的氨可被重新利用或经尿素循环转变成尿素排出体外。
(二)核酸的酶促降解核酸通过核酸酶降解成核苷酸,核苷酸在核苷酸酶的作用下可进一步降解为碱基、戊糖和磷酸。
戊糖参与糖代谢,嘌呤碱经脱氨、氧化生成尿酸,尿酸是人类和灵长类动物嘌呤代谢的终产物。
其它哺乳动物可将尿酸进一步氧化生成尿囊酸。
植物体内嘌呤代谢途径与动物相似,但产生的尿囊酸不是被排出体外,而是经运输并贮藏起来,被重新利用。
嘧啶的降解过程比较复杂。
胞嘧啶脱氨后转变成尿嘧啶,尿嘧啶和胸腺嘧啶经还原、水解、脱氨、脱羧分别产生β-丙氨酸和β-氨基异丁酸,两者经脱氨后转变成相应的酮酸,进入TCA循环进行分解和转化。
β-丙氨酸还参与辅酶A的合成。
(三)核苷酸的生物合成生物能利用一些简单的前体物质从头合成嘌呤核苷酸和嘧啶核苷酸。
嘌呤核苷酸的合成起始于5-磷酸核糖经磷酸化产生的5-磷酸核糖焦磷酸(PRPP)。
合成原料是二氧化碳、甲酸盐、甘氨酸、天冬氨酸和谷氨酰氨。
首先合成次黄嘌呤核苷酸,再转变成腺嘌呤核苷酸和鸟嘌呤核苷酸。
嘧啶核苷酸的合成原料是二氧化碳、氨、天冬氨酸和PRPP,首先合成尿苷酸,再转变成UDP、UTP和CTP。
在二磷酸核苷水平上,核糖核苷二磷酸(NDP)可转变成相应的脱氧核糖核苷二磷酸。
生物化学试题2

生物化学试题2姓名一.名词解释〔20分,每个4分〕1.糖异生2氮平衡3RFLP4Calvincycle5分子筛二填空题〔10分,每空1分〕12.核酸生物已合成肽链之间能够,这是3.酶的实质不仅是,某些也有酶活性。
4.米氏常数是酶的,其单位为,等于三.是非题〔20分,每题1分。
正确答+或√,错误答x〕1.各类核糖核酸中,稀有碱基含量最高的是tRNA。
2激酶在酶的系统中属于合成酶类。
3肽链延长所需要的能量由ATP提供。
4DNA中G、C含量和Tm成正比。
5绿色植物光反响的要紧产物是葡萄糖。
6原核生物起始tRNA是甲酰甲硫氨酰tRNA。
7直截了当从DNA模板合成的分子是RNA。
8.糖酵解的三个要害酶是己糖激酶、二磷酸果糖激酶和丙酮酸激酶。
9.氨基酸有64组密码子,终止密码子有3个。
10.遗传密码是Nirenberg等1965年提出的。
11线粒体和叶绿体的遗传密码和通用密码相同。
12.氯霉素、四环素、链霉素与核糖体结合抑制原核生物DNA翻译。
13.mRNA中的密码子和tRNA中的反密码子是平行配对的。
14真核生物基因往往是不连续的。
15.辅酶或辅基确定酶的反响性质,酶蛋白决定酶的专一性。
16.遗传信息要紧编码在DNA中,RNA不编码遗传信息。
17.DNA中G、C含量和Tm成正比。
18.人小便中嘌呤代谢的最终产物要紧是尿素。
19.糖酵解和磷酸戊糖途径是在细胞质中进行的。
20.光合作用中植物的二氧化碳受体是1,5二磷酸核酮糖。
四.选择题〔30分,每题1分〕1.各类核糖核酸中,稀有碱基含量最高的是AtRNAB5SrRNACmRNADtRNA前体2反密码子是UGA,它可识不以下哪个密码子AACUBCUACUCADUAC3人类免疫缺陷病毒〔HIV〕引起爱滋病,这种病毒是一种AdsDNA病毒BssDNA病毒CdsRNA病毒DssRNA病毒4.核苷酸从头合成中,嘧啶环的1位N原子来自A天冬氨酸B氨甲酰磷酸C谷氨酰胺D甘氨酸5.遗传密码中第几个碱基经常不带或特别少带遗传信息A第一个B第二个C第三个6.基因工程技术的创立是由于发现了A反转录酶BDNA连接酶C限制性内切酶D末端转移酶A尿素B尿囊素C尿酸D尿囊酸8.反转录酶是一类ADNA指导的DNA聚合酶BRNA指导的DNA聚合酶CRNA酶DRNA指导的RNA聚合酶9.嘌呤霉素的作用是A抑制DNA合成B抑制RNA合成C抑制核糖体中肽链的延长D破坏核糖体10.大肠杆菌中要紧行使复制功能内的酶是ADNA聚合酶IBDNA聚合酶IICDNA聚合酶IIIDKlenow酶11.为核糖体上的蛋白质合成提供能量的分子是AA TPBGTPCUTPDCTP12.非竞争性抑制剂使A Vmax不变,Km变大;BVmax变小,Km不变;CVmax变小,Km变小13.米氏常数〔Km〕值是A随酶浓度增大而增大B随酶浓度增大而减小C随底物浓度增大而减小D是酶反响的特性14.酶促反响中酶的作用在于A提高反响活化能B落低反响活化能C促使正向反响速度提高D改变Kcatß-氧化过程顺序是?A.脱氢,加水,再脱氢,加水B.脱氢,脱水,再脱氢,硫解C.脱氢,加水,再脱氢,硫解D.水合,脱氢,再加水,硫解E.水合,脱氢,硫解,再加水16.可由呼吸道呼出的酮体是?A.乙酰乙酸B.羟丁酸C.丙酮D.乙酰乙酰CoAE.以上都不是17.由胆固醇转变而来的是?A.维生素AB.维生素PPC.维生素CD.维生素DE.维生素Eβ-氧化后除生成乙酰CoA外还有A.丙二酰CoAB.丙酰CoAC.琥珀酰CoAD.乙酰乙酰CoAE.乙酰CoA19.乙酰CoA羧化酶催化的反响其产物是?A.丙二酰CoAB.丙酰CoAC.琥珀酰CoAD.乙酰乙酰CoAE.乙酰CoA20.蛋白质的消化要紧依靠?A.胃蛋白酶B.胰蛋白酶C.肠激酶D.寡肽酶E.二肽酶21.有关氮平衡的正确表达是?A.每日摄进的氮量少于排出的氮量,为负平衡B.氮平衡是反映体内物质代谢情况的一种表示方法C.氮平衡实质上是表示每日氨基酸进出人体的量D.总氮平衡常见于儿童E.正氮平衡和负氮平衡均见于正常成人22.关于必需氨基酸的错误表达是?A.必需氨基酸是人体不能合成,必须由食物提供的氨基酸B.动物种类不同,其所需要的必需氨基酸也有所不同C.必需氨基酸的必需性可因生理状态而改变D.人体所需要的8种,其中包括半胱氨酸和酪氨酸E.食物蛋白的营养价值取决于其中所含必需氨基酸的有无和多少23.一碳单位的载体是?A.二氢叶酸B.四氢叶酸C.生物素D.焦磷酸硫胺素E.硫辛酸24.在鸟氨酸循环中,尿素由以下哪种物质水解而得?A.鸟氨酸B.半胱氨酸C.精氨酸D.瓜氨酸E.谷氨酸25.鸟氨酸循环的要紧生理意义是A.把有毒的氨转变为无毒的尿素B.合成非必需氨基酸C.产生精氨酸的要紧途径D.产生鸟氨酸的要紧途径E.产生瓜氨酸的要紧途径26.尿素循环与三羧酸循环是通过哪些中间产物的代谢联结起来?A.天冬氨酸B.草酰乙酸C.天冬氨酸和延胡索酸D.瓜氨酸E.天冬氨酸与瓜氨酸27.尿素循环中,能自由通过线粒体膜的物质是?A.氨甲酰磷酸B.鸟氨酸和瓜氨酸C.精氨酸和延胡索酸D.精氨酸代琥珀酸E.尿素和鸟氨酸28.以下何者是DNA复制的底物?A.A TPB.dUTPC.dTTPD.dGDPE.dAMP29.以下有关DNA聚合酶III的论述,何者是错误的?5’→3’聚合酶活性C.有3’→5’外切酶活性D.有5‘→3’外切酶活性E.有模板依靠性30.以下有关DNA复制的论述,哪一项为哪一项正确的?A.DNA复制是全保持复制B.新链合成的方向与复制叉前进方向相反者,称前导链C.新链合成的方向与复制叉前进方向相同者,称前导链D.前导链是不连续合成的E.后随链是连续合成的三.答复题〔20分〕1.脂肪在体内的分解代谢要紧途径是什么,代谢的终产物如何样循环?〔10〕2.试述用超离心法将蛋白质、核酸〔DNA和RNA〕不离开来。
生化实验复习题及答案

生化实验复习题及答案一、单项选择题1. 酶的催化作用主要依赖于其活性中心中的哪种基团?A. 疏水基团B. 极性基团C. 金属离子D. 氨基酸残基答案:B2. 以下哪种物质不是蛋白质的组成单位?A. 氨基酸B. 核苷酸C. 多肽D. 糖类答案:D3. DNA复制过程中,以下哪种酶负责解开双螺旋结构?A. DNA聚合酶B. DNA连接酶C. 拓扑异构酶D. 解旋酶答案:D二、填空题1. 蛋白质的一级结构是指_________的线性排列顺序。
答案:氨基酸2. 脂质体是一种由_________构成的球形结构。
答案:磷脂双层3. 核酸分子中的碱基配对遵循_________原则。
答案:互补配对三、简答题1. 描述糖酵解过程中的关键酶及其作用。
答案:糖酵解过程中的关键酶包括己糖激酶、磷酸果糖激酶-1和丙酮酸激酶。
己糖激酶催化葡萄糖磷酸化生成葡萄糖-6-磷酸,磷酸果糖激酶-1催化果糖-6-磷酸磷酸化生成果糖-1,6-二磷酸,丙酮酸激酶催化磷酸烯醇丙酮酸转化为丙酮酸,同时生成ATP。
2. 简述细胞呼吸过程中的三个主要阶段及其能量产生。
答案:细胞呼吸的三个主要阶段包括糖酵解、柠檬酸循环和电子传递链。
糖酵解在细胞质中进行,产生少量ATP和NADH;柠檬酸循环在细胞线粒体基质中进行,产生NADH、FADH2和少量ATP;电子传递链在线粒体内膜上进行,通过氧化NADH和FADH2产生大量的ATP。
四、计算题1. 如果一个DNA分子中有1000个碱基对,其中腺嘌呤占20%,那么该DNA分子中鸟嘌呤的含量是多少?答案:由于DNA中腺嘌呤(A)和胸腺嘧啶(T)配对,鸟嘌呤(G)和胞嘧啶(C)配对,且A+T=G+C,所以如果A占20%,则T也占20%,G 和C各占30%。
因此,鸟嘌呤的含量是1000个碱基对的30%,即300个鸟嘌呤。
高等教育自学考试生物化学及生物化学检验(二)试题2

高等教育自学考试生物化学及生物化学检验(二)试题一、单项选择题(本大题共15小题,每小题2分,共30分)在每小题列出的四个备选项中只有一个是符合题目要求的,请将其代码填写在题后的括号内。
错选、多选或未选均无分。
1.血糖浓度的相对恒定对维持组织器官的正常生理功能具有重要的意义,其代谢特点为( )A.食物中的葡萄糖是正常人血糖的主要来源B.在体内血糖只能经肝糖原分解产生C.血糖可氧化分解产生能量,但不能转化成其他物质D.生长激素可升高血糖2.Km是酶的特征性常数,在临床酶学分析中的意义是( )A.Km值与酶与底物的亲和力成正比B.如果一个酶有几个底物,其Km值是一样的C.测定Km值可鉴定催化相同反应的一组酶是否是同工酶D.Km值与酶的浓度有关3.钠、钾测定的标本要求( )A.钾测定时不必报告样本是血清还是血浆B.测血钾时样本不能溶血C.测血钠时样本不能溶血D.测血钾时样本被冷藏不会影响结果4.关于慢性肝病对血浆蛋白质浓度的影响是( )A.清蛋白合成减少B.γ-球蛋白合成减少C.清蛋白合成增加D.γ-球蛋白合成增加5.关于尿蛋白检测指标正确描述的是( )A.尿中仅有少了清蛋白的为非选择性尿蛋白B.尿中含有大量大分子蛋白的为选择性尿蛋白C.选择性高者预后好D.选择性尿蛋白肾病较重6.不属于心肌损伤标记物的是( )A.葡萄糖激酶B.肌钙蛋白C.肌红蛋白D.肌酸激酶7.关于肌钙蛋白(Tn)论述不正确的是( )A.Tn存在于各种骨骼肌胞浆中B.Tn存在于平滑肌中C.Tn含有与钙结合的部位D.Tn含有与原肌球蛋白结合的部位8.正确的镁离子代谢的是( )A.只有少数食物中含有镁离子B.镁离子的吸收主要是被动扩散形式C.吸收部位主要在回肠D.肠道是镁离子的主要排泄器官9.Ⅰ型骨质疏松症临床检验呈现为( )A.碱性磷酸酶一般在正常范围B.清骨钙素增高C.总碱性磷酸酶增高D.25(OH)D3降低10.妊娠期母体血液的变化是( )A.红细胞的增加多于血浆容量的增加B.血红蛋白浓度增加C.凝血因子合成降低D.血栓栓塞危险性增加11.不符合甲胎蛋白(AFP)的选项是( )A.属于清蛋白B.存在几种亚型C.可用在胎儿先天性异常筛选D.可用作成人肿瘤筛选12.肿瘤是( )A.单克隆产物B.原发瘤增长快于转移瘤C.目前肿瘤标志物阳性率很高D.肿瘤标志物的特异性很高13.2型糖尿病的特点是( )A.以青少年发病为主B.起病较急C.血浆中胰岛素含量降低D.糖刺激后胰岛素释放迟缓14.多数血清酶在生理上存在较明显的差异,除了( )A.性别B.年龄C.进食D.运动15.关于钠代谢平衡紊乱叙述不正确的是( )A.缺失性低钠血症因为钠的丢失少于水的丢失B.缺失性低钠血症会表现为心动过速C.稀释性低钠血症会表现为水肿D.高钠血症可能是过渡丢失水二、填空题(本大题共12小题,每空1分,共22分)请在每小题的空格中填上正确答案。
生物化学复习题(1-3章)

生物化学复习题第一、二、三章1、生物化学是在什么水平研究生命现象的A 器官B 系统C 分子D 原子E 物质结构2、生物大分子物质是A糖类、脂类、蛋白质、核酸B糖类、脂类、维生素、核酸C糖类、脂类、蛋白质、酶D糖类、脂类、核酸E糖类、脂类、维生素3、下列哪种碱基只存在于RNA分子中:A G B A C T D U E4、、蛋白质一级结构的化学键是:A 氢键B 疏水键C 肽键D 二硫键E 范德华力5、蛋白质中氮的含量约为:A 27% B 19% C 13% D 6.25% E 16%6、32克氮元素相当于多少克样品中蛋白质的含量A 150B 64C 200D 180E 1007、氨基酸的紫外线吸收峰值A 280nmB 260nmC 290nmD 270nmE 300nm8\维持蛋白质二级结构的化学键是:A 氢键B肽键C疏水键D二硫键E范德华力9\非必需氨基酸为:A 色氨酸、苯丙氨酸B 亮氨酸、异亮氨酸C 苏氨酸、结氨酸D 赖氨酸、甲硫氨酸E 谷氨酸、天冬氨酸10\蛋白质的最佳生理需要量:A 30gB 50gC 80gD 60gE 120g11\蛋白质的基本单位是;A 氨基酸B 核糖C 核苷酸D 碱基E 磷酸12、下列哪种氨基酸不是必须氨基酸:A 异亮氨酸B 色氨酸C 蛋氨酸D 苏氨酸E 组氨酸13、氨基酸在其等电点是处于什么状态:A 正电荷B 负电荷C 正负电荷相等D 不一定E以上都不对14、当把氨基酸放在大于等电点的溶液中其状态A 正电荷B 负电荷C 正负电荷相等D 不一定E以上都不对15、蛋白质在其等电点是处于什么状态:A 正电荷B 负电荷C 正负电荷相等D 不一定E以上都不对16、能使蛋白质变性的因素不包括A 高温B 紫外线C 高压D 低温E 重金属20、200g蛋白质的含氮量:A 32gB 16gC 20gD 23gE 18g21、蛋白质的变性是由于:A 蛋白质一级结构被破坏B 蛋白质空间结构被破坏C 蛋白质水解D 蛋白质的辅基充分丢失E 蛋白质失去水化膜22、蛋白质多肽链的方向是:A 从3ˊ端到5ˊ端B 从5ˊ端到3ˊ端C 从C端到N端D 从N 端到C端E 没有方向性23、关于蛋白质四级结构描述正确的是:A 一定有多个不同的亚基B 一定有多个相同的亚基C 亚基必须具有三级结构 D 亚基之间依靠肽键结合起来 E 多为螺旋或片层状结构24、蛋白质变性过程中与下列哪项无关()A、理化因素致使氢键破坏B、疏水作用破坏C、蛋白质空间结构破坏D、蛋白质一级结构破坏,分子量变小25、RNA主要存在于A 细胞液 B 细胞核 C 线粒体 D 内质网 E 核糖体26、下列哪种碱基只存在于DNA分子中:A G B A C T D U E C27、DNA主要存在于 A 细胞液 B 细胞核 C 线粒体 D 内质网 E 核糖体28、DNA的紫外线吸收峰值A 280nmB 260nmC 290nmD 270nmE 300nm29、DNA 分子的二级结构是:Aα-螺旋 B 双螺旋 C β-折叠 D 茎环结构E 三叶草结构30、DNA的基本单位是:A 脱氧核苷酸B 核苷酸C 核糖D 磷酸E 碱基31、维持α-螺旋和β-折叠结构的主要是:A 二硫键B 氢键C 疏水键D 酯键E 范德华力32、RNA的基本单位是:A 脱氧核苷酸B 核苷酸C 核糖D 磷酸E 碱基33、维持核酸一级结构的化学键是A 肽键B 磷酸二酯键C 氢键D 疏水键E 二硫键34关于碱基配对正确的是A A和TB C和TC C和AD A和GE G和 T35、关于碱基配对正确的是A A和DB C和GC C和AD A和GE G和 T36、酶的化学本质是:A 活性中心B 小分子有机化合物C 核酸D 蛋白质E 以上都不是37、酶的活性中心是指:A 酶分子的中心部位B 辅酶C 酶分子的催化集团D 酶分子的结合集团E 由必需集团构成的具有一定空间构象的区域38、与酶促反应速度成正比关系的影响因素是A 底物浓度B 温度C 溶液的PHD 抑制剂的浓度E 最始温度及PH、底物浓度足够大时的酶浓度39、所有竞争性抑制作用可通过增加何物而接触:A 磺胺B H+浓度C 抑制剂浓度D 底物浓度E 对氨基苯甲酸40、酶原没有活性是因为A 缺乏辅酶或辅基B 酶蛋白肽链合成不完全C 酶原是普通蛋白质D 酶原已经变性E 活性中心未形成或未暴露41、酶的活性中心是指:A 酶分子的中心部位B 辅酶C 酶分子的催化集团D 酶分子的结合集团E 由必需集团构成的具有一定空间构象的区域42、磺胺类药物是下列哪个酶的抑制剂:A 四氢叶酸合成酶B 二氢叶酸合成酶C 四氢叶酸还原酶D 二氢叶酸还原酶E 转肽酶43、影响酶促反应的因素:A 底物浓度B 温度C PHD 酶浓度E 以上都是44、当发生心肌细胞缺血坏死,血液中的乳酸脱氢酶含量明显增多的是:A LDH1B LDH2C LDH3D LDH4E LDH545、当发生急性肝炎时,血液中的乳酸脱氢酶含量明显增多的是:A LDH1B LDH2C LDH3D LDH4E LDH5。
中国农业大学_806生物化学_《生物化学》 复习2

插入、缺失 染色体结构 畸变
19
通式、方向
模板与非模板
起始 RNA合成 (原核)
RNA Pol(全酶、核心酶、
σ)
启动子
延长(核心酶) 终止(2类终止子、ρ因子)
RNA合成(真核)
RNA Pol I、II、III
产物 位置 抑制剂
20
转录后加工
hnRNA、内含子 mRNA(内含子、帽子、尾巴) tRNA rRNA
磷酸戊糖途径
反应
第一阶段(不可逆反应)
意义
5
生物氧化
标准自由能的变化的计算
化学平衡常数 Keq→ΔG0’
ΔG0’ =- RT ln [C] [D] /[A] [B]
氧化还原电势ΔE0’→ΔG0’
ΔG0’=-nFΔE0’
6
高能磷酸化合物
高能键(定义)
化学中 生物化学中
核)
原核生物 起始氨基酸 起始tRNA 起始氨酰- tRNA
N-fMet-tRNAf N-fMet tRNAf (formyl-)
真核生物
Met tRNAi (initiation)
Met-tRNAi
(延伸中的甲硫氨酸tRNA
tRNAm)
23
rRNA和核糖体
结构组成(原核、真核) 活性中心 多核糖体
与复制、转录的方向匹配
氨酰tRNA合成酶
氨基酸的活化、转移
蛋白质合成的过程(原核)
起始
辨认起始密码子、SD序列 起始复合物、IF1、2、3、
延长
结合(EF-Tu、EF-Ts) 转肽 移位(EF-G)
终止(RF)
25
生物化学实验复习题库

生物化学实验复习题库生物化学实验复习题库1、卵磷脂的提取原理:卵磷脂在脑、神经组织、肝、肾上腺和红细胞中含量较多,蛋黄中含量特别丰富。
卵磷脂易溶于醇、乙醚等脂溶剂,可利用这些脂溶剂提取。
本实验用95%乙醇提取卵磷脂,用蒸汽浴分离乙醇和卵磷脂2、卵磷脂的提取原理鉴定新提取得到的卵磷脂为白色蜡状物,与空气接触后因所含不饱和脂肪酸被氧化而呈褐色。
卵磷脂中胆碱基在碱性条件中分解成三甲胺,三甲胺有特异的鱼腥臭味,可鉴别。
3、糖的颜色反应莫氏试验:糖经无机酸(浓硫酸、浓盐酸)脱水产生糠醛或糠醛衍生物,后者在浓无机酸作用下,能与а-萘酚生成紫红色缩合物。
因为糠醛或糠醛衍生物对此均呈阳性反应,故不是糖类的特异性反应,但可用来鉴定糖的存在。
4、糖的颜色反应塞氏试验:酮糖在浓酸的作用下,脱水生成5-羟甲基糠醛,后者与间苯二酚作用,呈红色反应;有时亦同时产生棕红色沉淀,此沉淀溶于乙醇,成鲜红色溶液。
此反应是酮糖的特异性反应,醛糖在同样条件下成色反应缓慢,只有在糖浓度高或煮沸时间长时,才微弱的阳性反应。
在实验条条件下蔗糖有可能水解而呈阳性反应。
塞氏试验可鉴别酮糖的存在。
5、何谓纸层析法?纸层析是最简单的液一液相分配层析。
滤纸是纸层析的支持物。
当支持物被水饱和时,大部分水分子被滤纸的纤维素牢牢吸附,因此,纸及其饱和水为层析的固定相,与固定相不相混溶的有机溶剂为层析的流动相。
因为不同的氨基酸在相同的溶剂中溶解度不同,所以利用在滤纸上迁移速度不同分离氨基酸6.何谓Rf值?影响Rf值的主要因素是什么Rf为氨基酸的比移值。
Rf=原点到层析点中心的距离/原点到溶液前沿的距离影响纸层析迁移率Rf值的主要因素:1、样品本身的性质和结构;2、溶剂的性质;3、PH 值;4、温度;5、滤纸性质。
7.怎样制备扩展剂?8.层析缸中平衡溶剂的作用是什么?9.牛乳中制备酪蛋白的原理和方法。
牛奶含有半乳糖、蛋白质、脂肪成分。
蛋白质中的酪蛋白通过等电点沉淀,再通过离心而获得,糖类小分子由于处于清液中而分离,沉淀物中所含有的脂肪通过有机溶剂抽提而去除,最终得到纯白色、晶状酪蛋白。
生物化学实验试题及答案

生物化学实验试题及答案一、选择题(每题2分,共10分)1. 下列哪种物质不是蛋白质的组成成分?A. 氨基酸B. 核苷酸C. 肽键D. 碳链答案:B2. 酶的活性中心通常包含哪种金属离子?A. 铁离子B. 铜离子C. 锌离子D. 钠离子答案:C3. 以下哪种物质不是脂质?A. 甘油三酯B. 胆固醇C. 磷脂D. 葡萄糖答案:D4. DNA复制过程中,哪个酶负责解开双螺旋结构?A. DNA聚合酶B. DNA连接酶C. DNA解旋酶D. DNA限制酶答案:C5. 细胞呼吸过程中,哪种化合物是最终的电子受体?A. 氧气B. 二氧化碳C. 水D. 葡萄糖答案:A二、填空题(每空1分,共10分)1. 蛋白质的基本组成单位是________。
答案:氨基酸2. 脂肪酸根据饱和程度可以分为________和不饱和脂肪酸。
答案:饱和脂肪酸3. 糖酵解过程中,第一个不可逆反应是由________催化的。
答案:己糖激酶4. 在DNA复制过程中,________酶负责合成新的DNA链。
答案:DNA聚合酶5. 线粒体是细胞内的能量工厂,它主要负责________过程。
答案:细胞呼吸三、简答题(每题10分,共20分)1. 描述一下细胞色素c在电子传递链中的作用。
答案:细胞色素c在电子传递链中起着电子传递的作用。
它能够从复合体III接收电子,并将电子传递给复合体IV,即细胞色素氧化酶。
在这个过程中,电子的传递伴随着质子的泵出,为ATP的合成提供能量。
2. 解释一下为什么说DNA是遗传信息的载体。
答案:DNA是遗传信息的载体,因为它包含了构成生物体所需的所有遗传指令。
DNA分子由四种核苷酸组成,这些核苷酸按照特定的顺序排列,形成了基因。
基因中的核苷酸序列决定了蛋白质的氨基酸序列,而蛋白质是细胞功能和结构的基本单位。
因此,DNA中的遗传信息通过指导蛋白质的合成来控制生物体的发育和功能。
四、实验操作题(每题15分,共30分)1. 描述一下如何使用SDS-PAGE电泳分离蛋白质样品。
生物化学试题2

生物化学试题一、选择题1.DNA二级结构为( )A.单链B.双链C.a-螺旋D.双螺旋2正常人空腹血糖为()mg/dLA.<70B.70~110C.80~120D.>1303.糖异生部位是( )和肾A.心B.肺C.肝D.脾4.将甘内脂肪运至肝外组织的是( )A.CMB.VLDLC.LDLD.HDLE.FA-白蛋白复合体5.红细胞短时间内大量死亡时变化是()A.血浆结合胆红素升高B.尿胆原生高C.尿胆红素阳性D.粪便颜色变浅E. 尿胆红素阴性6.某生物材料含氮4%,其蛋白质含量为()A.4%B.15%C.25%D.30%E.35%7.不能造成蛋白质变性的是()A.红外线B.超声波C.乙醇D.甲醛E.低温8.具二级结构的DNA含A20%.则含量G()A.20%B.30%C.40%D.60%E.80%9.血糖调节主要靠( )A.肝B. 肾C. 肺D.胰E.肌肉10.酶的化学本质是()A.核酸B.蛋白质C.脂肪D.糖原E.淀粉11.只能以糖酵解合成ATP的是( )A.肝细胞B肌肉细胞C.脑细胞D.红细胞E.白细胞12.DNA双螺结构AT对和GC对氢键数分别为()A.2、3 B.3、2C.2、4D.4、2E.3、313.生物转化的主要目的是()A.解毒B.灭活激素C.使药物药理作用减弱D.使药物有理作用增强E.增强水溶性加快排泄14.用于合成蛋白质的氨基酸有()A.16B.17C.18D.19E.2015.把组成酶可分为单纯酶和()两种A.同工酶B.脱氢酶C.合成酶D.结合酶E.转移酶16.含糖原总量最多的是()A.心B. 肝C. 脑D.肾E.肌肉17.人体能量贮存的主要形式是()A.血糖 B.糖原C.脂肪D.蛋白质E.磷脂18.胆固醇只存在于()A.玉米B.小麦C.苹果D.羊肉E.大米19.蛋白质变性后的性质改变为( )A.溶解度增大B.一级结构破坏C.肽键断裂 D.不易消化E.生物活性丧失20.酶与无机催化剂的不同是()A.降低活化能B.催化的反应速度均受温度影响C.高度专一性D.即催化正反应也催化逆反应E.只能催化热力学允许的反应21.只存在于琥珀酸呼吸链的是()A.FADB.FMNC.NADD.辅酶QE.细胞色素22.痛风与()有关A.尿素 B.尿酸C.肌酐 D.胆红素E.胆素原23.RNA将遗传信息传递给蛋白质称为()A.复制B.转录C.翻译D.中心法则E.以上均不会24.糖异生部位是()和肾A.心B.肺C.肝D.脾E.小肠黏膜25.运输外源性脂肪的是A.CMB.VLDLC.LDLD.HDLE.FA-白蛋白复合体26.红细胞短时间内大量死亡时变化是()A.血浆结合胆红素升高B.尿胆素原升高C.尿胆红素阳性 C.粪便颜色变浅E.尿胆红素阴性27.维持蛋白质三级结构的力量是()A.次级键B.氢键C.盐键D.疏水键E.范德华力28.蛋白质含氮量为()%A.12B.6.25C.12D.1629.维持核酸一级结构的力是()A.肽键B.二硫键C.离子键D.磷酸二酯键E.氢键30.DNA的二级结构的形状是()A.单链B双链C.单螺旋D。
临床生物化学检验技术考试题库及答案(2)

临床生物化学检验技术试题及答案一选择题(单项选择)1.下列可降低血糖的激素是A 胰高血糖素B 胰岛素C 生长素D 肾上腺素2.长期饥饿后,血液中下列哪种物质含量升高:A 葡萄糖B 血红素C 乳酸D 酮体3.检测静脉血葡萄糖,如果血浆标本放置时间过长,会造成测定结果:A 升高B 降低C 不变D 无法确定4.脑组织主要以什么为能源供给:A 葡萄糖B 氨基酸C 蛋白质D 脂肪5.当血糖超过肾糖阈值时,可出现: A 生理性血糖升高B 病理性血糖升高C生理性血糖降低D 尿糖6.下列哪种物质不属于酮体: A 丙酮 B 乙酰乙酸 C β-羟丁酸 D 丙酮酸7.正常情况下酮体的产生是在B脑垂体C 胰脏D 肾脏8.胆固醇可转化为下列化合物,但除外:A 胆汁酸B 维生素D3C 雄激素D 绒毛膜促性腺激素9.血浆中催化脂肪酰基转运至胆固醇生成胆固醇酯的酶是: A 血浆卵磷脂胆固醇脂酰转移酶B内质网脂酰COA胆固醇脂酰转移酶C 天冬氨酸氨基转移酶D 脂蛋白脂肪酶10.由胆固醇转变成的维生素是A VitAB VitBC VitCD VitD11.蛋白质占人体固体重量的百分率(%)是A 90B 45C 20D 1012.蛋白质的元素组成是A C、P、S、OB C、H、S、OC C、H、O、ND C、P、O、N13.组成蛋白质基本单位的氨基酸种类有B 20种C 21种D 23种14.某溶液中蛋白质的含量为50﹪,此溶液的蛋白质氮的百分浓度为:A 9.0﹪B 8.0﹪C 8.4﹪D 9.2﹪15.蛋白质结构中的α-螺旋属于A 一级结构B 二级结构C 三级结构D 四级结构16.酶活性测定中,对米-曼氏常数(Km)的叙述,那一种是不正确的:A ν=Vmax[S] /(Km + [S])B 反应速度为最大反应速度一半时,Km =[S]C Km对选择底物浓度有重大意义D Km作为酶的一种特征常数,与酶的性质与浓度有关17.关于同工酶的叙述正确的是A 催化相同化学反应B 不同组织中的含量相同C分子结构相同D 理化性质特性相同18.SI制定义酶活性单位时,代号为:A pmolB U/LC g/LD Katal19.根据国际酶学委员会的决定,酶的一个国际单位是指A.最适条件下,每小时催化生成1mmol产物所需的酶量B.37℃下,每分钟催化生成1μmol产物所需的酶量C.25℃下,其他为最适条件,每分钟催化生成1μmol产物所需的酶量D.在特定条件下,每分钟转化一个μmol底物所需的酶量20.乳酸脱氢酶是由两种亚基组成的四聚体,一般情况下共形成几种同工酶: A2 种B 3种C 4种D 5种21.胆红素主要由下列何种物质分解代谢产生A 白蛋白B 球蛋白C 血红蛋白D 氨基酸22.肝中参与胆红素生物转化的主要物质是A 甘氨酰基B 乙酰基C 葡萄糖醛酸D 甲基23.结合胆红素是A 胆素原B 间接胆红素C 直接胆红素D 胆红素-Z蛋白24.血清标本溶血,对下列哪种检测指标影响最大 A 钾离子B 钠离子C 氯离子D 葡萄糖25.在正常情况下体液中细胞内液与细胞外液钾离子浓度分布是A 细胞外液大于细胞内液B 细胞外液等于细胞内液C 细胞内液大于细胞外液D 以上都不对26.既能增强神经肌肉兴奋性,又能降低心肌兴奋性的离子是: A 钙离子B 镁离子C 氢离子D 钾离子27.嗜铬细胞瘤患者血中下列那项指标升高:A TSHB 儿茶酚胺C 17-酮类固醇D 17-皮质类固醇28.下列哪一组属于急性时相反应蛋白 A.α1-酸性糖蛋白,结合珠蛋白,铜蓝蛋白,C反应蛋白B.转铁蛋白,血红素结合蛋白,甲胎蛋白,结合珠蛋白C.甲胎蛋白,铜蓝蛋白,C反应蛋白,血红素蛋白D.铜蓝蛋白,结合珠蛋白,转铁蛋白,血红素蛋白29.对LDL描叙正确的是 A.运输内源性胆固醇B.运输内源性甘油三酯C.运输外源性胆固醇D.运输外源性甘油三酯30.临床上用于诊断肝脏疾病的酶,下列那组检测最恰当 A.CK GGT ALP AMY B.ALT AST ALP GGTC.AMY LDH α-HBD GGTD.ACP AST CK LDH31.醋酸纤维素薄膜电泳可把血清蛋白分成五条带,由正极到负极的顺序是A. A、α1 、β、γ、α2B.A、β、α1 、α2、γC.A、α1 、α2、γ、βD.A、α1 、α2、β、γ32.唯一能降低血糖的激素是A. 胰岛素E.肾上腺素F.生长素G.甲状腺素33. 下列对血清蛋白质叙述错误的是 A.白蛋白/球蛋白比值为1.5~2.5∶1 B.白蛋白参考范围为35~50g/LC.总蛋白参考范围为60~80g/LD.白蛋白和球蛋白均由肝实质细胞合成34. 血气分析仪直接测定的三项指标是: A.pH、PCO2、TCO2 B.pH、PO2、SATO2 C.pH、PO2、PCO2 D.pH、SB、AB35.正常糖耐量的OGTT结果为 y:A.空腹血糖6~7mmol/L υ?傊鲲?B.口服葡萄糖30~60分钟达最高峰蒪氙C.葡萄糖峰值>10mmol/L 冾赞LQ?瀁D.2小时血糖水平在7~8mmol/L36.. 有关C-反应蛋白(CRP)错误的论述是:D A.是结合肺炎球菌细胞壁C-多糖的蛋白质稫愒 b?C.在急性创伤和感染时血浆浓度升高 ;座弆`瞰?D.在肝细胞内分解37. 反映肾小球滤过功能最可靠的指标是: A.血尿酸 B.血肌酐 C.尿肌酐 D.内生肌酐清除率38.阻塞性黄疸的特征是A.血结合胆红素增多,尿胆原增高B.血结合胆红素增多,尿胆红素阳性C.血未结合胆红素增多,尿胆原增高捩uヾ)D.血未结合胆红素增多,尿胆红素阳性39.gv以下有关酸碱平衡的说法哪项是不正确的 A.血液正常pH为7.35~7.45??B.血液pH<7.35为失代偿性酸中毒C.血液pH>7.45为失代偿性碱中毒 ? 杅禟3?D.仅从pH改变即可确定是代谢性还是呼吸性酸碱中毒40. 胰淀粉酶的活性改变可出现在下列哪种疾病:A.心肌病变 ?皞湡(4赣B.前列腺疾病 a/@.%驛縞?C.骨髓疾病嚛G)儂辺D.胰腺疾病41.Ⅱa型高脂蛋白血症l?j?FAAAAA.血清外观清,总胆固醇值明显升高,甘油三酯正常,脂蛋白电泳β脂蛋白深染B.血清外观混浊,总胆固醇值升高,甘油三酯升高,脂蛋白电泳前β脂蛋白深染攻yd( 1韋?C.血清外观上层有奶油盖、下层透明,总胆固醇值升高,甘油三酯正常,脂蛋白电泳CM深染潠皼u{:?D.血清外观上层有奶油盖、下层混浊,总胆固醇值升高,甘油三酯明显升高,脂蛋白电泳CM深染,前β脂蛋白拖尾 ?jg?pa痝42.&主要用于诊断急性心肌梗死A.CK-MB?B.AMY u?C.ASTm测定D.γ-GT测定? 43.血钙减低常见于:A.甲状旁腺功能亢进 e飸驝崰B. 急性坏死性胰腺炎C.Addison病€? 1沰W?D.慢性肺功能不全44. 代偿性代谢性酸中毒时: ?酰 4"X? A. PCO2↓,pH↓B. PCO2↓,pH不变C. PCO2↓,pH ↑螠馚D. PCO2↑,pH不变45. 下列哪种不是反映肝细胞损伤的酶A.ALTB. ASTC.ACPD. CHE46. 氧饱和度是指是:A.血中存在游离氧的量 9锝竟葧g?B.血液完全被氧气饱和时的氧含量C.血液与空气平衡后的氧气含量 m皫?D.血中氧含量与氧结合量之比值47. A/G倒置可见于:A.肝硬化B.胆结石症C.急性肝炎D.营养不良48. 高蛋白饮食不影响血清哪种物质的检测:A. 尿素B. 血糖C. 尿酸D. 血氨49.以下哪种物质对光敏感,测定时血标本应尽量避光:A. 总蛋白B. 胆红素C. 葡萄糖D. 甘油三酯50. 剧烈运动会使以下哪种指标浓度增高:A. 总蛋白B. 尿素C. 葡萄糖D. ALT51. 离子选择电极法临床常用于下列哪些物质的测定:A. AST ,ALTB. 肌酐,尿素C. 胆固醇,甘油三酯D K+,Na+,Cl-,HCO3-52. 火焰光度法时什么样的血标本会出现假性低血钠或低血钾:A. 高脂或高蛋白血B. 低脂或低蛋白血C. 高溶血D. 高黄疸血53. 利用以下哪种支持介质电泳具有电泳和分子筛双重作用:A. 琼脂糖凝胶B. 醋酸纤维素薄膜C. 聚丙烯酰胺凝胶D. 淀粉胶54. 以下哪种电泳的主要缺点是本底着色高及膜保存较困难:A. 琼脂糖凝胶电泳B. 醋酸纤维素薄膜电泳C. 聚丙烯酰胺凝胶电泳D. 淀粉胶电泳55. 血清蛋白电泳时通常用pH8.6缓冲液,此时各种蛋白质带有的电荷为:A. 白蛋白带正电荷,其他蛋白带负电荷B. 白蛋白带负电荷,其他蛋白带正电荷C. 白蛋白和其他蛋白均带负电荷D. 白蛋白和其他蛋白均带正电荷56.下列哪项不是自动生化分析仪特点:A. 快速、准确、节省试剂B. 提高了工作效率C. 减少了系统误差D. 减少了人为误差57.半自动生化分析仪所用试剂约为全自动生化分析仪的:A. 三分之一B. 一半C. 三倍D. 两倍58.自动生化分析仪自动清洗取样针是为了:A. 提高分析精密度B. 防止试剂干扰C. 防止样品间的交叉干扰D. 提高反应速度59.以NAD+还原成NADH反应为基础的生化分析采用的波长及吸光度变化为:A. 340nm,从小到大B. 400nm,从小到大C. 400nm,从大到小D. 340nm,从大到小60.反渗透水不能去除以下哪种物质:A. 悬浮物B. 微小离子C. CO2D. 微生物61.IFCC 推荐的酶活性浓度测定温度为:A. 38℃B. 20℃C. 37℃D. 25℃62.用双波长测定样品时,有关副波长不正确的是: A. 副波长能补偿发光灯每次闪动给结果造成的差异B. 样品在副波长处的吸光度应为“0”C. 副波长可有助于去除内源性色源D. 副波长应远离主波长63.自动生化分析仪测定时应尽可能减少试剂用量,一般情况下,样品体积占反应总体积的:A. 2%B. 5%C. 10%D. 20%64.多数免疫比浊法采用的校正方法是:A. 二点校正B. 多点校正C. 线性校正D. 单点校正65.如果样本对测定单色光有干扰吸收,为抵消这一影响应采用:A. 平行操作空白B. 样品空白C. 试剂空白D. 溶剂空白66.胆固醇测定试剂中的赋型胆酸盐对血清哪种物质测定有干扰,应设法防止交叉污染:A. 胆红素B. 总胆汁酸C. ALTD. 尿素67.有关干化学法不正确的是:A. 仪器操作不需纯净水B. 仪器校正一次可稳定半年C. 仪器操作需酸碱冲洗液等辅助设备D. 重复性好、快速二填空题1.调节血糖浓度最主要的激素是________和________。
生物化学试卷2
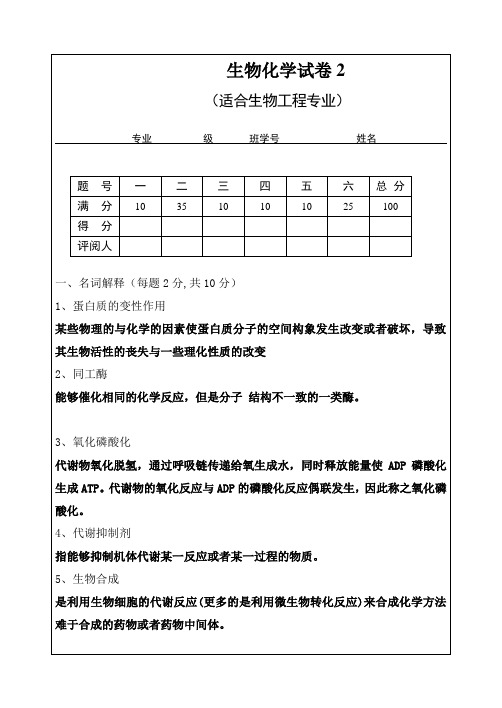
A. 3-磷酸甘油醛B.丙酮酸C.草酰乙酸D.乙酰辅酶A4.与糖异生有关的酶是(C )A.乳酸脱氢酶B. 丙酮酸激酶C.果糖二磷酸酶D.磷酸化酶5.酶Vmax app减小,Km app也减小是(C )作用的结果A.竞争性抑制剂B.非竞争性抑制剂C.反竞争性抑制剂D.都不是6.下列代谢过程不在线粒体中进行的是 (D )A.TCA循环B.脂肪酸氧化C.电子传递D.糖酵解7.下列氨基酸中(D )是营养必需氨基酸A. AlaB. GlyC. CysD. Met8.用于外源性脂肪运输的血浆脂蛋白是(A )9.磷脂生物合成所需的核苷酸是( A )A.ATP、CTPB. GTP、CTPC.CTP、UTPD. ATP、UTP10.嘌呤核苷酸代谢出现障碍时会导致产生(C )A. 白化病B. 尿黑酸症C.痛风性关节炎D.苯丙酮酸尿症四、完成反应方程式(每题2分,共10分,用结构式书写)1、23、琥珀酰辅酶A合成酶+H2ONH3 + CO2+ 2ATP氨甲酰磷酸合成酶ⅠM g2++ 2ADP + Pi H2N COO PO3H2~5. HMGCoA 羟甲基戊二酸单酰辅酶A是脂肪酸、酮体与胆固醇合成的共同中间产物,在脂类代谢中具有重要意义六、问答题(共25分)1. DNA 与RNA 分子构成有何异同?(3分)相同点:构成单位是核苷酸,连接键是磷酸二酯键(1分) 不一致点:戊糖----DNA 中是脱氧核糖,RNA 中是核糖(1分)碱基-----DNA 有A 、T 、G 、C,RNA 有A 、U 、G 、C (1分)2、简述α-螺旋结构特点及其影响因素?(6分) (1)右手螺旋(1分)(2)氢键是α螺旋稳固的要紧次级键(链内氢键)。
(1分)(3)肽链中氨基酸残基的R 基侧链分布在螺旋的外侧,其形状、大小及电荷均影响螺旋的形成与稳固性。
(1分) 影响α螺旋形成与稳固的因素➢ 连续酸性或者碱性氨基酸存在时,不利于α螺旋的生成。
生物化学试题2

一、名词解释1.磷酸甘油穿梭:2.脂肪酸的ß-氧化:3.ACP:4.超二级结构:5.盐析:6.肽平面:7.核酸复性:8.复制子:9.逆转录酶:10.酶原:二、判断题(正确的在括号内打“√”,错误的在括号内打“×”)()1.激活剂对酶具有激活作用,激活剂浓度越高,则酶活性越大。
()2.用透析法可解开蛋白质中的二硫键。
()3.许多植物和微生物能在乙酸环境中生活是因为它们细胞中有乙醛酸循环。
()4.非竞争性抑制中,一旦酶与抑制剂结合后,则再不能与底物结合。
()5.一个动物细胞内的DNA可以与该动物的所有RNA杂交。
()6.酵解途径就是无氧发酵,只在厌氧生物的细胞内发生。
()7.抑制RNA合成酶的抑制剂不影响DNA的合成。
()8.蛋白质分子中的肽键是单键, 因此能够自由旋转。
()9.糖蛋白分子中以蛋白质组分为主,蛋白聚糖分子中以黏多糖为主。
()10.高等动物和低等动物都各自具有特异的遗传密码。
()11.A TP在细胞的产能和贮能过程中起着重要的中间传递作用。
()12.要使酶反应速度达到Vmax的80%,此时底物浓度应是此酶Km值的1/4倍。
()13.脯氨酸是α-螺旋的破坏者。
因此,在肌红蛋白和血红蛋白的多肽链中,每一个脯氨酸残基处都产生一个转角。
()14.核苷中碱基和戊糖的连接一般为C-C糖苷键。
()15.在极低底物浓度时,酶促反应初速度与底物浓度成正比。
()16.机体缺少某种维生素会导致缺乏病,这是因为缺乏维生素能使物质代谢发生障碍。
()17.2,4-二硝基苯酚是氧化磷酸化的解偶联剂。
()18.脂肪酸的活化为脂肪酰CoA时,需消耗两个高能磷酸键。
()19.DNA修复合成时首先合成的DNA短片段称为冈崎片段。
()20.氨酰tRNA合成酶既能识别氨基酸,又能识别tRNA,使它们特异结合。
三、选择题(为单选题,请将正确答案填写到下表中)A.9或10 B.10或12.5 C.13或14D.14或15 E.17或18 F.19或202.跨膜蛋白与膜脂在膜内结合部分的氨基酸残基A.大部分是酸性B.大部分是碱性C.大部分疏水性D.大部分是糖基化3.氨甲酰磷酸合成酶Ⅱ需要的氮源是:A.NH3B.Gln C.GluD.Asp E.Gly F.Asn4.嘌呤核苷酸从头合成途径首先形成的核苷酸是:A.AMP B.XMP C.IMPD.UMP E.CMP F.GMP5.关于DNA复制过程的错误叙述是:A.亲代DNA双链分开,各自都可作为复制模板B.以dNTP为原料,在模板上合成复制链C.子代DNA的合成都是连续进行的D.在子代DNA分子中有一条来自亲代DNA分子E.子代与亲代的DNA分子核苷酸排列顺序完全相同6.RNA在细胞内的主要合成场所是:A.线粒体B.微粒体C.细胞核D.内质网E.高尔基体F.细胞浆7.磷脂作为生物膜主要成分,这类物质的分子最重要的特点是:A.两性分子B.能与蛋白质共价结合C.能替代胆固醇D.能与糖结合8.需PRPP参加的反应是:A.尿嘧啶转变尿嘧啶核苷酸;B.次黄嘌呤转变次黄嘌呤核苷酸C.氨基甲酰天冬氨酸转变为乳清酸D.腺嘌呤转变为腺嘌呤核苷酸;E.鸟嘌呤转变为鸟嘌呤核苷酸9.在效应物作用下,蛋白质产生的变构(或别构)效应是蛋白质的A.一级结构发生变化B.构型发生变化C.构象发生变化D.氨基酸顺序发生变化10.氰化物中毒是由于抑制了哪种细胞色素A.Cytaa3 B.Cytc C.CytB.D.Cytc111.酶促反应的初速度不收下面哪个因素影响:A.[S] B.[E] C.pH值D.时间E.温度12.关于凝胶过滤技术叙述正确的是:A.相对分子质量大的分子最先洗脱下来B.相对分子质量小的分子最先洗脱下来C.主要根据蛋白质带电荷的多少达到分离目的。
生物化学题库及答案(2)

一、名词解释#1、免疫球蛋白:是一类具有抗体活性的动物糖蛋白。
主要存在于血浆中,也见于其它体液及组织分泌物中。
一般可分为五种。
2、超二级结构:在蛋白质尤其是球蛋白中,存在着若干相邻的二级结构单位(α-螺旋、β-折叠片段、β-转角等)组合在一起,彼此相互作用,形成有规则的、在空间能辨认的二级结构组合体,充当三级结构的构件,称为超二级结构3、纤维状蛋白:纤维状蛋白分子结构比较有规律,分子极不对称,呈极细的纤维状,溶解性能差,在生物体内具保护、支持、结缔的功能,如毛发中的角蛋白,血纤维蛋白等。
4、盐析作用:向蛋白质溶液中加入大量中性盐,可以破坏蛋白质胶体周围的水膜,同时又中和了蛋白质分子的电荷,因此使蛋白质产生沉淀,这种加盐使蛋白质沉淀析出的现象,称盐析作用。
5、球状蛋白:球状蛋白的空间结构远比纤维状蛋白复杂,分子呈球形或椭圆形,溶解性能好,如血红蛋白、清蛋白、激素蛋白等。
#6、疏水相互作用:蛋白质分子某些疏水基团有自然避开水相的趋势而自相黏附,使蛋白质折叠趋於形成球状蛋白质结构时,总是倾向将非极性基团埋在分子内部,这一现象称为疏水相互作用。
7、简单蛋白与结合蛋白简单蛋白:完全由氨基酸组成的蛋白质称为简单蛋白。
结合蛋白:除了蛋白质部分外,还有非蛋白成分,这种蛋白叫结合蛋白。
8、别构现象:当有些蛋白质表现其生理功能时,其构象发生变化,从而改变了整个分子的性质,这种现象称别构现象。
9、分子病:指某种蛋白质分子一级结构的氨基酸排列顺序与正常的有所不同的遗传病。
10、多肽链:多个氨基酸以肽键相互连接形成多肽,多肽为链状结构,又叫多肽链。
11、桑格(Sanger)反应:即2,4二硝基氟苯与α—氨基酸中氨基反应生成DNP-氨基酸,是黄色二硝基苯衍生物。
用此反应可以N-端氨基酸的种类。
是生化学家Sanger创用,故称桑格反应。
12、等电点:当调节氨基酸溶液的pH值,使氨基酸分子上的-NH2和-COOH的解离度完全相等,即氨基酸所带净电荷为零,在电场中既不向正极移动,也不向负极移动,此时氨基酸所处溶液的pH值称为该氨基酸的等电点。
12级生物化学实验2期末复习题-考试

12级生物化学实验2期末复习题-考试生物化学实验(2)理论习题一、名词解释题1、聚丙烯酰胺凝胶电泳(PAGE):在样品介质和聚丙烯酰胺凝胶中加入离子去污剂和强还原剂后,蛋白质亚基的点泳迁移率主要取决于亚基分子量的大小,而电荷因素可以被忽略。
当蛋白质的分子量在15KD到200KD之间时,电泳迁移率与分子量的对数呈线性关系,可以用来测定蛋白质亚基的分子量。
2、电泳:带电颗粒在电场作用下,向着与其电性相反的电极移动,称为电泳3、层析分离技术:是一种物理的分离方法,利用多组分混合物中各组分物理化学性质的差别,使各组分以不同的程度分布在两个相中。
4、吸附色谱法:利用同一吸附剂对混合物中不同成分吸附能力的差异,从而使各成分达到分离目的的色谱法。
5、离子交换层析:以离子交换剂为固定相,依据流动相中的组分离子与交换剂上的平衡离子进行可逆交换时的结合力大小的差别而进行分离的一种层析方法。
6、分配层析:根据一种或多种化合物,在两种不相融合的溶剂间的分配来分离物质的方法。
7、亲和层析:是利用生物活性物质之间的专一亲和吸附作用而进行的层析方法。
是近年来发展的纯化酶和其他高分子的一种特殊的层析技术。
8、凝胶层析(凝胶色谱):混合物随流动相经过凝胶层析柱时,由于各组分流经体积的差异,使不同分子量的组分得以分离的层析方法。
9、电渗作用:指在电场作用下液体(通常是水)相对于和它接触的固定的固体相作相对运动的现象。
10、担体:担体是一种化学惰性的,多孔性的固体微粒,能提供较大的惰性表面,使固定液以液膜状态均匀地分布在其表面。
11、死时间:从进样到惰性气体峰出现极大值的时间称为死时间.。
12、保留时间:被分离样品组分从进样开始到柱后出现该组分浓度极大值时的时间,也即从进样开始到出现某组分色谱峰的顶点时为止所经历的时间,称为此组分的保留时间。
13、高效液相色谱法:,以液体为流动相,采用高压输液系统,将具有不同极性的单一溶剂或不同比例的混合溶剂、缓冲液等流动相泵入装有固定相的色谱柱,在柱各成分被分离后,进入检测器进行检测,从而实现对试样的分析。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
生物化学实验复习题:1.试述旋光法测定淀粉含量的实验原理。
在加热及稀盐酸的作用下,淀粉水解并转入盐酸溶液中。
在一定的水解条件下,不同谷物淀粉的比旋光度是不同的。
其在171~195之间,因此可用旋光法测定粗淀粉的含量。
2.淀粉含量测定的方法有几种?比较各方法特点。
淀粉是由多个葡萄糖缩合而成的多糖,测定淀粉的方法主要有酸水解法、酶水解法和旋光法等。
1、酸水解法:面粉经乙醚除去脂肪,乙醇除去可溶性糖类后,用酸水解淀粉为葡萄糖,按还原糖测定方法测定还原糖含量,再折算为淀粉含量。
2、酶水解法:面粉经除去脂肪及可溶性糖类后,其中淀粉用淀粉酶水解成双糖,再用盐酸将双糖水解成单糖,最后按还原糖测定,并折算成淀粉。
3、旋光法:在加热及稀盐酸的作用下,淀粉水解并转入盐酸溶液中。
在一定的水解条件下,不同面粉淀粉的比旋光度是不同的。
其淀粉的比旋光度在171~195之间,因此可用旋光法测定淀粉的含量。
3.简述旋光法测定淀粉的关键步骤。
1.样品的处理在电子天平上称取小麦粉2.5000g置于三角瓶中→加入50ml 1%HCl混成浆状(不能有结块)→沸水浴中准确加热15min→先加1ml 30% ZnSO4混匀→再加1ml 15%亚铁氰化钾混匀→移至100ml容量瓶中加水定容混匀后过滤→弃去最初15ml收集其余滤液。
2.旋光度测定取滤液20ml置于旋光管中,先用1%HCl 调节旋光仪“0”点,然后将样品溶液放入旋光仪中测α4.写出计算粗淀粉含量的公式并说明各符号的含义。
5.试述凯氏定氮法测定蛋白质含量的实验原理。
含氮的有机物与浓硫酸共热时,其中的碳、氢二元素被氧化成二氧化碳和水,而氮则转变成氨,并进一步与硫酸作用生成硫酸铵。
浓碱可使消化液中的硫酸铵分解,游离出氨,借水蒸汽将产生的氨蒸馏到一定浓度的过量硼酸溶液中,硼酸吸收氨后使溶液中氢离子浓度降低,然后用标准无机酸滴定,直到恢复溶液中原来氢离子浓度为止,最后根据所用标准酸的摩尔数(相当于待测物中氨的摩尔数)计算出待测物中的总氮量。
6.蛋白质含量测定的方法有几种?比较各方法特点。
定氮法,双缩尿法(Biuret法)、Folin-酚试剂法(Lowry法)和紫外吸收法.考马斯亮蓝法(Bradford法).凯氏定氮灵敏度低,适用于0.1.0mg氮,误差为±2%费时10小时将蛋白氮转化为氨,用酸吸收后滴定非蛋白氮(可用三氯乙酸沉淀蛋白质而分离)用于标准蛋白质含量的准确测定;干扰少;费时太长双缩脲法(Biuret法)灵敏度低 20mg 中速 20~30分钟多肽键+碱性Cu2+®紫色络合物硫酸铵;Tris缓冲液;某些氨基酸用于快速测定,但不太灵敏;不同蛋白质显色相似紫外吸收法较为灵敏 50~100mg 快速 10分钟蛋白质中的酪氨酸和色氨酸残基在280nm处的光吸收各种嘌吟和嘧啶;Folin-酚试剂法(Lowry法)灵敏度高 5mg 慢速 40~60分钟双缩脲反应;磷钼酸-磷钨酸试剂被Tyr和Phe还原硫酸铵;Tris缓冲液;甘氨酸;各种硫醇耗费时间长;操作要严格计时;颜色深浅随不同蛋白质变化考马斯亮蓝法(Bradford法) 灵敏度最高 5mg 快速5~15分钟考马斯亮蓝染料与蛋白质结合时,其lmax由465nm变为595nm 强碱性缓冲液;SDS 最好的方法;干扰物质少;颜色稳定;颜色深浅随不同蛋白质变化7.简述凯式定氮法测定蛋白质的关键步骤。
1、消化:在电子天平上称取小麦粉0.2000g--0.4000g 置于凯氏试管底部→加混合混合催化剂0.5g和3ml浓硫酸置于消化炉中高温加热至淡绿色透明(2h左右)取出放入通风橱内至不冒白烟,向其中加20ml水,并移至100ml容量瓶定容→即得样品消化液。
同时每4组8人做1空白实验:0.5g混合催化剂+3ml浓硫酸置于凯氏试管中放入消化炉加热至淡绿色(1h左右)→冷却后加水移入100ml容量瓶中定容得空白消化液。
2.蒸馏与吸收:吸取10ml 2%的硼酸于三角瓶中→加4d甲基红-溴甲酚绿混合指示剂(若变绿色则用0.01mol/L HCl调至紫红色)。
将其置于冷凝管下端并使管尖插入液面以下,再吸取5ml消化液从漏斗上方加入蒸馏室内用水洗两次,并加入10ml 40%NaOH后水封(注意:勿使漏斗内玻杆取下以防漏气),然后打开通气阀进行加热蒸馏,直至吸收液由紫红色变成绿色,计时蒸馏3min→先移去吸收液再停止加热以防倒吸。
3. 滴定:用0.01mol/L HCl 滴定吸收液由绿色退去变红色为止,记下耗去标准盐酸的体积(V1.V0)。
8.写出计算蛋白质含量的公式并说明各符号的含义。
9.试述淀粉酶活力测定的实验原理。
淀粉酶主要包括α-淀粉酶和β-淀粉酶两种。
α-淀粉酶可作用于淀粉中的α-1,4-糖苷键,生成葡萄糖、麦芽糖、麦芽三糖、糊精等还原糖,β-淀粉酶可从淀粉的非还原性末端进行水解,生成麦芽糖。
淀粉酶催化产生的这些还原糖能使3,5-二硝基水杨酸还原,生成棕红色的3-氨基-5-硝基水杨酸。
淀粉酶活力的大小与产生的还原糖的量成正比。
用标准浓度的麦芽糖溶液制作标准曲线,用比色法测定淀粉酶作用于淀粉后生成的还原糖的量,以单位重量样品在一定时间内生成的麦芽糖的量表示酶活力。
淀粉酶存在于萌发后的禾谷类种子中,,其中主要是α-淀粉酶和β-淀粉酶。
两种淀粉酶特性不同,α-淀粉酶不耐酸,在pH3.6以下迅速钝化。
β-淀粉酶不耐热,在70℃15min钝化。
根据它们的这种特性,采用加热的方法钝化β-淀粉酶,测出α-淀粉酶的活力。
在非钝化条件下测定淀粉酶总活力(α-淀粉酶活力+β-淀粉酶活力),再减去α-淀粉酶的活力,就可求出β-淀粉酶的活力。
10.淀粉酶活力测定的方法有几种?比较各方法特点。
11.简述淀粉酶活力测定的关键步骤淀粉酶活力测定①α-淀粉酶活力测定吸取原液1ml于具塞试管中→70℃保温15min用于钝化β-淀粉酶→加1ml 1%淀粉置于40℃水浴中保温5min→加1% 3.5一二硝基水杨酸2ml 沸水加热5min后加水至20ml混匀测A1(用1#管调零)②总酶活力测定吸取稀释液1ml于具塞试管中→加1ml 1%淀粉40℃保存5min→加入1% 3.5一二硝基水杨酸2ml沸水加热5min后加水至20ml混匀测A2(用1#管调零)12.写出计算淀粉酶活力大小的公式并说明各符号的含义。
13.试述SDS-PAGE法测定蛋白质分子量的实验原理。
聚丙烯酰胺凝胶电泳测定蛋白质相对分子质量的方法,主要是根据各蛋白质组分的分子大小和形状以及所带净电荷多少等因素所造成的电泳迁移率的差别。
在聚丙烯酰胺凝胶系统中,加入一定量的十二烷基硫酸钠(SDS),使所有蛋白质颗粒表面覆盖一层SDS分子,导致蛋白质分子间原有的电荷差异消失,此时,蛋白质分子的电泳迁移率主要取决于它的分子量大小。
当蛋白质的分子量在15000~200000之间时,电泳迁移率与分子量的对数呈直线关系。
14.试比较已做实验测定蛋白质分子量方法的异同点。
SDS-PAGE 超速离心凝胶过滤粘度法生物质谱技术15.简述SDS-PAGE法测定蛋白质分子量的关键步骤。
1. 电泳槽的安装:取两块玻璃板→将带玻璃条的板(高板)放置桌面上→在上面放置“U”型橡胶条→最后将凹槽玻璃板(低板)压在高板上,置于电泳槽内,用锲子压紧。
2. 凝胶液的制备与灌装:配置20ml凝胶液:在小烧杯中依次加入5ml 30%凝胶储液,10ml PH 7.2 凝胶缓冲液(用前混匀再取),2ml 1%TEMED,2.6ml重蒸水,0.4ml 10%过硫酸铵混匀后→立即沿高板内侧倒凝胶液于两板之间直至低板上沿→插上梳子置于35ºC培养箱中放置15min,待胶凝后取下“U”条→重新将胶板放置于电泳槽内→向外槽内加三分之一槽深电极缓冲液→向内槽加入电极缓冲液没过低板→最后拔出梳子。
3. 加样:用微量进样器加入10μl标准蛋白于中间胶槽内→其余槽内加入10μl下列样品①牛血清蛋白②绿豆分离蛋白4. 电泳:连接电极线,高板外侧接正极,低板内侧槽接负极,打开电源→调电流120mA →电泳2h(当指示剂前沿超过二分之一胶长时停止)5. 剥胶:取下胶板倒去电极缓冲液→测量指示剂迁移距离和染色前胶长,然后将胶板置于水龙头下方冲玻板四周直至胶与玻璃板分离6. 染色与固定:将胶板放入染色盒内→向其中加入0.1%考马斯亮蓝R250使其浸没置于摇床上染色过夜7. 脱色:用10%乙酸溶液脱色至谱带清晰,测定脱色后胶长及各谱带迁移距离。
16.写出电泳法测定蛋白质分子量的计算公式并说明各符号的含义。
17.试述赖氨酸含量测定的实验原理蛋白质中赖氨酸的含量是谷物品质的主要指标之一。
由于动物及人类不能合成,须从食物中得以补充,为此培育高含量赖氨酸的谷物,对于提高营养价值有重要意义。
本实验分别用茚三酮溶液显色法和染料结合法,测定小麦种子中赖氨酸含量。
谷物蛋白中赖氨酸残基有自由的ε-NH3与茚三酮试剂可发生颜色反应,生成紫红色物质,其颜色深浅与赖氨酸残基的数目成正相关,而其它氨基酸没有自由氨基,不能发生这一反应。
选用碳原子数目与赖氨酸相同的亮氨酸,配成标准溶液,做出标准曲线,可用以测定谷物蛋白内赖氨酸的含量。
18.氨基酸含量测定的方法有几种?比较各方法特点。
常用的有,半定量法:纸层析法;定量法:HPLC柱前衍生化法.19.简述测定赖氨酸的关键步骤。
1.标准曲线的制作(每2组4人做1标准曲线)2、样品的处理与测定:在电子天平上称取小麦粉10mg于具塞试管底部→加1ml 2% 碳酸钠于80℃水浴中保温提取10min→加2ml茚三铜试剂80℃水浴中保温30min后冷却至室温→加5ml 95%乙醇和5ml蒸馏水充分混匀后转移至离心管中3000转/分离心3min(离心前必须平衡)→取上清液测A(以1号管调零)20.写出计算赖氨酸的公式并说明各符号的含义。
21.试述甲醛滴定法测定氨基氮的实验原理。
常温下甲醛能迅速与氨基酸的氨基结合生成亚羟甲基化合物,使上述平衡右移促使NH3+释放H+,从而使溶液酸度增加,滴定终点移至酚酞的变色域内(pH值9.0左右),根据滴定终点时所消耗标准碱的量即可算出反应体系中存在的游离氨基即氨基氮的含量如果样品为一种已知的氨基酸,即可算出该氨基酸的含量。
如果样品为未知氨基酸或几种氨基酸的混合物,则只能算出其氨基氮的含量。
22.简述甲醛滴定法测定氨基氮的关键步骤。
已知氨基酸溶液中氨基酸含量的测定:取3只三角瓶编号①2ml 1% 甘氨酸②2ml 1% 甘氨酸③2ml 水(空白)均加5ml 水和5ml中性甲醛(用前加2滴 0.5% 酚酞滴加0.1mol/LNaOH调至淡红色),及4滴 0.5%酚酞混匀→用0.1mol/L滴至粉红色出现为止→分别记下耗去标准碱的体积(V1.V2.V0)23.写出甲醛滴定法测定甘氨酸的公式并说明各符号的含义。
