2018年初开始、中药批准不再需要临床试验
《中药注册管理补充规定》2008

关于印发中药注册管理补充规定的通知国食药监注[2008]3号2008年01月07日发布各省、自治区、直辖市食品药品监督管理局(药品监督管理局),总后卫生部药品监督管理局:为遵循中医药研究规律,体现中药注册特点,规范中药注册行为,促进中医药和民族医药事业发展,根据《药品注册管理办法》的有关规定,国家局组织制定了《中药注册管理补充规定》,现予印发,请遵照执行。
国家食品药品监督管理局二○○八年一月七日中药注册管理补充规定第一条为体现中医药特色,遵循中医药研究规律,继承传统,鼓励创新,扶持促进中医药和民族医药事业发展,根据《药品注册管理办法》,制定本补充规定。
第二条中药新药的研制应当符合中医药理论,注重临床实践基础,具有临床应用价值,保证中药的安全有效和质量稳定均一,保障中药材来源的稳定和资源的可持续利用,并应关注对环境保护等因素的影响。
涉及濒危野生动植物的应当符合国家有关规定。
第三条主治病证未在国家批准的中成药【功能主治】中收载的新药,属于《药品注册管理办法》第四十五条第一款第(四)项的范围。
第四条中药注册申请,应当明确处方组成、药材基原、药材产地与资源状况以及药材前处理(包括炮制)、提取、分离、纯化、制剂等工艺,明确关键工艺参数。
第五条中药复方制剂应在中医药理论指导下组方,其处方组成包括中药饮片(药材)、提取物、有效部位及有效成分。
如含有无法定标准的中药材,应单独建立质量标准;无法定标准的有效部位和有效成分,应单独建立质量标准,并按照相应的注册分类提供研究资料;中药提取物应建立可控的质量标准,并附于制剂质量标准之后。
第六条中药复方制剂除提供综述资料、药学研究资料外,应按照本规定第七条、第八条和第九条,对不同类别的要求提供相关的药理毒理和临床试验资料。
第七条来源于古代经典名方的中药复方制剂,是指目前仍广泛应用、疗效确切、具有明显特色与优势的清代及清代以前医籍所记载的方剂。
(一)该类中药复方制剂的具体目录由国家食品药品监督管理局协助有关部门制定并发布。
药品注册管理办法(局令第28号)附件1 中药、天然药物注册分类及申报资料要求

附件1:中药、天然药物注册分类及申报资料要求本附件中的中药是指在我国传统医药理论指导下使用的药用物质及其制剂。
本附件中的天然药物是指在现代医药理论指导下使用的天然药用物质及其制剂。
一、注册分类及说明(一)注册分类1.未在国内上市销售的从植物、动物、矿物等物质中提取的有效成份及其制剂。
2.新发现的药材及其制剂。
3.新的中药材代用品。
4.药材新的药用部位及其制剂。
5.未在国内上市销售的从植物、动物、矿物等物质中提取的有效部位及其制剂。
6.未在国内上市销售的中药、天然药物复方制剂。
7.改变国内已上市销售中药、天然药物给药途径的制剂。
8.改变国内已上市销售中药、天然药物剂型的制剂。
9.仿制药。
(二)说明注册分类1~6的品种为新药,注册分类7、8按新药申请程序申报。
1.“未在国内上市销售的从植物、动物、矿物等物质中提取的有效成份及其制剂”是指国家药品标准中未收载的从植物、动物、矿物等物质中提取得到的天然的单一成份及其制剂,其单一成份的含量应当占总提取物的90%以上。
2.“新发现的药材及其制剂”是指未被国家药品标准或省、自治区、直辖市地方药材规范(统称“法定标准”)收载的药材及其制剂。
3.“新的中药材代用品”是指替代国家药品标准中药成方制剂处方中的毒性药材或处于濒危状态药材的未被法定标准收载的药用物质。
4.“药材新的药用部位及其制剂”是指具有法定标准药材的原动、植物新的药用部位及其制剂。
5.“未在国内上市销售的从植物、动物、矿物等物质中提取的有效部位及其制剂”是指国家药品标准中未收载的从单一植物、动物、矿物等物质中提取的一类或数类成份组成的有效部位及其制剂,其有效部位含量应占提取物的50%以上。
6.“未在国内上市销售的中药、天然药物复方制剂”包括:6.1中药复方制剂;6.2天然药物复方制剂;6.3中药、天然药物和化学药品组成的复方制剂。
中药复方制剂应在传统医药理论指导下组方。
主要包括:来源于古代经典名方的中药复方制剂、主治为证候的中药复方制剂、主治为病证结合的中药复方制剂等。
中药、天然药物处方药说明书撰写指导原则

中药、天然药物处方药说明书撰写指导原则二○○六年六月目录一、概述二、说明书各项内容及撰写的一般要求三、说明书各项内容撰写的具体要求(一)核准日期和修改日期(二)特殊药品、外用药品标识(三)说明书的标题(四)警示语(五)【药品名称】(六)【成份】(七)【性状】(八)【功能主治】/【适应症】(九)【规格】(十)【用法用量】(十一)【不良反应】(十二)【禁忌】(十三)【注意事项】(十四)【孕妇及哺乳期妇女用药】(十五)【儿童用药】(十六)【老年用药】(十七)【药物相互作用】(十八)【临床试验】(十九)【药理毒理】(二十)【药代动力学】(二十一)【贮藏】(二十二)【包装】(二十三)【有效期】(二十四)【执行标准】(二十五)【批准文号】(二十六)【生产企业】一、概述根据《药品说明书和标签管理规定》(国家食品药品监督管理局令第24号)、《中药、天然药物处方药说明书格式》、《中药、天然药物处方药说明书内容书写要求》,制定《中药、天然药物处方药说明书撰写指导原则》。
本指导原则是指导药品注册申请人根据药品药学、药理毒理、临床试验的结果、结论和其他相关信息起草和撰写药品说明书的技术文件,也是药品监督管理部门审核药品说明书的重要依据。
二、说明书内容及撰写的一般要求(一)说明书应包括下列项目:核准日期和修改日期、特殊药品/外用药品标识、说明书标题、警示语、【药品名称】、【成份】、【性状】、【功能主治】/【适应症】、【规格】、【用法用量】、【不良反应】、【禁忌】、【注意事项】、【孕妇及哺乳期妇女用药】、【儿童用药】、【老年用药】、【药物相互作用】、【临床试验】、【药理毒理】、【药代动力学】、【贮藏】、【包装】、【有效期】、【执行标准】、【批准文号】、【生产企业】。
(二)说明书的内容必须包括对安全和有效用药所需的重要信息,应尽可能完善。
(三)说明书的内容应尽可能来源于可靠的临床试验(应用)的结果,以及与人体安全有效用药密切相关的动物研究信息。
2018年临床试验 各期l临床试验周期及案例数量

新药研发临床前研究周期及案例数量临床试验一共分成四个阶段(即四期),前三期为新药上市前的临床试验,第四期为上市后的临床试验。
具体包括:I期临床试验:是新药进行人体试验的起始期。
以20一30名健康志愿者为主要受试对象,进行初步的临床药理学及人体安全性评价试验,观察人体对于新药的耐受程度和药代动力学,为制定给药方案提供依据医|学教育网搜集整理。
Ⅱ期临床试验:是以新药预期应用的患病人群样本为对象,初步评价治疗作用的阶段。
其目的是初步评价药物对目标适应证患者的治疗作用和安全性,也包括为Ⅲ期临床试验研究设计和给药剂量方案的确定提供依据。
III期临床试验:试验的设计是采用多中心开放随机对照试验,随机分组方法和药物编码方法与Ⅱ期临床试验类似,通过增加样本量(试验组病例不少于300例和对照100例)并根据试验目的的调整选择受试者标准,适当扩大特殊受试人群,及更为丰富的观察项目或指标等措施,进一步考察不同对象所需剂量及依从性。
Ⅲ期临床试验的条件应尽可能接近该药的正常使用条件,试验药要经中国药品生物制品检定所检定合格,供药时,标明药物系专供临床试验用。
Ⅳ期临床试验:是新药上市后由申请人自主进行的应用研究阶段。
其目的是考察在广泛使用条件下药物的疗效和不良反应;评价在普通或者特殊人群中使用的利益与风险关系;改进给药剂量等。
新药Ⅳ期临床试验是新药临床试验的一个重要组成部份,是上市前新药I、Ⅱ、Ⅲ、期试验的补充和延续。
它可以验证上市前的结果,还可对上市前临床试验的偏差进行纠正,更重要的是可以弥补上市前临床试验缺乏的资料和信息,为临床合理用药提供依据。
新药研发的几个周期新药研发是一个耗时耗资都非常庞大的系统工程,完成前期的基础研究(药理、毒理、药效等动物研究)后开始申请进入人体临床试验阶段。
您所问的临床试验的周期,应该就是临床试验的期别(I、II、III、IV期): I 期临床试验:初步的临床药理学及人体安全性评价试验。
观察人体对于新药的耐受程度和药代动力学,为制定给药方案提供依据。
国家药监局关于发布《中药注册分类及申报资料要求》的通告-国家药品监督管理局通告2020年第68号

国家药监局关于发布《中药注册分类及申报资料要求》的通告正文:----------------------------------------------------------------------------------------------------------------------------------------------------国家药品监督管理局通告2020年第68号国家药监局关于发布《中药注册分类及申报资料要求》的通告为贯彻落实《药品管理法》《中医药法》,配合《药品注册管理办法》(国家市场监督管理总局令第27号)实施,国家药品监督管理局组织制定了《中药注册分类及申报资料要求》,现予发布,并说明如下。
一、中药注册按照中药创新药、中药改良型新药、古代经典名方中药复方制剂、同名同方药等进行分类,前三类均属于中药新药。
中药注册分类不代表药物研制水平及药物疗效的高低,仅表明不同注册分类的注册申报资料要求不同。
二、为加强对古典医籍精华的梳理和挖掘,改革完善中药审评审批机制,促进中药新药研发和产业发展,将中药注册分类中的第三类古代经典名方中药复方制剂细分为“3.1按古代经典名方目录管理的中药复方制剂(以下简称3.1类)”及“3.2其他来源于古代经典名方的中药复方制剂(以下简称3.2类)”。
3.2类包括未按古代经典名方目录管理的古代经典名方中药复方制剂和基于古代经典名方加减化裁的中药复方制剂。
三、古代经典名方中药复方制剂两类情形均应采用传统工艺制备,采用传统给药途径,功能主治以中医术语表述。
对适用范围不作限定。
药品批准文号采用专门格式:国药准字C+四位年号+四位顺序号。
四、3.1类的研制,应进行药学及非临床安全性研究;3.2类的研制,除进行药学及非临床安全性研究外,还应对中药人用经验进行系统总结,并对药物临床价值进行评估。
注册申请人(以下简称申请人)在完成上述研究后一次性直接提出古代经典名方中药复方制剂的上市许可申请。
中药要经过几期临床实验

中药要经过几期临床实验中药作为一种传统药物形式,凭借其独特的功效和疗效在世界范围内得到广泛应用。
然而,中药的临床实验是确保其安全性和有效性的重要环节。
那么,中药要经过几期临床实验呢?本文将针对这个问题展开讨论。
一、前期实验在中药进入临床实验之前,需要进行一些前期实验。
这包括药理学试验、毒理学试验和药代动力学试验等。
药理学试验用于研究中药的药理活性成分和作用机制。
毒理学试验则用于评估中药的毒副作用和安全性,确保中药使用的安全性。
药代动力学试验则是评估中药在体内的吸收、分布、代谢和排泄等动力学过程。
二、临床前期实验在中药正式进入临床实验阶段之前,还需要进行临床前期实验。
这些实验往往包括动物实验和人体初步试验。
1. 动物实验动物实验通常采用小鼠、大鼠、猪等动物模型,用于评估中药的安全性和疗效。
通过给动物灌胃、注射等方式给予中药,并观察动物的生理指标、器官病理等情况,以判断其安全性和可行性。
2. 人体初步试验人体初步试验是将中药应用于少数健康志愿者身上,观察中药的安全性和耐受性。
这些试验往往包括血液检测、尿液检测、心电图检测等,以及对志愿者进行询问和观察,以评估中药的疗效。
三、临床试验在通过前期实验的验证后,中药正式进入临床试验阶段。
临床试验一般分为三期。
1. 临床试验一期临床试验一期是在小范围内进行的试验,通常包括10-100名志愿者。
这一阶段主要考察中药的安全性和耐受性,确定合适的剂量范围。
2. 临床试验二期临床试验二期进行的范围较大,通常包括100-500名志愿者。
这一阶段旨在评估中药的疗效和安全性,进一步确定剂量和用药方案。
3. 临床试验三期临床试验三期是规模最大的一期试验,通常包括1000-3000名患者。
这一阶段旨在进一步评估中药的疗效和安全性,并与现有治疗方法进行对照研究,直至获得充分、可靠的证据。
四、上市后的监测研究一旦中药通过临床试验并获得批准上市,仍需要进行监测研究。
这些研究旨在进一步评估中药的长期疗效和安全性,以及发现可能出现的罕见不良反应。
国家食品药品监督管理局关于印发中药、天然药物处方药说明书格式内容书写要求及撰写指导原则的通知

国家食品药品监督管理局关于印发中药、天然药物处方药说明书格式内容书写要求及撰写指导原则的通知文章属性•【制定机关】国家食品药品监督管理局(已撤销)•【公布日期】2006.06.22•【文号】国食药监注[2006]283号•【施行日期】2006.06.22•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】药政管理正文国家食品药品监督管理局关于印发中药、天然药物处方药说明书格式内容书写要求及撰写指导原则的通知(国食药监注[2006]283号)各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为贯彻实施《药品说明书和标签管理规定》(国家食品药品监督管理局令第24号,以下简称《管理规定》),规范中药、天然药物处方药说明书的书写和印制,国家局制定了《中药、天然药物处方药说明书格式》(以下简称《说明书格式》)、《中药、天然药物处方药说明书内容书写要求》(以下简称《内容书写要求》)以及《中药、天然药物处方药说明书撰写指导原则》(以下简称《指导原则》),现予以印发,并就有关事项通知如下:一、自2006年7月1日起,国家局将按照《管理规定》、《说明书格式》、《内容书写要求》以及《指导原则》,对申请注册的中药、天然药物的说明书进行核准和发布,药品生产企业应当按照国家局核准的说明书进行印制。
二、2006年7月1日之前已经批准注册的中药、天然药物,药品生产企业应当根据《管理规定》、《说明书格式》、《内容书写要求》以及《指导原则》,并按《药品注册管理办法》修订说明书的申报资料要求,提交修订说明书的补充申请。
对于拟修订的说明书样稿(与原批准的说明书内容相比)不增加【孕妇及哺乳期妇女用药】、【儿童用药】、【老年用药】、【药物相互作用】、【临床试验】、【药理毒理】、【药代动力学】项目的,以及注射剂品种拟在【药物相互作用】项下仅表述为“尚无本品与其他药物相互作用的信息”的,药品生产企业应当向所在地省级食品药品监督管理局提交补充申请,省级食品药品监督管理局应当在60个工作日内完成审查,对符合要求的,发给《药品补充申请批件》并附核准后的说明书,同时报国家局备案。
中药注册管理专门规定(征求意见稿)

附件1中药注册管理专门规定(征求意见稿)为体现中医药特色,发挥中医药防病治病的独特优势和作用,遵循中医药研究规律,传承精华,守正创新,推动中药产业高质量发展,根据《中华人民共和国药品管理法》《中华人民共和国中医药法》《中华人民共和国药品管理法实施条例》《药品注册管理办法》等法律、法规,制定以下专门规定。
第一章总体要求一、【传承与创新并重。
】中药是指在我国中医药理论指导下使用的药用物质及其制剂。
中药的研制应当符合中医药理论,注重体现整体观及中医药原创思维,注重临床实践基础。
鼓励通过理论创新、技术创新提升中药新药的研制水平。
二、【坚持以临床价值为导向。
】中药新药研制应坚持以临床价值为导向,重视临床价值评估,注重满足尚未满足的临床需求。
三、【采用科学合理的审评证据体系。
】中药注册审评,应当采用中医药理论、人用经验和临床试验相结合的证据体系,综合评价中药的临床有效性、安全性。
四、【建立中药资源评估机制。
】申请人、上市许可持有人在中药立项、申请上市、上市后等阶段均应当开展药材资源评估,保障中药材来源的稳定和资源的可持续利用,并应关注对生态环境的影响。
涉及濒危野生动植物的,应当符合国家有关规定。
五、【强化中药研制全过程的质量控制。
】申请人研制中药应当保证药材来源可追溯,药材基原、产地、采收期等应当明确。
中药处方药味可经质量均一化处理后投料。
注重加强生产全过程的质量控制,保持批间质量的稳定可控。
药品标准的制定应关注与中药有效性、安全性关联。
第二章中药注册分类与上市审批六、【明确中药注册分类的定义。
】中药注册分类包括中药创新药、中药改良型新药、古代经典名方中药复方制剂、同名同方药等。
中药创新药指含有未在国家药品标准及药品注册标准【处方】中收载的中药新处方,具有临床价值,且未在境外上市的制剂。
中药改良型新药指改变已上市中药的剂型、给药途径,且具有明显临床优势,或增加功能主治等的制剂。
古代经典名方中药复方制剂指处方收载于《古代经典名方目录》且符合国家药品监督管理部门有关要求的中药复方制剂。
中药新药法规

中药新药法规
中药新药法规是指关于中药新药研发、审批及上市等方面的法律规定。
中药新药法规的主要内容包括中药新药的申报审批程序、临床试验要求、药物不良反应的监测和报告、质量控制要求等。
在中国,中药新药的研发、审批和上市需要符合《药品管理法》、《药品注册管理办法》、《中华人民共和国药品监督管理法》等相关法律法规的规定。
根据这些法规,中药新药的申报和审批程序一般包括以下几个步骤:
1. 申报:中药新药的研发机构首先需要向国家药监部门提交新药申报材料,包括研发进展报告、药物质量和安全性评价报告、临床试验数据等。
2. 审评:国家药监部门会组织专家组对中药新药申报进行审评,评估其药理学、药效学和安全性等方面的数据,并提出审评意见和建议。
3. 临床试验:中药新药在通过审评后,需要进行临床试验,以评价其疗效和安全性。
4. 上市许可:经过临床试验的数据评价后,国家药监部门会对中药新药进行终审,决定是否批准其上市销售。
此外,中药新药的质量控制也需要符合相关法规的要求,包括中药质量标准的制定、生产工艺的规范化等。
中药新药法规的制定旨在保障中药新药的安全性、有效性和质量,促进中药研发的科学化和规范化。
通过遵守中药新药法规,可以提高中药新药的研发质量,并为中药新药的上市提供法律依据和保障。
《中药新药研究各阶段药学研究技术指导原则(试行)》解读

·标准·规范·指南·DOI:10.13935/j.cnki.sjzx.201239作者单位:国家药品监督管理局药品审评中心,北京100022通信作者:马秀瞡,Email:maxj@cde.org.cn《中药新药研究各阶段药学研究技术指导原则(试行)》解读顾杰 宋菊 李培 赵巍 刘乐环 马秀瞡【摘要】 为促进中药创新,提高中药研发质量和效率,药品审评中心于2020年11月4日发布《中药新药研究各阶段药学研究技术指导原则(试行)》。
该指导原则作为总论性文件,是在新药研发的不同阶段对药材、饮片、生产工艺、质量研究及质量标准等研究需要达到的研究目标提出要求。
由于产品的具体情况不同,可不必拘泥于本指导原则的分阶段要求,结合产品特点和实际情况合理安排研究进度和研究内容。
【关键词】 中药新药;各阶段药学研究;指导原则【中图分类号】R285 【文献标识码】AInterpretationofTechnicalGuidelineforPharmaceuticalResearchatVariousStagesofModernChineseMedicine(TrialVersion)GUJie,SONGJu,LIPei,ZHAOWei,LIULe-huan,MAXiu-jing(CenterforDrugEvaluation,NationalMedicalProductsAdministration,Beijing100022)【Abstract】 InordertopromotetheinnovationoftraditionalChinesemedicineaswellastoimprovethequalityandefficiencyoftraditionalChinesemedicineresearchanddevelopment,CenterforDrugEvaluationissuedadocumentnamed“TechnicalGuidelineforPharmaceuticalResearchatVariousStagesofNewChineseMedicine(Trialversion)”onNovem ber4,2020.Asageneraldocument,theguidelinesetforthrequirementsfortheresearchgoalsintheresearchofmedicinalherbs,herbalpieces,productiontechnology,qualityresearchandqualitystandardsatdifferentstagesofnewdrugdevelop ment.Becausethespecificconditionsoftheproductsaredifferent,itisnotnecessarytosticktothephasedrequirementsofthisguideline,andrationallyarrangetheresearchprogressandcontent.【Keywords】 NodernChineseMedicine;VariousStagesofPharmaceuticalResearch;Guideline 中药新药研究是一项涉及药学、药理、毒理、临床、统计等多学科研究的系统工程,具有周期长、投入大、风险高等特点,有其自身研发规律,是不断探索、逐步深入的研究过程。
卫生部关于下发“《中药新药临床研究指导原则》(第一辑)”的通知-卫药发[1993]第12号
![卫生部关于下发“《中药新药临床研究指导原则》(第一辑)”的通知-卫药发[1993]第12号](https://img.taocdn.com/s3/m/5e6f4c7d26d3240c844769eae009581b6bd9bd62.png)
卫生部关于下发“《中药新药临床研究指导原则》(第一辑)”的通知
正文:
---------------------------------------------------------------------------------------------------------------------------------------------------- 卫生部关于下发“《中药新药临床研究
指导原则》(第一辑)”的通知
(卫药发[1993]第12号)
各省、自治区、直辖市卫生厅(局):
我部下发的《中药新药临床研究指导原则》(以下简称《指导原则》)第一、二批试行以来,对提高中药新药的临床研究和管理水平,促进中药新药临床研究的规范化,起到了积极作用。
根据几年来实践中发现的问题和有关单位及专家提出的意见和建议,为适应中药新药研制和审批管理工作发展的需要,我部组织有关中药临床药理基地及有关中医药专家,对第一、二批共45个病证的《指导原则》进行了修订,并审定了第三批31病证的《指导原则》,经合并整理后,编辑成《指导原则》第一辑,本辑共收载76个病证,现下发执行。
我部以[87]卫药字第3Z号和[88]卫药字第49号下发的第一、二批《指导原则》(试行)同时废止。
《指导原则》是中药新药临床研究和中药新药审评的标准,是已上市中成药临床再评价的主要依据。
请各地在执行中继续认真总结经验,以便进一步修订和补充完善。
附件:《中药新药临床研究指导原则》第一辑(略)
卫生部
一九九三年八月十六日
——结束——。
中药新药临床研究的技术要求

中药新药临床研究的技术要求中药新药的临床研究包括临床试验和生物等效性试验,临床试验分为Ⅰ、Ⅱ、Ⅲ、Ⅳ期,临床研究须符合我国《药品临床试验管理规范》(GCP)的有关规定。
一、临床试验(一)I期临床试验1.目的初步的临床药理学及人体安全性评价试验。
观察人体对于新药的耐受程度,在具有技术可行性时需进行药物代谢动力学研究,为制定给药方案提供依据。
2.适应范围对于一、二类及《新药审批办法》规定的某些三、四、五类新药,应进行Ⅰ期临床试验。
3.试验设计试验方案由申办者和研究者共同商定。
必须由有经验的合格的医师及相关学科的专业技术人员根据中医药理论,结合临床实际进行设计。
(1)临床研究单位国家药品监督管理局确定的具有Ⅰ期临床试验条件的药品临床研究基地。
(2)受试对象选择健康志愿者,特殊病证可选择志愿轻型患者。
年龄:一般以18-50岁为宜。
性别:一般男女例数最好相等。
健康状况:必须经过健康检查,除一般体格检查外,并经血、尿、粪便常规化验和心、肝、肾功能检查,均属正常者。
并注意排除有药物、食物过敏史者。
妊娠期、哺乳期、月经期,及嗜烟、嗜酒者亦应除外。
注意排除可能影响试验结果和试验对象健康的隐性传染病等。
受试例数:20-30例。
(3)给药方案剂量确定应当慎重,以保证受试者安全为原则。
应当充分考虑中医药特点将临床常用剂量或习惯用量作为主要依据。
亦可参考动物试验剂量,制定出预测剂量。
然后用其1/5量作为初试剂量;对动物有毒性反应的药物或注射剂的剂量,可取预测量的1/10~1/5量作为初试剂量。
试验应事先规定最大剂量,可参照临床应用该类药物单次最大剂量设定。
从初试起始量至最大量之间视药物的安全范围大小,应根据需要确定几个剂量级别,试验从低剂量至高剂量逐个剂量依次进行。
如在剂量递增过程中出现了不良反应,虽未达到规定的最大剂量,亦应终止试验。
在达到最大剂量时,虽无不良反应亦应终止试验。
一个受试者只能接受一个剂量的试验。
首先进行单次给药安全性考察,是否需要多次给药及给药次数应依据该药特性和疗程等因素确定。
《证候类中药新药临床研究技术指导原则》(2018)

关于发布证候类中药新药临床研究技术指导原则的通告(2018年第109号) 2018年11月06日发布为继承和发扬中医药诊疗特色和优势,完善符合中药特点的技术评价体系,落实《药品注册管理办法》《中药注册管理补充规定》的相关规定,国家药品监督管理局组织制定了《证候类中药新药临床研究技术指导原则》,现予发布。
特此通告。
附件:1.证候类中药新药临床研究技术指导原则2.《证候类中药新药临床研究技术指导原则》起草说明附件1证候类中药新药临床研究技术指导原则证候(简称证)是对疾病(泛指非健康)发展到一定阶段的病因、病性、病位及病势等的高度概括,具体表现为一组有内在联系的症状和体征,是中医临床诊断和治疗的依据。
为了更好地传承和发扬中医药特色和优势,国家药品监督管理局根据药品注册相关法规,特制定《证候类中药新药临床研究技术指导原则》(以下简称《指导原则》)。
证候类中药新药是指主治为证候的中药复方制剂新药。
《指导原则》旨在为证候类中药新药临床试验的开展和有效性、安全性评价提供基础性指导,其正文内容中的每一个原则性要求都可—1 —以随着后续研究的不断深入,进一步丰富和发展为更详实具体的技术标准。
一、证候类中药新药的处方来源及基本要求证候类中药新药的处方应来源于临床实践,符合中医药理论,体现理、法、方、药相一致的原则。
证候类中药新药申请临床试验应有充分的人用历史证明性文献材料,包括处方来源、组方合理性、临床应用情况(包括提供临床实践完善处方的演变过程)、功能主治、用法用量等相关内容。
如拟开发的证候类中药新药是来源于中医临床经验的积累,针对临床常见基本证候的,应提供相关证明;如是源于医案中对比分析研究所发现的相对成熟有效的处方,应提供典型医案和系列医案;如具有一定临床研究基础且有相应数据证明的成熟有效的处方,应提供相关临床研究总结报告,该总结报告应明确具体中医证候、疗效特点和安全性信息;如是源于国家科技立项的临床研究成果,应提供临床研究部分的总结资料及相关的成果鉴定材料。
2020年执业药师法规练习题0301

C. Ⅲ期临床试验 D. Ⅳ期临床试验 <1> 、观察人体对于新药的耐受程度和药代动力学,为制定给药方案提供依据的是 ABCD <2> 、进一步验证药物对目标适应症患者的治疗作用和安全性,可采用随机盲对照临床试验的方法的 是 ABCD <3> 、新药上市后的应用研究阶段,目的在于考察在广泛使用条件下的药物的疗效和不良反应的是 ABCD 3、A.国家药品监督管理局 B.药品审评中心 C.国家药典委员会 D.药品评价中心 <1> 、制定非处方药上市注册相关技术指导原则和程序,并向社会公布的机构是 ABCD <2> 、制定处方药和非处方药上市后转换相关技术要求和程序,并向社会公布的机构是 ABCD <3> 、建立收载新批准上市以及通过仿制药质量和疗效一致性评价的化学药品目录集,载明药品名称、 活性成分、剂型、规格、是否为参比制剂、持有人等相关信息,及时更新并向社会公开的机构是 ABCD <4> 、制定化学药品目录集收载程序和要求,并向社会公布的机构是 ABCD 4、A.优先审评审批程序 B.附条件批准程序 C.特别审批程序 D.突破性治疗药物程序 <1> 、药物临床试验期间,用于防治严重危及生命或者严重影响生存质量的疾病,且尚无有效防治手 段或者与现有治疗手段相比有足够证据表明具有明显临床优势的创新药或者改良型新药等,申请人可以 申请 ABCD <2> 、治疗严重危及生命且尚无有效治疗手段的疾病的药品,药物临床试验已有数据证实疗效并能预 测其临床价值的,申请人可以申请 ABCD <3> 、药品上市许可申请时,疾病预防、控制急需的疫苗和创新疫苗具有明显临床价值的,申请人可以 申请 ABCD <4> 、新冠肺炎疫情期间,国家药品监督管理局可以依法决定对其应急所需防治药品实行 ABCD 5、A.国药准字 H(Z、S)C+四位年号+四位顺序号 B.国药准字 H(Z、S)+四位年号+四位顺序号 C.国药准字 H(Z、S)G+四位年号+四位顺序号 D.国药准字 H(Z、S)J+四位年号+四位顺序号 <1> 、境内生产药品的批准文号的格式为 ABCD <2> 、中国香港、澳门和台湾地区生产药品的批准文号的格式为
2018最新免于进行临床试验医疗器械目录(2018年第94号):附件1+附件2
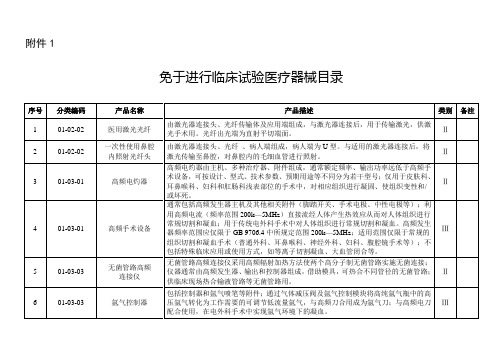
15
01-09-01
内窥镜手术动力系统
产品一般由主机、手柄、刨削刀头组成,通过电机马达带动手柄及刀头进行机械旋转,用于内窥镜手术中实现绞碎或切除组织等手术功能(鼻腔部位手术除外)。适用或参考行业标准YY/T 0955《内窥镜手术设备刨削器》。
Ⅲ
16
01-09-01
鼻窦镜手术动力系统
产品一般由主机、手柄、刨削刀头组成,通过电机马达带动手柄及刀头进行机械旋转,用于鼻窦镜手术中实现切除鼻腔部位组织等手术功能。适用或参考行业标准YY/T 0955《内窥镜手术设备刨削器》。
Ⅱ
13
01-08-02
LED手术照明灯
通常由光源、灯架等组成。用于手术辅助照明,也可单独用于小型手术。不具有无影效果。分为吊顶式、墙面式或移动式。
Ⅱ
14
01-08
一次性使用脊柱外科照明光纤
产品由光源连接头、光纤、头端组成。以无菌形式提供。与照明光源连接后,向手术部位传输光能,为脊柱微创手术提供照明。
通常外形呈直形或弧形,针尖有圆、三角、铲形状,针尾带孔。一般采用不锈钢材料制成。用于缝合组织、皮肤。产品性能指标采用下列参考标准中的适用部分,如:YY/T 0043医用缝合针。
Ⅱ
32
02-07-01
一次性使用荷包缝合针
一次性使用荷包缝合针用金属和缝线制成,由两根缝针、一根非吸收性缝线组成。产品以无菌形式提供,适用于消化道吻合手术中的荷包缝扎。产品性能指标参考YY 0877荷包缝合针标准中的适用部分。
Ⅱ
28
02-06-01
一次性止血夹
由金属、高分子聚合物或其他材料制成,用于外科手术时临时夹闭血管或组织,术后即刻取出。无菌提供,一次性使用。
Ⅱ
《新药审批办法》中有关中药问题的补充规定和说明

《新药审批办法》中有关中药问题的补充规定和说明文章属性•【制定机关】卫生部(已撤销)•【公布日期】1987.03.31•【文号】•【施行日期】1987.03.31•【效力等级】部门规范性文件•【时效性】失效•【主题分类】药政管理正文*注:本篇法规已被《卫生部门规章废止目录(含规范性文件)》(发布日期:1998年4月13日实施日期:1998年4月13日)废止《新药审批办法》中有关中药问题的补充规定和说明(1987年3月31日卫生部)中药新药的研制是在中医药理论指导下,突出中药特色,利用现代科学技术方法,在继承的基础上不断创新。
《新药审批办法》已对新药审批有关问题和技术要求作了规定,使新药研制工作逐步沿着科学化、规范化方向发展。
为进一步做好中药的审批工作,结合我国目前的实际情况,现就《新药审批办法》中的有关中药新药审批的某些问题做以下五个方面的补充规定及说明:一、新药(中药)分类和申报资料项目的补充规定和说明。
二、药材引种、试种栽培品种申报资料项目。
三、新药(中药)药理、毒理研究的技术要求补充说明。
四、新药(中药)稳定性试验资料的补充规定。
五、新药(中药)临床研究的技术要求补充说明。
附:中药制剂标准编写通则一、新药(中药)分类和申报资料项目的补充规定和说明分类部分:(一)第一类“中药材的人工制成品”。
1.以人工方法在动物身上的制取物,如人工牛体内育黄,人工引流熊胆等,原则上应按一类新药报送资料。
其中申报资料3、4、5、7项的研究应与天然品对比,如结果基本一致可免报11~16,18,22项。
但该药材审核批准试用后,应立即进行临床考察(参照Ⅲ期临床试验要求),在卫生行政部门指定的医院,观察该药的疗效和不良反应,并按照《新药审批办法》第15、16、17条要求申报正式生产。
如果资料3、4、5、7项研究与天然品差异较大,则按一类新药的要求,报送全部申报资料项目。
2.“中药材新的药用部位”的申报资料项目,按《药材引种、试种栽培品种申报资料项目》进行申报,并要求与原药用部位做对比试验(例如新的药用部位“人参叶”与“人参根”的成份、理化性质、药效、药理学的比较)的资料。
中药药品注册法规考核试卷

20.关于中药药品注册法规,以下哪项说法正确?()
A.中药药品注册法规适用于所有药品
B.中药药品注册法规仅适用于中药药品
C.中药药品注册法规适用于进口药品
D.中药药品注册法规适用于生物制品
二、多选题(本题共20小题,每小题1.5分,共30分,在每小题给出的四个选项中,至少有一项是符合题目要求的)
B.审评
C.核准
D.生产许可
7.关于中药药品注册的技术审评,以下哪项说法正确?()
A.审评时间不得超过30个工作日
B.审评时间不得超过60个工作日
C.审评时间不得超过90个工作日
D.审评时间根据具体情况进行调整
8.中药药品注册申请人在提交注册申请时,以下哪项资料不需要提供?()
A.药品名称
B.药品处方
D.生产许可
8.中药药品注册申请人在提交申请时,以下哪些内容需要提供中英文对照?()
A.药品名称
B.药品说明书
C.药品生产工艺
D.临床试验报告
9.下列哪些药品可以申请减免临床试验?()
A.古代经典名方制剂
B.仿制药
C.非处方药
D.生物制品
10.中药药品注册过程中,以下哪些阶段需要进行药品质量控制?()
2.请阐述中药新药注册时,申请人需要提交的临床试验资料的主要内容。
3.请分析中药药品注册法规中关于药品安全性评价的要求,并举例说明。
4.请结合实际,谈谈中药药品注册过程中如何确保药品质量符合规定标准。
标准答案
一、单项选择题
1. A
2. D
3. C
4. D
5. D
6. D
7. D
8. D
9. C
10. B
中药药品生命周期法规考核试卷

A.药物发现
B.临床前研究
C.临床试验
D.药品销售
2.以下哪些文件是中药药品注册时必须提交的?()
A.药品生产工艺
B.药品质量标准
C.药品广告审查批准文件
D.药品安全性、有效性研究报告
3.中药药品生产质量管理规范主要包括以下哪些内容?()
A.原料管理
7.中药药品销售过程中,以下哪种行为是违法的?()
A.未经批准发布药品广告
B.向患者提供虚假药品信息
C.按照规定储存、运输药品
D.对过期药品进行回收
8.以下哪项不是中药药品生命周期法规的基本要求?()
A.药品安全
B.药品有效
C.药品广告真实
D.药品价格合理
9.中药药品在注册时,对其安全性和有效性评价的主要依据是:()
C.使用未经批准的原料生产药品
D.药品生产过程中不进行质量检验
12.以下哪个阶段不属于中药药品生命周期?()
A.药物发现
B.药品研发
C.药品销售
D.药品淘汰
13.中药药品生命周期法规考核的内容不包括以下哪项?()
A.药品研发管理
B.药品生产管理
C.药品销售管理
D.药品售后服务
14.以下哪个法规与中药药品生命周期管理无关?()
D.药品使用
19.中药药品生命周期法规考核的主要目的是:()
A.提高药品质量
B.保障药品安全
C.规范药品市场
D. A、B、C都正确
20.以下哪个因素不影响中药药品的生命周期?()
A.药品质量
B.药品安全性
C.药品广告
D.患者年龄
二、多选题(本题共20小题,每小题1.5分,共30分,在每小题给出的四个选项中,至少有一项是符合题目要求的)
中药行业的药品市场准入与注册

中药行业的药品市场准入与注册中药行业作为我国医药产业的重要组成部分,在保护和发扬传统中医药文化的同时,也需要遵循相关的市场准入与注册规定。
本文将对中药行业药品市场准入与注册进行探讨,并分析其中的挑战和机遇。
一、概述中药是我国独有的宝贵资源,拥有悠久的历史和丰富的临床应用经验。
在我国,中药被广泛应用于疾病的预防和治疗中,并在不同的药物剂型中得到体现,如颗粒剂、丸剂、汤剂等。
然而,中药市场准入与注册也是中药行业发展中的重要环节。
二、中药行业的药品市场准入1.法律法规的遵守在中药行业的药品市场准入中,首要的要求是遵守国家和地方相关的法律法规。
中药企业需确保所生产的药品符合《药品管理法》、《医疗器械管理条例》等相关法律法规,以获得市场准入资格。
2.质量控制中药行业的药品市场准入还要求企业能够建立健全的质量控制体系。
企业需要进行药材的采购、加工、储存和质检等环节的监管,以确保中药的质量安全。
3.技术支持中药行业的药品市场准入也需要依托科技创新和技术支持。
企业应加强研发和创新能力,不断提高中药的研发水平和药效。
三、中药行业的药品注册1.申报材料准备中药企业在进行药品注册时,需要准备相关的申报材料。
包括药品说明书、药品质量标准、临床试验数据等。
这些材料应详细、准确,并满足国家药监部门的要求。
2.临床试验中药行业的药品注册还需要进行临床试验。
临床试验是评价药品疗效和安全性的重要手段,对于中药来说更具特殊性。
中药临床试验需要注意对疗效指标、不良反应和肝肾功能等的监测,以确保药品的安全性。
3.审核与批准中药行业的药品注册审核与批准是一个复杂且时间周期长的过程。
药监部门会对提交的申报材料进行审核和评估,严格把关,保证中药的质量、疗效和安全性,最终才会发放药品注册证书。
四、挑战与机遇中药行业的药品市场准入与注册过程中也存在一些挑战与机遇。
1.挑战中药行业药品市场准入与注册的挑战主要体现在质量控制、临床试验和申报材料准备等方面。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2018年初开始、中药批准不再需要临床试验这片土地上关于旧医的若干最新状况、告诉我们一个铁板钉钉的真相:这是最好的时代、也是最好的时代——旧医最好的时代已经到来。
昨天、著名期刊NATURE官网上发表了一篇可免费全文阅读的文章、对于接下来中国旧医的黄金时代作了些点评。
我摘取概要如下、各位读者不妨感受一下:↑https:///news/china-to-roll-back-regulations-for-traditional-medicine-des pite-safety-concerns-1.23038①从2018年初起、中国国内的传统中药将不再需要通过人体安全性和有效性临床试验。
传统中药药企只要拿得出『(古代)经典名方』作为依据、那两项成本巨高、周期漫长的临床试验就可以靠边站了、不再是阻碍。
②只需要提供临床试验之前基于动物或体细胞的药理与药物毒性研究即可。
③这份所谓的古代经典名方清单、将有国家中医药管理局和中国食药监(CFDA)共同拟定公表。
人世间已经没有更好的语言来形容明年年初这一政策所带给我的惊喜了。
说起来、今年7月份至今中医药专业毕业后可以跳开国家现代医学考试、只要以古来传统的学徒形式通过技能测试就可以从业、以及中医诊所的开设都不需要CFDA点头、像开发网站那样备个案就可以了——这前所未有的第一次冲击已经足够给力、意味着旧医的机构与从业人员的准入门槛彻底降低、甚至抛弃了现代医学所设立的基本原则。
而这是第二次。
意味着传统旧医药物的准入门槛彻底降低、甚至抛弃了现代医药所设立的基本原则。
一个是对于从业方的解绑、一个是对于医药品的解绑。
如此两大冲击波双璧同辉之后、捍卫传统旧医的两大护法利器已然形成、旧医在中国的地位恐怕将达到近代历史至今最高点、并且不再有挑战、质疑的条件甚至必要了——因为当现代医学缺席之后、挑战和质疑的逻辑与知识的切入点已不复存在、就好比你打算和人在一个擂台上打拳击的时候、忽然有人把你脚下的地板全部抽空、你直接坠到楼下、和对手都已经不在一个空间维度上、于是永远不会再有交手的可能以及必要了。
这真是一件好事、对于祖国规模极端庞大、渗透无比广泛的旧医行业而言、甚至对于祖国的GDP而言也是好事。
但是中国人的健康安全呢?我只能笑而不语。
在现代医学里、为什么临床试验必不可少?这个话题可以讲一千零一夜。
但这里、我用实际案例来说明问题。
大家都知道、激素替代疗法能够很好地改善更年期以及绝经之后女性的诸多不适、改善生活品质。
这理所当然、因为激素替代疗法(HRT)本来就是为了解决女性这个痛点应运而生的。
但推广时间久了、应用普及了之后、很多机构与医师开始将HRT应用到了其他目的上、譬如心脏病的预防、因为他们凭借自己的从业经验与感觉、认为HRT或对心脏病预防有益。
在现代医学的用药或治疗手段上、这就属于标签外应用、也就是说此时某种疗法的治疗目的已经在其原初所界定的范围之外了。
这种情况可能产生什么影响呢?Maybe 有效、Maybe 无效、Maybe 有效但同时有害、Maybe 无效同时却有害。
↑https:///studies/clinicaltrials/important既然出现了这样新的应用趋势、医学就需要对其进行严谨的研究。
因为这不是闹着玩的。
假如运气好有效哪怕运气一般无效倒也罢了、但万一运气不好:有效但同时有害并且害处超过了效果、甚至下下签地无效却同时有害的话、那可是人命关天的事情。
因此后来、美国国家心肺血液研究所(NHLBI)就开始调查HRT是否真的有利于蕨经后女性的心脏病预防、以及考察会不会有什么潜在的风险。
结果发现:①HRT运用前几年中、女性心脏病风险不降反升。
②HRT会升高中风与血栓的风险。
③雌激素与孕激素联用者、乳腺癌风险UP。
这、就是科学洞察的结果。
基于此、今日的美国FDA对于HRT的应用界定比早先更加严格、更加收窄:①HRT绝不可用于心脏病预防。
②HRT可用于改善更年期以及蕨经后症状、然而必须充分衡量对比收益与(癌症诱发等)风险。
③HRT可用于改善更年期以及蕨经后症状、然而必须坚持显效内最低剂量以及最短疗程之原则、绝对不能为了效果显著怎么爽怎么操起来用。
写了上面那么多为了说明什么?不妨先停止阅读、请读者各位品味一下。
接着、由我来总结一下:①现代医学里、直蕨是不可靠的(已经在蕨经公众号里重复了无数遍、但这一点我猜我会永远重复下去)。
再牛逼的医生、仅凭自己的感觉和经验完全可能出错。
专科医生一辈子能够看的病人人数比起正儿八经的研究、差远了、当中存在的Bias、安慰剂效应以及其他混淆因素更是毋庸赘言。
方法论严谨程度上也差远了。
越是没有科学思维能力、思辨能力、看不到直蕨背后陷阱的人才会越笃信直蕨的神奇、虽然这种神奇信仰无法理解是来源于何处的自信。
有时候到底是不是真的有效、不通过科学的话谁都说不清楚、无论是患者还是医生。
②现代医学里、某种药物和疗法的潜在风险、不是任何时候都能简单说清楚的。
很多急性不良反应与中毒反应还可能通过经验来总结、譬如你不小心服用了含草乌头的中药材、几小时之后嘴唇发麻视线模糊的时候。
然而一旦这种不良反应中毒反应是慢性的、需要很多年乃至数十年才能显示『威力』、尤其是和癌症诱发相关的时候、靠传统经验和观察哪怕数千年都不可能得出结论、甚至根本都联想不到一起。
马兜铃酸类中草药材就是一个最好的证明。
这是因为有太多混淆因素葛藤纠缠在一起、就像我们幼儿园时代都画过的小花猫钓鱼图一样:小花猫咪手里的钓鱼线乱麻一样结成一团、最后末端是许许多多的鱼、中间九曲十八弯、各种拐点和转向、没有适应过科学思维的人根本理不清头绪、不可能理得清头绪。
更可怕的是、诱发癌症的责任问题比小花猫到底钓了什么鱼更加复杂:譬如就算常年吃马兜铃酸类中草药的患者得了尿路上皮癌或者肾癌、他都没法去申诉赔偿、这是因为你根本没法证明你的癌是以马兜铃酸类草药为主导引发的——日常生活中各种致癌物质、致癌环境、致癌生活方式实在太多了、每一种角色都在对你的癌症形成捅刀子、但目前的科学你常常无法确切锁定每一个个例患者中、到底每一个癌症风险捅了你具体几刀子、究竟是从犯还是主犯。
所以、在慢性风险尤其癌症上、出了事情对不起、所有问题请你自己扛。
你能做到的最佳善待自己的方式、就是从一开始就不要让捅刀子的歹徒有机会靠近你。
怎么才能知道是不是歹徒?靠科研、靠临床试验。
尤其临床试验理应是药物批准道路上必不可少的环境、因为临床试验是针对人进行的、而你生病的时候服药的不是你家猫狗、是你本人、而你是一个人。
这一个环节是不可以跳跃的。
除了癌症以外呢?我再举一个真实案例、发生在距今60年前的故事。
各位体会一下60年前有一款西药:Thalidomide——商品名『反应停』、短期内突然在全球如雷贯耳、赫赫有名。
这种中枢神经抑制剂有着非常良好的镇静催眠、以及极其有效的妊娠反应抑制作用、由当时西德药厂Chemie Grünenthal研发完成、1957年欧洲上市、人气爆发、席卷欧洲、日本、澳洲甚至拉美。
大伙儿都惊呆了:这款药物是如此好用易用、而且几乎没有表现出任何副作用、孕妇最痛苦的那几个月里难道还可能有更好的药物伴侣吗?!然而这么『好』的东西却竟然没有能够进入美国。
绝不是因为不想进去、而是美国FDA对这款药物实施了极其冗长繁琐严苛的调查研究、而且有好几位官员表态了顾虑:该药动物实验结果和人体实验结果差距很大(请回味前文提到的2018年新规则第二要点:②只需要提供临床试验之前基于动物或体细胞的药理与药物毒性研究即可、同时再度品味一下临床人体试验为何不可或缺)、由此怀疑动物实验所获毒理学数据的可靠性。
其中最重要的人物就是FDA的一位女性药理学家:Frances Oldham Kelsey。
↑我心目中的女英雄——Frances Oldham Kelsey。
Frances Oldham Kelsey死死顶住了来自药厂和其他方面的压力、反反复复反反复复强调一句话:『还要研究、还要研究、还要研究』。
药厂Richardson-Merrell要求药物获得上市批准的申请提出了多达六次、结果每一次都被无情拒绝。
理由每一次就是这样:继续研究、报告结果。
药厂几乎要疯了。
就这样拖拖拉拉到最后、这款药物最终没有能够撬开美国的大门。
然而后来的事实证明、这简直是美国人民、尤其是美国准妈妈们的大幸——几年后的1960年代初开始、欧洲和日本相继发现新生儿畸形比例异常飙升、引发警觉以及相继而至的流行病学研究、然后锁定了反应停和新生儿畸形之间的相关性。
这下开始慌了、开始严格调查反应停的毒理、遂发现反应停对于灵长类动物的强烈致畸性。
1961年秋天Chemie Grünenthal公司撤回西德市场上所有反应停、立即其他国家都跟进、但已经晚了——因反应停而先天畸形的新生儿人数超过一万(还有估计超过10万的)、还有无数因反应停导致的本可避免的流产案例。
此事在日本引发巨大社会反响、甚至一度对西药产生恐慌。
然而美国人民在FDA的保护下幸免于难(即便如此由于临床试验以及其他途径进入美国的药物、美国本土依然有17名孩子出生携带了反应停所导致的先天畸形。
然而试想若没有FDA的严苛、这个数字将要在美国翻多少倍?!)。
↑反应停:人体毒理没有洞察透彻的代价。
Frances Oldham Kelsey因此成为很多人眼中的女英雄(在我心里绝逼是、永远是)、1962年获得肯尼迪总统授予的『杰出联邦公民服务总统奖』、2010年9月美国FDA再度授予她以她的姓命名的Kelsey奖。
老太太身体非常好、一直活到2015年8月、享年101岁。
总统对她表示感谢。
这就是美国FDA的价值。
这也就是为什么在我眼里美国FDA的观点和言论具有最高等级可信度的原因之一。
不是说FDA永远正确、FDA永远不会犯错、FDA不可能存在腐败、并非如此。
而是我想说:假如某个事件上连美国FDA都可能出错的话、那其他国家FDA体系出错的概率至少不会低于美国FDA。
而中国的CFDA?我能说的话已经说尽、我还能做的就是微笑。
想想至今还盛行着的种类丰富的中药注射剂(今年七月刚刚再度出事、因为严重不良反应召回了两款)、以及十年过去了才刚刚批准的在美国已经几乎失去了市场份额的宫颈癌疫苗、我不知道这一切到底是笑话还是孝话。
不要忘记:反应停事件发生在上世纪50年代末、距今60年。
60年过去了、我们的FDA和美国的FDA、扪心给自己三个问题:要不要比?比什么?怎么比?讲真、即便严格依照美国FDA流程旷日持久成本高昂地完成包括临床试验在内的所有三期考察、都不能100%确保药物上市之后完全没有问题、所以FDA才设置了第四期、也就是上市后观察期——哪怕FDA的四期都无法完全压住潘多拉魔盒、总有一丝缝隙里飞出意想不到的幺蛾子——直接跳开临床试验的话会飞出什么东西、多少东西就只能任凭各位自己想象了。
