红霉素杂质总结分享
青霉素杂质总结分享

青霉素杂质总结分享
序号
名称
CAS
分子式
规格
用途
结构式
1
Penicillin Impurity 1
37727-80-3C8H14N2O4S
10mg 25mg 50mg 100mg
研发申报
2
Penicillin Impurity 2
1978372-79-0
C16H24N4O6S
2
10mg 25mg 50mg 100mg
研发申报
3
Penicillin Impurity 3
76350-36-2C8H10ClNO5S
10mg 25mg 50mg 100mg
研发申报
4
Penicillin Impurity 4
97299-13-3
C14H19N2O4S
.K
10mg 25mg 50mg 100mg
研发申报
5
Penicillin Impurity 5
501-34-8C15H20N2O3S
10mg 25mg 50mg 100mg
研发申报
湖北瑞诺医药---专注杂质对照品、标准品:①维格列汀杂质②硼替佐米杂质③拉米夫定杂质④阿格列汀杂质⑤奥氮平杂质q:300-
⑥克拉霉素杂质⑦波舒替尼杂质⑧氨氯地平杂质⑨阿齐沙坦杂质⑩舒更葡糖钠杂质-8058-⑪普拉克索杂质⑫瑞戈非尼杂质⑬莫西沙星杂质
⑭美罗培南杂质
⑮瑞舒伐他汀杂质
-303
⑯己酮可可碱杂质
......等更多项目品种
并代理:CP/EP/USP/TRC/TLC/MC/LGC/RHINO 等品牌。
红霉素提取工艺

,废液可用于其他工业生产过程,减少废弃物排放。
03
清洁生产技术应用
采用清洁生产技术,如绿色溶剂替代、酶法提取等,减少对环境的影响
。
未来发展趋势预测
连续化、自动化生产
随着科技的不断进步,红霉素提取工艺将向连续化、自动化方向 发展,提高生产效率和质量稳定性。
智能化技术应用
利用人工智能、大数据等技术手段对红霉素提取过程进行智能化 控制和管理,实现精准化生产。
利用超临界流体(如CO2)对红霉素进行萃取。优点是提取效率高,且操作条 件温和,避免了对红霉素结构的破坏。缺点是设备投资大,操作技术要求高。
微波辅助提取法
利用微波加热原理,加速红霉素在溶剂中的溶解和扩散。优点是提取时间短, 效率高,且节能环保。缺点是可能对红霉素结构造成一定影响,且需要进一步 优化提取条件。
中间条件试验
03
在加速试验和长期试验之间设定一组中间条件,进一步了解红
霉素产品在不同条件下的稳定性变化。
06
红霉素提取工艺优化与改 进方向
提高原料利用率途径探讨
原料预处理
通过物理或化学方法对 原料进行预处理,如破 碎、浸泡、酶解等,以 提高有效成分的提取率 。
提取溶剂选择
针对不同原料特性,选 择适宜的提取溶剂,如 乙醇、丙酮、乙酸乙酯 等,以提高目标成分的 溶解度和提取效率。
红霉素提取工艺
演讲人:
日期:
目 录
• 红霉素概述 • 红霉素提取原料与预处理 • 红霉素提取方法与工艺流程 • 红霉素纯化与分离技术 • 红霉素产品质量控制与分析方法 • 红霉素提取工艺优化与改进方向
01
红霉素概述
红霉素结构及性质
化学结构
红霉素是一种大环内酯类抗生素 ,具有内酯环结构,通过糖苷键
红霉素的发酵、提炼工艺及过程

第三节红霉素的发酵、提炼工艺及过程红霉素的产生菌是红色链霉菌(5zrfA‘帅yc‘‘fr)/jA雕M)。
红霉京是多组分的抗生素,其中红留素A为有效组分,红霉素B、红霉素c为杂物。
国产红霉素中c为主要杂质。
红霉素c和A的结构极为相似,但红霉京c抗菌活性比A低很多,其毒性却是它的2 倍。
由于两者在提炼过程难以分离,故要提高产品质量、提高产品的抗菌活性和降低毒性(即减少成品中的红霉素C含量)。
一、菌种我国20世纪60年代开始红霉素的工业生产,采用的产生菌是门2—102菌株,生产水平不高,并易产生噬茵体污染。
随后,选育了抗噬菌体的菌株,并使用自然分离、紫外线、氮芥子气、硫酸二乙酯、亚硝酸、激光及快速中子处理等方法选育高产菌种。
随着菌种选育的发展,从控制红霉素生物合成的代谢路线进行定向筛选,得到抗乙琉氨酸的菌株,并采用原生质体融合的方法获得高产优质的菌种。
经生产实践,其红霉京A的含量高,c的含量低,结合工艺控制条件的改进,发酵单位提高I叫左右点证了成品的质量。
二、发酵工艺及过程(一)发酵工艺流程沙土袍子羊至罕字十母瓶斜面袍子(二)发酵工艺要点I.种子红霉素斜面袍子培养基是由玉米浆、淀粉、氯化钠、硫酸铵等组成。
其中玉米浆质量对袍子的外观及生产能力有直接影响,会出现“黑点”(即灰色焦状茵落)。
有的生产厂以蛋白陈代替玉米浆会使黑点减少甚至不出现,但其袍子量少。
袍子培养基消毒后必须快速冷却为妥,过长对袍子生长不利。
温度37℃,湿度要求50%左右,母瓶斜面培养9d,子瓶斜面培养7d。
要求成熟的把子呈深米黄色,色泽新鲜、均匀、无黑点,把子瓶背面有红色色素,并要求每瓶的袍子数不低于1亿个。
将子瓶斜面把子制成袍子悬浮液,用微孔接种的方式接人种子罐。
种子罐及繁殖罐的培养基由花生饼粉、蛋白陈、硫酸铵、淀粉、葡萄糖等组成。
种子罐的培养温度为35℃,培养时间65h左右;繁殖罐培养温度33℃,培养时间40h左右。
均按移种标准检查,符合要求进行移种。
青霉素杂质汇总

5985-13-7
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
青霉素杂质4
Benzylpenicillin Impurity 4
(Benzylpenicillin EP Impurity D)
13093-87-3
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
Benzylpenicillin
Impurity 5
青霉素杂质5 (Benzylpenicillin EP
N/A
Impurity E)
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
扬信医药代理各品种杂质对照品:舒更葡糖钠杂质,达托霉素杂质,依维莫司杂质,他克莫司杂质,阿奇霉素杂质,克拉维酸钾杂质, 红霉素杂质,克拉霉素杂质,林可霉素杂质,罗红霉素杂质,克林霉素杂质,恩曲他滨杂质,艾地那非杂质,瑞卢戈利杂质,艾氟康唑
杂质等;并提供COA、NMR、HPLC、MS等结构确证图谱;详情请点 用户名 ,谢谢!
专业<杂质对照品>解决方案,代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM/STD等品牌。
青霉素杂质列表集
中文名称
英文名称
CAS
青霉素杂质1
Benzylpenicillin Impurity 1
(Benzylpenicillin EP Impurity A)
551-16-6
规格
10mg 25mg 50mg 100mg 更大规格请咨询
用途
项目报批 纯度高于98%
结构式
青霉素杂质2
罗红霉素杂质汇总
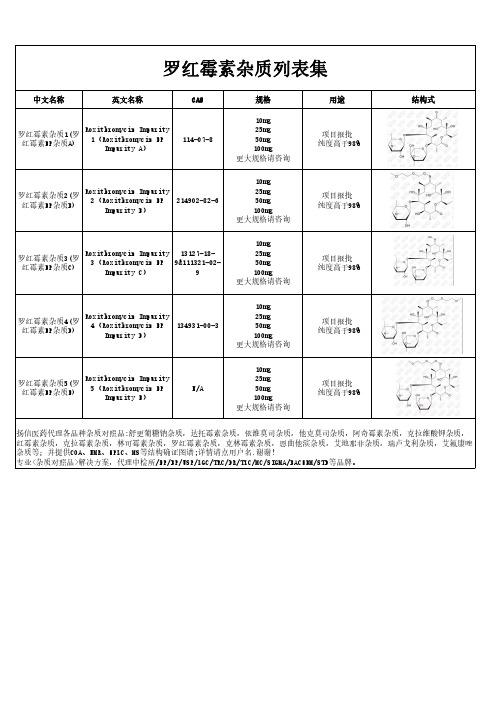
扬信医药代理各品种杂质对照品:舒更葡糖钠杂质,达托霉素杂质,依维莫司杂质,他克莫司杂质,阿奇霉素杂质,克拉维酸钾杂质, 红霉素杂质,克拉霉素杂质,林可霉素杂质,罗红霉素杂质,克林霉素杂质,恩曲他滨杂质,艾地那非杂质,瑞卢戈利杂质,艾氟康唑 杂质等;并提供COA、NMR、HPLC、MS等结构确证图谱;详情请点用户名,谢谢! 专业<杂质对照品>解决方案,代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM/STD等品牌。
9
10mg 25mg 50mg 100mg 更大规格请咨询
用途
项目报批 纯度高于98%
项目报批 纯度高于98%
项目报批 纯度高于98%
结构式
Roxithromycin Impurity 罗红霉素杂质4(罗
红霉素EP杂质D) 4(Roxithromycin EP 134931-00-3 Impurity D)
10mg 25mg 50mg 100mg 更大规格请咨询
ቤተ መጻሕፍቲ ባይዱ
罗红霉素杂质5(罗 Roxithromycin Impurity
5(Roxithromycin EP
N/A
红霉素EP杂质E)
Impurity E)
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
项目报批 纯度高于98%
214902-82-6
红霉素EP杂质B)
Impurity B)
10mg 25mg 50mg 100mg 更大规格请咨询
Roxithromycin Impurity 13127-18-
罗红霉素杂质3(罗 3(Roxithromycin EP 9&111321-02-
红霉素杂质总结分享
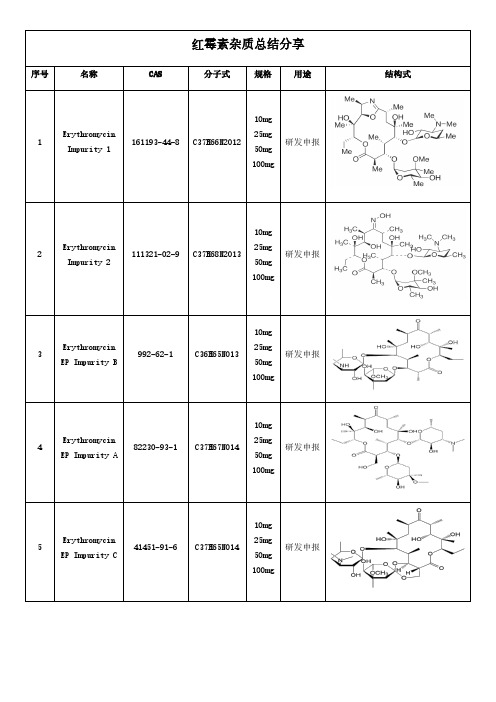
1
161193-44-8 C37H66N2O12
研发申报
Impurity 1
50mg
100mg
10mg
Erythromycin
25mg
2
111321-02-9 C37H68 2
50mg
100mg
Erythromycin 3
EP Impurity B
992-62-1
C36H65NO13
10mg 25mg 50mg 100mg
研发申报
10mg
Erythromycin
25mg
4
82230-93-1 C37H67NO14
研发申报
EP Impurity A
50mg
100mg
10mg
Erythromycin
25mg
5
41451-91-6 C37H65NO14
研发申报
EP Impurity C
维格列汀杂质硼替佐米杂质拉米夫定杂质阿格列汀杂质己酮可可碱杂质300克拉霉素杂质波舒替尼杂质氨氯地平杂质阿齐沙坦杂质舒更葡糖钠杂质8058普拉克索杂质瑞戈非尼杂质莫西沙星杂质美罗培南杂质瑞舒伐他汀杂质303奥氮平杂质
序号
名称
红霉素杂质总结分享
CAS
分子式
规格 用途
10mg
Erythromycin
25mg
50mg
100mg
结构式
湖北瑞诺医药---专注杂质对照品、标准品: ①维格列汀杂质 ②硼替佐米杂质 ③拉米夫定杂质 ④阿格列汀杂质 ⑤己酮可可碱杂质 300⑥克拉霉素杂质 ⑦波舒替尼杂质 ⑧氨氯地平杂质 ⑨阿齐沙坦杂质 ⑩舒更葡糖钠杂质 8058-
⑪普拉克索杂质 ⑫瑞戈非尼杂质 ⑬莫西沙星杂质 ⑭美罗培南杂质 ⑮瑞舒伐他汀杂质 303
阿奇霉素杂质汇总(1)

中文名称英文名称CAS规格用途结构式阿奇霉素杂质1(阿奇霉素EP杂质A)Azithromycin Impurity1(Azithromycin EPImpurity A)76801-85-910mg25mg50mg100mg更大规格请咨询项目报批纯度高于98%阿奇霉素杂质2(阿奇霉素EP杂质B)Azithromycin Impurity2(Azithromycin EPImpurity B)307974-61-410mg25mg50mg100mg更大规格请咨询项目报批纯度高于98%阿奇霉素杂质3(阿奇霉素EP杂质C)Azithromycin Impurity3(Azithromycin EPImpurity C)620169-47-310mg25mg50mg100mg更大规格请咨询项目报批纯度高于98%阿奇霉素杂质4(阿奇霉素EP杂质D)Azithromycin Impurity4(Azithromycin EPImpurity D)612069-26-810mg25mg50mg100mg更大规格请咨询项目报批纯度高于98%阿奇霉素杂质5(阿奇霉素EP杂质E)Azithromycin Impurity5(Azithromycin EPImpurity E)612069-27-910mg25mg50mg100mg更大规格请咨询项目报批纯度高于98%阿奇霉素杂质6(阿奇霉素EP杂质F)Azithromycin Impurity6(Azithromycin EPImpurity F)612069-28-010mg25mg50mg100mg更大规格请咨询项目报批纯度高于98%阿奇霉素杂质7(阿奇霉素EP杂质G)Azithromycin Impurity7(Azithromycin EPImpurity G)612069-31-510mg25mg50mg100mg更大规格请咨询项目报批纯度高于98%阿奇霉素杂质8(阿奇霉素EP杂质H)Azithromycin Impurity8(Azithromycin EPImpurity H)612069-30-410mg25mg50mg100mg更大规格请咨询项目报批纯度高于98%阿奇霉素杂质9(阿奇霉素EP杂质I)Azithromycin Impurity9(Azithromycin EPImpurity I)172617-84-410mg25mg50mg100mg更大规格请咨询项目报批纯度高于98%阿奇霉素杂质10(阿奇霉素EP杂质J)Azithromycin Impurity10(Azithromycin EPImpurity J)117639-41-110mg25mg50mg100mg更大规格请咨询项目报批纯度高于98%扬信医药代理各品种杂质对照品:舒更葡糖钠杂质,达托霉素杂质,依维莫司杂质,他克莫司杂质,阿奇霉素杂质,克拉维酸钾杂质,红霉素杂质,克拉霉素杂质,林可霉素杂质,罗红霉素杂质,克林霉素杂质,恩曲他滨杂质,艾地那非杂质,瑞卢戈利杂质,艾氟康唑杂质等;并提供COA、NMR、HPLC、MS等结构确证图谱。
红霉素链霉菌发酵液中提取红霉素

目录目录 (1)一、设计背景 (1)1.1、红霉素简介 (1)1、抗生素分为 (1)2、红霉素的作用及应用范围: (1)3、目前市场上的主要红霉素商品有: (1)1.2、红霉素的生物合成 (2)合成机理 (2)1.3、红霉素的生产原理及步骤 (2)二、红霉素的生产流程 (2)2.1、一般流程 (2)2.2、发酵工艺要点 (2)1、种子 (2)2.培养基 (3)(1)碳源: (3)(2)氮源: (3)(3)前体: (3)3.培养条件的控制 (3)(1)通气和搅拌: (3)(2)温度: (3)(3)pH: (3)(4)中间补料: (3)(5)通氨: (4)(6)发酵液浓度的控制: (4)(7)泡沫与消沫 (4)2.3、发酵液的成分和提取难度分析 (4)1、发酵液的成分 (4)2、红霉素的分离提纯具有以下特点: (4)三、提取红霉素的方法选择 (4)3.1、预处理 (5)1、预处理的目的: (5)2、发酵液预处理的常用方法: (5)(1)加水稀释法和加热法: (5)(2)调节PH值: (5)(3)凝聚和絮凝: (5)(4)使用惰性助滤剂: (5)(5)使用反应剂: (5)(6)膜处理 (5)(7)离心: (5)3、预处理方法的选择 (5)3.2、固液分离及粗提取 (6)3.3、分离纯化 (6)1、传统的提取工艺——溶媒萃取法 (6)(1)原理: (6)(2)缺点: (6)(3)实际生产中还存在的问题 (7)(4)改进方案——溶媒萃取结合中间盐沉淀法 (7)2、萃取法提取红霉素的改进技术 (8)(1)固定床溶剂萃取法 (8)(2)以乙酸仲丁酯为萃取剂 (8)(3)薄膜浓缩法 (8)(4)双水相萃取 (9)(5)相转变萃取 (9)3、盐析法 (9)4、膜分离技术的应用 (9)(1)50nm陶瓷膜过滤 (10)(2)超滤——纳滤 (10)(3)100nm陶瓷膜微滤——纳滤 (10)5、大孔树脂吸附法的应用 (10)3.4、各种分离纯化方法的比较: (11)四、工艺流程设计 (12)4.1、总工艺流程图: (12)1、工艺过程 (12)(1)絮凝剂 (13)(2)超滤 (13)(3)纳滤膜浓缩系统 (13)(4)萃取、结晶 (14)(5)EA(挥发性有机物萃取吸收)系统 (14)2、优点分析 (15)第2页一、设计背景1.1、红霉素简介1、抗生素分为:1、β-内酰胺类如青霉素类、头孢类等。
红霉素

滴加甲醇钠的温度应在-5℃,滴加甲氧基乙氧基 氯甲醚的温度应控制在≤-10℃,该条件反应时罗 红霉素的收率为 105%以上。
适应症
罗红霉素的抗菌谱和抗菌作用基本上与红 霉素相仿,对革兰阳性菌的作用较红霉素 略差,对嗜肺军团菌的作用较红霉素强。 对肺炎衣原体、肺炎支原体、溶脲脲原体
的抗微生物作用与红霉素相仿或略强。
抗菌谱与红霉素、罗红霉素等相同,但对革兰阳 性菌如链球菌属、肺炎球菌、葡萄球菌的抗菌作 用略优,且对诱导产生的红霉素耐药菌株亦具一 定抗菌活性。克拉霉素及其在体内的代谢产物对
流感杆菌的抗菌作用增强。
地红霉素
由德国 Boehring-Ingelheim的子公司 Dr Karl Thome GmbH 公司合成, 该公司于 1985 年将其许可证转让给美国EliLilly公 司, 该产品于 1993 年在西班牙首次上市,
罗红霉素C41H76N2O15
德国制药商赫希斯特公司于1987年首 次合成了罗红霉素。
化学合成
第一步:把红霉素或硫氰酸红霉素转 化成红霉素肟。 第二步:肟羟基与甲氧基乙氧基氯在 碱性条件下反应生成罗红霉素。
马昌东 徐鸿 李新柱 谢四清 硫氰酸红霉素与盐酸羟胺反应生成红霉素 A-9-肟, 红霉素肟与甲氧基乙氧基氯甲醚反应生成罗红霉 素。 实验研究了反应温度、反应时间对罗红霉素质量 的影响,得到优化的反应条件为: 甲醇钠及甲氧 基乙氧基氯甲醚的滴加时限为 10 min、30 min,
1995 年FDA批准地红霉素在美国销售,
1999 年地红霉素及其片剂被美国药典
XXIII Tenth Supplement 收载。
地红霉素C42H78N2O14
合成方法
安明 常珍 高雷 李眉
制药设备基础期末作业《红霉素及其生产工艺》

放。
可持续发展战略在红霉素生产中的应用
绿色生产工艺
采用先进的生产工艺和设备,提高原料利用率和产品质量, 减少生产过程中的能源消耗和废弃物排放,实现绿色生产。
资源循环利用
对红霉素生产过程中产生的废弃物进行回收利用,如废菌 丝体可用于生产有机肥料或饲料,废滤料可用于生产建筑 材料等,实现资源的循环利用。
05 红霉素生产的环保与可持 续发展
环保法规与标准
环保法规
国家出台了一系列环保法规,如《环境保护法》、《大气污染防治法》等,对制 药企业的生产活动进行严格监管,确保企业遵守环保法规,降低对环境的污染。
环保标准
针对制药行业,国家制定了相应的环保标准,如《制药工业水污染物排放标准》 、《制药工业大气污染物排放标准》等,规范制药企业的污染物排放,保障环境 质量。
检测方法
红霉素的检测方法主要包括高效液相色谱法(HPLC)、微生物效价测定法和分 光光度法等。这些方法能够准确、快速地测定红霉素的含量和杂质,保证产品 质量。
生产过程中的质量控制
原料控制
对原料进行严格的质量控制,包括来 源、纯度、微生物污染等方面的检测, 确保原料符合生产要求。
工艺控制
对生产工艺进行严格控制,包括反应 条件、反应时间、溶剂选择等,确保 生产过程的稳定性和可重复性。
培养基配制
发酵条件控制
根据菌种需求,配制适宜 的培养基,提供菌体生长 和红霉素合成的营养。
控制温度、pH值、溶氧 等发酵参数,优化红霉
素产量。
发酵过程监控
实时监测发酵液中的红霉素 含量、菌体生长情况等,确
红霉素提取工艺

四.红霉素的分离提取工艺
1.发酵液的预处理 2.红霉素分离提取的方法 (1)离子交换法 (2)有机溶剂萃取法 (3)膜分离法 3.浓缩与结晶 4.成品干燥
1、发酵液的预处理
在发酵生产中,发酵液中存在大量菌丝体、菌 种代谢产物、剩余培养基以及抗生素主要组分以 外的其他复合组分。所以,在抗生素提取、精制 之前,必须进行预处理、过滤,以除去这些干扰 物质。 预处理的方法完全取决于可分离物质的性质, 如对PH和热的稳定性、是蛋白质还是非蛋白质、 分子的质量和大小等等。具体方法主要有以下几 种:
2、提纯方法简介
2.1离子交换法 由于红霉素为大分子的碱性化合物,在水溶 液中能电离为带正电的阳离子化合物,故可采用 阳离子交换树脂来提取红霉素。一般先将树脂转 为钠型或铵型,在接近中性条件下进行吸附,因 为红霉素在pH5.5-7.0的范围内几乎全部电离。 再用碱性的醇溶液自树脂上解吸红霉素,解吸前 先用水、30%及60%的甲醛溶液进行洗涤,洗脱 液再经减压浓缩后进行结晶等。
1.发酵液预处理
(1) 加热法
加热可降低液体的黏度,从而提高过滤的速率
(2)调节悬浮液的pH值
pH值直接影响发酵液中某些物质的电离度和电荷性质,因 此适当调节发酵液的PH值可改善其过滤特性。
(3)凝聚与絮凝
凝聚和絮凝技术能有效地改变细胞、菌体和蛋白质等胶体 粒子的分散状态,使聚集起来,增大体积,以便于过滤。
三.红霉素的分离具有以下特点:
①目标产物浓度低。在发酵液中,红霉素的浓度很 低,约占0.14%、0.18%。分离对象的初始浓度 越低,分离提纯的成本就越高; ②红霉素的性质不很稳定,且发酵液容易被污染, 这就对能够采用的分离技术手段造成了严格的限 制; ③红霉素发酵液中杂质的浓度相对较高,其中一些 杂质的性质和红霉素很相似,用一些常规的分离 技术无法将它们分离以获得高纯度的红霉素产品 ④红霉素往往直接作为医药用品,需要符合特殊的 质量和安全要求。
红霉素杂质谱[最新]
![红霉素杂质谱[最新]](https://img.taocdn.com/s3/m/189636c6a5e9856a5712608f.png)
伪红
7 N-formyl 红霉素A 不明 文献报道
8 红霉素D 发酵过程 文献报道
红霉素杂质谱[最新]
红霉素杂质谱
编号 杂质名称 结构式 产生途径 备注
红霉素F 1 发酵过程 EP收载 (杂质A)
R1=OH,R2=CH 3
N-脱甲基红霉素A 2 发酵过程 EP收载 (杂质B)
R1=H,R2=H
红霉素E 3 发酵过程 EP收载 (杂质C)
脱水红霉素A 酸降解可产4 EP收载 (杂质D) 生
红霉素杂质谱红霉素杂质谱红霉素杂质谱编号杂质名称结构式产生途径备注1红霉素f杂质ar1ohr2ch3发酵过程ep收载2n脱甲基红霉素a杂质br1hr2h发酵过程ep收载3红霉素e杂质c发酵过程ep编号杂质名称结构式产生途径备注红霉素f杂质ar1ohr2ch发酵过程ep收载n脱甲基红霉素a杂质br1hr2h发酵过程ep收载红霉素e杂质c发酵过程ep收载脱水红霉素a杂质d酸降解可产ep收载红霉素a烯醇醚杂质e高温降解可产生epuspcp均收载伪红霉素a烯醇醚杂质f高温降解可产生epcpnformyl红霉素a不明文献报道红霉素d发酵过程文献报道
9-(E)-红霉素A肟杂质的分离与鉴定

9-(E)-红霉素A肟杂质的分离与鉴定孟祥燕;李娜;彭凤;刘瑶;黄鑫;沈永淼【摘要】目的分离、纯化HPLC图谱中紧跟着9-(E)-红霉素A肟的一个未知的杂质,并鉴定它的化学结构.方法通过柱层析色谱法和重结晶法分离该杂质,然后通过1H-NMR、MS、X-射线单晶衍射确定了该杂质的结构.结果实验最终确定了该杂质最佳的分离条件:流动相为CHC13∶C2H5OH∶NH4OH =10.0∶1.2∶0.1,重结晶的溶剂为氯仿和丙酮(V∶V=7∶3).并用双倍稀释法对红霉素A肟和杂质红霉素E 肟进行了抗菌活性研究.结论未知杂质为红霉素E的E式肟化产物,红霉素E肟的抗菌活性远低于红霉素A肟.【期刊名称】《中国抗生素杂志》【年(卷),期】2016(041)004【总页数】5页(P280-284)【关键词】红霉素A肟杂质;红霉素E肟;柱层析分离;结构鉴定;抗菌活性【作者】孟祥燕;李娜;彭凤;刘瑶;黄鑫;沈永淼【作者单位】绍兴文理学院化学化工学院,绍兴312000;浙江震元制药有限公司,绍兴312000;绍兴文理学院化学化工学院,绍兴312000;绍兴文理学院化学化工学院,绍兴312000;绍兴文理学院化学化工学院,绍兴312000;绍兴文理学院化学化工学院,绍兴312000;绍兴文理学院化学化工学院,绍兴312000【正文语种】中文【中图分类】R917红霉素(EA)是目前最广泛使用的高效抗大多数革兰阳性菌和一些革兰阴性菌的大环内脂类抗生素[1]。
由于红霉素在酸性条件下不稳定,红霉素经口服后很容易在胃酸作用下经分子内反应生成无抗菌活性的螺缩酮衍生物,造成生物利用率低[2]。
为了提高其稳定性,人们合成了一系列半合成的红霉素衍生物。
而9-(E)-红霉素A 肟(9-(E)-oxime erythromycin A)则是新一代大环内酯类红霉素衍生物罗红霉素、克拉霉素、阿奇霉素和地红霉素等抗生素的共用中间体(图1)[3]。
因此,对此关键中间体的合成从20世纪60年代开始就一直是国际医药界研究的一个热点,红霉素肟的有关物质的研究与分析也受到很多研究人员的关注[4-7]。
红霉素考点总结

红霉素考点总结
【作用机制】
不可逆地与细菌核糖体50S亚基结合,通过阻断转肽作用及mRNA位移,选择性抑制蛋白质合成。
由于大环内酯类在细菌核糖体50S亚基上的结合点与克林霉素和氯霉素相同,当与这些药物合用时,可发生相互拮抗作用。
【作用特点】
1.速效抑菌,碱性环境中抗菌作用增强。
2.抗菌谱较广
(1)对多数G+菌、G-球菌和部分G-杆菌(流感杆菌、百日咳杆菌、布氏菌、军团菌、弯曲杆菌等)以及螺旋体、放线菌等有良好抗菌活性。
(2)立克次体、衣原体、支原体等对该类药物也高度敏感。
(3)对耐青霉素G的金葡菌也有效。
【临床应用】
1.首选:用于支原体肺炎、沙眼衣原体婴儿肺炎或结肠炎、军团菌病、弯曲杆菌性肠炎或败血症、白喉带菌者的治疗。
2.百日咳。
3.耐青霉素G的金葡菌感染或青霉素适应证但对青霉素过敏者。
【不良反应】
大环内酯类毒性较低,一般很少引起不良反应。
1.胃肠道反应:红霉素口服或静注均可引起胃肠道反应。
2.肝损害。
肝功能不良者禁用红霉素。
3.耳毒性。
4.心脏毒性:特殊不良反应,静脉滴注速度过快时易发生。
X型选择题
1.下列属于红霉素的不良反应是( )。
A.胃肠道反应
B.耳毒性
C.肾毒性
D.心脏毒性
E.肝毒性
【参考答案】ABDE。
解析:本题主要考查红霉素不良反应。
红霉素眼膏的分析与检测.精选PPT

如正在使用其他药品,使用本品前请咨询医师或药师。 流速110m l•m in- 1; 使用后应拧紧瓶盖,以免污染药品。
10. 如正在使用其他药品,使用本品前请咨
询医师或药师。
二、红霉素眼膏含量测定
仪器、药剂: A gilent LC1100 高效液相色谱仪,A
精密称取样品5g,置分液漏斗中,加石油醚80mL,缓缓振摇,使其质溶解,用磷酸盐缓冲液(
(X)绘制标准曲线,回归方程为::Y= pH615)提取4次,每次约25mL,合并提取液,置100mL量瓶中,用磷酸盐缓冲液(pH615)稀释
至刻度,摇匀,配制成每1mL含红霉素15mg的供试品溶液。
32798+ 95934X, r= 019999。结果表明, 孕妇及哺乳期妇女应在医师指导下使用。
分对别本进 品8样过.敏2请0者LL禁,将用记,录本过色敏谱药体图质。品者慎放用。在儿童不能接触的地方。
0)稀释至刻度,摇匀,照红霉素项下的方法测定,即得。 红霉素眼膏使用注意事项 用药部位如有烧灼感、瘙痒、红肿等情况应停药,并将局部药物洗净,必要时向医师咨询。 1mol/L硫酸溶液5ml,置水浴上加热使溶解,冷却,倾取水层,加硫酸2ml,缓缓摇匀,即显红棕色
0)提取4次,每次约25ml,合并提取液,置100ml量瓶中,加磷酸盐缓冲液(pH 7.
红霉素在进样量310~ 80Lg 的范围内,峰 0)提取4次,每次约25ml,合并提取液,置100ml量瓶中,加磷酸盐缓冲液(pH 7.
结果表明,红霉素在进样量310~ 80Lg 的范围内,峰面积与进样量之间呈良好的线性关系。 使用后应拧紧瓶盖,以免污染药品。
质量检查
可见异物 粒度 沉降体积比 金属性异物 重量差异 装量 渗透压摩尔浓度 无菌
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
100mg
Erythromycin 3
EP Impurity B
992-62-1
C36H65NO13
10mg 25mg 50mg 100mg
研发申报
10mg
Erythromycin
25mg
4
82230-93-1 C37H67NO14
研发申报
EP Impurity A
50mg
100mg
10mg
Erythromycin
⑪普拉克索杂质 ⑫瑞戈非尼杂质 ⑬莫西沙星杂质 ⑭美罗培南杂质 ⑮瑞舒伐他汀杂质 303
⑯奥氮平杂质 ......等更多项目品种 并代理:CP/EP/USP/TRC/TLC/MC/LGC/RHINO 等品牌
25mg
5
41451-91-6 C37H65NO14
研发申报
EP Impurity C
50mg
100mg
结构式
湖北瑞诺医药---专注杂质对照品、标准品: ①维格列汀杂质 ②硼替佐米杂质 ③拉米夫定杂质 ④阿格列汀杂质 ⑤己酮可可碱杂质 300⑥克拉霉素杂质 ⑦波舒替尼杂质 ⑧氨氯地平杂质 ⑨阿齐沙坦杂质 ⑩舒更葡糖钠杂质 8058-
序号
名称
红霉素杂质总结分享
CAS
分子式
规格 用途
10mg
Erythromycin
25mg
1
161193-44-8 C37H66N2O12
研发申报
Impurity 1
50mg
100mg10mg来自Erythromycin
25mg
2
111321-02-9 C37H68N2O13
研发申报
Impurity 2
50mg
