2013年广州市高三一模化学试题及评分标准
广东省广州市2013届高三毕业班综合测试化学试题(一) 2013广州一模

O HO O C-H
CHO
HO
OH
、 (4)CD (2 分)
O CH2 CH CH2 O C
、
HO
OH
CH3 O C CH3
(5)取代(2 分) ;
(3 分)
31. (16 分) (1)3HCl (2 分) (2) (5 分) ① H3PO3 - 1 起始时各物质浓度(mol•L ) 0.10 - 1 反应的各物质的浓度(mol•L )2.5×10-2 平衡时各物质的浓度(mol•L-1)0.10-2.5×10-2
2NaAlO2+CO2↑
(2)碱 (1 分) ; 提高浸取速率(2 分) (3)HCO3- + OH- =H2O + CO32- (4)Na2CO3 、CO2 (4 分)
(3 分)
33. (16 分) (1)过滤 ;分液漏斗 (共 4 分,各 2 分) (2)除去杂质; (2 分) (3) (8 分,每空格 2 分) 实验步骤 步骤 1: 加入过量 2 mol•L-1HCl,充分振荡,再 滴加几滴 0.1 mol•L-1 BaCl2 溶液。 步骤 2: 将试管放入装有沸水的小烧杯中水浴加 热一段时间,取出试管观察。 (4)12.5 (2 分) 预期现象和结论 有白色沉淀生成 试管中有黑色固体生成
H+ + H2PO3- 0 0 - 2 2.5×10 2.5×10-2 2.5×10-2 2.5×10-2
c( H ) c( H 2 PO3 ) 2.5 10 2 2.5 10 2 K 8.3 10 -3 mol•L-1 c( H 3 PO3 ) 0.10 2.5 10 2
5.反应③的反应类型是_____________。在一定条件下,化合物 类似反应③的反应生成有机物Ⅴ。Ⅴ的结构简式是______________。
2013年广东各地一模化学试题汇总2——非选题部分

2013年广东各地一模化学试题汇总2——非选题部分(潮州、东莞、佛山、广州、惠州、茂名、汕头、增城、肇庆、中山、珠海)2013潮州市30.(16分)姜黄素具有抗突变和预防肿瘤的作用,其合成路线如下:化合物I 可以由以下合成路线获得:(1)有机物Ⅳ的分子式为 ,含有官能团的名称为醚键和 。
(2)有机物V 的名称为 ,其生成Ⅵ的化学方程式为(注明反应条件):。
(3)写出一种符合下列条件的Ⅳ的同分异构体的结构简式 。
①苯环上的一硝基取代物有2种 ②1 mol 该物质水解,最多消耗3 molNaOH(4)反应①中反应物的原子利用率为100%,请写出该反应的化学方程式 。
31.(16分)I.甲醇是一种优质燃料,可制作燃料电池。
工业上可用下列两种反应制备甲醇:CO(g) + 2H 2(g) CH 3OH(g) ΔH 1CO 2(g) + 3H 2(g)CH 3OH(g) + H 2O(g) ΔH 2已知:2H 2(g)+ O 2(g) = 2H 2O(g) ΔH 3 。
则2CO(g)+O 2(g) = 2CO 2(g) 的反应热ΔH =__________ ___(用ΔH 1、ΔH 2、ΔH 3表示)。
II.工业上可利用―甲烷蒸气转化法生产氢气‖,反应为:CH 4(g)+H 2O(g)CO(g)+3H 2(g)。
已知温度、压强和水碳比[n(H 2O)/ n(CH 4)]对甲烷平衡含量的影响如下图:甲烷平衡含量(%)水碳比600 甲烷平衡含量(%)温度(℃)图1(水碳比为3)图2(800℃)(1)温度对该反应的反.应速率和平衡移动........的影响是。
(2)其他条件不变,请在图2中画出..压强为2 MPa时,CH4平衡含量与水碳比之间关系曲线。
(只要求画出大致的变化曲线)(3)已知:在700℃,1MPa时,1mol CH4与1mol H2O在1L的密闭容器中反应,6分钟达到平衡,此时CH4的转化率为80%,求这6分钟H2的平均反应速率和该温度下反应的平衡常数是多少?(写出计算过程,结果保留小数点后一位数字。
2013年广东各地一模化学试题汇总--有机试题
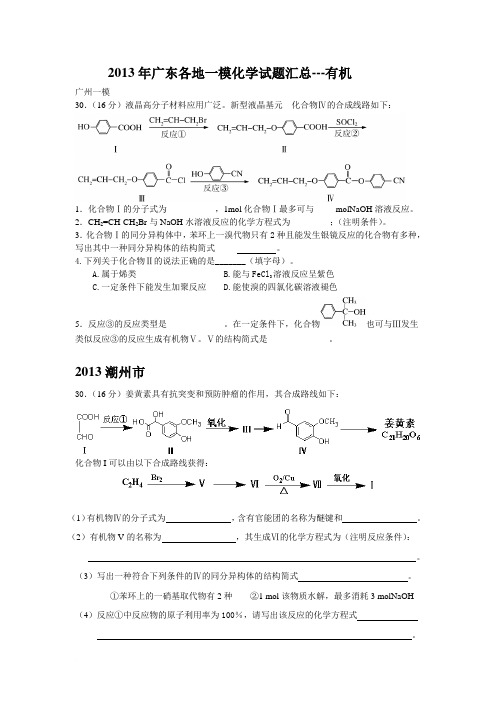
2013年广东各地一模化学试题汇总---有机广州一模30.(16分)液晶高分子材料应用广泛。
新型液晶基元---化合物Ⅳ的合成线路如下:1.化合物Ⅰ的分子式为__________ ,1mol化合物Ⅰ最多可与_____molNaOH溶液反应。
2.CH2=CH-CH2Br与NaOH水溶液反应的化学方程式为_________;(注明条件)。
3.化合物Ⅰ的同分异构体中,苯环上一溴代物只有2种且能发生银镜反应的化合物有多种,写出其中一种同分异构体的结构简式_____ 。
4.下列关于化合物Ⅱ的说法正确的是_______(填字母)。
A.属于烯类B.能与FeCl3溶液反应呈紫色C.一定条件下能发生加聚反应D.能使溴的四氯化碳溶液褪色5.反应③的反应类型是_____________。
在一定条件下,化合物也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ。
Ⅴ的结构简式是______________。
2013潮州市30.(16分)姜黄素具有抗突变和预防肿瘤的作用,其合成路线如下:化合物I可以由以下合成路线获得:(1)有机物Ⅳ的分子式为,含有官能团的名称为醚键和。
(2)有机物V的名称为,其生成Ⅵ的化学方程式为(注明反应条件):。
(3)写出一种符合下列条件的Ⅳ的同分异构体的结构简式。
①苯环上的一硝基取代物有2种②1 mol该物质水解,最多消耗3 molNaOH (4)反应①中反应物的原子利用率为100%,请写出该反应的化学方程式。
2013年东莞30.(16分) 已知:止咳酮(V)具有止咳祛痰作用。
它能由化合物III合成:(1)化合物I的分子式为,化合物Ⅲ的含氧官能团的名称(写一种)。
(2)反应①的反应类型是,反应③的反应类型是。
(3)化合物II与足量H 2在一定条件下加成后的产物能与NaOH溶液反应,写出该反应方程式:。
(4)化合物II也能发生类似②反应得到一种常见的有机溶剂,该物质结构简式为。
(5)写出满足下列条件的IV的同分异构体的结构简式。
2013届广东各地一模试题有机化学汇编

2013届广东各地一模试题有机化学汇编(广州)【广州答案】(深圳)30.(16分)有机合成中增长碳链是一个重要环节。
如下列反应:+Zn 苯(Ⅰ)CH 3Br-CH-COOC2H5(Ⅱ)CH-CH-COOC2H5CH 3OHCH 3-O用 通过以下路线可合成(Ⅱ):(1)(Ⅰ)的分子式为 ;(Ⅲ)的结构简式为 。
(2)(Ⅱ)与足量的热NaOH 溶液反应的化学方程式为 。
(3) 在生成(Ⅲ)时,还能得到另一种副产物C 6H 8O 4,该反应的化学方程式为 ,反应类型是 。
(4)(Ⅰ)的一种同分异构体能发生银镜反应,还能水解生成不含甲基的芳香化合物(Ⅳ)。
(Ⅳ)的结构简式为 。
【深圳答案】30、(16分)说明;所有的化学方程式或结构简式写成一般结构简式或键线式同样得分;化学方程式没有注明反应条件或条件错误扣1分,化学式错误和不配平0分,下同。
(1)C 8H 8O 2 (2分);CH 2=CH-COOH (3分)(2)或 (3分)(3) (3分) 取代反应(或酯化反应) (2分)(4) (3分)(番禺仲元中学等六校联合体)OHCH 3-CH -COOH OHCH 3-CH -COOH 浓H 2SO 4 △ OH CH 3-CH -COOH (Ⅲ)C 3H 4O 2 C 5H 8O 2C 2H 5OH /H + (Ⅱ) HBr一定条件下 CH 32H 5 + 2NaOHH 2O△OHCH 3-CH-COONa + C 2H 5OH + NaBr CH 3 2H 5+ 2H 2O NaOH△ OHCH 3-CH-COOH + C 2H 5OH + HBrOHCH 32 浓H 2SO 4 △ CH 3-CHCH-CH 3 O —CO C —O + 2H 2O CH 2OH30.(16分)黄酮醋酸(F )具有独特抗癌活性,它的合成路线如下:已知:RCN 在酸性条件下发生水解反应:(1)已知A 转化为B 的同时还生成了乙酸,则A 的结构简式为 ,该反应类型是 。
2013广州高三3月毕业班综合测试试题(一模)质量分析

31.原理题
组别 均分
难度 0.51 区分度 0.47 平均分 8.08
3 8.34 4 7.5 5 6.17 6 5.37 7 8.16
1 2 10.37 9.12
全卷难度最大,暴露知识盲点,存在的主要问题有: 3.定势思维 (1)起始浓度-转化浓度≈起始浓度 (2)Na2HPO3有H就是酸式盐,酸式盐溶液就呈酸性 (3)碘水也看作是Br2
31.原理题
组别 均分
难度 0.51 区分度 0.47 平均分 8.08
3 8.34 4 7.5 5 6.17 6 5.37 7 8.16
1 2 10.37 9.12
后阶段任务: 3.建构解决不同问题的思维模式,有理可循、切中分点 (1)利用平衡移动原理解释问题 (2)书写各种方程式的思考顺序
31.原理题
组别 均分
难度 0.51 区分度 0.47 平均分 8.08
3 8.34 4 7.5 5 6.17 6 5.37 7 8.16
1 2 10.37 9.12
全卷难度最大,暴露知识盲点,存在的主要问题有: 2.基本概念模糊 (1)K电离表达式 (2)阴极得/失电子 (3)亚磷酸具有还原性 (4)P元素最高价态 (5)“==”与“ ”
32.流程题
组别 均分
难度 0.6
区分度 0.44 平均分 9.54
4 8.98 5 7.66 6 6.74 7 10.05
1 2 3 11.77 10.52 9.79
3.非氧化还原反应书写折射出来的问题 (1)复习脱离课本 (2)不掌握物质的性质 (3)没有建构有效的分类观 4.不理解工艺流程中的专业术语 (1) “循环利用”错以为“回收利用”
2013年广东省普通高中学业水平考试化学试题-解答

2013年6月广东省普通高中学业水平考试化学试题解答本试卷共8页,65题,满分100分。
考试用时90分钟。
注意事项:1、答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考生号、试室号和座位号填写在答题上。
用2B铅笔将试卷类型(A)填涂在答题卡相应位置上。
将条形码横贴在答题卡右上角“条形码粘贴处”。
2、每题选出答案后,用2B铅笔把答题卡上对应题目选项的答案信息点涂黑,如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上.3、考生必须保持答题卡的整洁。
考试结束后,将试卷和答题卡一并交回。
可能用到的相对原子质量:H1,C12,N14,O16,C135.5,Ca40,Fe56一、单项选择题Ⅰ:本大题共30小题,每小题1分,共30分。
在每小题列出的四个选项中,只有一项最符合题意。
01、下列词语隐含化学变化的是(A)冰雪消融(B)木已成舟(C)蜡炬成灰(D)水落石出02、下列物质中,属于纯净物的是(A)白酒(B)陈醋(C)食用调和油(D)蔗糖03、3H在月球上储量丰富,4H主要来源于宇宙射线的初级粒子。
下列关于3H和4H的说法正确的是(A)两者互为同位素(B)两者互为同素异形体(C)两者为同一种核素(D)两者具有相同的中子数04、硅是无机非金属材料的主角,其元素符号是(A)S (B)Si (C)B (D)Be05、乙烯产量是衡量一个国家石油化工发展水平的标志。
下列关于乙烯说法正确的是(A)与乙烷互为同分异构体(B)分子中存在C≡C(C)能使酸性高锰酸钾溶液褪色(D)分子中存在C=O06、关于合金说法正确的是(A)合金为化合物(B)合金具有金属特性(C)合金都耐腐蚀(D)合金的硬度一定比成分金属的低207、漂白粉可由Cl 2通入消石灰中制备。
漂白粉的有效成分是(A )Ca (OH )2 (B )CaCl 2 (C)Ca (ClO)2 (D )CaCO 308、原子结构示意图为 的元素是(A)Li (B )Na (C)Al (D)K09、分类是学习和研究化学的一种重要方法,下列分类合理的是(A )K 2CO 3和K 2O 都属于盐 (B )H 2SO 4和HNO 3都属于酸(C )KOH 和Na 2CO 3都属于碱 (D)Na 2O 和Na 2SiO 3都属于氧化物10、下列气体可用固体NaOH 干燥的是(A)CO 2 (B )H 2 (C)SO 2 (D )NO 211、加热蒸发NaCl 溶液的过程中,下列物理量保持不变的是(A )NaCl 溶液的体积 (B )NaCl 的质量分数(C)NaCl 的物质的量 (D)NaCl 的物质的量浓度12、下列常见的物质分离和提纯操作中,将液体蒸发为气体再冷凝为液体的操作是(A )结晶 (B )萃取 (C)蒸馏 (D)过滤13、20℃时,NaCl 溶解于水的实验数据如下表所示 实验序号 水的质量/g 加入的NaCl 质量/g 未溶的NaCl 质量/g①10 2 0 ②10 3 0 ③ 10 4 0。
(有解析)2013年普通高等学校招生全国统一考试(广东卷) 化学试题

2013年普通高等学校招生全国统一考试(广东卷)化学试题可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 S 32 Cl 35.5 Cu63.5一、单项选择题:本大题共16小题,每小题4分,满分64分.在每小题给出的四个选项中,只有一项是符合题目要求的.选对的得4分,选错或不答的得0分。
7.下列说法正确的是A.糖类化合物都具有相同的官能团B.酯类物质是形成水果香味的主要成分C.油脂的皂化反应生成脂肪酸和丙醇D.蛋白质的水解产物都含有羧基和羟基8.水溶解中能大量共存的一组离子是A.Na+、Al3+、Cl-、CO32-B.H+、Na+、Fe2+、MnO4-C.K+、Ca2+、Cl-、NO3-D.K+、NH4+、OH-、SO42-9.设n A为阿伏加德罗常数的数值,下列说法正确的是A.常温常压下,8gO2含有4n A个电子B.1L0.1mol·L-1的氨水中有n A个NH4+C.标准状况下,22.4L盐酸含有n A个HCl分子D.1molNa被完全氧化生成Na2O2,失去个2n A电子1011A.用SO2漂白纸浆和草帽辫B.用硫酸清洗锅炉中的水垢C.高温下用焦炭还原SiO2制取粗硅D.用Na2S做沉淀剂,除去废水中的Cu2+和Hg2+12.50℃时,下列各溶液中,离子的物质的量浓度关系正确的是A.pH=4的醋酸中:c(H+)=4.0mol·L-1B.饱和小苏打溶液中:c(Na+)= c(HCO3-)C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-)D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol·L-1二、双项选择题:本大题共9小题,每小题6分,共54分。
在每小题给出的四个选项中,有两个选项符合题目要求,全部选对的得6分,只选1个且正确的得3分,有选错或者不答的得0分。
22.元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸。
2013年广东各地一模化学试题汇总--有机答案

2013年广东各地一模化学试题汇总---有机答案广州一模30.(16分)(1)C7H6O3(2分); 2 (2分)(2)CH2=CH-CH2Br + NaOH CH2=CH-CH2OH +NaBr (2分)(3)以下其中一种即可:(3分)OOH C-HO、OHCHOOH、OHOHCHO(4)CD (2分)(5)取代(2分);CH2CH CH2O OOCCH3CH3C(3分)2013潮州市30.(16分)(1)C8H8O3(2分),(酚)羟基、醛基(2分,下面每空3分)(2)1,2—二溴乙烷,(3(4)2013年东莞30.(16分)(1)C8H9Br(2分)羰基或酯基(任写一种)(2分)(2)取代反应(2分)加成反应(2分)(3)(3分)(4)(3分)(5)CH3COCH3(2分,写“CH3CH2OH”也给分)Δ2013佛山一模2013年惠州2013茂名市30.(16分)(1)41010O H C ………(2分) (2)……(每空3分,共6分)(3)缩聚反应 …(2分)(4) ……(3分)(5) ……(3分)CC O OONa+ CH CH 2013汕头市期末30.(16分,每空各2分)(1)对苯二甲酸;; (2)HX ;(3); (4)取代(或取代反应);可溶于水;(5)在对苄基氧化时保护苯环侧链烃基(1分);同时,使苄基在反应中既不会被彻底氧化,汕(1)C (2)201330(1)(2) (3)①写错反应物或生成物的其中一个,扣3分,即0分; ②配平错误的,扣1分; ③“→”写成“=”不扣分;④书写苯环的正六边形时,键若有明显的突出,扣1分。
(4)或其他合理答案(2分)(5)2CH 3CHCH 2OH+O 2→2CH 3CHCHO +2H 2O (2分) 氧化(2分)肇庆期末30.(15分)(1)(3分) CH 3CHO (2分) (2)(4分)取代反应(2分) (2分) (3)(2分,化学式1分,反应条件和配平1分)OHOCHO ∣ CH 3 ∣CH 3△Cu(4)(4分)a b (选1个且正确,给2分,错1个0分) (5)(2分)三 肇庆一模(2013-3) 30.(15分)(1)(共2分) C 12H 10O 4 (2)(共3分)或(3)(共3分)(4)(共2分)B (说明:间位和对位2种;羟基与醛基合并,形成苯甲酸和甲酸苯酚酯2种)(5)(共5分)N(2分)(3分)或:2013中山期末15.(14分)(每空2分)1、CH 3CHO ;CH 3CH=CHCHO2、羟基、醛基 3、氧化反应,消去反应(漏“反应”扣1分) 4、CH 3-CH-COOH5、2CH 3CH 2CH 2CH 2OH+COOHCOOH--+2H 2ON+HNO 3NNO 2+H 2ONHO NO 2+NNO 2+H 2OCHO OH+ 2Ag(NH 3)2443 +H 2OCHO OH+ 2Ag(NH 3)243 +H 2OCH CCOONaCOONaONaCH 32013珠海一模2013韶关一模 30.(16分)(1)醛基; CH 2OHCH 2OH (各2分); (2)3; C (各2分); (3)+2NaOH+2NaBr+2H 2O (3分)(4)加成反应; 酯化(取代)反应 (各1分); (5)(各1分,共3分)深圳一模30、(16分)说明;所有的化学方程式或结构简式写成一般结构简式或键线式同样得分;化学方程式没有注明反应条件或条件错误扣1分,化学式错误和不配平0分,下同。
2013年广东省各市高考一模化学试题汇总-工业流程题部分(教师版)

2013年广东各地一模化学试题汇总(工业流程)2013潮州市32.(16分)医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙工艺流程为:已知:查阅资料得知氢氧化物沉淀时的pH为:(1)CaCO3与盐酸反应的离子方程式。
(2)除杂操作是加入氢氧化钙,调节溶液的pH为,目的是除去溶液中少量的Al3+、Fe3+。
检验Fe(OH)3是否沉淀完全的实验操作是________________ 。
(3)过滤时需用的玻璃仪器有。
滤渣主要成分的化学式。
(4)酸化时加盐酸的目的为:①,②防止Ca2+ 在蒸发时发生水解。
(5)为什么蒸发结晶要保持在160℃:。
(6)若所测样品CaCl2·2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为。
答案:(1) CaCO3+ 2H+ =Ca2+ + CO2↑+ H2O(2)5.2~7.8(或之间的任意值);取少量上层清液于小试管中,滴加KSCN溶液,若不显红色,则Fe(OH)3沉淀完全(3) 烧杯、玻璃棒、普通漏斗; Fe(OH)3、Al(OH)3(4)除去过量的氢氧化钙(合理则给分);(5)温度太高CaCl2 ·2H2O会失水(6) Na+没除去析出NaCl,导致测定结果偏高2013东莞市32. (16分)实验室用硫酸厂烧渣(主要成分为Fe2O3及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下:(1)将过程②中产生的气体通入下列溶液中,溶液不会..褪色的是________(填编号);A.品红溶液B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水(2)在①中已知FeS中铁元素生成Fe3+,写出FeS、O2、H2SO4反应的方程式;(3)在③中,需加入的物质是________;(4)在④中,蒸发浓缩需要的硅酸盐仪器除酒精灯外,还有;(5)在⑥中,将溶液Z控制到70~80 ℃的目的是;(6)为测量聚铁样品中铁元素的质量分数,进行下列实验(假设杂质中不含铁元素和硫元素):称取2.700 g 样品,将样品溶于足量的盐酸后,滴加过量的BaCl2;过滤、洗涤、干燥,称量固体的质量为3.495 g。
2013年广州一模 试题及答案

2013年广州市普通高中毕业班综合测试(一)理科综合本试卷共12页,36小题,满分300分。
考试用时150分钟。
一、单项选择题:本题包括16小题,每小题4分,共64分。
在每小题给出的四个选项中,只有一个选项符合题目要求,选对的得4分,选错或不答的得0分。
D. 与等体积pH= 11的NaOH溶液混合后所得溶液中:c(Na+) =c(CH3COO- )13. 水压机是利用液体来传递压强的。
水压机工作时,水分子间A. 只有斥力B. 只有引力C. 既有引力也有斥力,但分子力表现为引力D. 既有引力也有斥力,但分子力表现为斥力14. 如图是压力保温瓶的结构简图,活塞a与液面之间密闭了一定质量的气体。
假设封闭气体为理想气体且与外界没有热交换,则向下压a的过程中,瓶内气体A. 内能增大B. 体积增大C. 压强不变D. 温度不变15. 如图,虚线表示a、b两个相同圆形金属线圈的直径,圆内的磁场方向如图所示,磁感应强度大小随时间的变化关系B=kt(k为常量)。
当a中的感应电流为I时,b中的感应电流为A. OB. O.5IC. ID. 2I16. 如图,细线a和b的一端分别固定在水平地面上,另一端系一个静止在空气中的氢气球,细线与地面的夹角分别为30°和60°。
若a、b受到的拉力分别为T a和T b;,氢气球受到的浮力为F,则A. T a >T bB. T a <T bC. F= T aD. F<T b二、双项选择题:本大题共9小题,每小题6分,共54分。
在每小题给出的四个选项中,有两个选项符合题目的要求,全部选对的得6分,只选1个且正确的得3分,有选错或不答的得0分。
17. 两个核反应方程:C②,其中x1x2各表示某种粒子,则下列说法正确的是A. ①是聚变反应B.②是裂变反应C. X1是D. X2是18. 某正弦交流电的i—t图象如图所示,则该电流的D 瞬时值表达式i =20sin100 t (A)19. 如图在同一竖直平面内,距地面不同高度的地方,以不同的水平速度同时抛出两个小球。
2013年6月广东省普通高中学业水平考试化学试卷和答案(标准版)

化学试卷A 第I 也{共!1血)2013年6月广东省普通高中学业水平考试化学试卷试卷类型:A2013年6月广东省普通髙中学业水平考试化学试卷本试卷共8贞* 65题,淆分100分’专试用时90分钟。
注意事项:1答卷前.考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考生号、试室 号和座位号填宵庄答题卡上。
用2B 铅笔将试卷类型(丸)填涂在答眩R 相 应位置上'将条形码橫贴在答题卡右上角“条形码粘贴处J2. 毎题选岀菩案石*用2B 铅笔耙答题卡上对应题怦选项的答案信息点涂黑* 如需改动*用橡皮擦干净后.再选涂其他答廉.荐案不能鲁在试卷匕。
3. 捋生必须保持答魁甘的整洁 考试结更肓.将试卷和符毬斤一并交冏可能用到的相对原子质・;H1 C 1214 O 16 Na 23 Cl 35. 5 K 39 Mn 553He 在月球上储蜀丰富「He 主要来激于宇宙射线的初级粒子。
下列关于订俺和」Hr •的说 法正确的星 &两者互为同位索 B.两者互为同索异形怵 C.胸背为同一种孩索D.两宵具有相同的中子效施是无机非金属材料的主角,耳元索符号是5.乙烯产兹是衡址-个国家石油化工发展水平的标志一 F 列关于乙烯说法正确的是A.与乙烷互为同分舁构休B.分子中存在C = C®单项选择融I ;本大翳共如小題, 中,只有一项最符合題竄。
L 下列诃信樹含化学变化的是 A+冰雪消融 C.蜡炬成灰 下列物质中"属于览净物的是 儿白酒 G 食用调和油每小题I 分.共范分’在每小題列岀的四个选项D. 木U 成舟 水疼石出2.B. D. 陈醋 蔗糖C.能便朝性kMnO.溶液樋色D分子中存在C = 0^化学试卷A第I也{共!1血)化学试卷A 第2页(共8页)6.关于合金说法正确的足 A.合金为化合物 B.合金具有金属特性C.合金都耐腐惶D.合金的硬度一定比成分金属的低7.漂白粉可由CI?通入消石灰中制备。
广东省广州市2013届高三化学第一次模拟试卷(含解析)新人教版

广东省广州市2013年高考化学一模试卷一、选择题(共7小题,每小题0分,满分0分)1.(2013•广州一模)在水溶液中能大量共存的一组离子是()2.(2013•济宁二模)下列说法正确的是()3.(2013•广州一模)下列实验不能达到目的是()4.(2013•广州一模)设n A为阿伏加德罗常数的数值,下列说法正确的是()5.(2013•广州一模)下列陈述I、II正确并且有因果关系的是()6.(2013•济宁二模)对于常温下pH=3的乙酸溶液,下列说法正确的是()7.(2013•广州一模)在容积为2L的密闭容器中进行反应:CO(g)+2H2(g)⇌CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)﹣反应时间t的变化曲线如图,下列说法正确的是()的平均生成速率为计算=mol•L二、解答题(共4小题,满分64分)8.(16分)(2013•广州一模)液晶高分子材料应用广泛.新型液晶基元﹣﹣化合物IV的合成线路如下:(1)化合物Ⅰ的分子式为C7H6O3,1mol化合物Ⅰ最多可与 2 mol NaOH反应(2)CH2=CH﹣CH2Br与NaOH水溶液反应的化学方程式为CH2=CHCH2Br+NaOH CH2=CHCH2OH+NaBr (注明条件).(3)化合物I的同分异构体中,苯环上一溴代物只有2种且能发生银镜反应的化合物有多种,写出其中一种同分异构体的结构简式(任写一种).(4)下列关于化合物Ⅳ的说法正确的是CD (填字母).A.属于烯烃 B.能与FeCl3溶液反应显紫色C.一定条件下能发生加聚反应 D.能使溴的四氯化碳溶液褪色(5)反应③的反应类型是取代.在一定条件下,化合物也可与III发生类似反应③的反应生成有机物V.V的结构简式是.)化合物Br+NaOHBr+NaOH故答案为:)由官能团的转化可知反应③属于取代反应,化合物﹣,反应物为故答案为:取代;9.(16分)(2013•广州一模)亚憐酸(H3PO3)是二元酸,与足量NaOH溶液反应生成Na2HPO3.(1)PCl3水解可制取亚磷酸:PCl3+32O═H3PO3+ 3HCl .(2)H3PO3溶液中存在电离平衡:H3PO3⇌H++H2PO3﹣.①某温度下,O.1Omol.L﹣1的 H3PO3溶液 pH=1.6,即溶液中 c(H+)=2.5x 10﹣2mol.L﹣1.求该温度下上述电离平衡的平衡常数K,写出计算过程.(H3PO3的第二步电离忽略不计,结果保留两位有效数字.)②根据H3PO3的性质可推测Na2HPO3稀溶液的pH >7 (填“>”、“=”或“<”).(3)亚磷酸具有强还原性,可使碘水褪色.该反应的化学方程式为H3PO3+I2+H2O=2HI+H3PO4(4)电解Na2HPO3溶液也可得到亚鱗酸,装置示意图如图:①阴极的电极反应式为2H++2e﹣=H2↑②产品室中反应的离子方程式为HPO32﹣+2H+=H3PO3.mol/L=8.3×1010.(16分)(2013•广州一模)某科研小组以难溶性钾长石(K2O.Al2O3.6SiO2)为原料,提取A1203、K2CO3等物质,工艺流程如下:(1)“煅烧”过程中有如下反应发生:①钾长石中的硅元素在CaCO3作用下转化为CaSiO3,写出SiO2转化为CaSiO3的化学方程式CaCO3+SiO2CaSiO3+CO2↑②钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的NaAlO2和 KAlO2,写出Al2O3转化为NaAlO2的化学方程式Al2O3+Na2CO32NaAlO2+CO2↑.(2)已知NaAlO2和KAlO2易发生如下反应:AlO+2H2O⇌Al(OH)3+OH﹣.“浸取”时,应保持溶液呈碱性(填“酸”或“碱”).“浸取”时不断搅拌的目的是提高浸取速率(3)“转化”时加入NaOH的主要作用是HCO3﹣+2OH﹣=CO32﹣+H2O (用离子方程式表示).(4)上述工艺中可以循环利用的主要物质是Na2CO3、CO2和水.2CaSiO232NaAlO311.(16分)(2013•广州一模)某铜矿石中铜元素含量较低,且含有铁、镁、钙等杂质离子.某小组在实验室中用浸出﹣萃取法制备硫酸铜:(1)操作I为过滤.操作II用到的玻璃仪器有烧杯分液漏斗(2)操作II、操作III的主要目的是除杂富集铜元素.(3)小组成员利用CuSO4溶液与Na2CO3溶液混合反应,制备环保型木材防腐剂 Cu2(0H)2C03悬浊液.多次实验发现所得蓝色悬浊液颜色略有差异,查阅资料表明,可能由于条件控制不同使其中混有较多Cu(OH)2或Cu4(0H)6S04.已知Cu(0H)2、Cu2(OH)2CO3,Cu4((OH)6SO4均难溶于水,可溶于酸;分解温度依次为800C、2000C、3000C.设计实验检验悬浊液成分,完成表中内容.限选试剂:2mol.L﹣1 HCl、1mol.L﹣1 H2SO4、O.1mol.L﹣1 NaOH、0.1mol.L﹣1 BaCl2、蒸馏水.仪器和用品自选.(4)上述实验需要1OOmL O.5mol.L﹣1的CuSO4溶液,配制时需称取125 gCuSO4.5H2O (化学式量:250).。
2013年广东各地一模化学试题汇总:非选择题部分:2013中山市.pdf

2013中山市15.(14分)在我国部分白酒中发现塑化剂超标,这些塑化剂是在白酒生产过程中接触塑料部件而带入的。
人体摄入超量塑化剂会造成内分泌失调、不育等症。
邻苯二甲酸二丁酯(DBP)是一种常见的塑化剂,可由乙烯和邻二甲苯合成。
已知①2CH3CHOCH3CHCH2CHO② -CH3-COOH DBP的合成过程如下: CH2=CH2 C有顺反异构 -CH3 1)写出A、C的结构简式 ; 。
2)B中含有的官能团名称__________________ 3)写出反应类型:反应① ; 反应③ ; 4)化合物B有多种同分异构体,如果这种同分异构体能与NaHCO3溶液反应生成气体,在核磁共振氢谱中只有3处吸收峰,写出其结构简式 。
5)写出反应⑥的化学方程式 。
四、(本题包括1小题,共15分) 16.(15分)碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是理想,更是一种值得期待的新的生活方式,请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应化学方程式为: ____C+____K2Cr2O7 +====___CO2↑+ ____K2SO4 + ____Cr2(SO4)3+ ____H2O 请完成并配平上述化学方程式。
其中氧化剂是________________,氧化产物是_________________ (2)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为: CO(g)+ 2H2(g) CH3OH(g)△H1=-116 kJ·mol-1 ①已知:△H2=-283 kJ·mol-1 △H3=-242 kJ·mol-1 则表示1mol气态甲醇完全燃烧生成CO 2和水蒸气时的热化学方程式为 ; ②在容积为1L的恒容容器中,分别研究在230℃、250℃ 270℃三种温度下合成甲醇的规律。
2013年普通高等学校招生全国统一考试(广东卷)化学

2013年普通高等学校招生全国统一考试(广东卷)化学一、单项选择题:本大题共6小题,每小题4分,满分24分.在每小题给出的四个选项中,只有一项是符合题目要求的.选对的得4分,选错或不答的得0分。
1.(4分)下列说法正确的是()A.糖类化合物都具有相同的官能团B.酯类物质是形成水果香味的主要成分C.油脂的皂化反应生成脂肪酸和丙醇D.蛋白质的水解产物都含有羧基和羟基解析:A.葡萄糖的官能团是羟基和醛基,而果糖的官能团是羟基和羰基,故A错误;B.酯类一般都是易挥发具有芳香气味的物质,故B正确;C.油脂在碱性条件水解生成高级脂肪酸盐和甘油,称之为皂化反应,故C错误;D.蛋白质的水解产物是氨基酸,氨基酸的官能团是羧基和氨基,故D错误。
答案:B.2.(4分)水溶液中能大量共存的一组离子是()A.Na+、Al3+、Cl﹣、CO32﹣B.H+、Na+、Fe2+、MnO4﹣C.K+、Ca2+、Cl﹣、NO3﹣D.K+、NH4+、OH﹣、SO42﹣解析:A.因Al3+、CO32﹣相互促进水解生成沉淀和气体,则不能共存,故A错误;B.因H+、Fe2+、MnO4﹣发生氧化还原反应,则不能共存,故B错误;C.因该组离子之间不反应,能共存,故C正确;D.因NH4+、OH﹣结合生成弱电解质,则不能共存,故D错误。
答案:C.3.(4分)设N A为阿伏加德罗常数的数值,下列说法正确的是()A.常温常压下,8g O2含有4N A个电子B.1L 0.1mol•L﹣1的氨水中有N A个NH4+C.标准状况下,22.4L盐酸含有N A个HCl分子D.1mol Na被完全氧化生成Na2O2,失去2N A个电子解析:A、常温常压下,8gO2物质的量==0.25mol,含有电子数=0.25mol×8×2×N A=4N A,故A正确;B、1L 0.1mol•L﹣1的氨水中,一水合氨物质的量为0.1mol,一水合氨是弱电解质存在电离平衡,溶液中有NH4+小于0.1mol,故B错误;C、盐酸是电解质溶液,溶液中氯化氢电离成氢离子和氯离子,不存在氯化氢分子,故C错误;D、1mol Na被完全氧化生成Na2O2,失去N A个电子,故D错误。
2013年广东各地一模化学试题汇总:非选择题部分:2013增城市.pdf

△H=-117kJ?mol-1
NH2COONH4(l) (NH2)2CO(g)+H2O(g) △H=+15kJ?mol-1
(1)由氨气和二氧化碳合成尿素的热化学方程式是:________________________________
(2)第一步反应在11.1Mpa、160oC的条件下反应较快,转化率也较高,第二步反应在相同条件下反应速率较慢
;若硫酸加入量过高,不利于产品形成,试从平衡移动的角度分析原因是
____________________________________________;
(3)氧化过程中生成一种气体,遇空气变红棕色,写出氧化过程发生的化学方程式:
________________________________________________________________。
同学根据硫酸型酸雨的形成过程,预测主要溶质还一定有
。
(2)设计实验方案验证以Ba(OH)2
溶液在答题卡上写出实验步骤、预期现象和结论。限选试剂及:盐酸、硝酸、BaC12溶液、Ba(OH)2溶液、AgNO3溶
液、紫色石蕊试液、品红溶液、烧杯、试管、胶头滴管。(3)酸雨部分组成测定:滴定:准确量取20.00mL该酸雨于锥
② 0.0090 mol·L-1 (2分,有效数字错误扣1分,单位没有或错误扣1分)
△
Cu
CH3
CH3
O
‖
溶解
氧化
气体
调节pH值
固体碱式硫酸铁产品
NaNO2 催化剂
硫酸
水、铁粉
K1
K2
转化率%
(P1 、160OC)
(P2 、180OC)
如图已知: Fe=3.1 , Fe2+沉淀完全时的pH=9.7
2013年一模化学评分细则+

2013年一模化学评分细则注:本卷中只要有错别字,每个扣1分;同一题中相同错别字重复出现不重复扣分。
2013年一模化学评分细则:30.(16分)(1)C 7H 6O 3 (2分); 2 (2分)(2)CH 2=CH-CH 2Br + NaOHCH 2=CH-CH 2OH +NaBr (2分)“H 2O ”或“Δ”未写得1分,写错结构简式得0分;写“=”得1分。
写成CH 2=CH-CH 2Br + H 2O CH 2=CH-CH 2OH +HBr 得1分。
(3)(3分,正确写出以下其中之一即可得3分。
书写正确但不规范(苯环的书写、化学键未正对相应原子等得2分;少原子得0分)O OH C-HO、 O HC HOO H 、O H OH C HO(—OOCH 、—O —CHO 得分,—OCOH 不得分)(4)CD (2分。
只答C 或D 得1分;其他答案得0分)(5)取代反应(2分)(只写“取代”得1分);C H 2C HC H 2OOOC C H 3C H 3C(3分)31.(16分)(1)3HCl (2分。
只写HCl 得1分) (2)(5分)① H 3PO 3H + + H 2PO 3-起始时各物质浓度(mol•L -1) 0.10 0 0 反应的各物质的浓度(mol•L -1)2.5×10-2 2.5×10-2 2.5×10-2 平衡时各物质的浓度(mol•L -1)0.10-2.5×10-22.5×10-22.5×10-2(正确列出1分)(得到平衡浓度就可得1分,格式无统一要求。
) 3-2223332103.8105.210.0105.2105.2)()()(⨯=⨯-⨯⨯⨯=⋅=----+PO H c PO H c H c K mol•L -1H 2OΔ NaOHΔ(正确列出平衡常数表达式1分;代入数据1分;计算结果1分;单位正确1分。
广州市2013年高考化学综合模拟题-推荐下载

A.可能出现三倍体细胞
C.多倍体细胞形成过程无完整的细胞周期
D.多倍体形成过程增加了非同源染色体重组的机会
7.下列说法正确的是
A.天然气、水煤气、汽油都是纯净物
B.二氧化硅可做直接用于制半导体的材料
C.钠在氧气中反应可能得到氧化钠或过氧化钠或二者的混合物
D.金属最高价氧化物对应的水化物一定呈碱性
8.下列相关叙述正确的是:
A.严重缺铁的病人可能会出现乳酸中毒 B.糖原氧化分解的最终产物是葡萄糖 C.脱氧核糖核苷酸是生物的遗传物质之一 D.脂肪和生长激素是生物体内的能源物 质 2.右图中①~④表示某细胞的部分细胞器,下列有关叙述正 确的是 A.该图一定是高倍光学显微镜下看到的结构 B.此细胞不可能是植物细胞,只能是动物细胞 C.结构①不能将葡萄糖分解成二氧化碳和水 D.结构①~④中都含有大量磷脂 3.在做“绿叶中色素的提取和分离”实验时,甲、乙、丙、丁四位同学对相关试剂的使用情 况如下表所示(“+”表示使用,“~”表示未使用),其余操作均正常,他们所得的实验结果依 次应为
A.聚乙烯能使溴水褪色
C.将 1-氯丁烷滴加到硝酸银溶液中有大量白色沉淀出现
D.苯环结构中单键和双键交替排布
9.设 NA 是阿伏加德罗常数的值,下列说法正确的是
A.6.4g 的 O2 和 O3 混合物中,含氧原子总数为 0.4N A
B.标准状况下,22.4L 乙醇中含有的氧原子数为 N A C. 1.0L O.1mol/L 的 FeC13 溶液中含有 0.1N A 个 Fe3 D.25℃时,pH=13 的 Ba(OH )2 溶液中含有 0H 数目为 0.2N A
H 2O
B.一定是曲线运动
A1O2
2013年广东各地一模化学试题汇总:非选择题部分:2013广州市

2013广州市30.(16分)某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。
实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。
该小组设计了如下的方案。
(1)已知反应后H2C2O4转化为CO2逸出,KMnO4转化为MnSO4,每消耗1mol H2C2O4转移_____mol 电子.为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为:c(H2C2O4):c(KMnO4) ≥______________.(2)探究温度对化学反应速率影响的实验编号是___________(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是_____________。
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=_______________ mol·L-1·min-1。
(4)已知50℃时c (MnO 4—)~反应时间t 的变化曲线如图。
若保持其他条件不变,请在答题卡坐标图中,画出25℃时c (MnO 4—)~t 的变化曲线示意图。
31.(16分)氨是最重要的化工产品之一.(1)合成氨用的氢气可以甲烷为原料制得。
有关化学反应的能量变化如下图所示。
反应①②③为_________反应(填“吸热”或“放热”).CH 4(g)与H 2O(g)反应生成CO (g )和H 2(g )的热化学方程式为__________________。
① ②③(2)用氨气制取尿素[CO (NH 2)2]的反应为:2NH 3(g )+CO 2(g )CO (NH 2)2(l)+H 2O(g)。
①某温度下,向容积为10L 的密闭容器中通入2mol NH 3和1molCO 2,反应达到平衡时CO 2的转化率为50%.该反应的化学平衡常数表达式为K =___________。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2013年广州市高三一模7.在水溶液中能大量共存的一组离子是A.Al3+、Na+、HCO3-、SO42-B.H+、Fe2+、ClO-、Cl-C.Mg2+、K+、SO42-、NO3-D.NH4+、Ag+、OH-、Br-8.下列叙述正确的是A.食盐、醋酸和蔗糖都是电解质B.纤维素、淀粉和蛋白质都是高分子化合物C.甲烷和乙烯均可使KMnO4溶液褪色D.乙酸乙酯和植物油均可水解生成乙醇9.下列实验不.能.达到目的的是A.用AlCl3溶液和过量氨水制备Al(OH)3B.用NH4Cl和Ca(OH)2混合加热制备NH3C.用NaOH溶液除去苯中的溴D.用足量铜粉除去FeCl2溶液中的FeCl3杂质10.设n A为阿伏加德罗常数的数值,下列说法正确的是A.16g CH4含有10n A电子B.常温常压下,22.4L Cl2含有2n A个Cl原子C.1 mol Cu与足量稀HNO3反应,转移3n A个电子D.1L 0.1 mol·L-1 Na2SO3溶液中含有0.1n A个SO32-11.下列陈述Ⅰ、Ⅱ正确并且有因果关系的是12.对于常温下pH=3的乙酸溶液,下列说法正确的是A.c(H+)=c(CH3COO-) + c(OH-)B.加水稀释到原体积的10倍后溶液pH变为4C.加入少量乙酸钠固体,溶液pH降低D.与等体积pH为11的NaOH溶液混合后所得溶液中:c(Na+)=c(CH3COO-)22.短周期元素的X 、Y 、Z 、W 原子序数依次增大,X 原子最外层电子数是电子层数的三倍,Y 与X 可形成Y 2X 2和Y 2X 两种离子化合物,Z 原子的核外电子数比原子Y 原子多1,W 与X 同主族,则A .原子半径:Y <Z <WB .单质的还原性:Y >ZC .气态氢化物的稳定性:X >WD .Y 和Z 两者最高价氧化物对应的水化物能相互反应23.在容积为2L 的密闭容器中进行反应:CO(g)+2H 2(g)CH 3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n (CH 3OH)-反应时间t 的变化曲线如图所示,下列说法正确的是A .该反应的△H <0B .其他条件不变,升高温度反应的平衡常数增大C .300℃时,0-t 1min 内 CH 3OH 的平均生成速率为121t n mol·L -1 min -1 D .A 点的反应体系从300℃升高到500℃,达到平衡时)OH CH (n )H (n 32减小30.(16分)液晶高分子材料应用广泛。
新型液晶基元---化合物Ⅳ的合成线路如下:1.化合物Ⅰ的分子式为__________ ,1mol 化合物Ⅰ最多可与_____molNaOH 溶液反应。
2.CH 2=CH-CH 2Br 与NaOH 水溶液反应的化学方程式为_________;(注明条件)。
3.化合物Ⅰ的同分异构体中,苯环上一溴代物只有2种且能发生银镜反应的化合物有多种,写出其中一种同分异构体的结构简式_____ 。
4.下列关于化合物Ⅱ的说法正确的是_______(填字母)。
A.属于烯类B.能与FeCl 3溶液反应呈紫色C.一定条件下能发生加聚反应D.能使溴的四氯化碳溶液褪色5.反应③的反应类型是_____________。
在一定条件下,化合物也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ。
Ⅴ的结构简式是______________。
31.(16分)亚磷酸(H 3PO 3)是二元酸,与足量NaOH 溶液反应,生和Na 2HPO 3。
(1)PCl 3水解能得到亚磷酸。
PCl 3+3H 2O = H 3PO 3+________。
(2)H3PO3溶液存在电离平衡:H3PO 3H+ + H2PO3-。
①某温度下,0.1000 mol·L-1的H3PO3溶液pH的读数为1.6,即此时溶液中c (H+) =2.5×10-2 mol·L-1。
求该温度下上述电离平衡的平衡常数K,写出计算过程。
(H3PO3第二步电离忽略不计,结果保留两位有效数字)。
②根据H3PO3的性质可推测NaH2PO3稀溶液的pH_______7(填“>”、“>”或“>”)。
(3)亚磷酸具有强还原性,可使碘水褪色。
该反应的化学方程式_______________________。
(4)电解Na2HPO3溶液也可得到亚磷酸,装置示意图如下:说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过。
①阴极的电极反应式为_____________________________。
②产品室中反应的离子方程式为_____________________。
32.(16分)某科研小组以难溶性钾长石(K2O•Al2O3•6SiO2)为原料,提取Al2O3、K2CO3等物质,工艺流程如下:(1)煅烧过程中有如下反应发生:①钾长石中的硅元素在CaCO3作用下转化为CaSiO3,写出SiO2转化为CaSiO3的化学方程式是:。
②钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的NaAlO2和KAlO2,写出Al2O3转化为NaAlO2的化学方程式是:。
O Al(OH)3 + OH—(2)已知NaAlO2和KAlO2易发生如下水解反应:AlO2—+ 2H2“浸取”时应保持溶液呈性(填“酸”或“碱”。
“浸取”时不断搅拌的目的是。
(3)“转化”时加入NaOH的主要作用是。
(4)上述工艺中可以循环利用的主要物质是、和水。
33.(16分)某铜矿石中铜元素含量较低,且含有铁、镁、钙等杂质离子。
某小组在实验室中用浸出-萃取法制备硫酸铜:(1)操作Ⅰ为_____________。
操作Ⅱ用到的玻璃仪器有烧杯、________。
(2)操作Ⅱ、操作Ⅲ的主要目的是______________、富集铜元素。
(3)某小组利用CuSO4溶液与Na2CO3溶液反应制备新型木材防腐剂Cu2(OH)2CO3。
多次实验发现所得蓝色悬浊液颜色略有差异,查阅资料表明,可能由于条件控制不同使其中混有较多杂质Cu(OH)2或Cu4(OH)6SO4。
已知Cu(OH)2、Cu2(OH)2CO3、Cu4(OH)6SO4均难溶于水,易溶于强酸;分解温度依次为80℃、200℃、300℃。
设计实验方案检验悬浊液成分,完成表中内容。
限选试剂:2 mol·L-1 HCl、1 mol·L-1 H2SO4、0.1 mol·L-1NaOH、0.1 mol·L-1BaCl2、蒸馏水。
仪器和用品自选。
(4)上述实验需要100mL 0.5 mol·L的CuSO4溶液,配制时需称取_______________g CuSO4•5H2O(化学式量:250)。
2013年一模化学参考答案30.(16分)(1)C 7H 6O 3 (2分); 2 (2分)(2)CH 2=CH-CH 2Br + NaOHCH 2=CH-CH 2OH +NaBr (2分)(3)以下其中一种即可:(3分)O OH C-HO、OHCHOO H 、 OH OH CHO(4)CD (2分)(5)取代(2分);CH 2CH CH 2OO OCCH 3CH 3C(3分)31.(16分)(1)3HCl (2分) (2)(5分)① H 3PO 3 H + + H 2PO 3-起始时各物质浓度(mol•L -1) 0.10 0 0反应的各物质的浓度(mol•L -1)2.5×10-2 2.5×10-2 2.5×10-2平衡时各物质的浓度(mol•L -1)0.10-2.5×10-2 2.5×10-2 2.5×10-23-2223332103.8105.210.0105.2105.2)()()(⨯=⨯-⨯⨯⨯=⋅=----+PO H c PO H c H c K mol•L -1 ② > (2分)(3)H 3PO 3 + I 2 +H 2O = 2HI + H 3PO 4 (3分) (4)① 2H + + 2e -=H 2↑ (2分)②HPO 32-+ 2H + = H 3PO 3 (2分)或:HPO 32-+ H + = H 2PO 3- 、H 2PO 3-+ H + = H 3PO 3(各1分) 32.(16分)Δ(1)①CaCO 3+SiO 2CaSiO 3+CO 2↑ (3分) ②Na 2CO 3+Al 2O 32NaAlO 2+CO 2↑ (3分)(2)碱 (1分);提高浸取速率(2分)(3)HCO 3- + OH - =H 2O + CO 32- (3分) (4)Na 2CO 3 、CO 2 (4分) 33.(16分)(1)过滤 ;分液漏斗 (共4分,各2分) (2)除去杂质; (2分)2013年一模化学评分细则注:本卷中只要有错别字,每个扣1分;同一题中相同错别字重复出现不重复扣分。
2013年一模化学评分细则:30.(16分)(1)C 7H 6O 3 (2分); 2 (2分)(2)CH 2=CH-CH 2Br + NaOH CH 2=CH-CH 2OH +NaBr (2分) “Δ”未写得1分,写错结构简式得0分写成CH 2=CH-CH 2Br + H 2O CH 2=CH-CH 2OH +HBr 得1分;(3)(3分,正确写出以下其中之一即可得3分。
书写正确但不规范(苯环的书写、化学键未正对相应原子等得2分;少原子得0分)Δ ΔO OH C-HO、OHCHOO H 、 OH OH CHO(—OOCH 、—O —CHO 得分,—OCOH 不得分)(4)CD (2分。
只答C 或D 得1分;其他答案得0分)(5)取代(2分); CH 2CH CH 2OO OCCH 3CH 3C(3分)2013年一模化学评分细则注:本卷中只要有错别字,每个扣1分;同一题中相同错别字重复出现不重复扣分。
31.(16分)(1)3HCl (2分。
只写HCl 得1分)(2)(5分)①H 3PO 3 H + + H 2PO 3-(正确列出1分)起始时各物质浓度(mol•L -1) 0.10 0 0反应的各物质的浓度(mol•L -1)2.5×10-2 2.5×10-2 2.5×10-2 (未列出不扣分)平衡时各物质的浓度(mol•L -1)0.10-2.5×10-2 2.5×10-2 2.5×10-2 (正确列出1分) (得到平衡浓度就可得2分,不必分开,而且格式并无统一要求。
)3-2223332103.8105.210.0105.2105.2)()()(⨯=⨯-⨯⨯⨯=⋅=----+PO H c PO H c H c K mol•L -1(正确列出平衡常数表达式1分;代入数据1分;计算结果1分,写成8×10-3或1.0×10-2结果得0分;未写单位不扣分,写错则得0分)② > (2分。
