【小初高学习]2017-2018九年级化学上册 综合训练 二氧化碳性质和制取 二氧化碳的制取及相关推
初三化学上册二氧化碳的实验室制取与性质

实验目的
1、练习实验室里制取二氧化碳和用向 上排空气法收集气体 2、加深对二氧化碳性质的认识
实验用品
•1、烧杯、集气瓶、量筒、玻璃导管、 胶皮管、单孔橡胶塞、铁架台、(带铁 夹)、试管、试管夹、玻璃片、酒精灯。 •2、大理石(或石灰石)、稀盐酸(1: 2)、澄清石灰水、紫色石蕊溶液。 •你还需要的实验用品:
PPT素材:/sucai/ PPT图表:/tubiao/ PPT教程: /powerpoint/ 范文下载:/fanwen/ 教案下载:/jiaoan/ PPT课件:/kejian/ 数学课件:/kejian/shu xue/ 美术课件:/kejian/me ishu/ 物理课件:/kejian/wul i/ 生物课件:/kejian/she ngwu/ 历史课件:/kejian/lish i/
中是否已收集满二氧化碳。用玻璃片盖住已收 集满二氧碳的集气瓶,备用。
试管里的 是否收集满:
用燃着木条平放在 集气瓶口,木条熄 灭,则已收集满
• 2、二氧化碳的性质
• (1)把一支短蜡烛固定在烧杯内,点燃。拿 起收集满二气化碳的集气瓶,向 烧杯内缓慢 倾倒二氧化碳,观察现象。
现象:红色溶液又 变成无色。
结论:碳酸不稳定,加热分解,生成氧气 和水。没有碳酸,不能使石蕊变红色。
•(3)另取一支试管,向其中注入少量 澄清石灰水,然后通入二氧化碳,观察 现象。
现象:澄清石灰水变混浊
CO2+Ca(HO)2=CaCO3 +H2O
实验步骤
• 1、制取二氧化碳 • (1)按照左图连接装置,并检 • 查装置的气密性。
如右图,双手握住试管,有 气泡冒出,则气密性良好。
初中化学人教版九年级上册实验活动2 二氧化碳的实验室制取与性质

总结交流
1、在倾倒二氧化碳气体的实验观察到的现象是 什么?
2、在用软塑料瓶做关于二氧化碳溶解性实验时 观察到的现象是什么?
3、在⑶中把二氧化碳气体通入石蕊溶液,现进 行加热,观察到的现象是什么?
实验活2 二氧化碳的实 验室制取与性质
宁安市海浪中学 李传华
实验目的
1、练习实验室里制取二氧化碳和用向上排空气 法收集气体。
2、加深对二氧化碳性质的认识。
实验用品
器材:烧杯、集气瓶、量筒、玻璃导管、胶皮管、 单孔橡胶塞、铁架台(带铁夹)、试管、试管 夹、玻璃片、酒精灯。
药品:石灰石、稀盐酸、澄清石灰水、紫色石蕊 溶液、蜡烛、木条、蒸馏水、火柴。
其它用品:软塑料瓶等
实验步骤
1、制取二氧化碳 2、二氧化碳的性质 ⑴两支高低验 ⑶二氧化碳气体通入石蕊溶液,再加热。 ⑷把二氧化碳通入澄清的石灰水。
1、制取二氧化碳
⑴按照图A所示连接装置或图B,并检查装置的 气密性。
⑵在试管或锥形瓶中放入几块石灰石,然后小心 地注入15mL稀盐酸。立即用带有导管的橡胶 塞塞住管口,观察试管或锥形瓶中的产生气体 的颜色,过一会儿,检查集气瓶中是否已收集 满二氧化碳。用玻璃片盖住已收集满二氧化碳 的集气瓶,备用。用同样的方法再收集一塑料 瓶二氧化碳气体。
二氧化碳的性质和制取_九年级化学教案_模板

二氧化碳的性质和制取_九年级化学教案_模板第四节二氧化碳的实验室制法阳光一.知识教学点二氧化碳的实验室制法。
二.重、难、疑点及解决办法1.重点:实验室制取二氧化碳的反应原理、实验装置和制取方法。
2.难点:从实验室制取气体的设计思路出发,学习二氧化碳的实验室制取方法。
3.疑点:实验室制取二氧化碳,为什么不能用稀硫酸?4.解决方法(1)采取讨论的形式,从学生学过的氧气和氢气的实验室制法,归纳和总结出气体实验室制法的设计思路和方法。
(2)通过演示和补充实验,组织学生分析讨论二氧化碳的实验室制取方法,使学生掌握实验室制取二氧化碳的原理,提高学生分析和解决实际问题的能力。
三.教学步骤(一)明确目标1.联系实验室制取氧气、氢气,学会实验室制取气体的一般方法。
2.掌握实验室制取二氧化碳的反应原理、实验装置、使用的药品、仪器名称和收集方法。
(二)整体感知本节主要采用讨论的形式,使学生掌握二氧化碳的实验室制法。
(三)教学过程[复习提问]:(1)CO2有哪些物理性质和化学性质?(2)实验室制取H2、O2的反应原理是什么?[小结]:实验室制取氧气的原理是利用高锰酸钾或氯酸钾(用二氧化锰作催化剂),在加热条件下得到氧气。
实验室制取氢气的原理是用金属锌和稀硫酸(或稀盐酸)反应得到氢气。
[教师活动]:投影出制取H2、O2的几套装置图,通过讨论得出这些装置图的适用范围:(1)当用固体反应,需要加热产生气体时,可采用制取氧气的装置;(2)当用固体与液体反应,不需加热就能生成气体时,可采用制取H2的装置(注意该气体难溶于水或酸)。
[提问]:(1)在实验室如何收集H2和O2,根据它们什么性质?(2)如何检验H2和O2?[学生活动]:通过讨论得出以下结论:(1)根据气体的物理性质(密度和溶解性)决定采用什么方法收集;(2)利用物质的特性来检验物质。
[总结板书]:实验室制取气体的思路和方法是: 1.首先了解在实验室的条件下,用什么药品,通过什么化学反应制取这种气体。
二氧化碳的实验室制取与性质--教案

教案:二氧化碳的实验室制取与性质教学目标:1. 了解二氧化碳的实验室制取方法。
2. 掌握二氧化碳的物理和化学性质。
3. 培养学生的实验操作能力和观察能力。
教学重点:1. 二氧化碳的实验室制取方法。
2. 二氧化碳的物理和化学性质。
教学难点:1. 二氧化碳的实验室制取操作。
2. 二氧化碳的化学性质的理解。
教学准备:1. 实验室制取二氧化碳所需的药品和仪器。
2. 实验室安全常识。
教学过程:一、导入(5分钟)1. 引导学生回顾二氧化碳的定义和重要性。
2. 提问:二氧化碳能否支持燃烧?能否使澄清石灰水变浑浊?二、二氧化碳的实验室制取(10分钟)1. 介绍实验室制取二氧化碳的原理和方法。
2. 演示实验室制取二氧化碳的实验操作。
3. 学生分组进行实验,观察制取二氧化碳的过程。
三、二氧化碳的物理性质(10分钟)1. 介绍二氧化碳的物理性质,如无色无味、密度比空气大等。
2. 学生进行实验,观察二氧化碳的物理性质。
四、二氧化碳的化学性质(15分钟)1. 介绍二氧化碳的化学性质,如与水反应碳酸、与碱反应盐等。
2. 学生进行实验,观察二氧化碳的化学性质。
五、实验室安全(5分钟)1. 强调实验室安全的重要性。
2. 讲解实验室制取二氧化碳时的安全注意事项。
教学评价:1. 学生能正确回答二氧化碳的实验室制取方法。
2. 学生能正确描述二氧化碳的物理和化学性质。
3. 学生能遵守实验室安全规定,正确进行实验操作。
六、实验探究:二氧化碳的溶解性(10分钟)1. 介绍二氧化碳在水中的溶解性。
2. 学生进行实验,观察二氧化碳的溶解过程。
七、二氧化碳的应用(10分钟)1. 介绍二氧化碳在日常生活中的应用,如碳酸饮料的制造、植物光合作用等。
2. 学生讨论二氧化碳的应用及其对环境的影响。
八、二氧化碳的减排(10分钟)1. 引导学生思考二氧化碳排放对环境的影响。
2. 讨论减少二氧化碳排放的方法和措施。
九、课堂小结(5分钟)1. 回顾本节课学习的二氧化碳的实验室制取与性质。
二氧化碳的性质及制备实验【例2二氧化碳气体可以用来灭火与
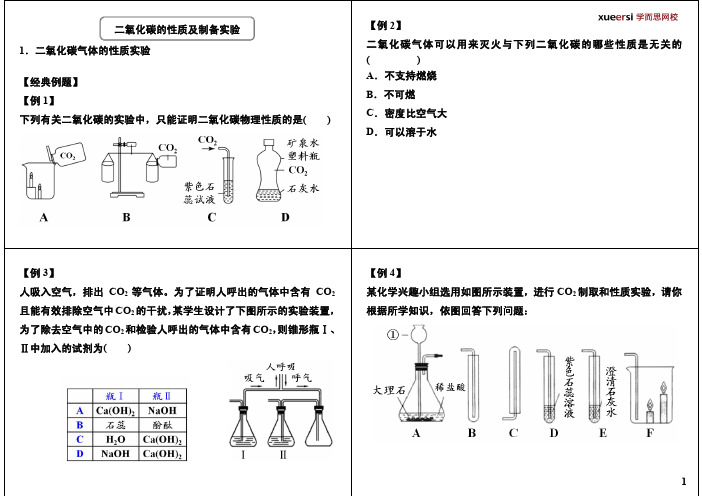
【例3】人吸入空气,排出CO2等气体。
为了证明人呼出的气体中含有CO 且能有效排除空气中CO的干扰,某学生设计了下图所示的实验装置,实验室制取和收集CO2应选用下列装置中的(填序号活动小组经查阅资料,知道CaCO3CaO+CO2↑,同学们研究得出实验室为什么不用A装置加热碳酸钙制取二氧化碳?其原因。
同学们对上述实验现象提出猜想,产生该现象的主要原因可能是:因为CO2气体溶于水(溶液中的溶剂),②因为CO2气体与水发生反应,因为CO2气体与NaOH发生反应。
你认为上述猜想正确的是(填序号);并请你设计一个实验,小虎同学认为上述实验是可行的。
小刚关闭K,通入二氧化碳,A、B中均无明显变化。
B溶液。
_____________________________________现象为_____________________________________,2HCl CaCl实验室用高锰酸钾制氧气的化学方程式是,反应的发生装置(填序号)。
若采用C装置收集氧气,验满的方法是⑵收集方法:向上排空气法⑶步骤:①检查反应装置的气密性②装入块状大理石,塞紧塞子,出气导管刚好伸入锥形瓶内③把反应装置固定好④从长颈漏斗加入稀盐酸至浸没漏斗导管末端⑤收集气体⑥检验是否集满⑷检验:验证:将被检验的气体通入澄清石灰水中,若澄清石灰水变浑浊,证明是CO2,否则不是。
验满:用燃着的木条靠近集气瓶口,若木条熄灭,证明已集满,否则未满。
⑸注意事项:①一般不用稀硫酸来代替稀盐酸,是因为反应生成的硫酸钙是微溶物,这种沉淀会附着在块状大理石或石灰石的表面,阻碍反应的继续进行。
②一般不用浓盐酸代替稀盐酸,是因为浓盐酸易挥发,挥发出来的氯化氢气体易混入产生的二氧化碳气体中,会给实验带来误差。
③实验室也不用碳酸钠,粉末状石灰石来代替块状石灰石或大理石,原因是反应速度太快,不便于控制。
课后作业1.下列有关实验室制取二氧化碳的方法不合理的是()A.因为通常情况下二氧化碳密度大于空气.故能用向上排空气法收集B.因为二氧化碳在水中的逸出速率大于溶解速率,故也可用排水法收集C.在发生装置中加入块状石灰石和稀盐酸D.因为碳酸钙和盐酸在常温下即可迅速反应,故气体发生装置不需要加热2.如图是实验室制取二氧化碳的装置,其中的错误共有()A.1处B.2处C.3处D.4处3.实验室制取二氧化碳和实验室制取氧气相比较,一定相同的是( )A.发生装置B.收集方法C.验满方法D.集满气体后的集气瓶的放置方法4.同学们设计了如图所示装置来探究二氧化碳的制取和性质,下列关于该实验的叙述正确的是()A.移动粗铜丝能控制反应的发生和停止B.该实验能证明二氧化碳的密度比空气大C.浸有紫色石蕊试液的棉花会变蓝D.产生的二氧化碳可用生石灰干燥5.长期盛石灰水的瓶子内壁上常会出现一层白膜,这层白膜是()A.Ca(OH)2B.H2SO4C.CaCO3D.HCl6.有关CO2的实验中,不能证明CO2化学性质的是()A.B.C.D.7.超临界CO2流体是一种与水相似、能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。
(完整版)二氧化碳的性质及制取和对应习题

二氧化碳的性质及制取知识点2 二氧化碳的性质(重点)1.物理性质⑴通常状况下,二氧化碳是一种无色无味的气体。
⑵标准状况下,二氧化碳的密度为1.977g/L,比空气大。
⑶在通常情况下,二氧化碳能溶于水,1体积水中能溶解1体积的二氧化碳气体,增大气压会溶解得更多。
升高温度,二氧化碳会溶解得少一些。
①打开“可乐”等饮料瓶时看到许多气泡从饮料中逸出,就是因为压强减小了,饮料中能溶解的二氧化碳减小了;②喝“可乐”等饮料时会打嗝,就是因为喝下去的饮料温度升高,饮料中能溶解的二氧化碳减小了。
2.化学性质⑴一般情况下,二氧化碳不能燃烧,也不能支持一般可燃物的燃烧,也不能供给呼吸。
①二氧化碳不能燃烧也不支持燃烧,可用二氧化碳灭火。
②二氧化碳不供给人呼吸,所以要进入一些可能含有较高浓度的二氧化碳气体的地方,应谨防二氧化碳含量过高使人窒息,可先进行灯火实验,如灯火燃烧不旺或熄灭可知二氧化碳含量较多,人就不宜进入。
【领悟·整合】①二氧化碳不能支持一般可燃物的燃烧,但不是所有物质,有些物质如金属镁能在二氧化碳中燃烧;②二氧化碳不能供给呼吸,并不是说二氧化碳有毒。
⑵二氧化碳与水反应。
二氧化碳与水反应生成碳酸(H2CO3),H2CO3是一种弱酸,可使紫色的石蕊试液变红,且H2CO3不稳定,常温或加热条件下,易分解为H2O和CO2。
因此二氧化碳通入紫色的石蕊试液中时,由于石蕊遇到生成的碳酸而变红;加热时,由于碳酸的分解,红色试液又恢复紫色。
文字表达式如下:二氧化碳+ 水→ 碳酸碳酸−−→−加热二氧化碳+ 水CO2H2O H2CO3H2CO3CO2H2O【辨析·比较】:①这里使紫色石蕊试液变红的不是二氧化碳,而是二氧化碳与水反应后生成的碳酸,我们不能说成“二氧化碳使紫色石蕊试液变红”。
②二氧化碳能溶于水和与水发生化学反应两者在本质上是有差异的,前者是二氧化碳的物理性质,后者是二氧化碳的化学性质,当然两者又有着密切的联系。
2017-2018九年级化学上册 综合训练 二氧化碳性质和制取 二氧化碳的性质天天练(无答案)(新版)新人教版
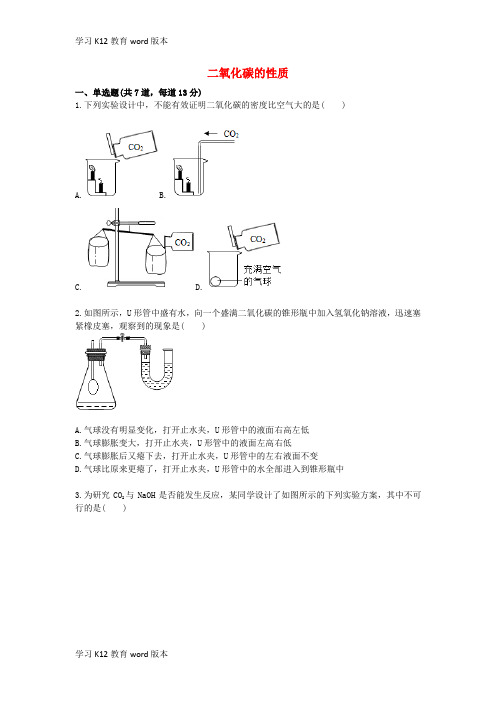
二氧化碳的性质一、单选题(共7道,每道13分)1.下列实验设计中,不能有效证明二氧化碳的密度比空气大的是( )A. B.C. D.2.如图所示,U形管中盛有水,向一个盛满二氧化碳的锥形瓶中加入氢氧化钠溶液,迅速塞紧橡皮塞,观察到的现象是( )A.气球没有明显变化,打开止水夹,U形管中的液面右高左低B.气球膨胀变大,打开止水夹,U形管中的液面左高右低C.气球膨胀后又瘪下去,打开止水夹,U形管中的左右液面不变D.气球比原来更瘪了,打开止水夹,U形管中的水全部进入到锥形瓶中3.为研究CO2与NaOH是否能发生反应,某同学设计了如图所示的下列实验方案,其中不可行的是( )A.B.C.D.4.为验证“CO2能与水反应”且“密度比空气大”的性质,将纯净干燥的CO2缓慢地通过如图装置(玻璃管为高低两根),最早明显变红的蓝色石蕊试纸是( )A.ⅠB.ⅡC.ⅢD.Ⅳ5.如图所示,三个集气瓶中分别盛有氢氧化钠溶液、澄清石灰水、紫色石蕊溶液中的一种。
通入一段时间的二氧化碳后,①②③三个集气瓶中出现的现象依次为变浑浊、无变化、无变化,则①②③三个集气瓶中所盛溶液分别为( )A.澄清石灰水、氢氧化钠溶液、紫色石蕊溶液B.紫色石蕊溶液、氢氧化钠溶液、澄清石灰水C.澄清石灰水、紫色石蕊溶液、氢氧化钠溶液D.氢氧化钠溶液、澄清石灰水、紫色石蕊溶液6.用紫色石蕊溶液将滤纸染成紫色,经烘干后做成两朵干燥紫色小花。
如图,先取一朵直接放入盛有二氧化碳的集气瓶中,再取另一朵喷上水后再放入盛有二氧化碳的集气瓶中。
下列叙述不正确的是( )A.实验中会观察到集气瓶中的现象是:第一朵小花不变红,第二朵小花变红B.根据图1中的现象可知,二氧化碳通入紫色石蕊溶液不会有明显现象C.取出第二朵小花加热,观察到小花变成紫色D.石蕊试液本身呈紫色,证明水不能使紫色石蕊变红7.如图是二氧化碳的制取和性质实验的微型一体化装置图,该装置的气密性良好。
下列说法不正确的是( )A.关闭止水夹1,打开止水夹2,挤压胶头,滴入稀盐酸,会产生二氧化碳B.反应开始后会观察到1处紫色石蕊溶液变红C.反应开始后会观察到2处澄清石灰水变浑浊D.关闭止水夹2,打开止水夹1,再次挤压胶头,一段时间后,会观察到导管中液面下降。
2018年秋人教版九年级化学上册二氧化碳的性质及制取专题训练课件(共21张PPT)

专题训练(六)
氧气和二氧化碳
(3) 实 验 室 制 取 并 收 集 二 氧 化 碳 气 体 , 选 择 的 仪 器 组 合 是
专题训练(六)
氧气和二氧化碳
图 ZT6-2 (2)关闭 K1 、打开 K2,观察到蜡烛缓慢地熄灭。蜡烛熄灭的原因是
B中产生二氧化碳气体,压强增大,大于外界大气压,气体进入烧杯中,二氧 ___________________________________________________________ 化碳不可燃也不助燃 __________________________________________________________ 。
图 ZT6-4 A.不可能收集到一瓶 CO2,因为 CO2 能溶于水 B.选择乙、丙两种装置,导管 b 接导管 d 可收集到一瓶 CO2 C.选择乙、丙两种装置,导管 c 接导管 d 可收集到一瓶 CO2 D.选择甲、乙两种装置,导管 a 接导管 c 可收集到一瓶 CO2
专题训练(六)
氧气和二氧化碳
专题训练(六)
类型2
氧气和二氧化碳
氧气和二氧化碳的制取
6.实验室用高锰酸钾制氧气和用石灰石与稀盐酸反应制二氧化碳 相比较,正确的是( C A.反应装置相同 B.实验时均无须加热 C.都能用向上排空气法收集气体 D.反应类型都是分解反应 )
专题训练(六)
氧气和二氧化碳
7.下列有关实验的描述中,正确的是( D ) A.实验室制二氧化碳,向容器中先加稀盐酸,后加入石灰石 B.将点燃的木炭迅速伸入充满氧气的集气瓶中 C.用燃着的木条检验气体是不是二氧化碳 D.用排水法收集氧气时,要等到水槽中出现连续均匀的气泡时才开始 收集
2018年秋九年级化学上册 第五章 燃料 5.3 二氧化碳的性质和制法 第2课时 二氧化碳的制法、用途、碳循环练习

第2课时 二氧化碳的制法、用途、碳循环
(2)解:设该石灰石样品中碳酸钙的质量为 x。
CaCO3+2HCl===CaCl2+H2O+CO2↑
100
44
x
4.4 g
100 x
44 =4.4 g
第2课时 二氧化碳的制法、用途、碳循环
7.2017·凉山 下列是实验室发生和收集气体的简易 请按题意要求完成填空。
图5-3-10
第2课时 二氧化碳的制法、用途、碳循环
(1)a仪器名称为___试__管_______,b仪器名称为___长_颈_ (2)实验室用石灰石和稀盐酸制取二氧化碳的装置是 发生化学反应的化学方程式为___Ca_C_O_3+__2_HC_l_=_=_=_Ca_C_l_2+_ 该气体通入装置E发生的现象是__澄__清_石__灰_水__变_浑__浊___, 式为_C_O_2_+_C_a_(_OH_)_2_==_=_C_a_CO_3_↓_+__H_2O_。实验室不用装置F收 原因是_二__氧__化_碳__能_溶__于__水_____。 (3)相对于B装置,G装置的优点是__可__以_控__制_反__应__速_率__
第2课时 二氧化碳的制法、用途、碳循环
B规律方法综合练
5.实验室制取CO2的有关操作如图5-3-8所示,其 是( B )
图5-3-8
第2课时 二氧化碳的制法、用途、碳循环
[解析]块状大理石与稀硫酸反应生成的硫酸钙微溶于水, 硫酸钙附着在大理石的表面,使大理石与稀硫酸隔绝,反 以不能用稀硫酸与大理石反应制取二氧化碳。
5.3 二氧化碳的性质和
第五章 燃料
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
二氧化碳的制取及相关推断
一、单选题(共4道,每道10分)
1.下列有关实验室制取二氧化碳的方法错误的是( )
A.药品可选用块状石灰石和稀盐酸
B.二氧化碳的密度比空气的大,故能用向上排空气法收集
C.可用紫色石蕊溶液检验生成的二氧化碳
D.将燃着的木条放在集气瓶口,检验二氧化碳是否收集满
2.取几粒石灰石放入试管中,向其中加入足量的酸,开始时有气泡产生,但是一会儿后就不再产生气泡,可能的原因是( )
A.装置漏气
B.加入的是稀硫酸
C.加入的是浓盐酸
D.生成的气体被酸溶解了
3.下列发生装置中可用于实验室制取二氧化碳的是( )
A. B.
C. D.
4.如图是小明设计的制取二氧化碳的发生装置,用铜丝网包住石灰石(铜不与盐酸反应),下列叙述错误的是( )
A.该实验设计要注意保证气密性良好,才能使实验成功
B.使用浓盐酸,能很快得到纯净的二氧化碳
C.将铜丝网浸入液面可使反应发生,拉出液面可使反应停止
D.该装置适用于常温下块状固体和液体的反应
二、填空题(共1道,每道20分)
5.如图是实验室常用来制取气体的装置,某实验小组想制取二氧化碳,请根据所学知识回答以下问题:
(1)甲同学想控制好反应的速率,则发生装置应选择____(填序号,下同)。
乙同学想随时控制反应的发生和停止,则发生装置应选择____。
(2)收集二氧化碳的装置可以是D、E、F中的____。
丙同学提议用G装置收集二氧化碳,则气体应从____(填“a”或“b”)端通入。
三、解答题(共3道,每道12分)
6.部分含碳物质的转化关系如图所示:
(1)写出下列物质的化学式:X,Y。
(2)Z转化成H2CO3的化学方程式为。
7.A、B、C、X、Y均为初中常见的物质,它们之间有如下转化关系(部分生成物已略去)。
(1)若X、Y均为氧气,则A是(写化学式),反应②的化学方程式为。
(2)若A、C均是大理石的主要成分,B是一种气体,则反应①的化学方程式为,反应②的化学方程式为。
8.A、B、C、D、E都是初中化学常见的物质。
A为白色难溶于水的固体,B、D、E均为氧化物,常温下B为固态,D为液态,E为气态。
它们之间的转化关系如图所示(部分生成物已略去)。
(1)写出下列物质的化学式:C,E。
(2)A→B的化学方程式为;
B→C的化学方程式为。
