链球菌溶血素O抗原的原核表达及条件优化
链球菌感染与抗O相关性研究

风湿热
青霉素? 青霉素?
ASO增高
ASO持 续增高
未知!
ASO增高
链球菌感染的风险? 风湿热、AGN的风险?
ASO增高与链球菌感染的关系
97.5% 平均值 2.5%
Clin. Vaccine Immunol. 2009, 16(2):172.
定的溶血毒素 • 大多数A族,许多C族、G族链球菌可产生
链球菌溶血素O • “O”指对氧不稳定
链球菌感染
• 近期咽喉部链球菌感染的证据:培养和抗 体检测,培养阳性率低
• 抗体检测成为主要手段
检测
• ASO通过血清学方法检测:乳胶凝集实验 或玻片凝集实验,ELISA可以定量检测,散 射比浊法。
• 凝集实验可以通过连续稀释法检测ASO滴 度进行定量
• 病史:2-3周前链球菌感染 • 临床表现:风湿热、肾小球肾炎、其他等
症状体征和实验室检查 • 链球菌的直接证据:培养(—) 病因? • 间接证据:ASO增高
链球菌
• 急性咽炎中15%-30%是由链球菌引起 • A族链球菌带菌者在学龄期儿童约占15%-
20% • 链球菌咽炎后1%-3%发生风湿热,急性肾
– 猩红热 – B族链球菌 免疫功能低下时,引起皮肤感染、心内膜炎、
产后感染、新生儿败血症和新生儿脑膜炎 – 甲型溶血性链球菌 若心脏瓣膜缺陷或损伤,引起亚急
性细菌性心内膜炎
• 超敏反应性疾病 风湿热,急性肾小球肾炎
ASO
• ASO是针对链球菌溶血素O的抗体 • 链球菌溶血素O是具有免疫原性,对氧不稳
抗链球菌溶血素“O” ASO
王晓川 复旦大学附属儿科医院临床免疫科
问题的提出
仅仅ASO增高的儿童 是否需要使用长效青霉素?
简述抗链球菌溶血素O实验的原理及应用

简述抗链球菌溶血素O实验的原理及应用1. 概述抗链球菌溶血素O实验是一种常用的实验方法,用于检测人类血清中是否存在对链球菌溶血素O的抗体。
链球菌溶血素O是链球菌菌株的一种分泌物,具有溶解红细胞的能力。
由于人体免疫系统可以产生抗体来对抗链球菌感染,因此抗链球菌溶血素O实验可以作为一种诊断工具,用于检测患者体内是否存在链球菌感染抗体。
2. 原理抗链球菌溶血素O实验的原理基于抗原-抗体反应。
抗原是指能够引发免疫反应的物质,抗体是人体免疫系统产生的一种特殊蛋白质,可以与特定抗原结合并发挥免疫作用。
在抗链球菌溶血素O实验中,链球菌溶血素O作为抗原,与患者体内的抗体相互作用。
具体操作原理如下: - 采集患者血液样本,离心分离血清。
- 准备链球菌溶血素O抗原。
- 将血清与链球菌溶血素O抗原反应,如果存在相应的抗体,血清中的抗体与抗原结合形成免疫复合物。
- 加入大肠杆菌裂解物,通过人工制备的人红细胞酶系统来检测溶血现象。
- 观察试管中血清的溶血情况,根据溶血程度判断患者体内是否存在抗链球菌溶血素O抗体。
3. 应用抗链球菌溶血素O实验的应用主要体现在以下几个方面:3.1 临床诊断抗链球菌溶血素O实验可以用来判断患者体内是否存在抗链球菌溶血素O抗体。
通过检测血清的溶血情况,可以评估人体免疫系统对链球菌感染的反应程度。
临床上通常将抗链球菌溶血素O实验作为一种辅助诊断手段,用于判断患者是否患有链球菌感染。
3.2 感染监测抗链球菌溶血素O实验也可用于监测链球菌感染的治疗效果。
通过定期检测患者血清中的抗链球菌溶血素O抗体水平,可以评估治疗的有效性。
如果抗体水平明显下降,说明治疗效果良好;反之,如果抗体水平升高或持续较高,可能需要调整治疗方案。
3.3 流行病学研究抗链球菌溶血素O实验在流行病学研究中也有一定的应用。
通过检测不同地区、不同人群血清中的抗体水平,可以评估不同人群对链球菌感染的暴露情况和免疫状况。
这对于了解链球菌传播途径、控制传染病的流行具有重要意义。
【关于优化原核表达的一些总结】

我认为,进行原核表达条件优化主要应注意以下几方面:1.密码子最优化(codon of optimization):大肠杆菌某些核糖体蛋白质中的使用频率不同,有最佳密码子(optimal codons)或偏爱密码子(preferred codons),稀有或利用率低的密码子(rare or low-usage codons)。
大肠杆菌稀有密码子主要有ATA,CTA,CCC,ACG,CGA,CGG,AGG,GGA,GGG等。
另外,大肠杆菌偏爱的终止密码子为UAA,而哺乳动物偏爱的终止密码子为UGA。
同时,终止密码子的下游碱基对翻译有效终止有影响,大肠杆菌中UAAN,N的影响力次序为:U>G>A,C;哺乳动物中UAGN,N的影响力次序为:A,G>>C,U。
我用的pET-43.1,先用宿主菌BL21(DE3),没有目的带出现,后改用RosettaBlueTM(DE3),目的蛋白表达效率达50%以上,并且是可溶的。
2.启动子是DNA链上RNA聚合酶的识别位点和结合位点,外源基因表达的理想启动子是可以指导高效转录,保证目的基因高效表达的启动子。
乳糖启动子是最常用的启动子,但容易引起外源基因的渗漏表达,对细胞的生长产生毒害作用;其他从乳糖启动子构建而来的启动子,多用IPTG诱导,IPTG对菌体也有毒害作用。
若IPTG对宿主菌有毒,可以同时加入IPTG和乳糖诱导表达,这样可减少IPTG的浓度。
若目的蛋白有毒,可用Invitrogen公司的pLEX系统等。
3.培养基的成分:用M9ZB和NZCYM培养基培养细菌,增加细菌质粒拷贝数;用LB培养基表达外源蛋白,提高蛋白表达量。
【毒性较大蛋白表达条件优化】:1)一般发酵时高温、高浓度诱导剂(IPTG)有利于表达表达包涵体形成,减少毒性。
2)加大氨苄的浓度(可达400mg/ml)并提高培养基中葡萄糖浓度(可达0.5%)有利于稳定表达,并要及时补充葡萄糖使其浓度维持在0.5%。
原核表达条件优化

原核表达条件优化E.coli中蛋白表达量的因素除载体启动子结构以外,还有质粒拷贝数、质粒稳定性、mRNA结构、密码子的偏爱性和宿主菌的生长状态等因素[58]。
由于V ector NTI suitor7.0软件模拟表达,可知mRNA结构和密码子的偏爱性两个影响因素不会造成表达困难,所以本实验的工作主要针对载体拷贝数、载体稳定和宿主菌的生长状态。
本实验中重组表达质粒PrP-pET-32a(+)不稳定的原因可能是PrP对E.coli BL21(DE3)具有细胞毒性。
pET-32a(+)来源于pBR-322,pBR-322源于ColE1。
ColE1、pBR-322 、pET-32a(+)都失去了分配功能区par。
而天然质粒具有功能区par,可以保证质粒在每次细胞周期中准确的进行分离,并均等的分配到子代细胞中去。
功能区par对质粒PrP-pET-32a(+)的稳定性是不可缺少的[4]。
缺少功能区par的pET-32a (+)质粒在每次细胞周期中随机分配到子代细胞中去,无细胞毒性时约98% E.coli BL21(DE3)会带有质粒(见《pET System Manual》34页)。
表达有细胞毒性蛋白的E.coli BL21(DE3)不具有生长优势,而且随细菌培养时间的增加β-内酰氨酶将逐渐释放到溶液中去,破坏溶液中的AMP。
【β-内酰氨酶功能强大,细菌培养稀释1000倍以后还能破坏几乎所有的AMP(见《pET System Manual》33页)】。
这样本不具有生长优势的表达菌又失去了选择压力,造成大部分新生细菌无质粒,表现为表达困难。
本实验证实约60%以上的细菌无质粒。
鉴于以上原因,本实验将融合蛋白Trx-PrP C27-30表达分成两个阶段,前一个阶段为质粒生长阶段,主要保证质粒的稳定性和提高质粒的拷贝数;后一个阶段为融合蛋白表达阶段,待细菌生长达饱和以后,诱导融合蛋白Trx-PrP C27-30的表达。
抗链球菌溶血素O(ASO)测试:原理,步骤,解释和临床意义

·什么是抗链球菌溶血素O(ASO)?抗链球菌溶血素O(ASO或ASLO)是针对链球菌溶血素O产生的抗体,链球菌溶血素O 是由A组的大多数菌株以及C和G 组的许多菌株产生的一种免疫原性,氧不稳定的溶血毒素。
在链球菌感染的过程中,细菌的细胞外产物充当抗原,机体通过产生特异性抗体对抗原作出反应。
链球菌溶血素O(SLO)是几乎所有化脓性链球菌菌株产生的两种溶血素之一(另一种是链球菌溶血素 S)。
字母“ O”表示该毒素对氧气不稳定。
SLO毒素对心脏组织有直接的毒性作用。
在链球菌感染的过程中,SLO刺激特异性抗链球菌溶血素(ASO)抗体的产生,该抗体可在体外中和抗原的溶血特性。
ASO检测的临床意义大于166 Todd单位(或> 200 IU)的抗链球菌溶血素滴度在成人中被认为是阳性测试,而成人的正常值小于166 Todd单位,这表明是阴性测试。
在研究链球菌后疾病,特别是急性链球菌后肾小球肾炎和风湿热中,ASO抗体滴度的测量很重要。
•超过80%的急性风湿热患者和95%的急性肾小球肾炎患者的ASO滴度升高。
•抗体水平在链球菌感染后的1-3周开始上升,在3-5周达到峰值,然后在6-12个月后又回落到微不足道的水平,因此阳性试验可以表明目前的,但最近的A,C,和G链球菌感染。
ASO测试ASO测试通过血清学方法如乳胶凝集或载玻片凝集进行。
可以进行ELISA以检测确切的滴度值。
此处介绍的测试原理,步骤和解释均基于乳胶抗链球菌溶血素O(ASO)测试。
测试原理ASO乳胶凝集是一种快速,简单的测试,用于定性和半定量测量人血清中抗链球菌溶血素-O抗体。
该方法基于与生物学惰性乳胶颗粒结合的链球菌外切酶与测试样品中的链球菌抗体之间的免疫反应。
已对试剂进行了调整,以使血清中存在200 IU / mL或更高的ASO滴度可以使胶乳颗粒明显凝集。
定性测试(筛选)程序:1.将所有试剂和标本置于室温。
2.将一滴(50微升)阳性对照和50微升患者血清放入载玻片上的不同圆圈中。
【专题讨论】原核表达条件优化

【专题讨论】原核表达条件优化!之所以首先介绍Novagen公司的产品是因为用过它的pET系列载体,感觉很好用。
Novagen的母公司是德国默克(Merck)公司,它是国际著名的化学及制药公司总部位于德国的Darmstadt,已有300多年的历史。
已在全世界55个主要国家设立了分公司,其中在28个国家建有62个生产基地。
Novagen公司出品的pET系列载体是目前应用最为广泛的原核表达系统,已经成功地在大肠杆菌中表达了各种各样的异源蛋白。
pET系列载体是利用大肠杆菌T7噬菌体转录系统进行表达的载体,其表达原理见下图。
T7噬菌体具有一套专一性非常强的转录体系,利用这一体系中的元件为基础构建的表达系统称为T7表达系统。
T7噬菌体基因编码的T7RNA聚合酶选择性的激活T7噬菌体启动子的转录。
它是一种高活性的RNA 聚合酶,其合成mRNA的速度比大肠杆菌RNA聚合酶快5倍左右。
并可以转录某些不能被大肠杆菌RNA聚合酶有效转录的序列。
在细胞中存在T7 RNA聚合酶和T7噬菌体启动子的情形下,大肠杆菌宿主本身基因的转录竞争不过T7噬菌体转录体系,最终受T7噬菌体启动子控制的基因的转录能达到很高的水平。
T7噬菌体启动子的转录完全依赖于T7 RNA聚合酶,因此T7 RNA聚合酶的转录调控模式就决定了表达系统的调控方式。
噬菌体DE3是λ噬菌体的衍生株,一段含有lacⅠ,lacUV5启动子和T7 RNA聚合酶基因的 DNA片段倍插入其int基因中,用噬菌体DE3的溶源菌,如BL21(DE3)、 HMS174(DE3)等作为表达载体的宿主菌,调控方式为化学信号诱导型,类似于Lac表达系统。
从开始涉及表达的时候可以根据是否要用基因本身的起始密码子进行选择,Novagen公司仅提供三个载体:pET-21(+),pET-24(+)和pET-23(+)。
如果你打算利用载体的起始密码子,那么就有许多选择。
根据是否要可溶性表达,选择加有不同标记的载体。
定量测定抗链球菌溶血素“O”的检测分析
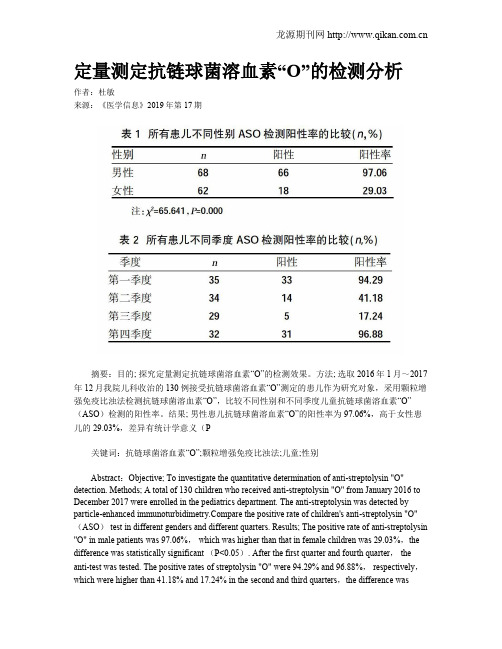
定量测定抗链球菌溶血素“O”的检测分析作者:杜敏来源:《医学信息》2019年第17期摘要:目的; 探究定量测定抗链球菌溶血素“O”的检测效果。
方法; 选取2016年1月~2017年12月我院儿科收治的130例接受抗链球菌溶血素“O”测定的患儿作为研究对象,采用颗粒增强免疫比浊法检测抗链球菌溶血素“O”,比较不同性别和不同季度儿童抗链球菌溶血素“O”(ASO)检测的阳性率。
结果; 男性患儿抗链球菌溶血素“O”的阳性率为97.06%,高于女性患儿的29.03%,差异有统计学意义(P关键词:抗链球菌溶血素“O”;颗粒增强免疫比浊法;儿童;性别Abstract:Objective; To investigate the quantitative determination of anti-streptolysin "O" detection. Methods; A total of 130 children who received anti-streptolysin "O" from January 2016 to December 2017 were enrolled in the pediatrics department. The anti-streptolysin was detected by particle-enhanced pare the positive rate of children's anti-streptolysin "O" (ASO) test in different genders and different quarters. Results; The positive rate of anti-streptolysin "O" in male patients was 97.06%, which was higher than that in female children was 29.03%,the difference was statistically significant (P<0.05). After the first quarter and fourth quarter, the anti-test was tested. The positive rates of streptolysin "O" were 94.29% and 96.88%, respectively,which were higher than 41.18% and 17.24% in the second and third quarters,the difference wasstatistically significant (P<0.05).Conclusion; The positive rate of anti-streptolysin "O" may be related to the child's own gender and season, among which male children and winter and spring seasons are more affected.Key words:Anti-streptolysin "O";Particle-enhanced immunoturbidimetry;Children;Gender溶血性鏈球菌(hemolytics streptococcus)又称沙培林,对热和化学清毒剂均敏感,常引起扁桃体炎、咽炎、中耳炎等感染。
抗链球菌溶血素“O”检测临床价值论文

抗链球菌溶血素“O”检测的临床价值摘要:目的:探讨抗链球菌溶血素“o”的诊断价值。
方法:对抗链球菌溶血素“o”采取胶乳法检测。
结果:抗链球菌溶血素“o”抗体测定,对于急性肾小球肾炎的诊断有重要价值。
急性肾小球肾炎有70%~80%患者可有抗链球菌溶血素“o”抗体滴度增高。
关键词:抗链球菌溶血素“o”;诊断;价值【中图分类号】r37【文献标识码】a【文章编号】1672-3783(2012)04-0127-01链球菌溶血素“o”是β-溶血性链球菌a族的重要代谢产物,是具有溶血活性的蛋白质,能溶解人及动物的红细胞[1]。
同时,链球菌溶血素“o”又具有抗原性,能刺激机体产生相应的抗体,称为抗链球菌溶血素“o”抗体(aso)。
临床实验室常用胶乳凝集法和免疫比浊法进行测定。
现对胶乳凝集法检测的方法分析如下。
1 材料方法1.1 标本来源:收集我院2011年1月~12月120例门诊或住院患者血清。
共中风温热50例,游走性关节疼痛伴发热39例,急性肾小球肾炎31例。
新鲜标本血清,如当天采集标本不能及时测定请保存于-20℃,临用前37℃快速解冻。
1.2 方法1.2.1 试剂:包被胶乳溶液。
1.2.2 操作:试剂在室温平衡15分钟。
在反应板的不同反应区(圈)内分别加入标本血清50 μl、阳性对照、阴性对照血清。
摇匀胶乳试剂,在上述反应区分别滴加1滴胶乳试剂,与血清标本混合混匀。
放在水平旋转振荡器上80~100 rpm 2分钟。
阳性可出现凝集反应。
阴性呈现均匀乳状。
2 结果正常参考值乳胶凝集法为阴性。
急性肾小球肾炎多见于链球菌感染后,链球菌感染后急性肾炎70%~90%抗链球菌溶血素“o”效价升高。
在链球菌感染后1~3周开始增加,3~5周达峰值,继之逐渐降低,约50%患者在半年内恢复正常。
3 讨论链球菌溶血素“o”是a族溶血性链球菌的代谢产物之一。
它是一种具有溶血活性的蛋白质,具有抗原性。
a族溶血性链球菌在人体中作为正常菌群存在,正常人体内的抗链球菌溶血素“o”(aso)具有一定基础值。
原核表达系统三大要素的选择及优化
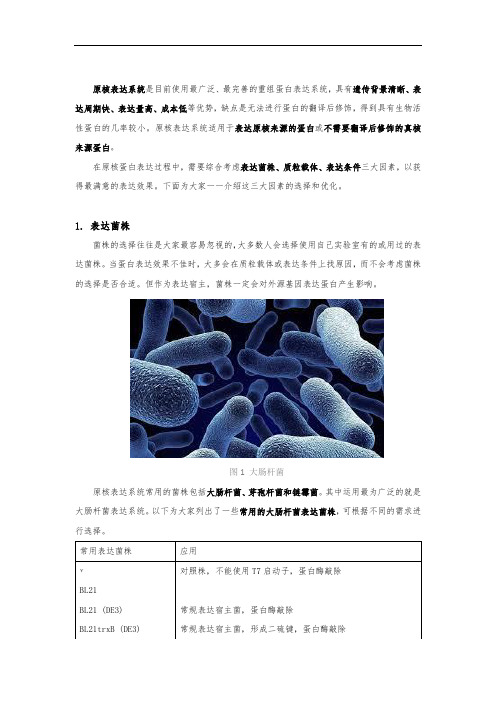
原核表达系统是目前使用最广泛、最完善的重组蛋白表达系统,具有遗传背景清晰、表达周期快、表达量高、成本低等优势,缺点是无法进行蛋白的翻译后修饰,得到具有生物活性蛋白的几率较小。
原核表达系统适用于表达原核来源的蛋白或不需要翻译后修饰的真核来源蛋白。
在原核蛋白表达过程中,需要综合考虑表达菌株、质粒载体、表达条件三大因素,以获得最满意的表达效果。
下面为大家一一介绍这三大因素的选择和优化。
1. 表达菌株菌株的选择往往是大家最容易忽视的,大多数人会选择使用自己实验室有的或用过的表达菌株。
当蛋白表达效果不佳时,大多会在质粒载体或表达条件上找原因,而不会考虑菌株的选择是否合适。
但作为表达宿主,菌株一定会对外源基因表达蛋白产生影响。
图1 大肠杆菌原核表达系统常用的菌株包括大肠杆菌、芽孢杆菌和链霉菌。
其中运用最为广泛的就是大肠杆菌表达系统。
以下为大家列出了一些常用的大肠杆菌表达菌株,可根据不同的需求进行选择。
2. 质粒载体质粒表达载体上的重要元件包括启动子,多克隆位点,终止子,复制子,信号肽,融合标签,筛选标记等。
根据载体上这些元件的特性,有多种质粒可供选择。
图2 大肠杆菌表达质粒pET-22b(+)图谱启动子:根据启动子的强弱考虑,强启动子可以提高蛋白表达量;弱启动子可以降低本底表达、增加可溶表达、表达小量伴侣蛋白等。
根据启动子的作用方式考虑,组成型启动子使宿主不停的表达重组蛋白;诱导型启动子使宿主在特定诱导条件下表达重组蛋白。
终止子:终止子的作用在于保护mRNA在核外不被降解,延长mRNA的寿命,以提高重组蛋白表达量。
对于T7系统来说,由于T7 RNA聚合酶效率非常高,保证一直有充足的mRNA 提供翻译,所以终止子对其影响不大,只有一些自身带有起始密码子的外源基因需要终止子。
~复制子:复制子决定质粒载体拷贝数,拷贝数越高,重组蛋白表达量就越高。
表达载体通常会选用高拷贝的复制子,但过高的拷贝数会影响质粒稳定性和宿主生长。
抗链球菌溶血素O在Cobas c501生化分析仪上的比对试验

抗链球菌溶血素O在Cobas c501生化分析仪上的比对试验(作者:___________单位: ___________邮编: ___________)【摘要】目的: 对“抗链球菌溶血素O诊断试剂盒”在Cobas c501生化分析仪上进行体外诊断和分析。
方法: 收集临床“风湿热”患者血标本135份, 用已具备中国注册证和临床常规使用的免疫比浊方法与罗氏诊断产品(上海)有限公司“抗链球菌溶血素O诊断试剂盒”作比对检测, 评价其试验结果。
结果: 用参比试剂和考核试剂共检测各类标本135份, 参比试剂与考核试剂显著有关(r=0.966, y=1.204x-22.217, R2=0.9333)。
结论: 抗链球菌溶血素O在Cobas c501生化分析仪上的应用与参比试剂间总体的符合情况良好。
【关键词】抗链球菌溶血素O; 质控品; 生化分析特异性抗体的免疫测定可为临床判断链球菌感染程度及病期提供有用信息。
其中, 抗链球菌溶血素O抗体(ASO)浓度的测定在临床上应用的最为广泛。
“抗链球菌溶血素O诊断试剂盒”采用免疫比浊法原理[1, 2], 在在Cobas c501生化分析仪上应用具有准确、快速检测的临床意义。
1 材料和方法1.1 标本收集收集本院2009-03/2009-06门诊和住院“风湿热”患者送检的血液样本共135份(其中含溶血标本10份、脂血标本10份、 RF(+)10份及黄疸标本5份)。
1.2 主要试剂抗链球菌溶血素O诊断试剂盒(规格150Test和Test), 及相关试剂Precinorm Protein(批号18234301)、 Precipath Protein(批号18234401)及C.f.a.s.PAC(批号18210901)均购自德国罗氏诊断产品(上海)有限公司。
对比试验产品的确立, 选择有国家食品药品监督管理局批准文号的“抗链球菌溶血素O诊断试剂盒”[注册证号: SFDA(I)20053402551]作为参比试剂, 与被考核试剂做对比试验。
抗链球菌溶血素o试验名词解释

抗链球菌溶血素O试验一、概述抗链球菌溶血素O试验(Antistreptolysin O Test,简称ASO)是一种常用的实验室检测方法,用于检测人体血清中抗链球菌溶血素O抗体的水平。
链球菌溶血素O是一种由溶血性链球菌分泌的外毒素,可引起机体产生相应的抗体。
ASO试验可以帮助医生诊断链球菌感染、风湿热等疾病,并追踪疾病的治疗过程。
二、检测原理链球菌溶血素O抗体是一种IgG类型的抗体,主要由B淋巴细胞产生。
ASO试验通过检测血清中的ASO抗体水平,间接反映出链球菌感染的程度。
具体的检测步骤如下:1.血清收集:从患者的静脉血样中分离出血清,作为后续实验的样品。
2.抗原溶液制备:将链球菌溶血素O抗原与试剂盒中提供的缓冲液混合,制备出抗原溶液。
3.反应操作:将待测血清样品与抗原溶液混合,使其发生免疫反应。
4.血凝抑制反应:观察反应液中是否有凝集发生,判断ASO抗体水平的高低。
三、ASO抗体的临床意义ASO抗体的浓度与链球菌感染的程度密切相关。
一般来说,链球菌感染后,ASO抗体的水平会在感染后的1-2周内明显升高,然后逐渐下降,通常在6-12周内恢复至正常水平。
因此,ASO试验可以用于以下方面的临床判断:1. 链球菌感染的诊断ASO试验可以辅助医生诊断链球菌感染,特别是对于那些没有明显症状或症状不典型的患者。
通过测定血清中ASO抗体的水平,可以判断是否存在链球菌感染,并评估感染的严重程度。
2. 风湿热的筛查与监测风湿热是一种自身免疫性疾病,常由链球菌感染引发。
ASO抗体与风湿热的发生有密切关系。
通过定期监测患者血清中ASO抗体的水平,可以及早发现风湿热的复发或趋势,指导治疗和预防措施的制定。
3. 抗生素疗效监测对于链球菌感染的治疗,抗生素是常用的治疗药物。
ASO试验可以用于评估抗生素疗效的监测。
如果ASO抗体的水平在治疗过程中逐渐下降,说明抗生素治疗有效;如果ASO抗体的水平持续升高或下降缓慢,可能需要调整治疗方案。
抗链球菌溶血素o试验原理

抗链球菌溶血素o试验原理一、前言抗链球菌溶血素O试验是一种常用的实验方法,用于检测人体中是否存在链球菌感染。
本文将详细介绍抗链球菌溶血素O试验的原理。
二、什么是链球菌链球菌是一种革兰氏阳性球形细菌,常见于口腔、喉咙、皮肤和泌尿生殖道等部位。
其中最常见的是A群链球菌,它可以引起多种疾病,如扁桃体炎、中耳炎、皮肤感染等。
三、什么是抗链球菌溶血素O抗链球菌溶血素O(Anti-streptolysin O, ASO)是一种特异性抗体,可与链球菌产生的溶血素O结合,并使其失去活性。
当人体受到链球菌感染时,会产生ASO以对抗这些致病微生物。
四、什么是抗链球菌溶血素O试验抗链球菌溶血素O试验(ASOT)是一种检测人体中ASO水平的实验方法。
通过测量患者血清中ASO的含量来判断是否存在链球菌感染,以及感染的程度。
五、抗链球菌溶血素O试验的原理ASOT的原理是利用链球菌产生的溶血素O与ASO之间的特异性结合反应。
首先,将待测血清与已知浓度的链球菌溶血素O标准品混合,使其发生特异性结合反应。
然后,加入一定量的红细胞悬液,使其在一定时间内与链球菌溶血素O和ASO之间发生反应。
最后,通过比较红细胞悬液中游离的溶血素量来判断ASO水平。
六、实验步骤1. 准备标准品:将已知浓度的链球菌溶血素O标准品稀释至不同浓度。
2. 取少量待测血清加入不同浓度的链球菌溶血素O标准品中混合。
3. 加入一定量红细胞悬液,并在恒温条件下孵育30分钟。
4. 离心沉淀后,比较各组游离溶血素量之差,即可得到ASO水平。
七、结果分析通过比较待检测样本中游离溶血素量与标准品中游离溶血素量之差,可以得到ASO水平。
如果ASO水平高于正常范围,则说明可能存在链球菌感染。
八、注意事项1. 实验前应检查试剂是否过期。
2. 血清应存放在冰箱中,避免反复冻融。
3. 操作时应注意无菌操作,避免污染。
4. 实验结果应结合临床症状和其他检查结果进行综合分析。
九、总结抗链球菌溶血素O试验是一种简单易行的实验方法,用于检测人体中是否存在链球菌感染。
一种抗链球菌溶血素“O”检测方法[发明专利]
![一种抗链球菌溶血素“O”检测方法[发明专利]](https://img.taocdn.com/s3/m/1625496c814d2b160b4e767f5acfa1c7aa008210.png)
(10)申请公布号(43)申请公布日 (21)申请号 201510227885.3(22)申请日 2015.05.02G01N 33/545(2006.01)G01N 33/543(2006.01)G01N 33/569(2006.01)(71)申请人王贤俊地址325000 浙江省温州市瓯海娄桥工业园区森茂路28号(72)发明人王贤俊 郑蓓蕾 郭二豪 江新涛(54)发明名称一种抗链球菌溶血素“O”检测方法(57)摘要本发明提供一种抗链球菌溶血素“O”(ASO)检测方法,所述检测方法原理基于胶乳增强免疫比浊法,其特点在于应用化学方法交联,通过水溶性碳化二亚胺(EDC)与N-羟基琥珀酰亚胺(NHS)使溶血素“O”与羧化聚苯乙烯胶乳共价交联,形成抗链球菌溶血素“O”胶乳颗粒(简称ASO 胶乳颗粒),同待测样品混合后在37℃恒温,波长为540nm 下,测定吸光度,计算出样品中ASO 抗体含量。
本检测方法灵敏度高,特异性强,试剂配制简单,值得进一步推广使用。
(51)Int.Cl.(19)中华人民共和国国家知识产权局(12)发明专利申请权利要求书1页 说明书4页 附图1页(10)申请公布号CN 104865379 A (43)申请公布日2015.08.26C N 104865379A1.一种抗链球菌溶血素“O”(ASO)检测方法,所述检测方法原理基于胶乳增强免疫比浊法,其特点在于应用化学方法交联,通过水溶性碳化二亚胺(EDC)与N-羟基琥珀酰亚胺(NHS)使溶血素“O”与羧化聚苯乙烯胶乳共价交联,形成抗链球菌溶血素“O”胶乳颗粒(简称ASO胶乳颗粒),同待测样品混合后在37℃恒温,波长为540nm下,测定吸光度,计算出样品中ASO抗体含量。
2.根据权利要求1所述化学交联方法制备ASO胶乳颗粒,其特征在于所用的羧化聚苯乙烯胶乳粒径为100-150nm。
3.根据权利要求1所述的化学交联法制备ASO胶乳颗粒,其特征在于包括如下步骤:1)配制含有N-吗啉乙磺酸(MES)和NaOH的PH6.1活化缓冲液;配制含有磷酸一氢钾,磷酸二氢钾和盐酸的PH7.4标记缓冲液;配制含有磷酸一氢钾,磷酸二氢钾,Tween 20和盐酸的PH7.4保存缓冲液。
【优利特】链球菌溶血素O的基因克隆、原核表达及在胶乳增强透射比浊法测ASO试剂盒的开发应用

【优利特】链球菌溶血素O的基因克隆、原核表达及在胶乳增强透射比浊法测ASO试剂盒的开发应用链球菌溶血素O的基因克隆、原核表达及在胶乳增强透射比浊法测ASO试剂盒的开发应用摘要目的:以乙型溶血性链球菌A群菌株总DNA为模板,通过PCR 扩增得到链球菌溶血素O (SLO)基因片段,与表达载体连接后转化大肠杆菌BL21(DE3)进行可溶性表达,目的蛋白纯化后用于胶乳增强透射比浊法测ASO试剂盒的开发应用。
结果:SDS-PAGE分析表明SLO能够在大肠杆菌中进行可溶性表达,纯化后的重组SLO蛋白纯度﹥95%。
Western Blot检测显示重组SLO能与ASO高值血清有特异的免疫反应。
纯化后的重组SLO包被本公司生产的胶乳颗粒制成ASO胶乳增强透射比浊试剂盒,并与市售同类试剂上BeckmanAU480自动生化分析仪做41份临床血清标本检测比对,结果显示两者之间有良好的相关性。
结论:成功构建了稳定、高效可溶性表达重组SLO蛋白的基因工程菌株,工程菌表达的重组SLO能用于胶乳增强透射比浊法测ASO试剂盒的开发。
关键词:链球菌溶血素O;原核表达;胶乳增强透射比浊;ASO 链球菌溶血素O (SLO)是由一种化脓性球菌分泌的蛋白,它可刺激人体产生SLO抗体(ASO)[1]。
SLO属于-SH基激活的细菌性毒素之一,对心脏有急性骤停作用[2],抗原性强,85%-95%链球菌感染的患者,感染后2-3周至病愈后数月甚至一年内均可检出ASO,临床上常测定ASO作为链球菌感染引起的扁桃体炎、急性肾小球肾炎、活动性风湿热、风湿性心肌炎、皮肤及软组织等的感染诊断和监控[3,4]。
因此ASO是临床检测的常规项目。
ASO体外诊断试剂盒的主要成分是SLO抗原,利用基因工程技术构建稳定、高效可溶性表达高活性SLO的工程菌便可以为试剂盒的研发大大节约成本。
本研究运用分子生物学技术克隆SLO蛋白的DNA编码序列,采用大肠杆菌对其进行表达,实现了SLO重组蛋白在大肠杆菌表达系统中的可溶性表达。
抗链球菌溶血素O(ASO)测定

抗链球菌溶血素O(ASO)测定1检验目的指导本室工作人员规范操作本检测项目,确保检测结果的准确。
2原理ASO的测试建立在胶乳免疫测定法基础上,当血清中含有ASO时,它与R2中的SLO反应形成浊度,通过测量反应生成的浊度,并与标准的进行比较,可得出样本中ASO的浓度。
3标本要求3.1使用新鲜血清,不使用血浆.3.2在采集血液后2h分离血清.3.3 8h内不能及时测定血清可存放于2-80C冰箱保存,3天后测定的血清置-150C―-200C 冰冻保存,但冰冻血清只能复融一次.3.4严重溶血或脂血的标本不能作测定.4试剂4.1试剂:本科使用浙江伊利康生物技术限公司的试剂盒. (浙食药监械(准)字2014第2400384号 YZB/浙 2314-40-2014)4.1.1试剂盒组成如下:R1:氯化铵缓冲液:0.2mmol/L叠氮钠:0.95g/LR2:抗链球菌溶血素“O”致敏胶乳液:适量叠氮钠:0.95g/L4.1.2 试剂准备:试剂为即用式。
4.1.3 试剂稳定性与贮存:在2~8℃避光、密封的储存条件下,试剂盒自生产之日起有效期为12个月。
4.1.4 变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。
4.1.5 注意事项:试剂中含有稳定剂,可能存在一定的刺激作用和毒性,请勿直接接触皮肤及眼睛。
一旦接触,即用大量清水冲洗。
请勿吞服。
4.2 校准品:使用浙江伊利康生物技术限公司提供的ASO校准品对自动分析仪进行校准。
4.3 质控品:使用正常值、病理值复合控制品。
5 仪器AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪6 操作步骤6.1 样品的准备:将标好号的样品离心后放到仪器规定的位置。
6.2 试剂的检测:仪器开机后,检查各种试剂的位置,体积等确认无误后方可进行测定。
6.3 项目基本参数:参见生化检验AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪项目测定参数。
抗链球菌溶血素“O”校准品产品技术要求shijiwode

抗链球菌溶血素“O”校准品
适用范围:与本公司生产的试剂盒配套使用,用于抗链球菌溶血素"O"项目检测系统的校准。
1.1包装规格
0.5mL×1;0.5mL×5;1mL×1;1mL×5;10mL×1;10mL×5。
1.2主要组成成分
液体,单水平,Tris缓冲液(0.02M,pH7.5),抗链球菌溶血素“O”目标浓度为950IU/mL。
校准品靶值批特异,详见校准品瓶签。
2.1 外观
无色至淡黄色澄清液体。
外包装完整无破损。
2.2 装量
不低于标示装量。
2.3 瓶内均一性
瓶内变异系数CV≤10%。
2.4准确度
待检系统与比对系统测值的相关系数r≥0.990;在[10,300﹚IU/mL区间内,绝对偏差不超过±45IU/mL;在[300,900] IU/mL区间内,相对偏差不超过±15%。
2.5 稳定性
2.5.1效期稳定性
原包装校准品在2℃~8℃密闭贮存,有效期为12个月。
在有效期满后2个月内,校准品性能指标应符合2.1、2.3、2.4的要求。
2.5.2校准品开瓶稳定性
开瓶后校准品在2℃~8℃条件下密闭贮存,可稳定30天。
在有效期满后2天内,测试结果的相对偏差不超过±10%。
2.6校准品溯源性
按照GB/T 21415及有关规定建立溯源性,提供校准品的来源、赋值过程及测量不确定度等内容,溯源至公司内部工作校准品,并与已上市产品比对赋值。
原核表达条件的优化

【专题讨论】原核表达条件优化!会不会是蛋白质的表达量低,电泳并不能反映出来,典型的例子是干扰素,虽然电泳没有新生条带,但是裂解上清的活性却很高。
“疑为降解条带”会不会是宿主菌蛋白,42度发酵,可抑制宿主菌蛋白表达疑为降解条带”会不会是宿主菌蛋白?那条带也挂在亲合柱子上的,发酵的细菌蛋白却没有。
挂在亲合柱子上,也有可能是非特异性条带,如用HIS TAG亲合柱,加大米错量试一下。
胞内表达有生物活性蛋白的一些策略包涵体的形成仍然是胞内基因表达巨大障碍,考虑到易聚合蛋白质复性的艰辛以及收得率的问题,胞内直接表达有生物活性的蛋白质仍然有一定的意义,到现在为止,形成包涵体的理化因素仍然不清楚,统计分析的出的结论是六个因素与包涵体的形成有关:电荷的分布、转型氨基酸残基的含量、半胱氨酸的含量、脯氨酸的含量、亲水性和总氨基酸数量(1)。
有多种手段用于减少包涵体的形成以及促进蛋白质的折叠,如低温培养(3、4、11)、宿主菌的选择(12)、某些氨基酸残基的取代(14)、共表达分子伴侣(17)、硫氧还蛋白的融合表达或与目标蛋白共表达(18)和利用硫氧还蛋白还原酶缺陷菌株作为宿主菌(2、16)等。
胞内的氧化还原势是另外的问题,细菌的胞内蛋白质半胱氨酸残基和二硫键较少,含有大量二硫键的蛋白质则被输送到胞浆以外。
这样那些依靠二硫键来稳定蛋白质四级结构的蛋白质在细菌的胞浆内因为缺乏形成二硫键的系统如DsbA/DsbB难以正确折叠。
有人分离到允许胞内二硫键形成的突变株,这些突变株使编码硫氧还蛋白还原酶的TrxB基因失活以及造成一定的还原势。
硫氧还蛋白本身对于二硫键的形成不是必需的(16),该作者认为胞内有其他的类似于硫氧蛋白的蛋白能被硫氧还蛋白还原酶还原,在硫氧还蛋白还原酶缺陷的情况下,处于氧化状态的这类蛋白质能促进二硫键的形成。
这些硫氧还蛋白还原酶缺陷菌被证实为在大肠杆菌中生产复杂蛋白质的很有价值的工具。
Novagen公司pET宿主菌系列中的AD494(DE3)和Origami B(DE3)都是TrxB基因突变菌株。
抗链球菌溶血素“O”测定试剂盒 (胶乳免疫比浊法)医疗器械产品注册技术要求

医疗器械产品技术要求编号:抗链球菌溶血素“O”测定试剂盒(胶乳免疫比浊法)1.产品型号/规格及划分说明1.1包装规格试剂1:60mL×8、试剂2:48mL×2;试剂1:50mL×4、试剂2:20mL×2;试剂1:50mL×1、试剂2:10mL×1;试剂1:100mL×2、试剂2:20mL×2;试剂1:65mL×3、试剂2:39mL×1;试剂1:20mL×1、试剂2:4mL×1;2400测试/盒(试剂1:70mL×4、试剂2:14mL×4);1680测试/盒(试剂1:99mL×2、试剂2:20mL×2);1260测试/盒(试剂1:50mL×3、试剂2:9mL×3);840测试/盒(试剂1:50mL×2、试剂2:10mL×2);1260测试/盒(试剂1:50mL×3、试剂2:10mL×3);900测试/盒(试剂1:25mL×2、试剂2:5mL×2);1200测试/盒(试剂1:70mL×2、试剂2:14mL×2);960测试/盒(试剂1:50mL×4、试剂2:10mL×4);1640测试/盒(试剂1:64mL×3、试剂2:39mL×1);600测试/盒(试剂1:50mL×1、试剂2:9mL×1);800测试/盒(试剂1:70mL×2、试剂2:18mL×2)。
1.2组成成分试剂1:磷酸盐缓冲液pH 6.560mmol/L试剂2:甘氨酸缓冲液pH8.220mmol/L 包被有链球菌溶血素“O”的乳胶颗粒适量1.3适用范围用于体外定量测定人血清中抗链球菌溶血素“O”的浓度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
关键词 : 链球 菌溶血素 。抗原 ; 包涵 体 ; 自诱 导 ; 蛋 白纯 化
D OI : 1 0 . 3 9 6 9 / j . i s s n . 1 6 7 3 — 4 1 3 0 . 2 0 1 4 . 1 9 . 0 0 3 文献标识码 : A 文章编号 : 1 6 7 3 - 4 1 3 0 ( 2 0 1 4 ) 1 9 - 2 5 8 1 — 0 3
国检验 医学 杂志 2 0 1 4 年 1 O月第 3 5卷第 1 9期
I n t J L a b Me d , O c t o b e r 2 0 1 4 , V o i . 3 5 , N o . 1 9
・
2 581 ・
・
基础 实 验研 究 论著 ・
链球 菌 溶血 素 O 抗原 的原 核 表 达及 条 件 优 化
Pr ok a r y o t i c e x pr e s s i on o f s t r e pt ol y s i n O a nt i g e n a n d i t s c o nd i t i o n o pt i mi z at i o n
Hu Xi l i n, Hu a Hu an, De n g Qu n y i n g
胡锡 林 , 花 欢, 邓 群 英
( 南京 军 区鼓浪 屿 疗养 院检 验 科 , 福 建厦 门 3 6 1 0 0 2 )
摘 要 : 目的 构 建链 球 菌 溶 血 素 O 抗 原 ( S L O) 的重组表达质 粒 , 并优 化 其 在 大 肠 杆 菌 中的 最 佳 表 达 条 件 。方 法 以 A 群
i t s b e s t e x p r e s s i o n c o n d i t i o n i n Es c h e r i c h i a c o l i . Me t h o d s The DNA f r a g me n t e n c o d i n g S LO wa s a mp l i f i e d f r o m s t r e p t o c o c c a l g e — n o mi c DNA t e mp l a t e b y PC R, a n d t h e n i n c o r p o r a t e d i n t o p E T一 3 2 a ( + )v e c t o r t o c o n s t r u c t p E T一 3 2 a ( +) 一 S L O r e c o mb i n a n t p l a s —
( De pa r t me n t o f Cl i n i c a l La b o r a t o r y, Gu l a n g y u S a n a t o r i u m o f Na n j i n g Mi l i t a r y Co mma n d, Xi a me n, Fu j i a n 3 6 1 0 0 2 , C h i n a ) Ab s t r a c t : Ob j e c t i v e To c o n s t r u c t t h e r e c o mb i n a n t s t r e p t o | y s i n O a n t i g e n( S LO)p r o k a r y o t i c e x p r e s s i o n p l a s mi d a n d e s t a b l i s h
包 涵体 表 达 , 且 表 达 量 均较 低 ; 自诱 导 的 方 式 , 不仅 表 达 量 明 显 提 高 , 且 实现 了部 分 可溶 性 表 达 。结 论 成 功 构 建 了 s I 0 的 原 核
表达质 粒, 优 化 筛 选 出能 高 效 可 溶 性 表 达 的 诱 导 条 件 , 纯化 获得 了 S L O 重 组 融 合 蛋 白质 , 为 进 一 步 的基 础 及 临 床 研 究 应 用 奠 定
p y l — B — D- t h i o g a l a e t o s i d e ( I P TG) 一 i n d u c t i o n a n d a u t o - i n d u c t i o n , r e s p e c t i v e l y . Re s u l t s Th e r e s u l t s o f DNA e l e c t r o p h o r e s i s a n d DNA s e q u e n c i n g s h o we d t h a t p ET一 3 2 a ( +) 一 S LO r e c o mb i n a n t p l a s mi d wa s c o n s t r u c t e d s u c c e s s f u l l y . Wh e n I P TG a t d i f f e r e n t c o n c e n t r a —
mi d . p E T一 3 2 a ( +) 一 S L0 wa s t r a n s f o r me d i n t o Es c h e r i c h i a c o l i BI 2 1 ( DE3 )a n d S LO p r o t e i n wa s e x p r e s s e d a n d p u r i f i e d b y i s o p r o —
链球茵D NA 为模 板 , 采用P C R 法扩 增 s I 0基 因, 将 扩 增 的 基 因连 接 p E T - 3 2 a ( +) 表达载体 构建 p E T 一 3 2 a ( +) 一 S L 0重组质粒 , 重 组 质 粒 转化 到 大 肠 杆 菌 B L 2 1 ( D E 3 ) 中, 转 化 后 的 表 达 菌 经 异 丙基 一 B — I ) _ 硫 代半 乳糖苷 ( I P T G) 诱 导 和 自诱 导 的 方 式 分 别 诱 导 及 纯 化, 最 终 确 定 最佳 的表 达 条 件 。结 果 P C R 扩 增 的基 因 大 小 与 s I 0基 因大小一致 , 测序 完全正确 。不 同浓度的 I P T G诱 导均 为
