11第十一章 醛和酮
第十一章 醛酮
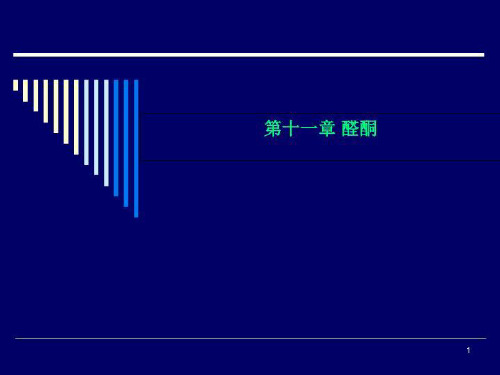
O CH3 C CH2CHCH3
CH3
4 _ 甲 基 _ 2 _ 戊 酮
CH3COCHCO3CH
CH2CH=CH2
3_烯丙基_2,4 _戊二酮
O
= CH3 C CH C CH3
CH3
4 _ 甲 基 _ 3 _ 戊 烯 _ 2 _ 酮
O C CH CH3
CH3
2 _ 甲 基 _ 1 _ 环 己 基 _ 1 _ 丙 酮
8
O
CH3
C CH=C CH3
CH3
CH3
3 _ 甲 基 _ 1 _ 2 ' , 4 ' _ 二 甲 基 苯 基 _ 2 _ 丁 烯 _ 1 _ 酮
练习: 写出下列化合物的名称或结构式:
(1). H= C CCH 2CC = H CH HCH (2)O . C3HCC2HCC3H
C3H
OO
=
=
= =
R C OH M 3 O +R C g O X 3 ° 醇 H
R
RR ' '
RR ' '
例:选择适当的原料合成2-甲基-2-戊醇。
24
4、与醇的加成反应
R H CO+
( R' )
无水HCR l OH
R''OH
C
H OR''
( R' )
R''OH R C OR''+H2O 干HCH l OR''
( R' )
OH
(C3H)2CC2H NH 2
OH
20
2、与饱和亚硫酸氢钠的加成反应
醇 钠 O C O+NaO-S-OH C ONa
第11章_醛和酮-2
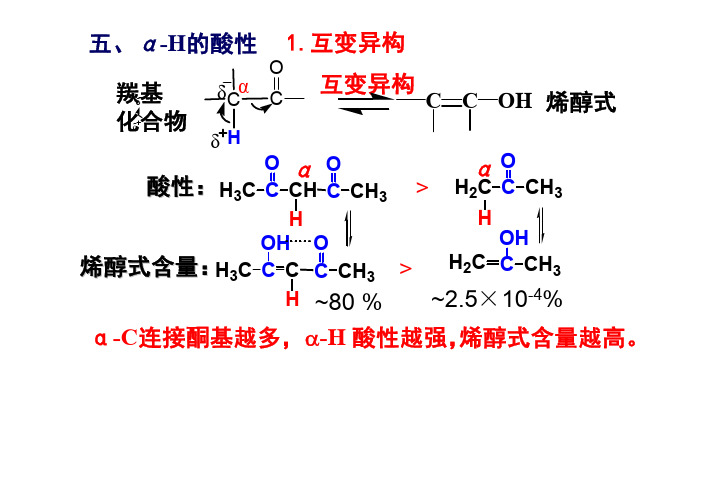
与RMgX的1,2加成后水解:
产物形式上:R-H与羰基的加成(R带负电)
δ-
δ+ C 4
Cδ-3δ+OC2 1
① R- L+i 或
δ- δ+
① RMgX
δ- δ+
①R2CuLi
δ- δ+ RH
②H3O+ 1,4-加成
HO CCC R
1,4加成后水解产物形式上:RH与双键的加成。
δ+ C 4
δCδ-3δ+OC2
Nu
R
L
L:大, M:中, S:小。
优势构象:L与C=O反式共平面;
亲核试剂易从S的一边进攻羰基。
O
S
M
Nu- + ·
RL
O-
S
M
·
Nu
R
Br
L
O
SH
M
Et
δMg H3δC H O
CH3MgBr
Et H2O H H H3C
OH Et
H
H Ph L
H Ph
Ph
主要产物
亲核试剂易从S的一边进攻羰基。
2. 亲核试剂的体积大小对加成方向的影响
C2H5 H
B. 4 位上位阻大,以1,2-加成为主。
Oδ-
C6H5CH=CHCδ+H
C2H5MgBr δ- δ+
H2O
C6H5CH
C2H5 H
OH CHCH
C2H5
2. 与强亲核试剂RLi反应,以1,2-加成为主.
δ-O
δ+
(1)PhLi
OH Ph
(2δ-)H2δO+ Ph H
有机化学 第十一章 醛酮(1)

E1
E2
19
四. 化学性质(C.P.)
结构分析 讨论1: 比较苯酚C-O与醛酮C=O的结构? C杂化形式 苯酚 醛酮 sp2 sp2 O杂化形式 sp2 sp2(国外)
H H
C O
H
C O
H
20
结构分析 讨论1: 比较苯酚C-O与醛酮C=O的结构?
H
H
C O
H
+
-
C O
H
C
H
O
H
O O CH3 C CH2 C CH3
14
2. 命名
普通命名法
醛:αβγδ… 标记取代基位置
CH3CHCH2CHO CH3 CH3OCH2CH2CH2CHO CH=CHCHO
-甲基丁醛
γ-甲氧基丁醛
-苯基丙烯醛
酮:某某基酮(与醚相似)
O CH 3 C HC CH 3
O CH2 CH C CH3
O C CH3
CH3
甲基异丙基酮
甲基乙烯基酮
苯基甲基酮 15
2. 命名
系统命名法
脂肪醛酮:选含羰基(位次小)的最长C链为母体,称某醛(酮);
O CH3CH2CHCH2C CH2CH3 CH3
5-甲基-3-庚酮
当主链中有 C=C 时,称烯醛或烯酮;
O CH2 CH C CH3
O (CH3)2CHCHCH=CHCCH3 Cl 6-甲基-5-氯-3-庚烯-2-酮
加酸反应速率减小,加入大量酸,放许多天也不反应。
● 反应条件:碱催化
● 增碳的反应:制备增1个C的羧酸
● 范围: 醛、大多数甲基酮
28
(一) 羰基的亲核加成 1. 与氢氰酸加成
11-区别醛与酮的试验

第十二节 区别醛与酮的试验醛和酮虽然都含有羰基,但由于具有不同的结构,通常表现不同的性质,可用下述反应区别醛和酮。
1. Fehling 试验[试剂组成] 由等体积的硫酸铜溶液(试剂A )和酒石酸钾钠的氢氧化钠溶液(试剂B )混合组成。
酒石酸钾钠的作用是与氢氧化铜形成络合物,避免氢氧化铜沉淀析出。
[概述] 脂肪醛可还原Fehling 试剂,析出黄至红色的Cu 2O 沉淀,而芳香醛、酮则显负性结果。
可用本试验鉴定醛,区别脂肪醛与芳香醛、脂肪醛与酮。
[反应式]2. Benedict 试验[试剂组成] Benedict 试剂是改进的Fehling 试剂。
它的组成为:硫酸铜+柠檬酸+碳酸钠。
Benedict 试剂久置后不易变质,也不必象Fehling 试剂那样配成A 、B 液分别保存。
所以,比Fehling 试剂使用方便。
[概述] 脂肪醛还原Benedict 试剂生成黄至红色Cu 2O 沉淀,而芳香醛、酮则成负性结果。
可用本实验鉴别脂肪醛和芳香醛、脂肪醛和酮。
[反应式]3. Tollen 试验[试剂组成] 由氨、硝酸银和氢氧化钠配制而成。
[概述] 醛(脂肪醛、芳香醛)遇到Tollen 试剂被氧化,试剂本身被还原成金属银,附在器壁形成银镜,故此实验又称为银镜实验。
本方法是鉴定醛,尤其是区别醛和酮的好方法。
[反应式]RCHO + 2Ag(NH 3)2OH → 2Ag + RCO 2NH 4 + 3NH 3 + H 2O4. Schiff 试验[试剂组成] 品红稀溶液经SO 2脱色。
[概述] 醛类与试剂作用显紫红色,加H 2SO 4后所显紫红色不消失者为甲醛,H 2O2++Cu 2O 2Cu(OH)2+RCHO RCO 2-H 2O2++Cu 2O 2Cu(OH)2+RCHO RCO 2-消失者为其它醛。
酮类显负性结果。
5.NaHSO3试验(见醛、酮部分)6.碘仿试验(见醛、酮部分)[习题5] 用化学方法区别(1)(2)(3)(4) CH3CHO CH3COCH3H COHºÍ¡¢CH3CH2OH CH3CH2CHCH2CH3CH3COCH3ºÍ¡¢O OºÍCH3CH2COCH2CH3CH3CHOOºÍ¡¢。
大学有机化学重点知识总结第十一章 醛、酮
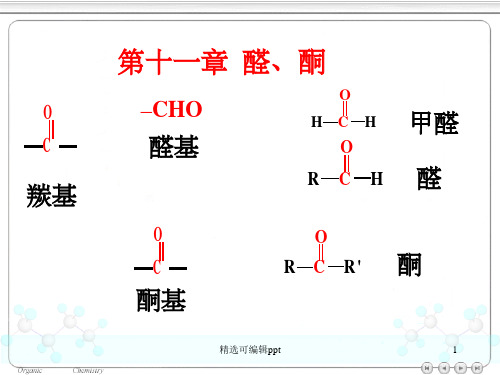
—制备增加2个C原子的伯醇:
+
H2C CH2
-+
RM gBr
O -
(C2H5)2O
R C H 2 C H 2 O M g B r
H 3O + H O C H 2C H 2R
精选可编辑ppt
42
33.
CH3 ( NBS )
CH2Br
Mg
(
干醚
CH2MgBr )
① O / 干醚
(
② H3O+
CH2CH2CH2OH )
R C O R '+H 2 O H +
R CO +2 R 'O H
(R '')HO R '
(R '')H
精选可编辑ppt
33
H +
O O C H 3
( )+ ( )
O
CH2CH2CH2CH CH3OH
HO
O
O
O
C OCH3 H
O O
C OCH3
H OC H2CH 2OH
精选可编辑ppt
34
(3)活性:醛>酮 酮一般用原甲酸三乙酯形成缩酮
O C
羰基
第十一章 醛、酮
–CHO
醛基
O HCH
O
RCH
甲醛 醛
O
C
酮基
O
R C R' 酮
精选可编辑ppt
1
烃基
脂肪族醛和酮 芳香族醛和酮
醛和酮
饱和醛和酮
的分类 烃基是否饱和 不饱和醛和酮
一元醛和酮
羰基个数 二元醛和酮
多元醛和酮
第11章--醛酮部分习题参考答案
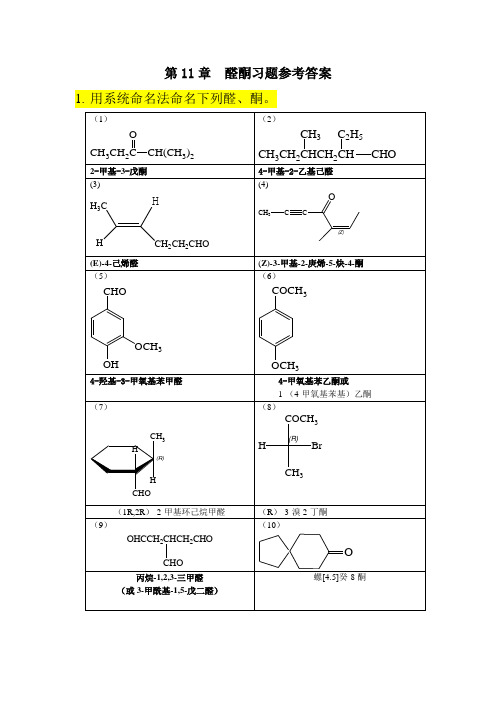
第11章醛酮习题参考答案1.用系统命名法命名下列醛、酮。
2.比较下列羰基化合物与HCN加成时的平衡常数K值大小。
答:(1)①Ph2CO②PhCO CH3③Cl3CCH O③>②>①(2)①ClCH2CHO②PhCH O③CH3CH O①>③>②3.将下列各组化合物按羰基活性排序。
(1)①CH3CH2CH O②PhCHO③Cl3CCHO答:③>①>②(2)①O②O③O④OCF3答:④>③>②>①(3)①O②O③O答: ③>②>①4.在下列化合物中,将活性亚甲基的酸性由强到弱排列。
(1)O 2NCH 2NO 2 (2) C 6H 5COCH 2COCH 3 (3) CH 3COCH 2COCH 3 (4) C 6H 5COCH 2COCF 3答: (1)>(4)>(2)>(3)5.下列羰基化合物都存在酮-烯醇式互变异构体,请按烯醇式含量大小排列。
(1)CH 3CCH 2CH 3O(2) CH 3CCH 2CCH 3OO(3) CH 32CO 2C 2H 5O(4)CH 3CCHCCH 3OO3 (5)CH 3CCHCOOC 2H 5O3答: (4)>(5)>(2)>(3)>(1)6.完成下列反应式(对于有两种产物的请标明主、次产物)。
答:(1)CHO+H 2NC N(2) H CCH 2OHOCH 2CCH+2CCH 2OH(4)NH 2OHO+NOH(5)OHCN/OH-H 2O/H +OH CNOH COOH(6)OH 2OH 2OOHPhOCH 3(7)O2PhPhPh OOPh C 2H 5(8)OCH 3+O(9)OOEtO +CHOOO(10)CH 3CCH 2BrOHOCH 2CH 2OHO O CH 3CH 2Br(11) CH 3O+H 2Pd/COCH 3(12)H 3CCH 3CH 3O4(CH 3)2CHOHH 3O+3CH(13)H 3O +(14)OPhC Ph PhC CH 3CH 3(15)O+Br 2H 2O,HOAcOBr(16)(17) PhCHO + HCHOOH -PhCH 2OH + HCOO -OCH 3CO 3HOO(18)CH 3CO 2Et 40℃7.鉴别下列化合物。
大学有机化学第11章__醛和酮

O C CH3
苯乙酮
(乙酰苯)
共九十一页
2)系统(xìtǒng)命名 法
O
5
CH3
CH3CH2-C-CH2-CH-CH2CH3
CH3-CH-CH2CH2CHO
HO-CH-CH3
6
4-甲基戊醛
5-乙基-6-羟基 3-庚酮
- (qiǎngjī)
共九十一页
C H 3
C H O
C H 2 C H 2 C H C H O O H C C H 2 C H C H 2 C H O
共九十一页
加成-消除(xiāochú)历程
R’
R—C=O + H2N—G
H+
R’ R-C — N—G
H+ -H2O
R’ R-C=N—G
OH H
(N-取代(qǔdài)亚胺)
这种加成-消除实际上可以看成由分子间脱去一分子水:
R’
R—C=O + H2 N—G
R’ R-C=N—G + H2O
共九十一页
加成-缩合产物(chǎnwù)的结构及名称:
加成-缩合产物的结构(jiégòu)及名称:
R’ R—C=O +
R’
H2N—R H2N—OH
R—C = N-R Schiff base R’
R—C = N-OH 肟(oxime)
H2N—NH2 H2N—NH-
O
R’
R—C=N-NH2 腙(hydrazone) R’
R-C=N-NH-C6H5 苯腙
H2N—NH-C-NH2
R’
R-C=N-NH-CO-NH2 缩氨脲
共九十一页
6) 与格氏试剂加成
有机化学第11章 醛和酮

O H3C C CH3
NaCN H2S O4
CH3 CH2=C-COOCH3
(CH3)2CCN OH
H2O
CH3 CH2=C-CN
CH3OH
CH3
H
CH2=C-COOCH3
α-甲基丙烯酸甲酯
2、与格氏试剂的加成反应
δ C
δ O
+ δR δMgX
无水乙醚
OMgX H2O C
R C OH + HOMgX
R
C H (R )
O
+ CH3-CH-CH3 ( i - Pr -O-)3Al
R CH OH
OH
H (R )
+ CH3-C-CH3 O
可逆反应,正反应称为麦尔外因-庞多夫-维尔莱还原反应, 其逆反应称为奥本奥尔氧化反应。 反应的专一性高,只使羰基与醇羟基互变而不影响其它基团, 故为一级醇、二级醇与醛酮对应转变的重要方法。
4-甲基-3-乙基己醛
2-甲基-3-戊酮
2-苯丙醛
例如:
CH3-C=CHCH 2CH2-CH-CH 2CHO
CH3
CH3
3,7 二甲基 6 辛烯醛
H3C O
3 甲基环戊酮
O
O
O
C-CH 2CH3
C-CH 3
2 环己烯酮
1 环己基 1 丙酮
1 苯基 1 乙酮
多元醛酮:称某二醛或酮
当酮羰基和醛羰基共存时,酮羰基称羰基、酰基或氧代;
醛的异构现象是碳链异构。 酮的异构现象是碳链异构和羰基的位置异构。
三、醛酮的命名
1、IUPAC命名法
选择含羰基的最长链为主链;从近羰基的一端开始编号, 醛基总在链端;取代基位次和名称写于母体名称之前。
11 醛和酮问题参考答案
11 醛和酮问题参考答案问题 1问题 2格氏试剂可以和二氧化碳反应制备羧酸。
问题 3这是一个类似卡尼扎罗反应(Cannizzaro)的反应机理,因为是两分子苯甲醛,会得到一分子苯甲醇,一分子二苯甲酮。
问题 4甲醛、乙醛、丙酮三个化合物,由于甲基和羰基的超共轭效应,化合物的稳定依次增加。
甲醛、乙醛、丙酮和两分子水反应后得到偕二醇,相应的羰基碳依次转化为仲碳,叔碳和季碳,因而产物的空间位阻依次增加,稳定性依次降低。
因而甲醛、乙醛、丙酮反应的转化率依次降低。
问题 5三氯甲基是一个吸电子基团,增加了羰基的亲核性,导致羰基容易和水发生亲核加成反应。
问题 6亚胺可能存在如图所示的顺反异构体,其中反式异构体比较稳定。
问题7酮的亲核性比醛弱,此外酮的空间位阻比醛大;因而显色反应的时候要比醛慢。
问题8该反应是一个可逆反应,酸会和硫酸氢根反应,促使平衡相底物方向移动;碱也会和硫酸氢根反应,促使平衡向底物方向移动。
问题9汞遇硫会形成不溶的硫化汞,从而促使反应向生成酮的方向移动。
问题10问题 11问题 12一缩乙二醇能够将水合肼和酮溶解到一相中,增加两者的碰撞机会,加快反应的进行。
同时一缩乙二醇的沸点也比较高,反应可以在高温下进行。
问题 13乙醛和三分子甲醛发生羟醛缩合,得到如图所示化合物a, a 进一步发生卡尼扎罗反应(Cannizzaro)得到季戊四醇。
OH CH 2O H H CH 2O H O H 2-++CH 3H 2O H CH 3CH CH 2CHO O C C -CH 3CH CH 2CHO O CH 3CH CH 2CHO OH OH HOH ++-。
醛酮

RC CH
末端炔
H2O Hg++
O R C CH3
甲基酮
HC CH
RX
RCCH
H2O Hg++
O R C CH3
MC CH (M = Na, MgX 等)
(1) O R C R'
(2) H2O
RC CR
H2O Hg++
OH R C C CH
R'
H2O Hg++
O R C CH2R
OH O R C C CH3
O RCH
2 R'OH
2 R'OH H+
2019/8/18
No Reaction
R'OH 为弱亲核试剂
OH RCH
Organic Chemistry
OR'
RCH
缩醛
OR'
16
第 十一章 醛 和 酮
2. 醛酮羰基上的亲核加成反应(1)
一些常见的与羰基加成的亲核试剂
负离子型
Nu
分子型
NuH
亲核试剂
Organic Chemistry
3
第 十一章 醛 和 酮
醛酮的命名
O CHO
O
H3C
巴豆醛 反-2-丁烯醛 (E)-but-2-enal
甲基乙基甲酮 丁酮
butanone
1-环己基-2-丁酮 1-cyclohexylbutan-2-one
O CHO
3-氧代(正)戊醛 3-oxopentanal
R1
C R2
CH2
KMnO4
R1
C O + CO2 R2
第十一章酸和酮
二、与氨衍生物的反应
氨的衍生物羟胺(N2NOH)、肼(H2NNH2)、苯肼
(H2NNHC6H5)、氨基脲
等分子中氮原子上
有孤对电子。它们可作为亲核试剂与醛、酮发生加 成,用通式表示如下:
由于反应加成物本身不稳定,容易脱水而生成 含C=N双键的化合物:
羟氨、肼等碱性试剂常常是将它们制成盐酸盐的 形式保存,以防止氧化。反应时用弱碱 (醋酸钠)将 盐分解,把亲核性较强的碱游离出来,然后与醛、酮 作用。
不饱和醛、酮的命名是从靠近羰基一端给主链编 号,要注意名称的正确写法。
羰基在环内的脂环酮,称为环某酮;如羰基在环 外,则将环作为取代基。例如:
“carbaldehyde”是以甲醛为母体命名的后缀。 命名含有芳基的醛、酮,总是把芳基看成取代
基。例如:
酮还有一种衍生物命名法,把酮看成是“甲酮” 的衍生物,在“甲酮”前边加上两个烃基的名称, “甲”字一般可省略。例如:
2. α商代及卤仿反应 醛、酮可以在α碳上进行卤代,酸、碱对反应 均有催化作用。 (1)酸催化下的卤代 醛、酮在酸催化下进行氯代、溴代、碘代,可 以得到一卤代物,例如:
(2)碱催化卤代反应 醛、酮的碱催化卤代反应机理是拉普沃斯(A. Lapworth) 1904年在研究丙酮溴代反应动力学的基 础上提出来的。动力学研究指出,丙酮溴代反应速 度取决于丙酮和碱的浓度,而与溴的浓度无关。
“ketone”是在这种英文命名法中的母体名称,也 是酮的类名。醛的类名为“aldehyde”。
11.2 醛、酮的物理性质 一、 沸点
醛、酮分子间不能形成氢键,沸点比相应醇的 低得多,但比同碳数烃、醚的要髙。在室温下,除 甲醛外,其他醛、酮都为液体或固体。 二、 溶解性
由于醛、酮的羰基氧原子能与水分子中的氢原 子形成氢键,所以低级醛、酮在水中有一定的溶解 度,例如,甲醛、乙醛、丙醛和丙酮可与水混溶。 其他醛、酮的水溶性随相对分子质量的增大而减小。 高级醛、酮微溶或不溶于水,而溶于一般的有机溶 剂。
有机化学高鸿宾第四版答案第十一章_醛酮醌
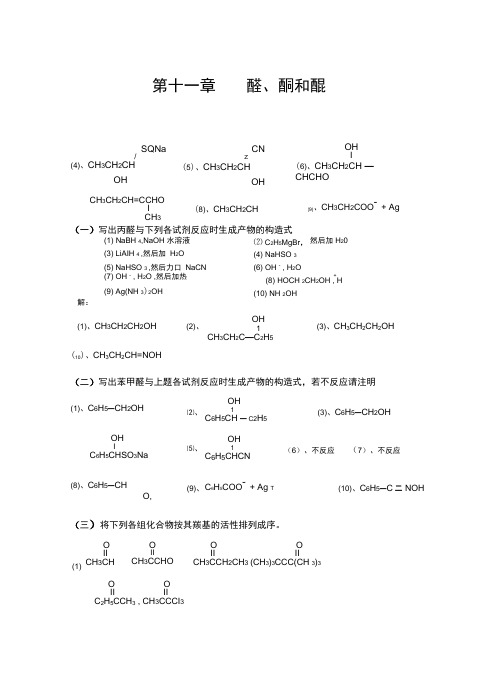
(1)第十一章 醛、酮和醌(一)写出丙醛与下列各试剂反应时生成产物的构造式(1) NaBH 4,NaOH 水溶液 ⑵ C 2H 5MgBr , 然后加H 20(3) LiAIH 4 ,然后加 H 2O (4) NaHSO 3(5) NaHSO 3 ,然后力口 NaCN (6) OH - , H 2O(7) OH - , H 2O ,然后加热 +(8) HOCH 2CH 2OH , H(9) Ag(NH 3)2OH(10) NH 2OH解:(1)、CH 3CH 2CH 2OH(2)、OH1CH 3CH 2C —C 2H 5(3)、CH 3CH 2CH 2OH(10)、CH 3CH 2CH=NOH(二)写出苯甲醛与上题各试剂反应时生成产物的构造式,若不反应请注明SQNa/(4)、CH 3CH 2CHOHCNz(5)、CH 3CH 2CHOHOHI(6)、CH 3CH 2CH —CHCHOCH 3CH 2CH=CCHOI CH 3(8)、CH 3CH 2CH(9)、CH 3CH 2COO -+ Ag(1)、C 6H 5—CH 2OHOHIC 6H 5CHSO 3Na(8)、C 6H 5—CHO,⑵、OH1(3)、C 6H 5—CH 2OHC 6H 5CH — C2H 5OH⑸、1C 6H 5CHCN (6)、不反应(7)、不反应(9)、C 6H 5COO -+ Ag T(10)、C 6H 5—C 二NOH(三)将下列各组化合物按其羰基的活性排列成序。
O II CH 3CH O IICH 3CCHOO OII IICH 3CCH 2CH 3 (CH 3)3CCC(CH 3)3O O II II C 2H 5CCH 3 , CH 3CCCI 3(四)怎样区别下列各组化合物?O解:⑴ CH 3CCHO • CH 3CHO .OOIl、IICH 3CCH 2CH 3(CH 3)3CCC(CH 3)3O(2)CH 3CCCI 3O IIC 2H 5CCH 3(1) 环己烯,环己酮,环己烯(2) 2-己醇,3-己醇,环己酮 CH 2OH解:f 析出白色结晶NaHSO 3 (饱和)、夕----------- ► < X \f 褪色B 「2/CCl4_不褪色f CHI 3 (黄色结晶)CH 3CH(CH 2)3CH 312+NaOHOH2,4-二硝基苯肼'xCH 3CH 2CH(CH 2)2CH 32,4-二硝基苯腙(黄色结晶)p-CH 3C 6H 4CHO r C 6H 5CH 2CHO C 6H 5COCH 3 P-CH 3C 6H 4OH C 6H 5CH 2OHFehli ngAg 镜k Ag(NH 3)2NO 3「x ,xI CU2O (砖红)12+NaOH 7---- < X](黄)FeCl 3|显色--------- *X⑶CH 3CH 2CH0⑴0H “0H(五) 化合物(A)的分子式C 5H 120,有旋光性,当它有碱性 KMnO 4剧烈氧化时变成 没有旋光性的C 5H IO O(B)。
第十一章醛和酮

第十一章醛和酮教学目的:能正确命名醛、酮,掌握羰基亲核加成反应的历程和影响反应速度的因素,了解其在分离、鉴别、有机合成中的应用。
掌握醛、酮的主要化学性质及其在分离、鉴别、有机合成中的应用。
教学重点:羰基亲核加成反应,醛、酮的化学性质教学难点:羰基亲核加成反应历程。
第一节醛、酮的分类,同分异构和命名一、分类根据烃基的不同可以分为脂肪醛、酮和芳香醛、酮。
脂肪醛CH3CH2CHO 脂肪酮CH3COCH3脂环醛CHO脂环酮O=芳香醛CHO芳香酮COCH3根据烃基是否含有重键又可以分为饱和醛、酮和不饱和醛、酮。
不饱和醛CH3CH=CHCHO不饱和酮CH3CH=CHCOCH3根据羰基的个数可以分为一元醛、酮和多元醛、酮。
二元醛CH2CHOCH2CHO二元酮CH3CH2COCH2COCH3二、同分异构现象醛的同分异构---碳链异构引起。
酮的同分异构---碳链异构、碳基位置异构。
同碳数饱和一元醛酮,分子式CnH 2n O ,互为同分异构:三、命名1. 系统命名法:(1)选择含羰基最长碳链作主链,称为某醛或某酮;(2)由于醛基是一价原子团,必在链端,命名时不必用数字标明其位置。
酮基的位置则需用数字标明,写在“某酮”之前,并用数字标明侧链所在的位置及个数,写在母体名称之前。
例如:2- 甲基丙醛 2- 苯基丙醛3-甲基-6-庚炔醛C 6H 5CHCHOCH 37HCCCH 2CH 2CHCH 2CHOCH 3654321CH 3CHCHOCH 3CH 3COCH 3丙酮CH 3COCH 2CH 3丁酮CH 3CO(CH 2)CH 32-己酮CH 3COCH 2COCH 2CH 32,4-己二酮COCH 2CH 31-苯-1-乙酮(苯乙酮)1-环己基-1-丙酮COCH 32. 普通命名法醛的命名与醇的习惯命名法相似,称某醛;脂肪酮则按酮基所连接的两个烃基而称为某(基)某(基)酮。
例如:CH 3CHO 乙醛 CH 3CH (CH 3)CHO 异丁醛甲基乙基酮甲基苯基酮(1-苯基-1-乙酮)CH 3C OCH 3C 2H 5C O另外,醛、酮命名时习惯上还采用希腊字母α、β、γ等,α碳指与醛基或酮基直接相连的碳原子。
11第十一章 醛和酮-自测题

7. 化合物:A. HCHO、B. CH3CHO、C. CH3COCH3、D. C6H5COC6H5相对稳定性次序为 (C ) A. A>B>C>D B. A>C>D>B C. D>C>B>A D. D>A>B>C
8. 下列化合物在IR谱中于3200~3600cm-1之间有强吸收 峰的是 ( A ) A. 丁醇 B. 丙烯 C. 丁二烯 D. 丙酮
14. 下列哪个反应能增长碳链? ( B ) A. 碘仿反应 B. 羟醛缩合反应 C. 康尼查罗反应 D. 银镜反应
15. 下列物质中不能发生碘仿反应的为 ( B )
16. 下列化合物中不发生碘仿反应的是 ( D )
17. 下列两个环酮与HCN加成的平衡反应中,平衡常数较大 的是 B ( )
18. 下列含氧化合物中不被稀酸水解的是 ( D )
4. 下列物质不能发生碘仿反应的是 ( D ) A. 乙醇 B. 乙醛 C. 异丙醇 D. 丙醇
5. 下列能发生碘仿反应的化合物是 ( A ) A. 异丙醇 B. 戊醛 C. 3-戊酮 D. 2-苯基乙醇
6. 下列能进行Cannizzaro(康尼查罗)反应的化合物是 (C ) A. 丙醛 B. 乙醛 C. 甲醛 D. 丙酮.
11. 缩醛与缩酮在( B )条件下是稳定的 A. 酸性 B. 碱性
12. 能够将羰基还原为亚甲基的试剂为 ( B ) A. Al(i-PrO)3 , i-PrOH, B. H2NNH2, NaOH, (HOCH2CH2)2O,△, C. ⑴ HSCH2CH2SH, ⑵ H2/Ni, D. NaBH4, 13. 下列试剂对羰基无作用的有 ( A ) A. 酒石酸钾钠 PhNH2 B. Zn-Hg/HCl C. R2CuLi D.
1. 下列化合物的沸点最高的是 ( A )
有机化学 第十一章 醛 和 酮

4.与醇的加成反应
R 无水HCl R OH C O + R''OH C H H OR'' ( R' ) ( R' ) 半缩醛(酮 ) 不稳定 一般不能分离出来 R''OH 干 HCl R H ( R' ) C OR'' OR'' + H2O ( 缩醛 酮) ,双醚结构。 对碱、氧化剂、还原剂稳定, 可分离出来。 酸性条件下易水解
R H (R')
CH OH
OH
CH3CH2CH2CH2CH2OH (C=C, C=O 均被还原 )
如要保留双键而只还原羰基,则应选用金属氢化物为 还原剂。
23
2、金属氢化物为还原剂还原 1)LiAlH4还原
CH3CH=CHCH2CHO ① LiAlH 4 干乙醚 ② H2O
CH3CH=CHCH2CH2OH ( 只还原 C=O )
C H δ C δ O R (H ) 酸和亲电试剂进攻富电子的氧 碱和亲核试剂进攻缺电子的碳 涉及醛的反应(氧化反应 ) α H 的反应 羟醛缩合反应 卤代反应
8
一、亲核加成反应
1.与氢氰酸的加成反应
C O + HCN α C OH CN 羟基睛
反应范围:醛、脂肪族甲基酮。ArCOR和ArCOAr难反应。αβγδ α-羟基腈是很有用的中间体,它可转变为多种化合物, 例如: CH 3 CH 3
C O 无水 NH2-NH2 加成,脱水 C N-NH2 KOH 或 C2H5ONa C 2H5OH 200 ℃ 加压 回流 50~100h CH2 + N2
4
1946年-黄鸣龙改进了这个方法。 改进:a 将无水肼改用为水合肼;碱用NaOH;用高沸 点的缩乙二醇为溶剂一起加热。加热完成后,先蒸去水和 过量的肼,再升温分解腙。
有机化学 11第11章_醛和酮
总目录
2. 卤代反应
(1)酸催化卤代,生成一卤代物。
O C CH3
O C CH2Br
+ Br2
CH3
CH3COOH 20℃
CH3
+
HBr
反应易停留在一取代上。
总目录
机理:
O CH3CCH3 + H∶B
+OH
CH3CCH2 H 慢
快
+O H
CH3CCH3 + ∶B
OH CH3 C CH2 + H∶B
总目录
3. 羟醛缩合反应
O 2 CH3C H
慢
稀 OH
CH3CH CHCHO
机理:
O CH3C H
+ -CH2C
O H
O CH3CHCH2CHO
H2O
OH CH3CHCH2CHO
- H2O
CH3CH CH CHO
总目录
交叉的羟醛缩合反应
CH3CH2CHO + CH3CHO 稀 OH ?
CH3CH CHCHO
如果没有保护,醛基也会被氧化!
总目录
5. 与氨及其衍生物的加成
(1)氨
H H C O OH H
+ NH2 H
H H
C
NH
(2)胺
C6H5C O H OH H
+ C6H5NH2
1°胺
C6H5
C N C6H5 H
H C C O
H
OH C NR2 C C
+ HNR2
2°胺
C
NR2
烯胺
烯胺是有机合成重要的中间体。
O
总目录
3. 与金属有机化合物反应
醛和酮

第十一章醛和酮课时:8课时教学目的要求:掌握醛酮与亲核试剂的加成反应及其历程,醛酮的氧化-还原反应,各类醛酮的鉴别,醛酮制法,α,β-不饱和醛酮的性质。
含羰基。
第一节醛、酮的分类,同分异构和命名一、分类烃基的类别:脂肪族醛、酮;芳香族醛、酮。
羰基的数目:一元醛、酮;二元醛、酮。
二、同分异构现象醛:碳链异构。
酮:碳链异构和羰基位置异构。
三、命名1 系统命名法选择含羰基的最长链。
编号从靠近羰基的一端开始。
CH3CHCHOCH3C6H5CHCHOCH3HC CCH2CH2CHCH2CHOCH32-甲丙醛2-苯丙醛3-甲基-6-庚炔醛CH3CO(CH2)3CH3COCH3COCH2CH32-己酮1-苯-1-乙酮1-环己基-1-丙酮碳原子的位置有时也用希腊字母表示:2酮的取代基命名法CH3CCH2CH3OCOCH3甲基乙基酮甲基苯基酮CHOOH CHOCHO3-羟基苯甲醛1,2-萘二甲醛111CHO2COOH CHOO4-甲酰苯基乙酸2,3-环氧苯甲醛COCH2CH2CH3CH2COCH31-( -萘基)-1-丁酮1-苯基-2-丙酮萘基丙基酮苄基甲基酮第二节醛、酮的结构、物理性质和光谱性质一、醛和酮的结构羰基碳原子sp2杂化。
氧原子上带部分负电荷,碳原子上带部分正电荷。
羰基是极化的,分子有偶极矩。
二、物理性质沸点比相应的烷烃和醚高(极化度大),低于相应的醇(不能形成分子间氢键)。
低级的醛、酮可溶于水(与水形成氢键),中级醛(九到十个碳)具果香味液体,用于香料工业,低级酮是液体,具有令人愉快的气味。
三、光谱性质红外光谱:碳氧双键的伸缩振动,醛在1730cm-1, 酮在1715cm-1, 形成共轭体系时,吸收的波数减小。
醛在2750cm-1处有醛氢与羰基碳之间的碳氢伸缩振动峰。
核磁共振谱:醛氢的化学位移为9-10, 与羰基相连的甲基或亚甲基的化学位移在2-2.5,紫外光谱:非共轭醛、酮在200 nm以上无强烈吸收,共轭的醛、酮则有强烈吸收。
Ch.11 醛和酮

第11章醛和酮羰基化合物:醛、酮、羧酸、羧酸衍生物……第一节分类同分异构命名一、分类脂肪族醛脂环族酮(包括环内酮)二、同分异现象分子式相同的饱和一元脂肪醛与酮互为官能团异构体。
三、命名1.普通命名法S 命名法醛的命名较简单,选好主链后,—CHO C的编号总是1,因此名称中—CHO的位次无须标示。
酮分子中的—CO—必须标示出来。
醛、酮分子主链 C 原子的位置可用1、2、3或希腊字母标示。
例见教材P.312第二节醛、酮的结构、物理性质和光谱性质一、结构羰基的双键是极化的,这导致的物理结果是——醛、酮分子通常具有较大的偶极矩,它们的偶极矩比醚的大。
有关数据见教材P.314 表–1。
少数低级醛、酮能与水形成氢键,但大多数不能与水形成氢键。
资料各类有机物的极性顺序大致为:酸和碱>羟基化合物>胺>酮>醛>酯>醚>不饱和烃>饱和烃二、物理性质醛、酮的b.p比分子量相当的醇低,但比醚、烯、烷高。
醛、酮的物态常温下,只有甲醛是气体,其余均为液、固体。
醛、酮的溶解度低级脂肪族醛、酮易溶于水,随C 数的增加,溶解度渐小。
醛、酮的气味常具有特征性。
脂肪醛的气味通常令人不愉快并使人感到窒息,这个系列头几个化合物尤其如此。
甲醛:气味辛辣;乙醛:气味辛辣;丙醛:刺激性气味。
但是,酮和芳香醛却具有令人愉快的气味:丙酮:微香气味;苯甲醛:苦杏仁气味,可作调味香料。
三、光谱性质该区域很少出现其它吸收峰,故羰基的伸缩振动峰最为有用,是解析红外光谱图时要首先查找的谱带之一。
一般情况下,醛的吸收频率稍高于酮,但这一差别不能用于区别醛与酮。
不过,大多数醛在 2750 cm-1附近会出现几个吸收谱带,这是–CHO的νC—H引起的,一般可看到二个中等强度的峰,有时只见到一个峰,这一特征可区别醛与酮。
共轭的不饱和醛、酮:νC=O峰向低波数区域位移(即红移),共轭链越长,红移越甚。
环酮:随环张力的增加(环越小),νC=O峰向高波数区域位移(即蓝移)。
第十一章 醛和酮

Chapter 11 Aldehyde and Ketone
C
δ
+
O
Company Logo
δ
Contents
1
醛和酮的分类和命名★
醛和酮的物理性质◎
2
3 4
2
醛和酮的化学性质★
醛和酮的制备◎
Company Logo
第一节 醛和酮的分类和命名 O 醛和酮均含有羰基的化合物 C
羰基碳原子上同时连有两个烃基的叫酮 羰基碳原子上至少连有一个氢原子的叫醛。
H3C CH CHO
3
2
1
CHO
2-苯基丙醛
12
苯甲醛
Company Logo
第一节 醛和酮的分类和命名 用系统命名法命名下列化合物
O
O
4-戊烯-2-酮
13
1-苯基丙酮
Company Logo
第一节 醛和酮的分类和命名
CHO OH
2-羟基苯甲醛
(水杨醛)★
O
8-甲基二环[3.2.1]-6-辛烯-3-酮
O R C H
羰基 carbonyl
R
O C R'
醛(aldehyde)
3
酮(Ketone)
Company Logo
第一节 醛和酮的分类和命名
一、醛、酮的命名 1、普通命名法 醛:脂肪醛按分子中含碳数称某醛。
HCHO
甲醛 丙醛
CH3CH2CHO
4
Company Logo
第一节 醛和酮的分类和命名
42
Company Logo
第三节 醛和酮的化学性质
CH3 CH3 C =CH(CH2)2CHCH2CHO CH3 HOOC(CH2)2CHCH2CHO CH3
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十一章 醛和酮
(3) 醛酮与炔化物的加成
O C M = Na, K, MgX等 M C C R(H) H2O OH C C C R(H)
a-炔基醇
应用
cis-烯基醇
trans-烯基醇
a-羟基酮
Organic Chemistry
a, b-不饱和酮
© 2014 11 07
第十一章 醛和酮
(4) 醛酮与 H2O 加成
(较稳定的共振式)
烯醇式
Organic Chemistry
© 2014 11 07
第十一章 醛和酮
羰基a位的反应概况
O B: CHR H
O C R'
E CHR R'
O C CHR E
R'
C
有亲核性
E
D O
OD
X O
X
R O CHR X R' C
X
C O CHR R R' C
第十一章 醛和酮
碳原子的位置也可用希腊字母表示:
δ γ β α O C C C C C H CH 3CH=CHCH 2CHO β 丁烯醛
11.1.3 醛、酮的结构
醛分子中,羰基至少要与一个氢原子直接相连,故醛基一定在链端。
酮分子中的羰基与两个烃基直接相连,故羰基必然位于碳链中间。
Organic Chemistry
C
C
脂肪族醛、酮
Organic Chemistry
芳香族醛、酮
a, b-不饱和醛、酮
© 2014 11 07
第十一章 醛和酮
11.1.2 醛酮的命名
CHO H3C O O
巴豆醛 反-2-丁烯醛
甲基乙基甲酮 丁 酮 1-环己基-2-丁酮
水杨醛
苯甲醛
Organic Chemistry
2-羟基苯甲醛
© 2014 11 07
π
C
O
C
O
δ C
δ O
电负性 C < O
Organic Chemistry
π 电子云偏向氧原子
极性双键
© 2014 11 07
第十一章 醛和酮
§11.2
醛、酮的性质
11.2.1物理性质
常温下,除甲醛是气体外,,十二个碳原子以下的醛酮是
液体,高级的醛酮和芳香酮多为固体。
分子一般具有较大的极性,因此沸点比分子量相近的烃和 醚要高,但比相应的醇要低。 醛酮的分子可以与水形成氢键,低级的醛酮(四碳以下的 脂肪醛酮)易溶于水,五碳以上的醛酮,微溶或不溶于水中, 而易溶于有机溶剂中。
Beckmann 重排机理
反式重排
Organic Chemistry
© 2014 11 07
第十一章 醛和酮
迁移基团的构型保持不变
构型不变
t-Bu H H Et H3C C N OH H3C O C NH t-Bu Et H
Organic Chemistry
© 2014 11 07
第十一章 醛和酮
Organic Chemistry
© 2014 11 07
第十一章 醛和酮
醛酮与金属试剂加成的立体化学 —— Cram规则
Ph (1) CH3MgBr CHO (2) H2O H Et CH3 Ph OH H + H Et CH3 Ph H OH
H Et
手性碳
2.5
非对映体
1
Cram的解释
S M
保护羰基
Organic Chemistry
© 2014 11 07
第十一章 醛和酮
缩醛(酮)形成机理
半缩醛(酮)
逆向为缩醛 (酮)水解机理
缩醛(酮)
Organic Chemistry
© 2014 11 07
第十一章 醛和酮
缩醛(酮)在合成上的应用 ——用于保护羰基
O O C (CH2)2 Br H3C (CH2)2
© 2014 11 07
第十一章 醛和酮
手性醛酮的消旋化(碱性条件)
R2 O B: / HB R R2 O C R
or
R1
C* C H 旋光性
R1
C H
OH ,
RO
消旋化
消旋机理
H B R2 R1 C* H B:
Organic Chemistry
(从平面上方成键)
R2 O C R
第十一章 醛和酮
第十一章
醛 和 酮
Organic Chemistry
© 2014 11 07
第十一章 醛和酮
§11.1 醛酮的类型、命名和结构
11.1.1类型
醛和酮
羰基
O R C H
R O C R'
醛
醛、酮的分类
O R C O R C R' Ar H Ar O C O C R H
酮
O
b a
C H(R)
L
Organic Chemistry
主要产物
© 2014 11 07
第十一章 醛和酮
LiAlH4和NaBH4还原羰基的立体选择性
位阻较小
位阻较大 位阻较大
主要产物
位阻较小
Organic Chemistry
主要产物
© 2014 11 07
第十一章 醛和酮
2、 醛酮 a - H 反应
碳负离子
烯醇负离子
(9) 醛酮与LiAlH4 或 NaBH4 加成 (还原反应)
LiAlH4 R'CHO or NaBH4 O R' C R LiAlH4 or NaBH4 H2O R' OH CH R H2O R CH2 OH
1o醇
2o醇
机理
Al O C Al H O C H H2O OH C H
Organic Chemistry
Organic Chemistry
© 2014 11 07
第十一章 醛和酮
11.2.2 化学性质
δ C δ O R (H ) 酸和亲电试剂进攻富电子的氧 碱和亲核试剂进攻缺电子的碳 涉及醛的反应(氧化反应 ) α H 的反应 羟醛缩合反应 卤代反应
C H
亲核加成 反应
• 因π键的极化,使得 O上带部分负电荷, C上带部分正电荷, O可以形成比较稳定的 O-,它较带正电荷的C要稳定得多,因此 反应中心是羰基中C+; • 羰基易与亲核试剂进行加成反应(亲核加成反应)。 • • 此外,受羰基的影响,α-H较活泼,而发生一系列反应。 亲核加成反应和α-H的反应是醛、酮的两类主要化学性质。
© 2014 11 07
Organic Chemistry
第十一章 醛和酮
1、 醛酮羰基上的亲核加成反应
一些常见的与羰基加成的亲核试剂
亲核试剂
亲核能力 强
负离子型
Nu
较强
分子型
NuH
不强
Organic Chemistry
© 2014 11 07
第十一章 醛和酮
(1) 醛酮与与HCN 的加成
a-羟基腈
例
H3C
OH C CH3 CH3
C
分析
分子内羰基将参与 反应,应先保护。
OH (CH2)2 C CH3 CH3 H3C O C (CH2)2 MgBr + H3C O C CH3
O C H3C
Organic Chemistry
© 2014 11 07
第十一章 醛和酮
合成:
O C H3C OH (CH2)2 Br H+ OH O C H3C O O C H3C (CH2)2 MgBr O C H3C (CH2)2 (2) H2O R O (1) H3C C CH3 O C O (CH2)2 OH C CH3 H2O H
醇均能发生碘仿反应。 如 CH3CH2-OH,
酸催化卤代
O C H C X = Cl, Br, I X2 , H C X O C
一取代产物
© 2014 11 07
Organic Chemistry
第十一章 醛和酮
碱催化机理
R
O CH2
O R CHCl
O R CCl2
Organic Chemistry
O C
O
H + H2O
H2O H H2O H H2O CH3
+
OH C OH
H2C(OH)2
难以分离,易失水!
偕二醇
例
H
C O
100%
H3C
C O
CH3CH(OH)2
~ 58%
H3C
C
(CH3)2C(OH)2
0%
OH Cl3C H2O Cl3C 若羰基上连有吸电子基团,可稳定存在: C C O H H OH
两个基团均 可被还原
O
只还原酮羰基
OMe
© 2014 11 07
Organic Chemistry
第十一章 醛和酮
(10) 羰基亲核加成立体化学
羰基:平面构型,试剂可进攻平面上方或下方。 试剂进攻两个面得相同产物。
试剂进攻两个面的机会相同,得到一对对映体。
试剂进攻两个面的机会不等同,得到不等量的产 物。
O R C R HS SH S C R R S H2 Raney Ni H C R R
© 2014 11 07
H
干HCl
Organic Chemistry
第十一章 醛和酮
(7) 与NaHSO3 加成
O HO S O HO O S O
NaHSO3的亲核性
OH
