第十七章_胺
第十七章____胺

第十七章 胺1. 完成下列反应,写出主要产物。
(1) CH 323OOCH 2N 2(2) CH 322H 5OOCH 2N 2(3)(4)3CH 2N 2HOH 2CCOOH(5)22HOCH 2OH(6)22(CH 3)2CHCCH 3O(7) 22OCH 3H 3CH 2C(8) 22CH 3CH 2CH 2CH 2CH 3(9) H 3COC HCH 2+CH 2I 2( Zn/Cu)(10) CH 2I 2( Zn/Cu)H 2C3O+(11) +(CH 3)2CN 2(12) H 3CHC CHCH 3+PhCHN 22. 下列三个反应均发生环扩大反应,根据所给反应物及试剂,写出反应中间体及环扩大的产物,并用箭头表明其反应过程。
(1)NMeHCH 3Li 22(2)H HCCl 2(3)3. 从指定原料出发,用必要的试剂合成。
(1) 从戊二酸合成己二酸二乙酯(2) 从2-甲基-2-苯基丁酸合成3-甲基-3-苯基戊酸(3) 从O 2NCOOH合成O 2NCH 2CONHCH 3(4) 从COOH合成CH 2COOC 2H 54.说明如何提纯下列化合物(指主要成分)。
(1) 三乙胺含少量乙胺及二乙胺 (2) 二乙胺含少量乙胺及三乙胺 (3) 乙胺含少量二乙胺及三乙胺5.用化学方法鉴别下列化合物。
(1) CH 3CH 2NH 2,CH 32O(2)NH 2NH(3) NH 3ClClNH 2(4) H 2CCHCH 2NH 2 CH 3CH 2CH 2NH 2(5) H 3CSO 2NHCH 3H 3CNH 3HSO 4-(6) (CH 3CH 2CH 2)4N +Cl - (CH 3CH 2CH 2)3NH +Cl -6. 按下列合成路线,写出化合物的构造式。
(1)(CH 3)3N(1)CH 3COCH 2Cl(2) H 2Pt(3)CH 3COClA (C 8H 18ClNO 2)(2)(CH 3)3NCH 3CHCH 2ClOH(1)ClCClO(2)NH 3(1mol)(3)B (C 7H 17ClN 2O 2)(3)(1)(3)(CH 3CH 2)2NHClCH 2CH 2OHZn (C)(C 15H 20N 2O 2)7. 将下列各组化合物按碱性从强到弱顺序编号。
第十七章胺1

CH3 C CH3 CH3
7、烯胺的生成及其反应
H C H C O + RNH2 H
H C H
H C H
C
NR
H2 C
C 亚胺
NR2
OH H
C H
H C H C O + R2NH
H
C OH
NR2
C 烯胺
NR2
生成烯胺的反应多用酸催化,二级胺常为:
O N H N H N H
烯胺的共振式有两种
R2N C C R2N C C 具有亲核性
NH 2
(CH3CO) 2O
NHCOCH 3
在乙酸中 NO 2 NH 2 NO 2
HNO 3
NHCOCH 3 NO 2 OH / H 2O
在乙酸酐中 (主要HNO 3
NH3HSO 4 2NaOH NO 2 H2O
+
H2C
CHCH2Cl
N CH2CH CH2
H3O
CH2CH CH2
+
O
N Cl
R
C
O C R
H3O
O CR
反应可看作是在醛酮的α-位的烃基化和酰基化,在合成上 有重要的应用。
O
例:试合成化合物
O + Br COOC2H5 C2H5ONa O
COOC2H5
O
COOC2H5
COOC2H5
有 机 化 学
第十七章
胺
一、分类、结构和命名
1、分类
氨 NH2R 伯胺
CH3 H3C C OH 叔丁醇(叔醇) CH3 H3C
NHR2 仲胺
NR3 叔胺
CH3 C NH2 叔丁胺(伯胺) CH3
第17章 胺(一)

O C N3
H2O
O C NH2
COOH Cl
+ NaN3
1) H2SO4 2) NaOH Cl
NH2
六. 布歇尔(Bucherer) 反应
OH
(NH4)2SO3 150 oC
NH2
压力NΒιβλιοθήκη 2(NH4)2SO3OH
七. 曼尼希(Mannich) 反应
具有α氢的酮与甲醛(或其他简单脂肪醛)及铵盐(伯、仲胺的盐)水
(与溶剂的性质,溶液浓度,温度等影响氢键缔合的 因素有关,可用D2O交换判定)
第三节. 胺的制法
一. 卤代烃氨解
一般在氨过量的情况下用于制备伯胺,伯胺是很好的亲核试 剂,可继续反应,生成仲胺和叔胺,因此往往得到混合物。
NH3 + R X RNH2 + NH4X RX R2NH + NH4X
RX 使用过量的氨, R3N + NH4X 可以得到伯胺为主的产物 控制条件,也可以得到某一胺为主的产物 RX R4N+X
已拆分出的对映体
二. 胺的命名
1. 以胺为官能团,加上与氮原子相连的烃基的名称和数目。(amine)
CH3
H3C N CH2CH3
CH3NH2
NH2
N CH2CH3
甲胺
苯胺
甲基乙基环丙胺
N-甲基-N-乙基苯胺
2. 结构复杂的胺,可以作为烃类的氨基衍生物来命名。(amino)
(CH3)2CHCH2CHCH3 NH2
4. 类似的反应: 酰氯与叠氮化钠作用及羧酸与叠氮酸反应均生成酰叠氮化合物。加热 后放出氮气生成胺类,前者叫克尔蒂斯重排,后者称施密特重排,这 是两个与霍夫曼重排类似的反应。
第十七章 胺

胺的光谱性质
红外光谱
N—H 伸缩带在3000-3500 cm-1之间
伯胺在这一区间有两个峰,一个是对称伸缩振动,一个
是非对称伸缩振动。
H
H
R
N H
R
N H
对称
非对称
17 - 19
红外光谱
伯胺有两个 N—H 伸缩峰, 仲胺有一个伸缩峰
RNH2
R2NH
17 - 20
1H-NMR谱
比较化学位移:
H3C
R +
•• – • • X • • ••
H
+ H3N
H + • •N H
R
17 - 36
H
1、氨或胺的烃基化
但实际上该法不实用,通常会得到伯胺、仲胺、 叔胺和季铵盐的混合物。
NH3
RX
RNH2
RX
R2NH RX
+ R4N
X
–
RX
R3N
17 - 37
2、脂肪伯胺的Gabriel合成法
只会生成伯胺,而没有其它胺类副产物 应用卤代烃的 SN2 反应形成 C—N 键 含氮的亲核试剂为 邻苯二甲酰亚胺钾 O – • •N • • O
示 例 O – • •N • • O O
• •N
K
+
+
C6H5CH2Cl DMF
CH2C6H5
(74%)
O
17 - 43
示 例 O NH +
C6H5CH2NH2 (97%) H2NNH2
NH
O O
• •N
CH2C6H5
O
17 - 44
3.含氮化合物的还原
几乎所有的含氮化合物都可以通过还原生成胺。 这些化合物可以是: 叠氮化合物 腈 硝基取代苯的衍生物
第十七章胺类 PPT

§17-4 胺得反应
一、烃基化 ( p391)
氨
RX + NH3 → RNH21°胺
RX + RNH2 → R2NH + HX R2N + H2X -
2°胺
RX + R2NH → R3N + HX
R3N + HX -
3°胺
RX + R3N → R4N + X -
CH2NH2 + 3CH3I CH3OH
H2O/OH-
R2NH
分层或沉淀
稀酸
溶解
稀碱
RNH2
R3N
三、 +HNO2(NaNO2/H+) (p394) 鉴别 1°,2°,3°胺
1、 1°胺
(1)RNH2
CH3CH2CH2NH2
NaNO2 HCl
CH3CH2CH2N
NCl
重氮盐(不稳定)
CH3CH2CH2 + Cl- + N2
CH3CH2CH2
与水分子形成氢键得能力: 1°>2°>3°
空间位阻:
3°> 2°>1°
➢ b、p与S/H2O:1°>2°>3° ➢b、p: 1°与2°胺高于相应得烃,低于相应得
醇。 3°胺与相应得烃相近。
三、波谱分析 1、IR
振动类型 伯 胺/cm-1 仲 胺/cm-1 叔 胺/cm-1
N—H
N—H (面内) N—H (面外)
3、结构与性质
➢氮原子得电负性小于氧原子,形成氢键得能力较弱。 ➢胺得化学性质在很大程度上与N原子一个sp3杂化轨 道上得一对孤电子对有关,同时也受N原子上所连烃基 得种类与数目得影响。
140pm
N H
第17章胺-精品文档
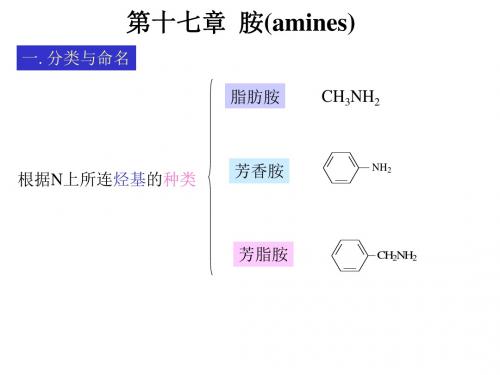
C H (C H 3 ) 2
C H (C H 3 ) 2
(2)化学还原
CH3 CH3 NO2 Fe E tO H , H C l h e at NH2 NH2
Sn、Fe/HCl
NO2
选择性还原试剂
硫化铵
硫氢化钠
硫化钠
还原剂计量: 二硝基化合物选择还原
p775
4. 腈及其它含氮化合物的还原
R C l + aC N N N i / H 2 R C H N H R C N 2 2 or L i A l H 4
O N N O
+ R N H + H O 2 2
O
氨基酸合成 p773
3. 硝基化合物还原
(1)催化氢化:污染少,逐步替代化学方法。中性条件下进行,
适于对含有对酸、碱敏感的官能团化合物进行还原
CH3 CH3 NO2 H 2, N i h e at , p re s s u re NH2
制备伯胺
Ni, Pd, Pt
5. 还原氨化——醛(酮)在氨存在下催化氢化生成 胺的反应(reductive amination)
RC O H (R') + NH 3 Ni/H 2 RC H NH 2 H (R')
NH RC H (R')
中间体
R
R ' C N R '' R '''
醛(酮)与伯胺的反应通过半缩胺 (亚胺)中间体发生,与仲胺的反应 则通过半缩胺(亚胺离子)
第十七章 胺(amines)
一. 分类与命名
脂肪胺 CH3NH2
根据N上所连烃基的种类
芳香胺
NH2
第十七部分胺Amine-精品文档

3.3.1 脂肪胺的亚硝化 仲胺
N a N O , H C l 2 ( C H ) N H ( C H ) N N O 3 2 3 2 H O 2
+ H O N O + H + H O N O 2 + ( C H ) N N O 3 2 + H O + N O 2 + ( C H ) N N O + H 3 2
熔点/沸点:71/284
114/306
148/322
邻位的熔沸点较低,是由于其形成了分子内氢键,而间对位形成分子 间氢键
2、偶极矩
C H C H N H 3 2 2 C H C H O H 3 2 N H 2
= 1.2D
= 1.7D
= 1.3D
说明苯胺中N孤对电子分散到了苯环中,形成了共轭体系 3、光谱 对称伸缩 IR: R-NH2 Ar-NH2 HNMR: N-CH3 2.2 3300---3200 3420—3300 N-CH2-R 2.4 不对称伸缩 3400—3300 3500--3390 N-CHRR 2.8
( C H ) N H ++ N O 3 2
H
伯胺
O H N a N O , H C l N 2 H O -2 2 C H C H C ( C H ) . C l 3 2 3 2 C H C H C ( C H ) C H C H C ( C H ) C H C H C ( C H ) 3 2 3 2 3 2 3 2 3 2 3 2 H O 2 + N H 2 N N
147.4 pm
N ( C H ) 3 2
乙胺
N-甲基苯胺
N-甲基-N-乙基异丁胺
N, N-二甲基苯胺
第十七章 胺

二甲基二苯基硝酸铵 硝酸二甲基二苯基铵
Dimethyldiphenyl ammonium nitrate
四乙基氢氧化铵 氢氧化四乙铵
Tetraethyl ammonium hydroxide
6
§2 Physical and Spectroscopic Properties
Physical Properties
R2NH
ArNH2
19
2 Alkylation of amines
RNH2 + RX R2NH
R3N R4NX
R4NX + AgOH R4NOH 季铵碱
PTC-Phase Transfer Catalysis
Hexane Hexane (n-Bu)4NCl
+ CHCl3
(n-Bu)4NCl OH-/H O 2
CH3 CH2C NH2 CH3
CH3 CH2C CONH2 CH3
CH3 CH2C CO2H CH3
PhCH2Br +
H H3C C2H5 CONH2 Br2/OHH3C C2H5 H NH2
(CH3)2CHCO2H
15
Related Reactions
Curtius Arrangement
O R C Cl (1) NaN3 (2) H2O O R C N3 RNH2
NH4X 卤化铵 R4NX 季铵盐
NH2 Aromatic amine
H N CH3
H2 CH3 C N CH3 Aliphatic amine
N
N H
Heterocyclic aromatic amine
N H
N H
Heterocyclic aliphatic amine
第十七章_胺

C H 2 H 3 CN C H 2 C HR O H
C H 3 H
( -消 除 )
C H 3 H 3 CN + C H 2 C HR
C H 3
2021/1/16
Hofmann消除的选择性 —— 主要生成取代基少的烯烃
'
H3CCH2 CH2 CH CH3
N(CH3)3 OH
H3CCH2 CH2 CH CH2 +
nh在乙酸中在乙酸酐中主要产物主要产物nh3磺化反应nh9601立体选择性很高第二节重氮化合物和偶氮化合物arnhcl重氮盐干燥时易爆炸与重氮盐稳定性有关的一些因素一芳香重氮盐重氮盐的反应还原反应1重氮盐的取代反应ararcnaroh离子性和自由基型反应1卤素或氰基取代经自由基机理
第十七章_胺
主要内容
( 两个峰,光、中) (强)
(宽、强)
二级胺 3300-3500
弱
(单峰)
2021/1/16
700-750 (弱)
NMR: —CH2—CH2—NH2
δ 1.1-1.7; 2.2-2.8;0.5-5ppm (与溶剂的性质,溶液浓度,温度有关,可影响H—键缔和)
MS:
R—NH2 —M+小 M+ 奇数个N ,M+奇数 Ar—NH2 M+大
CH3 C2H5 N CH2=CH—CH2 C6H5
CH3
N
C6H5
C2H5 CH2—CH=CH2
2021/1/16
2 、胺的物理性质
低级胺为气体或易挥发性液体; 高级胺为固体; 芳香胺为高沸点的液体或低熔点的固体; 胺具有特殊的气味; 胺能与水形成氢键; 一级胺和二级胺本身分子间也能形成氢键。
有机化学 第十七章 胺

邻苯二甲酰亚胺氮上的氢受到两个拉电子基团
影响呈现酸性(pKa8. 3),用K0H处理很容易生成相 应的钾盐。
该法除合成伯胺外,还用于合成α-氨基酸(参
阅第二十一章)。
三、硝基化合物还原 通过硝基化合物还原制备胺类是极为重要的方
法,因芳香硝基化合物很容易由芳烃硝化得到,因 此该法主要用于合成芳香伯胺。还原主要有催化氢 化和化学还原两种方式。
二、盖布瑞尔(Gabriel)合成 由卤代烃直接氨解制备伯胺时常会有仲、叔胺
生成,盖布瑞尔[S. Gabriel(1851—1924)出生于 德国,在Berlin大学获博士学位,而后在该校任化 学教授,主要在胺及氨基酸合成方面作出了贡献。] 提供了一个由卤代烃制备纯伯胺的好方法。邻苯二 甲酰亚胺的钾盐与卤代烃发生亲核取代反应,生成 N-取代亚胺后水解或肼解可获得高产率伯胺。
ቤተ መጻሕፍቲ ባይዱ
工业上由油脂水解得到高级脂肪酸(14.4节), 把该酸转化为酰胺,进而脱水生成腈,催化氢化可 得到长链伯胺(参看15. 3节)
2.酰胺还原
酰胺在醚中用LiAlH4处理可把羰基还原为亚甲 基获得较高产率的胺。氮上无取代基的酰胺可得到
伯胺,N-取代酰胺可得到仲、叔胺。
3.肟的还原 醛、酮与羟氨反应生成肟,肟是不饱和含氮化
17.4 胺的化学反应 由于胺中氮上具有孤对电子,使得它能在化学反
应中提供电子,体现了胺的一系列化学性质,如碱性、 亲核反应及氨基致活芳环上的亲电取代反应等。 一、碱性与成盐
1.碱性 按路易斯(Lewis)酸碱概念讲,反应中接受质子 或提供电子对的化合物为碱。由于胺中孤对电子的存 在,能从水中接受质子,故呈碱性。
七、曼尼希(Mannich)反应 具有α氢的酮与甲醛(或其他简单脂肪醛)及
17章-胺-1

O CH3 C
H H+ R2N C H O CH3 C
+
CH2CH2N(C2H5)2 + H2O
H 机理:R2NH + C H O CH3 C
OH2
R2N+
CH2
亚胺离子 CH2CH2 NR2 + H+
CH2=N+R2
含活泼氢的化合物:醛,酮,酸,酯 都可以。
NO2 Fe +HCl
NO2 NH2 + H2 Pt,C2H5OH O C OC2H5 O C OC2H5
NH2
※ 选择性还原: 选择性还原: 二硝基化合物:用硫化铵、硫氢化铵或硫化钠等,可得只还原 二硝基化合物:用硫化铵、硫氢化铵或硫化钠等, 一个硝基的硝基胺。 一个硝基的硝基胺。
第十七章 胺
Hale Waihona Puke 10Mannich反应 甲基酮+甲醛+ Mannich反应(α甲基酮+甲醛+伯、仲胺盐,生成β氨基酮)的一 反应( 仲胺盐,生成β氨基酮) 个重要用途是用于生物碱的合成。 颠茄酮又称托品酮的合 个重要用途是用于生物碱的合成。如,颠茄酮又称托品酮的合 两步mannich反应 收率40%左右 反应, 左右): 成(两步mannich反应,收率40%左右):
五、Hofmann降解反应 Hofmann降解反应
O RCNH2 NaOH + Br2 RNH2
未取代的酰胺用溴的碱溶液处理时,反应中发生分子重排生成 未取代的酰胺用溴的碱溶液处理时, 伯胺的反应称之。 伯胺的反应称之。 13 第十七章 胺
如:
(CH3)3CCH2CONH2
第十七章 胺

O C N R
RNH2
O R'OH O C N R R'NH2 RNH C OR' O RNH C NHR'
七. Mannich 胺甲基化反应
O R C CH2 + HCHO + H N R" R' R" H O R C CH CH2 N R" R' R"
二、胺的化学性质
碱 性
官能团: NH2
亲核性
季铵碱的制备
+
2 [ (CH3)4N ] I
+ Ag2O
2 [ (CH3)4N ]+ OH
+
2 AgI
季铵碱
季铵碱是一个强碱,其碱性与NaOH或KOH相当。
(三)彻底甲基化和霍夫曼消去反应 1. 反应及历程
RCH2CH2NH2 3CH3I RCH2CH2N(CH3)3I
•季铵碱制备及Hofmann消除
I
+ N2 F + N2
N2 BF4
被-OH取代
N2 HSO4 + H2O
H+ △
+
OH + N2↑ + H2SO4
被H原子取代
H3PO2 + H 2O
ArN2C l
+
Ar H + H3PO3 + N2↑ + HC l Ar H + CH3CHO + N2↑ + H 2SO4
C2H5OH , △
OCH3
2) 与酰氯反应
O R C Cl + 2CH2N2 O R C CHN2 CH3Cl N2
第十七章胺和酰胺ppt课件
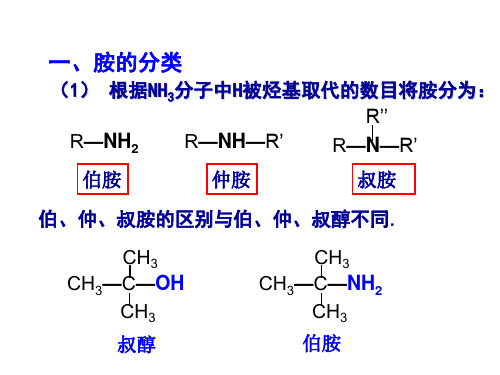
(2)N上连有脂肪烃基的芳香仲胺和叔胺的命名: 用“N”表示基团连在氮原子上。
-NH-C2H5
N-乙基苯胺
CH3 —N-C2H5
N-甲基-N-乙基苯胺
(3)较复杂的胺或多官能团化合物,按系统
命名法命名.
CH3
CH3
CH3-CH - CH—C—CH3
NH2 CH3
2,2,4-三甲基-3-氨基戊烷
O H
RCN
H
(二)水解反应
• 酰胺在通常情况下较难水解,在酸或碱的催化下 加热时,则可加速反应,但比酯的水解慢得多。
水解生成羧酸和胺。
O
O
HCl R C OH + NH4Cl
R C NH2 + H2O
O NaOH R C ONa + NH3
(三)与亚硝酸的反应
O R C NH2 + HNO2
O R C OH + N2
伯胺与亚硝酸的反应
脂肪伯胺与HNO2反应的产物常是醇、烯烃等的混 合物,并定量的放出 N2 。可用于-NH2 的定量测定.
RNH2 —Na—NO—2+—HC—l > N2
+ H2O + 混合物
芳香伯胺在较低温度及过量强酸溶液中与HNO2 反应,生成重氮盐。
NH2 N—a—N0O~—52—℃, H—C>l
H2N C N
H
O C NH2
在缩二脲的碱性溶液中,加入少许硫酸铜溶液, 溶液显紫红色或紫色,该反应称为缩二脲反应。
凡分子中含有两个或两个以上酰胺键结构的化 合物,如多肽、蛋白质等都能发生缩二脲反应.
二、丙二酰脲
丙二酰脲为无色结晶,熔点为245℃,微溶于水。
有机化学下册第17章胺ppt课件

三甲基苄基氢氧化铵 benzyltrimethylammonium hydrate
14
氨
作为取代基时,用“氨”
NH2 NHCH3
氨基 甲氨基
铵 氮上带正电荷时,用“铵”
H3C NH3Cl
氯化甲铵
H3C NH2
甲胺
H3C NHCH3 二甲胺
3
17.1.1 胺的分类
氨基 Amino group 亚氨基 Imino group
H HNH
R HNH
R R' N H
季胺盐(碱) R'
R N
R"
OH
R"'
R R' N R"
氢氧化四烃基铵 四烃基氢氧化铵
Tetra alkyl ammonium hydroxide
氨
Ammonia
伯胺 Primary amine
17.3 一元胺的化学性质
酸性
N H
H
碱性 亲核性
R
被氧化 亚硝化
20
17.3.1 酸碱性 Acidity and Basicity
碱性
1. 胺分子中N原子带孤对电子,可接受质子显碱性
H+
RNH2 + H2O
RNH3 + OH
RNH2 + HCl
RNH3Cl NaOH
RNH2
+ NaCl + H2O
H3C C
N CH3 C
H2 H2
2-甲基-4-氨基己烷
4-amino-2-methylhexane
2-(二乙氨基)丁烷
有机化学课件--第十七章胺

R-酸 +
R-胺 S-胺
R,R-盐 S,S-盐
2020/5/11
课件
19
另外一种色谱拆分方法是基于以光学活性的高分子化合物为固 定相的拆分方法。被拆分的物质以不稳定的键合作用与该固定 相结合,由于固定相的手性基团与被拆分外消旋体中的两个对 映异构体的亲和力不同,因而决定了这种方法的手性选性。
拆分 外消旋体胺时,首先使其与3,5-二硝基苯甲酰氯反应 生成相应的外 消旋体3,5-二硝基苯甲酰胺
RX + NaCN Q+X- RCN + NaX
催化剂
有机相 水相
有机相 水相
相转移催化:如果反应在两相中进行,相转移催化剂可以穿越两相的界面,将 反应物中的一种离子(如CN-)从水相转移到有机相中,使之与底物反应;然
后,又将反应物中的另一种离子带到水相中。相转移催化剂,只起“运送”离
子有的机作相用,本R身X并未+ 损Q+耗CN。-
RCN + Q+X-
水相 有机N相aCN +RQX+X+- Q+CN-Na+X- RCN + Q+X-
水相 NaCN + Q+X-
Na+X-
2020/5/11
课件
26
【实例】
CH2Cl
+
NaCN
TEBA / 水 回流1小时
+
TEBA= (C2H5)3N-CH2C6H5
Cl -
CH2CN 92%
某些低碳链的季铵盐具有生理活性。
第十七章 胺
主要内容
17.1 分类、结构与命名 17.2 物理性质 17.3 胺的制备 17.4 胺的化学反应 17.5 重氮化反应和重氮盐
第17章_材料有机化学胺

罗氏化学 出品
CH3
CH3
A
H3C
CH3
B
H3C
NH H3C
H3C N(CH3)2
H3C
H3C
H3C
N H
N H3C CH3
CH3
CH3
N H
罗氏化学 出品
CH3 N(CH3)2
17.7 胺的氧化和科普消除
1 氧化胺
(1)氧化胺的制备:
R3N
H2O2 or RCO3H
(2)性质:
R3N→O (R3N+-O-)
第 17 章 胺
罗氏化学 出品
17.1 胺的分类
本
17.2 胺的结构
章
17.3 胺的物理性质
提
胺的反应
纲
17.4 胺的成盐反应 四级铵盐的应用
17.5 四级铵碱和霍夫曼消除反应
17.6 胺的酰化、兴斯堡反应
17.7 胺的氧化和科普消除
17.8 胺与亚罗硝酸氏的化反学应出品17.9 重氮甲烷
本
胺的制备
CH3(CH2)7CN 95%
相转移催化剂的用处:提高产率、降低反应 温度、缩短反应时间。
罗氏化学 出品
(3)相转移催化剂的使用原理(参见第十章) 请同学分析下面的实例:
罗氏化学 出品
17.5 四级铵碱和霍夫曼消除反应
1 四级铵碱
2 霍夫曼消除反应 (1)定义 (2)霍夫曼消除的规律 (3)霍夫曼消除反应的机理 (4)霍夫曼消除反应的机理和霍夫曼规则的关系
胺的光谱特征
胺的红外和核磁共振谱见第5章。
罗氏化学 出品
胺的反应 17.4 胺的成盐反应 四级铵盐的应用
17.4.1 胺的碱性 17.4.2 胺与酸的成盐反应 17.4.3 四级铵盐及其相转移催化作用
第17章-胺

O N -K+ CH3CH2B r
O
O
O N CH2CH3 O
O H -/H 2 OFra bibliotekCOOCON HCH2CH3
COOCOO- + CH3CH2NH2
有时酰胺水解困难, 可采用肼解
O NR+NH2NH2.H2OC2H5OH O
氨基酸合成 p773
O
N
+ RNH2 + H2O
N
O
3. 硝基化合物还原
NH2 NH2
制备伯胺 Ni, Pd, Pt
Sn、Fe/HCl
选择性还原试剂
硫化铵
硫氢化钠
硫化钠
还原剂计量: 二硝基化合物选择还原
p775
4. 腈及其它含氮化合物的还原
R C l + aN N C
R C N
N i/H 2 or L iA lH 4
R C H 2N H 2
CON(CH3)2
LiAlH4 ether
CH2NH2 89%
CHO
CH3CH2NH2 LiBH3CN
CH2NHCH2CH3 89% N-benzylethanamine
O
(CH3)2NH
NaBH3CN
N(CH3)2
甲 酸 铵
: 提 供 氮、 作 为 还 原 剂
Leuckart反应——醛(酮)在高温下与甲酸铵 反应得一级胺的反应。
O CCH3
(CH3)2NH dimethyl amine
NH2
aniline 苯胺
NHCH3
N-methyl aniline
C H 3C H 2N H C HC H 2C H 2C H 2C H 2C H 3 C H 2C H 3
第十七章__胺

OH-
CH2=CH2 + R CH2CH2N(CH3)2 + H2O
4. 不符合霍夫曼规则的特殊例子
C6H5CH2CH2N+(CH3)OHC2H5
C6H5CH CH2 + C2H5N
H2N+(CH3)OHC2H5
O
C6H5CH CH2 + C2H5N(CH3)2
CH3 H 64 %
H N+(CH3)3OH立体化学特征:反式-H 被消除
用途二:测定结构 已知化合物(A)分子中不存在1o H原子,(A)经下列
反应得3-甲基-1,4-戊二烯,
求(A)的可能结构式。 A 2CH3I AgOH CH3I B AgOH
A:
N H
若A中可能存在H原子,则A就有三种 可能的结构
N N CH CH2CH CH 2CH 3 3 2C
hylamine aniline methylamine aniline ine aniline 甲胺 苯胺
cyclopropylethylmethylam cyclopropylethylmethyl cyclopropylethylmethylamine 甲基乙基环丙基胺
以烃基不同
以氨基数目 (-NH2)
一元 胺 二元胺 三元胺
伯胺 10 仲胺 20 RNH2 R2NH R3N
以氨基N原子上所 连烃基个数
叔胺 30
季铵盐(碱) R4N
二、胺的命名:
1. 普通命名法:可用胺为官能团,如:
CH3 CHCH 3 3 NH2 NH2 NH2 N
H CH 2 3NH2 23NH
有机化学第十七章_胺

NO2 NH4SH
NO2 (还原一个硝基)
选择性还原
NO2
NO2 Zn 2 NaOH 氢化偶氮苯 NH NH
NH2
碱性还原:双分 碱性还原: 子偶联
•联苯胺重排: 联苯胺重排: 联苯胺重排 氢化偶氮苯在酸催化下, 二氨基联苯的反应。 氢化偶氮苯在酸催化下 生成 4,4-二氨基联苯的反应。 二氨基联苯的反应
N(CH3)2 Br
NCH3
HBr OH-
CrO3-
TM
用苯及不超过三个碳的有机物合成: 例:用苯及不超过三个碳的有机物合成: 用苯及不超过三个碳的有机物合成
3-(N-乙氨基 庚烷 乙氨基)庚烷 乙氨基
O NH
3-甲基 甲基-2-(N-甲氨基 戊烷 甲氨基)戊烷 甲基 甲氨基
O H2N COC2H5
CH3CCH2CCH3
4-亚氨基 戊酮 亚氨基-2-戊酮 亚氨基 [季铵化合物 季铵化合物] 季铵化合物
对氨基苯甲酸乙酯
将负离子和取代基的名称放在“ 将负离子和取代基的名称放在“铵”字前
第十七章 胺
本章目录
分类、 第一节 分类、结构和命名 第二节 物理性质和波谱性质 第三节 胺的制备 第四节 胺的化学反应 第五节 重氮化反应和重氮盐
分类、 第一节 分类、结构与命名
一、分类
NH3 氨 RNH2 1o胺 R2NH 2o胺 R3N 3o胺 R4N+X季铵盐 R4N+OH季铵碱
季铵化合物: 季铵化合物:氮原子上连有四个烃基的衍生物 氨基: 氨基:-NH2 ; 亚氨基: 亚氨基:-NH-
肟的还原(催化氢化、LiAlH4,Zn/HCl等) 肟的还原(催化氢化、 等
NOH Na, C2H5OH or LiAlH4 NH2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.Sn +HCl 2.NaOH
82%
C
O
CH3
NO2
NaSH
C CH3 O
NO2
EtOH
78--83%
NO2
NH2
2020/11/11
NaAsO3
NO2
Fe,NaOH
Zn+NaOH Fe,HCl
O NN NN NH NH
催化氢化 NH2
3)联苯胺重排 NO2 Zn+NaOH
NHNH
2020/11/11
2)化学还原法
N H 2
F e + H C l N O 2
N H 2
CH3
CH3
HOCH2 C NO2Fe+FeSO4HOCH2 C NH2
H2SO4
CH3
90% CH3
2020/11/11
选择还原:
N O 2 FeSO 4 CH O N H 3,H 2O
N H 2 69--75%
CH O
NO2
NH2
CH3 C2H5 N CH2=CH—CH2 C6H5
CH3
N
C6H5
C2H5 CH2—CH=CH2
2020/11/11
2 、胺的物理性质
低级胺为气体或易挥发性液体; 高级胺为固体; 芳香胺为高沸点的液体或低熔点的固体; 胺具有特殊的气味; 胺能与水形成氢键; 一级胺和二级胺本身分子间也能形成氢键。
m ethylam inehydrochloride ethylamineacetate
甲胺盐酸盐
乙胺醋酸盐
CH2CH3
+
CH3CH2-N-CH2CH3
Br-
CH2CH3
Tetraethylammonium bromide
溴化四乙铵
CH2CH3
+
CH3CH2-N-CH2CH3
OH-
CH2CH3
Tetraethylammonium hydrooxide
NHNH
H+
H2N
NH2
4 、腈、肟和酰胺的还原
R CN
H2, Raney Ni NH3
LiAlH4
R CH2NH2
O
L i A l H 4
RCN H 2
2020/11/11
H 2 O
R C H 2 N H 2
例 :
CH 2CNH 12 20 /N -1 i30oC 130atm
CH 2CH 2N H 2 87%
O 邻苯二甲酰亚胺
KOH
or K2CO3
NH2NH2 (肼解) 或水解
R NH2
2020/11/11
O NK
O
RX 或 R OTs
R OTs
O R OS
O
O NR
O
CH3
R OH
O + Cl S
O (TsCl)
CH3
3、硝基化合物的还原: 1)催化氢化:
N i N O 2+H 2压 力 , 加 热
2020/11/11
第十七章
胺
主要内容
第一节 胺 第二节重氮化合物和偶氮化合物 第三节 硝基化合物
2020/11/11
第一节
(一)分类和命名 一 、胺的分类:
胺类
胺根据在氮上的取代基的数目,可分为一级(伯),二 级(仲),三级(叔)胺和四级(季)铵盐。
二、胺的命名:
1、普通命名法:可用胺为官能团,如:
C H 3 (C H 2 )5 C HNO H C 2 H H 5 2 O /N H i
C H 3 (C H 2 )6 N H 2 7 3 %
O C N (C H 3)2L iA lH 4
C H 2N (C H 3)2 88%
2020/11/11
5、羰基化合物的还原氨化
R CO
R'
H2 / Ni
NH3
• 伴有多取代产物,分离可能有困难,仲卤代物 和叔卤代物伴有消除产物
C H 3C H 23 C HC O O H + N H 3
C H 3 (C H 2 )3 C H C O O H
2020/11/11
B r 合 成 氨 基 酸 常 用 此 法
N H 2
2、盖布瑞尔(Gabriel) 伯胺合成法
O NH
2020/11/11
①芳胺毒性大,(吸,食,透0.25mL,严重中毒) β—萘胺,联苯胺——致癌物
②N—H键不如O—H键强,b.p较醇低。 N上的取代基使N—H键减少,2○,3○胺b.p↓,水溶性↓。
IR: 一级胺
νN—H
δN—H(面内)
3300-3500 1590-1650
δN—H(面外) 652-900
6、酰胺的 Hofmann 降解( Hofmann重排)
O
B r2 / N a O H
RCN H 2
RN H 2 + C O 2
H phC H 2
C
C H 3
O C N H 2
B r2,N aO HphC H 2H
C H 3N H 2
N H 2
C H 3 N
C H 2C H 3
m eth ylam in e
甲胺
2020/11/11
an ilin e
苯胺
cyclop rop yleth ylm eth ylam in e
甲基乙基环丙胺
3、胺盐和四级铵化合物的命名:
C H 3N H 2 H C l
CH3CH2NH2Байду номын сангаасHOAc
氢氧化四乙铵
2020/11/11
(二) 胺的结构及物理性质
1、 胺类化合物的结构: N 原子为 sp3 杂化
R'
快速翻转
R
R"
N
N
R
R"
R'
N
"R
R
R'
对映关系,无旋光性
N N
2020/11/11 无 法 翻 转 , 有 旋 光 性
R1 手性中心
N
R4
R2
R3
无法翻转,有旋光性
四级胺盐的对映体已经分离出来,N上四个SP3轨道 都用于成键,氮的翻转不易发生:
R'
R CN
R+C N
R''
2020/11/11
m /e=30+n*14
(三)胺类化合物的制备方法:
1 、氨的烷基化(卤代烃胺解,SN2 机理)
NH3 + R X
RNH2 + NH4X
RX R2NH+NH4X
使用过量的氨, 可以得到伯胺为主的产物
RX R3N + NH4X
控制条件,也可以得到某一胺为主的产物 RX R4N+X
R
H2 / Ni
C NH
R'
R CHNH2
R'
亚胺
CH3(CH2)5CHO NH3,H2/Ni CH3(CH2)5CH2NH2
O
60%
CH3(CH2)5C
CH3
NH3,H2/Ni CH3(CH2)5CHNH2
2020/11/11
O CCH3HCOO-NH+4
185oC
88---91%CH3
NH2 CCH3 66%
ΝC—N 1030-1230
( 两个峰,光、中) (强)
(宽、强)
二级胺 3300-3500
弱
(单峰)
2020/11/11
700-750 (弱)
NMR: —CH2—CH2—NH2
δ 1.1-1.7; 2.2-2.8;0.5-5ppm (与溶剂的性质,溶液浓度,温度有关,可影响H—键缔和)
MS:
R—NH2 —M+小 M+ 奇数个N ,M+奇数 Ar—NH2 M+大
