中考化学热身训练 物质构成的奥秘
中考化学复习专题物质构成的奥秘【精选】

正电荷 负电荷
N
H
+ 4
C
O
23
(4)离子符号表示的意义 1个镁离子带2个单位正电荷 2个镁离子
4. 原子与离子的区别与联系
【易错易混点】 ①元素的化学性质主要取决于最外层电子数; ②根据粒子的结构示意图判断原子、离子的种类
=0 原子 原子数-核外电子数 >0 阳离子
<0 阴离子
1.下列粒子结构示意图,属于阳离子的是( C )
6.长沙地铁正式开通,极大方便了市民出行,但也限制了
市民随意吃美食臭豆腐。因为在地铁车厢吃臭豆腐会影响
他人乘车舒适度。
请你从分子的角度解释乘车禁止吃有异味的食物的原
因是:__分__子__在__不__断__运__动________。
7.如图是“分子性质”的探究实验,在A中加入5 mL浓氨水, B中加入20 mL含酚酞的蒸馏水,
罩上大烧杯。请回答下列问题: (1)几分钟后,可以观察到___B_____ (填“A”或“B”)烧杯中溶液开始变红。
(2)该实验说明分子具有的一个基本性质是 ____分__子__是__不__断__运__动__的_________。 (3)该实验中大烧杯所起的作用是_防__止__氨__分__子_扩__散__到__空__气__中_,_ _对__空__气__造__成__污_染__(_或__使_氨__分__子__局__限__在__一_定__空__间__内__运__动_,__浓__度__增__大__, _使__实__验__现__象__更_明__显__)______ (任写一点即可)。
生成二氧化碳,说明同种分子化学性质不同
3.用分子、原子的观点分析下列生活中的现象,其解 释不合理的是D( )
A. 50 mL水与50 mL酒精混合后,总体积小于100 mL —— 分子之间有间隔
中考一轮复习物质构成的奥秘秒杀口诀及对应练习

物质构成的奥秘秒杀口诀及对应练习口诀:相对不能带克,元素不能论个,原子对比数字,宏组微构不错!典例:判断正误:1.过氧化氢是由氢、氧两种元素组成的()2.过氧化氢是由氢、氧两种元素构成的()3.过氧化氢是由两个氢元素、两个氧元素组成的()4.过氧化氢是由两个氢原子、两个氧原子组成的()5.过氧化氢分子是由两个氢原子、两个氧原子组成的()6.过氧化氢分子是由两个氢原子、两个氧原子构成的()7.一个过氧化氢分子是由两个氢原子、两个氧原子组成的()8.一个过氧化氢分子是由两个氢原子、两个氧原子构成的()真题重现1.硒是人体必需的一种微量元素,严重缺硒可能诱发皮肤病和癌症。
硒的原子结构示意图及其在元素周期表中的某些信息如图所示,下列分析正确的是()A.硒属于金属元素B.硒的相对原子质量为78.96gC.硒原子的核电荷数为34D.硒原子的核外有6个电子2.硒被誉为“抗癌大王”。
根据右图提供的硒的有关信息,下列说法中,正确的是()A.硒属于金属元素B.硒的原子序数是34C.硒的原子结构示意图中x=4 D.硒的相对原子质量是78.96 g3.镍在元素周期表中的信息如下图所示,下列有关镍元素的说法不正确...的是()A.原子序数是28B.属于金属元素C.原子中的质子数是28D.相对原子质量为58.69 g4.我国的稀土储量居世界第一位。
铕(Eu)是一种稀土元素,下列有关说法中错误的是( )A.铕属于非金属元素B.铕的原子序数是63C.铕原子中的质子数为63D.铕的相对原子质量是152.05.铬在元素周期表中信息如图所示,下列有关铬元素的说法正确的是()A.原子序数是24B.属于非金属元素C.一个铬原子核外有28个电子D.相对原子质量为52.00g6.如图是汞元素在元素周期表中的有关信息,下列说法错误的是()A.汞的原子序数是80 B.汞属于非金属元素C.汞原子核外有80个电子D.汞元素的相对原子质量是200.67.锶元素在元素周期表中显示的信息和粒子结构示意图如图所示。
专题03 物质构成的奥秘(考点专练)-备战2023年中考化学一轮复习考点微专题(全国通用)(解析版)

专题03 物质构成的奥秘1.物质是由微观粒子构成的,下列物质由原子直接构成的是()A.金刚石B.水蒸气C.氯化钠D.碳酸钠【答案】A【解析】A、金刚石是由碳原子直接构成,符合题意。
B、水蒸气是由水分子直接构成,不符合题意。
C、氯化钠是由氯离子和钠离子构成,不符合题意。
D、碳酸钠是由钠离子和碳酸根离子构成的,不符合题意。
故选A。
2.(2022上海交大附中一模)关于水分子的说法正确的是A.水分子是由氢原子和氧原子构成的B.水变成冰后,水分子是静止的C.水变成水蒸气后,水分子的体积变大了D.水分子可以保持水的物理性质【答案】A【解析】A、水分子是由氢原子和氧原子构成的,此选项表述正确;B、水变成冰后,水分子也在不断运动,只是运动速度慢了,此选项表述不正确;C、水变成水蒸气后,水分子的体积没变,水分子之间的间隔变大了,此选项表述不正确;D、水分子能保持水的化学性质,但不能保持水的物理性质,此选项表述不正确。
故选A。
3.(2022海南海南模拟)下列物质由离子构成的是A.氯化氢B.硝酸钾C.二氧化碳D.氦气【答案】B【解析】A、氯化氢是由非金属元素组成的化合物,是由氯化氢分子构成的,故选项错误;B、硝酸钾是含有金属元素和非金属元素的化合物,硝酸钾是由钾离子和硝酸根离子构成的,故选项正确;C、二氧化碳是由非金属元素组成的化合物,是由二氧化碳分子构成的,故选项错误;D、氦气属于稀有气体单质,是由氦原子直接构成的,故选项错误。
故选B。
4.(2022青海西宁模拟)从微观的角度解释下列现象,其中错误的是A.十里桂花飘香——分子在不停地运动B.金刚石和石墨的物理性质不同——分子构成不同C.水蒸发为水蒸气,所占体积变大——分子间隔变大D.1滴水中约含1.67×1021个水分子——分子的质量和体积都很小【答案】B【解析】A、十里桂花飘香,说明分子在不停地运动,故A不符合题意;B、金刚石和石墨都是由碳原子构成的,因此他们性质不同是因为碳原子的排列方式不同,故B符合题意;C、水蒸发为水蒸气,所占体积变大,是因为分子的间隔变大,故C不符合题意;D、1滴水中约含1.67×1021个水分子,说明分子的质量和体积很小,故D不符合题意;故选B。
中考化学物质构成的奥秘20篇(附带答案解析)经典

中考化学物质构成的奥秘20篇(附带答案解析)经典一、物质构成的奥秘选择题1.下列关于分子、原子、离子的叙述,正确的是A.分子是保持物质性质的最小粒子B.只有带电的原子才叫离子C.分子、原子、离子都可以直接构成物质D.原子是变化中最小的粒子【答案】C【解析】【分析】【详解】A、分子是保持物质化学性质的最小粒子,错误;B、带电的原子或原子团叫离子,错误;C、分子、原子、离子都可以直接构成物质,如水是由分子构成的,铁是由原子构成的,氯化钠是由离子构成的,正确;D、原子是化学变化中的最小粒子,错误。
故选C。
2.某元素R的原子序数为m,能够形成核外有x个电子的R n- 离子,则下列关系式一定正确的是( )A.m= x B.m = x –n C.m = n - x D.m = x + n【答案】B【解析】【详解】因为原子中:核电荷数=核内质子数=核外电子数=原子序数,元素R的原子中质子数为m,R n-离子是表示得到n个电子后形成的阴离子,所以m═x-n。
故选B。
3.地壳中含有丰富的氧、硅、铝、铁等元素.如图是四种元素的有关信息,关于四种元素的说法错误的是()A.氧元素的原子序数为8B.铁元素属于金属元素C.铝元素的原子在化学反应中易失去电子D.硅元素的相对原子质量为28.09g【答案】D【解析】试题分析:A、由氧原子的结构示意图可知,圆圈内的数字是8,氧原子的核电荷数为8,故选项说法正确;B、铁带“钅”字旁,属于金属元素,故选项说法正确;C、铝原子的最外层电子数为3,在化学反应中易失去3个电子而形成阳离子,故选项说法正确;D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,硅的相对原子质量为28.09,相对原子质量单位是“1”,不是“克”,故选项说法错误。
考点:考查原子结构示意图与离子结构示意图;元素周期表的特点及其应用。
4.在宏观和微观之间建立联系是化学学科特有的思维方式。
下列对宏观事实的微观解释错误的是( )A.A B.B C.C D.D【答案】C【解析】A、H2O和H2O2的化学性质不同,是因为它们是由不同种分子构成的,不同种物质的分子性质不同,正确;B、在阳光下,湿衣服更容易晾干,是因为温度升高,分子的运动速率加快,即分子的运动速率随温度升高而加快,正确;C、在化学变化中,分子可以再分,原子不能再分。
初三化学复习专题一物质构成的奥秘

02 物质构成的奥秘
原子的构成
原子的概念
原子是化学变化中的最小 粒子,是构成物质的基本 单位。
原子的结构
原子由原子核和核外电子 构成,原子核由质子和中 子组成。
同位素
质子数相同而中子数不同 的同一种元素的不同核素 互称为同位素。
分子与原子
分子的概念
分子是由两个或多个原子通过化 学键结合形成的相对稳定的粒子。
常见简化表示方法
用元素符号表示单质,用简化数字表示化合物的 组成。
示例
将氧化铁(Fe₂O₃)简化表示为FeO。
化学式与元素质量分数的计算
1 2
定义
元素质量分数是指某元素的质量占化合物质量的 百分比。
计算方法
元素质量分数 = (元素的相对原子质量 × 原子 个数)/ 化合物的相对分子质量 × 100%。
化学键
分子中原子之间的相互作用力称为 化学键,包括共价键、离子键和金 属键等。
分子与原子的关系
分子是由原子构成的,分子在化学 变化中可以再分,而原子是化学变 化中的最小粒子。
离子
离子的概念
离子的性质
离子是带电的原子或原子团,是构成 物质的重要粒子之一。
离子具有带电性和极性,可以影响物 质的溶解性、导电性和酸碱性等性质。
单质
由同种元素组成的纯净物,如氧气、 铁等。
化合物
由两种或多种元素组成的纯净物,如 水、二氧化碳等。
酸、碱、盐
01
02
03
酸
在水溶液中能解离出氢离 子和酸根离子的化合物, 如硫酸、盐酸等。
碱
在水溶液中能解离出金属 离子和氢氧根离子的化合 物,如氢氧化钠、氢氧化 钙等。
盐
在水溶液中能解离出金属 离子和酸根离子的化合物, 如氯化钠、硫酸铜等。
主题二 物质构成的奥秘-2022中考化学考前必背重难点知识手册

2022中考重难点知识手册专题二物质构成的奥秘知识点1:构成物质的基本微粒1.构成物质的微粒是不断运动的;且温度越高,微粒运动越快。
2.微粒之间有一定的空隙,不同物质微粒间的空隙大小不同,且温度越高,微粒之间的空隙越大。
同种物质,固体、液体中微粒之间的空隙较小,而气体中微粒之间的空隙大,所以气体容易被压缩,而固体和液体不易被压缩。
3.物质具有的“热胀冷缩”现象和固液气三态的变化实际上是:微粒间空隙大小发生的变化,而微粒本身大小不变。
4.构成物质的基本微粒有分子、原子、离子。
(1)由分子构成的物质:①气体单质,如H2 、O2、N2、Cl2等①非金属化合物,如H2O、CO2 、P2O5 等(2)由原子构成的物质:①金属单质,如Fe、Cu等特点:①稀有气体,如:He、Ne等是单质且化学式与①固态非金属单质,如金刚石等元素符号相同(3)由离子构成的物质:大多数金属化合物,如NaCl、CuSO4等特点:含有金属元素且是化合物5.分子和原子的本质区别是在化学变化中:分子可再分,原子不可再分。
6.分子和原子关系:分子是由原子构成的。
7.化学变化的微观实质就是分子分解成原子,原子重新组合成新的分子的过程。
8.分子用化学式表示,化学式前加数字仅表示几个某分子。
如:水分子 H2O 一个水分子 H2O 三个水分子 3H2O原子用元素符号表示,元素符号前加数字仅表示几个某原子。
如:氢原子 H 一个氢原子 H 三个氢原子 3H(注:当分子、原子的个数为“1”时,“1”一定..要省略。
)9.在化学反应的前后一定改变的微粒是分子的种类,一定不变的微粒是各原子的种类。
如:在电解水的前后,一定改变的微粒是水分子(H2O),一定不变的微粒是氢原子(H)和氧原子(O) 。
10.在原子中:核电荷数= 质子数 = 核外电子数 = 原子序数。
知识点2:物质的多样性1.物质的分类:(1)纯净物与混合物的区别:是否只含一种物质注意:纯净物有化学式,混合物无化学式(2)单质与化合物的区别:是否只含一种元素(微观:是否只含一种原子)注意:单质、化合物首先是纯净物,因此,只含一种元素的物质可能是单质也可能是混合物(3)有机物与无机物的区别:是否含碳元素注意:①有机物与无机物首先是化合物,单质和混合物一定不是有机物①CO、CO2、H2CO3、CaCO3等碳酸盐尽管含碳元素但它们不是有机物,是无机物(4)氧化物中只有两种元素且当中有一种是氧元素(如:Rx Oy )-2 知识点3:化学元素和物质的组成 1.元素的种类由 质子数 或 核电荷数 决定;元素是宏观概念,只讲种类不讲个数。
中考化学专题——构成物质的奥秘

中考化学专题——物质构成的奥秘1.食品添加剂溴酸钾(KBrO 3)会致癌,其中溴元素(Br)的化合价为 ( )A.+1B.+3C.+5D.无法确定2.石英砂的主要成分是二氧化硅(SiO 2)。
二氧化硅中硅元素的化合价为 ( )A.+4B.+3C.+2D.-23.今年1月份的雪灾对我国南方的电力、交通造成很大的危害。
有一种融雪剂含有Na 2SiO 3(硅酸钠),Na 2SiO 3中Si 元素的化合价是 ( ) A.+1价 B.+2价 C.+3价 D.+4价4、卟啉铁(C 34H 32ClFeN 4O 4)对缺铁性贫血有显著疗效。
以下说法正确的是 ( )A.卟啉铁中含有5种元素B.1个卟啉铁分子中含有34个碳原子C.人体补铁的唯一方法是服用卟啉铁D.“缺铁性贫血”中的“铁”指单质铁5. 20世纪20年代,就有人预言可能存在由4个氧原子构成的氧分子(O 4),但一直没有得到证实。
最近,意大利的科学家使用普通氧分子和带正电的氧离子制造出了这种新型氧分子,并用质谱仪探测到了它的存在。
下列叙述中正确的是( )A.O 4是一种新型的化合物B.一个O 4分子中含有2个O 2分子C.O 4和O 2的性质完全相同D. O 4和O 2混合后形成的是混合物6.染发时常用到的着色剂——对苯二胺,是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其化学式为C 6H 8N 2。
有关对苯二胺的说法正确的是( )A.对苯二胺属于有机物B.对苯二胺的相对分子质量为27C.对苯二胺中碳、氢、氮元素的质量比为3∶4∶1D.对苯二胺能被人体少量吸收7.抗震救灾,众志成城。
用于汶川震后防疫的众多消毒剂中,有一种高效消毒剂的主要成分为三氯异氰尿酸(C 3O 3N 3Cl 3),又称高氯精。
下列有关高氯精的说法不正确的是( )A.高氯精由4种元素组成B.高氯精中C.O 、N 、Cl 的原子个数比为1∶1∶1∶1C.高氯精中C.N 两种元索的质量比为12∶14D.高氯精中氯元素的质量分数为25%8.2008年北京奥运会主体育场的外形好似“鸟巢”(The Bird Nest),有一类物质也好似鸟巢,如化学式是B 5H 9的五硼烷。
中考化学专题复习 专题三 物质的构成奥秘
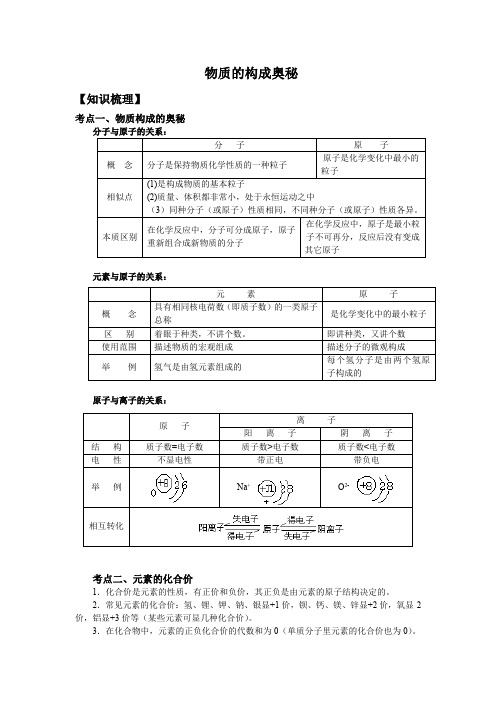
物质的构成奥秘【知识梳理】考点一、物质构成的奥秘 分子与原子的关系: 分 子 原 子 概 念 分子是保持物质化学性质的一种粒子 原子是化学变化中最小的粒子相似点 (1)是构成物质的基本粒子 (2)质量、体积都非常小,处于永恒运动之中(3)同种分子(或原子)性质相同,不同种分子(或原子)性质各异。
本质区别 在化学反应中,分子可分成原子,原子 重新组合成新物质的分子 在化学反应中,原子是最小粒子不可再分,反应后没有变成 其它原子元素与原子的关系:原子与离子的关系:考点二、元素的化合价1.化合价是元素的性质,有正价和负价,其正负是由元素的原子结构决定的。
2.常见元素的化合价:氢、锂、钾、钠、银显+1价,钡、钙、镁、锌显+2价,氧显-2价,铝显+3价等(某些元素可显几种化合价)。
3.在化合物中,元素的正负化合价的代数和为0(单质分子里元素的化合价也为0)。
元 素 原 子 概 念具有相同核电荷数(即质子数)的一类原子总称 是化学变化中的最小粒子 区 别着眼于种类,不讲个数。
即讲种类,又讲个数 使用范围描述物质的宏观组成 描述分子的微观构成 举 例 氢气是由氢元素组成的 每个氢分子是由两个氢原子构成的原 子 离 子 阳 离 子 阴 离 子 结 构质子数=电子数 质子数>电子数 质子数<电子数 电 性不显电性 带正电 带负电举 例 Na +O 2- 相互转化4.通过原子团或其他有固定化合价的元素,可求出不易确定的元素的化合价。
【典型例题】【例1】:已知六种微粒结构示意图分别为:(1)A 、B 、C 、D 、E 、F 共表示种元素;(2)表示原子的微粒是 (填序号);(3)表示离子的微粒是 (填序号)。
审题与思路:元素是具有同相同核电荷数的一类原子的总称。
在题所示的六种微粒中,(A )与(B )核电荷都是+8,(E )与(F )核电荷都是+12,所以这六种微粒结构代表核电荷为+8、+10、+11、+12四种元素。
必背3物质构成的奥秘-冲刺2023年中考化学必背重点知识(原卷版)

中考必背重点知识(三)物质构成的奥秘三分子和原子知识点一:物质由微观粒子构成1.构成物质的粒子物质是由微观粒子构成的,构成物质的粒子有:、和。
2.微粒的性质(以分子为例)①小:分子的质量和体积都很小1个水分子的质量约是3×10—26kg,一滴水(20滴为1mL)中大约有1.67×1023个水分子。
如果10亿人来数一滴水里的水分子每人每分钟数100个数,昼夜不停的数,需要3万年才能数完。
①分子在不断运动(温度越高,分子运动速率越快)①分子间是有间隔的①同种分子性质相同,不同分子性质不同其中①①①是分子、原子、离子的共同性质。
知识点二:分子和原子的关系1.分子——保持由分子构成的物质的化学性质的最小粒子原子——化学变化中的最小粒子二者关系:①在化学变化中,分子分成原子,原子重新组合成新的分子;①在化学变化中,分子可分,原子不可分。
2.用微粒的观点解释(1)物理变化和化学变化物理变化:微粒本身不改变,只是微粒的间隔发生了变化。
化学变化:微粒本身发生了改变,即微粒的构成发生了改变。
(2)纯净物与混合物纯净物:由 微粒构成。
混合物:由 微粒构成。
3.由原子构成的物质:①金属单质 如:铁、铜、汞等①固态非金属 如:碳、磷、硫等①稀有气体单质 如:氦、氖、氩等4.分子和原子比较(1)相同点分子和原子都是组成世界的稳定 ,它们的 和 都很小,它们都在不断的 ,它们之间都有可以变化的 。
(2)不同点(用分子、原子填空)① 相互结合形成②在化学变化中, 发生了破裂,分成了更小的粒子—— , 又重新组合成新的 。
是化学变化中的最小粒子, 是保持物质化学性质的最小粒子。
在化学变化中可分, 在化学变化中不可分。
原子的结构知识点一:原子的构成()()()⎪⎩⎪⎨⎧-⎩⎨⎧++个负电荷:一个电子带核外电子中子:不带电个质子带一个正电荷:质子原子核原子11说明: ①原子核位于原子中心,电子围绕原子核做高速运动。
2023年安徽省中考化学复习---物质构成的奥秘

02
考法一 分子、原子、离子及其性质
【例1】(2022·安徽)2021年12月9日,航天员王亚平在中国空间站开设的“天宫课堂”进行了泡腾片(由碳酸氢钠、酸和香料等组成)实验。下列对应解释错误的是( )
选项
实验操作及现象
解释
A
从水袋中挤出水,形成水球飘浮在空中
水由液态变成了气态
B
将水溶性颜料溶于水球,水球呈美丽的蓝色
原子核
核外电子
原子核
核外电子
原子核
质子
中子
2.最外层电子数与元素化学性质的关系
最外层电子数
得失电子趋势
化学性质
金属原子
一般①______4个
容易②____电子
观点
A
铁丝在氧气中燃烧后质量增大
化学反应前后质量守恒
B
水电解可得到氢气和氧气
分子是可分的
C
少量白糖加入水中,不久“消失”
微粒是不断运动的
D
苯和 冰醋酸混合后体积大于
微粒间有间隔
A
5.(2016·安徽)近年,我国科学家首次拍摄到水分子团簇图像,模型如图。下列说法正确的是( )
C
A.氢氧两种元素只能组成水 B.团簇中的水分子不再运动C.水蒸气冷凝成水,分子间隔减小 D.可燃冰和冰都是由水分子构成
(2)下列说法正确的是( )
A.超临界水与液态水具有相同的物理和化学性质B.将气态水升温或加压一定使水分子间距离变小C.超临界水是由液态水和气态水组成的混合物D.用超临界水处理含碳废物的方法比焚烧法更环保
D
4.(2017·安徽)下列实验事实不能作为相应观点的证据的是( )
选项
实验事实
D
2.(2022·郴州)按要求用化学符号填空:
【化学】 中考化学物质构成的奥秘20篇(附带答案解析)(word)

【化学】中考化学物质构成的奥秘20篇(附带答案解析)(word)一、物质构成的奥秘选择题1.如图1所示是元素周期表中铝元素的部分信息,图2铝原子的结构示意图.下列说法正确的是()A.铝的相对原子质量为26.98gB.铝元素是地壳中含量最多的元素C.铝原子核内的质子数为13D.铝离子的核电荷数为10【答案】C【解析】【分析】【详解】A、根据元素周期表中的一格中获取的信息,可知铝元素的相对原子质量为26.98,相对原子质量单位是“1”,不是“克”,故选项说法错误.B、地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其中含量最多的元素是氧元素,故选项说法错误.C、根据元素周期表中的一格中获取的信息,该元素的原子序数为13;根据原子序数=核电荷数=质子数=核外电子数,则铝原子核内的质子数为13;或由图2铝原子的结构示意图可知,铝原子核内的质子数为13;故选项说法正确.D、由图2铝原子的结构示意图,铝原子失去3个电子形成铝离子,铝离子的核电荷数为13,故选项说法错误.故选C。
2.如图为元素周期表第三周期的一部分。
据此判断下列说法中正确的是11 Na 22.912 Mg24.3113 Al26.9814 Si28.09A.Al的相对原子质量是26.98 g B.Si的元素名称是硅,其核电荷数为14 C.Mg原子的核外电子排布是D.它们都属于金属元素【答案】B【解析】【分析】【详解】A、相对原子质量的单位是1,故错误;B、原子序数=质子数=核电荷数,由图可知,Si的名称是硅,其核电荷数为14,故正确;C、原子的核外电子排布中,最外层的电子数不能超过8个,故错误;D、硅是非金属元素,故错误。
故选B。
3.工业用盐中含有的亚硝酸钠(NaNO2)是一种有毒物质,利用NH4Cl溶液可使NaNO2转化为无毒物质。
该反应分两步进行:①NaNO2+NH4Cl===NaCl+NH4NO2②NH4NO2===N2↑+2H2O下列叙述不正确的是A.NH4NO2由三种元素组成B.反应①为复分解反应,反应②为分解反应C.利用NH4Cl处理NaNO2最终转化为NaCl、N2和H2OD.上述反应所涉及的物质中,氮元素的化合价有四种【答案】D【解析】亚硝酸钠(NaNO2)是一种有毒物质,利用 NH4Cl溶液可使NaNO2转化为无毒物质。
中考化学专题训练 第三单元 物质构成的奥秘(含解析)

学习资料中考化学专题训练第三单元物质构成的奥秘(含解析)班级:科目:第三单元物质构成的奥秘一、单选题1。
日常生活中见到的“加碘食盐”“高钙牛奶”中“碘、钙”应理解为()A.分子B.原子C.离子D.元素2。
下列有关微观粒子的说法中正确的是()A.分子由原子构成,原子不显电性,则分子也不显电性B.分子是保持物质化学性质的唯一粒子C.原子中的粒子都不带电D.原子核不显电性3。
王安石的《梅花》诗:“墙角数枝梅,凌寒独自开。
遥知不是雪,为有暗香来。
"诗人在远处就能闻到淡淡的梅花香味的原因是()A.分子很小B.分子在不断地运动C.分子之间有间隙D.分子是可以分的4。
学习知识要真正做到融会贯通,疏而不漏,学习了原子的构成知识后,请你判断下列叙述错误的是( )A.分子、原子都能直接构成物质B.原子中原子核与核外电子的电量相等,电性相反,因而原子不显电性C.决定原子质量大小的主要是质子和电子D.在化学变化中,原子是不可再分的5。
下列对分子、原子、离子的认识,正确的是()A.原子是最小的粒子,不可再分B.相同原子可能构成不同的分子C.离子不能直接构成物质D.固体难压缩,说明固体分子间无间隔6。
关于氧分子和氧原子的说法,错误的是( )A.在化学变化中,氧分子能再分,氧原子不能B.氧分子大,氧原子小C.氧气的化学性质由氧分子保持D.氧气由氧分子构成,也由氧原子构成7.C—12和C-14是碳元素的两种不同的原子,二者的不同点有()①原子中的电子数;②原子核内的中子数;③原子核内的质子数;④原子的质量A.①②B.③④C.①③D.②④8.下列是一些微观粒子结构示意图,有关叙述正确的是()A.②⑤为同一周期元素的原子B.①②的元素在周期表的同一族C.①③④⑤是具有相对稳定结构的原子D.②③属于同种元素的同种粒子9。
下列结构示意图中,属于阳离子的是()A.B.C.D.10。
下列粒子中不能直接构成物质的是( )A.原子B.分子C.离子D.电子11.水结成冰是由于( )A.水分子的运动停止了B.水分子的化学性质发生了改变C.水分子变小了D.水分子间的间隔发生了变化12。
2021年中考化学专题训练:物质构成的奥秘

2021年中考化学专题训练:物质构成的奥秘考点一:分子与原子1.建立宏观和微观之间的联系对学习化学十分重要。
下列宏观事实的微观解释错误的是()A.品红在水中扩散﹣﹣分子在不断运动B.水蒸发由液态变成气态﹣﹣水分子发生改变C.NO与NO2化学性质不同﹣﹣构成物质的分子不同D.10mL H2O与10mL C2H5OH混合后体积小于20mL﹣﹣分子间有间隔2.下列事实能用分子或原子间有一定间隔解释的是()A.汽油要密封保存B.电解水生成氢气和氧气C.用水银温度计测量体温D.湿衣服在太阳下晾晒干得快3.分子与原子的本质区别是A.分子运动速率快,原子运动速率慢B.分子体积大,原子体积小C.在化学变化中,分子可以再分而原子不可再分D.分子可以构成物质而原子不可以直接构成物质4.下列物质直接由原子构成的是()A.H2B.Fe C.CO2D.NaCl5.用分子的观点解释下列生活现象,错误的是A.花香四溢——分子在不断地运动 B.热胀冷缩——分子的大小改变C.滴水成冰——分子间隔发生改变 D.蜡炬成灰——分子种类发生变化6.下列说法正确的是A.分子可以分,原子不可分 B.原子核都是由质子和中子构成的C.分子、原子都可以构成物质 D.相对于整个原子而言,原子核体积小、质量轻7.用分子的知识解释下列现象,正确的是A.缉毒犬能根据气味发现毒品,是由于分子不断运动B.铁丝在空气中不燃烧而在氧气中燃烧,说明空气和氧气中的氧分子化学性质不同C.变瘪的乒乓球放人热水中能鼓起来,是由于分子受热体积变大D.降温能使水结成冰,是因为在低温下水分子静止不动8.某兴趣小组的同学探究分子的运动,实验如图所示。
图中试管A和装置D的试管中装有体积和浓度相同的浓氨水,试管B和C中装有体积和浓度相同的酚酞溶液。
(1)实验前,另取少量酚酞溶液,向其中滴加浓氨水,观察到酚酞溶液变红。
这一操作的目的是________________________。
(2)实验①和实验②都会出现的现象是_________,但出现此现象的快慢不同。
2023年中考化学专题训练---物质构成的奥秘(含解析)

2023年中考化学专题训练---物质构成的奥秘一、单选题1.2017 年诺贝尔化学奖主要研究成果是快速冷冻可以使蛋白质和所在的水溶液环境发生变化。
其中组成蛋白质的一种丙氨酸分子式为C3H7NO2,下列有关的说法不正确的是A.冷冻的蛋白质分子之间有间隔B.丙氨酸是由C、H、O 三种元素组成C.冷冻的蛋白质分子运动的速度慢D.丙氨酸是由丙氨酸分子构成的2.下面符号中,既能表示一种元素,又能表示一个原子,还能表示一种物质的是A.Cu B.H2O C.O D.N23.下列化学用语关于数字“2”意义的说法正确的是①H2O;②2NH3;③S2-;④Ca2+;⑤+2Ba;⑥N2A.表示离子所带电荷数的是⑤B.表示分子个数的是①⑥C.表示化合价数值的是③④D.表示一个分子中含有某种原子个数的是①⑥4.化学变化前后发生改变的是A.元素种类B.原子个数C.原子质量D.分子种类5.下列关于分子和原子的解释,不正确的是A.1滴水中含有1.67×1021个水分子,说明分子很小B.水结冰后,水分子停止运动C.夏天温度计示数上升,说明温度升高汞原子之间间隔变大D.氧气和臭氧的性质不同,因为分子的结构不同6.我国化学家张青莲精确测定了铈(Ce)等元素的相对原子质量数值。
在元素周期表中铈元素的某些信息如图所示。
下列有关铈的说法不正确的是A.原子序数为58B.属于金属元素C.原子核内质子数为58D.相对原子质量为140.1g7.下列说法错误的是A.将一滴雨水滴在玻璃片上,凉干后有痕迹证明雨水不是纯净物B.溶有较多含钙、镁物质的水是硬水C.鉴别蒸馏水还是自来水可滴加肥皂水D.自来水可以饮用所以是纯净物8.下列说法错误的是A.原子是化学变化中的最小粒子B.分子是保持物质性质的最小粒子C.原子是由原子核和电子构成D.只含一种元素的物质不一定是单质9.如图是元素x的原子结构示意图,下列说法正确的是()A.X属于非金属元素B.该原子最外电子层达到了稳定结构C.该原子的核电荷数为l2D.x与Cl形成的化合物为XCl10.“染色”馒头中添加有铬酸铅(PbCrO4)颜色为柠檬黄,会使人体致癌,已被卫生部门明文禁用。
【初中化学】中考化学复习知识点 构成物质的奥秘

【初中化学】中考化学复习知识点构成物质的奥秘【初中化学】中考化学复习知识点构成物质的奥秘
物质的奥秘主要包括以下几点:
1.了解构成物质的基本微粒,树立物质由微观粒子构成的观念,从微观角度理解物质及其变化,把宏观和微观的分析联系起来,建立元素的概念,从宏观角度描述和表示物质的组成,能进行有关组成的简单计算。
2.认识到分子、原子、离子、电子、质子和中子是物质的基本粒子;初步了解各种粒子的基本特征以及它们之间的基本关系;它可以从微观角度解释物质的状态变化;结合有机质,了解有机分子结构的多样性和复杂性。
3.了解元素的多样性和统一性及其内在联系;粗略掌握元素周期表的知识;结合元素概念的学习掌握地壳中、生物体内元素分布。
4.记住常见元素和原子团的化合价,用化学式表示一些常见物质的组成。
物质的化学变化:
了解物理和化学变化;了解化学变化的特点及现象与本质的关系;了解人们如何利用化学变化来实现能量转换和材料资源的合理利用。
了解化学结合、分解、置换和复分解的四种反应类型,并了解它们遵循的基本规律。
掌握质量守恒定律,能写出常见的化学反应方程式,能计算简单的化学反应。
中考化学知识点专题训练十一:物质构成的奥秘

聚焦2020中考化学知识点专题训练——专题十一:物质构成的奥秘考点一:分子与原子1.用分子的观点解释下列现象,不合理的是()A.食物腐败—分子本身发生了变化B.汽油挥发—分子的大小发生了变化C.热胀冷缩—分子间的间隔改变D.花香四溢—分子不停地运动2.分子和原子都是构成物质的粒子。
分子与原子的根本区别在于()A.能否保持物质的化学性质B.是否大小相同C.能否直接构成物质D.是否在化学变化中再分3.类推是一种常用的学习思维方法。
下列四种类推中正确的是()A.分子可以构成物质,所以物质一定由分子构成B.原子不显电性,所以不显电性的粒子一定是原子C.原子在化学变化中不可再分,因此原子是化学变化中的最小粒子D.纯净物可由一种分子构成,因此冰水是一种混合物4.为了书写和学术交流的方便,常采用国际统一的符号。
下列符号中表示2个氢原子的是()5.下图是两种气体发生反应的微观示意图,其中相同的球代表同种原子。
下列说法正确的是()A.原子在化学反应中可分B.化学反应前后原子的种类不变C.分子在化学变化中不可分D.反应后生成了两种新的化合物6.下列生活中的现象用分子-原子观点进行合理的解释:⑴氢气和液氢都可作燃料,是由于。
⑵救援应急中心用警犬搜救地震中被埋人员,是由于。
⑶医生用水银温度计测量你的体温,是由于。
⑷一滴水大约1.67×1021个水分子,是由于。
7.某化学探究兴趣小组做以下实验探究分子的运动。
请回答实验中的有关问题:⑴实验Ⅰ:在盛有少量蒸馏水的小烧杯中滴入2~3滴酚酞溶液,再向其中滴加浓氨水。
由实验得出的结论有。
⑵实验Ⅱ(如图甲所示):烧杯B中的现象是,产生这一现象的原因是。
⑶为使实验结论准确可靠,该小组成员设计出实验Ⅲ(如图乙所示)作为对比实验。
你对他们的看法是(填“有必要”或“没有必要”),你的理由是。
考点二:原子的结构1.知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与a、b、c相对应的是()A.原子、原子核、核外电子B.原子核、原子、核外电子C.原子、核外电子、原子核D.核外电子、原子核、原子2.已知氧原子的相对原子质量为16,硫原子的相对原子质量为32。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
物质构成的奥秘
1.在地壳中含量最多的元素是()
A.O B.Si C.Al D.Fe
2.衡阳是有色金属之乡,水口山铅锌矿历史悠久,世界闻名,这里的铅、锌指的是()A.单质 B.元素 C.原子 D.化合物
3.不同元素间最本质的区别是()
A.中子数不同B.电子数不同
C.质子数不同D.相对原子质量不同
4.一种元素与另一种元素最根本的区别是()
A.质子数不同B.中子数不同
C.电子数不同D.相对原子质量不同
5.决定元素种类的是()
A.核外电子数B.中子数C.最外层电子数 D.质子数
6.地壳中含量最多的元素是()
A.氧元素B.硅元素C.铝元素D.铁元素
7.地壳中含量最多的元素是()
A.氧B.硅C.铝D.铁
8.元素在自然界里分布并不均匀,如智利富藏铜矿、澳大利亚多铁矿、我国山东富含黄金,但从在整个地壳含量来看,最丰富的金属元素是()
A.O B.Si C.Al D.Fe
9.地壳中含量最多的元素是()
A.铝B.铁C.硅D.氧
10.近日,央视曝光了“镉大米”事件,大米中镉含量严重超标,危害人体健康,其中“镉”指的是()
A.元素 B.原子 C.分子 D.单质
11.在商场的货架上,我们经常看到标有“补钙”、“补铁”、“补锌”等字样的食品和保健品,这里的“钙、铁、锌”指的是()
A.元素 B.分子 C.原子 D.离子
12.地壳中含量最多的元素是()
A.铝B.铁C.氧D.硅
13.目前市场上出售的“加碘食盐”、“高钙牛奶”、“加铁酱油”等,这些碘、钙、铁是指()A.原子 B.单质 C.元素 D.离子
14.6月1号为世界牛奶日.牛奶中的维生素D有助于人体对钙的吸收,这里的钙是指()A.分子 B.原子 C.元素 D.单质
15.日常生活常接触到“高钙牛奶”、“含氟牙膏”等用品,这里的钙、氟指的是()
A.单质 B.原子 C.离子 D.元素
16.化学与人体健康密切相关.市场上有“高钙牛奶”、“含氟牙膏”、“葡萄糖酸锌”等商品,食品名中的“钙、氟、锌”应理解为()
A.分子 B.元素 C.原子 D.单质
17.地壳中含量最多的金属元素是()
A.铝B.钙C.氧D.硅
18.地壳中含量最高的金属元素是()
A.Fe B.Si C.Al D.O
19.地壳中含量最多的元素是()
A.O B.Al C.Si D.Fe
20.地壳中和人体中含量最多的元素是()
A.O B.Si C.Al D.Fe
21.下列说法正确的是()
A.地壳中含量最高的元素是铝元素
B.纯净的空气中,含氧气78%,氦气21%
C.农作物一般适宜在中性或接近中性的土壤中生长,为此常用浓硫酸改良碱性土壤
D.硝酸钾(KNO3)是一种复合肥料,可以提供植物生长必需的K和N两种营养元素
22.决定元素种类的是()
A.质子数B.电子数C.中子数D.最外层电子数
23.地壳中含量最多的金属元素是()
A.氧B.硅C.铁D.铝
24.关于各元素相对含量说法正确的是()
A.地壳中含量最高的元素是氧 B.海洋中含量最高的元素是氯
C.空气中含量最高的元素是碳 D.人体中含量最多的元素是氢
25.下列各组微粒中,属于同一种元素的是()
A.Na+和Ne B.H2O和NH3 C.HF和Ne D.和
26.科学家成功合成了第117号新元素,填补了元素周期表中第116号和118号元素之间的空缺.确定该元素为117号元素的依据是()
A.中子数B.质子数C.电子数D.相对原子质量
27.决定原子种类的是()
A.质子数B.中子数C.电子数D.最外层电子数
28.下列描述错误的是()
A.补钙剂中的钙是指钙元素
B.分子和原子间都有间隔
C.钠原子和钠离子都有相同的化学性质
D.分子和原子都可再分
29.铝元素与人类关系密切.
(1)铝是地壳中含量最高的元素.
(2)元素周期表中铝元素的信息如图所示,其原子的核外电子数为.
(3)铝元素在自然界中主要以Al2O3存在,Al2O3属于(填字母序号).
A.单质 B.氧化物 C.碱 D.盐
(4)工业用电解熔融Al2O3的方法冶炼铝,化学方程式为2Al2O34Al+3O2↑,该反应属于基本反应类型中的反应.
(5)铝可制成蒸锅,主要利用铝的延展性和性.
(6)药品“氢氧化铝[Al(OH)3]”片剂能与胃酸(主要成分为盐酸)发生中和反应,治疗胃酸过多症,该反应的化学方程式为.
30.环境问题是全球关注的热点问题.
(1)我们生活中应使用“无铅汽油”、“无氟冰箱”、“无磷洗衣粉”.这里的“铅、氟、磷”是指
(填“元素”、“物质”或“原子”).
(2)PM2.5是指大气中直径小于或等于2.5微米的颗粒物.请你列举一个能引起大气中PM2.5增加的例子.
(3)汽车使用压缩天然气作燃料可减少尾气污染.天然气燃烧的化学方程式为.
(4)请你再提出一条防治环境污染的方法.
参考答案
一、选择题
1.A;2.B;3.C;4.A;5.D;6.A;7.A;8.C;9.D;10.A;11.A;12.C;13.C;14.C;15.D;16.B;17.A;18.C;19.A;20.A;21.D;22.A;23.D;24.A;25.D;26.B;27.AB;28.C
二、填空题
29.金属;13;B;分解;导热;Al(OH)3+3HCl═AlCl3+3H2O;30.元素;煤燃烧;CH4+2O2CO2+2H2O;使用太阳能。
