6-磷酸葡萄糖酸脱氢酶活性测定试剂盒使用说明
牛葡萄糖6磷酸脱氢酶(G6PD)elisa试剂盒说明书

牛葡萄糖6磷酸脱氢酶(G6PD)elisa试剂盒说明书牛葡萄糖6磷酸脱氢酶(G6PD)elisa试剂盒说明书elisa试剂盒常见组成部分:1)酶和底物:在ELISA中zui常用的酶为HRP和ALP。
2)抗体:在ELISA中应用的抗体可分为多克隆抗体(多抗)和单克隆抗体(单抗)。
3)抗原:在ELISA中应用的抗原要求有较高的特异性、亲和力和纯度。
主要有三类,即自然抗原、人工合成抗原和基因重组抗原。
4 人E选择素(ESelectin/CD62E)检测试剂盒包被:将免疫活性物质(抗原或抗体)结合于固相载体上的过程称为包被。
常用的材料有聚苯乙烯、硝酸纤维薄膜等;常用的方法有吸附法、化学交联法及亲和素生物素间接包被法5)固相载体:固相载体是ELISA中用以分离结合标记物和游离标记物的主要手段,应与各种免疫活性物质有良好的结合性能并且不改变其免疫活性。
常用的固相载体有聚苯乙烯塑料和硝酸纤维素膜。
牛葡萄糖6磷酸脱氢酶(G6PD)elisa试剂盒样本实验前准备:ELISA试剂盒液体样本:包括血清、血浆、尿液、胸腹水、脑脊液、细胞培养上清等。
(1)血清室温血液自然凝固1020分钟后,离心20分钟左右(20003000转/分)。
仔细收集上清。
保存过程中如有沉淀形成,应再次离心。
(2)血浆:应根据标本的要求选择EDTA、柠檬酸钠或肝素作为抗凝剂,混合1020分钟后,离心20分钟左右(20003000转/分)。
仔细收集上清。
保存过程中如有沉淀形成,应再次离心。
(3)尿液:用无菌管收集。
离心20分钟左右(20003000转/分)。
仔细收集上清。
保存过程中如有沉淀形成,应再次离心。
胸腹水、脑脊液参照此实行。
(4)细胞培养上清:检测分泌性的成份时,用无菌管收集。
离心20分钟左右(20003000转/分)。
仔细收集上清。
(5)培养细胞检测细胞内的成份时,用PBS(PH7.27.4)稀释细胞悬液,细胞浓度达到100万/ml左右。
葡萄糖-6-磷酸酶(G6P)试剂盒使用说明

葡萄糖-6-磷酸酶(G6P)试剂盒使用说明分光光度法货号:BC0930规格:50管/48样产品内容:提取液:60mL×1瓶,4℃保存;试剂一:液体47.5mL×1瓶,4℃保存;试剂二:粉剂×1支,-20℃保存;试剂三:粉剂×1支,-20℃保存;试剂四:液体×1支,-20℃保存;产品说明:葡萄糖-6-磷酸酶((glucose6phosphatase,G6Pase,EC3.1.3.9)广泛存在于动物、植物、微生物和细胞中,是糖异生过程水解葡萄糖-6-磷酸生成葡萄糖的限制酶,在保证血糖的动态平衡方面起着重要的作用。
G6P催化葡萄糖-6-磷酸生成葡萄糖,变旋酶和葡萄糖脱氢酶进一步依次催化NAD+还原生成NADH,在340nm下测定NADH生成速率,即可反映G6P活性。
需自备的仪器和用品:紫外分光光度计、台式离心机、可调式移液器、1mL石英比色皿、研钵、冰和蒸馏水。
操作步骤:一、样本的前处理:1、细菌或培养细胞:先收集细菌或细胞到离心管内,离心后弃上清;按照细菌或细胞数量(104个):提取液体积(mL)为500~1000:1的比例(建议500万细菌或细胞加入1mL提取液),超声波破碎细菌或细胞(冰浴,功率20%或200W,超声3s,间隔10s,重复30次);8000g4℃离心10min,取上清,置冰上待测。
2、组织:按照组织质量(g):提取液体积(mL)为1:5~10的比例(建议称取约0.1g组织,加入1mL提取液),进行冰浴匀浆。
8000g4℃离心10min,取上清,置冰上待测。
3、血清(浆)样品:直接检测。
二、测定步骤:1、分光光度计预热30min以上,调节波长至340nm,蒸馏水调零。
工作液的配制:临用前将试剂二、试剂三和试剂四转移到试剂一中混合待用;用不完的试剂4℃保存一周;2、将工作液置于37℃(哺乳动物)或25℃(其它物种)预热5分钟。
3、在1mL石英比色皿中加入50μL样本和950μL工作液,立即混匀,记录340nm处初始吸光值A1和2min后的吸光值A2,计算ΔA=A2-A1。
SIGMA 葡萄糖HK检测试剂盒说明书

SIGMA 葡萄糖HK 检测试剂盒说明书(Glucose (HK) Assay Kit; Product Code GAHK -20)一、产品介绍食品、生化和制药业普遍将酶作为分析工具。
酶法具有特异性高、重现性好、敏感性高以及反应快速的特点,是用于分析的理想工具。
由于酶具有高的特异性和敏感性,所以不需样品制备即可进行定量分析。
本试剂盒以酶法定量测定食品和其他材料中的葡萄糖。
原理:葡萄糖+ATP Hexokinase→ 6-磷酸葡萄糖+ADPG6P+NAD G6PDH → 6-磷酸葡萄糖酸+NADH葡萄糖在己糖激酶催化反应中被A TP 磷酸化,然后G6P 在NAD 存在下被6-磷酸葡萄糖脱氢酶催化,氧化为6-磷酸葡萄糖酸;反应中,等分子量的NAD 被还原为NADH 。
随后的340nm 吸光度的增加与葡萄糖含量成正比。
二、试剂组成1、葡萄糖检测试剂用20ml 水溶解小瓶内粉剂;加水后立即盖紧瓶塞,反转混匀数次,不可震动。
加水20ml 溶解后,每瓶溶液含有1.5 mM NAD ,1.0 mM ATP ,1.0 U/ml G6PDH ;并含有防腐剂苯甲酸钠和山梨酸钾。
小瓶粉剂保存于2-8℃。
如果粉剂受潮结块、加水不能充分溶解、或水溶液浑浊,则应将试剂弃用。
试剂水溶液比较稳定,18-26℃保存7天、2-8度保存4周不会有微生物生长。
以水作为空白参照,新配置的溶液340nm 吸光度如果大于0.350,则溶液不适合使用。
2、葡萄糖标准溶液D -葡萄糖,1.0mg/ml 溶于0.1%苯甲酸;该标准液为即用型,符合美国国家标准技术研究所标准;2-8℃可至少保存半年。
期间如果溶液浑浊,则应弃用。
三、需自备的实验仪器1、可测定340nm 吸光度的分光光度计2、测量杯3、10μl -1ml 量程的移液器四、注意事项和免责声明本试剂仅供科研使用,不能用于药品、家庭以及其他用途。
涉及危害和使用安全性问题,参照材料安全数据表。
葡萄糖-6-磷酸检测标准

葡萄糖-6-磷酸检测标准葡萄糖-6-磷酸(G6PD)缺乏是遗传性的红细胞缺陷,影响到葡萄糖代谢。
该缺陷可能会在接触到某些药物、疾病或环境压力后导致溶血性贫血。
因此,对G6PD缺乏的筛查尤为重要,而G6PD缺乏筛查的标准就是G6PD检测。
G6PD检测是通过分析红细胞中G6PD酶活性来确定G6PD缺乏。
下面将会介绍G6PD检测的标准方法。
1. G6PD活性检测G6PD活性检测是最常见的G6PD检测方法,它的思路是测量红细胞中G6PD酶的活性。
常用的测量方法有酵母三磷酸脱氢酶(yeast triosephosphate dehydrogenase)法和比色法。
酵母三磷酸脱氢酶法的原理是比较待测血液与正常血液在同一时间内对酵母三磷酸脱氢酶活性的变化,然后计算G6PD酶活性。
比色法是根据G6PD酶的还原剂作用来测量NADP/H的形成。
在进行G6PD活性检测的时候,需要注意以下几点:1)对于新生儿,G6PD酶活性会在出生后数日内升高,因此最好在出生后1个月后再测量。
2)血液抽取应注意避免对红细胞的损伤,通常采用静脉抽血或经表皮血流动力学监测系统(EMLA)麻醉后进行皮下抽血。
3)使用酶活性仪分析,不同仪器标准、笔头、反应体积等有较大影响,不同仪器的测量结果并不一致。
2.基因检测基因检测是另一种诊断G6PD缺乏的方法,其思路是检测G6PD基因的序列或突变。
现代基因检测技术使得这种方法越来越准确和可靠。
基因检测的优点是能够检测到隐性G6PD缺乏,而基于酶活性的检测方法无法检测到隐性缺陷。
此外,基因检测也更能够指导个性化的治疗计划。
3.红细胞形态学检测红细胞形态学检测是另一种筛查G6PD缺乏的方法。
红细胞在G6PD 缺乏的情况下更容易受损或产生微小的有色附着物质。
通过检查血涂片上红细胞的形态和有色附着物质,就可以初步判断是否存在G6PD缺乏的可能性。
在实际检测中,红细胞形态学检测通常与G6PD活性检测或基因检测结合使用,以增强诊断准确性。
小鼠葡萄糖 6磷酸脱氢酶 (G6PD) 酶联免疫分析试剂盒 使用说明书

小鼠葡萄糖6磷酸脱氢酶(G6PD)酶联免疫分析试剂盒使用说明书产品编号:E0716m10. 终止液:1×10ml/瓶(2N H2SO4)。
11. 覆膜:5张12. 使用说明书:1份自备物品1. 酶标仪(建议参考仪器使用说明提前预热)2. 微量加液器及吸头,EP管3. 蒸馏水或去离子水,全新滤纸标本的采集及保存1. 血清:全血标本请于室温放置2小时或4℃过夜后于1000 x g离心20分钟,取上清即可检测,或将标本放于-20℃或-80℃保存,但应避免反复冻融。
2. 血浆:可用EDTA或肝素作为抗凝剂,标本采集后30分钟内于2 - 8° C 1000 x g离心15分钟,或将标本放于-20℃或-80℃保存,但应避免反复冻融。
3. 其它生物标本:请1000 x g离心20分钟,取上清即可检测,或将标本放于-20℃或-80℃保存,但应避免反复冻融。
注:以上标本置4℃保存应小于1周,-20℃或-80℃均应密封保存,-20℃不应超过1个月,-80℃不应超过2个月;标本溶血会影响最后检测结果,因此溶血标本不宜进行此项检测。
操作步骤实验开始前,各试剂均应平衡至室温(试剂不能直接在37℃溶解);试剂或样品稀释时,均需混匀,混匀时尽量避免起泡。
实验前应预测样品含量,如样品浓度过高时,应对样品进行稀释,以使稀释后的样品符合试剂盒的检测范围,计算时再乘以相应的稀释倍数。
1. 加样:分别设空白孔、标准孔、待测样品孔。
空白孔加样品稀释液50μl,余孔分别加标准品或待测样品50μl,注意不要有气泡,加样将样品加于酶标板孔底部,尽量不触及孔壁。
为保证实验结果有效性,每次实验请使用新的标准品溶液。
2. 立即在每个孔中加入检测溶液A工作液50μl(在使用前半小时内配制),轻轻晃动混匀,酶标板加上覆膜, 37℃反应60分钟。
3. 弃去液体,甩干,洗板3次。
每次浸泡1-2分钟,大约400μl/每孔,甩干(也可轻拍将孔内液体拍干)。
葡萄糖-6-磷酸脱氢酶(G6PD)检测试剂盒(简易比色法)

葡萄糖-6-磷酸脱氢酶(G6PD)检测试剂盒(简易比色法)葡萄糖-6-磷酸脱氢酶(G6PD)检测试剂盒(简易比色法)简介:葡糖-6-磷酸脱氢酶( glucose 6-phosphatedehydrogenase ,G-6-PD 或G6PD)是糖酵解途径、柠檬酸循环以外的另一个葡萄糖分解途径的磷酸葡萄糖酸途径(磷酸戊糖途径)中的第一个酶(EC1.1.1.49)。
Leagene 葡萄糖-6-磷酸脱氢酶(G6PD)检测试剂盒(简易比色法)其检测原理是红细胞G-6-PD 催化葡萄糖-6-磷酸葡萄糖-内酯,后者很快氧化成6-磷酸葡萄糖酸(6-PGA),同时NAPD 被还原成NADPH ,其反应公式如下:G-6-P+NAPD +→6-PGA +L-NADPH 。
在上述偶联反应中,NADPH 生成速率与样本中酶活性呈正比,通过分光光度计或自动分析仪检测吸光度上升速率(ΔA /min),上升速率(ΔA /min)与G-6-PD 活性呈正比,比色杯光径1.0cm ,直接计算酶的活性单位。
100T 该试剂盒试剂可以检测50次样本,该试剂盒仅用于科研领域,不宜用于临床诊断或其他用途。
组成:自备材料:1、生理盐水2、水浴锅3、比色杯4、分光光度计操作步骤(仅供参考):1、预备溶血液:取新奇抗凝血,离心取上清及白细胞层,用4℃预冷的生理盐水洗涤,每次取上清时,务必去除剩余的白细胞层,再加预冷的生理盐水配成含红细胞压积为30%的红细胞悬液,4℃保存备用。
临用前,以样本稀释液稀释,即为溶血液。
4℃保存10h ,编号名称TE0085 100TStorage试剂(A): 样本稀释液100ml -20℃ 避光试剂(B): G6PD assay buffer 100ml 4℃ 试剂(C): NADP 18mg -20℃ 试剂(D): G-6-P 1支-20℃ 试剂(E): G-6-P 稀释液10mlRT 使用说明书1份-20℃保存48h。
生化分析仪直接测定葡萄糖-6-磷酸脱氢酶活性的临床应用

个 关键 酶 , 催 化反 应 生成 的还 原 型 辅 酶 Ⅱ 其
《 国临床检验操 作规 程》 全 中介 绍的 高铁 血红蛋 白还 原 试验操 作规程 执行 。取 还原 率小 于 7 %为缺乏 。 5
7 % 一8 %为可 疑 。大 于 8 %为正 常 。 5 0 0
使用 的试 剂盒。批 号:080 。( ) 一D 6P D 2001 3 G6P / G 比值法试 剂 采 用 广州 米 基 科技 有 限公 司生 产 的 试
剂盒 。批号 :7 180 。取 比值 <0 9 0 0 1—1 .5为 缺乏 。 比
1 1 材料 .
123 高铁血红蛋白还原试验的实验方法 ..
按照
中华人 发共和 国卫生 部 医政 司 的《 国临 床检 验操 全
111 仪 器 日本 日立一00全 自动 生 化分 析 仪 , .. 78
日本 岛津分光光 度计 。
作规程》 中介绍的高铁血红蛋白还原试验操作规程
执行。
比值法等 。这些 方 法存 在试 剂 稳 定性 差 、 作 步 骤 操
繁琐 、 为影 响 因素 多 、 人 且不 能直 接 测 定 G 6P -一D的 活性等 不足 。本 文 以长春汇力生 物技 术有 限公 司提
供 的试 剂盒检 测血 中 G6P 性 , -一D活 为临 床提 供一 种
简单 、 速 、 快 准确 , 直接 检测 血中 G 6P 能 -一D活性 浓 度 ( /' ) U oI 的方法 , - b 现报告 如下 。 1 材 料与 方法
2 1 同时用3 方法对 4 1 . 种 5 例标 本 进行检 测
见 表 1 。
6-磷酸葡萄糖酸检测

迪信泰检测平台
6-磷酸葡萄糖酸检测
6-磷酸葡萄糖酸(6-Phosphogluconic acid)是戊糖磷酸途径与恩特纳–杜德洛夫途径中的一种中间代谢产物,由6-磷酸葡萄糖酸内酯酶生成,并被磷酸葡萄糖酸脱氢酶作用以产生核酮糖5-磷酸。
6-磷酸葡萄糖酸也可以被6-磷酸葡萄糖酸脱水酶作用而产生2-酮, 3-脱氧-6-磷酸葡萄糖酸。
迪信泰检测平台采用液相质谱联用(LC-MS)的方法,使用Thermo Scientific的
U3000快速液相色谱对样品进行分离,Thermo Scientific™ Q Exactive™对样品进行鉴定,可高效、精准的检测6-磷酸葡萄糖酸的含量变化。
此外,我们还提供其他糖酵解类物质检测服务,以满足您的不同需求。
LC-MS测定6-磷酸葡萄糖酸样本要求:
1. 请确保样本量大于0.2g或者0.2mL。
周期:2~3周。
项目结束后迪信泰检测平台将会提供详细中英文双语技术报告,报告包括:
1. 实验步骤(中英文)。
2. 相关参数(中英文)。
3.质谱图片。
4. 原始数据。
5. 6-磷酸葡萄糖酸含量信息。
迪信泰检测平台可根据需求定制其他物质测定方案,具体可免费咨询技术支持。
葡萄糖检测试剂盒(O-toluidine 法) 产品说明书

葡萄糖检测试剂盒(O-toluidine法)产品编号 产品名称包装 S0201S 葡萄糖检测试剂盒(O-toluidine 法) 200次 S0201M葡萄糖检测试剂盒(O-toluidine 法)1000次产品简介:葡萄糖检测试剂盒(O-toluidine 法) (Glucose Assay Kit with O-toluidine)是一种基于葡萄糖与邻甲苯胺的显色反应,通过比色法超高灵敏度、超宽线性范围检测血清、血浆、尿液、细胞或组织裂解液、饮料等溶液中葡萄糖含量的试剂盒。
本试剂盒灵敏度高、线性范围极宽、使用便捷。
本试剂盒对于在5-10,000mg/dl (相当于约0.28-550mM)范围的葡萄糖内有良好线性,并且具有操作便捷、显色稳定、无需煮沸、成本低、适合高通量检测等优点。
本试剂盒检测下限可以达到5mg/dl (20µl 样品),相当于50ng/ml 或278µM ;检测上限可以达到2000mg/dl (5µl 样品)或10,000mg/dl (1µl 样品),相当于20mg/ml (约111mM)或100mg/ml (约555mM)。
本试剂盒既可以轻松检测正常血样中的葡萄糖浓度,也可以检测高血糖血样品。
市售常见血糖仪的葡萄糖浓度检测范围约为1-30mM ,相当于约20-600mg/dl ,在检测一些过高血糖或过低血糖样品时会存在困难,而本试剂盒提供了5-10,000mg/dl (相当于约0.28-550mM)极宽的葡萄糖浓度检测范围。
本试剂盒所需样品体积小。
本试剂盒推荐的样品用量为5-20µl ,也可以使用如1-2µl 或更小体积的样品。
本试剂盒特异性好。
与常用的葡萄糖氧化酶-过氧化酶偶联(GOD-POD)法相比,由于邻甲苯胺试剂只与醛糖显色,且不受其它还原性物质的影响,本试剂盒非常适合血清、尿液等溶液中葡萄糖浓度的检测。
葡萄糖(glucose),也被称为dextrose 或grape sugar ,被认为是自然界中分布最广且最为重要的一种单糖。
葡萄糖-6-磷酸检测标准

葡萄糖-6-磷酸检测标准
1. 试验原理:葡萄糖-6-磷酸酶催化葡萄糖-6-磷酸在存在
NADP+的条件下转化成6-磷酸葡萄糖和NADPH。
在一定温
度下,葡萄糖-6-磷酸浓度与生成的NADPH的光密度成正比。
2. 试剂准备:葡萄糖-6-磷酸酶混合物、缓冲液、NADP+、葡
萄糖-6-磷酸标准品。
3. 方法步骤:
(1)将标准品加入每个反应管中,加入缓冲液至总体积1ml。
(2)加入葡萄糖-6-磷酸酶混合物,混匀。
(3)在37℃恒温水浴中孵育10min,停止反应。
(4)加入1ml NADP+,混匀。
(5)在340nm波长下测定产生的NADPH的吸光度,作为光
密度读数。
(6)使用标准品测出样品中葡萄糖-6-磷酸的含量,并计算出
样品中葡萄糖-6-磷酸浓度。
4. 检测范围和灵敏度:检测范围为0.001-10mg/L,在最佳实验条件下,灵敏度为0.001mg/L。
5. 质量控制:在每次检测前,应首先测定内部标准,如标准品
和阳性对照,以确保试剂和设备的正常运行。
同时,每次检测均应伴有负对照(即不含葡萄糖-6-磷酸的样品)的检测结果以防止假阳性的发生。
葡萄糖6磷酸脱氢酶(G6PD)试剂盒性能验证

中国卫生标准管理CHSM 373葡萄糖-6-磷酸脱氢酶(Glucose-6-phosphate Dehydrogenase,G6PD)缺乏常见于我国长江流域及其以南各省[1],福建省也属于高发区域,其是红细胞磷酸戊糖代谢途径中的一个关键酶,其催化反应生成的还原型辅酶Ⅱ(NADPH)是谷胱甘肽还原酶的辅酶,宫颈癌诊断中的意义[J]. 中国实验诊断学,2017,21(10):1708-1710.[10] Dasari S,Wudayagiri R,Valluru L. Cervical cancer:Biomarkersfor diagnosis and treatment[J]. Clin Chim Acta,2015,445:7-11.[11] Zhi W,Ferris D,Sharma A,etal. Twelve serum proteinsprogressively increase with disease stage in squamous cell cervical cancer patients[J]. Gynecol Cancer,2014,24(6):1085-1092.[12] 李群,刘淑玉,刘红丽,等. 血清鳞状细胞癌抗原水平变化在诊断子宫颈鳞癌复发中的临床意义[J]. 中华妇产科杂志,2015,50(2):131-136.[13] 王静,郑群,余素飞,等. Logistic 回归联合分类树CHAID 法建立SCC 在宫颈癌中的辅助诊断模型[J]. 中华检验医学杂志,2015,38(11):761-764.[14] Xu F ,L i Y ,F an L,et al. Pr eoperat ive SCC-A g andthrombocytosis as predictive markers for pelvic lymphatic metastasis of squamous cervical cancer in early FIGO stage[J]. Cancer,2018,9(9):1660-1666.[15] 罗业琳,雷嘉,黄卓华. 联合检测血清 SCC、CEA、CA125、CA199在宫颈癌诊断中的价值[J]. 临床合理用药杂志,2016,9(13):137-138.[16] 梁指荣,杨洁飞,苏锡康. 多种肿瘤标记物检测在宫颈癌诊治中的意义[J]. 国际检验医学杂志,2016,37(1):21-23.作者单位:厦门市妇幼保健院医学检验科,福建 厦门 361003张炎胜 陈婷婷 甘月滨 张福辉【摘要】目的 评价葡萄糖-6-磷酸脱氢酶(G6PD)试剂盒是否可应用于临床检测。
6-磷酸-葡萄糖脱氢酶(G6PDH)、苹果酸酶(ME)两种酶酶活测定方法

6-磷酸-葡萄糖脱氢酶(G6PDH)、苹果酸酶(ME)两种酶酶活测定方法(1)6-磷酸-葡萄糖脱氢酶(G6PDH)活力测定6-磷酸-葡萄糖脱氢酶(G6PDH)活力测定方法根据文献略有改动6979。
测定反应体系(5ml)为:0.1mI浓度为1M的Tris-HCl缓冲液、0.1ml 浓度为25mM的底物G-6-P溶液、0.1ml浓度为2mM的NADP+、0.1ml 浓度为0. 2 M的氯化镁溶液及2.5ml ddH20,混合均匀后,在340 nm 下测定吸光度值A0,作为空白值。
再加入0.1 ml粗酶液,摇匀后,与25℃条件下保温,每30S于340 nm下测定吸光度值A,连续测定4 min。
以A对时间作图,取反应最初线性部分计算△A值。
根据公式计算酶活力。
酶活力单位(U)定义为:25℃条件下,每分钟G6PDH催化生成1μmol NADH的酶量为一个单位。
式中:△A/min为340 nm处每分钟吸光度的变化值;V为酶促反应体积(mL);为NADH的摩尔消光系数(6.22×103L/mol·cm-1);b 为比色皿光程(cm)。
(2)苹果酸酶(ME)活力测定测定反应体系(3ml)为:0.5 mI浓度为0.4 M的Tris-HCl缓冲液、0.1 ml 浓度为30 mM的底物苹果酸溶液、0.2ml浓度为3.4 mM的NADP+、0.1ml浓度为0.12 M的氯化镁溶液及2 ml ddH20,混合均匀后,在340 nm下测定吸光度值A0,作为空白值。
再加入0.1 ml粗酶液,摇匀后,与250C条件下保温,每30s于340 nm下测定吸光度值A,连续测定4 min。
以A对时间作图,取反应最初线性部分计算△A值。
根据公式2-1计算酶活力。
酶活力单位(U)定义为:25℃条件下,每分钟ME催化生成1μmol NADH的酶量为一个单位。
定量比值法测定葡萄糖-6-磷酸脱氢酶活性的实验评价

・
检 验 与 临 床・
定 量 比值 法 测 定 葡 萄糖 一 一 酸 脱 氢 酶 活 性 6磷 的实 验 评 价
谭 晓 明 张 小玲 杨 丽媛 容莉 莉
摘 要 目的: 定量比值 法检 测葡萄糖一 一 酸脱 氢酶 ( 6 D) 对 6磷 G P 活性 的方法进行 实验评 价 方法 : 日立 7 0 用 60 型 生化分析仪 对改 良 G P 6 D定量 比值 法试 剂盒进行 精 密度 、 线性 、 干扰和 稳定性 实验 。 该方 法作 出评 价 结果 : 对
稳定性 能都 较好 , 能够 满足 临床 常规检 验的 需要 , 适合 常规推广使 用 关键词 葡糖磷 酸脱氢酶 ; 6 G 比值 ; 酶活性 ; 线性 ; 干扰 P D;
红细胞 葡 萄糖一 6一磷 酸 脱 氢 酶 (lcs.. guoe6
测 定 6 G 活性 ( , 过 两 个 酶 的 活 性 比值 计 算 A PD B)通
popa eyr eaeG P ) hsht dhd gns, 6 D 是磷 酸戊 糖旁路 中产 e o 生还原 型辅酶 Ⅱ( A P N D H)的关键酶。以 G P 6 D基 因 突 变 为分 子 基 础 的 G P 6 D缺 陷症 是 最 常 见 的 x连 锁 遗传 病 。全 球 G P 6 D缺 乏 者 高 达 4亿 以上 , 人 群 发 其 生率呈 明显的地域性 ,我国以广东省发生率最高[。 2 世纪 8 0 0年代 以前 G P 6 D缺 陷症 的筛查 方 法 已达 1 种[。 3 近年又有新 的方法应用 于临床 。 现阶段 主要 的检测方法有定量 比值法 、 紫外分 光光度法 、 高铁血 红蛋 白还 原 法 , 以及 基 因检 测 等 [。 目前 定 量 比值 法 = I ] GP 6 D测定试剂盒 已在临床上得到使用 ,因此我们对 定 量 比值 法测 定 G P 6 D酶活性 方法 进行 实验评 价 , 具体报告如下 。
6-磷酸葡萄糖酸脱氢酶(6PGDH)活性检测试剂盒说明书__微量法UPLC-MS-4359
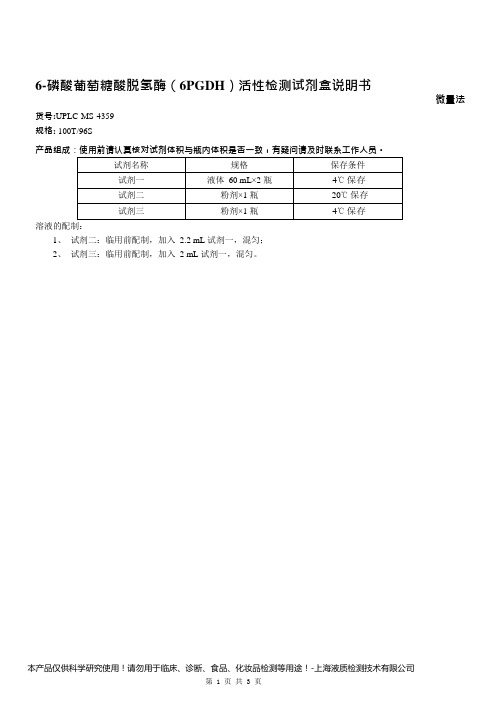
6-磷酸葡萄糖酸脱氢酶(6PGDH)活性检测试剂盒说明书微量法货号:UPLC-MS-4359规格: 100T/96S产品组成:使用前请认真核对试剂体积与瓶内体积是否一致,有疑问请及时联系工作人员。
溶液的配制:1、试剂二:临用前配制,加入2.2 mL 试剂一,混匀;2、试剂三:临用前配制,加入2 mL 试剂一,混匀。
产品说明:磷酸戊糖途径途径中6-磷酸葡萄糖脱氢酶(G6PDH)和6-磷酸葡萄糖酸脱氢酶(6PGDH)依次催化NADPH 合成,与能量的平衡、生长速率和细胞活力等密切相关。
此外,6PGDH 逆境生理中具有重要作用。
6PGDH 催化6-磷酸葡萄糖酸和NADP+生成NADPH,NADPH 在340nm 有特征吸收峰,而NADP+没有;通过测定340nm 吸光度增加速率,计算6PGDH 活性。
注意:实验之前建议选择2-3 个预期差异大的样本做预实验。
如果样本吸光值不在测量范围内建议稀释或者增加样本量进行检测。
需自备的仪器和用品:低温离心机、水浴锅、可调式移液枪、紫外分光光度计/酶标仪、微量石英比色皿/96 孔UV 板、研钵/匀浆器、蒸馏水。
操作步骤:一、样本处理(可适当调整待测样本量,具体比例可以参考文献)称约0.1g 组织,加入1mL 试剂一,冰上充分研磨,10000rpm 4℃离心10min,取上清粗酶液,待测。
二、测定步骤1.紫外分光光度计/酶标仪预热30min 以上,调节波长到340nm,蒸馏水调零。
2.试剂一置于37℃水浴预热30min 以上。
3.于340nm 处测定3min 内吸光值变化,第0s 吸光值记为A1,第180s 吸光值记为A2。
记ΔA 测定=A2 测定-A1 测定,ΔA 空白=A2 空白-A1 空白。
三、6PGDH 活性计算a.使用微量石英比色皿测定的计算公式如下(1)按蛋白浓度计算活性单位定义:每毫克蛋白每分钟催化产生1nmol NADPH 的酶量为1 个酶活单位。
6PGDH 酶活性(U/mg prot) =[(ΔA 测定-ΔA 空白)×V 反总÷(ε×d)×109]÷(Cpr×V 样)÷T=536×(ΔA 测定-ΔA 空白)÷Cpr(2)按样本质量计算活性单位定义:每克组织每分钟催化产生1nmol NADPH 的酶量为1 个酶活单位。
葡萄糖-6-磷酸脱氢酶试验

指导葡萄糖-6-磷酸脱氢酶的测定。
【该SOP变动程序】本标准操作程序的改动可由任一使用本SOP的工作人员提出,并报经下述人员批准签字:专业主管、质控主管、科主任。
【检验的适应证】可用于G-6-PD缺乏症高发地区对蚕豆病进行普查普防,在高疟地区对需要服抗疟药的对象进行G-6-PD缺乏症的筛选,防止药物性溶血的发生。
【仪器与试剂】1.仪器:电热恒温水浴箱、离心机、紫外分光光度计。
2.试剂:2.1 Tris-HCI-EDTA缓冲液。
2.2 0.1mol/L氯化镁溶液。
2.3 2mmol/LNADP2.4 6mmol/L葡萄糖-6-磷酸二钠2.5 6mmol/L-磷酸葡萄糖酸【操作程序】加入物 6-PGD测定 6-PGD+G-6-PD测定1(U) 2(B) 3(U) 4(B)Tris-HCL-EDTA缓冲液0.3 0.3 0.3 0.3MgCl2溶液 0.3 0.3 0.3 0.3NADP﹢溶液 0.3 0.3 0.3 0.3溶血液 0.06 0.06 0.06 0.06蒸馏水 1.74 2.04 1.44 2.04混匀,置37℃水浴10分钟G6P溶液 0.36-PGA溶液0.3 0.3根据每升血液每分钟催化反应产生1umol的NADPH为1个国际单位,换算成每克血红蛋白的酶活力。
先分别求6-PGD及(6-PGD+G-6-PD)的活力,再求G-6-PD 的活力。
8040酶活力(U/gHb)=△Amin×——Hb(g/L)G-6-PD活力=(6-PGD+G-6-PD)-6-PGD【参考值范围及报告单】G-6-PD活力(已校正6-PGD)=8.34±1.59U/ gHb(37℃)G-6-PD活力(未校正6-PGD)=12.1±2.09 U/ gHb(37℃)【葡萄糖-6-磷酸脱氢酶测定的注意事项】1.溶血液制备:取新鲜抗凝血离心去上清及白细胞层,用生理盐水洗涤两次,再加盐水使压积红细胞约为30%,将此红细胞悬液置冰水备用。
葡萄糖-6-磷酸脱氢酶三种测定方法的比较

3 参 考 范 围 :1G6 D酶 活 性 测 定 : 人 G P 活性 13 0 . () P 成 6D 0
3 6 0U/ 新 生 儿 G6 D活 性 2 5 0 58 0 U/ ; 2 改 良 0 L; P 0 ~ 0 L ( )
G6 D 定 量 比值 法 。 现 将 我 科 使 用 的三 种 方 法 进 行 对 比试 验 , P
并进行评价 , 报道 如 下 。 资 料 与 方 法 1 标 本 来 源 : 择 我 院 门诊 育龄 夫妇 和住 院新 生 儿 血 标 本 . 选 共 4 0例 , 中成 年 男 性 血 标 本 14例 , 性 成 年 血 标 本 14 8 其 8 女 8
维普资讯
国 际检验 医学杂志 20 年 7 第 2 卷 第 7期 07 月 8
It a n 2
・6 63 ・
・
经 验 交 流
・
葡 萄糖一一 酸 脱氢 酶 三种 测 定 方 法 的 比较 6磷
G6 D定 量 比值 法 : P 成人 1 0 ~ 1 6 , < 1 O . 0 .7 如 . 0则 为 G6 D缺 P
乏 ; 带血 】 】 2 3 ( ) 铁 血 红 蛋 白 还 原 试 验 : 常 人 > 脐 . ~ . ;3 高 正 7 ,1 ~ 7 % 为 杂合 子 , 3 纯 合 子 。 5 3 4 ( 1 . 0 4为
【 键 词 】 葡糖 磷 酸脱 氢 酶 ; 高 铁 血 红 蛋 白 ; 实 验 室 技 术 和 方 法 关
中 图 分 类号 : 4 6 1 2 R 4 .1’ 文献标识码 : B 文章 编 号 : 6 34 3 ( 0 7 0 — 6 — 2 1 7 — 1 0 2 0 ) 76 30
新生儿葡萄糖-6-磷酸脱氢酶定量测定(实验注意事项)

Neo-G6PD定量测定试剂盒实验步骤及注意事项1. 试剂的准备G6PD底物试剂(复溶后+2~+8℃稳定一月):在每个冻干的G6PD底物试剂小瓶中加入11ml G6PD复溶缓冲液(配制后的溶液为1个96微孔板用量),轻轻混匀。
2. 将所需数量的空白反应条(白色不透明板)置室温平衡( 23-28℃,30分钟)。
注意事项及建议:本实验受温度影响,在一定范围内随温度的提高,反应加快。
平衡温度可保证实验反应的均一性3. 用打孔器轧下校准品、质控品和待测样品的滤纸干血片(每片直径3.0 mm左右),按顺序放入微孔反应条小孔中,然后各孔加入100 μl 复溶G6PD底物试剂,盖上封片,室温慢速振动孵育30分钟。
注意事项及建议:(a)用自动打孔器轧下滤纸干血片取样时,应尽量向中间靠拢,避免取边缘血片而造成检测时CV值增大(血片中心到边缘的1/2以内区域是检测的最佳部位)。
每个校准品滤纸干血片打孔最好不要多于4个;(b)尽量避免手接触血片,以免造成血片污染4. 每孔加铜试剂200 μl,并加贴封条,室温无振动孵育。
注意事项及建议:加铜试剂时,吸头应悬空,避免因吸头碰到小孔边缘或其中试剂而造成铜试剂污染5. 15~20分钟内,在激发波长355nm,发射波长460nm时测定荧光值。
注意事项及建议:(a)血片漂浮对G6PD测定将造成影响,测定荧光值前请用小镊子或者大头针将漂浮血片挑出后再检测,以免造成假阳性结果;(b)质控品在受控范围内,反之,则该次实验无效,应重复实验;(b)务必在15~20分钟内检测完毕,否则曲线会漂移。
其他:(1)不同批号的试剂盒不要混用。
(2)本试剂盒各组分只能一次性使用,不能重复使用(3)为了避免样本中任何潜在的生物危险,检测样本应视为具有传染性物质,避免接触到皮肤和粘膜。
葡萄糖含量试剂盒使用说明(测组织、细菌或细胞)

葡萄糖含量试剂盒说明书(测组织、细菌或细胞)使用说明分光光度法正式测定前务必取2-3个预期差异较大的样本做预测定货号:BC2500规格:50管/48样产品内容:试剂一:0.5μmol/mL葡萄糖溶液10mL×1瓶,4℃保存;试剂二:液体25ml×1瓶,4℃保存;试剂三:液体25ml×1瓶,4℃保存;产品说明:葡萄糖不仅是细胞能量代谢的主要底物,而且其代谢中间产物是生物合成的重要底物。
植物可通过光合作用产生葡萄糖。
就哺乳动物而言,葡萄糖不仅是大脑神经系统、肌肉、脂肪组织等的唯一能源,而且与还原性辅酶、乳糖和乳脂的合成密切相关。
葡萄糖氧化酶催化葡萄糖氧化成葡萄糖酸,并产生过氧化氢;过氧化物酶催化过氧化氢氧化4-氨基安替比林偶联酚,生成有色化合物,在505nm有特征吸收峰。
需自备的仪器和用品:可见分光光度计、水浴锅、可调式移液器、1mL玻璃比色皿、研钵和蒸馏水操作步骤:一、葡萄糖提取:1、组织的处理:按照组织质量(g):蒸馏水体积(mL)为1:5~10的比例(建议称取约0.1g组织,加入1mL蒸馏水),研磨成匀浆,95℃水浴10分钟(盖紧,防止水分散失),冷却后,8000g,25℃离心10min,取上清液备用。
2、细菌或细胞处理:收集细菌或细胞到离心管内,离心后弃上清;按照细菌或细胞数量(104个):蒸馏水体积(mL)为500~1000:1的比例(建议500万细菌或细胞加入1mL蒸馏水),超声波破碎细菌或细胞(冰浴,功率20%或200W,超声3S,间隔10S,重复30次),95℃水浴10分钟(盖紧,防止水分散失),冷却后,8000g,25℃离心10min,取上清液备用。
二、测定步骤:1、分光光度计预热30min以上,调节波长至505nm,蒸馏水调零。
2、混合试剂的配制:使用前将试剂二和试剂三1:1等体积混合,用多少配多少。
3、加样表(在EP管中加入下列试剂):试剂(μL)空白管标准管测定管样本100试剂一100蒸馏水100混合试剂900900900混匀,置37℃(哺乳动物)或25℃(其它物种)水浴中,保温15min,于505nm波长处读取吸光度。
葡萄糖-6-磷酸脱氢酶基因突变检测技术的开发及应用说明书

年份 2019推荐奖种 医学科学技术奖项目名称 葡萄糖-6-磷酸脱氢酶基因突变检测技术的开发及应用推荐单位 推荐单位:广东省医学会推荐意见: 葡萄糖-6-磷酸脱氢酶(G6PD)缺乏症是全球最常见的一种X连锁不完全显性遗传病,估计全球有4亿人受累。
目前临床上常用的检测方法为传统化学法,这些方法准确性较差,存在假阳性或假阴性,特别对隐性携带者(杂合子)的孕妇易漏诊,从而造成未对出生的患儿进行应有的临床指导,危及患儿的健康或生命。
本项目是基于PCR-反向点杂交技术的基因检测方法,一个实验同时检测G6PD基因常见的17个位点20种突变,能直接对待检者的基因型进行确诊,具有准确性高、特异性强,能检出基因隐性携带者等优点。
用本法进行检测不需要贵重的专用仪器,只需要PCR实验室常规的设备即可,适用于在国内高发区医院包括广东地区医院大范围推广使用。
目前G6PD缺乏症化学试验检测已是高发区(包括广东省)婚检和产前检查的常规检测项目之一,但基因检测方法还基本未开展,因此,为了增加检测的准确性,降低发病率,应针对高发区的婚检夫妇、孕妇和新生儿开展G6PD缺乏症基因检测,建立患者遗传病档案,及时向患者或其监护人说明该病潜在的危险性,避免服用氧化药物或食用蚕豆等,以防患于未然,保护儿童的健康成长。
因G6PD缺乏症人口基数大,本项目检测意义重大,所以,本项目具有良好的应用市场。
综上,该成果具有一定的创新性、先进性和社会效益,对推动区域科技进步具有积极作用,符合中华医学会医学科学技术奖申报条件,同意提名中华医学会医学科学技术奖三等奖。
项目简介 一、技术内容G6PD缺乏症是全球最常见的一种X连锁不完全显性遗传病,临床上表现为新生儿黄疸、蚕豆病、药物性及感染性溶血等疾病,如发生急性溶血、新生儿核黄疸等重大疾病不及时救治将危及患儿生命及留下严重后遗症。
本项目是基于PCR-反向点杂交技术的基因检测方法,是国内首款检测G6PD基因17个位点共20种基因突变(95A-G、392G-T、487G-A、493A-G、517T-C、519C-T/G、592C-T、835A-G/T、871G-T、1004 C-T/A、1024C-T、1311C-T、1360C-T、1376G-T、1381G-A、1387C-T、1388G-A)的产品。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
6-磷酸葡萄糖酸脱氢酶(6-phosphogluconate dehydrogenase,6-PGDH)活性测定试
(50T/48S)说明书货号:BC2100
测定意义:
磷酸戊糖途径途径中6-磷酸葡萄糖脱氢酶(G6PDH)和6-磷酸葡萄糖酸脱氢酶(6-PGDH)依次催化NADP+生成NADPH,与能量的平衡、生长速率和细胞活力等密切相关。
此外,6PGDH 在逆境生理中具有重要作用。
测定原理:
6PGDH催化6-磷酸葡萄糖酸和NADP+生成NADPH,NADPH在340nm有特征吸收峰,而NADP+在260nm处有特征吸收峰;通过测定340nm吸光度增加速率,计算6-PGDH活性。
自备仪器和用品:
紫外分光光度计、低温离心机、水浴锅、可调式移液枪、1mL石英比色皿和蒸馏水。
试剂组成和配置:
试剂一:液体×1瓶,4℃保存。
试剂二:粉剂×1瓶,4℃保存。
临用前配制,加入5mL试剂一,混匀。
试剂三:粉剂×1瓶,4℃保存。
临用前配制,加入5mL试剂一,混匀。
粗酶液提取:
称约0.1g组织,加入1mL试剂一,冰上充分研磨,10000rpm4℃离心10min,取上清液,待测。
测定:
1.分光光度计预热30min以上,调节波长到340nm,蒸馏水调零。
2.试剂一置于37℃(哺乳动物样本)或者25℃(其他)水浴预热30min以上。
3.空白管:取1mL石英比色皿,依次加入100μL蒸馏水,100μL试剂二,700μL试剂一,100μL试剂三,于340nm处测定3min内吸光值变化,第0s吸光值记为A1,第180s 吸光值记为A2。
4.测定管:取1mL石英比色皿,依次加入100μL粗酶液,100μL试剂二,700μL试剂一,100μL试剂三,于340nm处测定3min内吸光值变化,第10s吸光值记为A3,第190s 吸光值记为A4。
6PGDH活性计算:
活性单位定义:每毫克蛋白每分钟催化产生1nmol NADPH的酶量为1U(U/mg pr)。
6PGDH酶活性(U/mg prot)
=[(△A测定管-△A空白管)×V反总÷ε÷d×109]÷(Cpr×V样)÷T
=535.9×(△A测定管-△A空白管)÷Cpr
△A测定管:A4-A3;△A空白管:A2-A1;ε:NADPH摩尔消光系数,6220;d:比色皿光径,1cm;V反总:反应体系总体积,0.001L;Cpr:粗酶液蛋白质浓度,mg/mL,需要另外测定,建议使用本公司BCA蛋白质含量测定试剂盒;V样:反应体系中加入粗酶液体积,0.1mL;T:反应时间,3min。
注意事项:
(1)样品处理等过程均需要在冰上进行,且须在提取当日完成酶活性测定,粗酶液避免反复冻融;
(2)试剂二和试剂三须现配现用,当天未用完试剂保存在4℃,可保存1周。
