chapt 14 含氮化合物
有机课件 第十四章 含氮化合物

4>、和用,生成结晶的硝 肟酸,溶于NaOH中形成红色溶液。
NOH
RCH2NO2+HONO
R
C
NO2 +H2O
第二硝基化合物与亚硝酸作用,生成结晶的 假硝醇,溶于NaOH中形成蓝色溶液。 NO R2CHNO2+HONO R2C- NO2+H2O
第三硝基化合物不与亚硝酸作用。 3、芳香族硝基化合物的 性质: 1>、还原反应:
OH–
2R'
3、烃基化:
RNH2+R'X R'' RN + HR'
OH– SN2
RN+H
RNHR' R''
R''X
R''
R'''X
RNR'
RN + R'''X R' 季胺盐
4、酰化反应:伯胺、仲胺能向NH3一样,作 为亲核试剂与酰卤、酸酐、酯作用生成酰胺。 叔胺由于氮原子上无H,所以不能。 如:C6H5NH2+(CH3CO)2O
R4N+ CN –也可溶于有机相。它到有机相时 CN –就在有机相与RX。这样就加快了CN – 与RX的接触。提高了反应速度。所以在有 机合成中得到了广泛的应用。
常用的相转移催化剂有季铵盐、冠醚、 非环多醚等。
五、胺的制法:
1、氨的烃基化:
RX与NH3作用时得伯、仲、叔胺以及季 铵盐的混合物。所以无合成价值。只有少 数情况列外:
二、胺的物理性质和光谱性质: 1、 物理性质: 1>、分子间能形成氢键,所以沸点较高,并且 伯>仲>叔胺。 2>、低级脂肪胺如甲胺、二甲胺、三甲胺和乙 胺,在常温下为气体,芳香胺为无色高沸点液 体或低熔点固体。 3>、一般都有氨味,有一定的毒性。
第十四章 有机含氮化合物

(1)硝基烷:烷烃分子中一个或几 个氢原子被硝基取代的化合物;
CH3 NO2
CH3NO2
CH3CHNO2
O2NCH2CH2CH2CH2CH2NO2
脂肪族硝基化合物的化学正在发展当中:
(2)芳香族硝基化合物
a: 结构
• b: 制法:直接硝化
NO2 H3C CH3 Cl 混酸 Cl NO2 + NO2 CH3 HNO3 CH3COOH CH3 Cl H3C CH3
胺
CHO + NH3 过量
H2/Ni
CH2NH2
(CH3)2CO + H2NCH2CH2OH
H2/Ni 醇
(CH3)2CHNHCH2CH2OH
d) Hofmann降解 O
Br2/NaOH NH2
C NH2 O RCH2CNH2
Br2/NaOH
RCH2NH2
e) Gabriel反应 O NH3 O
H3CO2CHN Cl Cl
例题:
Cl
Cl
一种高效, 低毒除草剂;
Cl
Cl
Cl COCl2
Cl CH3OH
NH2
N C O H3CO2CHN Cl Cl
4)磺酰化:磺酰基取代胺(芳香族伯胺、仲胺, 脂肪族伯胺、仲胺)氮原子上氢的反应;
O 磺酰基:(Ar)R S O
RNH2 +
SO2Cl
SO2NHR
N,N’-二苯基对苯二胺
H N H N
对亚硝基-N,N-二甲基苯胺
O2N H N NO2 CH2NH
4,4’-二硝基二苯胺
N-苯基苯甲胺
练习
CH3CH2CHCH2CH2CH2CH3 NHCH2CH3 CH3CH2CHCHNHCH3 H3C CH3
含氮化合物ppt课件

NHCH3 CH3 CH CH3 CH CH2 CH CH3
2-甲基-4-氨基戊烷
18
也可将胺作为母体,用阿拉伯数标明氨基的位次。
CH3 CH CH CH2CH3 CH3 NH2
2-甲基-3-戊胺
CH3 CH CH2CH2CH3 NHCH3
N-甲基-2-戊胺
CH3(CH2)3OH CH3(CH2)3NH2 CH3(CH2)3CH3
分子量
74
73
72
沸点(oC)
117.7
77.8
36.1
25
1o 、2o、 3o 胺,由于H的数目不同,分子间形成氢 键能力不同,b.p.随之改变。叔胺中N原子上无活泼氢, 不能形成分子间氢键,所以其沸点最低。
CH3CH2CH2NH2 CH3CH2NHCH3 (CH3)3N
2. 据取代的烃基类型的不同,可分为:
脂肪胺
芳香胺
RCH2NH2 ArNH2
3. 根据氨基的数目还可分为:一元胺、二元胺、多元胺
14
注意:伯、仲、叔胺是按NH3中H被取代的数目来分类。而 伯、仲、叔醇以及不同级数的卤代烷是按与-OH或X
相连的碳的级数来分类的。
CH3 H3C C NH2
CH3
叔丁基胺:1o 胺
(CH3)3N+Cl- + NaOH
(CH3)3N + NaOH + NaCl
NH3+HSO4- + 2NaOH
NH2 + Na2SO4 + 2H2O
利用此性质,可从混合物中分离出并提纯胺。 也可用于胺的定性鉴别。
29
CH2NH2
OH
HCl
CH3 CH2OH
第十四章 含氮有机化合物

硝基式(假酸式)
仲硝基化合物
R2CHNO2 +
NaOH
- + ( R2CNO2 )Na + H2O
叔硝基化合物没有α-H不反应。
由于硝基的吸电子性,使其α-H的脂肪族硝基化合物有 一定的酸性,其酸性强弱则随α-碳上取代基增多而增加。 pka CH3-NO2 10.2 CH3CH2-NO2 8.5 CH3CH-NO2 7.8 CH3
按氨所连烃基数目分
R (叔胺或三级胺) R-N R + R4N X (季铵盐)
脂肪胺 R-NH2 按烃基不同分 芳香胺
NH 2
2. 命名
简单胺:
由简单烃基组成的胺,按其所有含烃基的名称命名为某胺。 CH3NH2 甲胺 H2NCH2CH2NH2 乙二胺 CH3CH2NH2 乙胺 (CH3)2NH 二甲胺 苯胺 NH 2 H2N CH3
① 硝基化合物的还原 -NO2
H2 / 催化剂 或化学还原
-NH2
化学还原: Fe 、Zn 、Sn + HCl(H2SO4) 、LiAlH4等 NO2 NH2
-
-
Sn + HCl
-CHO O NHC-CH3
H2 / Ni
-CHO O NHC-CH3
-
NO2
NO2 NH2
NH2 NO2
NH2
-
-
-
-
NH4SH
CH3 O2N-NO2 TNT 炸药
-
③ 有很多硝基化合物有强烈的香味,但有毒性。
-
m.p. 80.8℃
NO2
二、硝基化合物的化学性质
1. 脂肪族硝基化合物
① 还原 R-NO2 + H2
第十四章 含氮有机化合物

硝基乙烷
2-硝基丁烷
2-甲基-2-硝基丁烷
(伯硝基化合物,1°) (仲硝基化合物,2°) (叔硝基化合物,3°)
2、命名:以烃基为母体,硝基为取代基
14-3
一、硝基化合物的分类、命名和结构
3、结构
用物理方法测得有关硝基化合物的结构证明:
(1)硝基有对称结构;(2)两个N-O键相等(0.121nm);
Cl NO2 Na2CO3
OH NO2
Cl
OH
O2N
NO2 Na2CO3 O2N
NO2
130 oC
35 oC
NO2
NO2
随着邻对位-NO2数目的增加,反应所需的条件逐渐降低,即卤
素越来越容易取代。
Cl
OH
-NO2处于间位,则不能产生类
NO2 NaOH
NO2
似的活化效应。
Cl
Cl
14-13
(二)硝基对芳环影响
14-17
三、硝基化合物的化学性质
(三)硝基的还原反应
Fe(orSn)+HCl
Zn+NH4Cl+H2O
NO2
As2O3+NaOH
Zn+NaOH
NH2
苯胺
NHOH
N-羟基苯胺
N=N+ O- 氧化偶氮苯 Fe(orSn)+HCl
N=N
偶氮苯 Zn+NaOH
NH-NH
氢化偶氮苯
NH2
苯胺
14-18
第二节 胺 类
“二、三”等数字表示氨基的数目。
CH3CHCH2CH2CH2NH2 1,4-戊二胺 NH2
芳香胺的命名以苯胺为母体,将取代基的位 次及名称写在母体名称前。
Cp14-含氮有机化合物

CH3
核磁共振氢谱(1H NMR) / ppm δ
N
0.6 ~ 5
C
H
2.3 ~ 3.1
H
五、胺的化学性质 (一)碱性
练习14-2:解释碱性强弱
CH 3CH2 NH2
NH 3
NH 2
pKb
3.37
NH 2
NH 2
4.76
NH2
9.38
NH2
NH 2
OCH 3
CH 3
Cl
NO2
pKb
9.66
8.93
2、芳环上的亲电取代:卤代、磺化、硝化、酰化 练习14-5:完成下列反应,并说说你的看法
NH2 Br2 水 NH 2
?
(CH 3 CO)2 O
? CH 3 CO)2 O
Br2
H 2O
NH 2 H 2 SO4 HNO3 NaOH
N(CH 3 )2 CH 3COCl AlCl3
O H HO N CH3
(S)-毒芹碱 (S)-coniine
H
古柯碱 cocaine
N(CH 3 )2
吗啡 morphine
NH2 CH2 CH CH 3
Cl
H
CH 2 CH(CH3 )2
西布曲明 meridia
苯丙胺 benzedrine
dopamine 多巴胺
第十四章 含氮有机化合物
Chapter 14 Organic Nitrogen Compounds 【基本要求】
H 3O +, CuCl, HCl CuBr, HBr Ar N N Cl Ar OH Ar Cl Ar Br
Sandmeyer 反应
CuCN, KCN Ar CN KI , Ar I HBF4 , Ar F Schiemann H 3PO2 Ar H or C2 H5 OH
第十四章 含氮有机化合物

νC-N
1100 cm-1 (脂肪胺),1350-1250 cm-1 (芳香胺);
N-H摇摆振动:910-650 cm-1
四、 胺的化学性质
1.碱性
胺和氨相似,具有碱性,能与大多数酸作用成盐。
R NH2 + HCl R NH2 + HOSO3H
R NH3Cl R NH3 OSO3H
胺的碱性较弱,其盐与氢氧化钠溶液作用时,释放出游离胺。
N=N+ ON=N
¡¡¡¡ª Fe(orSn)+HCl ¡ ¡« ª©
Zn+NaOH
NH2
¡¡ª ¡ Zn+NaOH
NH-NH
¡¡¡¡ª ¡
2、苯环上的取代反应
NO2 发烟HNO3 浓H2SO4 100℃
NO2 Br2/Fe 135~145℃ NO2 发烟H2SO4 110℃
NO2 NO2
NO2 Br NO2 SO3H
+
NH2
+
NH2
-
(I)
¡ ¬ ¡¡¡ p-p ¡é
(II)
(III)
(IV)
N¡¡¡¡¡ª¡¡¡¡ ¡ ¡« ¡¡¬¡¡¡¡¡¬ ¡ ¬ ¡
问题:苯胺与二苯胺,何者碱性大?
答案:二苯胺分子中有两个苯环分享N上孤对电子,碱性更弱。
(2) 烃基化
SN2
RNH2(过量) + R'CH2Cl
RNHCH2R'
R NH3Cl + NaOH
RNH2 + Cl + H2O
碱性:脂肪胺 > 氨 > 芳香胺 pKb < 4.70 4.75 >8.40 脂肪胺 在气态时碱性为: (CH3)3N > (CH3)2NH > CH3NH2 > NH3 在水溶液中碱性为: (CH3)2NH > CH3NH2 > (CH3)3N > NH3
14有机含氮化合物

氨、甲胺和三甲胺的结构如下:
sp3杂化
..
N H H H 氨
未共用 电子对
..
N H3 C H H 甲 胺
..
N H3 C CH3 CH3 三 甲 胺
N 原子为 sp3 杂化
R' N R R' R" 快速翻转 R N "R R' R" N R
对映关系,无旋光性 R1 N N 无法翻转,有旋光性 R4 R3 N R2 无法翻转,有旋光性 手性中心
溶剂化效应是给电子的,N上的H越多,溶剂化效应越大, 形成的铵正离子就越稳定。不同溶剂的溶剂化效应是不同的。
H O H H
R-N-H + H H O H
O
H H
综合上述各种因素, 在水溶液中,胺的碱性强弱次序为: 脂肪胺(2°>1°>3°)>氨>芳香胺 在氯苯中,脂肪胺的碱性强弱次序为: 3 ° > 2° > 1 °
O 酸式 (较少)
R CH
N
R CH
N
Na
(2)与羰基化合物缩合
有α- H的硝基化合物在碱性条件下能与某些羰基化 合物起缩合反应。
R CH 2 NO 2 O OH + R' C H (R'' ) OH H R' C C NO 2 H R' (R'' ) H2O R' C C NO 2 H R' (R'' )
分类
芳香胺与亚硝酸的反应
ArNH2
NaNO2, HCl 0-5oC
1o胺
RNH2 R+
[R-NN]Cl[R2N-N=O]
14第十四章含氮有机化合物习题答案(第四版).docx

1. 给岀下列化合物的名称或写岀结构式:2. 按典碱性的强弱排列下列各组化合物,并说明理由:⑵乙酰胺、甲胺和氨3. 比较正丙醇、正丙胺、甲乙胺、三甲胺和正丁烷的沸点高低并说明理由: 4 .如何完成下列转变:CH 尸 CHCHoBr I> CH°=CHCH° C 出 NH°⑴⑶由(CH^OCOOH 至ij (CH 3)C-COCH 2C1CH 3CH 2-CH-CH 3 CH 3CH 2CH 2CH 2BrNH 2(2)(CH 3)2CHNH 2(3) (CH3)2NCH 2CH 3 (5)a NHCH^CH 3A^ethylbenzen amine(7)对硝基氯化节/V^3-diniethylbenzenaniineN + ■ NCf(9)(8)HO (10)苦味酸N=N ■ OHH 3CH(11) 1,4, 6-三硝基蔡NH,•HNH 2NH 2⑵rti5.完成下列反应,并指出最后产物的构型是(R)或(S):HEC 、H2Phs・(+)6.完成卜•列反应:(5) (7)⑴CHJ(过量).°加热-⑵ Ag2O,H2O '(1)CH3I(2)Ag2O,H2O(3)加热混酸OCH3CH3NH2CH2CH2NH2H+,H9O 9 NaNO2,HCl 9----------------- --------- ►•HNO3AcOHFe+HCl o (CH3CO)9O------------------ ► ! -------------- --------OCH3CH2N+(CH3)3CrCH3NH-COCH3■(1) SOC12 (2) NH^(3) Br2,OH-~~<Q^CH2OH亠―H+CH37•指出下列重排反应的产物:加热H+a ? CH2=CHCOCgt °HOAc3HCH3話(3(6)Ag2°Eg 2史CHC1 * HOAc8.解释下述实验现象:(1)对澡甲苯与NaOH在高温下反应,生成儿乎等量的对和间甲苯酚。
第十四章 含氮有机化合物

第一节 硝基化合物(nitro compounds)
第二节 胺 (amine)
第三节 重氮和偶氮化合物(diazo- and azo-compounds) 第四节 分子重排(molecular rearrangement)
第一节 硝基化合物
一.
二.
硝基化合物的命名和结构 1. 命名 2. 结构 硝基化合物的性质 1. 物理性质 2. 化学性质 脂肪族硝基化合物 芳香族硝基化合物
胺的碱性:脂肪胺>氨>芳香胺
2. 酸性 伯胺和仲胺上含有氢原子,可在碱作用下失去而表现出酸性。
[(CH 3 )2 C H]2 N H + n-C 4 H 9 L i [(CH 3 )2 C H]2 N - Li + + C 4 H 10
二异丙氨基锂(LDA) LDA:由于空间位阻大而不发生亲核反应,是有机合成中有用 的不亲核性强碱试剂,广泛用于碳负离子或烯醇负离子的制备 反应中。 Li
1. 物理性质:
低级胺为气体或低沸点液体,具有氨的气味
低级胺可溶于水;(因为可与水形成分子间氢键) 芳香胺为高沸点液体或低熔点固体,有毒性。
沸点:1o 胺>2o 胺>3o 胺(因为分子形成氢键的能力下降);
2. 光谱特点:
(1)红外光谱(IR):
N-H伸缩振动:3500~3300 ㎝-1,伯胺有两个吸收峰,仲胺 有一个吸收峰,叔胺在此区域无吸收峰; C-N伸缩振动:1350~1000 ㎝-1。
C 2H5HN CH 2CH 2NH 2
N-甲基-N-乙基苯胺 N-methyl-N-ethylaniline N, N-二甲基苯胺 N-乙基乙二胺 N, N-dimethylaniline N-ethylethylenediamine
含氮有机化合物

硝基化合物第一节第十四章含氮有机化合物一、硝基化合物的命名与结构分子中含有硝基(一NO)的化合物称为硝基化合物。
RNO或ArNO。
它的命名类似卤代烃.厂[」乙硝基乙烷「一对硝基甲苯根据硝基化合物具有较高的偶极矩,键长测定两个氧原子和氮原子之间的距离相等,从价键理论观点看,氮原子的sp2杂化轨道形成三个共平面的(7键,未参加杂化的一对电子的p轨道与每个氧原子的p轨道形成共轭体系,因此,硝基化合物的分子结构可以表示如下:共振结构式:氮带一个正电荷,每个氧各带?负电荷,这与硝基化合物高的偶极矩相联系。
根据R 的不同,偶极矩在3.5D和4.0D之间,由于硝基化合物的偶极特征,结果比相同分子量的酮沸点高(挥发慢)。
如硝基甲烷(MW61沸点101C,丙酮(MW5)沸点56C。
意外地,在水中溶解度低,在水中硝基甲烷的饱和溶液,以重量计少于10%而丙酮完全溶于水。
二硝基化合物的制备1 •烷烃的硝化:烷烃可与硝酸进行气相或液相硝化,生成硝基烷烃。
其中以气相硝化更具有工业生产价值.烷烃的硝化是以游离基历程进行的:RH + ' N02 一►R + HNO2R* + *N02—R-N02CX3CH2CK3 + H0IQ2 425° C四或°CH^H2CK2flO2 + CH3CKCH3 + CH3CH2MO2 + CM3NO2NO225%40%烷烃的碳骼对硝化速度具有一定的影响,活性次序为:叔C-H > 仲C-H > 伯C-H。
在高温气相硝化,产物为混合物。
2.亚硝酸盐的烃化①与卤代烃:两者的比例与卤代烃的结构有关,生成硝基烷烃比例为:伯卤代烃〉仲卤代烃〉叔卤代烃卤代烃中卤素被取代的难易是:l>Br>CI>FS N2硝基化合物i卤代烃与亚硝酸银的反应:CHstCH2)e CH2I +AgN02—他代血减Ife惟 + CH3(CH2)60N0 8 翅11 %ii 卤代烷与亚硝酸锂(钠、钾)反应烷基亚硝酸酯对称伸縮振动(诜57255川)反对称伸缩振动(1655^151OC+ CH -B『⑴%“卞氐■ RYH 厂 1TO 戈R>60^实际上硝基化合物和亚硝酸酯两者同时生成,在 DMF ffi DMSO 中,硝基化合 物为主要产物。
有机化学课件(李景宁主编)第14章_含氮有机化合物习题

+ + +
H2O
HCl
CH3CHCOOH
+
NH3Cl-
CH3CHCO2C2H5
NH2
(CH3CO)2O HNO2 (过量)
CH3CHCO2C2H5
NHCOCH3
CH3CHCONH2
NH2
CH3CHCOOH
OH
A B
茚三酮反应
显色 不显色
A B
H2NCH2CH2COOH
NH2
(B)
(C)
C
b.
苏氨酸
H3CCH-CHCOOH
OH NH2
I2/NaOH
CHI3
丝氨酸
HOCH2CHCOOH
NH2
无变化
c.
乳酸 丙氨酸
H3CCHCOOH
OH
茚三酮
不显色
H3CCHCOOH
NH2
显色
二、
a. b. c.
CH3CHCO2C2H5
3、化合物A(C8H17N)其NMR中无双峰,A与2molCH3I反应后再与 湿的Ag2O作用,并加热生成B(C10H21N),再重复以上反应则生成 三甲胺及1,4—辛二烯和1,5—辛二烯,给出A、B 的结构并写出有 关反应方程式。
4、化合物A(C6H13O2N)有旋光性,A与HNO2作用放出N2,与 NaHCO3作用放出CO2,A与HNO2的水溶液作用生成B(C6H12O3), B仍有旋光性,B与浓H2SO4作用于脱水生成C(C6H10O2),C能使 KMnO4溶液褪色,与酸性KMnO4作用并加热则生成草酸和2—甲基丙 酸,写出A、B各对映异构体的Fisher投影式,并用R/S命名法命名, 写出C的结构式。
Ag2O H2O
最新14-第十四章-含氮有机化合物习题答案(第四版)
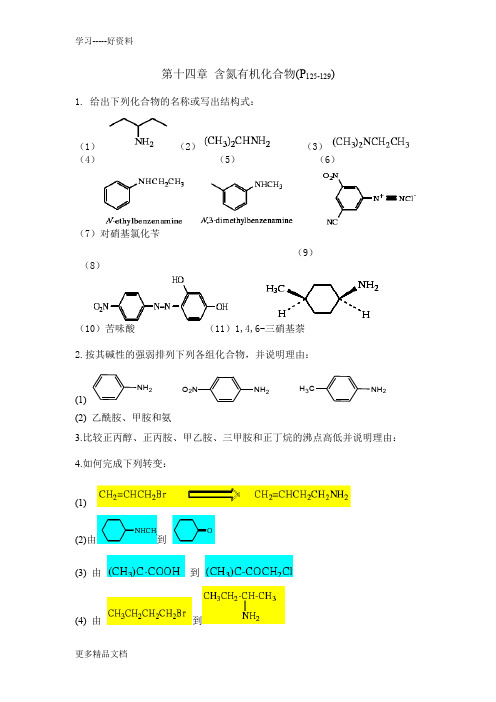
第十四章含氮有机化合物(P125-129) 1.给出下列化合物的名称或写出结构式:(1)(2)(3)(4)(5)(6)(7)对硝基氯化苄(9)(8)(10)苦味酸(11)1,4,6-三硝基萘2.按其碱性的强弱排列下列各组化合物,并说明理由:(1) NH2NH2NH2 O2N H3C(2) 乙酰胺、甲胺和氨3.比较正丙醇、正丙胺、甲乙胺、三甲胺和正丁烷的沸点高低并说明理由:4.如何完成下列转变:(1)(2)由到(3) 由到(4) 由到5.完成下列反应,并指出最后产物的构型是(R)或(S):(1) SOCl 232-6.完成下列反应:(1)N HCH 3322?加热??(1) CH 3I (2)Ag 2O,H 2O (3) 加热CH 3CH 3O 2NFe+HCl?(CH 3CO)2O??H +,H 2O?NaNO 2,HCl??O 2NCH 3(2)(3)OCH 3OCH 3H 2N(4)(5)2(6)CH 3CH 2CH 2NH 2(7)NH-COCH 3BrHNO AcOH?(8)NO 2F O 2N+N HCH 3O2?(9)N H+CH 3H +?CH 2=CHCOOEt?H +?(10)N +3CH3H 3C-?加热7.指出下列重排反应的产物:(1)(2)(3(4)(5)(6) ? ??(7) ? ?(8)8.解释下述实验现象:(1) 对溴甲苯与NaOH在高温下反应,生成几乎等量的对和间甲苯酚。
(2) 2,4-二硝基氯苯可以由氯苯硝化得到,但如果反应产物用NaHCO3水溶液洗涤除酸则得不到产品。
9.请判断下述霍夫曼重排反应能否实现,为什么?9. 完成下列反应,并为该反应提供一个合理的反应机理。
(3)解:本题为Hofmann重排类型的题目。
只是反应体系发生了变化,NaOH水溶液改变了CH3ONa的甲醇溶液,所以最后形成的是较稳定的氨基甲酸甲酯,,而不是易分解的氨基甲酸。
10.从指定原料合成:(1)从环戊酮和HCN制备环己酮;(2)从1,3-丁二烯合成尼龙-66的两个单体-己二酸和己二胺;(3)由乙醇、甲苯及其他无机试剂合成普鲁卡因(4)由简单的开链化合物合成11.选择适当的原料经偶联反应合成:(1)2,2′-二甲基-4-硝基-4′-氨基偶氮苯(2)12.从甲苯或苯开始合成下列化合物:(1)间氨基苯乙酮 (2)邻硝基苯胺(3)间硝基苯甲酸 (4)1,2,3-三溴苯(5) (6)13.试分离PhNH2、PhNHCH3和PhN(CH3)2:14.某化合物C8H9NO2(A)在NaOH中被Zn粉还原产生B,在强酸性下B重排生成芳香胺C,C用HNO2处理,再与H3PO2反应生成3,3-二乙基联苯(D)。
硝基化合物

生物与化学工程系
有机化学
第十四章 含氮有机化合物 常见的硝基化合物的物理常数
生物与化学工程系
有机化学
第十四章 含氮有机化合物
2.化学性质 (1)α-氢原子的酸性 硝基是吸引电子的取代基,导致其α-位上的氢有明显 的酸性。所以,不溶与水的这类硝基化合物可与强碱氢氧 化钠反应生成钠盐而溶于氢氧化钠水溶液。
生物与化学工程系
第十四章 含氮有机化合物 有机化学 (a)金属加酸性介质:
在上述的催化加氢和酸性介质中用金属还原的条件下, 奋力不出中间产物亚硝基苯和N-羟基苯胺,因为它们比硝 基苯更易还原,所以只能得到还原的最终产物苯胺。
生物与化学工程系
有机化学
第十四章 含氮有机化合物
(b)金属加水、醇等中性介质:
生物与化学工程系
有机化学
第十四章 含氮有机化合物
一、硝基的结构 按照价键理论,硝基(—NO2)的结构通常表示为:
这表明在硝基中,N原子于O原子之间 一个是双键,另一个是配价键。
生物与化学工程系
有机化学
第十四章 含氮有机化合物
硝基甲烷分子的键长、键角为:
两个N-O键的键长相等,说明它们没有区别,因此,硝 基的结构应用共振式表示:
第十四章 含氮有机化合物
在亚硫酸胺或亚硫酸氢胺的催化下,氨与萘酚反应生成 相应的萘胺。
上述反应是可逆的,在酸性条件下,萘胺也能转变成相 应的萘酚。
生物与化学工程系
有机化学
第十四章 含氮有机化合物
二、由还原反应制胺 1.硝基化合物的还原—制备芳胺的常用方法。 2.醛和酮的还原氨化 醛和酮与氨反应生成亚胺,亚胺经催化加氢后转变为 伯胺: 上述反应包括胺 化和还原两种过程, 因此称为还原胺化。 生成的伯胺还可以与 反应物醛、酮起加成 反应,从而产生仲胺。 氨的用量多,有利于 伯胺的生成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
使用 过量 的氨 可以得到伯胺为主的产物
控制条件,也可以得到某一胺为主的产物
Organic Chem
R4N+X
AgOH
R4N+OH 季胺碱
Hoffmann烯
例: CH3CH2CHCH3 OH
Organic Chem
IR: :
νN-H
δN-H(面内 δN-H(面外 面内) 面外) 面内 面外
1590-1650 652-900
νC-N
1030-1230
一级胺
3300-3500
( 两个峰,尖、中) (强) 两个峰,
(宽、强)
二级胺
3300-3500 (单峰) 单峰)
弱
700-750 (强)
(1)与碱作用生成盐 )
O RCH2 N O OH O RCH N NaOH RCH N O O
Na+
(2)与羰基化合物缩合 )
CH3 NO2 CH2 O H2O NO2 + R C R'(H) OH R C CH2NO2 R'(H)
Organic Chem
二、 胺
(一). 分类和命名
R—NH2 一级胺
Organic Chem
空间因素: 空间因素:
例:
N+(CH3)3-OH CH3CH2CH2 CH CH3 H H H CH2CH2CH3 H C1上有三个H,都可以与 C2上的N(CH3)3处于对位交叉式, 发 生反 式 消 除.
N+ H3C CH3 CH3 C1-C2 Newman投影式 投
Organic Chem
.. N N
..
CH3
.. Troger碱
四级胺盐的对映体也已经分离出
CH3 + I N C2H5 Ph CH2 CH CH2 CH3 IPh C#43;
芳胺的分子结构: 芳胺的分子结构:
具有较多p成份 140pm .. N H 142.5O H N介于sp2~sp3杂化之间
Organic Chem
+
N上的取代基多了 , 空间障碍就不利于 接受 上的取代基多了, 空间障碍就不利于N接受 上的取代基多了 H+——碱性减弱。 碱性减弱。 碱性减弱 具体的胺的碱性是这两种相反因素协同作用的 结果,一级胺与三级胺哪个碱性强, 结果,一级胺与三级胺哪个碱性强,要看是什 么烃基,不同的烃基得出的次序可能不同。 么烃基,不同的烃基得出的次序可能不同。 芳胺的碱性较弱, 主要是p-π共轭 , N上电子 芳胺的碱性较弱 , 主要是 共轭, 上电子 共轭 云向苯环转移, 原子与质子结合能力降低 原子与质子结合能力降低。 云向苯环转移,N原子与质子结合能力降低。
副反应: 副反应:
..
δO + RCH2 X N O δRCH2 ONO 亚硝酸酯 O取代 取
c. 芳烃的硝化
浓H2SO4
..
+ HONO2
NO2
50~60 C
Organic Chem
O
+ H2O
3. 化学性质
a. 还原反应
3 H2/Ni
R NO2
R NH2 + 2 H2O
NO2
Fe HCl
NH2
+ N(CH ) 3 3
CH3CH2CH 主要 95%
CH3
CH2 + (CH3CH 次
CHCH3)
用于胺的结构测定: 用于胺的结构测定:
CH3
2CH3I
OH
N CH3
+
H
CH3
N
OH
CH3
CH3I
N CH3 CH3
OH
CH3
Organic Chem
优先生成取代基较少的烯烃——Hoffmann烯 烯 优先生成取代基较少的烯烃
二级胺( 三级胺( 二级胺(当R≠R');三级胺(当R≠R'≠R"时) ≠ ) 三级胺 ≠ 应当有旋光异构体,实际分离不出,因为: 应当有旋光异构体,实际分离不出,因为:
R' R''
N R
..
N R'' R'
R
..
10 3 ~ 10 5 /秒 秒 E=25Kj/mol
Organic Chem
有些环状结构的三级胺,可以分离出对映异构体: 有些环状结构的三级胺,可以分离出对映异构体:
Organic Chem
一、硝基化合物 R—NO2 ArNO2
1. 物性
δO R N O δO R N O
两个N—O键等长 键等长 两个
不能反应其真正的结构
高极性,( 稳定,良溶剂,有毒。 高极性,(CH3—NO2) 稳定,良溶剂,有毒。 ,( u=4.30
Organic Chem
2. 制备方法
有 机 化 学
第十四章
含氮化合物
University
of
Science
and
Technology
of
China
内容提要
1、硝基化合物 、 2、 胺 、 3、重要的重氮化合物 )、分类和命名 、 (1)、分类和命名 )、 4、叠氮化合物 )、胺的物理性质 、叠氮化合物(Azides) (2)、胺的物理性质 )、 和氮烯(Nitrene) )、胺的化学性质 和氮烯 (3)、胺的化学性质 )、
CH3
CH3 N+ CH3 OHC2H5
氢氧化三甲乙胺
Organic Chem
(二). 胺的物理性质
1. ①芳胺毒性大,(吸,食,透0.25mL,严重中毒) 芳胺毒性大,(吸 ,( ,严重中毒) β-萘胺 联苯胺 萘胺, 联苯胺——致癌物 萘胺 致癌物
氢键不如O-H的氢键强,b.p.较醇低。 的氢键强, 较醇低。 ②N-H氢键不如 氢键不如 的氢键强 较醇低 N上的取代基使 上的取代基使N-H键减少,2○,3○胺b.p.↓, 键减少, 上的取代基使 键减少 , 水溶性↓ 水溶性
C2H5 NH CH3 甲乙胺
Organic Chem
N-甲基-N-乙基异丁胺 甲 乙
比较复杂的胺, 基当作取代基, 比较复杂的胺,把胺 基当作取代基, 烃基作为母体来命名
CH3CH CH2CH(CH3)2 NH2 2-氨基-4-甲基戊烷 氨 甲 CH3 N(C2H5)2 CH3CH2CH CHCH3 2-(N,N-二乙胺基)-3-甲基戊烷 二 甲
烃的硝化: a. 烷烃的硝化:
CH3CH2CH2 NO2 CH3 CH2 CH3 HONO2 400OC CH3 CHCH3 NO2 CH3CH2 NO2 CH3 NO2
混 合 物
Organic Chem
b. 硝基对卤代烃的取代反应
δO N + RCH2 X δ-O
RCH2 NO2 硝基化合物
N取代 取
Organic Chem
(2) 酸性
键可电离, 伯、仲胺中N-H键可电离 仲胺中 - 键可电离
R2NH
R2 N + H+
-
酸性很弱。例如(C2H5)2NH,pKa=36 酸性很弱。例如( ,
(i-Pr)2NH + n-C4H9Li pKa ~40 THF (i-Pr)2NLi + n-C4H10 LDA ~50
R
NH2 + HCl
R
+NH Cl 3
碱性强弱顺序:脂肪胺 > NH3 > 芳香胺 碱性强弱顺序: pKb 3—4.5 4.75 9—10
在脂肪胺中: 在脂肪胺中: RNH2 < R2NH > R3N 一级 二级 三级
Organic Chem
一些常见的胺的pKb值: 值 一些常见的胺的
化合物 NH3 CH3NH2 (CH3)2NH (CH3)3N
2
pKb(25℃) ℃ 4.75 3.38 3.27 4.21
化合物 C2H5NH2 (C2H5)2NH (C2H5)3N
NH2
O2N
pKb(25℃) ℃ 3.36 3.06 3.25
NH 13.8
NH2 8.0
9.4
H3C
NH2 14.3
Organic Chem
从电子效应看 : R基给电子, 使 N上的电子云 从电子效应看: 基给电子 基给电子, 上的电子云 更集中,孤对电子接受H 的能力增强, 更集中,孤对电子接受 的能力增强,碱性顺 序应是: 序应是:R3N >R2NH > RNH2> NH3,(在气 相中测定或非质子性溶剂中( 相中测定或非质子性溶剂中(如CHCl3, CH3CN, Ph-Cl等)测定确按此顺序) 等 测定确按此顺序) 从溶剂效应和空间位阻效应看:N上取代基多, 从溶剂效应和空间位阻效应看: 上取代基多 上取代基多, 形成氢键少, 结合形成铵离子后, 与H2O形成氢键少,与H+结合形成铵离子后, 形成氢键少 溶剂化稳定作用弱,碱性减弱。 溶剂化稳定作用弱,碱性减弱。
Organic Chem
NMR: : δ
—CH2———CH2———NH2 1.1-1.7 2.2-2.8 0.5-5ppm
(与溶剂的性质,溶液浓度,温度等影响氢键缔合 与溶剂的性质,溶液浓度, 与溶剂的性质 的因素有关,可用D 交换判定 交换判定) 的因素有关,可用 2O交换判定)
MS:
R-NH2 Ar-NH2
Organic Chem
不同的还原条件可以得到一系列不同的还原产物
O NaAsO3 N N N Fe,or Sn+HCl N
Fe,NaOH NO2 Zn+NaOH Fe,HCl Zn ,H2O Zn +NH4Cl NO
