有机化学(第四版)第二十章 蛋白质和核酸
2024版生物化学第四版

生物化学第四版•生物化学概述•蛋白质结构与功能•酶学基础与应用•糖代谢与糖异生作用•脂类代谢与血浆脂蛋白•基因表达调控与疾病关系•细胞信号传导与受体介导作用目录生物化学概述01生物化学定义与研究对象生物化学定义生物化学是研究生物体内化学过程和物质代谢的科学,它探讨生物分子结构、功能、相互作用以及生物分子与生物体之间的关系。
研究对象生物化学的研究对象包括蛋白质、糖类、脂质、核酸等生物大分子,以及维生素、激素、酶等生物小分子。
这些物质在生物体内的合成、分解、转化和调控等过程都是生物化学的研究范畴。
生物化学发展历史及现状发展历史生物化学起源于19世纪中期,随着有机化学和分析化学的发展,人们开始研究生物体内的化学过程。
20世纪以来,生物化学在揭示生命现象本质方面取得了重大突破,如DNA双螺旋结构的发现、基因工程的诞生等。
现状目前生物化学已经成为生命科学领域的重要分支,它与分子生物学、遗传学、细胞生物学等学科相互渗透,共同推动生命科学的发展。
同时,生物化学在医学、农业、工业等领域的应用也越来越广泛。
生物化学在医学领域重要性疾病诊断生物化学方法可以用于检测生物标志物和代谢产物,帮助医生诊断疾病。
例如,通过检测血液中葡萄糖、胆固醇等物质的含量可以判断糖尿病、高血脂等疾病。
药物研发生物化学在药物设计和合成中发挥着重要作用。
通过研究药物与生物大分子的相互作用,可以设计出具有更高疗效和更低副作用的药物。
疾病预防和治疗生物化学可以帮助人们了解疾病发生的机制,从而制定针对性的预防措施和治疗方案。
例如,通过调节饮食和生活方式可以预防糖尿病等代谢性疾病的发生;通过基因工程手段可以治疗遗传性疾病等。
蛋白质结构与功能02氨基酸种类与性质氨基酸的种类根据R基的不同,氨基酸可分为脂肪族氨基酸、芳香族氨基酸、杂环族氨基酸等。
氨基酸的性质包括两性解离、等电点、紫外吸收、茚三酮反应等。
蛋白质一级结构的定义指多肽链中氨基酸的排列顺序,包括二硫键的位置。
有机化学 第二十章杂环化合物
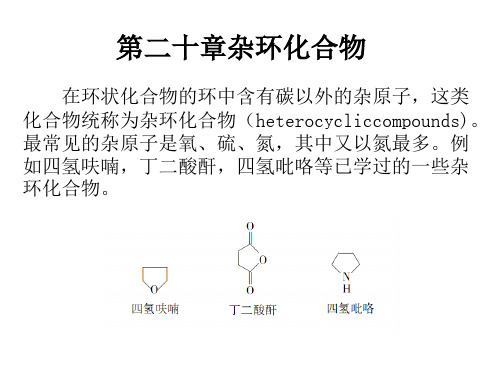
2.加成反应 呋喃、吡咯催化氢化,失去芳香性,得到饱和 的杂环化合物:
四氢吡咯为有机碱,广泛存在于自然界中的某 些生物碱中。
四氢呋喃是重要的有机溶剂。
噻吩中含硫,会使一般的催化剂中毒,氢化时必 须采用特殊催化剂。
工业上通常用开链化合物合成四氢噻吩。四氢噻 吩氧化成四亚甲基砜(或环丁砜),它是一个重要的 溶剂。
(6 )取代呋喃、噻吩、吡咯的定位效应
一取代呋喃、噻吩及吡咯进一步取代,定位效 应应由环上杂原子的α定位效应及取代基共同决定。 例如,3位上有取代基,第二个基团进入环的1位或5 位(即α位),是1位还是5位又由环上原有取代基 的性质决定◦例如,噻吩-3-甲酸溴代,生成5-溴噻 吩-3-甲酸。羧基是间位定位基,因此第二个基团进 入5位即羧基的间位。
一、五元杂环
五元环中含两个或两个(至少有一个氮原子) 以上的杂原子的体系称唑(azole)。如果杂原子不 同,则按氧、硫、氮的顺序编号。
二、六元杂环 三、稠杂环
20.2 五元单杂环化合物
一、呋喃、噻吩、吡咯的物理性质和结构
呋喃、噻吩、吡咯是最重要的含一个杂原子的 五元杂环化合物。它们的重要性不在于它们的单体, 而是它们的衍生物。它们的衍生物不但种类繁多, 而且有些是重要的工业原料,有些具有重要的生理 作用。
叶绿素与蛋白质结合,存在于植物的叶和绿色 的茎中,叶绿素利用卟啉环的多共辗体系易吸收紫 外光,成为激发态,促进光合作用,使光能转变为 化学能。
血红素存在于哺乳动物的红血球中,它与蛋白 质结合成血红蛋白,血红素中的Fe2+具有空的d轨道, 可以可逆地络合氧,在动物体内起到输送氧气的作 用。一氧化碳会使人中毒,其原因之一是因为它与 血红蛋白结合的能力强于氧,从而阻止了血红蛋白 与氧的结合。
核酸-蛋白质互作

核酸-蛋白质互作的生物化学研究方法张金璧, 潘增祥, 林飞, 马雪山, 刘红林南京农业大学动物科技学院, 南京210095摘要:研究核酸-蛋白质的互作是揭示生命活动机理的基础, 文章简要综述了用于研究核酸-蛋白质互作的各种生物化学方法。
从体内、体外两个研究角度, 针对核酸、蛋白以及复合物3个研究水平, 概述了硝化纤维膜过滤实验、足迹法、EMSA、Southwestern杂交等经典分析方法的原理、发展和运用。
还着重介绍了最近在表观遗传学领域中广泛运用的nChIP、xChIP等基本染色质免疫沉淀(ChIP)技术及其衍生出的ChIP-on-chip等方法。
关键词: 核酸; 蛋白质; 互作; 足迹; 染色质免疫沉淀Biochemical methods for the analysis of DNA-protein interactionsZHANG Jin-Bi, PAN Zeng-Xiang, LIN Fei, MA Xue-Shan, LIU Hong-LinCollege of animal science and technology, Nanjing Agricultural University, Nanjing 210095, ChinaAbstract: Investigation of DNA-protein interactions is fundamental to understand the mechanism underlying a variety of life processes. In this article, various types of biochemical methods inDNA-protein interaction study in vivo and in vitro at the level of DNA, protein, and the complex, respectively were briefly reviewed. Traditional assays including Nitrocellulose filter-binding assay, Footprinting, EMSA, and Southwestern blotting were summarized. In addition, chromatin immunoprecipitation techniques including nChIP, xChIP, and ChIP-on-chip, which were widely usedin epigenetics, were particularly introduced.Keywords: nucleic acid; protein; interaction; footprinting; chromatin immunoprecipitation (ChIP) 核酸-蛋白的互作在生命活动中发挥着广泛而重要的作用, 二者的协作是各种生命现象的基础。
高中化学第四章第3节 蛋白质和核酸知识点

第三节蛋白质和核酸蛋白质是生物体内一类极为重要的功能高分子化合物,是生命活动的主要物质基础。
它不仅是细胞、组织、肌肉、毛发等的重要组成成分,而且具有多种生物学功能。
一、氨基酸1、氨基酸的分子结构氨基酸是羧酸分子烃基上的氢原子被氨基(—NH2)取代后的产物。
氨基酸的命名是以羧基为母体,氨基为取代基,碳原子的编号通常把离羧基最近的碳原子称为α碳原子,离羧基次近碳原子称为β碳原子,依次类推。
2、氨基酸的物理性质常温下状态:无色晶体;熔、沸点:较高;溶解性:能溶于水,难溶于有机溶剂。
3、氨基酸的化学性质(1)甘氨酸与盐酸反应的化学方程式:;(2)甘氨酸与氢氧化钠反应的化学方程式:氨基酸是两性化合物,基中—COOH为酸性基团,—NH2为碱性基团。
(3)成肽反应两个氨基酸分子(可以相同也可以不同)在酸或碱存在下加热,通过一分子的氨基和另一分子的羧基脱去一分子水,缩合形成含有肽键的化合物,称为成肽反应。
二、蛋白质的结构与性质1、蛋白质的结构蛋白质是一类高分子化合物,主要由C、H、O、N、S等元素组成。
蛋白质分子结构的显著特征是:具有独特而稳定的结构。
蛋白质的特殊功能和活性与多肽链的氨基酸种类、数目及排列顺序、特定空间结构相关。
2、蛋白质的性质(1)水解蛋白质在酸、碱或酶的作用下,水解成相对分子质量较小的肽类化合物,最终水解得到各种氨基酸。
(2)盐析少量的盐能促进蛋白质溶解。
当向蛋白质溶液中加入的盐溶液达到一定浓度时,反而使蛋白质的溶解度降低而从溶液中析出,这种作用称为盐析。
盐析是一个可逆过程,不影响蛋白质的活性。
因此可用盐析的方法来分离提纯蛋白质。
(3)变性影响蛋白质变性的因素有:物理因素:加热、加压、搅拌、振荡、紫外线照射、超声波等。
化学因素:强酸、强碱、重金属盐、三氧乙酸、乙醇、丙酮等。
变性是一个不可逆(填“可逆”或“不可逆”)的过程,变性后的蛋白质生理活性也同时失去。
(4颜色反应颜色反应一般是指浓硝酸与含有苯基的蛋白质反应,这属于蛋白质的特征反应。
有机化学 蛋白质和核酸

Phe
2). C-末端测定
羧肽酶法: 羧肽酶只能水解C端氨基酸的肽键。
O O O H2NCH 2CNHCHCNHCHCOH CH2C6H5 CH3
H2O, 羧肽酶
O O O H2NCH2CNHCHCOH + H2NCHCOH CH3 CH2C6H5
新C端 根据各氨基酸放出的先后和含量,就可以推断出C端 氨基酸的种类和次序。 对于大分子蛋白质或较长的肽链,必须结合部分水解 法,利用各个肽片断中的重叠结构推出整个肽链的氨基酸 排列次序。
α-羟基-α氨基酸
α-酮酸
α - 氨基酸中的氨基被氧化剂氧化,或在生物体内酶的作 用下生成α - 亚氨基酸,然后经过水解、脱氨生成α - 酮酸。
3.脱水反应—成肽
O -H2O H2N CH C OH + H NH CH COOH R R
O H2N CH C NH CH COOH R
二肽
肽键
R
4. 与水合茚三酮的反应
pH=9 说明为碱性氨基酸,调pI 应加碱,故pI >9。
2.氨基酸中氨基的性质
(1)与亚硝酸反应
R CH COOH + HNO2 NH2
R CH COOH + N2 + H2O
OH α - 氨基酸中的伯氨基可与亚硝酸反应生成羟基酸, 并放出氮气,根据放出氮气的量可计算出α - 氨基酸的 含量。脯氨酸不含伯氨基除外。
(3)与生物碱试剂作用
+ NH3 Pr COOH
+ Cl 3COO
Pr
NH2 COOH
+ OOCCCl 3
5、蛋白质的变性 蛋白质因受物理或化学因素的影响,改变了分子内部 的特有结构,导致理化性质改变,生理活性丧失的现象称 为蛋白质的变性。
有机化学答案下册

第十二章 羧酸习题解答1、解:(1)3-甲基丁酸 (2)3-(4-氯苯基)丁酸 (3)1,3-苯二酸 (4)9,12-十八碳二烯酸(5)CO 2H(6)HO 2CCO 2HOH(7)CO 2HCl(8)CO 2H2、解:(1) CH 3COOH + CH 3CH 2OHH +CH 3C OOC 2H 5(2) CH 3COOH + PCl 3CH3C O Cl + H 3PO 3(3) CH 3COOH + PCl 5CH 3C O Cl + POCl 3 + HCl(4) CH 3COOH + NH 3CH 3COONH 4(5) CH 3COOHCH 4NaOH,CaO+ Na 2CO 33、解:¼×ËáÒÒËáÒÒÈ©+ CO+ CO -(1)ÒÒ´¼ÒÒÃÑÒÒËá£-£- £« CO(2)乙酸草酸丙二酸-+CO 2+CO 2KMnO 4溶液+褪色-(3)丙二酸丁二酸己二酸CO 2CO 2CO (4)4、解:(1)C 6H 5CH 2MgCl ,C 6H 5CH 2COOH ,C 6H 5CH 2COClNC CH 2Cl CH 2ClOHHOOC CH 2Cl CH 2Cl OH HOOC CH 2CN CH 2CN OH HOOC CH 2COOHCH 2COOHOH(2)5、解:H 2C CH 23C CH 2NaCN3CH 2H 3O +3CH 2COOH(1)CH 3CH 2CH 2H +∆H 3CHC CH 2HBr¹ýÑõ»¯ÎïCH 3CHCH 3BrNaCNCH 3CHCH 3CNH 3O +CH 3CHCH 3COOH(2)CH 3CH 2COOH P + BrCH 3Br OH -CH 3CHCOOHOH (3)CH 3CH 2COOH +(4)CH 3CH 2COOH P 2O5∆(CH 3CH 2CO)2OBrEt 2OMgBr CO 2H 2OCOOH 2C 2H 5(5)6三个碳原子,只能是CH 3CH 2COOH 。
蛋白质和核酸化学PPT课件.ppt

▪ 2. 用凯氏微量定氮法测得0.2ml血清中含
氮2.1mg,问100ml血清中含蛋白质多少克?
二、蛋白质的基本单位—氨基酸
▪ 氨基酸是蛋白质的基本组成单位。 ▪ 20标准氨基酸 ▪ 氨基(-NH2)和羧基(-COOH)
COOH H2N—Cα—H
R
不带电形式
COO+H3N—Cα—H
2.空间结构与功能的关系
▪ 蛋白质的空间
结构一旦改变 就会影响蛋白 质的生物活性。
▪ (如右图)牛
核糖核酸酶的 空间结构与功 能。
•牛脑海绵状病,简称BSE。1985年4月,医学家 们在英国发现了一种新病,专家们对这一世界 始发病例进行组织病理学检查,并于1986年11 月将该病定名为BSE,首次在英国报刊上报道。 •食用被疯牛病污染了的牛肉、牛脊髓的人,有 可能染上致命的克罗伊茨费尔德—雅各布氏症 (简称克-雅氏症),其典型临床症状为出现 痴呆或神经错乱,视觉模糊,平衡障碍,肌肉 收缩等。病人最终因精神错乱而死亡。 医学 界对克-雅氏症的发病机理还没有定论,也未 找到有效的治疗方法。
(1)
(2)
(二)
一级结构是空间结构的基础。结构与功能密切相关,蛋白质的一级 结构一旦确立,其空间结构以及生理功能也基本确立。
四、蛋白质的空间结构
▪ 多肽链需通过各种方式卷曲成特定的空间
结构。蛋白质肽链通过折叠、盘曲,使分 子内部原子形成一定的空间排布及相互关 系,称为蛋白质的构象,即空间结构。
(2)分子病
——蛋白质分子一级结构的氨基酸排列顺序与 正常有所不同的遗传病。
镰状细胞贫血(sick-cell anemia) 从患者红细胞中鉴定出特异的镰刀型或月牙型细胞。
人教版高二化学选修5课件4.3蛋白质和核酸

丙氨酸
苯丙氨酸
课前篇自主预习
系统命名 氨基乙酸 α-氨基丙酸 α-氨基苯丙酸
课前篇自主预习
新知预习
自主测试
2.性质
(1)物理性质。
溶剂
水
强酸或强碱 乙醇、乙醚
溶解性 大多数能溶 能溶
难溶
(2)化学性质。 ①两性:在氨基酸分子中,羧基是酸性基团,氨基是碱性基团,甘氨 酸分别与盐酸、氢氧化钠反应的化学方程式分别为
【例题】 下列是某蛋白质的结构片段:
课堂篇探究学习
(1)上述蛋白质结构片段的水解产物中不属于α-氨基酸的结构简
式为
。
(2)上述蛋白质结构片段水解后的氨基酸中,某氨基酸碳氢原子数
比值最大。
①该氨基酸与NaOH溶液反应的化学方程式为 。
②该氨基酸两分子缩合形成环状结构物质的分子式为 。
③该氨基酸的同分异构体中,属于硝基化合物且苯环上有甲基的
课前篇自主预习
新知预习
自主测试
3.误食重金属盐会引起中毒,下列措施不能用来解毒的是( )
A.服大量鸡蛋清 B.服用豆浆
C.喝大量牛奶 D.喝加盐开水
答案D
4.下列物质属于高分子化合物且其主要成分是蛋白质的是( )
A.牛油
B.淀粉 C.羊毛 D.棉花
解析牛油的主要成分是油脂,不属于高分子化合物,A错误;淀粉
提示加酶洗衣粉主要是利用酶的催化作用去污,绝大多数酶是蛋
白质,由于加热可以使蛋白质变性,使酶失去催化作用,因此用热水
溶解加酶洗衣粉去污效果较差。
3.医院里常用高温、高压的方法对医疗器械进行消毒,给病人注
射时常用酒精棉球擦拭皮肤消毒。它们的原理是什么?
提示病菌、病毒中都含有蛋白质,高温、高压及擦拭酒精都能使
《有机化学1A》和《有机化学1B》教学大纲

《有机化学1A》和《有机化学1B》教学大纲课程编号:2100300,2100301学时:96学时(讲课:96 学时,实验:0 学时)学分:6授课学院:天津大学理学院, 药学院,化工学院,材料学院,环境学院适用专业:化学、药学、应用化学、材料化学、环境科学教材:《有机化学》(第四版)主编:高鸿宾出版社:高等教育出版社出版时间:2005年5月主要参考资料:[1]Solomons T W G,Fryhle C B.Organic Chemistry[M].10th ed.Hoboken:John Wiley &Sons,Inc,2011.[2]Carey F A, Giuliano R M.Organic Chemistry[M].8th ed.New York:McGraw-HillCompanies,Inc,2010.[3]McMurry J.Organic Chemistry[M].7th ed.Belmont:Brooks/Cole Publishing Company,2008.[4]Peter K,V ollhardt C,Schore N E.Organic Chemistry: Structure and Function.4th ed.戴立信,席振峰,王梅祥,等译.有机化学:结构与功能[M].北京:化学工业出版社,2006.[5]邢其毅,裴伟伟,徐瑞秋,等.基础有机化学上下册[M].3版.北京:高等教育出版社,2005.[6] 张文勤, 郑艳, 马宁, 赵温涛. 《有机化学》(第五版).北京:高等教育出版社,2014.一.课程性质、目的和任务有机化学是化学、化工类及其相关专业本科生的必修基础课,主要讲授有机化合物的结构、性质及其相互转化的规律。
通过本门课程的学习,使学生掌握有机化学的基本概念、基本理论、基本有机反应及有机化合物结构与性能之间的关系,了解常见有机化合物在化工生产中以及人们日常生活中的地位和作用,提高学生的认知能力,培养学生的创新思维能力。
有机化学课后答案
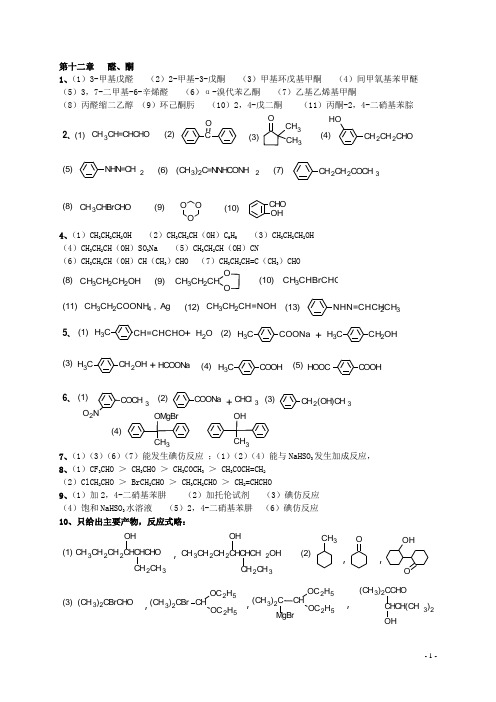
第十二章 醛、酮 1、(1)3-甲基戊醛 (2)2-甲基-3-戊酮 (3)甲基环戊基甲酮 (4)间甲氧基苯甲醚 (5)3,7-二甲基-6-辛烯醛 (6)α-溴代苯乙酮 (7)乙基乙烯基甲酮(8)丙醛缩二乙醇 (9)环己酮肟 (10)2,4-戊二酮 (11)丙酮-2,4-二硝基苯腙(2)(1)(3)(4)C O CH 3CH 3O CH 2CH 2CHO OH CH 3CH=CHCHO 2、 (6)(5)(7)NHN=CH 2CH 2CH 2COCH 3(CH 3)2C=NNHCONH 2(10)(9)(8)CHO OHCH 3CHBrCHOO OO4、(1)CH 3CH 2CH 2OH (2)CH 3CH 2CH (OH )C 6H 5 (3)CH 3CH 2CH 2OH (4)CH 3CH 2CH (OH )SO 3Na (5)CH 3CH 2CH (OH )CN(6)CH 3CH 2CH (OH )CH (CH 3)CHO (7)CH 3CH 2CH=C (CH 3)CHO(10)(9)(8)OCH 3CH 2CHO CH 3CH 2CH 2OHCH 3CHBrCHO(13)(12)(11)NHN=CHCH 2CH 3CH 3CH 2COONH 4 , Ag CH 3CH 2CH=NOH(2)(1)C H 3CH 2OHCH 3COONaCH 3CH=CHCHO H 2O ++5、(3)(5)(4)CH 3COOH CH 3CH 2OH HOOCCOOHHCOONa +(3)(2)(1)(4)CH 2(OH)CH 3COONa OMgBr3COCH 3O 2N+CHCl 3OH 36、7、(1)(3)(6)(7)能发生碘仿反应 ;(1)(2)(4)能与NaHSO 3发生加成反应, 8、(1)CF 3CHO > CH 3CHO > CH 3COCH 3 > CH 3COCH=CH 2 (2)ClCH 2CHO > BrCH 2CHO > CH 3CH 2CHO > CH 2=CHCHO 9、(1)加2,4-二硝基苯肼 (2)加托伦试剂 (3)碘仿反应 (4)饱和NaHSO 3水溶液 (5)2,4-二硝基苯肼 (6)碘仿反应 10、只给出主要产物,反应式略:(2)(1)CH 3CH 2CH 2CHCHCHO OH2CH 3CH 3CH 2CH 2CHCHCH 2OHOHCH 2CH 3CH 3OOOH,,,(3)(CH 3)2CBrCHO CH OC 2H 5OC 2H 5(CH 3)2C CHCH(CH 3)2(CH 3)2CCHO,,,(CH 3)2CBr CHOC 2H 5OC 2H 5MgBr(4)OMgBr CH 3OH CH 3①H+,△② B 2H 6 , H 2O 2/OH ,,,-(1)CH 3CH=CH 2CH 3CH 2CH 2BrNaC≡CNaCH 3CH 2CH 2C≡C CH 2CH 2CH 3CH 3CH 2CH 2COCH 2CH 2CH 2CH 3HBr2322242411、也可通过格氏试剂增碳、水解、氧化得到。
有机化学第二十章 蛋白质和核酸

第二十章 蛋白质和核酸1.写出下列化合物的结构式:(1)门冬酰门冬酷氨酸;(2)谷-半胱-甘三肽(习惯称谷胱甘肽)(Glutathiene,一种辅酶,生物还原剂); (3)运动徐缓素Arg-Pro-Gly-Phe-Pro-phe-Arg;(4)3’-腺苷酸; (5)尿芏-2’,3‘- 磷酸; 6)一个三聚核苷酸,其序列为腺-胞-鸟. (7)苯丙氨酰腺苷酸; 答案:(1)H 2NCH CCH 2COOH NHOCHCCH 2COOHONHCHCOOHCH 2OH(2)H 2N CHCCH 2CH 2COOHO NHCH2SHCONHCH 2COOHCNHCH 2CONHCHC O CH 2NHCC CH 2OHNC ONCHO H 2N 2)3NHCHNH 2NO C ONHCHC CH 2ONH CHCOOH CH 2CH 2NH CH 2NO(3)ONH(4)NNNN O HH O OH NH 2H HOPOOHOHO H HH HOHNNH OOOO P P OOOOOHOH(5)N NN N O H H O O NH 2H OHOH H H HN N ONH 2O OH P OP OOHOH O OOOOO N NN N O H H NHCHHNNN N O H HO OHH HONH 2OP O OHOOCHNH 2CH 2OHHO(6)(7)2.写下列化合物在标明 的pH 时的结构式:(1)缬氨酸在pH8时; (2)丝氨酸在pH1时; (3)赖氨酸在pH10时; (4)谷氨酸在pH3时; (5)色氨酸在pH12时; 答案:(1)CH3CH 3CHCOO NH 2(2)HOCH 2CHCOOHNH 3(3)H 2NCH 2CH 2CH 2CH 2CHOONH 2(4)2CH 2HONH 3O(5)N CH 2CHCOONH 2H3.举列说明下列名词的定义:(1)α-螺旋构型;(2)变性;(3)脂蛋白; (4)三级结构; (5)β-折叠型.答案:(1)α-螺旋构型:(α-helix )是蛋白质最常见,含量最丰富的二级结构。
第20章 蛋白质和核酸(proteins and nucleic acid)

奋斗,合成的牛胰岛素经过物理化学及生物活性的测定,与天然 的完全相同,这是当时世界上第一次用人工方法合成的与天然产 物完全相同的分子量最大的多肽,牛胰岛素的合成不仅是一项技 术上的成就,更重要的是它使人类在认识生命,揭开生命的奥秘 的伟大历程又前进了一步。 蛋白制是一类含氮的天然的高聚物,由N,C,O,H,有少量S,P, Cu,Mn,Zn,I等元素组成,它是生物体内一切组织的基本组成部分, 细胞内除水外,其余的80%的物质是蛋白质,在生物体内蛋白质 的功能是极其复杂的。 生理作用:负责输送氧气 ——血红蛋白 新陈代谢起调节作用——激素 催化作用——酶 预防疾病的发生(免疫)——抗体 与生物遗传有关——核蛋白(RNA,DNA)
+
H 2N C H C O N H R
鲜红色,比色分析 用已知的丙氨酸做成的比色,从而知道N端是什么氨基
NH2 NH2
应用:1) 在等电点(PI)时,偶极离子浓度最大,氨基酸的溶解度 最小,通过调节溶液的PI值,可以从氨基酸的混合物中分离出某 中氨基酸。 2) 知道等电点,在查什么类型的氨基酸,做鉴定用。 3. 氨基酸的物性和光谱性质 物性:1. ɑ-氨基酸 无色结晶 2.在PI等电点时,两性离子,有极强的静电力 3.由于是偶极离子,难溶于有机溶剂 4.IR: υ –COOH=1600cm-1 υ –NH=3100-2600cm-1(宽)
-10
H 3O ++NH 2CH2 COO = 1.6×10-10 = 6.3 ×10-5
苷胺酸中 -COO碱性基团
+ H 3NCH2 COO - + H 2O + [H 3NCH 2COOH][OH -] Kb = + [H 3NCH 2COO -][H2 O] ka .kb= 10-14 ka =10-14 kb
化学蛋白质和核酸知识点

化学蛋白质和核酸知识点蛋白质是组成人体一切细胞、组织的重要成分。
核酸是由许多核苷酸聚合成的生物大分子化合物,为生命的最基本物质之一。
接下来店铺为你整理了化学蛋白质和核酸知识点,一起来看看吧。
化学蛋白质和核酸知识点(一)氨基酸的结构与性质羧酸分子中烃基上的氢原子被氨基(-NH2)取代后的生成物称为氨基酸;分子结构中同时存在羧基(-COOH)和氨基(-NH2)两个官能团,既具有氨基又具有羧基的性质。
说明:1、氨基酸的命名有习惯命名和系统命名法两种。
习惯命名法如常见的氨基酸的命名,如:甘氨酸、丙氨酸、苯丙氨酸、谷氨酸等;而系统命名法则是以酸为母体,氨基为取代基,碳原子的编号通常把离羧基最近的碳原子称为α-碳原子,次近的碳原子称为β-碳原子,依次类推。
如:甘氨酸又名α-氨基乙酸,丙氨酸又名α-氨基丙酸,苯丙氨酸又名α-氨基β-苯基丙酸,谷氨酸又名α-氨基戊二酸等。
2、某些氨基酸可与某种硝基化合物互为同分异构体,如:甘氨酸与硝基乙烷等。
3、氨基酸结构中同时存在羧基(-COOH)和氨基(-NH2),氨基具有碱性,而羧基具有酸性,因此氨基酸既具有酸性又具有碱性,是一种两性化合物,在与酸或碱作用下均可生成盐。
氨基酸在强碱性溶液中显酸性,以阴离子的形式存在,而在强酸性溶液中则以阳离子形式存在,在溶液的pH合适时,则以两性的形式存在。
如:4、氨基酸结构中存在羧基(-COOH)在一定条件下可与醇作用生成酯。
5、氨基酸结构中羧基(-COOH)和氨基(-NH2)可以脱去水分子,经缩合而成的产物称为肽,其中-CO-NH-结构称为肽键,二个分子氨基酸脱水形成二肽;三个分子氨基酸脱水形成三肽;而多个分子氨基酸脱水则生成多肽。
如:发生脱水反应时,酸脱羟基氨基脱氢多个分子氨基酸脱水生成多肽时,可由同一种氨基酸脱水,也可由不同种氨基酸脱水生成多肽。
6、α-氨基酸的制取:蛋白质水解可得到多肽,多肽水解可得到α-氨基酸。
各种天然蛋白质水解的最终产物都是α-氨基酸。
有机化学 第二十一章 氨基酸、蛋白质和核酸

氨基酸等电点可由相应氨基酸盐酸盐的pKa值求 出。如丙氨酸盐酸盐,可看作一个二元酸,具有两
个平衡常数K1和K2
用碱调节丙氨酸盐酸盐水溶液pH值,当加入 0.5mol碱时,平衡中氨基酸正离子4的浓度与偶极 离子5的相同,[4] =[5]此时溶液pH值等于pK1,实 际上此溶液中只有50%的偶极离子5。当加入1.5mol 碱时,溶液中氨基酸偶极离子5的浓度等于负离子6, [5]=[6]此时溶液的pH值等于pK2 ,溶液中也含50% 偶极离子5。所以使丙氨酸完全以偶极离子5存在时, pH值应为pK1和pK2的平均值,这个pH值即为丙氨酸 的等电点(pI),pI=(pK1 + pK2)/2。根据表21-2数据, 丙氨酸盐酸盐的pK1为2. 3、pK2为9. 7,可求出丙 氨酸等电点为6. 0:
三、氨基酸的来源与合成 氨基酸不仅是组成蛋白质的结构单元,而且它
们本身也是人体生长的重要营养物质,具有特殊的 生理作用,因此氨基酸的生产和应用早就得到人们 的重视。
生产氨基酸主要有以下四条途径: 1.蛋白质的水解
由蛋白质水解制备氨基酸是从1820年开始的, 这是一个最古老的方法。味精早期就是由小麦蛋白 质—面筋水解得到。胱氨酸、半咣氨酸是由头发水 解制得的。
天然氨基酸,除甘氨酸外, α碳原子都有手 性,且都是L构型。氨基酸的构型是与乳酸相比而 确定的(也就是从甘油醛导出来的)。例如,与L -乳酸相应的L -丙氨酸的构型是:
正像糖类化合物一样,氨基酸的构型习惯于用 D,L标记法。如果用R/S法标记,那么天然氨基酸大 多属于S构型。但也有R构型的,如L-半胱氨酸为R构 型。
胺与羧酸反应很容易形成铵盐,当氨基和羧基存在 于同一分子时,可在分子内发生质子迁移而形成内盐 (zwitterion):
第四章第三节《蛋白质和核酸》

第三节蛋白质和核酸一.氨基酸的结构与性质1.组成和结构(1)组成:氨基酸可看作是羧酸分子中烃基上的H被氨基取代后的产物。
(2)结构特征:氨基酸分子里既有氨基又有羧基,属于取代羧酸。
组成蛋白质的氨基酸几乎都是α氨基酸。
α氨基酸的结构简式可表示为,其官能团为氨基(—NH2)和羧基(—COOH)。
氨基:氨分子(NH3)去掉一个氢原子后剩余的部分(—NH2)。
—COOH(或—CHO)的邻位碳原子称为α碳原子,该原子上的氢原子称为αH,氨基称为α氨基。
依次类推:β—碳原子,γ—碳原子等。
氨基酸的命名:是以羧基为母体,氨基为取代基,碳原子的编号通常把离羧基最近的碳原子称为α碳原子,离羧基次近碳原子称为β碳原子,依次类推。
2.常见的氨基酸3.性质(1)物理性质:天然的氨基酸常温下均为无色晶体;熔、沸点:较高(200-300℃熔化分解);溶解性:一般能溶于水(除少数外),能溶于强酸或强碱溶液,难溶于乙醇等有机溶剂。
(2)化学性质①两性:氨基酸分子中含有酸性官能团—COOH和碱性官能团—NH2,因此具有两性,可与碱、酸反应生成盐。
可用电离的观点解释:⇌R—CH(NH3+)—COO—,从平衡移动的角度看,向氨基酸中加入碱,电离平衡向酸式电离方向移动,从而使溶解度增大;加入酸,电离平衡向碱式电离方向移动,其溶解度也增大。
当溶液中的氨基酸主要以两性离子的形态存在时(R—CH(NH3+)—COO—),其在水中溶解度最小,可以形成晶体析出。
a.与盐酸的反应:+HCl→(R为H时盐酸甘氨酸,呈酸性)b.与氢氧化钠反应:+NaOH→(R为H时甘氨酸钠,呈碱性)+H2O。
②成肽反应:两个氨基酸分子,在酸或碱的存在下加热,通过一分子的—NH 2和另一分子的—COOH 间脱去一分子水,缩合成含有肽键的化合物。
例如:氨基酸――→脱水二肽或多肽――→脱水蛋白质。
(3)注意:①肽键可简写为—CONH —,但不能写为—CNHO —。
第二十章 氨基酸 蛋白质 核酸

完全水解后,经分析氨基酸的组成为:丙、亮、赖、苯丙、脯、丝、 酪、缬。 端基分析:N-端 丙……………………亮 C-端。 胰蛋白酶催化水解:分离得到酪氨酸,一种三肽和一种四肽。 用 Edman 降解分别测定三肽、四肽的顺序,结果为:丙-脯-苯丙;赖丝-缬-亮。 由上述信息得知,八肽的顺序为:
丙 脯 苯丙 酪 赖 丝 缬 亮 三肽 糜蛋白酶 四肽
NH2NH2
C
O NH
C NH O
+
NH2 CH COOH CH2Ph
D,L-苯丙氨酸 合成法合成的氨基酸是外消旋体,拆分后才能得到 D-合 L-氨基酸。 氨基酸的化学合成 1850 年就已实现,但氨基酸的发酵法生产在一百年后的 1957 年才得以实现用糖类(淀粉)发酵生产谷氨酸。
第二节 多 肽
一、多肽的组成和命名 1. 肽和肽键 一分子氨基酸中的羧基与另一分子氨基酸分子的氨基脱水而形成的酰胺叫 做肽,其形成的酰胺键称为肽键。
位于左边的为 L 型。例如:
COOH H C R NH2 NH2
COOH C R H
D-氨基酸
L-氨基酸
天然氨基酸(出甘氨酸外)其他所有α-碳原子都是手性的,都有旋光性, 而且发现主要是 L 型的(也有 D 型的,但很少) 。 二、氨基酸的性质 1.氨基酸的酸-碱性——两性与等电点 氨基酸分子中的氨基是碱性的,而羧基是酸性的,因而氨基酸既能与酸反 应,也能与碱反应,是一个两性化合物。
R CH COOH NH2 OH H H OH
R CH COO NH2
R CH COO NH3
R CH COO H NH3
溶Байду номын сангаас pH> 等电点 pH<等电点
等电点 (pI)
蛋白质和核酸 大学有机化学

1.氨基酸的酸-碱性——两性与等电点
(1)两性
R CH NH2 COOH
+ H 2O
R
CH NH2
COO
-
+
H3 O
+
R
CH NH3
+
COOH
+
OH
-
R
CH COOH NH 3
H
OH R CH COOH NH 2 R CH COO NH 2
(2)等电点
R- CH-C O O NH 2
H
+
HO
-
R- CH-C O O NH 3
CHO OH OH OH CH 2 OH β
CHO CH 2 CH 2 OH H OH OH O H OH H H H H OH CH 2 OH H OH
OH
β
D
β D 2 脱氧呋 脱氧呋喃核糖 -D-2-脱氧呋喃核糖
2
2. 碱基 核苷酸中的碱基都是嘧啶或嘌呤的衍生物
CH 3 O N H NH O CH 3 HO N N OH
RNA 酸 单 体 中 的 核 苷中 的 核 苷 酸 单 体 RNA中的核苷酸单体
DNA 中 的 核 苷 酸 单 体 酸 单 DNA 中 的 核 DNA中的核苷酸单体苷
二、核酸的结构
1
N O O P OH H O O P OH H O O P OH O O O CH2 O H H H OH CH2 O H N
T(胸腺嘧啶)
N HO N OH
NH O N H O
U(脲嘧啶)
NH 2 N N H O
NH 2 N N OH
C(胞嘧啶)
NH 2 N N N N H
有机上课纲要

林素英 2012/8/2211应用化学《有机化学A》教学纲要一、课程说明《有机化学A》是研究有机化合物的组成、结构、制备、物理性质、化学性质及其相互转化规律的学科,是应用化学专业的重要基础课,是一门理论性和实践性并重的课程。
它使学生掌握各类有机物的特性,组成与结构,理解有机物反应的基本原理及规律,掌握一般有机物的合成方法等基本知识,学会鉴定、表征有机化合物,培养学生扎实的理论基础,为以后学习后继课程和进一步掌握新的科学技术成就打下必要的基础。
本课程教学时间安排:每周4学时,计划教学周数17周,总课时数68学时。
课程基本要求:1、掌握重要类型有机物的结构、命名、物理性质、化学反应、常用制备方法及主要用途。
熟悉主要官能团的典型反应、官能团互变的方法并能用以解决一般合成问题。
2、正确熟练地书写构型式、构象式,理解取代、加成、消去等反应的立体化学过程。
3、正确理解反应的势能曲线图、过渡状态、活泼中间体、速率控制、平衡控制和酸碱理论等基本概念,正确熟练地书写表示机理的反应式,理解结构对一些重要反应的影响。
4、了解核磁共振、红外光谱、紫外光谱、质谱在有机化学中的用途,熟悉主要类型有机物的谱学特征并用以测定不太复杂化合物的结构。
二、学时分配表教学内容授课学时备注第一章第二章第三章第四章第五章第六章第七章第八章第九章第十章第十一章第十二章第十三章第十四章第十五章第十七章第十九章第二十章绪论饱和烃不饱和烃二烯烃和共轭效应芳香烃立体化学卤代烃有机化合物的波谱分析醇、酚醚醛、酮、醌羧酸羧酸衍生物β-二羰基化合物有机含氮化合物杂环糖类化合物氨基酸、蛋白质和核酸机动44+1444+1454628+24225222讲评作业讲评作业课堂测试分散讲授,见红色标记期中考课堂测试、作业课堂测试70三、各章内容要求第一章绪论本章的主要知识点是:有机化合物和有机化学、有机化合物的特点及有机化学在国民经济中的地位和作用、有机化合物构造式的表示方法、价键理论、轨道的杂化(sp3、sp2、sp杂化)、共价键的属性、共价键的断裂和有机反应的类型、酸碱理论、有机化合物分类。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有机化学(第四版)第二十章 蛋白质和核酸
1.写出下列化合物的结构式:
(1)门冬酰门冬酷氨酸;
(2)谷-半胱-甘三肽(习惯称谷胱甘肽)(Glutathiene,一种辅酶,生物还原剂); (3)运动徐缓素Arg-Pro-Gly-Phe-Pro-phe-Arg;
(4)3’-腺苷酸; (5)尿芏-2’,3‘- 磷酸; 6)一个三聚核苷酸,其序列为腺-胞-鸟. (7)苯丙氨酰腺苷酸; 答案:
(1)
H 2N
CH CH 2COOH NH
O
CH
CH 2COOH
O
NH
CH
COOH
2
OH
(2)
H 2N CH
CH 2CH 2COOH
O NH
CH
CH 2SH
O
CH 2COOH
C
NHCH 2O
NHCHC O CH 2
NHCC CH 2OH
N
C N
CH
O H 2N 2)3NHCHNH 2
N
O C O
NHCHC 2O
NH CHCOOH 2
CH 2NH H 2N
O
(3)
O
NH
(4)
N
N
N
N O H
H O OH NH 2
H HO
P
O
OH
O
H
O H H
H HO
H
N
NH O
O
O
O P P O
O
O
O
(5)
N
N
N N O H H O O NH 2
H O
H
O
H
H H H
N N O
NH 2
O P P OH
O
H O O
O
O
O N N
N N O H H NHC
H
H
N
N
N N O H HO OH
H H
O
NH 2O
P O O
HO
O
CHNH 22
(6)
(7)
2.写下列化合物在标明 的pH 时的结构式:
(1)缬氨酸在pH8时; (2)丝氨酸在pH1时; (3)赖氨酸在pH10时; (4)谷氨酸在pH3时; (5)色氨酸在pH12时; 答案:
(1)CH
3
CH 3
CHCOO 2
(2)HOCH 2CHCOOH
3(3)H 2NCH 2CH 2CH 2CH 2CHOO
2
(4)2CH 2HO
NH 3
O
(5)
N CH 2CHCOO
2
3.举列说明下列名词的定义:
(1)α-螺旋构型;(2)变性;
(3)脂蛋白; (4)三级结构; (5)β-折叠型.
答案:
(1)α-螺旋构型:(α-helix )是蛋白质最常见,含量最丰富的二级结构。
蛋
白质分子是由氨基酸通过酰胺键连接而成的,其中由C O
N
C 结构单元组成的
平面称为肽平面,肽平面内C O 与N H 及呈反式排列,肽链主链上,只有α碳原子连接的两个键
C C
α
及C
N
α
是单键,可以自由旋转。
绕C
N
α
旋转的角度称为
φ角,绕C C
α键旋转的角度称为ψ角,多肽主链可以通过C
N
α与C C
α
的旋转
形成螺旋结构,每一圈螺旋占3。
6个氨基酸残基,沿螺旋轴放射上升0.54nm 每一个残基绕
轴旋转100○
,沿轴上升0.15nm 。
螺旋可以按右手放射或左手方向盘绕形成右手螺旋或左手螺旋。
蛋白质中的α-螺旋几乎都是右手螺旋的。
(2)变性:变性作用是蛋白质受物理或化学因素的影响,改变其分子内部结构和性质的作用。
能使蛋白质变性的物理方法有干燥,加热,高压,激烈振荡或搅拌,紫外线,超声波等;化学方法是加入强酸,碱,尿素,重金属盐,三氯乙酸,乙酸,乙醇,丙酮等。
(3)脂蛋白:由单纯蛋白与脂类结合而成的物质。
(4)三级结构:蛋白质的二级结构单元通过氢键等各种作用力使其多肽链卷曲
盘旋和折叠成更为复杂的构象,这种侧链构象及各种主链构象单元互相间的复杂的空间关系就是蛋白质的三级结构。
(5)β-折叠型:β-折叠型是一种肽链良好伸展的结构,它依靠两条肽链,或
一条肽链内两段肽链之间的N
H 与C 形成氢键而成,两条肽链可以是平行的,也可以是反平行。
前者两条肽链人N 端到C 端是同方向的。
后者是反方向的。
由于这种肽
链之间可形成氢键,从而使氨基酸残基间保持最大的距离。
4.写出下列反应产物的结构:
(1)
CN
H 2N
CH3CO
NH
CN
CO
NH
CH
CH 2
CO NH
H
C CHOOH
CH
H 33
N
N
H
(1)(2)
HCl
(2)
Ala-His-Phe-Val
H 2O
胰凝乳蛋白酶
C
6H 5
N
答案:
(1)
H 2N
CH3
CO
NH
CN
CO
NH
CH
CH 2
CO NH
H C CHOOH
CH
H 33
N
NH
(2)
(2)
Ala-His-Phe-Val
H O
C 6HNH
NH S
CHCO CH 3
NH CHCO NH CHCO CH 2
NH CHCOOH CH
H 33
N
NH NH
CHCO CH 3
NH
CHCO NH
CHCO CH 2
NH
CHCOOH CH
H 33
N NH
C NH C 6O
C S
C 6H 5N=C=S
A la-His-Phe+Valine
5.在冷丙醛的醚溶液中,加入KCN ,之后通往气体HCl ,反应混合物用氨处理,所得化合物再加浓盐酸共沸。
写所发生各反应的方程式。
答案:
CH 3CH 2CHO
CH 3CH 2CH
OK
HCl
CH 3CH 2CH
OH
HCl
CH 3CH 2CH
Cl
NH 3
CH 3CH 2CH
NH 3Cl
H 2O
CH 3CH 2CH
NH 2
KCN
6.合成下列氨基酸:
(1)从β-烷氧基乙醇合成丝氨酸;
(2)从苯甲醇通过丙二酸酯法结合加布里埃制第一胺的方法合成苯丙氨酸。
答案:
ROCH 2CH 2OH [O]
ROCH 2
CH0
ROCH 2
NH 2
HOCH 2NH 2
+RBr
(1)
(2)
CH 2OH
+
SOCl 2
CH 2Cl
H 2NCHCH 2OOH
CH 2
7.预计四肽丙酰谷氨酰谷氨酰苷按酰亮氨酸(Ala-Glu-Gly-Leu)的完全水解和部分水解的产物?
答案:
完全水解产物为
丙氨酸+谷氨酸+甘氨酸+亮氨酸
部分水解产物为:
(1)丙氨酸+ Glu-Gly-Leu (2) Ala-Glu-Gly + 亮氨酸
(3) Ala-Glu + Gly-Leu (4) 丙氨酸+ Glu-Gly + 亮氨酸
8.一个七肽是由甘氨酸,丝氨酸,两个丙氨酸,两个组氨酸和门冬氨酸构成的,它的水解成三肽:
Gly-SSEr-Asp
His-Ala-Gly
ASp-His-Ala
试写出引七肽氨基酸的排列顺序。
答案:
根据水解产物和三肽的未端氨基酸残基,可以判断出该七肽的氨基酸排列顺序为
His-Ala-Gly-Ser-Asp-His-Ala。
