大学化学第一章1.3热学第二定律1.4化学平衡PPT课件
《化学热力学》课件

详细描述
05
CHAPTER
和实际生产数据,对化学反应过程进行优化与设计。
要点一
要点二
详细描述
在化学工业中,通过对热力学数据的分析,可以指导反应过程的优化与设计。例如,通过分析反应速率常数、活化能等数据,可以优化反应条件,如温度、压力、浓度等,以达到理想的反应效果。同时,热力学数据也是新型反应过程和工艺开发的重要依据。
02
01
04
03
随着科技的不断发展和人类对能源、环境等问题的关注度不断提高,化学热力学将面临更多的挑战和机遇。
未来化学热力学的研究将更加注重绿色环保和可持续发展,为解决能源危机和环境问题提供更多可行的方案和技术支持。
随着计算机技术和数值模拟方法的不断发展,化学热力学将更加注重计算机模拟和实验验证的结合,以更加精准地预测和优化化学反应和相变化过程。
未来化学热力学的研究将更加注重跨学科的交叉融合,如与物理学、生物学、环境科学等领域的结合,以解决更加复杂的问题。
THANKS
感谢您的观看。
目的
定义
化工生产
化学热力学理论在化工生产过程中用于优化反应条件,提高产率和降低能耗。
新能源开发
通过化学热力学原理研究新能源转化和储存技术,如燃料电池、太阳能电池等。
环境科学
化学热力学在环境科学领域用于研究污染物治理和资源回收等问题。
03
02
01
从19世纪中叶开始,科学家们开始研究化学反应中的能量转化问题,奠定了化学热力学的基础。
总结词
自由能变化是化学反应过程中体系自由能的变化,用于衡量反应过程中的能量和熵的综合效应。
详细描述
自由能变化是焓变和熵变的综合结果,其变化值可以用于判断反应是否自发进行。在等温、等压条件下,自发反应总是向着自由能减少的方向进行。自由能变化的大小和方向对化学反应的方向和平衡状态具有决定性影响。
热力学第二定律1ppt课件

分热量给低温热源为代价,否则不能做功.
• 卡诺循环的热温商之和等于零,不可逆循环的热温商之和小
于零。
.
22
§3.3 熵
1.熵的导出
卡诺循环结论
2 pa
Q1 Q2 0 T1 T2 推广到任何可逆循环:
Q Ri0 或 Q 0
i Ti
TR
b 1
• 任意可逆循环的V 分割 红线恒温可逆, 蓝线绝热可逆.
2.卡诺定理
卡诺定理:在高低温两个热源间工作的所有热机中,以可逆 热机的热机效率为最大。(反证法)
.
21
irW Q1Q1Q 1Q21Q Q1 2
r
1Q2 Q1
1-T2 T1
结论:
1 2 0 TT
可逆循环取等号
1
2
• 循环过程是可以对外做功的.
• 理想气体卡诺热机的效率η恒小于1, 且只与两个热源的温度 (T1, T2)有关, 温差愈大, η愈高。也就是说,卡诺热机要对外
开尔文:从一个热源吸热,使之完全转化为功,而不产生其 它变化是不可能的。即热功转变的不可逆性。
热:能量传递的低 级形式:无序能
高级能可以无条件地 转变为低级能;低级 能全部转变为高级能 是有条件的——给环
境留下影响。
.
功是能量传递的高 级形式:有序能
10
第二类永动机是不可能造成的
.
11
对热力学第二定律的说明: (1)热力学第二定律是实验现象的总结。它不能被任 何方式加以证明,其正确性只能由实验事实来检验。 (2)热力学第二定律的各种表述在本质上是等价的, 由一种表述的正确性可推出另外一种表述的正确性。
01章(一)_化学热力学基础热力学第一定律.

上一内容
下一内容
回主目录
返回
2018/12/22
体系分类
上一内容
下一内容
回主目录
返回
2018/12/22
体系的性质
用宏观可测性质来描述体系的热力学状态, 故这些性质又称为热力学变量。可分为两类:
广度性质(extensive properties) 又称为容量性质,它的数值与体系的物质的 量成正比,如体积、质量、熵等。这种性质有加 和性,在数学上是一次齐函数。 强度性质(intensive properties) 它的数值取决于体系自身的特点,与体系的 数量无关,不具有加和性,如温度、压力等。它 在数学上是零次齐函数。指定了物质的量的容量 性质即成为强度性质,如摩尔热容。
上一内容 下一内容 回主目录
返回
2018/12/22
热力学能
热力学能(thermodynamic energy)以前 称为内能(internal energy),它是指体系内部 能量的总和,包括分子运动的平动能、分子 内的转动能、振动能、电子能、核能以及各 种粒子之间的相互作用位能等。
热力学能是状态函数,用符号U表示, 它的绝对值无法测定,只能求出它的变化值 (相对值)。
上一内容
下一内容
回主目录
返回
2018/12/22
第一定律的文字表述
第一类永动机(first kind of perpetual motion mechine) 一种既不靠外界提供能量,本身也不减少能 量,却可以不断对外源源不断作功的机器称为第一 类永动机,它显然与能量守恒定律矛盾。 历史上曾一度热衷于制造这种机器,均以失
上一内容
下一内容
回主目录
返回
2018/12/22
物理化学课件 第一章 热力学

The first law of themodynamics and thermochemistry
第一节 热力学概论
一. 热力学
热力学(Thermodynamics): 研究宏观系统各种过程中能量相互转换所遵循的规 律的科学, 化学热力学:
热力学应用于化学及其相关的过程 主要原理:
内容:通过导热壁分别与第三个物体达热平衡的任意两个物 体彼此间也必然达热平衡。
定律延伸:任一热力学均相体系,在平衡态各自存在一个称 之为温度的状态函数,对所有达热平衡的均相体系,其温 度相同。
温标:a)摄氏温标 以水为基准物,规定水的凝固为零点, 水的沸点与冰点间距离的1/100为1℃。
b)理想气体温标 以低压气体为基准物质,规定水的三相点 为273.16K,温度计中低压气体的压强为 pr
平衡态公理: 一个孤立体系,在足够长的时间内必将趋于唯一的
平衡态,而且永远不能自动地离开它。
四、状态和状态函数
(一)状态 —系统所有性质的综合表现 ➢系统处于确定的状态,系统所有性质具有确定值;
➢系统所有性质具有确定值,系统状态就确定了;
➢系统的性质是相互关联的,通常采用容易直接测量 的强度性质和必要的广度性质来描述系统所处状态。
五、过程与途径
过程:系统从始态到终态发生的变化 途径:系统完成一个过程的具体方式和步骤
过程 -系统从始态到终态状态随发生的一系列变化
➢ 化学变化过程 按变化的性质分 ➢ 物理过程
p、V、T变化过程
相变化过程
过程按变化的条件分: 等温(T = 0) 等容(V = 0)
表述为热力学第一定律(相变和化学反应热效应)、热力 学第二定律(方向、限度和平衡)、热力学第三定律(熵)
大学化学热力学基础ppt课件

01
耗散结构理论
研究非平衡态系统中自组织现象的理论 框架,探讨系统如何通过自组织形成有 序结构。
02
03
协同学
研究非平衡态系统中各部分之间协同 作用的理论,揭示系统如何通过协同 作用实现自组织过程。
谢谢聆听
03
开放系统
与外界既有能量交换又有物质交换的系统。
热力学平衡态与过程
平衡态
在不受外界影响的条件下,系统各部 分的宏观性质不随时间变化的状态。
热力学过程
系统由一个平衡态转变到另一个平衡 态的经过。
热力学第一定律
内容
热量可以从一个物体传递到另一个物体,也可以与机械能或其他能量互相转换,但是在转换过程中,能量的总值 保持不变。
热力学性质的计算
热容
系统在某一过程中,温度升高(或降低)1K 所吸收(或放出)的热量,称为该系统在该过 程中的“热容”,用C表示。
热力学温度
热力学温标所表示的温度叫做热力学温度,用T表示, 单位是开尔文(K)。
焓变与熵变
在化学反应中,反应前后物质的焓的差值称为 焓变,用ΔH表示;反应前后物质的熵的差值 称为熵变,用ΔS表示。
03
热化学方程式的书写与计算
04
生成焓与燃烧焓的概念及应用
盖斯定律及应用
盖斯定律的内容与意义 利用盖斯定律计算反应热
热化学方程式的加和与相 减
盖斯定律在工业生产中的 应用
化学反应方向判据
焓变与熵变对反应方向 的影响
沉淀溶解平衡与溶度积 常数
01
02
03
自由能变化与反应方向 的关系
04
影响沉淀溶解平衡的因 素
实际循环效率分析
循环效率定义
评价热机或制冷机性能的重要指标,表示有用功与输入功的比值。循环效率越高,表示 机器性能越好。
《化学平衡教学》课件

在制药、石油化工、冶金等领域,化学平衡的计 03 算和分析对于工艺流程的优化和改进具有重要意
义。
环境保护中的应用
01 化学平衡在环境保护中发挥着重要作用,如大气 中温室气体的平衡、水体中污染物的平衡等。
02 通过研究污染物在环境中的化学反应和迁移转化 规律,可以预测和控制环境污染,制定有效的治 理措施。
THANKS
感谢观看
化学平衡的计算方法
平衡图解法
通过作图和观察图像,利用平衡 常数和温度的关系,求出平衡常
数和温度的关系。
代数法
通过建立化学平衡的代数方程组 ,求解未知数。
微分法
利用化学反应速率和浓度的关系 ,建立微分方程,求解未知数。
04
化学平衡的应用
工业生产中的应用
化学平衡在工业生产中有着广泛的应用,如化学 01 反应器的设计和优化、催化剂的选择和制备等。
的结构和功能研究等。
05
化学平衡的实验研究
实验目的与原理
实验目的
通过实验探究化学平衡的原理,加深对化学平衡概念的 理解。
实验原理
化学平衡是指在一定条件下,可逆反应的正逆反应速率 相等,反应物和生成物浓度不再发生变化的状态。实验 将通过具体反应来展示化学平衡的形成和特点。
实验步骤与操作
实验步骤 1. 准备实验器材和试剂,包括反应容器、温度计、搅拌器、可逆反应的试剂等。
《化学平衡教学》 ppt课件
目录
• 化学平衡的基本概念 • 化学平衡的原理 • 化学平衡的计算 • 化学平衡的应用 • 化学平衡的实验研究
01
化学平衡的基本概念
平衡的定义
热力学完整ppt课件

01
02
空调制冷技术原理:利 用制冷剂在蒸发器内蒸 发吸收室内热量,再通 过压缩机将制冷剂压缩 成高温高压气体,经冷 凝器散热后变成低温低 压液体,如此循环实现 制冷。
节能措施探讨
03
04
05
采用高效压缩机和换热 器,提高制冷效率。
优化控制系统,实现精 准控温和智能节能。
采用环保制冷剂,减少 对环境的影响。
THANKS
感谢观看
05
化学热力学基础
化学反应热效应计算
反应热的概念及分类
反应热的计算方法及 实例
热化学方程式的书写 及意义
盖斯定律在化学热力学中应用
盖斯定律的内容及意义 盖斯定律在反应热计算中的应用
盖斯定律在相变热计算中的应用
化学反应方向判断依据
化学反应自发进行的方向判据
焓变与熵变对反应方向的影响
自由能变化与反应方向的关系
热力学完整ppt课件
目 录
• 热力学基本概念与定律 • 热量传递与热平衡 • 气体性质与过程分析 • 相变与相平衡原理 • 化学热力学基础 • 热力学在能源工程领域应用
01
热力学基本概念与定律
热力学系统及其分类
孤立系统
与外界既没有物质交换也没有能量交 换的系统。
开系
与外界既有能量交换又有物质交换的 系统。
04
相变与相平衡原理
相变现象及分类
相变现象
物质从一种相转变为另一种相的过程 ,如固、液、气三相之间的转变。
分类
一级相变和二级相变。一级相变涉及 热量的吸收或释放,体积发生变化; 二级相变无热量交换,体积不变。
相平衡条件与克拉珀龙方程
相平衡条件
在一定温度和压力下,各相之间达到动 态平衡,各相的性质和组成不再发生变 化。
物理化学热力学第一定律

§1.1 热力学概论 §1.2 热力学基本概念 §1.3 热力学第一定律 §1.4 体积功与可逆过程 §1.5 焓 §1.6 热容 §1.7 热力学第一定律的应用 §1.8 热化学 §1.9 化学反应热效应的计算 §1.10 能量代谢与微量量热技术简介(自习)
-1-
物理化学
第一章 热力学第一定律
-12-
Vm
V n
物理化学
§1.2 热力学基本概念
四、状态函数与状态方程 (state function & equation of state)
(一) 状态函数
体系状态一定时, 其值一定的物理量.
又称为系统的热力学性质.
eg. T 、p 、V、U、H 等。
-13-
物理化学
§1.2 热力学基本概念
eg.
dT =0 isothermal process dp =0 isobaric process
dV =0 isochoric process Q =0 idiabatic process dZ =0 cyclical process
-17-
物理化学
§1.2 热力学基本概念
状态函数法 ── 计算状态函数的改变值△Z △Z =Z2 - Z1 与路径无关
Q > 0 Q < 0
物理化学
§1.2 热力学基本概念
2. 功W ── 系统在广义力的作用下, 产生
了 广义位移时, 系统与环境交换的能量
为功W .
[W ] = J
其微变量用δW 表示;
规定: 体系从环境 得功为正. W > 0
体系对环境 作功为负. W < 0
-21-
物理化学
§1.2 热力学基本概念
大学化学课件第一章

思考
1. 101.325 kPa,273.15 K下,H2O(l), H2O(g)和 H2O(s)同时共存时,系统中的相数为多少?
2. CaCO3(s)分解为CaO (s)和CO2(g)并且达到平 衡的系统中有多少相?
二、状态与状态函数 (state function )
1. 状态是体系内一切性质的总和。
例1.1 在容积为10.0 L的真空钢瓶内,充入氯气, 当温度为288 K时,测得瓶内气体的压强为 1.01×107 Pa。 试计算钢瓶内氯气的质量,以千克表示。
解:由pV=nRT, 推出 m MpV RT
m 71.0103 1.01107 10.0 103 8.314 288
单相体系:均匀体系,只有一个相的体系。 多相体系:不均匀系,有两相或两相以上的体系。 相变:同一物质的气相、液相、固相间的相互转
化,叫做相变。固态物质不同晶形间的转 化也属相变。
TiO2/MgTiO3 界面结构
高分辨透射电子显微镜(HRTEM) High-resolution Transmission Electron Microscope
1. 理想气体 为了研究的方便,假设有一种气体:
只有位置不占有体积,是一个具有质量的几何点。 分子之间没有相互作用力, 分子间及分子与器壁间的碰撞不造成动能损失。 这种气体称之为理想气体。
说明
1) 理想气体只是一种人为的气体模型, 实际中它是不存在的。
2) 研究结果表明: 在温度不太低,压力不太高(高温、低压)条件下, 气体分子间的距离相当大, 气体分子自身体积与气体体积相比可以忽略, 分子间的作用力也显得微不足道, 可以近似认为是理想气体。 高温、低压: 温度高于0 oC, 压强低于1 atm。
《化学平衡状态》课件

总结词
详细描述
反应速率受温度、浓度、压力和催化剂等 因素影响。
温度越高,反应速率越快;浓度越高,反 应速率越快;压力越大,反应速率越快; 适当使用催化剂可以加快反应速率。
化学反应的方向
总结词
反应方向决定了化学平衡的移 动方向。
详细描述
根据勒夏特列原理,如果改变 影响平衡的条件,平衡就会向 着减弱这种改变的方向移动。
在制药工业中,化学平衡状态对于药物的合成和分离过程至关重要,通过调节平衡 条件可以获得高纯度的药物。
环境保护中的应用
化学平衡状态在环境保护中也有着重 要的应用,例如在大气污染控制中, 通过化学反应原理来降低大气中的污 染物浓度。
在土壤污染修复中,通过调节土壤中 的化学平衡来降低重金属等有害物质 的活性,从而减少对生态环境的危害 。
用率。
促进环境保护
通过研究化学平衡状态,可以减少 有害物质的排放,促进环境保护。
推动科学研究
化学平衡状态是化学反应动力学和 热力学研究的重要内容,有助于深 入了解化学反应的本质和规律。
02
化学平衡状态的建立
化学反应的速率
总结词
详细描述
反应速率是化学平衡状态建立的关键因素 。
化学反应速率决定了反应进行的快慢,对 于可逆反应,正逆反应速率相等是平衡状 态的特征之一。
《化学平衡状态》ppt课件
目录
• 化学平衡状态的定义 • 化学平衡状态的建立 • 化学平衡状态的移动 • 化学平衡状态的应用 • 化学平衡状态的实验验证
01
化学平衡状态的定义
什么是化学平衡状态
01
化学平衡状态是指在一定条件下 ,可逆反应进行到正、逆反应速 率相等且不再改变的状态。
02
第一章 热力学第一定律
糖水
糖水 糖
均相系统
多(复、非均)相系统
化学平衡:系统内化学组成不变
物理化学 第一章 热力学第一定律 宁夏大学新华学院
Joule(焦耳)和 Mayer(迈耶尔)自1840年起,历经 20多年,用各种实验求证热和功的转换关系,得到的结 果是一致的。
即: 1 cal = 4.1840 J
状态函数:确定体系状态的物理量 (p,V,T)
特点: (1) 状态一定,状态函数一定。
(2) 状态变化,状态函数也随之而变,且状态函数
的变化值只与始态、终态有关,与变化途径无关。
物理化学
第一章 热力学第一定律
宁夏大学新华学院
§1.2 热力学基本概念及术语
容量(广度)性质:与物质的数量成正比,具有加和性 如:V、n、C 强度性质:与物质的数量无关,不具有加和性 如:P、T、Vm 、ρ T1 P1 V1 T2 P2 V2
(c)整个膨胀过程中,始终保持外压比气体压力p只差无限小数值
p外=p-dp
W p外dV ( p d p)dV pdV dpdV
V1 V1 V1 V1
V2
V2
V2
V2
物理化学
第一章 热力学第一定律
宁夏大学新华学院
§1.4 体积功
准静态过程:由无限多个极其接近平衡态(静态)的步骤组成
学能的变化 (能量守恒定律)
物理化学 第一章 热力学第一定律 宁夏大学新华学院
1.3 能量守恒----热力学第一定律
热和功的取号与热力学能变化的关系 系统吸热 Q>0 环境 U > 0 W>0 系统 系统放热 Q<0 U <0 W<0
U = Q + W
2024版化工热力学精ppt课件

化工热力学精ppt课件目录•化工热力学基本概念•流体的热物理性质•化工过程能量分析•相平衡与相图分析•化学反应热力学基础•化工热力学在工艺设计中的应用PART01化工热力学基本概念孤立系统与外界既没有物质交换也没有能量交换的系统。
开放系统与外界既有能量交换又有物质交换的系统。
封闭系统与外界有能量交换但没有物质交换的系统。
热力学系统及其分类热力学基本定律热力学第零定律如果两个系统分别与第三个系统处于热平衡状态,那么这两个系统也必定处于热平衡状态。
热力学第一定律热量可以从一个物体传递到另一个物体,也可以与机械能或其他能量互相转换,但是在转换过程中,能量的总值保持不变。
热力学第二定律不可能把热从低温物体传到高温物体而不产生其他影响,或不可能从单一热源取热使之完全转换为有用的功而不产生其他影响,或不可逆热力过程中熵的微增量总是大于零。
状态方程与状态参数状态方程描述系统或它的性质和本质的一系列数学形式。
将系统的物理性质用数学形式表达出来,即建立该系统各状态参数间的函数关系。
状态参数表征体系特性的宏观性质,多数指具有能量量纲的热力学函数(如内能、焓、吉布斯自由能、亥姆霍茨自由能)。
偏微分与全微分概念偏微分在多元函数中,函数对每一个自变量求导数,就是偏导数。
全微分如果函数z = f(x, y) 在(x, y) 处的全增量Δz = f(x + Δx, y + Δy) -f(x, y) 可以表示为Δz = AΔx + BΔy + o(ρ),其中A、B 不依赖于Δx, Δy 而仅与x, y 有关,ρ = √[(Δx)2 + (Δy)2],此时称函数z = f(x, y) 在点(x, y) 处可微,AΔx + BΔy 称为函数z = f(x, y) 在点(x, y) 处的全微分。
PART02流体的热物理性质基于实验数据的经验方法利用已有的实验数据,通过拟合、插值等数学手段,得到纯物质的热物理性质随温度、压力等条件的变化规律。
第一章热力学第一定律

方法——状态函数法。
在数学上,状态函数的微分是全微分
例 :U f (T ,V ) U U dU dT dV T V V T
22
《物理化学》
• 1.2.3 热力学平衡
• 热力学研究的对象是处于平衡态的系统。
• 一个处在一定环境下的系统的所有性质均不随时 间变化而变化,且当此系统与环境隔离后,也不会引
32
《物理化学》
• 1.3 热力学第一定律
• 1.3.1 能量守恒与热力学第一定律
能量守恒定律:能量既不会凭空产生,也不会凭空消失, 它只会从一种形式转化为另一种形式,或者从一个物体 转移到其它物体,而能量的总量保持不变。孤立系统的
总能量保持不变。
热力学第一定律:本质为能量守恒定律 • 第一类永动机是不可能制成的。 • 内能是系统的状态函数。 • 隔离系统中发生任何变化,其内能不变。
•能判断变化能否发生以及进行到什么程度,但 不考虑变化所需要的时间。
局限性 不知道反应的机理、速率和微观性质,只讲可能 性,不讲现实性。
17
《物理化学》
• 1.2.1 系统和环境
• 系统:我们所研究的那部分物质世界; • 环境:系统以外且与系统相关的部分。 系统与环境间有界面(假想的或真实的)分开, 可以有物质和能量的交换。
服从 pV=nRT 的气体为理想气体 或服从理想气体模型的气体为理想气体
(低压气体)p0 理想气体
8
《物理化学》 吸引力 分子相距较远时,有范德华力;
排斥力 分子相距较近时,电子云及核产生排斥作用。
E吸引 -1/r 6 E排斥 1/r n
Lennard-Jones理论:n = 12
E总 A B E吸 引+E 排 斥=- 6 12 r r
大学化学 第一章

例题
计算下列反应的rGm: H2O2(l) == H2O(l) +1/2 O2(g) 解:查表得 fGm(H2O2,l)= -120.42 kJ· -1 mol fGm(H2O,l)= -237.18 kJ· -1 mol rGm=fGm(H2O,l)- fGm(H2O2,l) =(-237.18)-(-120.42) = -116.76 (kJ· -1) mol
化学与化工学院
影响熵的因素 (2)
同族元素组成的化合物,聚集态、温度、 原子个数都相同时,原子半径越大熵越大: Sm(HF) < Sm(HCl) < Sm(HBr) < Sm(HI) 同分异构体中,对称性低或结构复杂的异 构体,其Sm大: Sm(CH3OCH3,g) < Sm(CH3CH2OH,g)
化学与化工学院
化学反应的G与自发性
H S G= H-TS 低温 高温
–
+
+
–
–
+
–
+
+
–
+
–
+
– 自发反应
T转
–
+
正向反应自发性 随温度的变化 任何温度下 均自发 任何温度下 均非自发 低温时 非自发 高温时 自发 低温时 自发 高温时 非自发
化学与化工学院
影响熵的因素 (3)
温度:同物质的同种聚集态,温度越高, 物质的混乱度增大,物质的熵也增大: Cu: Sm(s,298.15K)<Sm(s,773K)<Sm(s,1273K) 4. 压力:压力增大时,将物质限制在较小的 体积之中,物质的混乱度减小,因此物质 的熵也减小。压力对固体或液体物质的熵 影响很小,但对气体物质的熵影响较大。
物理化学第1章 热力学第一定律及其应用

Q U W U H=40.69kJ
37.59kJ
§2.6 理想气体的热力学能和焓
一、理想气体U
理想气体有两个基本特点:a 分子本身不占有体积 b分子间没有相互作用力
理气内能只是温度的函数,即 U =f (T )
具体写成数学式为:
功可以分为:
体积功:本教材又称膨胀功 定义——由于系统体积变化而与环境交换的功 We
非体积功:也称非膨胀功,其他功 指体积功以外的功 Wf 热力学中一般不考虑非膨胀功
四、数学表达式
设想系统由状态(1)变到状态(2),系统与环
境的热交换为Q,功交换为W,则系统的热力学能的变
化为:
U U2 U1 QW
二、内能(热力学能)
1.定义:指系统内部能量的总和, 包括分子运动的平动能、 分子之间相互作用的位能、 分子内部的所有能量 符号:U
系统总能量通常(E )有三部分组成:
(1)系统整体运动的动能
(2)系统在外力场中的位能 (3)内能
热力学中一般只考虑静止的系统,无整体运动,不考虑 外力场的作用,所以只注意内能
对于微小变化
dU Q W
说明:(1)W指的是总功,包括We、Wf (2)适用范围:封闭体系 、孤立体系 (没有物质交换的体系)
§2.4 体积功 W Fdl
一、体积功的计算 pi > pe We FedlFe AAdlpedV
公式说明:
(1)不管体系是膨胀还是压缩,体积功都用-p外dV表示; (2)不用-pdV表示;p指内部压力, p外指外压,也不能用-p外V、 -Vdp外表示。
§2.3 热力学的一些基本概念
一、系统与环境
物理化学目录

物理化学目录第一章热力学基础概念1.1 热力学系统的分类与性质1.2 温度与热量1.3 内能与热力学第一定律1.4 焓与熵的概念1.5 热力学第二定律及其表述1.6 热力学函数与可逆过程第二章能量转化与计算2.1 热功转化与热机效率2.2 化学反应热与热化学方程式2.3 焓变的计算与标准生成焓2.4 熵变的计算与标准熵2.5 自由能与吉布斯自由能变2.6 反应方向与平衡常数第三章过程变化与平衡3.1 理想气体状态方程及其应用3.2 实际气体与范德华方程3.3 相变与相平衡3.4 化学平衡与平衡常数3.5 化学反应的方向与限度3.6 多相平衡与相图第四章物质分离与提纯4.1 溶液的基本概念与性质4.2 溶解度与溶度积4.3 溶质分配定律与萃取分离4.4 蒸馏与分馏原理及应用4.5 结晶与重结晶方法4.6 色谱分离技术与原理第五章电化学与界面现象5.1 电解质溶液的电导与电导率5.2 离子迁移数与电迁移5.3 电动势与电池反应5.4 电解与极化现象5.5 界面张力与吸附作用5.6 双电层理论与界面电位第六章化学动力学基础6.1 化学反应速率的定义与表示6.2 反应速率的影响因素6.3 反应速率方程与速率常数6.4 反应机理与速率控制步骤6.5 温度对反应速率的影响与阿累尼乌斯方程6.6 催化作用与催化剂第七章物理化学实验方法7.1 热力学实验方法与技术7.2 电化学实验方法与技术7.3 化学动力学实验方法与技术7.4 仪器分析方法与技术在物理化学中的应用7.5 数据处理与实验误差分析第八章相关领域应用与拓展8.1 物理化学在能源与环境领域的应用8.2 物理化学在材料科学中的应用8.3 物理化学在生命科学中的应用8.4 物理化学在化工生产中的应用8.5 物理化学的前沿领域与发展趋势本目录旨在为读者提供一个系统的物理化学知识体系框架,涵盖了热力学、能量转化、过程变化、物质分离、电化学、化学动力学以及物理化学实验方法等多个方面。
大学化学课件

第二节 液体
2-1 液体的蒸发
1、蒸发过程 影响蒸发速度的因素: ①温度;②分子间作用力
2、饱和蒸气压 ①饱和蒸气压:简称蒸气压
②影响蒸气压的因素:
a、液体本身的性质 b、温度
图:几种液体的蒸气压曲线
lgp与1/T关系图
lg p A( 1 ) B T
混合后 V总= 1.0L,T=25℃
根据分压的定义及理想气体方程式,有
p氢V氢 n氢RT p氢分V总
同理可得:
p氮分
p氮V氮 V总
p氢分
p氢V氢 V总
代入数据得:p氢分=50.5KPa, p氮分=15.0KPa
所以p总=50.5+15.0=65.5KPa
三、格雷姆气体扩散定律
同温同压下,某种气态物质的扩散速度与其密度的平方根 成反比,这就是气体扩散定律
要求
手机,上课之前请把手机设成静音或关机,如果上课时听到 手机铃声或者发现有人接电话或者发短信,手机没收!
上课睡觉,请自觉站起来听课! 准备一个笔记本,养成记笔记的习惯! 准备一个作业本,独立完成作业! 准备一个计算器,平时上课或者考试的时候会用到。
绪论
第一节 化学的研究内容 第二节 化学与材料科学的关系 第三节 大学化学的学习方法
第一节 化学的研究内容
第一层次
天体
第二层次 第三层次
单质和化合物
原子、分子、离子
化学的 研究对象
第四层次
电子、质子、中子等
第一节 化学的研究内容
化学变化
物质的组成、结构
化
学
研
物质的化学性质
第一章 化学热力学基础(2)
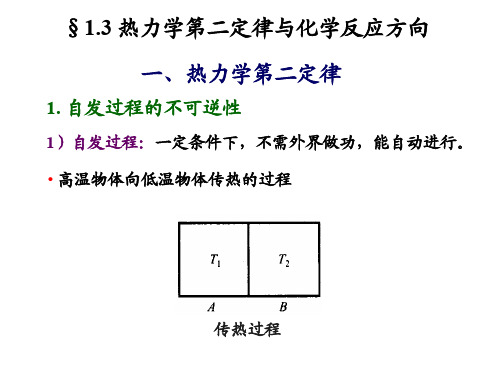
• △G的物理意义:等温等压下系统做非体积功的能力。
在恒温恒压下 W′≥(△G)T,P
> 不可逆 = 可逆
经过一个等温等压不可逆过程,一个封闭系统的吉布斯函数的增加 必小于环境对系统所做的非体积功。
2. 吉布斯函数的判据
0;自发过程 ,不可逆过程 G T ,P ,W ' 0;可逆过程或平衡态 0;不可能发生
Δr S m T2 Δr S m T1 ΔC
T2 T1
θ p ,m
dT T
近似处理:ΔrSmθ(TK)≈ΔrSmθ(298.15K)
三、化学反应自发方向的判据
1. 吉布斯函数(J. W. Gibbs)
定义:G = U + PV-TS = H-TS
• G是状态函数;容量性质;单位J ;绝对值无法测知 • 摩尔吉布斯函数:Gm= G/n;单位J· mol-1
= KΘ
r G RT ln K
m
Δ r Gm RT ln K θ RT ln Q
• 平衡常数意义: K 值越大,表示正反应进行得越完全。
• 影响K 的因素:反应的本性;系统的温度。 • 反应商Q与标准平衡常数K 区别: 平衡状态:Q = K,K 是反应达到平衡时的反应商。
ΔrGm = 0,化学平衡是可逆反应的最终状态。
动
υ正 = υ逆 ,并非反应停止进行,只是正逆反应的影响 相互抵消,是一种 动态平衡 。 化学平衡是有条件的、相对的和暂时的。
变
2. 化学反应等温式和标准平衡常数
等温等压下,对任一气相反应: aA(g) + bB(g) = gG(g) + hH(g) 反应商Q
r
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
其热温商不是dS,
ΔS相同。
其热温熵为零,而dS不 为零
§1.3 热力学第二定律与化学反应方向 1.3.2 熵变的计算
(二版P179-181,三版P188-190)
1.理想气体简单状态变化 等温膨胀(压缩)过程
S nR ln V2 nR ln p1
V1
p2
无论过程是否可逆,该公式 都适用
1.3.2 熵变的计算
就能自动进行的过程。 ① 高温物体向低温物体的传热
过程。 ② 高压气体向低压气体的扩散
过程。
3
1.3.1 热力学第二定律(二版P171-175,
三版P178-186)
1.自发过程的不可逆性
自发过程:一定条件下,不需外界做功,能自 动进行的过程。
自发过程共同的特征 :
① 方向性 :单向,反方向不能自发 ② 其逆过程若发生需环境对系统做功 ③有做功能力但没(完全)做功 ④不可逆性 (造成能量品位下降)
表达了一切自发过程(以传热过程,以及功变成热的过程举例)的不 可逆性。根本原因是,自发过程是能量品位下降的过程。能量品位一 旦下降,就不能升高了。
由此可以判断自然界所有过程的方向:向着能量品位下降的方向。 需要引进一个状态函数来判断过程的方向。
1.3.1 热力学第二定律(二版P171-175,三版 P178-186)
T
pdV T
nR dV V
体积增大10倍,求系统 的熵变。
S dS nR ln V2 V1
假定膨胀过程是(1(2)自由膨胀。 191.4J / mol
解:途径(1)是可逆过
程,其热温商是dS
状态函数的改变值与途
途径(2)是不可逆过程, 径无关,所以两个途径的
1.理想气体简单状态变化
2. 化学变化过程中熵变的计算 (二版P183-185,三版P192-194)
(1可)以各查物附质录的4标得准到摩尔熵Smθ
各种物质在298K的标准摩尔熵Smθ见二版 P646,三版P748附录4:
Smθ :单位:J·K-1·mol-1 注意:Smθ(稳定单质)≠0
a.同一物质,同一温度 : S(气)>S(液)>S(固)
(4)熵判据 :孤立系统=封闭系统+环境
(3)熵增原理
① 绝热过程δQ=0, δQ/T =0:
ΔS孤立≥0
②
(dS)绝热≥0
,不可逆 ,可逆
, 不可能
孤立系统δQ=0, δQ/T
(dS)孤立≥0
=0
:
0,自发过程,即不可逆过程,
0,平衡态,或可逆过程
下 列0,叙不述可能是发否生正确?错误之处请纠
度量系统无序程度(或混乱度)的函数。
1.3.1 热力学第二定律(二版P171-175,三 版P178-186)
3. 熵以及热力学第二定律的数学表达式
(1)熵的引出
(2)热力学第二定律的数学表 达式
δQr/T>δQir/T;说明同样始
末态之间,可逆过程的热温商 大于不可逆过程的热温商。
dS=δQr/T>δQir/T;说明不
自发过程都是不可逆过程。
1.3.1 热力学第二定律(二版P171-175,
三版P178-186)
1.自发过程的不可逆性
2. 热力学第二定律的表达方式 (second law of thermodynamics) 叙述1:克劳修斯说法---不可能把热从低温物体传到高 温物体而不产生其它影响 。
叙述2:开尔文说法 ---不可能从单一热源取热,使之 完全变为功而不引起其它的变化。
§1.3 热力学第二定律与化学反应方向 (二版P171-193,三版P135-204)
1.3.1 热力学第二定律 1.3.2 熵变的计算 1.3.3 化学反应自发方向的判据
§1.3 热力学第二定律与化学反应方向 1.3.1 热力学第二定律(二版P171-175,
三版P178-186)
1.自发过程的不可逆性 自发过程:不需外界对系统做功,
正。
① 在可逆过程中,体系的熵值不变。
,不可逆 ,可逆
② 封闭系统进行不可逆循环过程,
, 不可能
熵增大。
孤立系统不可能发生熵减小 的过程—熵增原理,也适用于
③ 由熵增原理可知,封闭系统不可 能发生熵减小的过程。
封闭系统的绝热过程。
§1.3 热力学第二定律与化学反应方向 (二版P171-193,三版P135-204)
1.3.1 热力学第二定律 1.3.2 熵变的计算 1.3.3 化学反应自发方向的判据
§1.3 热力学第二定律与化学反应方向 1.3.2 熵变的计算(二版P179-181,三版P188-190)
1.理想气体简单状态变化
[例1-9] 10mol理想气 体在298K时等温膨胀,
dS Qr
T
Wr
1.自发过程的不可逆性 2.热力学第二定律的表达方式
3. 熵以及热力学第二定律的数学表达式
(1)熵的引出 热温商: δQ/ T 环 可逆过程的热温商:δQr/T ( δQr/T沿着闭合曲线的环积分为零)
熵的定义: dS = δQr/T;T-系统的温度; △S=∫ (δQr/T)
① 熵是状态函数。单位: J·K-1。 ② 熵的物理意义:
第一章 化学热力学基础
§1.1 气体的 pVT (二版P5-8 ,三版 P6-12)
§1.2 热力学第一定律与热化学 (二版 P128128-156,三版P178-164)
§1.3 热力学第二定律与化学反应方向 (二版P171-193,三版P135-204)
§1.4 化学平衡 (二版P246-258 ,三 版P263-283)
可逆过程系统的熵变大于不可
逆过程的热温商。
可逆过程系统做最大
功,因此吸最多热
dS≥δQ/T
,,不可可逆-逆-- 热力学第二定律的数学表达式
1.3.1 热力学第二定律(二版P171-175,三版P178-186)
3. 熵以及热力学第二定律的数学表达式
(1)熵
(2)热力学第二定律的数学表达式 dS≥δQ/T
b.同一物质,聚集状态相同 :温度升
高,熵值增大
物质
H2O(l) H2O(g)
Smθ / J·K 69.91 188.8 -1·mol-1
I2 (s) 116.1
I2 (g) 260.7
1.3.2 熵变的计算
1.理想气体简单状态变化
2. 化学变化过程中熵变的计算 (二版P183-185,三版P192-194)
