硅胶G薄层色谱分离叶绿素
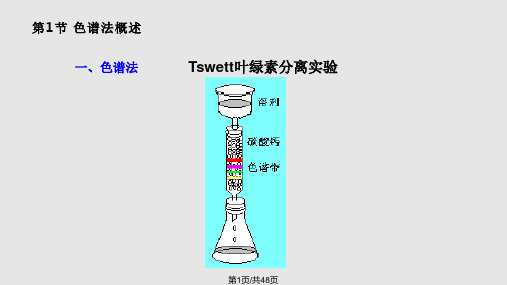
实验二叶绿素的提取与分离

试验二叶绿素的提取与分别试验二叶绿素的提取与分别试验二叶绿素的提取与分别一、试验目的从富含叶绿素的菠菜叶片中提取叶绿素,并在薄层色谱上取样,使叶绿素呈现不同的颜色。
2、试验原理要求同学们先查询资料,了解叶绿素相关学问,试验课上教师讲解。
三、试验材料和仪器研钵、托盘天平、分液漏斗、枯燥锥形瓶、毛细管、薄层层析板、饱和nacl 溶液、无水 na2so4 四、试验步骤 1、叶绿素的提取将几片〔约 5 克〕菠菜叶放入容器中〔颖或冷冻均可。
假设是冷冻的,解冻后用纸包裹,轻轻按压以吸取左侧水分〕。
参与 10ml 石油醚和丙酮的 2:1 混合物,并适当研磨。
用滴管将萃取物转移到分别漏斗中,参与 10ml 饱和NaCl 溶液〔防止形成乳液〕以去除水溶性物质,分别H2O 层,然后用蒸馏水冲洗两次。
将有机层转移到一个小的枯燥锥形烧瓶中,参与2G 无水Na2SO4 并通风。
将处理过的液体倒入另一个锥形瓶中〔假设溶液颜色太浅,可以在通风柜中蒸发并适当浓缩〕。
2.采样点用一根内径 1mm 的毛细管,吸取适量提取液,轻轻地点在距薄板一端1cm在两个平行点上,两个点相距约 1 厘米。
假设第一次取样缺乏,可在样品溶剂挥发后进展其次次取样,但取样点直径不得超过 2mm。
3.开放先在小烧杯中放入开放剂[用石油醚和丙酮按 3:1 的比例进展混合作为开放剂,再将薄层板斜靠于层析缸内壁。
点样端接触开放剂但样点不能浸没于开放剂中,密闭层析缸。
待开放剂上升到距薄层板另一端约 1cm 时,取出平放,用铅笔或小针划前沿线位置,在空气中晾干或用电吹风吹干薄层。
毛细管取样薄层色谱开放4.观看色谱板并记录试验结果。
薄层层析时rf 值表示的是原点到层析斑点中心的距离与原点的到展层溶剂的前沿距离包括什么是最快的集中,什么是最慢的集中,什么是最宽的色素带,什么是最窄的色素带,哪两个色素带最远,哪两个最近,等等各种色素在层析液中的溶解度不同,溶解度高的随层析液在滤纸上集中的快,反之则慢。
薄层色谱法分离鉴定叶绿素

(3) 试比较叶绿素 a、叶绿素b和β-胡萝卜素的极性, 为什么β-胡萝卜素在薄层板上移动最快? 答:极性:叶绿素 b >叶绿素 a >β- 胡萝卜素;β胡萝卜素在层析液中的溶解度大,对薄层板的吸附能力 小,所以移动最快。
分层
分去 下部水层
5 mL饱和食盐水 15 mL蒸馏水
分去 下部水层Βιβλιοθήκη (2)提取液的进一步提纯:
粗提纯的 提取液 离心管 用保鲜膜 盖住管口 1000 rad/min转速 离心10 min 取其上层清 液避光保存
较纯的色素 提取液
转入25 mL 容量瓶中
用石油醚 定容
0.5 cm 比色皿
测量其在662 nm、 644 nm的吸光值
晾干
(3) 展开:
液面不能 超 过点样线 点好样的 硅胶玻片 层析缸 要尽可能多地分 离叶片各种色素 盖好盖子 进行上行层析
待展开剂上升到终点线 附近时(约20~30 min) 取出并在通风橱内晾干
(4) 鉴定:
观察各斑点的颜色 计算比移值Rf
Rf =
样品中某组分移动离开原点的距离 展开剂前沿距原点中心的距离
2. 叶绿体色素的提取:
称取1 g预处理过的大 叶黄杨叶片 剪细碎 量取30 mL提取剂(95%乙醇) 置于研钵
边加入提取剂 边快速 研磨叶片
通风橱中
用不锈钢网 得到提取液 滤去残渣
研磨约10 min
(1)提取液的粗提纯:
分液漏斗 15 mL石油醚 上步的提取液 静置30s 5 mL饱和食盐水 15 mL蒸馏水 得到 提取液 转入棕色瓶 中保存
122.6 参考答案
(1) 绿色植物叶片的主要成分是什么?提取液可能 含有哪些化合物? 答:色素主要成分有脂溶性和水溶性色素,脂溶性 色素主要为叶绿素与类胡萝卜素,水溶性色素主要为花 色甙类,又称花青素。提取液可能含脂溶性色素。
薄层层析及绿色叶色素提取

薄层层析及绿色叶色素提取1.什么叫薄层层析法?原理是什么啊?薄层层析又叫薄层色谱,是色谱法中的一种,是快速分离和定性分析少量物质的一种很重要的实验技术,属固-液吸附色谱,它兼备了柱色谱和纸色谱的优点,一方面适用于少量样品(几到几微克,甚至0.01微克)的分离;另一方面在制作薄层板时,把吸附层加厚加大,因此,又可用来精制样品,此法特别适用于挥发性较小或较高温度易发生变化而不能用气相色谱分析的质。
此外,薄层色谱法还可用来跟踪有机反应及进行柱色谱之前的一种"预试"。
薄层色谱(Thin Layer Chromatography)常用TLC表示,又称薄层层析,属于固-液吸附色谱。
是近年来发展起来的一种微量、快速而简单的色谱法,它兼备了柱色谱和纸色谱的优点。
一方面适用于小量样品(几到几十微克,甚至0.01μg)的分离;另一方面若在制作薄层板时,把吸附层加厚,将样品点成一条线,则可分离多达500mg的样品。
因此又可用来精制样品。
故此法特别适用于挥发性较小或在较高温度易发生变化而不能用气相色谱分析的物资。
此外,在进行化学反应时,常利用薄层色谱观察原料斑点的逐步消失来判断反应是否完成。
薄层色谱是在被洗涤干净的玻板(7×3cm左右)上均匀的涂一层吸附剂或支持剂,带干燥、活化后将样品溶液用管口平整的毛细管滴加于离薄层板一端约1cm处的起点线上,凉干或吹干后置薄层板于盛有展开剂的展开槽内,浸入深度为0.5cm。
待展开剂前沿离顶端约1cm附近时,将色谱板取出,干燥后喷以显色剂,或在紫外灯下显色。
薄层层析,又名薄层色谱.是色谱法的一种类型.其基本原理是利用混合物各组分在某一物质中的吸附或者溶解性能(即分配)的不同,或者其他亲和作用性能的差异,使混合物的溶液各种物质,进行反复的吸附或者分配等作用,从而将各种组分分开.流动的混合物溶液称为流动相;固定的物质称为固定相.薄层层析法的固定相是涂在玻璃板上的硅胶或者氧化铝.2、薄层层析取三块显微载玻片,用硅胶G加0.5%羧甲基纤维素调制后制板,晾干后在110?活化1h。
实验二 叶绿素的提取与分离

实验二叶绿素的提取和分离一、实验目的从富含叶绿素的菠菜叶片中提取叶绿素,并在薄层层析板上点样使叶绿素显示不同颜色。
二、实验原理要求同学们先查询资料,了解叶绿素相关知识,实验课上老师讲解。
三、实验材料、器具研钵、托盘天平、分液漏斗、干燥锥形瓶、毛细管、薄层层析板、饱和NaCl溶液、无水Na2SO4四、实验步骤1、叶绿素的提取在中放入几片(约5g)菠菜叶(新鲜的或冷冻的都可以.如果是冷冻的,解冻后包在纸中轻压吸左水分)。
加入10mL2:1石油醚和丙酮混合液,适当研磨。
将提取液用滴管转移至分液漏斗中,加入10mL饱和NaCl溶液(防止生成乳浊液)除去水溶性物质,分去H2O层,再用蒸馏水洗涤两次。
将有机层转入干燥的小锥形瓶中,加2g无水Na2SO4,通风处理。
处理后的液体倾至另一锥形瓶中(如溶液颜色太浅,可在通风柜中适当蒸发浓缩)。
2、点样用一根内径1mm的毛细管,吸取适量提取液,轻轻地点在距薄板一端1cm 处,平行点两点,两点相距1cm左右。
若一次点样不够,可待样品溶剂挥发后.再在原处点第二次,但点样斑点直径不得越过2mm。
3、展开先在小烧杯中放入展开剂[用石油醚和丙酮按3:1的比例进行混合作为展开剂,再将薄层板斜靠于层析缸内壁。
点样端接触展开剂但样点不能浸没于展开剂中,密闭层析缸。
待展开剂上升到距薄层板另一端约1cm时,取出平放,用铅笔或小针划前沿线位置,在空气中晾干或用电吹风吹干薄层。
毛细管点样薄层色谱展开4、观察层析板并记录实验结果。
薄层层析时Rf值表示的是原点到层析斑点中心的距离与原点的到展层溶剂的前沿距离包括扩散最快的是什么,扩散最慢的是什么最宽的色素带是什么,最窄的色素带是什么哪两个色素带距离相距最远,哪两个最近等等各种色素在层析液中的溶解度不同,溶解度高的随层析液在滤纸上扩散的快,反之则慢。
最快:胡萝卜素次之:叶黄素次之:叶绿素A最慢:叶绿素B颜色分别为:橙黄色、黄色、蓝绿色和黄绿色,最宽的是叶绿素A最窄的是胡萝卜素胡萝卜素和叶绿素B最远叶绿素A和叶绿素B最近实验十四、植物色素的提取和薄层色谱分析一、实验目的:1、了解薄层色谱的基本原理和应用。
薄层色谱分离叶绿素

一实验目的1.掌握提取叶绿素的方法;2.了解薄层层析的原理,掌握薄层层析的一般操作和定性鉴定方法二实验原理1.叶绿素提取高等植物体内的叶绿体色素有叶绿素和类胡萝卜素两类,主要包括叶绿素a(C55H72O5N4Mg)、叶绿素b(C55H70O6N4Mg)、β—胡萝卜素(C40H56)和叶黄素(C40H56O2)等4种。
叶绿素a和叶绿素b为吡咯衍生物与金属镁的配合物,胡萝卜素是一种橙色天然色素,属于四萜类,为一长链共轭多烯,有α、β、γ三种异构体,其中,β异构体含量最多。
叶黄素为一种黄色色素,与叶绿素同存在于植物体中,是胡萝卜素的羟基衍生物,较易溶于乙醇,在乙醚中溶解度较小。
根据它们的化学特性,可将它们从植物叶片中提取出来,并通过萃取、沉淀和色谱方法将它们分离开来。
2.薄层色谱薄层层析是快速分离和定性分析微量物质的一种极为重要的实验技术,具有设备简单、操作方便而快速的特点。
它是将固定相支持物均匀地铺在玻片上制成薄层板,将样品溶液点加在起点处,置于层析容器中用合适的溶剂展开而达到分离的目的。
用此法分离时几乎不受温度的影响,可采用腐蚀性显色剂,而且可在高温下显色,特别适用于挥发性小或在较高温度下易发生反应的物质,同时也常用来跟踪有机反应或监测有机反应完成的程度。
薄层层析的器材选择:(1)基板:玻璃、塑料、金属箔,常用玻璃板。
2)吸附剂:吸附剂要有合适的吸附力,并且必须与展开剂和被吸附物质均不起化学反应。
可用作吸附剂的物质很多,常用的有硅胶和氧化铝,由于吸附性好,适用于各类化合物的分离,应用最广。
选择吸附剂时主要根据样品的溶解度、酸碱性及极性。
氧化铝一般是微碱性吸附剂,适用于碱性物质及中性物质的分离;而硅胶是微酸性吸附剂,适用于酸性物质及中性物质的分离。
以下简单介绍吸附剂的几个基本参数。
种类:常用:氧化铝(强极性)、硅胶(中强极性)不常用:硅藻土、纤维素、糖类、活性碳符号:H——无任何添加剂;G——加有锻石膏(Gypsum,CaSO4·1/2 H2O)粘合剂;F——加有荧光素(Fluorescein)CMC——加有羧甲基纤维素钠(Carboxymethyl cellulose)例:硅胶GF254表示硅胶中既加有煅石膏粘合剂,也加有荧光素,可以在波长254nm的紫外光下激发出荧光粒度:目:1cm2内的筛孔数,数目越大,颗粒越小。
色谱法叶绿素分离实验PPT课件
五、检测技术
检测灵敏度
1.系统适用性试验 比移值
分离效能
第37页/共48页
2.鉴 别
等浓度对照法----同板---大致同位、同大、同色泽
等体积混合法----斑点单一、紧密 结构相似对比法-----Rf不同或两斑点
杂质对照品法 3.杂质检查 样品溶液的自身稀释对照法
二者合用法
第38页/共48页
4.定量方法 (1)目视比色法 -----半定量法(精度±10%) (2)斑点洗脱法
第11页/共48页
• (2)如何选择流动相?
最佳方案总是实验确定
第12页/共48页
❖想一想 在吸附色谱
中,以硅胶为固定相, 当用三氯甲烷为流动 相时,样品中某些组 分保留时间太短,若 改用三氯甲烷–甲醇 (1:1)时,则样品中 各组分的保留时间是 变长,还是变得更短? 为什么?
4.吸附柱色谱操作技术
• (1)装柱
• A.质量要求
装柱之前,先将空柱洗净干燥,再将空柱垂直固定在铁架台上。如果色谱柱下端没有砂芯横隔,就 取一小团脱脂棉,用玻璃棒将其推至柱底,再在上面平铺上一层厚0.5~1cm的洗过、干燥石英砂,有助于 分离时色层边缘整齐,加强分离效果。柱的长度与直径比一般为10 ~ 20:1。色谱柱的填装要均匀,不能有 气泡。
(3)特点
消除系统误差, 值的重复性和可靠性都比 好
Rr
Rf
第23页/共48页
3.分离度
(1)定义 衡量薄层色谱分离效果的重要指标,是 指相邻两斑点中心至原点的距离之差与 两斑点平均径向宽度(径向宽度是指斑 点沿着展开方向的宽度)的比值
(2)计算方法
R l2 l1 2(l2 l1 ) (W1 W2 ) / 2 W1 W2
薄层色素分离实验报告

薄层色素分离实验报告一、实验目的本实验的主要目的是通过薄层色素分离实验,掌握薄层色谱分离的基本原理和操作技巧,以及了解不同色素的迁移行为和染料的特性。
二、实验原理薄层色谱法是一种对于溶液中的某些物质进行初步分离和鉴定的实验方法。
它利用薄层类似于吸收性固体的涂层(如硅胶、氧化铝等)作为固定相,涂层上的液滴溶液在各种溶剂的作用下,其成分迁移速率不同,从而实现物质的分离和检测。
三、实验步骤1. 准备好薄层色谱板,并标出起点线。
2. 首先制备待分离的色素溶液。
3. 将待分离的色素溶液滴于起点线上,并保持板面平衡。
4. 将色相溶液的涂层板直立放在色相槽中,使溶液与涂层充分接触。
5. 当溶液接近色相板顶端时,立即取出,并迅速用铅笔圈出色素斑点位置。
6. 用热风枪迅速干燥板面。
7. 将干燥的色谱板放入显色槽中,并使其与显色液充分接触。
8. 观察色谱板上的色素斑点的变化,并及时记录。
9. 根据实验结果,对色素进行初步分析和鉴定。
四、实验结果实验中,我们使用了红色食用色素溶液作为待分离的物质。
经过实验观察和记录,我们观察到了不同色素分离出的斑点,并记录了其位置和颜色变化。
我们发现红色食用色素溶液由于其化学成分的不同,在薄层色谱板上呈现出不同的色素斑点。
通过对色素斑点的鉴定,我们初步确定了红色食用色素溶液中的主要成分。
五、实验讨论与分析在本次实验中,我们成功地利用薄层色谱法将红色食用色素溶液进行了初步分离和鉴定。
通过对色素斑点的观察和分析,我们可以初步了解不同色素的化学成分和性质。
然而,本实验中的色素鉴定还不够准确和全面。
为了得到更可靠的结果,可以尝试使用更多的色素溶液进行分离实验,并对色素斑点进行定量分析,以确定各色素的含量比例。
同时,还可以添加更多的显色试剂,以增强色素斑点的显色效果。
六、实验总结通过本次薄层色素分离实验,我们了解了薄层色谱分离的基本原理和操作技巧,掌握了薄层色谱实验的步骤和注意事项。
同时,我们也发现了实验中的一些不足之处,并提出了改进的建议和进一步的研究方向。
薄层色谱法分离鉴定叶绿素实验报告

薄层色谱法分离鉴定叶绿素实验报告院(系)生物与化学工程系年级专业姓名学号课程名称专业基础实验实验日期2011年月实验地点报导老师一、实验目的1.通过白菜叶中叶绿素的提取和分离,进一步理解和掌握柱色谱分离技术的原理和操作方法。
2.了解薄层层析色谱分离鉴别物质的原理方法。
二、实验原理植物叶片中的叶绿体色素有叶绿素和类胡萝卜素两类,主要包括叶绿素a、叶绿素b、β-胡萝卜素及去镁叶绿素等四种。
叶绿体色素是脂溶性色素,植物叶绿体色素通常可用乙醇、丙酮等有机溶剂提取。
在波长662 nm、644 nm测定吸光值。
可根据下列公式计算叶绿素a和叶绿素b的含量。
叶绿素a的含量(mg·g-l)=[12.7A622-2.69A644]×2V/1000m (1)叶绿素b的含量(mg·g-l)=[22.7A622-4.68A644]×2V/1000m (2)通过薄层色谱(TLC)对叶绿体色素提取液进一步分离,可分离叶绿素a、叶绿素b、β-胡萝卜素及去镁叶绿素,经多次制备可得少量叶绿素纯品,并进行光谱表征。
三、仪器和药品仪器:离心机,紫外可见分光光度计,层析缸,硅胶G薄层板,容量瓶,毛细管,分液漏斗,研钵,其它常用玻璃仪器。
试剂:石油醚(60~90℃),乙醇,乙醚,丙酮,脱脂棉,饱和NaCl溶液,蒸馏水,无水Na2SO4。
材料:白菜叶。
四、实验步骤1、绿素的提取在研钵中放入几片(4g)白菜菜叶,剪成碎块,放在研钵中加人6mL丙酮,适当研磨,将绿色溶液沿着玻璃棒倒入小烧杯中,再用丙酮重复上述操作二次,每次6mL将提取液用脱脂棉过滤,滤液转移至分液漏斗中,加人10mL石油醚和10mL饱和NaCl溶液(防止生成乳浊液)除去水溶性物质,分去H2O层,再用20mL 蒸馏水洗涤两次。
将有机层转入干燥的小锥形瓶中,加4g入无水Na2SO4干燥。
2、分光光度法测叶绿素的含量将叶绿素提取液放入离心试管中,盖好盖子,在3200r/min的转速下离心10min,取上清液转入50mL容量瓶中用石油醚定容,以石油醚为参比溶液,用0.5cm的比色皿测量其在波长644nm,662nm的吸光度并计算叶绿素的含量。
简述采用硅胶板薄层色谱分离实验时具体的操作步骤和注意事项

简述采用硅胶板薄层色谱分离实验时具体的操作步骤和注意事项一、实验操作步骤采用硅胶板薄层色谱分离实验的操作步骤如下:1.硅胶板的制备:选择合适的硅胶板,如硅胶G板或硅胶H板。
将硅胶与适量的黏合剂混合,搅拌均匀后涂在玻璃板上,制成硅胶薄层板。
薄层板制成后需干燥,然后活化处理,以提高分离效果。
2.点样:将待分离的样品溶液点在硅胶板上,用毛细管或自动点样器进行点样操作。
点样时需注意控制点样量,过量的样品可能导致拖尾、边缘效应等。
3.展开:在密闭的容器中进行展开,选择合适的展开剂,确保待分离的组分能够得到较好的分离。
展开剂的选择应根据样品的性质进行优化。
4.显色:展开后的薄层板需进行显色处理,以便观察和检测组分的斑点。
根据待分离组分的性质选择合适的显色剂,如荧光剂、金属盐等。
5.检测与记录:通过合适的方法对薄层板上的组分进行检测,如紫外可见吸收光谱法、荧光法等。
记录各组分的斑点位置、大小及颜色等信息,以便后续的分析和处理。
6.薄层板的回收和处理:实验结束后,需对薄层板进行回收和处理。
对于有价值的组分,可进行进一步分离和纯化。
对于不再需要的薄层板,需按照实验室规定进行处理,避免对环境造成污染。
二、注意事项在进行硅胶板薄层色谱分离实验时,需要注意以下几点:1.硅胶板的选择与制备:根据实验需求选择合适的硅胶板类型(如硅胶G 板或硅胶H板)。
制备时需确保硅胶与黏合剂的比例合适,搅拌均匀,避免出现硅胶颗粒等杂质。
同时,制成的薄层板需干燥并活化处理,以提高分离效果。
2.点样操作:点样时需控制点样量,避免过量的样品导致拖尾、边缘效应等问题。
可以采用毛细管或自动点样器进行点样,提高点样精度和效率。
3.展开剂的选择与优化:展开剂的选择对于薄层色谱分离的效果至关重要。
应根据待分离组分的性质选择合适的展开剂,并进行优化实验,以提高分离效果。
同时,需注意展开剂的配比和组成,以获得最佳的分离效果。
4.显色处理:选择合适的显色剂对展开后的薄层板进行显色处理,以便观察和检测组分的斑点。
叶绿体色素的提取分离和理化性质实验报告

生物学导论实验报告叶绿体色素的提取分离和理化性质一、提取与分离1、实验目的学习应用薄层色谱法分离叶绿体色素的实验方法。
2、实验原理提取:叶绿体色素为有机酯类化合物,根据相似相容原理,常用有机溶剂提取。
如酒精、丙酮、乙酸乙酯、氯仿等。
分离:薄层层析法是将吸附剂均匀的涂抹在玻璃板上形成一薄层,将此吸附剂薄层作为固定相,把待测分离的样品溶液点在薄层板的下端,然后用一定量的溶剂作流动相,将薄层板的下端浸入到展开剂中。
流动相通过毛细管作用由下而上逐渐浸润薄层板,并带动样品在板上也向上移动,样品中各组成分在吸附剂和展开剂之间发生连续不断的吸附、脱吸附、再吸附……的过程。
由于吸附剂对不同物质的吸附能力大小不同,吸附能力强的物质相对移动慢一些,儿媳妇能力弱的物质相对移动快一些,从而使各组分有不同移动速度而彼此分开。
3、实验材料与试剂(1)新鲜的菠菜叶;(2)体积分数为95%的乙醇,碳酸钙粉末、展开剂(3)钵体、漏斗、三角瓶、剪刀、点样本、毛细管、层析缸、硅胶预制板、滤纸。
4、实验步骤(1)色素提取液的制备取叶4~5片新鲜叶片,洗净,擦干叶表面,去中脉剪碎,放入钵体中。
加入少量碳酸钙,加2~3ml体积分数为95%的乙醇,研磨至糊状,再加入10ml乙醇,上清液过滤,残渣再用10ml乙醇冲洗过滤。
(2)叶绿体色素的分离取硅胶预制板一个,用点样毛细管取上述提取液,平行于硅胶板的短边,距下边缘1cm处用毛细管划线,风干,重复操作3~4次;在干燥的层析缸中加入适量展开剂,高度0.5cm,将硅胶预制板带有色素一端放入,使其下端浸入展开剂中;当色素较好分离,展开剂前沿接近硅胶预制板的上端边缘时,取出,画线。
Rf=斑点中心到原点距离/溶剂前沿到原点距离5、实验结果与分析从上至下为胡萝卜素(橙色):Rf=6.95/7.35=0.946叶绿素a(蓝绿色):Rf=5.35/7.35=0.728叶绿素b(黄绿色):Rf=4.95/7.35=0.673叶黄素(黄色):Rf=4.10/7.350.558可知,胡萝卜素、叶绿素a、叶绿素b、叶黄素极性依次增大,与硅胶吸附能力依次增强。
叶绿素的提取分离及理化性质

叶绿素的提取分离及理化性质实验人:张建宇2011010780 汽车系14班实验时间:2011年10月29日实验地点:生物馆普生实验室实验合作人:王博远实验名称:叶绿素的提取分离及理化性质实验原理:叶绿体中的叶绿素a,叶绿素b,胡罗卜素,叶黄素与类囊体膜结合成的色素蛋白复合体不溶于水,而溶于有机溶剂,固可用乙醇等有机溶剂提取,提取液可用薄层色谱法加以分离和鉴别。
实验材料:1.新鲜的菠菜叶片。
2.体积分数为95%的乙醇,碳酸钙粉末,展开剂。
3.天平,研钵,漏斗,三角瓶,剪刀,点样毛细管,层析缸,硅胶预制板,滤纸。
实验步骤:(一)色素的提取:1.取新鲜叶片洗净,擦干表面,剪碎,放入研钵中。
2.加入少量的碳酸钙,加2-3ml的95%的乙醇,研磨至糊状,再加10-15ml的95%的乙醇,过滤上清液,残渣再用10ml的95%的乙醇冲洗一次,一同过滤到三角瓶中,制成了叶绿体色素的提取液。
(二)色素的分离:1.用点样毛细管取上述清液,在平行于硅胶板的短边,局下边缘1cm处用毛细管划线,等干了之后重复上述操作3-4遍;2.在层析钢中加入0.5cm高的,将有色素的一段放入,使其下端侵入展开剂中。
迅速的盖好层析缸盖;3.当各种色素得到较好的分离,展开剂前沿接近硅胶预制板上端的时候,取出硅胶预制板,并迅速用铅笔标出展开剂前沿和各条色素带的位子。
实验结果:溶剂前沿至原点的距离:7.7cm实验讨论:这个实验让我们明白了构成叶绿素的色素主要有4种,我们可以根据它们在层析液中的溶解度不同来提取分离它们,并能够进行进一步的研究。
课上老师讲了叶黄色的保健作用,说明了我们今天做的这个实验是很有现实意义和医学价值的,不过因为我们是初次接触到这类试验,可能在操作的熟练度上还有很大的欠缺。
不过我相信只要我们认识到了这样一个小小的实验也是包含着很大的科学奥秘,通过这个实验的探究我们能够造福更多的人,那么我想我们会在这个上面有更大的专研和思考。
绿叶菜中主要色素的提取和鉴定

一、实验目的
1. 掌握 用薄层色谱法提取和鉴定绿叶菜中天 然色素的方法。 2. 掌握薄层色谱的分离原理和操作技术。
பைடு நூலகம்
二、实验原理
绿叶菜中含有叶绿素、胡萝卜素、叶黄素等多种天然色素。 叶绿素是吡咯衍生物与镁的配合物,包括叶绿素a和叶绿 素b两种异构体。 叶绿素是植物进行光合作用不可缺少的催化剂,通常在植 物中叶绿素a的含量是叶绿素b的3倍。 胡萝卜素呈橙黄色,属于四萜类化合物,有α、β、γ三种 异构体,一般在植物体中β-胡萝卜素的含量最多。
色斑最高浓度中心至原 点中心的距离 展开剂前沿至原点中心 的距离
Rf值计算示意图 1.起点线; 2. 展开剂前沿 a. 色斑最高浓度中心至原点中心的距离 b. 展开剂前沿至原点中心的距离
Rf
a Rf b
三、实验用品
1. 仪器 恒温水浴器、 烘箱、 顶载天平(精确至0.01g)、 层析缸(高8 cm,内径3.0 cm)、干燥器、 梨形分液漏斗(60mL)、 循环 水式真空泵、滤过漏斗 (3号,60mL)、 抽滤瓶、 研钵、 载 玻片(2.5cm×7.5cm)、 点样用毛细管(1mm)、 研钵或粉 碎机、 锥形瓶(50 mL)、量筒(10mL)、 刻度试管 2. 试剂 硅胶G(300目~400目)、 石油醚(60~90℃)、 95%乙醇、 丙酮、 乙酸乙酯、 无水Na2SO4、 饱和NaCl,均为化学纯试剂。 蒸馏水 3. 其他 滤纸、 剪刀、 镊子、 酒精棉球、 刻度尺、 铅笔、 新鲜绿叶菜
四、实验步骤
1. 绿叶菜中色素的提取 将绿叶菜洗净后,用滤纸吸干叶片表面附着的水珠。称取5g左右的绿叶菜, 剪碎后放入研钵中,加入10mL石油醚-乙醇混合液(V:V = 2:1),研磨萃 取,抽滤。滤渣重复萃取一次,合并提取液。 将提取液转移至60mL分液漏斗中,加入10mL饱和NaCl溶液除去水溶性物 质,弃去水-乙醇层,加入10mL蒸馏水洗涤,重复洗涤一次,弃去水层。 石油醚层转入已装有少量无水Na2SO4的50mL锥形瓶中,干燥约15min后将 石油醚转移至刻度试管中,水浴加热浓缩至约1mL。
普通生物学实验实验报告叶绿素的提取分离与理化性质

普通生物学实验实验报告一、实验名称叶绿素的提取分离与理化性质二、实验目的1.学习应用薄层色谱法分离叶绿体色素的实验方法2.验证叶绿体色素的多种理化性质三、实验原理1.叶绿素中的叶绿素a、叶绿素b、胡萝卜素和叶黄素是色素蛋白复合体,不溶于水而易溶于有机溶剂,可以用乙醇进行提取。
2.由于硅胶板的吸附剂对不同色素的吸附能力不同,不同色素在展开剂中的溶解度不同,因而叶绿素提取液进行薄层层析时各组分移动速度不同而分开,因此可以用薄层层析法对色素进行分离,进而对色素进行观察鉴别。
3.叶绿素是由叶绿酸与甲醇和叶绿醇形成的复合酯,能与碱性物质发生皂化反应生成甲醇和叶绿醇及能溶于水的叶绿酸盐,从而绿色素和黄色素分离。
4.叶绿素可以吸收光量子变成不稳定的激发态,当它变回基态时可发射红光量子产生荧光。
5.叶绿素的化学性质不稳定,在强光照下易被破坏,类胡萝卜素则较稳定。
6.叶绿素中的镁可被氢离子取代生成绿色的去镁叶绿素。
去镁叶绿素可与铜离子反应生成稳定的铜代叶绿素。
四、实验仪器和材料1.新鲜的菠菜叶片。
2.体积分数为95%的乙醇,碳酸钙粉末,展开剂。
3.天平,研钵,漏斗,三角瓶,剪刀,毛细玻璃管,层析缸,硅胶预制板,滤纸。
4.刻度试管,小试管,试管架,水浴锅,10mL移液管。
5.苯,醋酸铜粉末,质量分数为5%的稀盐酸,醋酸-醋酸铜溶液,氢氧化钾-甲醇溶液。
五、实验步骤1.叶绿素提取液的制备2.叶绿体色素的分离3.光对叶绿素的破坏作用取两只小试管,各加入2.5mL 的叶绿素提取液和2.5mL 的95%乙醇。
一支试管放在直射阳光下,另一支试管用锡箔纸包严,均静置40分钟。
4.皂化作用5.H 离子和Cu 离子对叶绿素Mg 离子的取代作用1) 取两只试管,试管1中加入5mL 叶绿素提取液作为对照。
试管2中加入5mL叶绿素提取液后再加入质量分数为5%的盐酸数滴并摇匀,当溶液变褐后再加入少量醋酸铜粉末,60℃水浴加热,观察溶液颜色变化并和试管1比较。
薄层色谱原理(硅胶吸附)

薄层色谱原理及应用的一点心得薄层色谱鉴别为我们在中药质量控制中常用的定性鉴别方法,有关的原理及小知识总结如下。
一、小知识薄层色谱常用的硅胶较细,一般粒度在10~40μ,而柱层析常用的粒度为100~160目。
我们在试验中也常用到的硅胶板其成分及组成如下硅胶板硅胶G-高效板硅胶粉煅石膏(12%~13%的石膏(CaS04)),硅胶H-高效板硅胶粉硅胶GF254-高效板硅胶粉煅石膏12%~13%的石膏(CaS04) 254nm下吸收的荧光物质硅胶GF365-高效板硅胶粉煅石膏12%~13%的石膏(CaS04) 365nm下吸收的荧光物质手铺板硅胶粉12%~13%的石膏(CaS04) 一般加入3%CMC-钠为黏合剂二、薄层色谱原理薄层色谱是吸附色谱,其过程实际上是组分的分子与展开剂的分子竞争占据吸附剂表面活性中心的过程,所以展开剂的选择应同时考虑被测物质的性质,吸附剂的活性及展开剂的极性三个因素。
2.以硅胶作为吸附剂为例,其过程实际上是组分的分子与展开剂的分子竞争占据吸附剂表面活性中心的过程,硅胶是极性吸附,根据相似相溶原理,如果选择极性大的展开剂,展开剂与硅胶吸附能力增强,则组分相对吸附能力下降,则容易被展开或洗脱下来;如果组分的极性比展开剂的极性大,则组分与硅胶的吸附能力较展开剂强,则不容易被展开或洗脱下来。
所以说在用极性吸附剂如硅胶,氧化铝时,选用极性大的展开剂(相对于组分来说)均可以使组分跑到前沿。
常用的展开系统石油醚-乙酸乙酯,氯仿-甲醇-水,乙酸乙酯-甲醇,正丁醇-乙酸-水,极性由小到大,还有看你的物质,比例自己可以摸索,还有如果你的物质偏酸性,可加点甲酸,偏碱性,可用碱板来爬,或者用氨水饱和后再展开。
三、在应用中的一点体会1、争宠我们把硅胶比作皇帝,硅胶极性大,根据相似相溶原则,喜欢极性大的,就好比,皇帝喜欢丰满的妃子,比如杨贵妃,是待分离组分,很丰满,极性大,而田贵妃是流动相,比杨贵妃瘦,极性小,皇帝不喜欢他,田贵妃就离皇帝远远的,也就是说,硅胶(即皇帝)更喜欢杨贵妃-待测组分,因而很不容易被展开,Rf值小。
实验1 叶绿素提取试验

实验1 叶绿素提取试验实验一绿色植物色素的提取及分离一、实验目的与要求1、通过绿色植物色素的提取与分离,了解天然物质分离提纯的方法。
本原理及操作技术,加深了解微量有机物色2、学习薄层色谱和柱色谱分离的基谱分离、鉴定的原理。
二、实验原理绿色植物(如菠菜)叶、茎中含有叶绿素(绿)、胡萝卜素(橙)和叶黄素(黄)等多种天然色素。
叶绿素存在两种结构相似的形式即叶绿素a(CHONMg)557254和叶绿素b(CHONMg),其差别仅是叶绿素a中一个甲基被甲酰基所取代而形成557064 了叶绿素b。
它们都是吡咯衍生物与金属镁的络合物,是植物进行光合作用所必需的催化剂。
也是使用的绿色色素,可用于糕点、饮料水中,添加于胶姆糖中还可以消除口臭。
植物中叶绿素a的含量通常是叶绿素b的三倍。
尽管叶绿素分子中含有一些极性基团,但大的烃基结构使它易溶于醚、石油醚等一些非极性的溶剂。
胡萝卜素(CH)是具有长链结构的共轭多烯。
它有三种异构体,即α-胡4056 萝卜素、β-胡萝卜素和γ-胡萝卜素,其中β-胡萝卜素含量最多,约占胡萝卜素的78%,也最重要。
在生物体内,β-胡萝卜素受酶催化氧化可转化成维生素A。
目前,β-胡萝卜素已进行工业生产,可作为维生素A使用,也可作为食品工业中的色素。
叶黄素(CHO)是胡萝卜素的羟基衍生物,它在绿叶中的含量通常是胡萝40562 卜素的两倍。
与胡萝卜素相比,叶黄素较易溶于醇而在石油醚中溶解度较小。
本实验先根据各种植物色素的溶解度情况将胡萝卜素(橙)、叶黄素(黄)、叶绿素a和叶绿素b从菠菜叶中提取出来,然后根据各化合物物理性质的不同用色谱法进行分离和鉴定。
薄层层析时,上述化合物的展开速度不同;柱层析时,流出速度有差异,可被极性不同的溶剂洗脱。
RNN 2+Mg NNCH 叶绿素a(R=CH) 32OCOOCHCH叶绿素b(R=CHO) 23COORRβ-胡萝卜素(R=H) 叶黄素(R=OH)CHOH2维生素A色谱法是分离、提纯和鉴定有机化合物的重要方法。
绿色植物中色素的提取和分离薄层色谱和柱色谱

四、实验步骤
3. 柱色谱分离色素:
(1) 用10g中性氧化铝和石油醚装层析柱。
(2) 将菠菜色素浓溶液用滴管小心加到层析柱顶部。 加完后打开下部活塞,让液面下降到柱面以下1mm左 右关闭活塞。加入数滴石油醚,重新打开活塞使液 面下降,重复几次使有色物质全部进入柱体内。
(3) 依次用不同洗脱剂进行洗脱,收集各色带。
上页 下页 返回 退出
各洗脱剂对应的色带
石油醚-丙酮(9:1体积比)混合液 胡萝卜素(橙黄色)
石油醚-丙酮(7:3体积比)混合液 叶黄素(黄色) 丁醇-乙醚-水(3:1:1体积比)混合液 叶绿素a(蓝绿色)和叶绿素b(黄绿色)
上页 下页 返回 退出
五、注意事项
1. 甲醇有毒,请在通风良好处使用;
上页 下页 返回 退出
洗脱剂
柱色谱原理:
混合物上页 下页 返回 源自出吸附剂常用吸附剂有氧化铝、硅胶、氧化镁等。 吸附剂对化合物的吸附能力与分子的极性有 关,极性越强,吸附能力越大,分子中含有 极性较大的基团,其吸附能力也越强。
氧化铝对下列化合物的吸附性: 酸、碱>醇、胺、硫醇>酯、醛、酮> 芳香族化合物>卤代物、醚>烯烃>饱和烃
原理及其操作方法。
上页 下页 返回 退出
二、实验原理
绿色植物如菠菜叶中含有叶绿素(绿)、胡萝卜 素(橙)和叶黄素(黄)等多种天然色素。 通过柱色谱(层析)和薄层色谱(层析)对菠菜 叶中的上述几种色素进行分离。
提问
叶绿素a、叶绿素b、胡萝卜素和叶黄素极性 次序为何?
上页 下页 返回 退出
R
N Mg N
上页 下页 返回 退出
三、试剂及仪器
[Word]叶绿素的提取和薄层色谱
![[Word]叶绿素的提取和薄层色谱](https://img.taocdn.com/s3/m/abcdf14c551810a6f424866f.png)
[Word]叶绿素的提取和薄层色谱叶绿素的提取和薄层色谱植物光合作用是自然界最重要的现象,它是人类所利用能量的主要来源。
在把光能转化为化学能的光合作用过程中,叶绿体色素起着重要的作用。
高等植物体内的叶绿体色素有叶绿素和类胡萝卜素两类,主要包括叶绿素a、叶绿素b、β?胡萝卜素和叶黄素四种。
它们所呈现的颜色和在叶绿体中含量大约比例见表12.1。
叶绿素(chlorophylls)是叶绿酸的酯,它在植物进行光合作用中吸收可见光,并将光能转变为化学能。
叶绿素是植物进行光合作用所必需的催化剂。
在绿色植物中叶绿素主要以叶绿素a(CHONMg)和叶绿素b(CHONMg)两种结557254557064构相似的形式存在,其差别仅是叶绿素a中一个甲基被叶绿素b中的甲酰基所取代。
叶绿素的基本结构见图47.1。
在叶绿素分子结构中含有四个吡咯环,它们由四个甲烯基联结成卟啉环,在卟啉环中央有一个镁原子,它以两个共价键和两个配位键与四个吡咯环的氮原子结合成内配盐,形成镁卟啉。
在叶绿素分子中还有两个羧基,其中一个与甲醇酯化成COOCH,另一个与叶绿醇酯化成COOCH32039长链。
类胡萝卜素(carotenoids)是一类不饱和的四萜类碳氢化合物(例如胡萝卜素,carotenes),或它们的氧化衍生物(例如叶黄素类,xanthophylls)。
所有的类胡萝卜素均源于非环状的CH结构。
类胡萝卜素在强光下可防止叶绿素的光4056氧化;在弱光下,可作为辅助色素吸收光能并传递给叶绿素分子。
胡萝卜素有三种异构体,即α?、β?和γ?胡萝卜素,其中β?胡萝卜素含量最多,也最为重要。
β? 胡萝卜素还具有维生素A的生理活性,其结构是由两分子维生素A 在端链失去两分子水结合而成。
在生物体内,β?胡萝卜素受酶催化氧化即形成维生素A。
叶黄素(3,3`-二羟基-α-胡萝卜素,lutein,CHO)是一种常见的40562氧化型的类胡萝卜素。
β?胡萝卜素和叶黄素均属于脂溶性化合物。
生物化学实验一:可溶性糖的硅胶G薄层层析

生物化学实验一:可溶性糖的硅胶G薄层层析指导教师:李玉芹一、目的1. 学会薄层板的制备方法和薄层层析操作。
2. 学会比移值Rf的测定方法二、原理层析法又叫色谱法,是分离、提纯和鉴定混合物各组分的一种重要方法,有极广泛的用途。
它是一种物理化学分离方法,利用混合物各组分的物理化学性质的差异在两相间的分配比不同而进行分离。
其中一相是固定相,另一相是流动相。
常用的色层分离法有薄层层析、柱层析、纸层析和气相色谱法等。
薄层层析(Thin Layer Chromatography)常用TLC表示,兼有柱层析和纸层析的优点,是近年来发展起来的一种微量、快速而简单的分离方法。
它是将吸附剂(固定相)均匀地铺在一块玻璃板表面上形成薄层(其厚度一般为0.1mm~2mm),在此薄层上进行色谱分离。
由于混合物中的各个组分对吸附剂的吸附能力不同,当选择适当的溶剂(被称为展开剂,即流动相)流经吸附剂时,发生无数次吸附和解吸过程,吸附力弱的组分随流动相向前移动,吸附力强的组分滞留在后,由于各组分具有不同的移动速率,被流动相带到薄层板不同高度,最终得以在固定相薄层上分离。
这一过程可表示为:化合物在固定相K化合物在流动相平衡常数K的大小取决于化合物吸附能力的强弱。
一个化合物愈强烈地被固定相吸附,K值愈低,那么这个化合物随着流动相移动的距离就愈小。
薄层层析除了用于分离外,更主要的是通过与已知结构化合物相比较来鉴定少量有机物的组成。
此外,薄层层析也经常用于寻找柱层析的最佳分离条件。
试样中各组分的分离效果可用它们比移值Rf的差来衡量。
Rf值是某组分的色谱斑点中心到原点的距离与溶剂前沿至原点距离的比值,即Rf =ab,Rf值一般在0~1之间,当实验条件严格控制时,每种化合物在选定的固定相和流动相体系中有特定的Rf 值。
Rf值大表示组分的分配比大,易随溶剂流下。
混合样品中,两组分的Rf相差越大,则它们的分离效果越好。
应用薄层层析进行分离鉴定的方法是将被分离鉴定的试样用毛细管点在薄层板的一端,样点干后放入盛有少量展开剂的器皿中展开。
可溶性糖的硅胶G薄层层析

可溶性糖的硅胶G 薄层层析一、实验目的1.了解薄层层析测定可溶性糖的原理。
2.掌握硅胶G 薄层层析的操作方法。
二、实验原理薄层层析(简称TL C)是一种微量而快速的层析方法,是在吸附剂或支持剂均匀涂布的薄层上进行的,故称薄层层析。
为了使所要分析的样品各组分得到分离,必须选择合适的吸附剂。
硅胶、氧化铝和聚酰胺是广泛采用的吸附剂,硅藻土和纤维素是分配层析中常用的支持剂,在吸附剂或支持剂中添加合适的粘合剂后再涂布,可使薄层紧贴在玻璃板上。
硅胶G 是一种添加了粘合剂的硅胶粉,约含12%~13%的石膏(C aS04),它可以把一些物质从溶液中吸附于自身表面。
利用它对各种物质吸附能力的不同,再用适当的溶剂系统展层,使不同的物质得以分离。
例如,糖在硅胶G 薄层上的移动速度与糖的相对分子质量和羟基数有关,经过适当的溶剂展开后,糖在薄板上的移动速度是戊糖>己糖>双糖>三糖。
对已分开的斑点显色,而将与它位置相当的另一个末显色的斑点从薄层上与硅胶G 一起刮下,以适当的溶剂将糖从硅胶G 上洗脱下来,就可用糖的定量测定方法测出各组分的含糖量。
薄层层析与其他方法比有明显的优点:层析时间短、样品用量范围大(1μg~0.5g)、观察结果方便、可以分离多种化合物等,其灵敏度比纸层析高10~100倍,显色方法甚至可以用腐蚀性显色剂。
而且薄层层析法操作方便,设备简单,所以薄层层析法目前应用范围相当广泛。
三、仪器和试剂仪器烘箱、吹风机、薄层玻板(20cm×20cm)、分光光度计。
试剂1.1%糖标准溶液:取木糖、葡萄糖、果糖和蔗糖各l00mg,分别用75%的乙醇定容10mL,使其浓度均为10mg/mL。
