人教版化学第六章有机化学课件PPT
有机化学课件-6烯烃
三、烯烃的命名(CCS系统命名法): (一)命名原则:
1. 主链选择:含碳碳双键(官能团)在内的最长碳链作为主链;
如:CH3CH2CH2CH2C=CH2 (√) CH2CH2CH(3 没有把碳碳双键都包含在内)
2-丙基-1-己烯 或2-丙基己烯(官能团处于1位时可省略去位次)
2. 主链编号:使碳碳双键处于尽量小的编号;
2×7 +2 - 8
,C7H8 ,Ω=
=4; 三个C=C和一个环
2
CH3CH2OH ,C2H6O ,Ω=
O
CH3C NH2,C2H5ON ,Ω=
2×2 +2 - 6
=0
2 2×2 +2 - 5 +1
=1
2
二、烯烃的同分异构: (一)构造异构:
如分子式为 C4H8 的烯烃的构造异构体有: CH3 CH3CH2CH=CH2 ,CH3CH=CHCH3 ,CH3C=CH2
CH3 CH
CH3
CH2CH3
C H
(E)-2,3-二甲基-3-己烯
和顺反命名法相比较,顺式的可能是Z构型的,也可能是E构型;
§2 烯烃的相对稳定性
一、燃烧热:
燃烧热kJ/mol
稳定性
例: CH3CH2CH=CH2
2718
H3C
CH3
CC
2711
HH
H3C
H
CC
2708
H
CH3
高
烯烃中碳碳双键上的烷基越多,稳定性越高;
6 CH3 如:CH3CH2CH=CHCH2CHCHCH3
1 2 3 4 5 CH37 8
6,7-二甲基-3-辛烯
3. 标明双键的位次;只写双键两个碳原子中位次较小的一个,放
有机化学课件

定义
烷烃是一类仅由碳和氢两种元素组成 的有机化合物,分子中的碳原子都以 单键相连,其余的价键均用于与氢原 子结合,达到“饱和”。
命名
根据碳链的长度,分别称为甲烷、乙 烷、丙烷等。对于含有支链的烷烃, 采用“基数命名法”,并标注支链位 置。
性质
烷烃具有较低的沸点、熔点和密度, 不溶于水,化学性质相对稳定,主要 发生取代反应。
醛、酮、醌
醌的分类和命名
醌是含有两个羰基的六元环状化合物,根据取代基的不同 ,醌可分为苯醌和萘醌等。醌的命名遵循系统命名法。
醌的物理性质
醌通常为固体,颜色较深,具有特殊的气味。
醌的化学性质
醌具有较高的化学稳定性,可发生亲电取代反应和亲核加 成反应等。
羧酸及其衍生物
羧酸的分类和命名
羧酸是羧基与氢原子和一个烃基相连的化合物,根据烃 基的不同,羧酸可分为脂肪酸和芳香酸。羧酸的命名遵 循系统命名法。
胺的化学性质
胺类化合物具有碱性,可以与 酸反应生成盐;同时胺类化合 物还具有还原性,可以被氧化
剂氧化。
重氮和偶氮化合物
重氮化合物的定义和性质
重氮化合物是一类含有重氮基(-N=N-)的有机化合物,具有不稳定 性,容易发生分解反应。
偶氮化合物的定义和性质
偶氮化合物是一类含有偶氮基(-N=N-)的有机化合物,通常为有色 物质,具有良好的染色性能。
醚的化学性质
醚可发生开裂反应、氧化反应等,其反应活性受氧原子和烃基结 构的影响。
醛、酮、醌
醛的分类和命名
醛是羰基与氢原子和一个烃基相连的化合物,根据烃基的不同, 醛可分为脂肪醛和芳香醛。醛的命名遵循系统命名法。
醛的物理性质
醛的沸点、熔点和密度等物理性质与烃类相似,但受羰基影响,其 性质有所差异。
有机化学课件
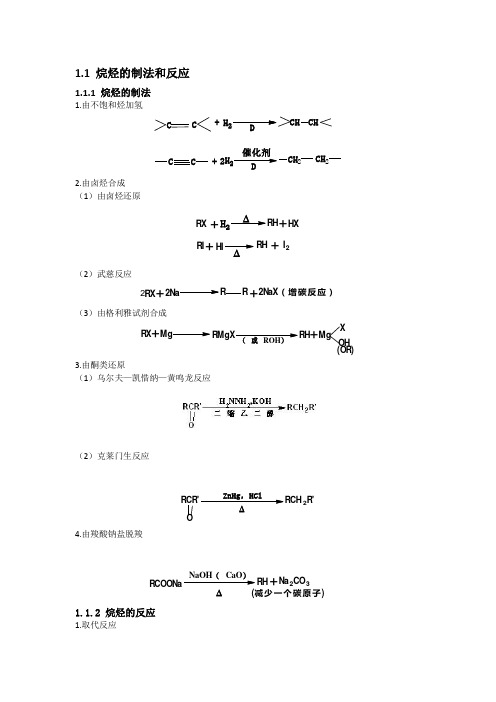
1.1 烷烃的制法和反应1.1.1 烷烃的制法1.由不饱和烃加氢C C+H 2CHCHCC+H 22D DCH 2CH 22.由卤烃合成 (1)由卤烃还原RX+H 2RHHX +RI HI+∆RH +I 2∆(2)武慈反应R X2+2N aRR2N aX (增碳反应)+ (3)由格利雅试剂合成RX+MgRMgX(或ROH )RH +MgX OH (OR)3.由酮类还原(1)乌尔夫—凯惜纳—黄鸣龙反应(2)克莱门生反应RCR'O2R'4.由羧酸钠盐脱羧NaOH (CaO )∆RH +Na 2CO 3(减少一个碳原子)1.1.2 烷烃的反应1.取代反应RH +X2光RX +HX (反应活性3'H>2'H>1'H>CH 4)例CH 3CH 2CH 3Cl 2光CH 3CH CH 3Cl+CH 3CH 2CH 2Cl(57%)(43%)2.氧化反应 (1)完全氧化CH 4+2O CO 2+2H 2O +热能(2)部分氧化RCH 2CH 2O 2,锰盐RCOOH +R'COOH (可制肥皂)4CH 4+O 21500C CH CH+2CO +7H 2O(3)裂化反应CH 3CH 2CH 2CH 3C H 2CH 2+C H 3CH 3+CH 3CH 2CH=CH 2+H 2+CH 4+CH 2CH 3(4)异构化反应CH 3CH 2CH 2CH 3AlBr 3 HBrCH 3CHCH 3CH 320%80%1.2 烯烃的制法和反应1.2.1烯烃的制法1 烷烃脱氢C C H H催化剂∆-H2C C (适合于简单烯烃,通常得混合物)CH3CH2CH2CH3Pt,500C CH3CH2CH=CH2+CH3CH3HH+CH3CH3H H+CH2=CHCH=CH2+H22.卤烷脱卤化氢C CX碱,热-HXC CHHHCl(CH3)3CO-K+3.醇脱水4.霍夫曼消除5.由炔烃加氢6.魏梯希反应1.2.2烯烃的反应1.烯烃的亲电加成(2)加水直接水合间接水合以上都符合马氏规律硼氢化-氧化反应(3)加卤素(4)加次卤酸2.烯烃的催化氢化CH3CH2H2,Pt CH3CH2CH33与碳烯加成CC+CC CC (X,Y=H,Cl,Br,I 或COOEt)+CHCl 3(CH 3)3COK+Cl4烯烃的氧化(1) 烯烃的环氧化C C+21O2CC OCH 2CH 2+21O 2O环氧丙烷C C+RCOOH C C O+RCOHCH 3CH CH 2+CH3OCH 2H 3CHCO+CH 3COOH(2) 高锰酸钾氧化C C稀KMnO OH C C (或OsO 4,H 2O 2)RCHCH KMnO R CO +CO 2+H 2OCH 3CH 2CH CH 2KMnO CH 3CH 2C O+CO 2+H 2OCR O+CR'OHORC RR C R'KMnOCH 3CHCCH 3CH 3KMnO 4CH 3COHO+CH 3CH 3O5烯烃的臭氧化反应C RR C R'+O 3OO COC RRR'H H 2ORO +CR'H ORCH 3CHCH CH 32Zn ,H 2OCH 3CHO +CH 3CH 3O6聚合反应nCH 2CH2>100℃,100MPaCH 2CH 2nn>100nCH 3CH CH 2烷基铝-三氧化钛50℃,1MPaCH3CH 2n7烯烃的a 氢原子反应(1) 卤代C Ha 氢+X 2C X+HX(或NBS)+NBSBr(2) 氧化烯烃的a氢易被氧化,在不同条件下,得到不同产物:CH 3CHCH 2+O 2CuO 370℃CH 2CHCHOCH 3CH CH 2+23O 磷钼酸铋 0.7~1.4MPa CH 2CHCOOHCH 3CHCH 2+NH 3+23O 2磷钼酸铋470℃2CHCN +3H 2O1.3 炔烃的制法和反应1.3.1 炔烃的制法1.金属炔化合物与卤烷反应RCC -Na ++R'XS N 2RCCR'+X -(1。
有机合成化学:第六章 缩合反应
第六章 缩合反应
上例是由于选择不同的起始原料,而选择不同的合成路线,使 产品成本大大降低。如果没有很好的路线选择时,可以通过优化 反应条件,提高产物的收率,降低成本。从产品收率上讲,能提 高1-5%。我们可能认为没什么意义,可对企业讲,产品成本会降 低2-8%左右。如果一个产品产值上亿时,可估算一下其价值了。 所以,一个化工产品刚上市时价格较高,随着生产时间延长,价 格逐渐降低,很大可能是由于生产工艺和生产条件的改变所致。
-CO2
CH3CH CH2CO2H
H3C
O O O
60~76%
CH3NO2 + H3CCH
C H
CO2C2H5
NaOC2H5 CH3CH CH2CO2C2H5
55%
CH2NO2
第六章 缩合反应 CH3
CN
PhCH CO2C2H5 + H2C
C H
CN
KOH 83%
CN
PhC CH2CH2CN CO2C2H5
LDA
H3C
CH3
第六章 缩合反应
羰基化合物烷基化最大负反应是O-烷基化产物。如:
副产物
第六章 缩合反应
LDA CH3(CH2)3CO2CH3 BrCH2CH
CH2
CH3CH2CH2CH CO2CH3 CH2CH CH2
LDA
CH2CH3
C2H5Br CH3CH2Байду номын сангаас CO2CH3
可以分步引入
90%
5. Knoevenagel反应:
这类反应的特点是一个亚甲基上连接两个吸电子基团,使
得其氢活性明显提高,反应较易进行。一般使用弱碱 (有机胺)
高中化学ppt课件

酸碱盐反应与性质
酸的性质
酸具有酸性和腐蚀性,能 与碱发生中和反应,生成 盐和水。
碱的性质
碱具有碱性和腐蚀性,能 与酸发生中和反应,生成 盐和水。
盐的性质
盐具有咸味和腐蚀性,能 与酸或碱发生化学反应。
其他化学反应类型
氧化还原反应
指有电子转移的化学反应,包括 氧化反应和还原反应。
水解反应
指在水溶液中,弱酸或弱碱离子 与水电离出的氢离子或氢氧根离 子结合生成弱电解质的反应类型
化学与健康生活的联系
详细描述
化学与我们的健康生活密切相关。它不仅可 以提供许多营养物质和药物,还可以帮助我 们了解人体的生理和生化过程。例如,许多 营养物质和药物都需要通过化学反应来生产 和作用。同时,化学还可以提供许多先进的 医疗技术和材料,例如高分子材料、药物载 体和生物材料等。
化学与健康生活
有机化学在日常生活中的应用
制药行业
有机化学在制药行业中有着广 泛的应用,如抗生素、抗病毒 药物、抗肿瘤药物等的合成和
生产。
农业领域
有机化学在农业领域中也有着 广泛的应用,如农药、化肥、 植物生长调节剂等的合成和生 产。
食品工业
有机化学在食品工业中也有着 广泛的应用,如食品添加剂、 调味品等的合成和生产。
材料科学
有机化学在材料科学中也有着 广泛的应用,如塑料、橡胶、
纤维等的合成和生产。
05
CATALOGUE
第五章 化学与生活
化学与能源利用
总结词
化学在能源利用中的重要性
详细描述
化学在能源利用中扮演着至关重要的角色。它不仅可以提 供清洁、高效的能源,还可以提高能源的转化率和利用率 。例如,通过化学反应可以将太阳能转化为电能或燃料, 同时也可以将化石燃料转化为热能或电能。
有机化学ppt课件完整版

重排反应通常发生在含有不稳 定结构或官能团的化合物中, 需要加热或加入催化剂。在重 排过程中,分子的骨架结构可 能发生变化。
重排反应在有机合成中具有重 要的应用价值,可以用于合成 具有特定结构或官能团的有机 化合物。同时,重排反应也是 研究有机化合物结构和性质的 重要手段之一。
08
有机化学在生活中的应 用
定义
特点
加成反应在有机合成中具有重要的应用价值,可以用 于合成各种烯烃、醇、醛、酮等有机化合物。
应用
加成反应通常发生在分子中的不饱和键上,需要一定 的反应条件和催化剂。
消除反应
定义
消除反应是指有机化合物分子中 失去一个小分子(如水、卤化氢
等),形成不饱和键的反应。
种类
包括脱水消除、脱卤化氢消除、 热消除等。
反应。此外,醇还可以与酸反应生成酯,是重要的有机合成原料。
酚类化合物结构与性质
结构特点 酚类化合物的分子中含有苯环和羟基(-OH)官能团,通 式为Ar-OH,其中Ar为苯基或其衍生物。
物理性质 酚类化合物一般为无色或淡黄色的固体或液体,具有特殊 的气味和较强的毒性。酚的熔点和沸点较高,易溶于有机 溶剂。
化学性质
03
可发生加成、氧化、还原等反应,如与氢气加成生成醇,被弱
氧化剂氧化成酸。
酮类化合物结构与性质
结构特点
羰基(C=O)两侧连接烃基或芳基,无双键性质。
物理性质
沸点较高、难溶于水、易溶于有机溶剂。
化学性质
主要发生加成和还原反应,如与氢气加成生成醇,被还原剂还原 成仲醇。
醌类化合物结构与性质
结构特点
04
醇、酚、醚类化合物
醇类化合物结构与性质
01
结构特点
高中化学有机化学ppt课件

03有机物主要由碳、氢元素组成,还可能含有氧、氮、硫、磷等元素;无机物则可能包含各种元素。
组成元素有机物分子结构复杂,具有同分异构现象;无机物分子结构相对简单。
结构特点有机物大多具有可燃性、难溶于水、反应速率较慢等性质;无机物性质各异,有些具有与有机物相似的性质。
性质特征有机物与无机物区别古代人们对天然动植物和矿物的利用,如木材、药材、染料等。
萌芽时期18世纪末至19世纪初,贝采利乌斯等化学家提出有机化学概念,并合成尿素等有机化合物。
创立时期19世纪中后期,合成染料、香料、药物等有机化合物的出现,推动了有机化学的快速发展。
发展时期20世纪以来,随着物理和化学方法的不断进步,有机化学在合成、结构、反应机理等方面取得了巨大成就。
现代时期有机化学发展简史有机化合物分类及命名分类根据碳骨架形状,有机化合物可分为链状化合物和环状化合物;根据官能团类型,可分为烃类、醇类、醛类、酮类、羧酸类等。
命名有机化合物的命名遵循一定的规则和原则,包括选取主链、编号原则、官能团优先顺序等。
常见的命名法有普通命名法、系统命名法和衍生命名法等。
01结构特点碳原子间以单键相连,其余价键被氢原子饱和。
02物理性质随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
03化学性质相对稳定,主要发生取代反应,如卤代反应。
含有一个或多个碳碳双键。
结构特点物理性质化学性质随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
较为活泼,可发生加成反应、氧化反应、聚合反应等。
030201含有一个或多个碳碳三键。
结构特点随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
物理性质非常活泼,可发生加成反应、氧化反应、聚合反应等。
化学性质1 2 3含有苯环或其他芳香环结构。
结构特点具有特殊芳香味,沸点、熔点较高,密度较大。
物理性质相对稳定,可发生取代反应、加成反应等。
化学性质芳香烃结构和性质卤代烃结构和性质卤代烃的分子结构由烃基和卤素原子组成,卤素原子与烃基通过共价键连接。
有机化学PPT课件

目录
• 有机化学简介 • 有机化学基础知识 • 有机化学反应 • 有机化学的应用 • 有机化学的未来发展
01 有机化学简介
有机化学的定义
总结词
有机化学是一门研究有机化合物 的组成、结构、性质、合成和反 应的学科。
详细描述
有机化学主要关注碳氢化合物及 其衍生物,即有机化合物,它们 是构成生命体的基本物质。
将有机化学与计算机科学、数学等学科交叉融合,利用计算机模拟和预测有机化学反应和 分子的性质,为有机化学研究和应用提供新的工具和手段。
THANKS FOR WATCHING
感谢您的观看
有机化学的发展历程
总结词
有机化学的发展经历了从天然有机化学到合成有机化学的演变,并不断推动着 人类社会的进步。
详细描述
早期的有机化学主要研究天然有机物,如动植物体内的化合物。随着科技的发 展,合成有机化学逐渐崛起,人们开始能够合成大量原本自然界不存在的有机 化合物,从而极大地丰富了人类的物质生活。
农业领域
1 2
农药合成
有机化学在农药合成中扮演着关键角色,通过设 计并合成新的农药分子,可以开发出更安全、更 有效的农药。
植物生长调节剂
有机化学也可用于合成植物生长调节剂,通过调 节植物生长代谢,提高作物产量和品质。
3
转基因作物
利用有机化学手段,可以修改作物的基因组,培 育出抗逆性更强、产量更高的转基因作物。
举例
乙醇被氧化生成乙醛。
04 有机化学的应用
医药领域
药物合成
有机化学在药物合成中发挥着重要作用,通过设计并合成新的有 机分子,可以开发出具有治疗作用的创新药物。
药物代谢
有机化学也涉及药物代谢的研究,了解药物在体内的代谢过程有助 于优化药物的疗效和降低副作用。
《有机化学》PPT课件

羧酸衍生物命名
羧酸衍生物结构
物理性质
以相应的羧酸为母体,将衍生物 中的官能团作为取代基、酸酐、酯 等,它们都具有不同的官能团, 但都与羧基相连。
羧酸衍生物的物理性质因官能团 的不同而有所差异。例如,酰卤 具有刺激性气味,易挥发;酸酐 多为无色晶体,具有吸湿性;酯 类具有芳香气味,难溶于水。
亚硝基化合物
含有亚硝基(-NO)的化合物称为亚硝基 化合物。亚硝基化合物不稳定,易转化 为其他含氮化合物,如硝基化合物或胺 类。
07
杂环化合物和生物碱
杂环化合物定义与分类
定义
杂环化合物是指分子中含有杂原子(如O、S、N等)的环状有机化合物。
分类
根据杂原子的种类和数量,杂环化合物可分为单杂环、双杂环和多杂环等。
06
含氮有机化合物
胺类命名、结构及物理性质
1 2 3
胺类的命名 根据与氮原子相连的烃基的不同,胺可分为伯胺、 仲胺和叔胺。命名时,需注明烃基的名称和胺的 类别。
胺类的结构 胺分子中的氮原子具有孤对电子,可接受质子形 成铵盐。同时,氮原子上的氢原子可被烃基取代, 形成不同种类的胺。
胺类的物理性质 低级胺具有刺激性气味,易溶于水。随着烃基增 大,高级胺的气味逐渐减弱,溶解度降低。
酮类命名、结构及物理性质
命名
酮的命名通常是以含有酮羰基的碳链作为主体,称为某酮。例如, 丙酮、丁酮等。
结构
酮类化合物分子中含有酮羰基(>C=O),酮羰基中的碳原子与两个 烃基相连。
物理性质
酮类多为无色液体,具有特殊的气味。酮类化合物密度比水小,难 溶于水,易溶于有机溶剂。
醌类命名、结构及物理性质
《有机化学》PPT课件
目录
• 有机化学概述 • 烃类化合物 • 卤代烃和醇酚醚类化合物 • 醛酮醌类化合物 • 羧酸及其衍生物 • 含氮有机化合物 • 杂环化合物和生物碱
有机化学PPT完整全套教学课件

有机化合物种类繁多,结构复杂 ,具有独特的物理和化学性质。
有机化学的历史与发展
01
02
03
早期历史
有机化学的起源可以追溯 到古代,但真正的发展始 于18世纪。
近代发展
19世纪以后,随着化学理 论的不断完善和实验技术 的进步,有机化学得到了 迅速发展。
现代有机化学
20世纪以来,有机化学在 理论、实验方法和应用领 域等方面都取得了巨大进 展。
通过有机合成制备具有特定功能的材料, 如光电材料、催化剂等。
合成具有生物活性的化合物,如酶抑制剂、 受体配体等,并进行生物活性评价。
05
有机化合物的鉴定与分析
Chapter
有机化合物的分离与纯化技术
蒸馏法
利用物质沸点的差异进行分离, 包括简单蒸馏、分馏、减压蒸馏
等。
萃取法
利用物质在两种不互溶溶剂中的 溶解度差异进行分离,包括液-
有机化合物的化学性质
• 取代反应:有机化合物分子中的某些原子或原子团被其他原子或原子团所代替的反应,如卤代烃的水解反应、 酯的水解反应等。
• 加成反应:有机化合物分子中不饱和键(双键或三键)两端的原子与其他原子或原子团直接结合生成新的化合 物的反应,如烯烃与氢气的加成反应、炔烃与卤素的加成反应等。
对已知化合物进行结构修饰和改造, 优化其性能,满足特定需求。
有机合成的基本策略与方法
逆合成分析
从目标分子出发,逆向分析其结 构,设计合理的合成路线。
保护与去保护策略
在合成过程中,对某些官能团进 行保护,以避免不必要的副反应 ,合成完成后再进行去保护。
01 02 03 04
合成子的选择与连接
选择合适的合成子,通过化学键 的连接形成目标分子。
《有机化学》PPT课件
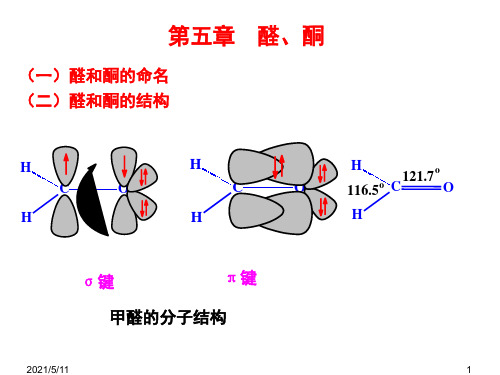
H R C COOH
H
COOH H
2021/5/11
16
R
α氢
卤代
O 羰基
生成 羧酸衍生物
还原为亚甲基
H O
H H 断C-C键
脱羧,失去CO2
断O-H键
酸的 离解作用
2021/5/11
17
(1)羧酸的酸性
O
甲、羧酸的酸性比醇强:
R CH2OH 乙、成盐
RCH2O + H 定域
RC OH
RCOOH + NaOH
2021/5/11
12
(c) Meerwein-Pondorf 还原
O
OH CH3CHCH3
Al(OCHMe)3
异丙醇是还原剂,异丙醇铝是催化剂。
O OH CH3 C CH3
异丙醇只还原羰基,不还原不饱和碳键。
(d) Clemmensen 还原
O
Zn(Hg), 浓HCl
C CH2CH2COOH reflux, 30 h 要求底物不含对酸或还原剂敏感基团:
pKa
Cl < RCOO < RO < NH2
HCl > RCOOH > ROH > NH3
-2.2 4~5
16~19 34
2021/5/11
28
(2)还原反应
用氢化铝锂还原
O RCCl
OO RCOCR
O
① LiAlH4,乙醚 ②H2O
RCH2OH
RCOR'
O
① LiAlH4,乙醚
RCNR2 ②H2O
2HCHO NaOH HCO2Na CH3OH
O HCH
HO-
OHC
H
OH
有机化学PPT06halide卤代烃课件

R X + M g 无 水 乙 醚 R M g X ( G r i g n a r d 试 剂 )
格氏试剂结构中的 C — M 键极性很强, 常可起碳负离子的作用,具有很强的亲核性。 它可与其它有机物中带部分正电荷的碳原子 连接形成新的 C—C 键(加长碳链)。
南京医科大学康达学院化学教研室 有机化学
问题: 完成下列反应
CH3C=CHCH2Cl+NaOHH2O?C H 3 C = C H C H 2 O H
Cl
C l
南京医科大学康达学院化学教研室 有机化学上页 下页 首页 27
南京医科大学康达学院 博学至精 明德至善
四、卤代烃与金属反应
卤代烃能与 Mg、Li、Na、K、Al 等多种 金属反应生成含 C—M 键的金属有机化合物。
博学至精 明德至善
RI + LiBr
R
CH3CH3CH2(CH3)2CH(CH3)3C-
k 221000 1350 1 0
结论:或的取代基越 多,SN2反应的速度越慢。
卤代烃的活性顺序为: CH3X>1RX>2RX>3RX
练习:按SN2机制反应,速率大小比较:
南京医科大学康达学院化学教研室 有机化学
B r -Br-
SN1历程的特点:
(1) 反应分两步进行
CH3 C + CH3 CH3
(2) 有正碳离子生成
OH CH3
CH3 构型保持产物
CH3
HO
CH3
CH3
构型翻转产物
(3) 为1级反应
(4) 构型外消旋化
ν=k[R—X]
南京医科大学康达学院化学教研室 有机化学
17
有机化学课件ppt完整版

阐述烷烃的碳原子以单键相连形成的链状 或环状结构,以及碳原子剩余的价键全部 与氢原子结合的特点。
烷烃的物理性质
烷烃的化学性质
探讨烷烃的沸点、熔点、密度等物理性质 随碳原子数增加的变化规律。
介绍烷烃的取代反应、氧化反应、裂化反应 等化学性质及反应机理。
烯烃、炔烃和芳香烃概述
烯烃的结构与性质
阐述烯烃分子中含有碳碳双键的结构 特点,以及烯烃的物理性质、化学性 质及反应类型。
羧酸及其衍生物的合成
阐述通过醛酮的氧化反应、腈的水解反应等方法合成羧酸 及其衍生物的方法。
04
醇、酚、醚类化合物
醇类化合物结构与性质分析
80%
醇类化合物的结构特点
含有羟基(-OH)官能团,与碳 链相连。
100%
物理性质
随着分子量的增加,醇的沸点逐 渐升高,水溶性逐渐降低。
80%
化学性质
醇具有还原性,可被氧化为醛或 酮;与羧酸反应生成酯;与卤化 氢反应生成卤代烃。
研究方法
主要包括实验方法和理论方法。实验方法包括合成、分离提纯、结构测定、性 质测试等;理论方法包括量子化学计算、分子模拟等。同时,现代有机化学还 借鉴了物理学、生物学等其他学科的研究手段和技术。
02
有机化合物结构与性质
有机化合物分类及命名规则
按碳骨架分类
开链化合物、碳环化合物
按官能团分类
烃类、醇类、醛类、酮类、羧酸类、胺类等
羧酸衍生物的合成
通过羧酸的衍生化反应,如酯化、酰卤化、 酰胺化等方法合成相应的衍生物。
绿色合成策略
采用环保、高效的合成方法,如原子经济性 反应、生物催化等,实现绿色合成。
07
含氮有机化合物
胺类化合物结构与性质探讨
有机化学ppt课件完整版

氨基酸、蛋白质和多肽
氨基酸
构成蛋白质的基本单元,分为必需氨基酸和非必 需氨基酸。
蛋白质
由氨基酸通过肽键连接而成的高分子化合物,具 有多种生物功能。
多肽
由多个氨基酸通过肽键连接而成的化合物,生物 活性多样,包括激素、生长因子等。
脂类化合物
脂肪酸
构成脂肪的基本单元,分为饱和脂肪酸和不饱和脂肪酸。
甘油酯
原理。
现代时期
20世纪至今,以量子力学和统计 力学为基础,发展出了现代有机 化学的理论和方法,如分子轨道 理论、价键理论、反应机理理论
等。
有机化学与生产生活的关系
材料领域
合成纤维、塑料、橡胶等高分子材料广泛应用于服装、家 居用品、交通工具等领域。
医药领域
合成药物如抗生素、抗癌药物等对于治疗疾病具有重要意 义。同时,天然药物中提取的有效成分也是有机化学的研 究对象。
炔烃
炔烃的通式与结构特点
通式为CnH2n-2,含有碳碳三键。
炔烃的物理性质
与烷烃和烯烃相比,炔烃的物理性质有所不同。
炔烃的化学性质
主要包括加成反应、氧化反应、聚合反应等,与烯烃类似但也有所 不同。
芳香烃
01
02
03
04
芳香烃的结构特点
含有苯环或其他芳香体系的烃 类化合物。
芳香烃的分类
根据苯环上取代基的不同,可 分为苯、甲苯、二甲苯等。
感谢观看
01
分子式相同但连接方式不同,如正丁烷和异丁烷。
立体异构
02
分子式相同、连接方式也相同,但空间构型不同,如顺反异构
、对映异构等。
同分异构体的性质差异
03
由于结构上的差异,同分异构体在物理性质、化学性质以及生
有机化学优秀课件

有机化学优秀课件有机化学优秀课件有机化学优秀课件复习目标:1、了解有机化合物中碳的成键特征。
2、了解甲烷、乙烯、苯等有机化合物的主要性质。
3、了解乙烯、氯乙烯、苯的衍生物等在化工生产中的重要作用。
4、了解乙醇、乙酸的组成和主要性质及重要应用。
5、了解糖类、油脂、蛋白质的组成和主要性质及重要应用。
6、了解常见高分子材料的合成反应及重要应用。
7、以上各部分知识的综合应用。
基础知识:认识有机化合物一、有机物的特点1、无机化合物和有机化合物的划分无机化合物(简称无机物)通常指不含碳元素的化合物,无机物包括酸、碱、盐、氧化物等,另外,单质也属于无机物。
有机化合物(简称有机物)是一类含有碳元素的化合物,比如烃及其各种衍生物就是我们常见的有机物。
无机物和有机物的划分不是绝对的.,少数含碳化合物性质更像无机物,所以将它们划分为无机物的范畴。
中学常见含碳无机物有:①碳的氧化物:CO、CO2 ;②碳酸及其盐:如H2CO3、CaCO3、NH4HCO3等;③碳化物:如SiC、CaC2等;④其它:如HCN、NaCN、KSCN等。
2、有机物的特点在结构上:通常由C原子结合形成分子骨架,其它原子或原子团以共价键结合在碳骨架上;每种原子通常以特定的价键数与其他原子结合(C-4,O-2,H-1);绝大多数属于共价化合物,往往形成分子晶体。
在性质上:多数难溶于水,易溶于有机溶剂;绝大多数有机物不导电不导热,具有熔沸点低、硬度小的特点;有机物密度通常不打;多数有机物受热易分解,且易燃烧。
在反应上:反应复杂而缓慢,并且常伴有副反应;反应往往往往需要加热、加压或使用催化剂等条件;反应一般不能全部转化成产物(所以有机反应常用“→”而不用“=”)二、碳原子的成键特点和结合方式1、C原子成键特点(1)通常以共价键与其它原于结合——所以有机物多数是共价化合物(2)总是形成4个价键——是有机物种类繁多的一个重要原因(3)C原子的价键具有一定的空间伸展方向——这样有机物具有一定的立体空间形状 2、C原子结合方式有机物中C原子可以以单键结合,也可以以双键、叁键结合,还可以像苯环这样介于单键和双键之间的独特方式相结合。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
NaOH溶液 银氨溶液 金属钠
A 中和反应
—— 产生氢气
B
——
有银镜 产生氢气
C 水解反应 有银镜
——
D 水解反应
——
——
则A、B、C、D的结构简式?
14、已知:
利用上述信息
合成
某芳香烃A有如下转化关系:
回答下列问题: (1)写出反应类型:⑤___________,⑥_____________ (2)写出结构简式:A___________,F_______________ (3)写出反应的化学方程式: ②________________________________________________ ⑦_______________________________________________ (4)E有多种同分异构体,其中苯环、官能团的种类和数目都不变 的同分异构体有______________ 种(E除外)
A B + x—y
AB
x
y
3、消去反应
包含醇分子内脱水生成烯烃、卤代
烃脱HX生成烯烃
一定条件下
AB
A
B + x—y
x
y
重要知识规律
(1)卤代烃的消去反应规律
①分子中碳原子≥2; ②与-X相连碳原子相邻的碳原子上有氢原子。
重要知识规律
(2)醇类的消去反应规律
①分子中碳原子≥2; ②与-OH相连碳原子相邻的碳原子上有氢原子。
D CH 3 (CHBr )2 CH 3
11、已知有机物 的结构简式为:
OH
CH2=CH-CH2-
-CHO
下列性质中该有机物不具有的是( C ) (1)加聚反应 (2)加成反应 (3)使酸性高锰酸钾溶液褪色 (4)与NaHCO3溶液反应放出CO2气体 (5)与KOH溶液反应 A 、 (1)(3) B、 (2)(4) C 、 (4) D 、(4)(5)
某有机物分子结构如下:
关于该分子结构的说法正确的是 B A.除苯环外的其余碳原子有可能都在一条直线上 B.除苯环外的其余碳原子不可能都在一条直线上 C.12个碳原子不可能都在同一平面上 D.12个碳原子一定都在同一平面上
2.下列分子中的14个碳原子不可能处在同一平面上的是 ()
:BD
• 1、取代反应 :原理可简述为:“有进有出”
试写出不能发生消去反应的某醇(C8H18O) 的结构简式
CH 3CH 3 CH3 C C CH2 OH
CH3CH3
4.有机反应类型——氧化反应
• 原理:有机物得氧或去氢 • 包括:
燃烧反应、被空气(氧气)氧化、(醇是去氢氧化) 被酸性KMnO4溶液氧化, 醛基的银镜反应和被新制Cu(OH)2悬浊液氧化 烯烃被臭氧氧化 (O3,Zn/HCl,双键断裂,原双键碳变为C=O)
应
3、有机化合物I转化为II的反应类型是
(
)
( A )氧化反应 ( B )加成反应
( C )还原反应 ( D )水解反应
4. 某有机物,当它含有下列的一种官能团 时,既能发生取代反应,氧化反应,酯 化反应,又能发生消去反应的是( )
A.-COOH C.-OH
B.-C=CD.-CHO
某种解热镇痛药的结构简式如下,在酸性条件下水
12、在一定条件下,下列药物的主要成分都能发生
下列六种反应的是( B
)
①取代 ②加成 ③水解
④中和 ⑤酯化 ⑥与碳酸氢钠溶液反应
O
D.散热痛 HO
O
-C-OR(R为烃基)
CH2CH(CH3)OH
13、现有分子式均为C3H6O2的四种有机物A、B、C、 D,把它们分别进行下列实验以鉴别之,其实验记 录如下:
高二化学有机复习
有机化学反应类型复习专题
●有机分子空间构型
1.几个特殊分子的空间构型 ①CH4分子为正四面体结构,其分子最多有3个原 子共处同一平面。 ②乙烯分子中所有原子共平面。 ③乙炔分子中所有原子共直线。 ④苯分子中所有原子共平面。 ⑤H—CHO分子中所有原子共平面。 2.单键的转动思想 有机物分子中的单键,包括碳碳单键、碳氢单键、 碳氧单键等可转动。
重要知识规律
(3)醇类的催化氧化反应规律
由羟基所连接的碳原子上的氢原子数目所决定的
a.如果羟基所连的碳原子上有两个(或两个以上)
氢原子,其产物为醛;
b.如果羟基所连的碳原子上只有一个氢原子,其
产物为酮( O
);
RCR
c.如果羟基所连的碳原子上无氢原子,则此醇不
能被催化氧化。
有机反应类型——还原反应
解,写出水解产物的化学式?
O
1mol该物质完全水解,消耗
O-C-CH3
NaOH的物质的量为?
O
C-O OH O
NH-C-CH2CH3
NH2
OH COOH
CH3COOH CH3CH2COOH
(06上海模拟)已知卤代烃在碱性条件下,易水解。某 有机物的结构简式如下: lmol该有机物与足量的NaOH溶液混合共热,充分反应最 多灰可 共消热耗,又am消ol耗NabOmHo,lN将aO所H得,溶则液a与蒸b干的后值再分与别足是量(的D碱石) A.5mol,10mol B.6mol,2mol C.8mol,4mol D.8mol,2mol
物①甲醇和乙醇的混合物与浓硫酸
加热得醚;②乙二醇与乙酸酯化得
酯;③氨基乙酸与氨基丙酸生成二
肽;④苯酚与浓溴水反应,所生成
的有机物种类由多到少的顺序是( )
A.③①②④
B.①②③④
C.③②④①
D.④③②①
10.化合物丙可由如下反应得到:丙的结构简式 不可能是( )
A CH 3CH(CH 2Br )2 B (CH 3 )2 CBr 2CH 2Br C C2H5CHBrCH 2Br
)
(A)CH3CHOC2H5OH (B)C2H5ClCH2=CH2
(D)CH3COOHCH3COOC2H5
2、已知柠檬醛的结构简式为
下列说法不正确的是 (
)
A、它可是跟银氨溶液发生银镜反应
B、它催化加氢的最终产物分子式为
C10H20O
C、它能使酸性KMnO4溶液和溴水褪色
D、它既能发生加成反应又能发生消去反
• 原理:有机物得氢或去氧 • 包括:烯、炔、苯环、醛、油脂等和氢气加
成, 硝基被还原为氨基 (如硝基苯被Fe+HCl还
原为苯胺) • 说明:“氧化”和“还原”反应是针对有机
物而言的,有机物被氧化则定义为氧化反应, r—CH2Br的变化
属于同一反应类型的是(
7.下列各种醇与浓硫酸共热到一定
温度不能产生烯烃的是( )
.
A
B CH 3OH
C
D
8.有一种脂肪醇通过一系列反应可得
丙三醇,这种醇可通过氧化、酯化、
加聚反应而制得高聚物
,
这种脂肪醇为( )
A CH 3CH 2CH 2OH C
B CH 2 CH CH 2 OH D
9.在一定条件下加热有机物的混合
• 含括:烷烃的卤代(扩展到饱和碳原子的特征反应), 醇和氢卤酸的反应,苯的溴代、硝化、磺化,苯酚和 溴水的反应,广义说、酯化、水解也可归属此列。如 酯化反应:
A—x + B—y
A—y + B—x
O
R C O H+H
O CH2 R’
R C O CH2R
O
’+ H O H
2、加成反应 原理可简述为:“有进无出” 包含烯烃、炔烃、苯环、醛和油脂等加H2,烯 烃、炔烃等加X2,烯烃、炔烃等加HX,烯烃、 炔烃等加H2O等等。加成反应是不饱和碳原子 的特征反应之一。其中加氢的反应又可定为还 原反应。
