肌萎缩侧索硬化诊疗指南
渐冻症(肌萎缩侧索硬化)

渐冻症(肌萎缩侧索硬化)肌萎缩侧索硬化(ALS)也叫运动神经元病(MND),后一名称英国常用,法国又叫夏科(Charcot)病,而美国也称卢伽雷(Lou Gehrig)病。
我国通常将肌萎缩侧索硬化和运动神经元病混用。
它是上运动神经元和下运动神经元损伤之后,导致包括球部(所谓球部,就是指的是延髓支配的这部分肌肉)、四肢、躯干、胸部腹部的肌肉逐渐无力和萎缩。
2018年5月11日,国家卫生健康委员会等5部门联合制定了《第一批罕见病目录》,肌萎缩侧索硬化被收录其中。
病因肌萎缩侧索硬化是一种什么病?症状和治疗手段有哪些?肌萎缩侧索硬化的病因至今不明。
20%的病例可能与遗传及基因缺陷有关。
另外有部分环境因素,如重金属中毒等,都可能造成运动神经元损害。
产生运动神经元损害的原因,目前主要理论有:1.神经毒性物质累积,谷氨酸堆积在神经细胞之间,久而久之,造成神经细胞的损伤。
2.自由基使神经细胞膜受损。
3.神经生长因子缺乏,使神经细胞无法持续生长、发育。
临床表现早期症状轻微,易与其他疾病混淆。
患者可能只是感到有一些无力、肉跳、容易疲劳等一些症状,渐渐进展为全身肌肉萎缩和吞咽困难。
最后产生呼吸衰竭。
依临床症状大致可分为两型:1.肢体起病型症状首先是四肢肌肉进行性萎缩、无力,最后才产生呼吸衰竭。
2.延髓起病型先期出现吞咽、讲话困难,很快进展为呼吸衰竭。
检查要早期诊断肌萎缩侧索硬化,除了神经科临床检查外,还需做肌电图、神经传导速度检测、血清特殊抗体检查、腰穿脑脊液检查、影像学检查,甚至肌肉活检。
诊断1.病史采集和神经系统检查诊断过程的第一个重要步骤,就是由神经科医生进行的临床接诊。
进行包括详细的现病史,家庭史,工作和环境接触史的采集。
接诊过程中,神经科医生将寻找肌萎缩侧索硬化的典型表现:(1)检查要评估咀嚼和吞咽的肌肉力量,包括口腔、舌及咽喉肌。
(2)下运动神经元(LMN)功能,如肌肉萎缩情况,肌肉力量或肌肉跳动(称为肌束震颤)。
肌萎缩侧索硬化症

肌萎缩侧索硬化症一、病因及发病机制1.ALS动物模型是研究ALS病因、发病机制和治疗的基础。
选择大鼠的原因是其与人类基因DNA序列相似。
动物模型系统分为基因型和表现型动物模型。
前者如SOD1基因突变(G93A)模型,用于研究发病机制和临床前的治疗;后者基因尚不清楚但表现为ALS,用于神经元变性机制的研究。
2.细胞死亡机制的研究二、临床常见类型1.肌萎缩侧索硬化症2.原发性侧索硬化症3.进行性脊肌萎缩症4. 进行性延髓麻痹分遗传性与获得性两类。
遗传性:1、Ⅰ型:急性婴儿型脊肌萎缩症(Werdnig-Hoffmann病)2、Ⅱ型:儿童型脊肌萎缩症(Kugelberg-Welander 综合征)3、Ⅲ型:成人型脊肌萎缩症4.进行性延髓麻痹5.慢性近端脊肌萎缩症AD遗传,2/3有阳性家族史,男性稍多见,且病情较女性为重。
偶有散发病例和X-性连隐性遗传。
病程长,多数患者存活30年以上。
婴儿型2岁前起病,占36%,青少年型3-18岁起病,占48.8%,成人型18岁后起病,最大年龄达63岁。
占15.25%。
6.婴儿型脊肌萎缩症7.X-性连延髓脊髓运动神经元病8.远端型脊肌萎缩症9.肩腓型脊肌萎缩症●Ⅰ型:●Ⅱ型:●肩腓型脊肌萎缩症伴感觉神经病变●肩腓型脊肌萎缩症伴心肌病10.其他类型脊肌萎缩症慢性不对称性脊肌萎缩症病变仅累及一个肢体,出现无力和下运动神经元性肌萎缩,数年或10年后才完全累及这一肢体的全部肌群,也可在某一时间内停止发展而不累及这一肢体的其他部分。
腱反射减退或消失,感觉正常。
不累及延髓和身体其他部分。
肌电图检查受累肌肉呈失神经改变。
神经传导速度正常。
面肩肱型脊肌萎缩症AD遗传,面、肩带、肱肌的下运动神经元损害的肌无力和肌萎缩,肌电图呈失神经改变。
单上肢脊肌萎缩症见于日本和亚洲报告,多发于10-20岁青年人,一侧上肢肌无力、肌萎缩、肌电图呈失神经改变。
病情在1-2年内缓慢发展,以后即停止发展。
节段性脊肌萎缩症Segmental spinal muscular atrophy 1978年Sobue报告运动障碍仅限于C8-T1神经节段支配的肌肉,肌电图呈失神经改变。
肌萎缩侧索硬化分为几个临床类型

肌萎缩侧索硬化分为几个临床类型我国一般将肌萎缩侧索硬化和运动神经元病混用,通常分肌萎缩侧索硬化(ALS),进行性球麻痹(PBP),进行性性肌萎缩(PMA)和原发性侧索硬化(PLP)等四类临床亚型。
但研究证明有些患者的表现符合ALS的临床诊断标准,但用这四个亚型难以概括。
近年研究按世界神经病学联合会埃斯科里亚尔(El Escorial)诊断ALS,主要将ALS分八个临床表型,这些类型在发病年龄,延迟诊断的时间,合并额颞叶痴呆的比率,生存期,3、5、10年存活率等均有差异。
这8个分型建立诊断时的临床表现基础上,但在随访中要收集患者所有可用的资料,不断修订。
1、经典(夏科)型ALS(C-ALS):在上肢或下肢出现特征性症状或体征,锥体束征明确,但不突出。
2、延髓型ALS(B-ALS):这些患者为延髓发病,有构音障碍和/或吞咽困难,舌萎缩,肌束震颤。
在发病后的前6个月内没有周围脊髓损害症状。
在前6个月锥体束征可以不明显,但之后要显而易见。
3、连枷臂综合征(FA-ALS):本类型患者的特点是逐渐发展,主要是上肢近端无力和萎缩。
此类型包括病程中某一阶段患者上肢的病理性深部腱反射或霍夫曼征,但无肌张力增高或阵挛。
在发生症状后局限于上肢的受累功能至少有12个月。
4、连枷腿综合征(FL-ALS):患者特点是逐渐进展,下肢远端出现的无力和萎缩。
此类型包括病程中某一阶段患者下肢的病理性深部腱反射或巴彬斯基征,但无肌张力增高或阵挛。
患者下肢近端起病的萎缩和无力,在无远端受累时列为经典型ALS。
5、锥体束征型ALS(P-ALS):这些患者的临床表现主要是锥体束征,主要表现为严重的痉挛性截瘫/四肢瘫,有一个或多个体征:巴宾斯基或Hoffmann征,腱反射亢进,下颌阵挛性抽动,构音障碍和假性球麻痹。
痉挛性麻痹可以存在于发病初期或疾病晚期。
这些患者在发病时可以至少在两个不同区域同时表现有明显的下运动神经元损害的体征如肌肉无力和萎缩,肌电图检查存在慢性和活动性的失神经损害。
肌萎缩侧索硬化症黄金海岸标准

肌萎缩侧索硬化症黄金海岸标准全文共四篇示例,供读者参考第一篇示例:肌萎缩侧索硬化症,简称ALS,是一种神经系统退行性疾病,主要影响人体的肌肉控制功能。
这种疾病会导致患者逐渐失去肌肉力量和控制能力,最终导致全身瘫痪。
ALS是一种不可逆的疾病,目前尚无有效的治疗方法,只能通过康复训练和支持性疗法来缓解症状和延缓疾病进展。
黄金海岸是澳大利亚昆士兰州一个著名的旅游胜地,同时也是一个重要的医疗中心。
在黄金海岸,有许多优秀的医疗机构和专家团队,他们致力于研究和治疗各种疾病,包括ALS。
针对ALS患者,黄金海岸医疗界提出了一系列的标准化治疗方案,希望能够为患者提供更好的医疗服务和关怀。
一、综合评估:对于ALS患者,首先需要进行全面的身体评估,包括神经系统、肌肉状况、呼吸功能等方面。
通过这些评估,医生可以了解患者的病情发展情况,制定个性化的治疗方案。
二、康复训练:康复训练是ALS治疗的重要环节,通过物理治疗、作业治疗和言语治疗等方式,帮助患者维持和提高肌肉功能和日常生活能力。
黄金海岸医疗机构提供了一系列高质量的康复训练方案,旨在帮助患者尽可能延缓病情进展。
三、营养支持:ALS患者常常会出现吞咽困难和体重下降等问题,因此营养支持是治疗的关键。
黄金海岸的医疗机构会配备专业的营养师,根据患者的情况制定个性化的饮食计划,保证患者能够获得充足的营养。
四、呼吸治疗:呼吸困难是ALS患者的常见症状,严重的呼吸问题可能会危及患者的生命。
黄金海岸的医疗机构配备了专业的呼吸治疗团队,他们会定期监测患者的呼吸功能并进行及时干预,确保患者能够维持足够的呼吸功能。
五、心理支持:ALS是一种不可逆的疾病,患者常常会面临种种困难和挑战,容易产生负面情绪。
心理支持在治疗过程中显得尤为重要。
黄金海岸的医疗机构拥有专业的心理医生和心理咨询师,他们会为患者提供心理支持和心理治疗,帮助患者积极面对疾病。
黄金海岸的ALS治疗标准是基于最新的临床研究和治疗指南,旨在提供全面的医疗服务和关怀。
肌萎缩性侧索硬化疾病研究报告

肌萎缩性侧索硬化疾病研究报告疾病别名:肌萎缩性侧索硬化所属部位:全身就诊科室:骨科病症体征:肌肉萎缩,上肢周围性瘫痪,舌肌萎缩,腱反射亢进,构音不清疾病介绍:肌萎缩性侧索硬化是怎么回事?本病特点是脊髓前再细胞和锥体束同时受累,出现广泛的肌萎缩,肌束震颤,同时存在锥体束征,肌萎缩性侧索硬化症(ALS) 是成人运动神经元病中最常见的形式,ALS 以进行性上下运动神经元损伤为主,本病特点是脊髓前再细胞和锥体束同时受累,出现广泛的肌萎缩,肌束震颤,同时存在锥体束征症状体征:肌萎缩性侧索硬化的症状有哪些?肌萎缩性侧索硬化起病缓慢,但进展较快。
前驱症状可以为手臂无力、吞咽发音困难、小腿无力或者前述症状联合出现,但通常的方式为手和臂的对称性软弱无力,精细动作困难,逐步出现肌萎缩,骨间肌、蚓状肌及鱼际肌早期受累,向邻近和近端肌群蔓延。
下肢受累在后或与上肢同时发生。
舌肌、口轮匝肌、咀嚼肌萎缩无力逐渐发生,引起吞咽和发音困难,流涎或呛咳,肌束震颤广泛地出现于四肢、躯干、口舌、面等部位,不定时出现。
锥体束病征与肌萎缩、肌束震颤等下运动神经元病征共存,四肢腱反射亢进并出现病理反射。
有时上肢腱反射减弱或消失,而下肢反射亢进,出现痉挛。
括约肌与性功能障碍不常见,多无客观的感觉障碍。
大部分病例2~5年内死亡,以延髓症状起病或为主者存活时间更短。
化验检查:肌萎缩性侧索硬化要做哪些检查?以下的检查方法有利于本病的诊断:1、神经电生理:肌电图呈典型神经源性改变。
静息状态下可见纤颤电位、正锐波,有时可见束颤电位;小力收缩时运动单位电位时限增宽、波幅增大、多相波增加,大力收缩呈现单纯相。
神经传导速度正常。
运动诱发电位有助于确定上运动神经元损害。
2、肌肉活检:有助于诊断,但无特异性,早期为神经源性肌萎缩,晚期在光镜下与肌源性肌萎缩不易鉴别。
3、其他:血生化、CSF检查多无异常,肌酸磷酸激酶(CK)活性可轻度异常,MRI可显示部分病例受累脊髓和脑干萎缩变小。
运动神经元病临床诊断治疗指南

运动神经元病临床诊断治疗指南【概述】运动神经元病(motor netlron disease,MND)为一组病因不清的系统性疾病。
主要累及上、下运动神经元的慢性进行性变性疾病。
根据受损的病变部位不同而分为进行性脊肌萎缩症、进行性延髓麻痹、原发性侧索硬化和肌萎缩侧索硬化数种类型。
一、肌萎缩侧索硬化【临床表现】肌萎缩侧索硬化(amyotrophic lateral sclerosis,ALS)可分为三型,即散发型(或称经典型)、家族型(5%~10%)和关岛型。
散发型表现为中年或中年以后起病,40岁以下起病者亦不少见。
国内报告最早发病为18岁。
男性多于女性。
起病隐袭,呈慢性进展病程,部分患者为亚急性病程,少数起病后呈急剧进展,可于病后半年左右死亡。
早期出现肌肉无力、肌肉萎缩及肌纤颤。
常自上肢远端手部肌肉开始,可自一侧手肌开始,数月后可波及对侧;也可双侧手肌同时受累,随后波及前臂肌肉及上臂和肩胛部肌肉。
部分患者可以三角肌或冈上、下肌无力开始,造成肩胛下垂,抬肩或臂上举无力。
少数患者可以下肢起病,表现为下肢无力、沉重、走路无力,骨盆带肌肉受累后可有上台阶、楼梯、蹲下起立困难,下肢肌肉萎缩。
随着病情的发展,肌无力和萎缩可延至颈部、躯干、面肌及延髓支配的肌肉,表现为抬头困难、转颈障碍,呼吸肌受累出现呼吸困难,延髓支配肌肉受累则有吞咽困难、咀嚼费力、舌肌萎缩、发音障碍等。
延髓麻痹通常出现于疾病晚期,但也可于手肌萎缩不久后出现,少数情况下为首发症状。
肌纤颤为常见的症状,可在多个肢体中发生。
在舌体由于肌膜薄而可看到肌纤维颤动。
本病很少有感觉障碍,客观感觉异常少见,有少数患者可有痛性痉挛。
绝大多数患者无括约肌障碍。
本病的生存期随临床类型而有不同,短者数月,长者可十余年,最长可至35年,平均生存3年左右。
严重者多因延髓麻痹或呼吸麻痹而死亡。
本病患者在肌肉萎缩的同时出现上运动神经元损害体征,表现为腱反射亢进,手部可引出Hoffmann及Rossolimo等病理征。
肌萎缩侧索硬化(渐冻症)-解决办法

• 随着病情的发展,手臂和双腿开始变的纤细,随着肌肉组织萎缩。ALS患者最 终失去肌肉力量和行走能力,依赖轮椅,并且越来越需要他人照顾自己的日 常生活。
• 随着时间的推移,肌肉无力让患者无法使用手臂,呼吸肌的衰弱导致呼吸困 难。大多数ALS患者在ALS首次出现体征和症状后的2〜10年内死于呼吸衰竭, 但病情的进展在患者之间的差异很大。
临床病例
• 患者情况:患者吴磊(化名)、男、19岁,据吴磊母亲王女士描述,孩子1年 前不知什么原因出现右下肢无力的症状,就诊于当地医院,检查右侧大腿肌 肉最大周长较左侧减少10cm。肌电图检查报告显示神经源性损害,诊断为肌 萎缩侧索硬化症。
• 王女士听到这个消息非常震惊,家族没有人有相关疾病史,为什么孩子会患 病,他之前是那么爱跑爱跳,接下来的路他该怎样去面对。为了明确诊断, 医生帮助王女士联系到了佳学基因致病基因鉴定,为吴磊进行致病基因鉴定, 从基因层面查找病因。
• 与家族性ALS相关的其他基因突变各占一少部分。 • 据估计,60%的家族性ALS患者有遗传性基因突变。C9***72,S**1,TA***P,
和F*S基因是运动神经元和其他细胞发挥正常功能的关键。*1基因突变引起15 %至20%家族性ALS,TA***P和F*S基因突变各约5%
• 通过基因解码可以分析不同的基因突变是如何导致运动神经元的死亡,如何 引起运动神经元过大而过度敏感导致功能异常?
什么是肌萎缩侧索硬化症?
• 肌萎缩侧索硬化症(ALS)简称渐冻症,又称为运动神经元病(MND)、 夏科(Charcot)病、卢伽雷(Lou Gehrig)病,是一种影响运动神经 元的进行性疾病。运动神经元是专门控制肌肉运动的神经细胞,这些神 经细胞存在于脊髓和脑中。
• 美国报告ALS的发病率(每年新发病例)为2/10万~4/10万,患病率为 4/10万~6/10万,中国尚无确切的流行病学资料。
颈椎病并肌萎缩侧索硬化症的诊断

三٠神经电生理检查 的重要性
同心针EMG检测
判明是神经源性损害,还 是肌源性损害。
若为前者,确定神经源性 损害的部位及病变活动性。
CSM及ALS均为神经 源性损害
CSM特点:其受损神经根是节段 性分布,如C5神经根受损,可有 三角肌、冈上肌、大圆肌等来自 同一神经根水平的支配不同肌肉, 不同程度的肌萎缩。
3, 反射与反应:双侧胫神 经H反射潜伏期正常、左 侧波幅正常低限。
结论:多发神经原性损害 符合ALS诊断
检测结果:
1.神经传导:双侧胫神经、 尺神经感觉、运动传导速 度正常,运动波幅正常低 限,双侧正中神经感觉、 运动传导速度正常,运动 潜伏期延长。
2, 肌电图(MUP):右侧拇短 展肌、小指展肌、肱二头肌、 胸锁乳突肌、双侧胫前肌 MUP面积增大、波幅增高、 时限延长。右侧拇短展肌、 小指展肌、肱二头肌可见自 发电位,右侧胸锁乳突肌卫 星电位增多。
全组病人均进行 常规颈部X线摄片及 MRI检查, 部分为 CT扫描。
X线片显示不同程度的颈 椎退变,如椎体后缘骨赘 形成,生理曲线改变,椎 间隙变窄及颈椎不稳等。
MRI表现为一个或多个节 段脊髓硬膜囊受压,呈凹 陷或波浪改变,部分伴有 黄韧带肥厚,全组除2例 外均无脊髓内高信号改变。
全组经详细的EMG测定 (部分作了SEP或神经传 导速度测定)。EMG呈广 泛性神经源损害(3个肢 体以上,包括胸锁乳突 肌,胸椎旁肌)。
ALS的EMG常表现为三个 肢体以上的肌肉为广泛 性神经损害,特别是临 床上无症状而肌电图有 改变的部位更有意义。
康德萱等认为:
胸锁乳突肌的EMG检查对 CSM和ALS的诊断与鉴别诊 断具有重要意义。
其资料显示:
ALS组(37/38)胸锁乳 突肌异常率为97%.
渐冻症的治疗方法和进展药物康复和干细胞治疗的最新进展

渐冻症的治疗方法和进展药物康复和干细胞治疗的最新进展渐冻症,又称为肌萎缩侧索硬化症(Amyotrophic Lateral Sclerosis,ALS),是一种进行性神经退化性疾病。
目前,科学界对于渐冻症的治疗一直在进行深入研究,并取得了许多进展。
本文将探讨渐冻症的治疗方法以及最新的进展药物康复和干细胞治疗。
一、常规治疗方法1. 药物治疗目前,主要用于治疗渐冻症的药物是Riluzole,它是一种抗谷氨酰胺释放剂。
该药物能够减轻症状的进展速度,延缓功能丧失的时间。
此外,其他一些药物如Baclofen和Tizanidine也可以用于缓解痉挛和肌肉僵硬等症状。
2. 物理疗法物理疗法是渐冻症患者常用的治疗方法之一。
康复医师可以根据患者的具体症状设计一系列的物理疗法方案,包括按摩、牵引、电刺激等,以帮助患者恢复肌肉功能和改善生活质量。
3. 呼吸支持渐冻症患者往往会因呼吸肌无力而出现呼吸障碍。
呼吸支持是一种重要的治疗方法,可以通过机械通气或者使用呼吸肌辅助设备来维持患者的呼吸功能。
二、进展药物的康复治疗除了常规治疗方法外,一些新型的进展药物康复治疗逐渐被引入临床实践,取得了一定的效果。
以下是一些值得关注的进展药物康复治疗方法:1. 小分子化合物近年来,科学家们发现一些具有潜力的小分子化合物可以干预渐冻症的进展。
例如,由金黄色葡萄球菌产生的一种化合物称为FLZ (Farnesyltransferase Inhibitor)被发现可以改善渐冻症的症状,并在动物模型中显示出潜在的治疗效果。
2. 基因治疗基因治疗是一种目前较为前沿的治疗方法。
研究人员可以通过将修饰的基因导入患者的细胞中,来纠正渐冻症相关基因的突变。
然而,基因治疗的应用还处于实验阶段,需要进一步的研究和临床试验来验证其安全性和有效性。
三、干细胞治疗的最新进展干细胞治疗是一种前沿的治疗方法,具有很大的潜力。
干细胞可以分化为各种类型的细胞,包括神经细胞,这为治疗渐冻症提供了新途径。
中国肌萎缩侧索硬化诊断和治疗指南

中国肌萎缩侧索硬化诊断和治疗指南中国肌萎缩侧索硬化诊断和治疗指南(2012)运动神经元病是一种病因未明、主要累及大脑皮质、脑干和脊髓运动神经元的神经系统变性疾病,包括肌萎缩侧索硬化(amyotrophic lateral sclerosis,ALS)、进行性肌萎缩、进行性延髓麻痹和原发性侧索硬化4种临床类型。
ALS是运动神经元病中最常见的类型,一般中老年发病多见,以进行性加重的骨骼肌无力、萎缩、肌束颤动、延髓麻痹和锥体束征为主要临床表现,生存期通常3~5年。
ALS的早期临床表现多样,缺乏特异的生物学确诊指标。
详细的病史、细致的体检和规范的神经电生理检查对于早期诊断具有关键性的作用,影像学等其他辅助检查在鉴别诊断中具有一定价值。
临床诊断过程中,确定上、下运动神经元受累范围是诊断的关键步骤,根据患者所出现症状、体征的解剖部位,通常将受累范围分为脑干、颈段、胸段和腰骶段4个区域。
一、临床检查通过详细询问病史和体格检查,在脑干、颈段、胸段、腰骶段4个区域中寻找上、下运动神经元共同受累的汪据,是诊断ALS的基础。
根据情况可选择适当的辅助检查以排除其他疾病,如神经电生理、影像学以及实验室检查等。
对于在发病早期诊断的ALS,特别是当临床表现不典型或进展过程不明确时,应定期(3个月)进行随诊,重新评估诊断。
1.病史:是证实疾病进行性发展的主要依据,应从首发无力的部位开始,追问症状发展、加重以及由一个区域扩展至另一个区域的时间过程。
注意询问吞咽情况、呼吸功能以及有无感觉障碍、尿便障碍等。
2.体格检查:在同一区域,同时存在上、下运动神经元受累的体征,是诊断ALS的要点。
(1)下运动神经元受累体征主要包括肌肉无力、萎缩和肌束颤动。
通常检查舌肌、面肌、咽喉肌、颈肌、四肢不同肌群、背肌和胸腹肌。
(2)上运动神经元受累体征主要包括肌张力增高、腱反射亢进、阵挛、病理征阳性等。
通常检查吸吮反射、咽反射、下颏反射、掌颏反射,四肢腱反射、肌张力,Hoffmann征、下肢病理征、腹壁反射,以及有无强哭强笑等假性延髓麻痹表现。
肌萎缩侧索硬化(ALS)的临床分型,分期及病情评估@MedSci

肌萎缩侧索硬化(ALS)的临床分型,分期及病情评估@MedSci肌萎缩侧索硬化(Amyotrophic lateral sclerosis,ALS)是一种进展性神经系统变性疾病。
由于上、下运动神经元丢失导致球部、四肢、胸部肌肉逐渐无力和萎缩,动眼肌及括约肌不受累。
发病率约1.5/10万,患病率4-6/10万。
隐袭起病,进展缓慢,呼吸衰竭死亡。
发病年龄平均55岁,发病起计算平均存活3.5年。
50%患者平均存活时间为2.5年。
5年后20%患者存活,10年后10%存活。
球部起病者存活期约2.2年,存活很少超过5年。
一般发病年龄越早,存活时间越长。
目前尚无治愈的方法,但近年来研究表明有许多措施可以延长患者存活期,提高患者的生活质量。
为了科学合理地治疗ALS,本文就其临床分型,分期,治疗模式及对ALS病情进展的评估和随访方法进行了介绍。
一、ALS的定义及分类ALS在一些国家有不同的名称,在法国也称为Charcot病,为纪念1869年首次描述这一疾病的马丁夏科医生;在英国称为运动神经元病,强调该病归属的类别;在美国公众称为Lou Gehrig病,这是以患此病并使此病引起公众注意的著名棒球手的名字命名的;专业杂志遵循国际神经病学联盟的命名称为ALS。
我国一般将ALS和运动神经元病混用(近年来国内非医学媒体还称其为渐冻人症,源于台湾运动神经元病协会进行科普宣教所使用的俗称)。
建议国内同行统一采用ALS为该病的病名,便于和国际交流。
二、ALS的诊断1990年,由世界神经病学联合会在埃斯科里亚尔(El Escorial,西班牙)举办了一次研讨会,制定了第一个共识文件[3]。
其核心为将病变累及的神经系统区域分为颈区、胸区、腰骶区、延髓区,根据所制定标准,在临床怀疑ALS的患者确诊ALS需要同时存在下运动神经元变性临床表现及上运动神经元变性的临床表现和逐步向身体其他区域扩展,且没有可以解释其临床表现的其他疾病的依据。
电生理检查可以用来确认某一区域的下运动神经元损害,如每个身体区域至少两个不同的脊神经根和周围神经支配的肌肉同时存在纤颤电位和长时程的巨大运动单位电位和运动单位募集减少。
肌萎缩侧索硬化症(ALS)
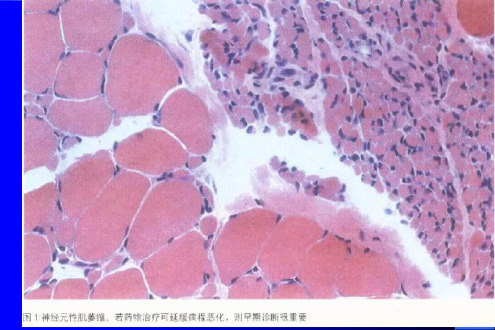
症状和体征
最早一个肢体非对称性无力,或构音不清 大约35%的患者首先在上肢, 多从肩部无力开始, 有时在轻微的局部损伤后发现远端无力常较明显,表 现为持物无力 大约40%的患者从脊髓腰段开始,由于单侧足下垂跛 行或由于无力难以站立 肌肉跳动早于无力和肌萎缩数月之久
症状和体征
肌电图为神经源性损伤,仅有患侧上肢远端EMG异常, 伴健侧上肢远端手肌EMG异常,而患肢近端肌和双下 肢的EMG大多正常,这和MND表现为四肢广泛神经源性 损伤有区别
肌活检为神经源性损害,病理特点反映了脊髓节段受 损较局限,受损肌肉从邻近健康神经元接受神经再支 配的能力大,这与MND不同
ALS的处理原则
症状和体征
65%患者有明显上、下运动神经元体征 肌肉跳动可出现在无其它下运动神经元体征时, 具特征性,大多在上肢 10%患者仅表现下运动神经元体征,但晚期发展至 上运动神经元。 5%表现为进行性肌肉萎缩 除非临床上有合理的解释如腕管综合症等,否则客 观感觉体征可排除ALS的诊断
诊断原则
绪 要及时使用抗抑郁药及抗焦虑药 –常用阿米替林25mg-150mg/每日 –选择性五羟色胺再摄取抑制剂副作用小,但价 格贵 帕罗西叮20mg/每日,氟西叮20mg/每日
并发症的治疗---构音障碍
临终前绝大多数患者有构音障碍。及早期由
语言康复医生指导非常重要 处理措施包括: 鼓励患者减慢讲话速度 局部使用冰块或巴氯芬减轻舌肌痉挛 软腭修复及抬高软腭
青年上肢远端肌萎缩症
平山病,良性局灶性肌萎缩,单肢MND。
青年期起病,男性多见 在发病后3-4年停止发展 上肢远端手肌萎缩及无力,累及前臂尺侧,肱 桡肌不受累,呈斜坡状肌萎缩特征 病因为青年硬膜囊前后径与椎管前后径比例 失调,头前屈时反复小的损伤引起
肌萎缩侧索硬化的诊治

【 e w rs A ytpile lc r i Da os T e p K y od】 m ooh t as e s ; i ns ; hr y r c a r lo s g i a
肌萎缩侧 索硬化 ( L )是 一种选 择性侵 犯脊 髓 前角 细 AS 胞 、脑干后组运 动神经元 、皮质锥体 细胞及锥体束的上 、下运 动神经元同时受 累的神经系统变性疾病 。该病呈慢性 、进行性 发展 ,发病 以成人 为 主,男 女 比例 为 16 1 ,年发 病率 为 . : (. 2 0 1 ,多 数患者仅 能存 活 2— 15~ . )/ 0万 5年 ,5 一1 % % 0 的患者 为家 族遗传 性 。由于 A s的病 因、发病 机制 目前 L 尚不明确 ,发病部位不定 ,发病早期临床表现多样 ,且缺乏特 异的生化检查指标 ,使临床医生在诊治方面面临很大困难 ,现
m t i si C i s ai t wt t e2 daee [ ] C t e ua o hn ept nsi h y i t tn n e e p b s J . [n M dJ i ( n1 ,20 ,14 ( 1 :10 E g) 0 1 1 1 ) 2 5—10 . 27
状 、体征 出现 的4个部位 :延髓 、颈 髓 、胸髓 、腰骶髓 ,A J 工 s 诊 断分为 :( )临床确诊 A S,在4个部位中至少有 3个部位 1 L 存在上 、下运动神经元同时受 累的证据 ; ( ) 临床拟诊 A S 2 L,
在 4个 部 位 中 有 2个 或 更 多部 位 存 在 上 、下 运 动 神经 兀 同时 受
19 94年 世 界 神 经 病 学 联 盟 运 动 神 经 元 病 委 员 会 制 定 了
A 5的 E soi 诊 断标准 ,19 L I er l E a 9 8年又对 其进 行 了进一 步修
肌萎缩侧索硬化症诊断及鉴别诊断综述

神经病学与神经康复学杂志2008年12月第5卷第4期J N eur ol N eur or ehabi l,D ecem ber2008,V01.5,N o.4肌萎缩侧索硬化症诊断及鉴别诊断综述李佳莹综述支惠萍审校(上海中医药大学附属曙光医院,上海200021)肌萎缩侧索硬化(am yot r ophi c l at e r r al scl er osi s,A L S)是一种病因尚未明确,选择性侵犯脊髓前角细胞、脑干运动神经元、皮质锥体细胞及锥体束的致命的慢性进行性变性疾病,其病理特征为进行性上、下运动神经元的变性,临床以上或/和下运动神经元损害引起的肌无力、肌肉萎缩和锥体束征的不同组合为主要表现,患者最终因呼吸衰竭致死,感觉和括约肌功能一般不受影响。
A LS目前尚无特异性诊断指标,电生理、影像方面可提供帮助。
A L S的诊断由于A LS病程早期临床表现的多样性,以及缺少任何诊断性的生物学标记,使得作出诊断很困难,而且妨碍临床实践和治疗试验。
治疗方面目前获认可具有肯定l临床疗效的药物只有力如太,但只能延长患者生命。
即便如此,早期诊断仍然重要,让患者及家属尽早完成心理建设,尽快接受系统的治疗,对延缓疾病的进展有一定的作用。
目前对于A LS的诊断运用比较广泛的诊断标准是由世界神经病学联盟(W FN)于1994年所制订的诊断标准…。
A L S的诊断标准1.临床诊断:根据W FN诊断标准,A L S诊断需要4个区域(延髓、颈部、胸部和腰骶部)中有1个或以上区域有下运动神经元(L M N)变性的征象(通过临床、电生理或神经病理学检查测定)、有1个或以上区域有上运动神经元(U M N)变性的征象(以临床检查测定)、在一个区域内进行性播散或向另一个区域播散的征象。
此外,必须排除无可以用于解释L M N或U M N变性征象的其他疾病过程的电生理证据,也无可能解释观察到的临床和电生理征象的其他疾病过程的神经影像学证据。
渐冻症 病情说明指导书

渐冻症病情说明指导书一、渐冻症概述渐冻症又称肌萎缩侧索硬化(amyotrophic lateral sclerosis ,ALS),是运动神经元病的一种,是累及上、下运动神经元的一种慢性进行性神经系统变性疾病。
临床常见表现为肌无力和萎缩、延髓麻痹和锥体束征,通常感觉系统和括约肌功能不受累。
肌电图是诊断本病的主要方法。
本病预后较差,病情常呈持续性进展。
尽管该病目前是一种无法治愈的疾病,但临床上医生会根据患者的实际情况采取多种治疗方法,以争取改善患者的生活质量。
英文名称:amyotrophic lateral sclerosis,ALS其它名称:肌萎缩侧索硬化相关中医疾病:痿证ICD 疾病编码:暂无编码。
疾病分类:暂无资料。
是否纳入医保:部分药物、耗材、诊治项目在医保报销范围,具体报销比例请咨询当地医院医保中心。
遗传性:可能与遗传有关,5%~10%患者有家族史,遗产方式主要为常染色体显性遗传。
发病部位:全身常见症状:进行性加重的骨骼肌无力、肌萎缩、肌束颤动、延髓麻痹和锥体束征主要病因:遗传因素、氧化应激、兴奋性毒性、神经营养因子障碍、自身免疫因素、病毒感染、环境因素检查项目:肌电图、脑脊液检查、血常规、免疫功能检查、脊髓电子计算机断层摄影(CT)及磁共振成像(MRI)、肌肉活检重要提醒:累及呼吸肌可出现呼吸肌麻痹,患者呼吸道防御功能下降,常危及生命,因此要格外关注患者的呼吸道健康状况管理,防患于未然。
临床分类:1、临床确诊 ALS 通过临床或神经电生理检查,证实在4个区域中至少有3个区域存在上、下运动神经元同时受累的证据。
2、临床拟诊 ALS 通过临床或神经电生理检查,证实在4个区域中至少有2个区域存在上、下运动神经元同时受累的证据。
3、临床可能ALS 通过临床或神经电生理检查,证实在仅有1个区域存在上、下运动神经元同时受累的证据,或者在2或以上区域仅有上运动神经元受累的证据。
二、渐冻症的发病特点三、渐冻症的病因病因总述:本病病因目前尚不完全清楚。
ALS的诊断与治疗ppt课件

这些NTF通过结合于细胞表面的受体而发
挥各自的作用。BDNF能有效保护因切断轴索 所引起的下运动神经元的减少。IGF能促进脊 髓前角细胞的生长,在ALS脊髓IGF结合密度 减低,ALS的NGF受体异常。1993年,美国、 加拿大和欧洲进行了IGF-I治疗ALS的大规模多 中心III期临床双盲实验,经过9个月的治疗,受 试组的Appel量表评分明显好于对照组,提示 IGF-I可减缓病人运动功能的丧失。
5. 环境因素:
6. 病毒感染:
英国某些地区的ALS患病人群中,既往有 较高的脊髓灰质炎发病史,因而推测两病之间 可能存在密切关系,是否为脊髓灰质炎病毒或 脊髓灰质炎样病毒的慢性感染。但在ALS患者 的血清及脑脊液中均未发现脊髓灰质炎病毒抗 体。在ALS患者的神经组织中亦未找到脊髓灰 质炎病毒、病毒有关的抗原以及核酸系列。
近年来对CNTF的研究较多,它主要在雪 旺氏细胞表达,能减缓神经元死亡的过程。动 物试验显示CNTF基因的破坏可产生肌萎缩及 运动神经元的消失,在ALS脊髓侧角其免疫活 性显著下降。
1993年,美国和加拿大开始进行CNTF治 疗ALS的多中心II/III期临床双盲实验。但因 CNTF产生明显的副作用且受试病人肌力反而 比未受试病人差,此实验被迫终止。有人分析 CNTF疗效不好的主要原因是其半衰期太短。 此外,CNTF本身就可以作为致热源使病人产 生恶病质。如何延长CNTF作用的有效时间并 减少其副作用是CNTF治疗ALS的关键。
1978年,Olney等人发现向未成年动物 注射某些兴奋性氨基酸可致中枢神经系统局部 损毁,而且不同氨基酸对神经元毒性的大小与 其产生兴奋性电位的能力有关。Onley将这种 由于暴露于兴奋性氨基酸而导致的神经元损伤 称为“兴奋毒性”。
当胞外Glu浓度过高时,主要通过两方面 作用使神经元受损。首先,AMPA受体激活导 致Na+大量内流,继发Cl-和水份的内流,使神 经元严重水肿,细胞急性肿胀而死亡,这一过 程较快;其次,NMDA受体激活使Ca2+大量内 流,胞内Ca2+浓度持续增高而引起一系列毒性 反应,这一过程相对较慢 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
肌萎缩侧索硬化诊疗指南概述肌萎缩侧索硬化(amyotrophic lateral sclerosis,ALS )是一种病因未明、主要累及大脑皮质、脑干和脊髓运动神经元的神经系统变性疾病。
其局限性分型包括进行性球麻痹(PBP),连枷臂、腿,进行性肌萎缩(PMA ),原发性侧索硬化(PLS)。
ALS 以进行性发展的骨骼肌萎缩、无力、肌束颤动、延髓麻痹和锥体束征为主要临床表现。
一般中老年发病,生存期通常3~5 年。
病因和流行病学大约90%的ALS 发病机制目前尚不明确。
国内外学者普遍认为,ALS 的发病是基因与环境共同作用的结果。
较为常见的ALS 致病基因包括SOD1,TDP-43,研究显示,由FUS、SOD1 及OPTN3 种基因的突变造成的患者不超过2%,而25.6%~30.6%的家族性ALS 患者有SOD1 突变。
其他可能的发病机制包括RNA 加工异常、谷氨酸兴奋性毒性、细胞骨架排列紊乱、线粒体功能障碍、病毒感染、细胞凋亡、生长因子异常、炎症反应等。
欧洲及美国年发病率是2/10 万~3/10万,患病率为(3~5)/10万。
发病的高峰年龄为50~75 岁,不随着年龄增加而增高。
约10%ALS 患者为家族性,余90%为散发性。
ALS 中男女患病率比例为(1.2~1.5):1。
家族性ALS 的平均发病年龄较散发性ALS 发病年龄早。
中国ALS 的流行病学数据主要来自中国(中国香港地区),发病率约0.6/10万人,患病率约3.1/10 万人。
临床表现ALS 是一种上、下运动神经元同时受累的神经系统变性疾病。
临床主要表现为球部、四肢、胸腹部肌肉进行性无力和萎缩。
而眼球运动神经和括约肌功能一般并不受累,但在有些患者晚期也可能会被累及。
20%~50%的患者可以表现有认知功能障碍,5%~15%的患者甚至会发展为额颞叶痴呆。
发病后平均3~5 年因呼吸衰竭死亡,但5%~10%的患者可以存活10 年以上。
辅助检查通过详细的病史和体格检查,在脑干、颈、胸、腰骶4 个区域中寻找上、下运动神经元共同受累的证据,是诊断ALS 的基础。
查体发现在同一区域,同时存在上、下运动神经元受累的体征是诊断ALS 的要点。
其中下运动神经元受累体征主要包括肌肉无力、萎缩和肌束颤动。
通常检查舌肌、面肌、咽喉肌、颈肌、四肢不同肌群、背肌和胸腹肌。
上运动神经元受累体征主要包括病理征阳性、腱反射亢进、肌张力增高、阵挛等。
通常检查吸吮反射、咽反射、下颌反射、掌颌反射,有无强哭、强笑等假性延髓麻痹表现,四肢腱反射、肌张力、霍夫曼征、下肢病理征、腹壁反射等。
临床查体是发现上运动神经元受累的主要方法,在出现萎缩、无力的区域,如果腱反射不低或活跃,即使没有病理征,也可以提示锥体束受损。
1. 神经电生理检查当临床考虑为ALS 时,需要进行神经电生理检查,以确认临床受累区域为下运动神经元病变,并发现在临床未受累区域也存在的下运动神经元病变,同时协助排除其他疾病。
神经电生理检查可以看作是临床查体的延伸,应该由合格的肌电图医生或技师完成,并依据明确的标准进行判断。
(1)神经传导测定:神经传导测定主要用来诊断或排除周围神经疾病。
运动和感觉神经传导测定应至少包括上、下肢各2 条神经。
1)运动神经传导测定:远端运动潜伏期和神经传导速度通常正常,无运动神经部分传导阻滞或异常波形离散。
随病情发展,复合肌肉动作电位波幅可以明显下降,传导速度也可以有轻微减慢。
2)感觉神经传导测定:一般正常。
当存在嵌压性周围神经病或同时存在其他的周围神经病时,感觉神经传导可以异常。
在进行下肢的感觉神经传导测定时,有些老年患者很难引出感觉神经动作电位,并不一定是异常。
3)F 波测定:通常正常。
当肌肉明显萎缩时,相应神经可见 F 波出现率下降,而传导速度相对正常。
(2)同芯针肌电图检查:下运动神经元病变的判断主要通过同芯针肌电图检查。
肌电图可以证实进行性失神经和慢性失神经的表现。
1)进行性失神经表现:主要包括纤颤电位、正锐波和束颤电位。
当同时存在慢性失神经的表现时,束颤电位与纤颤电位、正锐波具有同等临床意义。
2)慢性失神经的表现:运动单位电位的时限增宽、波幅增高,通常伴有多相波增多;大力收缩时运动单位募集相减少,发放频率升高,当同时存在上运动神经元受累的体征时,发放频率的测定会受到影响;大部分ALS 可见发放不稳定、波形复杂的运动单位电位。
3)诊断ALS 时,肌电图必须存在慢性失神经的表现,但并不一定都有纤颤电位或正锐波。
当肌电图检查提示进行性失神经和慢性失神经共存时,对于诊断ALS 有更强的支持价值。
如果所有测定区域均无进行性失神经表现,诊断ALS 需慎重。
4)肌电图诊断ALS 时的检测范围:应对4 个区域均进行肌电图测定。
其中脑干区域可以测定一块肌肉,如胸锁乳突肌、舌肌、面肌或咬肌。
胸段可在胸6 水平以下的脊旁肌或腹直肌进行测定。
对于颈段和腰骶段,应至少测定不同神经根和不同周围神经支配的两块肌肉。
5)在ALS 早期,肌电图检查时可以仅仅出现1 个或2 个区域的下运动神经元损害。
此时对于临床怀疑ALS 的患者,需要间隔3 个月进行随访复查。
6)肌电图出现3 个或以上区域的下运动神经源性损害时,并非都是ALS。
电生理检查结果应该密切结合临床进行分析,不应孤立的对肌电图结果进行解释。
(3)运动诱发电位:经颅磁刺激运动诱发电位检测有助于发现临床下的锥体束损伤,主要表现为中枢运动传导时间延长。
2. 神经影像学检查(1)脑或脊髓的影像学检查有助于ALS 与其他疾病鉴别,排除结构性损害。
例如颅底、脑干、脊髓或椎管结构性病变导致上和(或)下运动神经元受累时,相应部位的MRI 检查可提供帮助。
(2)某些常见疾病,如颈神经根脊髓病等,常与ALS 合并存在,需要注意鉴别。
3. 基因检测自20 世纪90 年代以来,已发现SOD1、ANG、VAPB、VCP、SQSTM1、TARDBP、DCTN1、DAO、SETX、FUS、C9ORF72、ATXN2、OPTN、SCFD1、NEK1、C21ORF2等20多个基因突变。
建议充分、详细询问ALS 患者及其兄弟姐妹的病史以及患者父母、祖父母的详细病史和其兄弟姐妹的病史。
诊断ALS 的早期临床表现多样,缺乏特异的生物学确诊指标。
详细的病史、细致的查体和规范的肌电图检查对于早期诊断具有关键性的作用。
影像学等其他辅助检查在鉴别诊断中具有一定价值。
根据患者所出现症状、体征的解剖部位,可分为脑干、颈、胸和腰骶4 个区域;根据临床和肌电图检查所证实的上、下运动神经元受累区域多少,可分为不同的ALS 诊断级别(EI Escorial标准修订版)(表4-1)。
1. 临床确诊ALS 通过临床或电生理检查,证实在4 个区域中至少有3 个区域同时存在上、下运动神经元同时受累的证据。
2 临床拟诊ALS 通过临床或电生理检查,证实在4 个区域中至少有2 个区域同时存在上、下运动神经元同时受累的证据。
3.实验室支持的拟诊ALS1 个区域上、下运动神经元同时受累或仅有上运动神经元受累伴电生理检查提示至少2 个区域的下运动神经元受累,影像和实验室检查排除其他疾病。
4)临床可能ALS :通过临床或电生理检查,证实仅有1 个区域存在上、下运动神经元同时受累的证据,或者在2 个或以上区域仅有上运动神经元受累的证据。
已经行影像学和实验室检查排除了其他疾病。
表4-1ALS 诊断标准核心标准:1.下运动神经元体征(包括肌电图有表现但在临床上未累及的肌肉)2.上运动神经元体征3.症状和体征逐渐进展排除标准:1.感觉症状2.括约肌障碍3.视觉障碍4.自主神经功能5.基底神经节功能障碍6.阿尔茨海默型痴呆7.类ALS 综合征(如解剖变异/压迫综合征,获得性酶缺陷,自身免疫性综合征,中毒,感染,内分泌异常等)支持标准:1.在一个或多个区域肌束震颤2.肌电图示神经源性损害3.运动和感觉神经正常4.无传导阻滞鉴别诊断在ALS 的诊断过程中,根据症状和体征的不同,需要与多种疾病进行鉴别,常见的有颈椎病、腰椎病、多灶性运动神经病、平山病、成人脊髓性肌萎缩、肯尼迪病、遗传性痉挛性截瘫等。
治疗尽管ALS 仍是一种无法治愈的疾病,但有许多方法可以改善患者的生活质量。
早期诊断,早期治疗,尽可能地延长生存期。
治疗上除了延缓病情发展和对症治疗的药物外,还包括营养管理、呼吸支持和综合治疗等。
1.药物治疗(1)利鲁唑:化学名为2-氨基-6(三氟甲氧基)-苯并噻唑。
其作用机制包括稳定电压门控钠通道的非激活状态、抑制突触前谷氨酸释放、激活突触后谷氨酸受体以促进谷氨酸的摄取等。
该药是目前唯一证实可以在一定程度上延缓病情发展的药物,用法为50mg,每日2 次口服。
常见不良反应为疲乏和恶心,个别患者可出现肝转氨酶升高,需注意监测。
当患者已经使用有创呼吸机辅助呼吸时,不建议继续服用。
(2)其他药物:依达拉奉在部分国家被批准可以用于早期ALS 患者的治疗,众多针对不同发病机制的临床试验也仍在进行。
临床上也常使用多种维生素治疗。
另外,根据患者情况,可以选用不同的对症治疗药物以改善抑郁、焦虑、失眠、流涎、肢体痉挛、疼痛等症状。
2. 营养管理(1)能够正常进食时应采用均衡饮食;吞咽困难时宜采用高蛋白、高热量饮食以保证营养摄入。
进食软食、半流食,少食多餐。
(2)当患者吞咽明显困难、体重下降、脱水或存在呛咳误吸风险时,应尽快行经皮内镜胃造瘘术(percutaneous endoscopic gastrostom,y PEG)。
对于拒绝或无法行PEG 者,可采用鼻胃管进食。
3. 呼吸支持当ALS 患者出现呼吸肌无力时,需要尽早考虑治疗的方法,与患者和家属就无创通气、有创通气以及后期的处理达成共识。
在使用有创呼吸机辅助呼吸前,建议定期检查肺功能。
4. 综合治疗ALS 患者治疗过程中,应注重多科协作,涉及神经科、呼吸内科、消化内科、心理科、康复科、营养科等,护理人员在其中也发挥着重要作用。
诊疗流程(图4-1)图4-1 肌萎缩侧索硬化(ALS )诊疗流程根据EI Escorial 标准修订版参考文献[1] Brown RH, Al-Chalabi A.Amyotrophic Lateral Sclerosis. N Engl JMed,2017,377(2):162-172.[2] Brooks BR, Miller RG , Swash M, et al. For the World Federation of NeurologyResearch Committee on Motor Neuron Disease. EI Escorial revisited: revised criteria for the diagnosis of amyotrophic lateral sclerosis. Amyotrophic Lateral Sclerosis, 2000,1:293-300.[3] Ludolph A, Drory V , Hardiman O, et al. Arevisionof theElEscorialcriteria-2015.Amyotroph Lateral Scler Frontotemporal Degener, 2015,16(5-6):291-292. [4] 中华医学会神经病学分会. 肌萎缩侧索硬化的诊断标准. 中华神经科杂志,2001,34:190.。
