N端脑钠肽前体检测试剂盒(胶体金免疫层析法)产品技术要求huachengyuan
氨基末端脑利钠肽前体测定试剂盒(磁微粒化学发光免疫分析法)产品技术要求华大吉比爱

氨基末端脑利钠肽前体测定试剂盒(磁微粒化学发光免疫分析法)
适用范围:用于体外定量测定人血清、血浆或全血中氨基末端脑利钠肽前体(NT-proBNP)的含量。
1.1 包装规格
24人份/盒、48人份/盒。
1.2 主要组成成分
注:定标液浓度具有批特异性,具体浓度见标签。
2.1 外观
外观应符合如下要求:
a)试剂盒各组分应齐全、完整,液体无渗漏;
b)包装标签应清晰,无破损。
2.2 溯源性
根据GB/T21415-2008的要求提供定标液的来源、赋值过程以及测量不确定度等内容,溯源至企业工作校准品。
2.3 准确度
对企业准确度质控品进行检测,其测量结果的相对偏差应不超过±10%。
2.4 检出限
检出限应小于28pg/mL。
2.5 线性
在[30,30000]pg/mL线性范围内,相关系数r应≥0.9900。
2.6 重复性
分别用高、中、低3个浓度的样本,各重复检测10次,其变异系数(CV)应不大于10%。
2.7 批间差
用3个批号试剂盒分别检测高、中、低3个浓度的样本,则3个批号试剂盒之间的批间变异系数(CV)应不大于15%。
2.8 分析特异性
检测浓度为3.5μg/mL BNP,检测结果<30pg/mL。
2.9 稳定性
2℃~8℃保存12个月,取效期末的试剂盒进行检测,应符合2.3、2.4、2.5、2.6、2.8的要求。
N末端心房利钠肽前体(NT-proBNP)测定试剂盒(免疫荧光层析法)说明书 新健康成

N末端心房利钠肽前体(NT-proBNP)测定试剂盒(免疫荧光层析法)说明书1. 产品概述本产品是一种针对人体内N末端心房利钠肽前体(NT-proBNP)的测定试剂盒,采用免疫荧光层析法进行测定。
该试剂盒适用于临床医学实验室分析仪器的使用,用于定量测定人体血清或血浆中NT-proBNP的浓度,以协助临床诊断与治疗。
2. 产品原理本试剂盒采用免疫荧光层析法进行测定,利用特定的抗体与目标物NT-proBNP结合形成复合物,通过荧光信号的检测和定量分析,确定样本中目标物的浓度。
3. 试剂组成本试剂盒包含以下组分:•试剂盒盖板(1个)•试剂盒外盒(1个)•标准品(包含不同浓度的NT-proBNP,1套)•样本稀释液(1瓶)•封闭液A(1瓶)•封闭液B(1瓶)•洗涤缓冲液(1瓶)•底物A(1瓶)•底物B(1瓶)•停止液(1瓶)•离心管(适量)•微孔板(96孔)4. 操作步骤步骤1:准备工作1.首先将待测样本,标准品和试剂从冰箱中取出,并使其回至室温。
2.打开试剂盒外盒,检查试剂的完整性和有效期。
3.预热分析仪器至指定温度。
步骤2:标准曲线的制备1.将标准品稀释为不同浓度的工作液。
依次取出标准品管的适量体积,加入稀释液中,充分混合。
2.取出微孔板中的一行作为空白对照,加入适量的稀释液。
3.将制备好的工作液分别加入微孔板中,每个孔加入相同体积的工作液。
4.注意用标签标记好每行的标准品浓度。
步骤3:样本测定1.取出样本离心管,将待测样本加入管中。
2.取出微孔板中的一行作为样本孔,将样本离心管中的样本加入样本孔中。
3.热封微孔板,确保样本充分与试剂反应。
4.将微孔板放入分析仪器中,按照仪器操作说明进行测定。
步骤4:结果分析1.仪器完成测定后,读取测定结果。
2.通过标准曲线,根据测定结果计算出样本中NT-proBNP的浓度。
5. 结果解读对于NT-proBNP的浓度结果,根据临床实验室的参考值范围进行判断和解读。
6. 注意事项•本试剂盒仅适用于专业实验室内使用,禁止非专业人员操作。
胶体金免疫层析分析仪产品技术要求zhongbaihecheng

胶体金免疫层析分析仪适用范围:与本公司已上市的胶体金法定量检测试剂盒配套使用。
用于检测人体血清中肌红蛋白/肌钙蛋白I/肌酸激酶同工酶(Myo/cTnI/CK-MB)的含量。
1.1 型号TT-06TT-TalenTank即智慧盒的英文字头06-开始研发年份的缩写1.2 结构组成胶体金免疫层析分析仪由成像系统、分析系统和液晶显示屏组成。
2.1正常工作条件a)环境温度:5℃~40℃;b) 相对湿度:≤80%;c) 电源要求:AC 220V,50Hz;d) 大气压力:860hPa~1060hPa;e) 环境光强度:避免阳光直射。
2.2外观2.2.1胶体金免疫分析仪表面应整齐、清洁,面层无明显剥落、擦伤及污垢;2.2.2铭牌及标志应清楚,所有紧固件不得松动,各种控制器件功能正常。
2.3准确度2.3.1分析仪测试肌红蛋白的结果与贝克曼校准品标示值之间的偏差不超过±5%。
2.3.2分析仪测试肌酸激酶同工酶的结果与贝克曼校准品标示值之间的偏差不超过±5%。
2.3.3分析仪测试肌钙蛋白I的结果与贝克曼校准品标示值之间的偏差不超过±5%。
2.4重复性胶体金免疫分析仪的重复性应符合表1的要求表1胶体金免疫分析仪重复性要求2.5线性胶体金免疫分析仪的线性要求应符合表2的要求表2 胶体金免疫分析仪线性要求2.6稳定性分析仪开机处于稳定工作状态后第4个小时、第8个小时的测试结果与处于稳定工作状态初始时的测试结果的相对偏倚不超过±10%。
2.7软件功能a、测试分为即时方式和全时间方式两种。
即时方式:由操作员自己计时,手动启动应用程序开始测试。
全时间方式:由检测仪自动计时,计时结束后自动开始测试。
b、胶体金免疫分析仪具有病历信息输入功能。
C、胶体金免疫分析仪具有打印输出功能。
2.8安全要求应符合GB4793.1—2007《测量、控制和实验室用电气设备的安全要求第1部分:通用要求》、GB 4793.9-2013《测量、控制和实验室用电气设备的安全要求第9部分:实验室用分析和其他目的自动和半自动设备的特殊要求》瞬间过压类别II类,额定污染等级2级设备的要求;以及YY0648-2008《测量、控制和试验室用电气设备的安全要求第2-101部分体外诊断(IVD)医用设备的专用要求》的要求。
N末端脑利钠肽前体(NT-proBNP)测定试剂盒(电化学发光免疫分析法)产品技术要求lianzhongtaike
N末端脑利钠肽前体(NT-proBNP)测定试剂盒(电化学发光免疫分析法)适用范围:该试剂盒用于体外定量测定人体血清样本中N末端脑利钠肽前体(NT-proBNP)的含量。
1.1产品型号/规格:50人份/盒、100人份/盒。
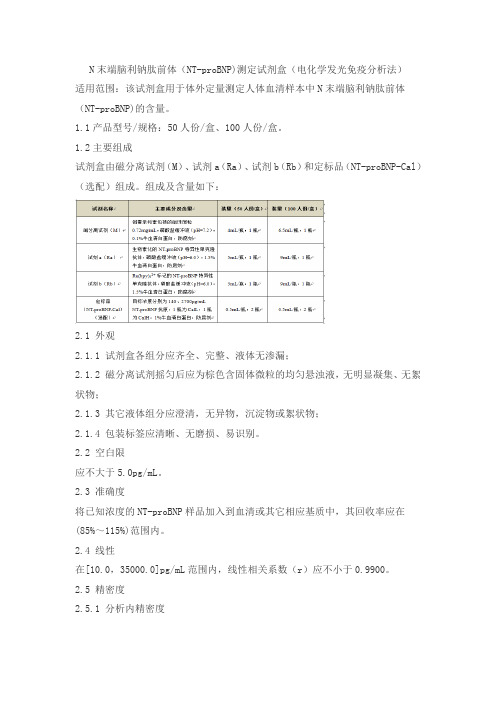
1.2主要组成试剂盒由磁分离试剂(M)、试剂a(Ra)、试剂b(Rb)和定标品(NT-proBNP-Cal)(选配)组成。
组成及含量如下:2.1 外观2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物;2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物;2.1.4 包装标签应清晰、无磨损、易识别。
2.2 空白限应不大于5.0pg/mL。
2.3 准确度将已知浓度的NT-proBNP样品加入到血清或其它相应基质中,其回收率应在(85%~115%)范围内。
2.4 线性在[10.0,35000.0]pg/mL范围内,线性相关系数(r)应不小于0.9900。
2.5 精密度2.5.1 分析内精密度在试剂盒的线性范围内,浓度为(500.0±100.0pg/mL)、(1000.0±200.0pg/mL)和(5000.0±1000.0pg/mL)的样品检测结果的变异系数(CV)应不大于8%。
2.5.2 批间精密度在试剂盒的线性范围内,用3个批号试剂盒分别检测浓度为(500.0±100.0pg/mL)、(1000.0±200.0pg/mL)和(5000.0±1000.0pg/mL)的样品,检测结果的变异系数(CV)应不大于15%。
2.6 效期末稳定性本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。
2.7 溯源性依据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,定标品溯源到罗氏的NT-proBNP定标液。
N端脑钠肽前体测定试剂盒(胶体金免疫层析法)产品技术要求yuepu

N端脑钠肽前体测定试剂盒(胶体金免疫层析法)适用范围:本试剂盒配合北京x普医疗科技有限责任公司生产的免疫定量分析仪,用于临床样本(全血/血清/血浆)中N端脑钠肽前体的定量检测。
1.1 规格卡型1人份、10人份/盒、20人份/盒、50人份/盒。
1.2组成每盒含1/10/20/50人份检测卡和1份说明书、批号卡和样品缓冲液。
每人份检测卡包括1份N端脑钠肽前体检测卡、1支滴管和1包干燥剂,选配件为医用酒精棉、无菌采血针(注:选配件均为外购已获得医疗器械注册证的产品)。
N端脑钠肽前体检测卡由样品垫、硝酸纤维素膜(T线包被鼠抗人NT-proBNP单克隆抗体;C线包被抗鼠抗体)、金标垫(包被胶体金标记的鼠抗人NT-proBNP单克隆抗体)、吸水纸、塑料载板组成。
2.1物理性状2.1.1 外观检测卡应整洁完整、无毛刺、无破损、无污染;材料附着牢固;标签字迹清晰,无破损。
2.1.2 膜条宽度检测卡的膜条宽度≥2.5mm。
2.1.3 液体移行速度液体移行速度应不低于10 mm/min。
2.2 空白检出限空白检出限应不高于100pg/mL。
2.3 精密度2.3.1批内精密度批内精密度CV(%)应不高于15.0%。
2.3.2 批间精密度批间精密度CV(%)应不高于15.0%。
2.4 剂量-反应曲线的线性在100pg/ml~6000pg/ml的范围内,用线性拟合公式拟合,剂量-反应曲线相关系数应不低于0.975。
2.5 准确度2.5.1型式检验项目:检测N端脑钠肽前体纯品,样本回收率应高于85%。
2.5.2出厂检验项目:检测已知浓度的N端脑钠肽前体测定样品液,实测值与标示值的偏差范围应不高于15%。
2.6稳定性将试剂盒在4℃~30℃的环境中放置18个月后,取样分别检测2.1、2.2、2.3.1、2.4、2.5.2项,结果应符合各项目的要求。
氨基末端脑钠肽前体测定试剂盒(荧光免疫法)产品技术要求yuepu

氨基末端脑钠肽前体测定试剂盒(荧光免疫法)组成:每盒包含相应规格检测卡和1份产品二维码(内含校准信息)。
每人份检测卡包括1份氨基末端脑钠肽前体检测卡和1包干燥剂。
氨基末端脑钠肽前体检测卡由PMMA镀膜、反应室(T线包被鼠抗人NT-proBNP单克隆抗体;C线包被羊抗鼠抗体)、荧光微球室(储存荧光微球标记的鼠抗人NT-proBNP单克隆抗体)、回收池、塑料结构支撑层组成。
适用范围:本产品用于体外定量检测人全血、血清、血浆中氨基末端脑钠肽前体含量。
1.1规格卡型1人份/盒、10人份/盒、20人份/盒、50人份/盒。
1.2组成每盒包含相应规格检测卡和1份产品二维码(内含校准信息)。
每人份检测卡包括1份氨基末端脑钠肽前体检测卡和1包干燥剂。
氨基末端脑钠肽前体检测卡由PMMA镀膜、反应室(T线包被鼠抗人NT-proBNP单克隆抗体;C线包被羊抗鼠抗体)、荧光微球室(储存荧光微球标记的鼠抗人NT-proBNP单克隆抗体)、回收池、塑料结构支撑层组成。
2.1物理性状2.1.1外观应整洁完整、无毛刺、无破损、无污染;材料附着牢固;标签字迹清晰,无破损。
2.1.2液体移行速度液体移行速度应不低于10 mm/min(到达Test区应低于2min)。
2.2检出限检出限应不高于30pg/mL。
2.3重复性分别用低、中、高3个浓度的氨基末端脑钠肽前体样本液,测定变异系数(CV)应不大于15%。
2.4批间差用3个批号试剂卡分别检测低、中、高3个浓度的氨基末端脑钠肽前体样本液,变异系数(CV)应不大于15%。
2.5线性在[30,30000]pg/mL线性范围内,相关系数应不低于0.990。
2.6准确度以指定的已上市试剂盒作为比对方法,进行比对试验,相关系数(r)应不小于0.950,斜率应在[0.9,1.1]内。
2.7校准信息溯源性应根据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》提供所用校准品的来源、赋值过程以及测量不确定度等内容,校准信息可溯源至本公司工作校准品,工作校准品由罗氏试剂盒比对赋值。
氨基末端脑利钠肽前体测定试剂盒(荧光免疫层析法)产品技术要求北京协和洛克
氨基末端脑利钠肽前体测定试剂盒(荧光免疫层析法)适用范围:本试剂盒适用于体外定量测定人全血或血浆中氨基末端脑利钠肽前体(NT-proBNP)浓度。
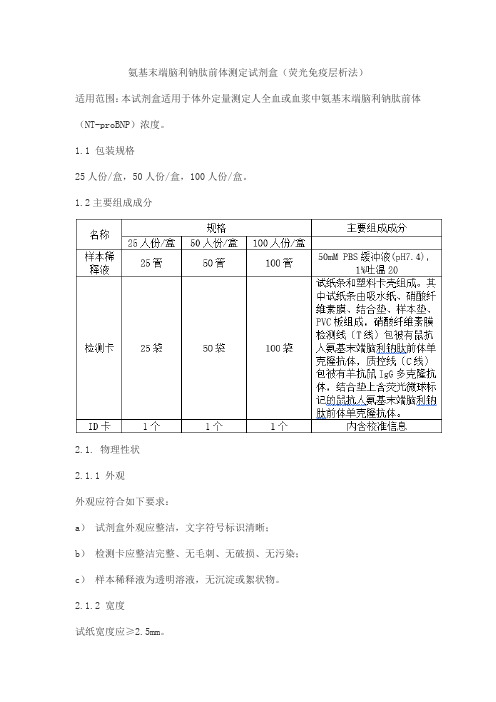
1.1 包装规格25人份/盒,50人份/盒,100人份/盒。
1.2主要组成成分2.1. 物理性状2.1.1 外观外观应符合如下要求:a)试剂盒外观应整洁,文字符号标识清晰;b)检测卡应整洁完整、无毛刺、无破损、无污染;c)样本稀释液为透明溶液,无沉淀或絮状物。
2.1.2 宽度试纸宽度应≥2.5mm。
2.1.3 移行速度液体移行速度应不低于10mm/min。
2.1.4 样本稀释液装量液体体积为180μL±3.6μL。
2.2 准确度对高、低浓度质控品进行检测,其测量结果的相对偏差应不超过±15%。
2.3 检出限不高于20pg/mL。
2.4 线性试剂盒的线性范围为[30,30000]pg/mL,相关系数r不小于0.990。
2.5重复性分别用高、中、低3个浓度的质控品,各重复检测10次,其变异系数(CV)应不大于13%。
2.6 批间差用3个批号试剂盒分别检测高、中、低3个浓度的质控品,3个批号试剂盒之间的批间变异系数(CV)应不大于15%。
2.7 特异性分别将浓度为1ng/mL肾上腺素、1ng/mL NT-proANP、2μg/mL C型钠肽CNP、0.6ng/mL血管紧张素作为样本进行特异性反应,交叉反应率应小于5%。
2.8效期稳定性试剂盒在2℃~30℃储存有效期为18个月,取到效期后产品进行检测,检测结果应符合2.1~2.5,2.7项要求。
2.9溯源性根据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》及有关规定提供所用校准品的来源、赋值过程以及不确定度等内容,溯源至企业工作校准品,并与已上市产品比对赋值。
N-末端脑钠肽前体(NT-proBNP)测定试剂盒(胶体金免疫层析法)产品技术要求贝尔

N-末端脑钠肽前体(NT-proBNP)测定试剂盒(胶体金免疫层析法)适用范围:用于体外定量测定人血清或血浆中的N-末端脑钠肽前体(NT-ProBNP)含量。
1.1 包装规格20人份/盒1.2主要组成成分本试剂盒由NT-ProBNP检测卡、干燥剂和滴管组成。
NT-ProBNP检测卡由试纸条外壳与试纸条构成,试纸条由样品垫、胶体金垫(喷有由胶体金标记的NT-ProBNP 单克隆抗体)、层析膜(T线包被有NT-ProBNP单克隆抗体,C线包被有羊抗鼠IgG抗体)、吸水纸、衬垫构成。
检测卡为20人份/盒,干燥剂为1个/袋,滴管为20个/盒。
2.1 物理性状2.1.1 外观试剂盒各组分齐全、完整;包装袋应密封性好无破损;标签清晰;材料附着牢固,条宽应适应于卡壳且装配紧密。
2.1.2 膜条宽度膜条宽度应不低于4.0mm。
2.1.3 液体移行速度液体移行速度应不低于10mm/min。
2.2 空白检测限应小于200pg/ml。
2.3 分析特异性与5ng/ml cTnI、250ng/ml Myoglobin和50ng/ml CK-MB分析特异性参考品进行交叉反应测定,测定结果应均小于200pg/ml。
2.4 重复性用500pg/ml N-末端脑钠肽前体(NT-proBNP)参考品和6000pg/ml N-末端脑钠肽前体(NT-proBNP)参考品各重复检测10次,其变异系数(CV)应不大于15%。
2.5 准确度将12000pg/ml N-末端脑钠肽前体(NT-proBNP)血清参考品加入到N-末端脑钠肽前体(NT-proBNP)含量为200pg/ml正常人血清参考品中,按照体积比1:9混合,对混合后样本进行检测,回收率应在85%~115%范围内。
2.6 线性线性范围为[200,12000]pg/ml,试剂盒的相关系数r应≥0.99。
2.7 批间差用3个批号试剂盒对500pg/ml N-末端脑钠肽前体(NT-proBNP)参考品和6000pg/ml N-末端脑钠肽前体(NT-proBNP)参考品各重复检测10次,则3个批号试剂盒之间的批间相对偏差(R)应不大于15%。
N末端脑钠肽(NT—proBNP)检测试剂盒(免疫层析法)产品技术要求模板

医疗器械产品技术要求编号:
N末端脑钠肽(NT—proBNP)检测试剂盒
(免疫层析法)
1.产品型号/规格及划分说明
1.1产品型号/规格
20人份/盒。
1.2结构组成
由检测卡、干燥剂和说明书组成;检测卡由鼠抗NT-proBNP单抗、胶体金鼠抗NT-proBNP单抗,羊抗鼠IgG和硝酸纤维素膜等支持物组成。
1.3 适用范围
用于体外定性检测血清中的N末端脑钠肽(NT-proBNP)。
2.性能指标
2.1外观
2.1.1检测卡应无明显划痕、气泡、外观平整,材料附着牢固。
2.1.2检测卡的文字和标记应清晰、准确。
2.2膜条宽度
检测条的宽度应≥2.5mm。
2.3液体移行速度
液体移行速度应不低于 10mm/分钟
2.4灵敏度(最低检出限)
本试剂盒对 NT-proBNP 最低检出限为 200 pg/mL。
2.5检测范围
本试剂盒 NT-proBNP 检测范围为 200 pg/mL~15,000 pg/mL。
2.6特异性
试剂盒与心肌钙蛋白-I(cTn-I)、肌酸激酶同工酶(CK-MB)、肌红蛋白(Myoglobin) 均不发生交叉反应。
2.7精密度
2.7.1批内精密度
取同一批号试剂对精密度参考品(NT-proBNP 1000 pg/mL)分别进行 10 次测定,反应结果应一致,且显色度应均一。
2.7.2批间精密度
分别取连续三个批号试剂对精密度参考品(NT-proBNP 1000 pg/mL)分别进行 10 次测定,反应结果应一致,且显色度应均一。
N-末端脑钠肽前体测定试剂盒(荧光免疫层析法)产品技术要求zhongjianantai

N-末端脑钠肽前体测定试剂盒(荧光免疫层析法)适用范围:本试剂盒用于体外定量检测人体血清、血浆或全血样本中N-末端脑钠肽前体(NT-proBNP)的含量。
1.1包装规格:20人份/盒,40人份/盒。
1.2主要组成:表1 试剂盒产品组成表2.1 物理检查2.1.1 外观外观平整,材料附着牢固,内容齐全,试剂无杂质,外包装完整无破损,标签清晰可辨。
2.1.2 膜条宽度膜条宽度应满足4.0mm±0.2mm。
2.1.3 液体移行速度液体移行速度应不低于10mm/min。
2.1.4 样本稀释液样本稀释液的净含量应不少于标示值,且其pH值为7.0±0.2。
2.2准确度准确度应符合以下要求之一。
a). 回收率:将已知浓度的高浓度质控品加入到低浓度血清中测定回收率,要求在85%~115%范围内。
b). 比对试验采用与罗氏诊断产品(上海)有限公司的脑利钠肽前体检测试剂盒(电化学发光法)检测的样本进行对比试验,相关系数(r)应不小于0.950,斜率应在[0.9,1.1]内。
2.3线性范围在[56,35000]pg/ml范围内,相关系数(r)应不低于0.990。
2.4 重复性分别检测高、中、低三个浓度的样本,变异系数(CV)应不高于10.0%。
2.5批间差用三个批号试剂盒分别检测高、中、低三个浓度的样本,三个批号试剂盒之间的批间变异系数(CV)应不高于15.0%。
2.6 检出限检出限低于30pg/mL。
2.7校准信息溯源性校准信息所用工作校准品根据GB/T 21415-2008 《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的规定,溯源至企业工作校准品,工作校准品通过已上市产品进行赋值。
2.8稳定性试剂盒在规定的条件下保存至有效期末,取到效期后两个月内试剂盒,检测2.2、2.3、2.4、2.6项,结果应符合要求。
脑自然肽N端前体蛋白测定试剂盒(化学发光法)产品技术要求新产业

2.性能指标
2.1外观和性状
试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰、准确、牢固;试剂盒内组分(磁性微球溶液除外)应为澄清的液体,无沉淀、无悬浮物、无絮状物。
2.2装量及允差
试剂盒的装量应不少于额定装量(见表1)。
表 1
2.3重复性
分别用高、中、低 3 个浓度的样本,各重复检测10 次,其变异系数(CV)应不大于8%。
2.4批间精密度
用3个批号试剂盒分别检测高、中、低3个浓度的样本,3个批号试剂盒之间的变异系数(CV)应不大于15%。
2.5准确度
相对偏差应在±10% 范围内。
2.6空白限
试剂盒的空白限应小于 2.0 pg/mL。
2.7检出限
试剂盒的检出限应≤5.0 pg/mL
2.8线性
在(5.0~35000.0)pg/mL 浓度范围内,线性相关系数(r)绝对值应大于0.9900。
一种用于N-端脑利钠肽前体测定的免疫层析试纸[实用新型专利]
![一种用于N-端脑利钠肽前体测定的免疫层析试纸[实用新型专利]](https://img.taocdn.com/s3/m/b78ebe10fab069dc512201cf.png)
专利名称:一种用于N-端脑利钠肽前体测定的免疫层析试纸专利类型:实用新型专利
发明人:熊晶,余占江,陈永强,梅鸥
申请号:CN202020936125.6
申请日:20200528
公开号:CN212364322U
公开日:
20210115
专利内容由知识产权出版社提供
摘要:本实用新型提供一种用于N‑端脑利钠肽前体测定的免疫层析试纸,具体涉及到生物应用技术领域。
本实用新型包括底板,底板的一端高于底板的另一端,底板上设有样品垫,样品垫设于底板的一端,样品垫的端部设有结合垫,结合垫的一端设于样品垫与底板之间,结合垫的另一端设有反应膜,反应膜的一端设于结合垫和底板之间,反应膜上设有检测线和质控线;样品垫与结合垫相接触的端面和结合垫与反应膜相接触的端面分别呈圆弧状;反应膜的另一端设有吸水垫,吸水垫的端面与反应膜的上端面和下端面相接。
本实用新型提出的一种用于N‑端脑利钠肽前体测定的免疫层析试纸,能够缩短反应测试的时间,提高实验效率。
申请人:江苏奥雅生物科技有限公司
地址:225300 江苏省泰州市中国医药城口泰路西侧、陆家路东侧0004幢G59号三层
国籍:CN
代理机构:南京常青藤知识产权代理有限公司
代理人:金迪
更多信息请下载全文后查看。
氮末端脑利钠肽前体的免疫胶体金的快速定性检测盒[发明专利]
![氮末端脑利钠肽前体的免疫胶体金的快速定性检测盒[发明专利]](https://img.taocdn.com/s3/m/99ce270d551810a6f42486ad.png)
专利名称:氮末端脑利钠肽前体的免疫胶体金的快速定性检测盒
专利类型:发明专利
发明人:方艳秋,谭岩,刘力华,段秀梅,许淑芬,姜艳芳,宋艳,刘玲丽,时阳
申请号:CN200410011165.5
申请日:20041020
公开号:CN1763531A
公开日:
20060426
专利内容由知识产权出版社提供
摘要:一种氮末端脑利钠肽前体的免疫胶体金的快速定性检测盒,涉及一种对血液进行检测的方法。
本发明采用高亲和力特异性单克隆抗体,按照免疫化学方法和免疫层析技术的原理制备的氮末端脑利钠肽前体的免疫胶体金的快速定性检测盒。
本发明具有灵敏度高、特异性好、符号显示结果、操作简便、无需特殊仪器设备、反应迅速、5~15分钟判读结果等特点。
虽然NT pro-BNP和BNP检测的意义相同,但NT pro-BNP测定有2个优点,半衰期比BNP长而且测定水平的影响因素比BNP 少。
申请人:吉林大学第一医院
地址:130061 吉林省长春市新民大街1号
国籍:CN
代理机构:吉林长春新纪元专利代理有限责任公司
代理人:白冬冬
更多信息请下载全文后查看。
N末端脑钠肽前体(NT—proBNP)测定试剂盒(化学发光免疫分析法)产品技术要求深圳锦瑞

N末端脑钠肽前体(NT-proBNP)测定试剂盒(化学发光免疫分析法)2性能指标2.1外观和性状试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰,准确、牢固;外观和性状应符合表2 要求。
表 2 试剂盒内各组分的外观性状2.2装量试剂盒内各组分装量应不少于标示值。
2.3准确度对工作校准品进行检测,其测量结果的相对偏差应不超过±10%。
2.4检出限应不高于15 pg/mL。
2.5线性试剂盒在15 pg/mL~30000 pg/mL 区间范围内,其线性相关系数r≥0.9900。
2.6重复性分别用(125±25) pg/mL、(1200±240) pg/mL、(15000±3000) pg/mL 浓度范围内的3 个样本,各重复检测10 次,其变异系数(CV)应不大于8%。
2.7批间差用3 个批号试剂盒分别检测(125±25) pg/mL、(1200±240) pg/mL、(15000±3000)pg/mL 浓度范围内的3 个样本,3 个批号试剂盒之间的批间变异系数(CV)应不大于10%。
2.8质控品测定值用试剂盒配套的校准品校准测量系统后,以试剂盒配套的质控品作为样本进行检测,其测定结果应在标示浓度范围内。
2.9质控品均一性瓶间变异系数(CV)应不大于10%。
2.10校准品测量准确度用工作校准品校准测量系统后,以试剂盒配套的校准品作为样本进行检测,其测定结果与标示值的相对偏差应在±10%范围内。
2.11校准品均一性瓶间变异系数(CV)应不大于10%。
N-端脑利钠肽前体检测试剂盒(胶体金法)

N-端脑利钠肽前体检测试剂盒(胶体金法)使用说明书【产品名称】通用名称:N-端脑利钠肽前体检测试剂盒(胶体金法)英文名称:One Step Test for NT-proBNP (Colloidal Gold)【包装规格】包装规格:10人份/盒,25人份/盒【预期用途】本检测试剂盒适用于临床体外定量或半定量检测人血中N-端脑利钠肽前体(NT-proBNP,下文中“N-端脑利钠肽前体”均使用其英文缩写“NT-proBNP”)的含量。
【检验原理】以一株高特异性、高敏感性NT-proBNP单克隆抗体和另一株NT-proBNP多克隆抗体,其中单克隆抗体为标记抗体,多克隆抗体为捕获抗体,结合链亲和素-生物素放大系统,应用免疫金标层析技术,检测人血中NT-proBNP的含量。
NT-proBNP是BNP激素原(proBNP)分裂后无活性的N端片段,主要在心肌细胞受到容量负荷和压力负荷增高时由左心室分泌。
NT-proBNP可用于评价心脏收缩功能不全以及舒张功能不全和心室壁节段运动协调性,有较高的敏感性和阴性预测价值;应用于早期发现心力衰竭(HF)病人,并进行危险分层,监测心衰药物的疗效评估,判断心衰病人的预后,区分心衰及其他原因引起的呼吸困难;可作为急性冠状动脉综合征(ACS)的风险评估指标。
【主要组成成份】1. N-端脑利钠肽前体检测试剂盒:内含10条单人份或25条单人份检测卡;检测卡由试纸条外壳与试纸条构成,试纸条由样品垫、胶体金垫(喷有由胶体金标记并结合了链亲和素-生物素放大系统的NT-proBNP单克隆抗体)、层析膜(T线包被有NT-proBNP捕获多克隆抗体,C线包被有兔抗鼠IgG 抗体)、吸水纸、衬垫构成;2. 说明书一份;3. 标准比色卡一张。
注:不同批的N-端脑利钠肽前体检测试剂盒(胶体金法)各组分不可以互换。
【适用仪器】南京普朗医用设备有限公司FIA8000系列免疫定量分析仪。
【储存条件及有效期】试剂盒于4~30℃保存,铝箔袋密封状态下存放,有效期为12个月;铝箔袋拆封后,有效期为1小时。
N末端B型钠尿肽前体检测试剂盒(胶体金免疫层析法)产品技术要求热景

N末端B型钠尿肽前体检测试剂盒(胶体金免疫层析法)产品技术要求热景N末端B型钠尿肽前体检测试剂盒(胶体金免疫层析法)适用范围:用于体外半定量检测人血清、血浆及全血样本中的N 末端B型钠尿肽前体(NT-proBNP)。
1.1包装规格:20人份/盒、40人份/盒1.2 主要组成成分:2.1 外观液体组分应澄清透明、无沉淀或絮状物,铝箔袋应无破损漏气现象。
2.2 物理性能2.2.1 试纸条宽度应为6.0±0.1mm。
2.2.2 液体移行速度应不低于10mm/min。
2.3准确性分别对浓度为4000pg/mL、900pg/mL、450pg/mL、200pg/mL的质控品进行重复测试20次,检测结果与相应质控品标示值相差同向不超过一个量级,不得出现反向相差。
阳性质控品不得出现阴性结果,阴性质控品不得出现阳性结果,各浓度检测结果一致性不低于90%。
2.4 HOOK效应使用浓度为10000pg/mL的质控品重复测定3次,结果应不出现阴性。
2.5最低检测限最低检测限应不大于200pg/mL。
2.6精密度2.6.1重复性:取同一批检测卡测定450pg/mL的质控品10次,反应结果一致,全部为阳性。
2.6.2批间差:取三批检测卡测定450pg/mL的质控品10次,反应结果一致,显色度均一,全部为阳性。
2.7特异性与人血清白蛋白(HSA)、胆红素无显著干扰反应。
与其它物质的干扰反应数据2.8稳定性本产品有效期18个月,取到效期产品在2个月内进行检测,测定结果应符合上述2.1、2.2、2.3、2.4、2.5、2.6.1、2.7项要求。
产品技术要求性能指标部分-N末端脑钠肽前体

医疗器械产品技术要求编号:
N末端脑钠肽前体测定试剂盒(荧光免疫层析法)
2. 性能指标
2.1 外观
2.1.1试剂盒外观应整洁,文字符号标识清晰,封装无破损,内容物齐全。
2.1.2检测卡的外观应符合下列要求:外观平整、色泽均匀、边缘无毛刺,不能有色斑或污渍。
2.1.3稀释液应澄清透明、无沉淀、无悬浮物、无絮状物、无渗漏。
2.1.4检测卡内的膜条要求:宽度为4.0±0.5mm,长度为67±2mm。
2.2 净含量
稀释液瓶装量应≥100μl。
2.3物理检测
样本在检测卡上的移行速度应≥10mm/min。
2.4 准确度
分别测定高、中、低三个浓度的NT-proBNP企业内部参考品,相对偏差不超过±10%。
2.5检出限
检出限应小于30 pg/ml。
2.6线性范围
在线性范围30-30000pg/ml内,
a)其线性相关系数(r)应不小于0.990;
b)在[30~4000]pg/ml区间内测定的线性绝对偏差不超过±400 pg/ml,在(4000~30000] pg/ml 区间内测定的线性相对偏差应不超过±10%。
2.7 重复性
用同一批次试剂盒分别测定高、中、低三个浓度企业内部参考品,各重复检测10次,所得结果的批内变异系数(CV)应不大于10%。
2.8批间差
用3个批号的试剂盒分别测定高、中、低三个浓度的企业参考品,所得结果的批间变异系数(CV)应不大于15%。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
N端脑钠肽前体检测试剂盒(胶体金免疫层析法)
适用范围:本产品适用于体外半定量检测人血清、血浆、全血中N-端脑钠肽前体的含量。
1.产品型号/规格及其划分说明
1.1 产品型号
产品型号及分类如下表1:
表1 产品型号及分类
U系列(卡型)G系列(条型)宽度(mm)
U2 G2 2.5
U3 G3 3.3
U4 G4 4.0
U5 G5 5.0
注:产品相同系列不同型号间除试剂条宽度外,其余完全一致。
U系列是在G系列试剂条的基础上加卡壳,其余完全一致。
1.2 包装规格
卡型:1人份/盒、1人份/袋;
条形:100人份/盒、50人份/盒、25人份/盒、1人份/袋。
1.3 主要组成成分
(1)检测试剂卡/条由样品垫、金结合物垫(金垫上固定胶体金标记的N-端脑钠肽前体鼠源单克隆抗体)、硝酸纤维素膜(T线包被N-端脑钠肽前体鼠源单克隆抗体,C线包被有羊抗鼠IgG抗体)、吸水纸、PVC胶板构成。
(2)干燥剂。
2.性能指标
2.1 物理性状
2.1.1 外观
a) 试剂盒的外观应平整、边缘无毛刺,包装完整,标签清晰可见;
b) 测试块与基底片固定应紧密、不能有缺损或脱落;
c) 测试块外观整齐、色泽均匀、不能有色斑或污渍。
2.1.2 膜条宽度
试纸条宽度应U2、G2不小于2.5mm;U3、G3不小于3.3mm;U4、G4不小于4.0mm;U5、G5不小于5.0mm。
2.1.3 液体移行速度
液体移行速度应不低于10mm/min。
2.2 重复性及准确性
分别用浓度为200pg/ml、300pg/ml、1800pg/ml的质控液重复测试≥20次,检测结果与相应质控液标示值相差同向不超过一个量级,不得出现反向相差。
阳性质控液不得出现阴性结果,阴性质控液不得出现阳性结果,各浓度检测结果一致性不低于90%。
2.3 HOOK效应
用浓度为30000pg/ml的NT-proBNP的质控液重复测定3次,结果应不出现阴性。
2.4 批间差
取三个批次的试剂盒,分别用浓度为200pg/ml、300pg/ml、1800pg/ml 的质控液重复测试≥20次,检测结果与相应质控液标示值相差同向不超过一个量级,不得出现反向相差。
阳性质控液不得出现阴性结果,阴性质控液不得出现阳性结果,各浓度检测结果一致性不低于90%。
2.5 特异性
测定以下常见干扰物的样本,在下列浓度时结果不出现阳性,见表2:
表2 常见干扰物质浓度及检测结果
干扰物名称浓度检测结果
BNP 30000pg/ml 不得为阳性
2.6 稳定性
试剂盒于4℃~30℃干燥、避光保存,有效期18个月,超过有效期后一个月内分析性能至少应符合2.1、2.2、2.3、2.5的要求。
