磺胺喹恶啉钠可溶性粉生产工艺规程
磺胺氯吡嗪钠可溶性粉生产工艺规程

磺胺氯吡嗪钠可溶性粉生产工艺规程目录1 产品概述2 处方和依据3 工艺流程图4 制剂工艺过程及工艺条件5 原辅材料的预处理6 原辅材料质量标准和检查方法7 中间产品质量标准和检查方法8 成品质量标准和检查方法9 包装规格、包装材料质量标准10 说明书、产品文字说明和标志11 工艺要求12 设备一览表和主要设备生产能力13 技术安全与劳动保护14 劳动组织15 原辅料消耗定额16 包装材料消耗定额17 动力消耗定额18 综合利用与环境保护目的:制定本标准的目的是规范磺胺氯吡嗪钠可溶性粉生产过程,对一定数量的成品所需的起始原辅料和包装材料,以及工艺、加工说明、技术参数、注意事项等进一步标准化。
适用范围:适用于磺胺氯吡嗪钠可溶性粉生产全过程。
责任人:质量部部长、生产部部长、车间主任。
内容:1 产品概述:本品为磺胺氯吡嗪钠可溶性粉。
1.1 产品特点:1.1.1性状:本品为淡黄色粉末。
1.1.2规格:100g:磺胺氯吡嗪钠30g1.1.3贮藏:遮光,密闭保存。
1.1.7有效期:二年1.1.8批准文号:2.处方和依据2.1处方:100g磺胺氯吡嗪钠: 30g无水葡萄糖:加至100g2.2处方依据:3生产工艺流程图及环境区域划分示意图4 制剂工艺过程及工艺条件4.1总述:按生产指令领取磺胺氯吡嗪钠原料药和预处理过的无水葡萄糖,将磺胺氯吡嗪钠与无水葡萄糖用等量递增法混合均匀,定量分装即可。
4.2分述:4.2.1投料量:为处方量的整数倍。
5 原辅材料的预处理5.1 按生产指令单领取无水葡萄糖粉的预处理按粉碎机操作规程操作,粉碎,使完全通过80目筛。
过筛结束后,检查合格将粉碎好的药粉装入洁净容器,称量、记录,挂上标签,注明品名、批号、数量、日期等,填写中间产品交接单,转入下工序。
进行物料平衡计算,收率99.0%~99.5%。
5.2 称量配料:按生产指令单称取磺胺氯吡嗪钠和无水葡萄糖5.3混合:将上述称量好的药粉置V型混合机中,用等量递增法每次预混10分钟,再总混合30分钟,检验含量合格后,装入洁净不锈钢桶密封并标明名称、规格、批量(或数量)等,填写中间产品交接单,转入中间站。
磺胺氯吡嗪钠可溶性粉

磺胺氯吡嗪钠可溶性粉生产工艺规程1产品概述1.1产品名称通用名:磺胺氯吡嗪钠可溶性粉汉语拼音:Huanganl ubi qinna Kerongxingfen1.2剂型:粉剂1.3批准文号:1.4规格:100g:30g1.5包装:100g x 100 袋/ 箱1.6贮存:遮光,密闭保存1.7有效期:两年2处方和依据2.1处方2.2处方依据:本处方依据《中华人民共和国兽药典》2005年版一部磺胺氯吡嗪钠可溶性粉项下制订。
3生产工艺流程图4 操作过程及工艺条件4.1粉碎过筛4.1.1如磺胺氯吡嗪钠和乳糖不能通过五号筛,应进行粉碎。
4.1.2操作人员按本岗位的操作规程将磺胺氯吡嗪钠和乳糖分别粉碎,药粉应通过五号筛。
4.1.3车间质量监督员对粉碎过筛岗位进行检查,符合要求后即可生产。
4.1.4粉碎过筛后的药粉装入洁净容器中,容器外挂物料状态卡,注明名称、规格、批号、数量、日期、操作者和复核人。
4.1.5操作人员填写粉碎过筛批记录,并将记录随物料传入称量配料工序。
4.2称量配料4.2.1磺胺氯吡嗪钠和乳糖使用前应再次检查外观情况,确保质量合格。
称量前操作人员应先核对原料的名称、批号、数量、生产单位等。
确认无误后,进行称量配料。
处方计算和称量过程必须由双人操作,一人称量、一人复核,并由质量监督员监督。
操作过程中,操作人员应及时填写称量记录。
4.2.2称好的物料置于清洁干燥的周转容器内,容器外应挂物料状态卡,注明物料名称、批号、数量、规格、日期、操作人和复核人。
4.3 混合4.3.1混合前操作人员应先核对物料的名称、批号、数量等,确认无误后进行下一步操作。
4.3.2检查各准备工作无误后,将称量好的原料与辅料依次倒入V 型混合机开始混合,混合30分钟。
并保证混合机的装量不超过该机总量的2/3 。
4.3.3经过混合具有均一性的物料为一个批量,编为一个批号。
4.3.4混合好的物料装入洁净的容器内,容器外应挂物料状态卡,写明物料品名、规格、批号、数量、日期、操作者和复核人,传入中间站。
磺胺喹恶啉钠质量标准

一、目的:建立磺胺喹噁啉钠的质量标准,保证产品质量。
二、适用范围:适用于磺胺喹噁啉钠原料药的采购检验。
三、责任者:质保部对本标准执行负责。
四、正文:品名:磺胺喹噁啉钠拼音:Huang’an kuielinna英文名:Sulfaquinoxaline Sodium分子式:C14H11N4NaO2S 322.32本品为N-2喹啉基-4-氨基苯磺酰胺的钠盐。
按干燥品计算,含C14H11N4NaO2S不得少于98.0%。
【性状】本品为类白色或淡黄色粉末;无臭。
本品在水中易溶,在乙醇中微溶。
【鉴别】(1)取本品约1g,加水25ml溶解后,加醋酸2ml,即析出黄色沉淀;滤过,沉淀用水洗涤,在105℃干燥1小时,照磺胺喹噁啉项下的鉴别试验,显相同的结果。
①显芳香第一胺类的鉴别反应(附录20页):取供试品约50mg,加稀盐酸1ml,必要时缓缓煮沸使溶解,放冷,加0.1mol/L 亚硝酸钠溶液数滴,滴加碱性β—萘酚试液数滴,视供试品不同,生成由橙黄到猩红色沉淀。
②取上述干燥物,加0.01mol/L氢氧化钠溶液制成每1ml中含5μg的溶液,照紫外-可见分光光度法(附录23页)测定。
在230nm~350nm的波长范围内测定,在252nm的波长处有最大吸收,吸光度约为0.55。
(2)本品的水溶液,显钠盐的鉴别反应(附录20页)。
①取铂丝,用盐酸湿润后,蘸取供试品,在无色火焰中燃烧,火焰即显鲜黄色。
②取供试品的中性溶液,加醋酸氧铀锌试液,即生成黄色沉淀。
【检查】碱度取本品1.0g,加水5ml溶解后,依法测定(附录51页),PH值应为9.5~10.5。
有关物质取本品适量,加水溶解并稀释制成每1ml中含25mg的溶液,作为供试品溶液;精密量取适量,用0.1mol/L氢氧化钠溶液稀释成每1ml中含0.25mg的溶液,作为对照溶液。
照薄层色谱法(附录30页)试验,吸取上述两种溶液各1µl,分别点于同一硅胶G薄层板上,以正丁醇-浓氨(15:3)为展开剂,展开,晾干,喷以0.1%对二甲氨基苯甲醛的盐酸乙醇(1→100)溶液,检视。
磺胺氯吡嗪钠可溶性粉成产工艺规程

制药有限公司磺胺氯吡嗪钠可溶性粉工艺规程颁发单位:GMP办公室工艺规程批准程序目录1、产品概述 (3)2、生产的工艺流程图 (5)3、操作过程及工艺条件 (6)4、工艺过程中所需SOP名称及要求 (9)5、工艺卫生及环境卫生 (9)6、工艺验证及具体要求 (10)7、设备一览表及主要设备生产能力 (10)8、物料平衡及经济技术指标计算 (10)9、技术安全及劳动保护 (11)10、岗位定员 (12)1.产品概述1.1 产品名称:通用名:磺胺氯吡嗪钠可溶性粉商品名:1.2 性状:本品为淡黄色的粉末1.3 规格:30%磺胺氯吡嗪钠30g 口服葡萄糖70g。
1.5 依据:2005版《中国兽药典》一部。
1.6 适应症:磺胺类药。
主用于球虫病。
1.7 有效期:二年1.8 成品贮存方法及注意事项:遮光、密封,在干燥处保存。
1.9 原辅材料、半成品和成品质量标准:磺胺氯吡嗪钠质量标准见磺胺氯吡嗪钠内控质量标准。
口服葡萄糖质量标准见口服葡萄糖内控质量标准。
半成品质量标准见磺胺氯吡嗪钠可溶性粉可溶性粉半成品内控质量标准。
成品内控质量标准见磺胺氯吡嗪钠可溶性粉内控质量标准。
1.10 原辅材料贮存注意事项:磺胺氯吡嗪钠:遮光、密封,在干燥处保存。
口服葡萄糖:密封保存。
1.11 半成品检查方法及岗位控制:a质量控制要点:b 半成品检查方法见磺胺氯吡嗪钠可溶性粉半成品检验操作规程。
1.12包装要求:应符合铝箔袋质量内控标准要求。
1.13用法用量:肉鸡、火鸡混饮每1L水 1g 混饲每1000kg饲料2000g 连用3天兔混饲每1000kg饲料 2000g 连用5-10天羊内服配成 10%水溶液每1kg体重 1.2ml 连用3-5天1.15 批准文号:2.生产的工艺流程图注:加粗部分为主要控制点3.操作过程及工艺条件3.1 生产前准备:3.1.1 上一批次是否进行清场。
清场者、检查者是否签字,将“清场合格证”副件归入本批生产记录。
磺胺喹恶啉钠原料检验操作规程
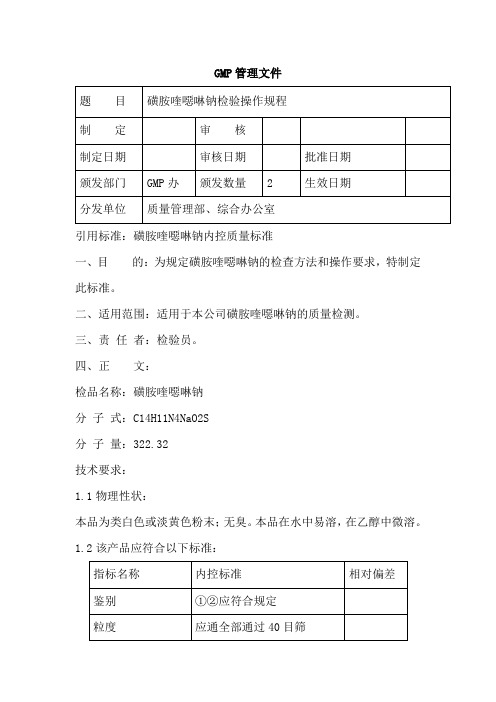
GMP管理文件引用标准:磺胺喹噁啉钠内控质量标准一、目的:为规定磺胺喹噁啉钠的检查方法和操作要求,特制定此标准。
二、适用范围:适用于本公司磺胺喹噁啉钠的质量检测。
三、责任者:检验员。
四、正文:检品名称:磺胺喹噁啉钠分子式:C14H11N4NaO2S分子量:322.32技术要求:1.1物理性状:本品为类白色或淡黄色粉末;无臭。
本品在水中易溶,在乙醇中微溶。
1.2该产品应符合以下标准:2.鉴别2.1仪器与用具:电热干燥箱2.2试剂与溶液:醋酸2.3操作方法2.3.1取本品约1g,加水25ml溶解后,加醋酸2ml,即产生黄色沉淀;过滤,沉淀用水洗涤,在105℃干燥1小时,照磺胺喹噁啉项下的鉴别(335 页)试验,显相同的结果。
2.3.2本品的水溶液,显钠盐的鉴别反应。
3.检查3.1仪器与用具:电热干燥箱、PH计、硅胶G薄层板、层析缸3. 2操作方法粒度取本品约50g,过筛,应能全部通过40目的筛眼。
碱度取本品1.0g,加水5ml溶解,加水5ml溶解,依《pH值测定标准操作规程》测定测定,PH值应为9.5-10.5.有关物质取本品,加水制成每1ml中含25mg的溶液,做为供试液;精密量取适量,用0.1mol/L氢氧化钠溶液稀释成每1ml中含0.25mg的溶液,作为对照溶液。
照薄层色谱法试验,吸取上述三种溶液各1ul,分别点于同一硅胶G薄层板上,以正丁醇-浓氨(15:3)为展开剂,展开后,晾干,喷以0.1%对二甲氨基苯甲醛的盐酸-乙醇(1:100)溶液,检视。
供试品溶液如显杂质斑点,不得多于1个,与对照溶液的主斑点比较,不得更深。
干燥失重取本品,依《干燥失重测定标准操作规程》在105℃干燥至恒重,减失重量不得过5.0%。
重金属取本品1.0g,依《重金属检查标准操作规程》法检查,含重金属不得过百万分之二十。
4含量测定4.1仪器与用具:分析天平、永停滴定仪4. 2试剂与溶液亚硝酸钠滴定液(0.1 mol/L):见亚硝酸钠滴定液 (0.1mol/L)的配制与标定操作规程、稀硫酸4.3操作方法含量测定: 取本品适量(约相当于磺胺喹噁啉钠0.5g),精密称定,加水20ml,溴化钾5g,溶解后,加甘油15ml,硫酸(1→2)20ml,照永停滴定法,用亚硝酸钠滴定液 (0.1mol/L)滴定,即得。
【兽药名称】通用名:硫酸粘菌素可溶性粉

1.治疗输卵管炎;痢菌净15%、二甲硝眯唑5%、无水葡萄糖80%。
2.鸭病抗病毒:金刚烷胺15%、地米混合粉2%、硫酸粘杆菌素5%、无水葡萄糖78%3.治疗小肠球虫:磺胺喹恶啉钠30%、VK3、2%、无水葡萄糖68%。
4.治疗鸭浆膜炎:头孢拉定10%、舒巴坦钠1%、痢菌净5%、地米混合粉1.5%、无水葡萄糖82.5%。
5.治疗呼吸道:硫酸新霉素15%、酒石酸泰乐菌素15%、乳酸TMP3%、痢菌净2%、无水葡萄糖65%。
6.治疗大肠杆菌:异烟井10%、痢菌净15%、硫酸新霉素20%、地米混合粉1.5%、无水葡萄糖53.5% 7.治疗大肠杆菌。
肠炎混合:硫酸新霉素10%、盐酸溴已新1%、地米混合粉1%、盐酸左旋眯唑2%、痢菌净5%、盐酸二丙嗪粉0.5%、无水葡萄糖80.5%8.治疗呼吸道:异烟井10%、病毒灵20%、盐酸溴已新1.3%、甘草浸粉5%、冰片0.1%、地米混合粉1%、盐酸二丙嗪粉1%、无水葡萄糖61.6%9.治疗法氏囊:乳酸环丙沙星2%、金刚烷胺6%、病毒灵20%、地米混合粉1%、牛黄0.4%、无水葡萄糖70.6%10.治疗爆发球虫:磺胺二甲嘧啶钠20%、、VK3、1%、二甲硝眯唑10%、二甲氧苄啶5%、无水葡萄糖64%11.抗病毒:金刚烷胺10%、痢菌净10%、异烟井8%、地米混合粉1%、无水葡萄糖76%12.黄芪多糖:牛黄酸10%、金刚烷胺10%、地米混合粉1.5%、甘草浸粉10%、无水葡萄糖68.5%。
13.抗应激、解暑:无水硫酸钠5%、甘草浸粉10%、氯化钠10%、氯化钾10%、薄荷油0.5%、无水葡萄糖64.5%14.治疗肠毒终合症:痢菌净15%、二甲硝眯唑8%、地米混合粉1%、无水葡萄糖76%15.保肝通肾:氯化钠30%、氯化钾15%、小苏打45%、甘草浸粉10%16.维生素:Va、0.03%、Vc、0.8%、VK3、0.1%、Ve、0.1%、复合b、0.8%、柠檬黄0.2%、17。
磺胺喹恶啉59-40-5

2.2 GHS 标记要素,包括预防性的陈述
2.3 其它危害物
-无
3 成分/组成信息
3.1 物质
分子式 - C14H12N4O2S 分子量 - 300.34
4 急救措施
4.1 必要的急救措施描述
一般的建议 请教医生。出示此安全技术说明书给到现场的医生看。 如果吸入 用水冲洗眼睛作为预防措施。 在皮肤接触的情况下 用肥皂和大量的水冲洗。请教医生。 在眼睛接触的情况下 无数据资料 如果误服 用水雾,耐醇泡沫,干粉或二氧化碳灭火。
https://
Powered by TCPDF ()
4/4
化学品安全技术说明书
10 稳定性和反应活性
10.1 反应性
无数据资料
10.2 化学稳定能性)
无数据资料
10.4 避免接触的条件
无数据资料
10.5 不兼容的材料
吸入可能有害。可能引起呼吸道刺激。
10.6 危险的分解产物
误吞对人体有害。
11 毒理学资料
11.1 毒理学影响的信息
9 理化特性
9.1 基本的理化特性的信息
a) 外观与性状
形状 : 无数据资料
颜色 : 无数据资料
b) 气味
无数据资料
c) 气味临界值
无数据资料
d) pH值
无数据资料
e) 熔点/凝固点
无数据资料
f) 起始沸点和沸程
无数据资料
g) 闪点
无数据资料
h) 蒸发速率
无数据资料
i) 可燃性(固体,气体) 无数据资料
6.1 人员的预防,防护设备和紧急处理程序
收集、处理泄漏物,不要产生灰尘。扫掉和铲掉。存放进适当的闭口容器中待处理。
药场配方

杆康安普霉素可溶性粉硫酸安普霉素 5g粘杆菌素 4g乳酸TMP 2g小苏打 6g糖加至100g新普素硫酸新霉素可溶性粉硫酸新霉素 10g磺胺嘧啶钠 15g小苏打 20g地芬诺脂 0.04g兑水量200公斤糖加至100g肠立清乳酸诺氟水星可溶性粉痢菌净 15g水杨酸钠 8g无水硫酸钠 36g糖加至100g兑水量为150公斤杆菌清乳酸环丙沙星可溶性粉头孢噻肟钠6g痢菌净 12g环丙沙星 5g元明粉10g葡萄糖加至100g卵复康阿莫西林可溶性粉阿莫西林 5g维生素a 4g金刚烷胺 2g小苏打 20g葡萄糖加至100g血虫安磺胺喹恶啉钠磺胺喹恶啉钠 15g甲硝唑 15g安络血 0.6g磷酸氯喹 2g乳酸TMP 4g小苏打 20g糖加至 100g呼泰泰乐菌素可溶性粉酒石酸泰乐菌素 5 克盐酸呋吗唑酮 8 克地塞咪松磷酸钠 20 毫克葡萄糖 10 克碳酸氢钠加至 100 克黄芪合剂黄芪多糖 10g左旋咪唑 2g扑热息痛 20g糖加至100g雏健ABC 氧氟沙星可溶性粉氧氟沙星 4g粘杆菌素 2g无水硫酸钠 20g糖加至 100g磺胺氯吡嗪钠可溶性粉磺胺氯吡嗪钠 15g水溶红霉素 3g磷酸氯喹 4g甲硝唑 10g碳酸钠 10g糖至 100g恩诺沙星可溶性粉恩诺沙星 2g碳酸钠 5g丁胺卡那 2.4g无水糖至 100g兑水 150kg用于白痢、伤寒、大杆。
甲磺酸培氟水星可溶性粉甲磺酸培氟 5g金刚烷胺 4g扑热息疼 15g糖至 100g用于产蛋下降。
氟苯尼考粉氟苯尼考及助剂 2.5g多西环素 5gTMP 2g无水硫酸钠 20g粘杆 2.5g麻黄碱 1g安乃近 5g糖至 100g盐酸氨丙啉、乙氧酰胺苯甲酯预混剂盐酸氨丙林 5g氯苯胍 5g轻质碳酸钙至 100g盐酸大观霉素、盐酸林可霉素可溶性粉盐酸林可霉素 10g丁胺卡那霉素 5g无水硫酸钠 10g糖至 100g。
停药期规定1

停药期规定停药期规定附件1:停药期规定兽药名称执行标准停药期1乙酰甲喹片兽药规范92版牛、猪35日2二氢吡啶部颁标准牛、肉鸡7日,弃奶期7日3二硝托胺预混剂兽药典2000版鸡3日,产蛋期禁用4土霉素片兽药典2000版牛、羊、猪7日,禽5日,弃蛋期2日,弃奶期3日5土霉素注射液部颁标准牛、羊、猪28日,弃奶期7日6马杜霉素预混剂部颁标准鸡5日,产蛋期禁用7双甲脒溶液兽药典2000版牛、羊21日,猪8日,弃奶期48小时,禁用于产奶羊8巴胺磷溶液部颁标准羊14日9水杨酸钠注射液兽药规范65版牛0日,弃奶期48小时10四环素片兽药典90版牛12日、猪10日、鸡4日,产蛋期禁用,产奶期禁用11甲砜霉素片部颁标准28日,弃奶期7日12甲砜霉素散部颁标准28日,弃奶期7日,鱼500度日13甲基前列腺素F2a注射液部颁标准牛1日,猪1日,羊1日14甲硝唑片兽药典2000版牛28日15甲磺酸达氟沙星注射液部颁标准猪25日16甲磺酸达氟沙星粉部颁标准鸡5日,产蛋鸡禁用17甲磺酸达氟沙星溶液部颁标准鸡5日,产蛋鸡禁用18甲磺酸培氟沙星可溶性粉部颁标准28日,产蛋鸡禁用19甲磺酸培氟沙星注射液部颁标准28日,产蛋鸡禁用20甲磺酸培氟沙星颗粒部颁标准28日,产蛋鸡禁用21亚硒酸钠维生素E注射液兽药典2000版牛、羊、猪28日22亚硒酸钠维生素E预混剂兽药典2000版牛、羊、猪28日23亚硫酸氢钠甲萘醌注射液兽药典2000版0日24伊维菌素注射液兽药典2000版牛、羊35日,猪28日,泌乳期禁用25吉他霉素片兽药典2000版猪、鸡7日,产蛋期禁用26吉他霉素预混剂部颁标准猪、鸡7日,产蛋期禁用27地西泮注射液兽药典2000版28日28地克珠利预混剂部颁标准鸡5日,产蛋期禁用29地克珠利溶液部颁标准鸡5日,产蛋期禁用30地美硝唑预混剂兽药典2000版猪、鸡28日,产蛋期禁用31地塞米松磷酸钠注射液兽药典2000版牛、羊、猪21日,弃奶期3日32安乃近片兽药典2000版牛、羊、猪28日,弃奶期7日33安乃近注射液兽药典2000版牛、羊、猪28日,弃奶期7日34安钠咖注射液兽药典2000版牛、羊、猪28日,弃奶期7日35那西肽预混剂部颁标准鸡7日,产蛋期禁用36吡喹酮片兽药典2000版28日,弃奶期7日37芬苯哒唑片兽药典2000版牛、羊21日,猪3日,弃奶期7日38芬苯哒唑粉(苯硫苯咪唑粉剂)兽药典2000版牛、羊14日,猪3日,弃奶期5日39苄星邻氯青霉素注射液部颁标准牛28日,产犊后4天禁用,泌乳期禁用40阿司匹林片兽药典2000版0日41阿苯达唑片兽药典2000版牛14日,羊4日,猪7日,禽4日,弃奶期60小时42阿莫西林可溶性粉部颁标准鸡7日,产蛋鸡禁用43阿维菌素片部颁标准羊35日,猪28日,泌乳期禁用44阿维菌素注射液部颁标准羊35日,猪28日,泌乳期禁用45阿维菌素粉部颁标准羊35日,猪28日,泌乳期禁用46阿维菌素胶囊部颁标准羊35日,猪28日,泌乳期禁用47阿维菌素透皮溶液部颁标准牛、猪42日,泌乳期禁用48乳酸环丙沙星可溶性粉部颁标准禽8日,产蛋鸡禁用49乳酸环丙沙星注射液部颁标准牛14日,猪10日,禽28日,弃奶期84小时50乳酸诺氟沙星可溶性粉部颁标准禽8日,产蛋鸡禁用51注射用三氮脒兽药典2000版28日,弃奶期7日52注射用苄星青霉素(注射用苄星青霉素G)兽药规范78版牛、羊4日,猪5日,弃奶期3日53注射用乳糖酸红霉素兽药典2000版牛14日,羊3日,猪7日,弃奶期3日54注射用苯巴比妥钠兽药典2000版28日,弃奶期7日55注射用苯唑西林钠兽药典2000版牛、羊14日,猪5日,弃奶期3日56注射用青霉素钠兽药典2000版0日,弃奶期3日57注射用青霉素钾兽药典2000版0日,弃奶期3日58注射用氨苄青霉素钠兽药典2000版牛6日,猪15日,弃奶期48小时59注射用盐酸土霉素兽药典2000版牛、羊、猪8日,弃奶期48小时60注射用盐酸四环素兽药典2000版牛、羊、猪8日,弃奶期48小时61注射用酒石酸泰乐菌素部颁标准牛28日,猪21日,弃奶期96小时62注射用喹嘧胺兽药典2000版28日,弃奶期7日63注射用氯唑西林钠兽药典2000版牛10日,弃奶期2日64注射用硫酸双氢链霉素兽药典90版牛、羊、猪18日,弃奶期72小时65注射用硫酸卡那霉素兽药典2000版28日,弃奶期7日66注射用硫酸链霉素兽药典2000版牛、羊、猪18日,弃奶期72小时67环丙氨嗪预混剂(1%)部颁标准鸡3日68苯丙酸诺龙注射液兽药典2000版28日,弃奶期7日69苯甲酸雌二醇注射液兽药典2000版28日,弃奶期7日70复方水杨酸钠注射液兽药规范78版28日,弃奶期7日71复方甲苯咪唑粉部颁标准鳗150度日72复方阿莫西林粉部颁标准鸡7日,产蛋期禁用73复方氨苄西林片部颁标准鸡7日,产蛋期禁用74复方氨苄西林粉部颁标准鸡7日,产蛋期禁用75复方氨基比林注射液兽药典2000版28日,弃奶期7日76复方磺胺对甲氧嘧啶片兽药典2000版28日,弃奶期7日77复方磺胺对甲氧嘧啶钠注射液兽药典2000版28日,弃奶期7日78复方磺胺甲噁唑片兽药典2000版28日,弃奶期7日79复方磺胺氯哒嗪钠粉部颁标准猪4日,鸡2日,产蛋期禁用80复方磺胺嘧啶钠注射液兽药典2000版牛、羊12日,猪20日,弃奶期48小时81枸橼酸乙胺嗪片兽药典2000版28日,弃奶期7日82枸橼酸哌嗪片兽药典2000版牛、羊28日,猪21日,禽14日83氟苯尼考注射液部颁标准猪14日,鸡28日,鱼375度日84氟苯尼考粉部颁标准猪20日,鸡5日,鱼375度日85氟苯尼考溶液部颁标准鸡5日,产蛋期禁用86氟胺氰菊酯条部颁标准流蜜期禁用87氢化可的松注射液兽药典2000版0日88氢溴酸东茛菪碱注射液兽药典2000版28日,弃奶期7日89洛克沙胂预混剂部颁标准5日,产蛋期禁用90恩诺沙星片兽药典2000版鸡8日,产蛋鸡禁用91恩诺沙星可溶性粉部颁标准鸡8日,产蛋鸡禁用92恩诺沙星注射液兽药典2000版牛、羊14日,猪10日,兔14日93恩诺沙星溶液兽药典2000版禽8日,产蛋鸡禁用94氧阿苯达唑片部颁标准羊4日95氧氟沙星片58部颁标准28日,产蛋鸡禁用96氧氟沙星可溶性粉部颁标准28日,产蛋鸡禁用97氧氟沙星注射液部颁标准28日,弃奶期7日,产蛋鸡禁用98氧氟沙星溶液(碱性)部颁标准28日,产蛋鸡禁用99氧氟沙星溶液(酸性)部颁标准28日,产蛋鸡禁用100氨苯胂酸预混剂部颁标准5日,产蛋鸡禁用101氨茶碱注射液兽药典2000版28日,弃奶期7日102海南霉素钠预混剂部颁标准鸡7日,产蛋期禁用103烟酸诺氟沙星可溶性粉部颁标准28日,产蛋鸡禁用104烟酸诺氟沙星注射液部颁标准28日105烟酸诺氟沙星溶液部颁标准28日,产蛋鸡禁用106盐酸二氟沙星片部颁标准鸡1日107盐酸二氟沙星注射液部颁标准猪45日108盐酸二氟沙星粉部颁标准鸡1日109盐酸二氟沙星溶液部颁标准鸡1日110盐酸大观霉素可溶性粉兽药典2000版鸡5日,产蛋期禁用111盐酸左旋咪唑兽药典2000版牛2日,羊3日,猪3日,禽28日,泌乳期禁用112盐酸左旋咪唑注射液兽药典2000版牛14日,羊28日,猪28日,泌乳期禁用113盐酸多西环素片兽药典2000版28日114盐酸异丙嗪片兽药典2000版28日115盐酸异丙嗪注射液兽药典2000版28日,弃奶期7日116盐酸沙拉沙星可溶性粉部颁标准鸡0日,产蛋期禁用117盐酸沙拉沙星注射液部颁标准猪0日,鸡0日,产蛋期禁用118盐酸沙拉沙星溶液部颁标准鸡0日,产蛋期禁用119盐酸沙拉沙星片部颁标准鸡0日,产蛋期禁用120盐酸林可霉素片兽药典2000版猪6日121盐酸林可霉素注射液兽药典2000版猪2日122盐酸环丙沙星、盐酸小檗碱预混剂部颁标准500度日123盐酸环丙沙星可溶性粉部颁标准28日,产蛋鸡禁用124盐酸环丙沙星注射液部颁标准28日,产蛋鸡禁用125盐酸苯海拉明液射液兽药典2000版28日,弃奶期7日126盐酸洛美沙星片部颁标准28日,弃奶期7日,产蛋鸡禁用127盐酸洛美沙星可溶性粉部颁标准28日,产蛋鸡禁用128盐酸洛美沙星注射液部颁标准28日,弃奶期7日129盐酸氨丙啉、乙氧酰胺苯甲酯、磺胺喹恶啉预混剂兽药典2000版鸡10日,产蛋鸡禁用130盐酸氨丙啉、乙氧酰胺苯甲酯预混剂兽药典2000版鸡3日,产蛋期禁用131盐酸氯丙嗪片兽药典2000版28日,弃奶期7日132盐酸氯丙嗪注射液兽药典2000版28日,弃奶期7日133盐酸氯苯胍片兽药典2000版鸡5日,兔7日,产蛋期禁用134盐酸氯苯胍预混剂兽药典2000版鸡5日,兔7日,产蛋期禁用135盐酸氯胺酮注射液兽药典2000版28日,弃奶期7日136盐酸赛拉唑注射液兽药典2000版28日,弃奶期7日137盐酸赛拉嗪注射液兽药典2000版牛、羊14日,鹿15日138盐霉素钠预混剂兽药典2000版鸡5日,产蛋期禁用139诺氟沙星、盐酸小檗碱预混剂部颁标准500度日140酒石酸吉他霉素可溶性粉兽药典2000版鸡7日,产蛋期禁用141酒石酸泰乐菌素可溶性粉兽药典2000版鸡1日,产蛋期禁用142维生素B12注射液兽药典2000版0日143维生素B1片兽药典2000版0日144维生素B1注射液兽药典2000版0日145维生素B2片兽药典2000版0日146维生素B2注射液兽药典2000版0日147维生素B6片兽药典2000版0日148维生素B6注射液兽药典2000版0日149维生素C片兽药典2000版0日150维生素C注射液兽药典2000版0日151维生素C磷酸酯镁、盐酸环丙沙星预混剂部颁标准500度日152维生素D3注射液兽药典2000版28日,弃奶期7日153维生素E注射液兽药典2000版牛、羊、猪28日154维生素K1注射液兽药典2000版0日155喹乙醇预混剂兽药典2000版猪35日,禁用于禽、鱼、35kg以上的猪156奥芬达唑片(苯亚砜哒唑)兽药典2000版牛、羊、猪7日,产奶期禁用157普鲁卡因青霉素注射液兽药典2000版牛10日,羊9日,猪7日,弃奶期48小时158氯羟吡啶预混剂兽药典2000版鸡5日,兔5日,产蛋期禁用159氯氰碘柳胺钠注射液部颁标准28日,弃奶期28日160氯硝柳胺片兽药典2000版牛、羊28日161氰戊菊酯溶液部颁标准28日162硝氯酚片兽药典2000版28日163硝碘酚腈注射液(克虫清)部颁标准羊30日,弃奶期5日164硫氰酸红霉素可溶性粉兽药典2000版鸡3日,产蛋期禁用165硫酸卡那霉素注射液(单硫酸盐)兽药典2000版28日166硫酸安普霉素可溶性粉部颁标准猪21日,鸡7日,产蛋期禁用167硫酸安普霉素预混剂部颁标准猪21日168硫酸庆大—小诺霉素注射液部颁标准猪、鸡40日169硫酸庆大霉素注射液兽药典2000版猪40日170硫酸粘菌素可溶性粉部颁标准7日,产蛋期禁用171硫酸粘菌素预混剂部颁标准7日,产蛋期禁用172硫酸新霉素可溶性粉兽药典2000版鸡5日,火鸡14日,产蛋期禁用173越霉素A预混剂部颁标准猪15日,鸡3日,产蛋期禁用174碘硝酚注射液部颁标准羊90日,弃奶期90日175碘醚柳胺混悬液兽药典2000版牛、羊60日,泌乳期禁用176精制马拉硫磷溶液部颁标准28日177精制敌百虫片兽药规范92版28日178蝇毒磷溶液部颁标准28日179醋酸地塞米松片兽药典2000版马、牛0日180醋酸泼尼松片兽药典2000版0日181醋酸氟孕酮阴道海绵部颁标准羊30日,泌乳期禁用182醋酸氢化可的松注射液兽药典2000版0日183磺胺二甲嘧啶片兽药典2000版牛10日,猪15日,禽10日184磺胺二甲嘧啶钠注射液兽药典2000版28日185磺胺对甲氧嘧啶,二甲氧苄氨嘧啶片兽药规范92版28日186磺胺对甲氧嘧啶、二甲氧苄氨嘧啶预混剂兽药典90版28日,产蛋期禁用187磺胺对甲氧嘧啶片兽药典2000版28日188磺胺甲噁唑片兽药典2000版28日189磺胺间甲氧嘧啶片兽药典2000版28日190磺胺间甲氧嘧啶钠注射液兽药典2000版28日191磺胺脒片兽药典2000版28日192磺胺喹噁啉、二甲氧苄氨嘧啶预混剂兽药典2000版鸡10日,产蛋期禁用193磺胺喹噁啉钠可溶性粉兽药典2000版鸡10日,产蛋期禁用194磺胺氯吡嗪钠可溶性粉部颁标准火鸡4日、肉鸡1日,产蛋期禁用195磺胺嘧啶片兽药典2000版牛28日196磺胺嘧啶钠注射液兽药典2000版牛10日,羊18日,猪10日,弃奶期3日197磺胺噻唑片兽药典2000版28日198磺胺噻唑钠注射液兽药典2000版28日199磷酸左旋咪唑片兽药典90版牛2日,羊3日,猪3日,禽28日,泌乳期禁用200磷酸左旋咪唑注射液兽药典90版牛14日,羊28日,猪28日,泌乳期禁用201磷酸哌嗪片(驱蛔灵片)兽药典2000版牛、羊28日、猪21日,禽14日202磷酸泰乐菌素预混剂部颁标准鸡、猪5日不需要制订停药期的兽药品种附件2:不需要制订停药期的兽药品种兽药名称标准来源1乙酰胺注射液兽药典2000版2二甲硅油兽药典2000版3二巯丙磺钠注射液兽药典2000版4三氯异氰脲酸粉部颁标准5大黄碳酸氢钠片兽药规范92版6山梨醇注射液兽药典2000版7马来酸麦角新碱注射液兽药典2000版8马来酸氯苯那敏片兽药典2000版9马来酸氯苯那敏注射液兽药典2000版10双氢氯噻嗪片兽药规范78版11月苄三甲氯铵溶液部颁标准12止血敏注射液兽药规范78版13水杨酸软膏兽药规范65版14丙酸睾酮注射液兽药典2000版15右旋糖酐铁钴液射液(铁钴针注射液)兽药规范78版16右旋糖酐40氯化钠注射液兽药典2000版17右旋糖酐40葡萄糖注射液兽药典2000版18右旋糖酐70氯化钠注射液兽药典2000版19叶酸片兽药典2000版20四环素醋酸可的松眼膏兽药规范78版21对乙酰氨基酚片兽药典2000版22对乙酰氨基酚注射液兽药典2000版23尼可刹米注射液兽药典2000版24甘露醇注射液兽药典2000版25甲基硫酸新斯的明注射液兽药规范65版26亚硝酸钠注射液兽药典2000版28安络血注射液兽药规范92版29次硝酸铋(碱式硝酸铋)兽药典2000版30次碳酸铋(碱式碳酸铋)兽药典2000版31呋塞米片兽药典2000版32呋塞米注射液兽药典2000版33辛氨乙甘酸溶液部颁标准34乳酸钠注射液兽药典2000版35注射用异戊巴比妥钠兽药典2000版36注射用血促性素兽药规范92版37注射用抗血促性素血清部颁标准38注射用垂体促黄体素兽药规范78版39注射用促黄体素释放激素A2部颁标准40注射用促黄体素释放激素A3部颁标准41注射用绒促性素兽药典2000版42注射用硫代硫酸钠兽药规范65版43注射用解磷定兽药规范65版44苯扎溴铵溶液兽药典2000版45青蒿琥酯片部颁标准46鱼石脂软膏兽药规范78版47复方氯化钠注射液兽药典2000版48复方氯胺酮注射液部颁标准49复方磺胺噻唑软膏兽药规范78版50复合维生素B注射液兽药规范78版51宫炎清溶液部颁标准52枸橼酸钠注射液兽药规范92版53毒毛花苷K注射液兽药典2000版54氢氯噻嗪片兽药典2000版55洋地黄毒甙注射液兽药规范78版56浓氯化钠注射液兽药典2000版57重酒石酸去甲肾上腺素注射液兽药典2000版58烟酰胺片兽药典2000版59烟酰胺注射液兽药典2000版60烟酸片兽药典2000版61盐酸大观霉素、盐酸林可霉素可溶性粉兽药典2000版62盐酸利多卡因注射液兽药典2000版63盐酸肾上腺素注射液兽药规范78版64盐酸甜菜碱预混剂部颁标准65盐酸麻黄碱注射液兽药规范78版66萘普生注射液兽药典2000版67酚磺乙胺注射液兽药典2000版68黄体酮注射液兽药典2000版69氯化胆碱溶液部颁标准70氯化钙注射液兽药典2000版71氯化钙葡萄糖注射液兽药典2000版72氯化氨甲酰甲胆碱注射液兽药典2000版73氯化钾注射液兽药典2000版74氯化琥珀胆碱注射液兽药典2000版75氯甲酚溶液部颁标准76硫代硫酸钠注射液兽药典2000版77硫酸新霉素软膏兽药规范78版78硫酸镁注射液兽药典2000版79葡萄糖酸钙注射液兽药典2000版80溴化钙注射液兽药规范78版81碘化钾片兽药典2000版82碱式碳酸铋片兽药典2000版83碳酸氢钠片兽药典2000版84碳酸氢钠注射液兽药典2000版85醋酸泼尼松眼膏兽药典2000版86醋酸氟轻松软膏兽药典2000版87硼葡萄糖酸钙注射液部颁标准88输血用枸橼酸钠注射液兽药规范78版89硝酸士的宁注射液兽药典2000版90醋酸可的松注射液兽药典2000版91碘解磷定注射液兽药典2000版92中药及中药成份制剂、维生素类、微量元素类、兽用消毒剂、生物制品类等五类产品(产品质量标准中有除外)。
磺胺氯吡嗪钠可溶性粉

磺胺氯吡嗪钠可溶性粉Huang′anLvbiqinna KerongxingfenSulfachoropyrazin Sodium Soluble Powder本品为磺胺氯吡嗪钠与乳糖或无水葡萄糖等适宜基质配制而成。
含磺胺氯吡嗪钠(C10H8CIN4NaO2S·H2O)应为标示量的90.0%~110.0%。
【性状】本品为淡黄色粉末。
【鉴别】(1)取本品,加甲醇制成每1ml中含磺胺氯吡嗪钠1mg的溶液,作为供试品溶液;另取磺胺氯吡嗪钠对照品,加甲醇制成每1ml中含磺胺氯吡嗪钠1mg的溶液,作为对照品溶液。
吸取上述两种溶液各2ul,照有关物质项下的方法试验,供试品溶液所显主斑点的颜色和位置应与对照品溶液的主斑点相同。
(2)取本品适量(约相当于磺胺氯吡嗪钠50mg),加稀盐酸2ml使溶解,显芳香第一胺类的鉴别反应。
【检查】溶解性取本品15g,加水l00ml,搅拌后应全部溶解。
粒度取本品,用500um孔径筛检查,500μm孔径筛通过率应不少于90%。
有关物质取本品,加甲醇溶解制成每lml中含磺胺氯吡嗪钠10mg的溶液,超声,取上清液,作为供试品溶液;精密量取供试品溶液适量,加甲醇制成每lml中含磺胺氯吡嗪钠0.3mg的溶液,作为对照品溶液。
照薄层色谱法(附录30页)试验,吸取上述两种溶液各2μl,分别点于同一硅胶G薄层板上,用甲苯-醋酸乙醋-甲醇〔3:1:1)为展开剂,展开,晾干。
将薄层板置于充满亚硝酸气体(用亚硝酸钠2g,加盐酸5ml产生)的密闭容器中,5分钟后取出,室温下放置3~5分钟,喷以0.1%盐酸萘乙二胺溶液,供试品溶液如显杂质斑点,其颜色与对照品溶液的主斑点比较,不得更深。
水分取本品,照水分测定法(附录69页,第一法A)测定,含水分不得过2.5%。
其他应符合可溶性粉剂项下有关的各项规定。
【含量测定】取本品(约相当于磺胺氯吡嗪钠0.5g),精密称定,加水25ml 使溶解,加二甲替甲酰胺15ml,缓缓加入氢溴酸溶液(1→2)40ml,照永停滴定法(附录52页),用亚硝酸钠液(0.lmol/L)滴定。
磺胺喹恶啉钠可溶性粉(成品)检验操作规程
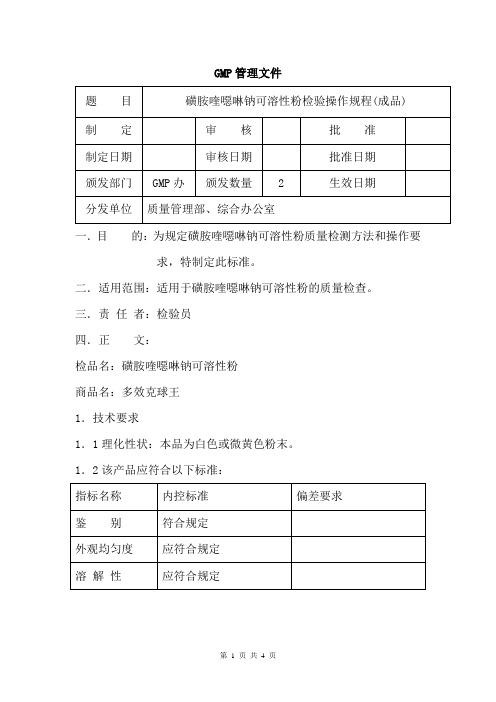
GMP管理文件一.目的:为规定磺胺喹噁啉钠可溶性粉质量检测方法和操作要求,特制定此标准。
二.适用范围:适用于磺胺喹噁啉钠可溶性粉的质量检查。
三.责任者:检验员四.正文:检品名:磺胺喹噁啉钠可溶性粉商品名:多效克球王1.技术要求1.1理化性状:本品为白色或微黄色粉末。
1.2该产品应符合以下标准:2.实验方法2.1鉴别:2.1.1试剂与溶液氢氧化钠溶液(0.01mol/L)2.1.2仪器与设备分光光度计2.1.3鉴别方法2.1.3.1取本品约1g,加水25ml溶解后,加醋酸2ml,即产生黄色沉淀;过滤,沉淀用水洗涤,在105℃干燥,照磺胺喹噁啉项下鉴别1、2项,试验,显相同的结果。
2.1.3.2本品的水溶液,显钠盐的鉴别反应。
2.2检查:2.2.1外观均匀度:取本品适量,平铺于光滑纸上,成5cm2,将表面压平,在亮的背景下观察,呈均匀色泽,无花纹与色斑。
2.2.2溶解性:取本品0.1g,,置纳氏比色管中,加水50ml,上下翻转10次,应全部溶解。
静置30分钟,无浑浊与沉淀产生。
2.2.3干燥失重:2.2.3.1仪器与用具:恒温干燥箱:温度在 105±2℃干燥扁形称量瓶:玻璃,带盖2.2.3.2测定方法:用干燥至恒重的称量瓶称取试样1g,准确至0.0002g,放入105±2℃的干燥箱中,打开称量瓶盖,干燥4小时。
盖好盖,放入干燥器中,冷却至室温,称量。
2.2.3.3结果的计算干燥失重百分含量=(m1-m2)/(m1-m)×100%式中:m1—样品与称量瓶干燥前重量m2—样品与称量瓶干燥后重量m—称量瓶干燥后重量2.2.4装量:2.2.4.1仪器与用具:干燥器:用氯化钙或硅胶作为干燥剂2.2.4.2测定方法取样品3个,清洗干净并在干燥器中干燥,称重,准确至0.1g。
除去内容物,将外包装清洗干净,干燥,称重,求出每个的装量及平均装量。
2.3含量测定;2.3.1仪器与设备:永停滴定仪、天平2. 3. 2试剂与溶液:亚硝酸钠滴定液见亚硝酸钠滴定液的配制与操作规程(0.1mol/L) 2.3.3测定方法取本品适量(约相当于磺胺喹噁啉钠0.5g),精密称定,加水20ml,溴化钾5g,溶解后,加甘油15ml,硫酸(1→2)20ml,照永停滴定法,用亚硝酸钠滴定液(0.1 mol/L)滴定,即得。
盐酸氨丙啉磺胺喹恶啉钠可溶性粉

盐酸氨丙啉磺胺喹噁啉钠可溶性粉Yansuan Anbinglin Huang'an Kuielinna Kerongxingfen Amprolium Hydrochloride and Sulfaquioxaline Sodium Soluble Powder 本品为盐酸氨丙啉、磺胺喹吴噁啉钠与葡萄糖配制而成。
含盐酸氨丙啉(C14H19ClN4·HCl)、磺胺喹噁啉钠(C14H11N4NaO2S)均应为标示量的90.0%~110.0%。
【性状】本品为淡黄色粉末。
【鉴别】在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
【检查】干燥失重取本品,在105℃干燥至恒重,减失重量不得过10.0%(附录69页)其他应符合可溶性粉项下有关的各项规定(附录16页)。
【含量测定】照高效液相色谱法测定。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂,以乙腈-0.02mol/L磷酸二氢钾溶液-三乙胺(40:60:0.5)(磷酸调节pH至3.0±0.1)为流动相,检测波长260nm。
理论板数按磺胺喹噁啉峰计算应不低于2000,盐酸氨丙啉和磺胺喹噁啉钠峰的分离度应符合要求。
测定法取本品约0.8g,精密称定,置100ml量瓶中,加乙腈50ml,振摇15分钟,加水15ml 和0.1mol/L氢氧化钠溶液4ml,超声5分钟,放置至室温,加水至刻度,摇匀,滤过,精密量取续滤液2ml,置50ml量瓶中,用流动相稀释至刻度,摇匀,精密量取20ul注入液相色谱仪,记录色谱,另取盐酸氨丙啉对照品60mg、磺胺喹噁啉对照品36mg,置100ml量瓶中,加水15ml和氢氧化钠溶液4ml,振摇使溶解,加水至刻度,摇匀。
精密量取2ml,置50ml量瓶中,用流动相稀释至刻度,摇匀,同法测定。
按外标法以峰面积计算,磺胺喹噁啉钠结果与1.073相乘,即得。
【作用与用途】抗原虫药。
磺胺喹恶啉钠可溶性粉内控质量标准

GMP管理文件
一.目的:制定磺胺喹噁啉钠可溶性粉内控质量标准(成品),规范公司磺胺喹噁啉钠可溶性粉的生产。
二.适用范围:适用于磺胺喹噁啉钠可溶性粉生产和质检。
三.责任者:生产部经理、质管部经理、检验员
四.正文:
【名称】磺胺喹噁啉钠可溶性粉
【质量指标】本品为磺胺喹啉钠与适宜的辅料制成。
含磺胺喹噁(C14H11N4NaO2S)
应为标示量的93.0%--107.0%。
性状本品为白色至微黄色粉末。
鉴别1、取本品约1g,加水25ml溶解后,加醋酸2ml,即析出黄色沉淀;滤过,沉淀用水洗涤,在105℃干燥1小时,照磺胺喹噁啉项下的鉴别1、3项试验,显相同的结果。
2、本品的水溶液显钠盐的鉴别反应。
检查干燥失重取本品,在105℃干燥4小时,减失重量不得过8.0%。
其它应符可溶性粉剂项下有关的各项规定。
装量每袋装量不少于标示量的标示量平均装量不少于标示量含量规定取本品适量(约相当于磺胺喹噁啉纳0.5g),精密称定,加水20ml
与溴化钾5g,溶解后,加甘油15ml,硫酸溶液(1→2)20ml,照永停滴定法,
用亚硝酸钠滴定液(0.1mol/L)滴定。
每1ml亚硝酸钠滴定液(0.1mol/L)相当
于32.23mg的C14H11N4NaO2S 。
【规格】 100g:10g
【贮藏】遮光,密闭保存。
【有效期】2年。
磺胺醋酰钠药物的合成工艺研究

磺胺醋酰钠药物的合成工艺研究(一)已有的合成路线或相关合成路线1.2.改进后磺胺醋酰钠合成工艺.. 反应中保持pH 12~ 13, 必要时需补加碱液。
滴加醋酐的方法对反应影响较大, 慢滴快加搅拌是操作的关键, 有两种方法有利于磺胺醋酰的生成, 一是将交替滴加醋酐的时间由原来每次5 m in 延长至10 m in左右( 9~ 13 m in) , 或将原来交替滴加醋酐5 次(每次2m l)改为交替滴加4次(每次2. 5m l), 并保持每次滴加醋酐的时间为10 m in。
将反应温度提高到60~ 65 .. , 或延长反应时间至40~ 60 m in, 均可提高磺胺醋酰的产率。
3.将以上所得的磺胺醋酰投入50ml烧杯中,滴加少量水润湿(<0.5ml)(附注1)。
于水浴上加热至90 ℃,滴加40%氢氧化钠至恰好溶解,溶液pH为7~8,趁热抽滤,滤液转至小烧杯中放冷析出结晶(附注2),抽滤,干燥,得磺胺醋酰钠9g。
(二)确定合成路线及步骤1、磺胺醋酰的制备在装有搅拌棒及温度计的100 mL三颈瓶中,加入磺胺17.2 g,22.5%氢氧化钠22 mL,开动搅拌,于水浴上加热至50℃左右。
待磺胺溶解后,滴加醋酐3.6 mL,77% 氢氧化钠2.5 mL(首先,加入醋酐3.6 mL,77% 氢氧化钠2.5 mL;随后,每次间隔5 min,将剩余的77% 氢氧化钠和醋酐分5次交替加入,每次2 ml)。
加料期间反应温度维持在50~55℃及pH12~13;加料完毕继续保持此温度反应30 min。
反应完毕,停止搅拌,将反应液倾入100mL烧杯中,加水20 mL 稀释。
用36% 盐酸调至pH 7,于冰水浴中放置30 min,并不时搅拌析出固体,抽滤固体,用适量冰水洗涤。
洗液与滤液合并后用浓盐酸调至pH 4~5,抽滤,得白色粉末。
用3倍量(3 mL / g)10% 盐酸溶解得到的白色粉末,放置30min,不时搅拌,尽量使单乙酰物成盐酸盐溶解,抽滤除不溶物。
磺胺土法合成实验报告(3篇)

第1篇一、实验目的1. 了解磺胺药物的合成原理和工艺流程。
2. 掌握土法合成磺胺的实验操作步骤。
3. 学习对实验数据进行记录和分析。
二、实验原理磺胺药物是一种广泛应用于临床的抗感染药物,其合成原理主要是通过磺酰化反应制备磺胺类药物。
本实验采用土法合成磺胺,即利用实验室现有设备和材料,通过一系列化学反应制备磺胺。
三、实验材料与仪器1. 实验材料:- 硫磺(S)- 碳酸氢钠(NaHCO3)- 硫酸(H2SO4)- 氨水(NH3·H2O)- 碳酸钠(Na2CO3)- 氢氧化钠(NaOH)- 硫酸钠(Na2SO4)- 碳酸钾(K2CO3)- 氯化钠(NaCl)- 乙醇(C2H5OH)- 碘化钾(KI)- 硫酸铜(CuSO4·5H2O)- 氯化铁(FeCl3)- 硝酸银(AgNO3)- 氢氧化铵(NH4OH)- 氢氧化钠溶液(NaOH溶液)- 水浴锅- 烧杯- 烧瓶- 玻璃棒- 滤纸- 滤斗- 移液管- 滴定管- 精密天平- pH计- 显微镜2. 实验仪器:四、实验步骤1. 硫磺磺酰化:- 将一定量的硫磺加入烧杯中,加入适量的硫酸,搅拌均匀,加热至60-70℃。
- 在搅拌下,缓慢滴加氨水,直至溶液呈中性(pH=7)。
- 继续加热反应30分钟,冷却后过滤,得到磺酰化产物。
2. 碳酸氢钠反应:- 将磺酰化产物加入烧瓶中,加入适量的碳酸氢钠,搅拌均匀。
- 加热反应30分钟,冷却后过滤,得到碳酸氢钠反应产物。
3. 氢氧化钠反应:- 将碳酸氢钠反应产物加入烧瓶中,加入适量的氢氧化钠溶液,搅拌均匀。
- 加热反应30分钟,冷却后过滤,得到氢氧化钠反应产物。
4. 硫酸钠反应:- 将氢氧化钠反应产物加入烧瓶中,加入适量的硫酸钠,搅拌均匀。
- 加热反应30分钟,冷却后过滤,得到硫酸钠反应产物。
5. 碳酸钾反应:- 将硫酸钠反应产物加入烧瓶中,加入适量的碳酸钾,搅拌均匀。
- 加热反应30分钟,冷却后过滤,得到碳酸钾反应产物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
磺胺喹噁啉钠可溶性粉生产工艺规程
1 产品概述
1.1 产品名称
商品名
通用名:磺胺喹噁啉钠可溶性粉
汉语拼音:Huangankuiwulinna Kerongxingfen
1.2 剂型:可溶性粉剂
1.3 批准文号:
1.4 规格:100g:10g
1.5 包装:100g×80袋
1.6 贮存:遮光,密闭保存
1.7 有效期:两年
2 处方和依据
2.1 处方
名称用量
磺胺喹噁啉钠10g
无水葡萄糖90g
共制成100g 2.2 处方依据:本处方依据《中华人民共和国兽药典》2015年版一部磺胺喹噁啉钠可溶性粉项下制订。
3 生产工艺流程图
4 操作过程及工艺条件
4.1干燥粉碎过筛
4.1.1 如磺胺喹噁啉钠和无水葡萄糖原料不能通过五号筛,应进行粉碎过筛;
4.1.2如水分超标应进行干燥,温度控制在70℃--80℃。
4.1.3车间质量监控员按规定对粉碎间进行检查,符合要求后允许生产。
4.1.4粉碎过筛后的药粉装入洁净容器中,容器外挂物料状态卡,注明名称、规格、批号、数量、日期、操作者和复核人。
4.1.5 操作人员填写粉碎过筛批记录,清场结束后将本岗位记录交于车间质量监控员。
4.2称量配料
4.2.1车间质量监控员按规定对称量配料间进行检查,符合要求后允许生产。
磺胺喹噁啉钠和无水葡萄糖使用前应再次检查外观情况,确保质量合格。
称量前操作人员应先核对原料的名称、批号、数量等。
确认无误后,进行称量配料。
处方计算和称量过程必须由双人操作,一人称量、一人复核,并由质量监控员监督。
操作过程中,操作人员应及时称量记录,并将记录随物料传入混合工序。
4.2.2 称好的物料置于清洁干燥的周转容器内,容器外应挂物料状态卡,注明物料名称、批号、数量、日期、称量人和复核人。
4.3 混合
4.3.1车间质量监控员按规定对混合间进行检查,符合要求后允许生产。
混合前操作人员应先核对物料的名称、批号、数量等,确认无误后进行下一步操作。
4.3.2检查各准备工作无误后,按配方依次将原料与辅料以等量递增法倒入V型混合机开始混合,预混10分钟后,将全部辅料投入V型混合机中,开始总混,再混合20分钟。
4.3.3经过最后一次混合具有均一性的物料为一个批量,编为一个批号。
4.3.4混合好的物料装入洁净的容器内,容器外应挂物料状态卡,写明品名、规格、批号、数量、日期、操作者和复核人,传入中间站。
4.3.5混合岗位班长填写请验单,交于中间产品化验员,中间产品化验员检验合格后,中间产品化验员将检验报告书交于车间质量监控员。
4.3.6操作人员填写混合批记录,并将中间产品检验报告书归入批生产记录中。
清场结束后将本岗位记录交于车间质量监控员。
4.4 包装
4.4.1车间质量监控员按规定对包装间进行检查,符合要求后允许生产。
操作人员根据批包装指令领取包装铝塑复合袋、包装箱等包装物品。
包装用的标签与大箱箱签应打印批号、生产日期、有效期,且印字清晰。
4.4.2核对该中间产品的品名、批号、数量、规格等,按包装岗位标准操作规程进行操作,控制装量范围为100~102g。
4.4.3分装时,包装岗位班长应间隔30分钟检查一次装量,每次检查数量为5袋。
每袋装量不少于100g,平均装量不少于100g。
不得出现少装、漏装、多装,封
装要整齐。
分装时操作人员要及时填写分装批记录。
清场结束后将本岗位记录交于车间质量监控员。
4.4.4装箱过程中,将袋按一致方向摆放整齐,并保持垫板清洁完整,车间质量监控员应随时抽检药品包装情况。
4.4.5 取样:装箱结束后,包装小组组长填写请验单交于中心化验室,取样员按成品取样操作规程的规定取样,包装岗位人员填写产品寄库单,将成品搬运至仓库待验区待验。
化验室检验合格后,包装岗位人员再办理入库手续。
4.4.6 有零头产品,要求合箱的,要保证每箱的零头产品不多于2个批号。
每个批号均应在外箱与合格证上印注,并填写合箱记录。
4.4.7 包装结束后,要清点、校对包装材料、标签,剩余的、报废的按包材、标签的按照相关的管理规定处理,并做好记录。
4.5 入库
4.5.1 物料管理员收到质量部出具的合格成品检验报告书和车间填写的成品入库单后验收成品。
4.5.2 仓库物料管理员目测外观包装是否符合要求。
查看品名、规格、批号、数量、生产日期等是否与报告书相符。
4.5.3 同意入库的合格成品填写入库成品总账,放置于合格品区。
4.5.4 成品应遵循物料贮存管理规程,按品种、规格、批号、分类码放,不准混堆混放,以防止发货时产生错发事件。
4.5.5 成品的储藏条件应保证密闭、防潮、干燥。
5 原辅料、包装材料、中间产品、成品的质量标准
5.1 原辅料质量标准
5.1.1 磺胺喹噁啉钠质量标准:ZL-YLNB-007-00
5.1.2 无水葡萄糖质量标准:ZL-FLNB-001-00
5.2 包装材料质量标准
5.2.1 铝塑复合袋质量标准; :ZL-BCNB-001-00
5.2.2内包装标签质量标准:ZL-BCNB-003-00
5.2.3外包装标签质量标准:ZL-BCNB-004-00
5.2.4 包装箱质量标准:ZL-BCNB-005-00
5.3 中间产品、成品质量标准
5.3.1 磺胺喹噁啉钠可溶性粉中间产品质量标准: ZL-ZCZB-001-00
5.3.2 磺胺喹噁啉钠可溶性粉成品质量标准:ZL-CPNB-001-00
8 原辅料、包装材料消耗定额
10 安全生产及劳动防护
10.1 安全生产
10.1.1 严格按照工艺规程规定进行生产,熟练掌握标准操作规程的每个操作要领,不得任意更改。
10.1.2 生产设备在使用前应先检查,必要时作空机试验,正常后再进行生产,生产结束后,要把设备清洁干净,摩擦部件要按规定加油拆洗。
10.1.3 各生产车间要设有安全小组,车间及仓库应配备消防器材及泡沫灭火器。
操作室严禁烟火。
生产人员上岗前必须能熟练使用车间配备的消防器材。
对易燃物要随领随用,如有剩余应及时入库。
10.1.4 电器的设备要定期检查,电线开关不得裸露,管道破损时要及时修理或更换,不得受潮,不得用湿手去碰电器开关。
10.1.5 机器旋转部位应有防护罩。
禁止用铁锤或类似工具敲打包装机、管道等。
10.1.6 新工人上岗操作前,必须经过培训,并有上岗证。
10.1.7 发生安全事故后,要立即报告有关领导,事后写出详细的事故报告。
10.2 劳动保护
10.2.1 要严格按照GMP的要求,定时开动空调机,使车间内湿度、温度等环境
条件符合规定。
10.2.2 粉碎高尘工序应安装吸尘装置以降尘。
10.2.3 岗位操作人员每年体检一次。
10.2.4 按不同工种,及时发放劳动保护用品。
10.2.5 按不同工种,每半年进行一次劳动安全教育。
10.2.6 企业的安全生产组织每月对生产车间的安全生产检查一次,每年考核班组的情况一次。
