EBV与细胞永生化
EBV_对宿主免疫的调控作用研究进展

生物技术进展 2023 年 第 13 卷 第 5 期 681 ~ 689Current Biotechnology ISSN 2095‑2341进展评述ReviewsEBV 对宿主免疫的调控作用研究进展张旭娟 , 赵鹏翔* , 刘子怡 , 蔡子松 , 刘梦昱 , 谢飞 , 马雪梅北京工业大学环境与生命学部,北京 100124摘 要:EB 病毒(epstein -barr virus ,EBV )在人群中的感染率高达90%,其能够通过对宿主的免疫调控作用在人体内建立长期感染。
众多肿瘤的发生及发展与EBV 对宿主免疫的调控密切相关,但目前关于EBV 的免疫调控作用机制尚未完全阐明。
EBV 在不同的感染状态下均发展出了一系列对宿主的免疫调控策略,即主要通过靶向Toll 样受体(Toll like receptors , TLRs)信号通路,利用或限制部分免疫效应以促进长期感染的建立和逃避宿主免疫监控,从而维持EBV 基因组的稳定存在。
概述了EBV 在潜伏期和裂解期与宿主之间的相互作用,探讨了EBV 逃避宿主免疫的策略,旨在为病毒感染防治和病毒相关肿瘤的治疗提供基础理论依据及研究思路。
关键词:EB 病毒;Toll 样受体;免疫调控;核因子κB DOI :10.19586/j.2095‑2341.2023.0048中图分类号:Q939.91, R373 文献标志码:AResearch Progress on the Immune Regulation of EBV on the HostZHANG Xujuan , ZHAO Pengxiang * , LIU Ziyi , CAI Zisong , LIU Mengyu , XIE Fei , MA XuemeiFaculty of Environment and Life , Beijing University of Technology , Beijing 100124, ChinaAbstract :As a virus with a human infection rate of up to 90%, EBV can establish long -term infection in the human body through the immune regulation of the host. The occurrence and development of many tumors are closely related to the regulation of host immunity by EBV , but the mechanism of immune regulation by EBV has not been fully elucidated. EBV has developed a series of strategies for host immune regulation in different infection states , mainly by targeting Toll like receptors (TLRs ) signaling pathways , using or limiting part of their immune effects to promote the establishment of long -term infection and evade host immune surveillance to maintain the stability of the EBV genome. This article reviewed the immunoregulatory mechanism of EBV , a double -stranded DNA herpesvirus , in order to provide basic theoretical basis and research ideas for the prevention and treatment of virus infection and virus -associated tumors.Key words :epstein -barr virus ; Toll like receptors ; immune regulation ; NF -κBEBV 又名人类γ疱疹病毒Ⅳ型(human gammaherpesvirus Ⅳ),在全球范围内的感染率超过90%[1]。
如何构建永生化细胞?

研究背景正常组织来源的细胞在体外培养条件下可分裂生长,但经过有限次数的传代后,就会停止增殖,发生衰老和死亡,这种现象称之为海弗利克极限。
有的细胞自发或受外界因素的影响,可以从增殖衰老危机中逃离,从而拥有无限增殖的能力,该过程称之为细胞永生化。
然而自发永生化的几率非常小,啮齿类动物为10-5-10-6,而人类细胞则更为罕见,小于10-12。
通过转染技术将外源性永生化基因导入目的细胞或诱导衰老相关基因突变,可以增加永生化的发生率,从而建立稳定的永生化细胞株。
研究意义永生化细胞能够提供稳定均一、性状一致的细胞来源,并且可以降低材料成本,因此,它是体外研究细胞增殖、分化、凋亡、衰老等的理想模型,加之,永生化细胞和肿瘤细胞关系密切,所以永生化细胞也是研究肿瘤发生机制的重要模型。
另外,由于永生化细胞具有可以多次传代的特性,可以利用各种细胞永生化的方法使那些传代困难、增殖缓慢、容易衰老的细胞获得永生,从而为研究人员提供更多的细胞资源。
研究方法目前,人们已建立了多种细胞永生化的方法,包括:1病毒基因转染很多病毒感染能够诱导细胞永生化,例如EB病毒(epstein-barr virus, EBV)、猿猴病毒40 (simian virus40, SV40)和人乳头瘤病毒(human papillomavirus, HPV)。
这些病毒感染其天然宿主细胞,能诱导细胞永生化。
EBV能使B淋巴母细胞永生化形成淋巴母细胞样细胞系,它是通过潜伏蛋白激活细胞因子与其受体相互作用的途径使细胞永生的。
EBV永生化B细胞的一个最显著的特点是端粒酶活性的提高,这可能是导致B细胞永生的主要原因。
目前,EB 病毒介导的细胞永生化应用最多的是B淋巴细胞,其他细胞中的应用很少。
SV40是简单的真核细胞病毒,SV40的T抗原片段是最常用的目的片段,将其整合入靶细胞核内并表达,可导致细胞增殖活力的改变并表现出多种与肿瘤相关的转化显型。
应用的方法包括:野生型SV40病毒共培养感染靶细胞、磷酸钙法、电穿孔以及逆转录病毒载体法等。
EB病毒检测技术进展及临床应用

EBV实验室检测方法
嗜异凝集抗体试验:也称“Monospot”试验。在EBV还未 确定为IM的病因之前,1932年引入临床实践诊断IM。 当时发现IM患者的血清或血浆可以凝集马或绵羊的红细胞。 该抗体在病程第1~2周出现,持续约6个月。 在青少年原发性EBV感染中其阳性率可达80%-90%,约10% 的青少年缺乏对嗜异性抗体的阳性反应。
1975年Horwitz首次描述一些持续性IM患者血清存在高滴 度的抗EBV-VCA和EA抗体
1982年Tobi进一步描述并证实该病 1984年被称为慢性单核细胞增多样综合征 1986年被定义为慢性症状性EBV感染 1991年被称为慢性活动性EBV感染
CAEBV
发生于儿童或年轻成年人 该病表现为慢性或反复的单核细胞增多样症:发热、肝脾
概述
➢ 传播途径:EBV感染主要通过唾液接触传播,也可通过 血液传播;
➢ 人感染EBV后建立终身潜伏感染,人群感染率超过90%。 ➢ 1-6岁儿童、14-20岁青少年及年轻成年人高度易感,发
展中国家EBV感染多发生在儿童早期。
病原学
疱疹病毒科,γ疱疹病毒亚科,淋 巴隐病毒属,人疱疹病毒4型
球形双链DNA病毒,基因组平均 大小约为172 kb
EBV病毒核酸检测
➢ 实时荧光定量PCR是目前最主要的监测EBV载 量的方法
➢ 鉴别EBV健康携带者的低水平复制与EBV相关 疾病患者高水平活动性感染。
EBV病毒核酸检测
EBV载量检测有多种方法,Real-time PCR是 目前最主要的监测EBV载量的方法,有较强的敏 感性和特异性。不同的EBV疾病进行Real-time PCR检测时,需要的标本不同。
EB病毒检测技术及临床应用
肿瘤的发生与发展

肿瘤的发生与发展肿瘤的定义:肿瘤是机体在各种致瘤因素作用下,局部组织的细胞在基因水平上失去对其生长的正常调控,导致克隆性异常增生而形成的新生物,常表现为局部肿块.过程:局部组织的细胞—基因突变—细胞异常增生—新生物—局部肿块发病机制:肿瘤的发病是一个多因素、多步骤参与的过程.恶性肿瘤的病因〔尚未完全了解〕,1.环境因素:化学,物理,生物因素2.机体因素化学致癌化学致癌物:目前认为凡接触引起人或动物形成肿瘤的化学物质,称为化学致癌物〔chemical carcinogen〕.目前发现对动物有致癌作用的化学物质已达2000余种,其中有些可能和人类肿瘤的形成有关分类:1.作用分式:直接致癌物,间接致癌物,促癌物2.与肿瘤的关系:肯定致癌物,可疑致癌物,潜在致癌物⏹ 1.直接致癌物:进入机体后与细胞直接作用,诱导细胞癌变的化学物质.⏹ 2.间接致癌物:进入体内经微粒体氧化酶活化,变成具有致癌作用的化学物质⏹ 3.促癌物:能促进其他致癌物诱发肿瘤形成的化学物质⏹ 4.肯定致癌物〔defined carcinogen〕经流行病学调查确定,临床医师和科学工作者都承认对人和动物有致癌作用,其致癌作用具有剂量反应关系的化学致癌物.⏹ 5.可疑致癌物〔suspected carcinogen〕具有体外转化能力,而且接触时间和发病率相关,动物致癌实验阳性,结果不恒定,且缺乏流行病学方面的证据.⏹ 6.潜在致癌物〔potential carcinogen〕是在动物实验中可获得某些阳性结果,但在人群##无资料证明对人具有致癌性的物质.1、化学致癌物的作用点:为细胞的癌基因和抑癌基因2、作用:使癌基因激活,抑癌基因失活.1、累积作用:<summation effect>是指两种或多种致癌物同时或相继作用于机体,其复合效应等于单独作用之和2、协同作用:<synergistiic effect>机体同时暴露于几种致癌物中其致癌作用高于个单独致癌物作用之和常见的化学致癌物:多环芳香烃类,芳香胺与偶氮染料,亚硝胺类化学致癌例子.苯胺染料:膀胱癌,烟草:肺癌,黄曲霉素:肝癌物理致癌1.电离辐射是最主要的物理性致癌因素2.放射性同位素:镭、铀、氡等放射性同位素3.紫外线:皮肤癌,着色性干皮病病毒致癌1/3为DNA病毒,2/3为RNA病毒⏹一、乳头状瘤病毒与宫颈癌〔HPV〕⏹二、乙型肝炎病毒与肝癌〔HBV〕⏹三、EB病毒与鼻咽癌和Burkit肉瘤〔EBV〕⏹四、HTLV与人类T细胞白血病〔HTLV〕致瘤性DNA病毒1、共同特征:〔1〕致癌作用发生在病毒进入细胞后复制的早期阶段,瘤基因整合在宿主DNA上.〔2〕在宿主DNA上的定位具有选择性.〔3〕病毒DNA编码的蛋白质调节细胞周期、与抑癌基因相互作用.感染致瘤性DNA病毒后宿主细胞的分类:(1)允许性细胞:DNA病毒感染宿主细胞后它能够复制并最终导致细胞的死亡. (2)非允许性细胞:指当病毒感染与其无关的种属细胞时,病毒复制的效率很低,甚至不能复制.致瘤性RNA病毒分类.根据病毒形态:A,B,C,D型根据基因组是否完整:缺陷型,非缺陷型致瘤病毒致瘤分子机制:1、病毒编码产物模拟细胞内分子信号2、病毒编码产物激活细胞信号传导途径3、病毒编码产物对细胞周期的干预调节肿瘤发病的分子基础:细胞在基因水平上失去对其生长的正常调控恶性肿瘤发病的分子过程:获得性DNA损伤因素〔化学物质、电离辐射、病毒〕—细胞DNA损伤—体细胞基因异常—促生长癌基因激活,调控细胞凋亡基因异常,肿瘤抑制基因失活—正常调控蛋白丧失,异常基因蛋白表达—恶性肿瘤形成原癌基因:是细胞中固有的基因,正常下参与细胞增殖与分化的调控,当基因的功能、结构发生变异,并具有使细胞发生恶性转化的作用的时候,称为癌基因原癌基因的活化1.点突变:H-Ras基因第12位密码子:GGC 变为GTC检测方法:限制性内切酶长度多态性<RFLP>、单链构象多态性<SSCP>、寡核苷酸探针杂交和PCR直接测序等技术.2.基因扩增3.染色体易位,基因重排4.癌基因甲基化改变:某些癌基因<H-ras、c-Myc>低甲基化和抑癌基因<Rb、p16>的高甲基化改变是细胞癌变的一个重要特征抑癌基因:正常细胞内有一类对细胞增殖起负调节作用的基因,能抑制细胞生长,其功能丧失则可促进细胞恶性转化.Rb基因:最早发现的肿瘤抑制基因P53基因:研究得最多的抑癌基因,功能是调节细胞周期和DNA损伤所致的凋亡细胞周期与肿瘤癌基因、抑癌基因突变—细胞周期失控—失控性生长〔以增殖过多、凋亡过少为主要形式〕—肿瘤细胞凋亡与肿瘤细胞凋亡调控机制失常—凋亡受阻,增殖加强—肿瘤凋亡:又称之程序性细胞死亡,是细胞死亡的一种方式,是生理性调节过程,受多种因素调控凋亡的特征性形态学改变:核固缩、核碎裂、DNA断裂等,但细胞器完整,周围无炎症反应凋亡调节基因:调节细胞进入程序性死亡的基因与其产物称为凋亡调节基因bcl-2蛋白抑制细胞凋亡,bax蛋白则促进细胞凋亡DNA修复基因:即对DNA损伤有修复作用的基因,基因通过修复原癌基因、肿瘤抑制基因、凋亡调控相关基因的非致死性损伤,间接影响细胞增殖与存活.端粒:真核细胞染色体末端的DNA重复序列和特异结合蛋白的复合体,能维持染色体的稳定性和完整性,在细胞增殖和分化中发挥作用.细胞有丝分裂时,染色体末端的端粒丢失,随细胞分裂次数增加,端粒逐步缩短,当缩短至某一长度时,失去了染色体免受重组和降解的保护,细胞停止分裂,导致细胞衰老和死亡.端粒酶:细胞核内RNA和蛋白质复合体,激活的端粒酶能以自身的RNA为模板,合成端粒DNA重复序列,使其连接于染色体端粒末端,稳定端粒长度,维持细胞的无限增殖能力.恶性肿瘤细胞端粒酶活性增高.机体免疫与肿瘤肿瘤免疫逃逸机制:肿瘤细胞的抗原缺失和抗原调变,肿瘤细胞的漏逸--肿瘤细胞迅速生长,超越了机体抗肿瘤免疫效应的发生,致使宿主不能有效地清除大量的肿瘤细胞恶性肿瘤的特点:分裂快,永生化,无限增殖,侵袭,转移肿瘤的生长1.生长速度:取决于分化程度,良性慢,恶性快2.生长方式:a.膨胀性生长:大多数良性肿瘤的生长方式B.外生性生长:与部位有关,良、恶性肿瘤皆可呈外生性生长,但恶性肿瘤会外生加浸润,可形成溃疡.C.浸润性生长:大多数恶性肿瘤的生长方式细胞永生化:是指体外培养的细胞经过自发的或受外界因素的影响从增殖衰老危机中逃离, 从而具有无限增殖能力的过程.了解细胞永生化的意义:了解细胞增殖与衰老分子机制与保存一些重要疑难病例的样本.为我们提供更多的细胞资源.为治疗肿瘤、控制肿瘤细胞的增殖以与器官移植的研究奠定了坚实的基础.肿瘤的扩散:恶性肿瘤的重要特征之一1.直接蔓延:随着肿瘤不断长大,瘤细胞可连续不断地沿着组织间隙、淋巴管、血管或神经束衣侵入并破坏临近正常组织或器官继续生长,称直接蔓延2.转移:是指恶性肿瘤细胞从原发部位侵入淋巴管、血管或体腔,迁徙到他处继续生长,形成与原发肿瘤同类型的继发性肿瘤,这个过程称为转移.方式:血道转移,淋巴道转移,种植性转移淋巴道转移是癌最常见的转移途径,血道转移是肉瘤最常见的转移途径肿瘤转移的基本过程早期原发癌生长:在原发肿瘤生长早期,肿瘤细胞生长所需的养料是通过临近组织器官微环境渗透提供,这足以使微小原发肿瘤生长和扩展.肿瘤血管形成:当肿瘤直径达到或超过1—2mm时,经微环境渗透提供的营养物质已不能保证肿瘤细胞的生长.此时,向肿瘤提供养料的血管逐步形成.这种由宿主组织血循环形成的毛细血管网最终进入肿瘤组织,整个形成过程是在各种血管形成因子和相应的抑制因子相互作用共同调控进行的.肿瘤细胞脱落并侵入基质:部分肿瘤细胞能分泌一种物质,使黏附因子的表达受到抑制,从而增加肿瘤细胞运动能力,使其从原发肿瘤病灶上脱离形成游离细胞.这些脱落细胞通过分泌各种蛋白溶解酶,可以破坏细胞外基质,从而导致肿瘤细胞突破结缔组织构成的屏障.进入脉管系统:肿瘤诱导形成的毛细血管网不仅与原发肿瘤生长有关,而且也为侵入基质的游离肿瘤细胞进入循环系统提供了基本条件.癌栓形成:进入血循环的肿瘤细胞再运送过程中大多数都被杀死破坏,只有极少数转移倾向极高的细胞相互聚集形成微小癌栓并在循环系统中存活下来.继发组织器官定位生长:在循环中幸存的癌细胞到达特定的继发组织或器官时,通过黏附作用特异性地锚定在毛细血管壁上,并穿透管壁逸出血管进入周围组织.转移癌继续扩散:当转移灶直径超过1—2mm时,新生毛细血管形成并与肿瘤连通.肿瘤细胞通过上述相同机制,可以形成新的转移癌灶.肿瘤的转移的器官选择性肿瘤转移的倾向性:从乳腺、肺、肾—到骨从前列腺、宫颈癌—到骨盆、腰椎从甲状腺—到颈椎从乳腺、胃肠道—到区域淋巴结从胃肠道、胰腺—到肝和腹腔转移从乳腺—到肝、肺、骨、肾上腺从胃—到卵巢从小细胞肺癌、肺腺癌—到脑、骨、肾上腺从颅内肿瘤—到很少转移颅外肿瘤转移的分子生物学基础1.粘附分子与肿瘤转移:肿瘤侵袭的第一步肿瘤细胞从原发肿瘤脱落游离,本质是肿瘤细胞间黏附因子的损失所致2.血管生成和肿瘤转移:肿瘤本身能诱导血管的形成,肿瘤细胞可释放血管生成因子刺激血管内皮细胞的生长和移行.肿瘤血管生成的调节:血管内皮基质膜溶解,内皮细胞向肿瘤组织迁移,内皮细胞在迁移前沿增殖,内皮细胞管道化,分支形成血管环,形成新的基底膜3.纤维蛋白溶解酶与其调节因子:纤维蛋白溶解酶激活因子〔PA〕在肿瘤转移过程中如肿瘤血管形成、肿瘤细胞脱落、基质浸润、侵入和逸出循环系统、继发脏器移行和环境改造等重要步骤中起重要的正调节作用.PAI起负调节作用.肿瘤细胞从发生到转移需要具备的条件:生长增殖,转移潜能,免疫脱逸参与控制转移的免疫细胞主要有:NK细胞巨噬细胞T细胞阻止肿瘤转移存在的问题和发展方向一肿瘤转移的基因治疗二血管形成抑制剂与抗肿瘤转移三细胞黏附因子抑制剂与抗肿瘤转移四基质金属蛋白酶抑制剂与抗肿瘤转移干细胞和肿瘤干细胞干细胞:来源于胚胎和成体的细胞,在一定条件下具有自我更新和分化潜能,具有分化形成至少一种特定细胞类型的特性.<1>胚胎干细胞:指胚胎早期的干细胞.这类干细胞分化潜能宽,具有分化为机体任何组织细胞的能力.如囊胚期内细胞团的细胞.<2>成体干细胞:指成体各组织器官中的干细胞,成体干细胞具有自我更新能力,但分化潜能窄,只能分化为相应<或相邻>组织器官组成的细胞.如神经干细胞,表皮干细胞.干细胞类型:全能干细胞,多能干细胞,专能干细胞1.全能性干细胞<胚胎干细胞>:具有形成完整个体的分化潜能.2.多能干细胞:具有分化出多种细胞组织的潜能,但失去了发育成完整个体的能力. 3.专能性干细胞<成体干细胞>:这类干细胞只能向一种类型或密切相关的两种类型的细胞分化.研究干细胞的科学意义1.细胞治疗.干细胞可恢复因重大疾病而损害的细胞,这是干细胞潜在的最大优势.由于丧失正常细胞功能的疾病都可以通过移植由胚胎干细胞分化来的特异组织细胞来治疗.2.基因治疗.即通过胚胎干细胞和基因工程技术,矫正缺陷基因.因干细胞能自我复制更新,是基因治疗的理想靶细胞.将治疗基因整合到干细胞,再将干细胞移植入人体中,能够持久地发挥作用肿瘤干细胞:在肿瘤中的一小部分具有无限增值能力,并形成肿瘤能力的细胞,也称癌干细胞,肿瘤干细胞在肿瘤组织中所占的比例很少肿瘤干细胞的特点:自我更新性,高致瘤性,分化潜能,耐药性针对肿瘤干细胞进行治疗:1.抑制肿瘤干细胞信号通路和相关酶的活性,削弱增殖能力.2.诱导肿瘤干细胞分化,消耗其分裂潜能,达到抑制肿瘤发展的目的.3. 破坏为肿瘤干细胞提供养分和保护的微环境,抑制增殖和成瘤的能力.4.用靶向性病毒载体携带促凋亡基因诱导肿瘤干细胞进入凋亡程序,达到清除目的.5.抑制抗性相关蛋白的表达,增加对放疗和化疗的敏感性,提高放化疗的有效率.。
12.23儿童EB病毒感染相关性疾病

内容
Epstein-Barr病毒(EBV)简介
• EB病毒是嗜淋巴细胞的双链DNA病毒,属于疱 疹病毒科,又称人类疱疹病毒4型
• 编码约100个基因,其中编码壳抗原(VCA)、早期 抗原(EA)、核抗原(EBNA)的基因尤为重要
• 人类是EBV唯一的宿主,感染EBV后建立终身潜 伏感染,人群感染率超过90%
hypersensitivity to mosquito bites
CAEBV的诊断标准(2)
• 血清抗体滴度异常升高
• 抗VCA-IgG≥1:640和抗EA-IgG≥1:160 • 抗VCA-IgA和/或抗EA-IgA常呈阳性
• 受累组织和外周血检测到EBV-DNA、RNA、有 关抗原和克隆
• PCR:外周血PBMC中EBV-DNA定量 >102.5copies/µg
EB病毒表达的抗原
• EBV潜伏感染期,选择性表达早期抗原(EA)以及:
• 核抗原(EBNA-1,-2,-LP,-3A,-3B,-3C):
• 为DNA结合蛋白,在感染的B细胞核内 • EBNA-1与感染有关,EBNA-2与细胞转化和永生化有关 • EBNA抗体出现在感染晚期
• 潜伏膜蛋白(LMP-1,-2A,-2B):
• 淋巴瘤/白血病
• Burkitt’s淋巴瘤 • Hodgkin淋巴瘤
• 上皮细胞癌
• 鼻咽癌 • 胃腺癌 • 唾液腺癌 • 口腔毛发粘膜白斑病
• 肉瘤
• 平滑肌肉瘤
EBV感染的规范性诊断
• 传染性单核细胞增多症:治疗 • EBV原发感染:可能需要治疗
* 症状性:治疗 * 无症状性:不需要治疗 • EBV既往感染:不需要治疗 • EBV感染再激活/再感染:可能需要治疗 * 症状性:治疗 * 无症状性:不需要治疗
EB病毒感染相关性疾病

【中图分类号】【文献标识码】【文章编号】 ( )·综述·!"病毒感染相关性疾病四川大学华西第二医院儿科(四川成都 )李强综述病毒( )是已知的 个人类疱疹病毒之一。
自 年 首次报道 淋巴瘤及 年 和 在 淋巴瘤标本的体外传代细胞中发现 以来,已有多种疾病被证实与 感染有关,现综述如下。
一、 生物学特点(一) 基因组、感染方式: 是线性双链 病毒,基因组长度 ,编码大约 个基因,其中重要的有编码壳抗原( )、早期抗原( )、核抗原( , )的基因 。
特点为亲淋巴细胞性和亲上皮细胞性,有 种感染方式:复制性感染(细胞溶解性感染)和潜伏感染(持续性感染)。
在复制性感染期间,病毒 转录, 、 充分表达,有成熟病毒颗粒产生并伴有受感染宿主细胞的溶解和死亡,这种感染方式主要见于 感染性疾病如传染性单核细胞增生症( )。
在潜伏感染期间, 、 表达受到抑制,主要表达 、( ),不产生新的病毒颗粒,这种感染方式主要见于 相关性恶性肿瘤性疾病。
(二) 潜伏感染时表达的基因:研究发现,在潜伏感染的 细胞内, 的表达与病毒的复制和细胞的永生化有关。
是 潜伏感染最重要的基因,可诱导 表达并且反式激活 ,在受感染的 细胞转化 永生化过程中起着关键的作用。
潜伏感染时还有 编码的( )表达, 和 是迄今所知在潜伏感染的细胞内表达最为丰富的病毒 ,广泛用于 潜伏感染的诊断,但其功能目前还不清楚。
潜伏感染期间 表达以后, 、 、 表达于受到感染的细胞上。
是一种整合膜蛋白并且是潜在的致癌基因,它可剌激细胞间和细胞内信号传导途径,包括核因子 ! ( ! ),后者是转录因子,控制与细胞增殖和生长调控有关的基因。
体外培养已证实受 潜伏感染的细胞可有 种不同形式的 潜伏感染基因表达,见表 。
不同的潜伏感染类型与不同的临床恶性肿瘤性疾病有关 。
二、 感染的诊断(一)特异的血清学实验测定 相关抗体: 感染后可通过特异的血清学实验测定 相关抗体以证实 感染(见表 )。
EB病毒相关淋巴母细胞样细胞系的建立及鉴定

瘤性 的相关研究提供基 础 。 方 法
表面标记 以及核 型的鉴定 。 结果
利用体外培 养 B 5 细胞产 生 E 9. 8 B病毒原型 株感染正 常人 外周血淋 巴
a di i o Me h d Noma eih r l lo mp o ye r a som e t n vt . n r to s r l r ea o dl p p b y h c tsweet n fr dwi EBV r ttp r d c d r h p oo epo u e y
淋 巴母 细胞 样细胞 系能不断传代 , 能表达 E V基 因 , B 具有成 熟 B细胞
细胞培养传代 得到 5 E 株 B病 毒相关淋 巴母 细胞 , 并用 R -C TP R对 其进行 了基 因表达 、 流式细胞仪 进行细胞
表面 标记 ; 细胞 传 代过 程 早期 未 发 生 核 型改 变 。 结论
LCL — L 2 5、 CL3 5、 — LCL — 0、 4 3 LCL5 3 。 — 0
建 立 了 5 永 生 化 细胞 株 , 别 为 L L1 、 株 分 C — 5
【 关键词] E B病毒 ; 生化 ; 永 转化细胞 系 ; 巴细胞 淋
De eo me t n e t c t no mp o lsodc ll e s o itdwi p t i- r vr s v lp n d i n i a i fl a d i f o y h ba t i eli sa s cae t E sen Ba r i n h u
i mmo tl a in a s c a e t BV e a s fi e ai e y smp e p o e s f r e mo e s me c a a t r fB r i t s o it d wi E az o h b c u eo sr l t l i l r c s , u t r r o h r c e so t v h
EB病毒疾病健康教育问答

EB病毒疾病健康教育问答第一节认识EB病毒一、概念传染性单核细胞增多症(infectiousmononuc1eosis,IM)是由EB病毒感染引起的淋巴细胞增生性的一种急性传染性疾病,主要见于儿童和青少年。
IM患者血清中噬异凝集抗体(Heterophi1eantibody)效价增高,并可检出EBV抗体。
典型临床三联征为发热、咽峡炎和淋巴结肿大、可合并肝脾肿大、外周淋巴细胞及异型淋巴细胞增高。
EB病毒(Epstein-Barrvirus,EBV)为疱疹病毒科嗜淋巴细胞病毒属的成员,被90%以上的成人所携带,它是传染性单核细胞增多症的病原体,是一种普遍存在、主要侵犯人类B淋巴细胞的疱疹病毒群,且与淋巴细胞增殖性疾病如BUrkitt淋巴瘤、鼻咽癌有关。
EBV属疹病毒科丫亚科。
EPStein和Barr于1964年首次成功地将Burkitt非洲儿童淋巴瘤细胞通过体外悬浮培养而建株,并在建株细胞涂片中用电镜观察到疱疹病毒颗粒,EB病毒因此得名。
二、EB病毒的危害EB病毒感染在世界各地均有发生,多呈散发性,也可引起小范围流行。
潜伏期5~15天,起病缓急不一,四季均可发病,晚秋至初春较多。
患者和EB病毒携带者为传染源。
病毒大量存在于唾液腺及唾液中,可持续或间断排毒数周、数月甚至数年。
一次得病后可获较持久的免疫力。
人群对EB病毒普遍易感,EB病毒可长期潜伏在人体淋巴组织中,当机体免疫功能低下及口腔皮肤破损时,潜伏的EB病毒活化形成而复发感染,进入血液导致病毒血症,继而累及全身淋巴系统。
因B淋巴细胞表面有EB病毒受体,EB病毒感染后可使B淋巴细胞表面抗原改变,继而引起T淋巴细胞防御反应,形成细胞毒性T淋巴细胞(CytotoxicT1ymphocyte,CT1)效应,直接破坏被感染的B淋巴细胞。
EB病毒可异位感染T淋巴细胞、上皮细胞及NK细胞等,还可逃避宿主免疫,干扰免疫功能,导致细胞免疫功能紊乱,并可通过诱导细胞增殖,抑制细胞分化及凋亡,诱导细胞永生化和转化等致癌。
EB病毒感染相关性疾病

1. B u r ki t t 淋巴瘤 (BL ) : 地方性 BL 是发生于东部非洲 儿童的地方病 , 临床主要表现为下颌骨肿瘤 , 也形成腹膜后 肿块和侵犯内脏 。患者血清中抗 EBV 抗体 ( EBNA1) 强阳性 , 多数病例肿瘤组织中 EBV 基因组和 EB ER 阳性 , 病理特征 为“星空”现象 , 肿瘤组织可有 3 种特征性染色体异常之一 种 : t ( 8 ∶14) 、t ( 2 ∶8) 、t ( 8 ∶22) 。目前认为 ,第 8 号染色体 上的 c- myc 癌基因易位到第 2 、14 、22 号染色体上邻近 Ig 基 因的部位 , 导致 c- myc 癌基因的活化 , 与本病的发病机制有 关。
EBV的信号转导机制
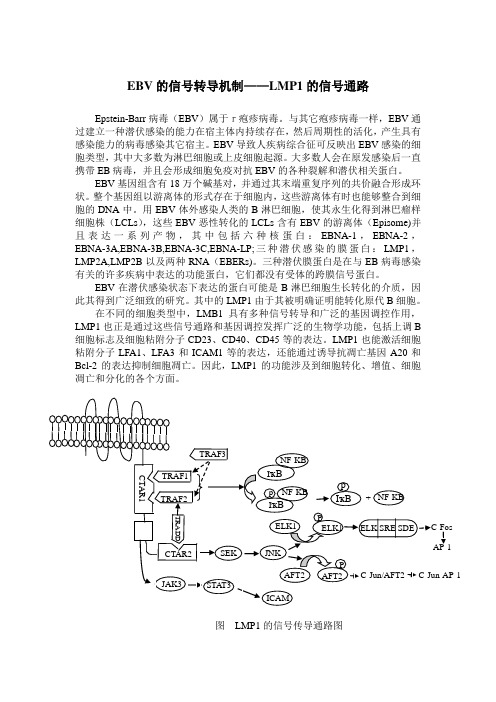
EBV 的信号转导机制——LMP1的信号通路Epstein-Barr 病毒(EBV )属于r疱疹病毒。
与其它疱疹病毒一样,EBV 通过建立一种潜伏感染的能力在宿主体内持续存在,然后周期性的活化,产生具有感染能力的病毒感染其它宿主。
EBV 导致人疾病综合征可反映出EBV 感染的细胞类型,其中大多数为淋巴细胞或上皮细胞起源。
大多数人会在原发感染后一直携带EB 病毒,并且会形成细胞免疫对抗EBV 的各种裂解和潜伏相关蛋白。
EBV 基因组含有18万个碱基对,并通过其末端重复序列的共价融合形成环状。
整个基因组以游离体的形式存在于细胞内,这些游离体有时也能够整合到细胞的DNA 中。
用EBV 体外感染人类的B 淋巴细胞,使其永生化得到淋巴瘤样细胞株(LCLs ),这些EBV 恶性转化的LCLs 含有EBV 的游离体(Episome)并且表达一系列产物,其中包括六种核蛋白:EBNA-1,EBNA-2,EBNA-3A,EBNA-3B,EBNA-3C,EBNA-LP;三种潜伏感染的膜蛋白:LMP1,LMP2A,LMP2B 以及两种RNA (EBERs)。
三种潜伏膜蛋白是在与EB 病毒感染有关的许多疾病中表达的功能蛋白,它们都没有受体的跨膜信号蛋白。
EBV 在潜伏感染状态下表达的蛋白可能是B 淋巴细胞生长转化的介质,因此其得到广泛细致的研究。
其中的LMP1由于其被明确证明能转化原代B 细胞。
在不同的细胞类型中,LMB1具有多种信号转导和广泛的基因调控作用,LMP1也正是通过这些信号通路和基因调控发挥广泛的生物学功能,包括上调B 细胞标志及细胞粘附分子CD23、CD40、CD45等的表达。
LMP1也能激活细胞粘附分子LFA1、LFA3和ICAM1等的表达,还能通过诱导抗凋亡基因A20和Bcl-2的表达抑制细胞凋亡。
因此,LMP1的功能涉及到细胞转化、增值、细胞凋亡和分化的各个方面。
图 LMP1的信号传导通路图 P AFT2 AFT2 P ELK1 ELK1 JNK SEK + NF-KB p I ҡB p NF-KB I ҡB NF-KB I ҡB TRAF3 TRAF2 TRAF1 CTAR2 TRADDCTAR1 ELK SRE SDE JAK3 STA T3 ICAM C-Fos C-Jun/AFT2C-Jun-AP-1 AP-11 LMP1的分子结构及其转录调控LMP1是由EBV基因组右端的BNLF-1基因编码的跨膜蛋白,其分子量因EBV株的变异介于60~66kDa之间。
《微生物学》期末复习简答题及答案一

《微生物学》期末复习简答题及答案1.简述免疫球蛋白的基本结构。
答:①四肽链结构:重链、轻链②免疫球蛋白的分区:可变去和恒定区高变区和骨架区、铰链区③免疫球蛋白的其他结构:连接片(J链)、分泌片(SP).2.抗体的生物功能主要有哪些?答:①特异性的生物学作用、②激活补体、③与细胞表面FC受体结合:调理作用、抗体依赖性细胞介导的细胞毒作用,介导I型超敏反应④穿过胎盘和粘膜。
3.比较五类免疫球蛋白结构和功能的异同点。
答:共分为五类:①IgG、②IgM。
③IgA、④IgD、⑤IgE:①IgG血清含量最高,半衰期最长;功能最多:结合抗原、激活补体、调理吞噬并介导ADCC、通过胎盘、结合SPA.为再次免疫应答的主要抗体:抗感染的主要抗体(抗菌、抗病毒。
抗毒素抗体)。
并介导II、III型超敏反应。
2、IgM分子量最大,不能通过血管壁,主要存在于血液和粘膜表面。
是血管内抗感染的主要抗体。
在个体发育过程和体液免疫应答中均是最早合成和分泌的抗体。
脐带血IgM增高提示胎儿有宫内感染;感染过程中血清IgM 水平升高,说明有近期感染。
天然的血型抗体和类风湿因子亦属IgM.其激活补体的能力比IgG强。
膜表面IgM 是B细胞抗原受体(BCR)的主要成分。
只表达mIgM是未成熟B细胞的标志,记忆B细胞表面的mIgM逐渐消失。
3、IgA(1)血清型IgA:以单体形式存在。
(2)分泌型IgA(sIgA):由J链连接的二聚体和分泌片组成。
合成和分泌的部位在肠道、呼吸道、乳腺、唾液腺和泪腺,主要存在于胃肠道和支气管分泌液、初乳、唾液和泪液中。
是参与粘膜局部免疫的主要抗体。
婴儿可从母亲初乳中获得分泌型IgA,是一种重要的自然被动免疫。
4、IgD正常人血清IgD浓度很低,平均约0.03mg/ml.半寿期很短(仅3天)。
血清IgD的确切功能仍不清楚。
B细胞表面的mIgD可作为B细胞分化发育成熟的标志,未成熟B细胞仅表达mIgM,成熟B细胞可同时表达mIgM和mIg。
EB病毒感染机制及其检测方法

03 EBV流行病学研究
a 地域分布
• 世界性,分布广泛 • 散发性,四季皆可
c 传播途径
• 飞沫传播 • 血液传播或性传播
b 传染源
• 病毒携带者 • 患者
d 易感人群
• 不论种族、性别,20岁以下女性略多 • 感染率高,大多呈潜伏状态
贰
EBV感染致病机制
Pathogenic mechanism of EB virus infection
04 检测方法—原位杂交(EBER)
EBER定位:细胞核 常用检测组织:鼻咽癌、 淋巴瘤及胃癌组织等
04 检测方法—原位杂交(EBER)
原位杂交
• 细胞形态保持较好
优点 • 细胞定位准确:细胞核,少数细胞浆亦着色
• 稳定性好、特异性高
• 对病理诊断具有重要的参考价值
• 组织和细胞中EBV检测的金标准
潜伏性感染
多见于EBV相关的恶性肿瘤
EBNA:核相关肿瘤抗原 LMPs:EBV潜伏膜蛋白
03 EBV感染机制----免疫逃逸机制
潜伏期EBV基因表达下调
01
抑制Th1免疫应答 06
02 干扰抗原加工和提呈
调节CTL免疫应答 05
03 干扰细胞因子作用
04
抑制宿主细胞凋亡
04 EB病毒参与肿瘤发生发展的分子机制
e 结果观察
胞膜及胞浆阳性
不同疾病免疫组化检测结果
LPM1
NSCHL-LMP1
NK/T-LMP1
03 检测方法—免疫组化
优点 • 简便易行 • 成本较低 • 细胞定位准确
免疫组化
不足
• 稳定性、特异性低 • 易出现假阴性 • 病理诊断参考价值不高 • 阳性率低
细胞永生化实验

• EBV主要通过结合人类B淋巴细胞膜上的 EB病毒受体而感染B淋巴细胞,初次受到 感染便被迅速致敏,36h后就可有DNA 合成。被感染的B细胞在EB病毒核抗原的 刺激下转化为类淋巴母细胞,其端粒酶活 性提高,维护了细胞染色体端粒长度的稳 定,并能够不断分裂增殖,从而促使B淋 巴细胞的永生性生长。转化的细胞株染色 体稳定,保留了原有的遗传性状。人淋巴 细胞转化是建立永生细胞系及进行细胞遗 传和分子遗传研究的极好方法。
• Epstein-Barr病毒(EBV)是1964年首先从 非洲恶性Burkitt淋巴瘤(BL)的淋巴母细胞 系中发现的,属疱疹病毒科γ亚科。EBV 有一个与其他DNA病毒不同的特点,就是 它在体外对B细胞的感染可刺激细胞的持 续性生长并引起细胞的永生化,从而形成 淋巴母细胞样细胞系(1ymphoblastoid cell lines,LCLs) ,尤其对人二倍体淋巴细 胞转化效果极佳。
实验材料和方法
试剂 产生 EBV的 B95-8细胞株,RPMI1640培
养基,PBS缓冲液,胎牛血清,淋巴细 胞分离液,环孢霉素A,植物凝集素, 台盼蓝染液 标本的收集 取样:无菌、轻轻摇动使血液与肝素混匀 秦巴山区精神发育迟滞患者家系(两天 之内的血样)
实验方法
EB病毒的制备
• EB病毒基因组序列及其表达研究主要是 用B95-8 株进行的,B95-8 细胞系是用 传染性单核细胞增多症患者的EB 病毒感 染绒猴B 淋巴细胞建立的。在B95-8 细 胞系中只有很少一部分细胞可以自发产 生病毒, 其他细胞呈隐性状态, 用不同的 诱生剂如TPA诱生后, 使产生病毒的细胞 明显增加。B95-8在EB病毒转化B-淋巴 细胞过程中非常重要, 通过培养B95-8细 胞制备出大量高效价的EB病毒液, 对于 B95-8细胞的培养质量是EB病毒转化B淋巴细胞成败的关键。
细胞永生化处理方法

细胞永生化处理方法引言细胞永生化处理方法是指通过一系列的技术手段,使细胞能够长时间保持活力和增殖能力,从而实现细胞的永生化。
这项技术在生物医学研究、药物开发和组织工程等领域具有重要的应用价值。
本文将介绍几种常见的细胞永生化处理方法,并分析它们的优缺点。
方法一:基因修饰基因修饰是一种常见的细胞永生化处理方法。
通过改变特定基因的表达或功能,可以延长细胞的寿命和增加其增殖能力。
常用的基因修饰方法包括下调抑制性基因、上调促进性基因以及改变染色体结构等。
下调抑制性基因是一种常见的策略。
例如,通过RNA干扰技术或CRISPR-Cas9系统靶向沉默p53等抑制性基因,可以减少细胞凋亡和老化现象,延长细胞寿命。
上调促进性基因也是一种有效的方法。
例如,通过转染特定基因或使用激活子等技术,可以增加细胞的增殖能力和代谢活性,从而延长细胞寿命。
改变染色体结构是另一种常见的基因修饰方法。
例如,通过转座子或合成染色体等技术,可以改变细胞染色体的结构和组成,提高其稳定性和抗衰老能力。
然而,基因修饰方法存在一些局限性。
首先,基因修饰可能引发不可预测的副作用或导致细胞功能异常。
其次,基因修饰需要精确的操作和复杂的技术支持,对于一些非专业人员来说较为困难。
方法二:药物干预药物干预是另一种常用的细胞永生化处理方法。
通过使用特定药物或化合物,可以调节细胞的代谢、增殖和凋亡等过程,从而延长细胞寿命。
一种常用的药物干预方法是使用抗衰老剂。
目前已经发现了多种具有抗衰老效果的化合物,如雷帕霉素、二甲双胍等。
这些化合物可以通过激活特定信号通路或改变细胞内环境来延长细胞的寿命。
另一种常见的药物干预方法是使用激素。
例如,雌激素在一些细胞中具有促进增殖和减少凋亡的作用,可以延长细胞寿命。
然而,激素使用需要注意剂量和时间的控制,以避免不良反应和副作用。
虽然药物干预方法相对简单易行,但也存在一些问题。
首先,不同细胞对药物的敏感性存在差异,需要进行个体化处理。
EB病毒的研究进展

BE病毒的研究进展EB病毒(epstein-barr virus,EBv),又称人类疱疹病毒(Human herpesvirus 4 (HHV-4))。
是epstein和barr于1964年首次成功地将burkitt非洲儿童淋巴瘤细胞通过体外悬浮培养而建株,并在建株细胞涂片中用电镜观察到疱疹病毒颗粒,故名。
病毒简介EB病毒是Epstein和Barr于1964年首次成功地将Burkitt非洲儿童淋巴瘤细胞通过体外悬浮培养而建株,并在建株细胞涂片中用电镜观察到疱疹病毒颗粒,认为该病毒是多种恶性肿瘤(如鼻咽癌)的病因之一,它主要感染人类口咽部的上皮细胞和B淋巴细胞。
在中国南方鼻咽癌患病人群中检测到有EB病毒基因组存在。
本病分布广泛,多呈散发性,亦可引起流行。
病毒携带者和病人是本病的传染源。
经口密切接触为主要传播途径,飞沫传播虽有可能,但并不重要。
发病以15~30岁的年龄组为多,6岁以下多呈不显性感染。
全年均有发病,似以晚秋初冬为多。
一次得病后可获较持久的免疫力。
形态特征EB病毒的形态与其他疱疹病毒相似,圆形、直径180nm,基本结构含核样物、衣壳和囊膜三部分。
核样物为直径45nm的致密物,主要含双股线性DNA,其长度随不同毒株而异平均为17.5×104 bp分子量108。
衣壳为20面体立体对称,由162个壳微粒组成。
囊膜由感染细胞的核膜组成,其上有病毒编码的膜糖蛋白,有识别淋巴细胞上的EB病毒受体,及与细胞融合等功能。
此外在囊膜与衣壳之间还有一层蛋白被膜。
传播途经1、经口密切传播2、飞沫传播3、输血传播引发病症EB病毒感染引起的相关疾病:非肿瘤性疾病1.传染性单核细胞增多症患者感染EBV后多数表现为IM。
1968年首次发现该病毒是引起IM的病源,后经血清流行病学等研究得到证实。
该病是目前所知道的由EBV直接引起的唯一疾病,有以下理论依据:(1)此种病毒只能在淋巴网状系统的细胞中生长增殖;(2)培养过程中该病毒能刺激淋巴细胞的增生;(3)急性期周围血淋巴细胞可培养出EBV;(4)患者血清中具有高滴定度EBV的特异抗体,并可长期存在;(5)无此特异抗体者对此病易感,而抗体阳性者则不发病。
ebv基因组

ebv基因组EBV基因组是指爱泼斯坦-巴尔病毒(Epstein-Barr virus,EBV)的基因组,该病毒是一种人类病毒,属于疱疹病毒科。
EBV是一种广泛存在于全球人群中的病毒,它可以引起多种疾病,包括传染性单核细胞增多症、某些类型的癌症等。
EBV基因组是由一条双链DNA组成的,它包含有多个基因,这些基因编码了病毒所需的各种蛋白质。
EBV基因组的大小约为172 kb,其中包括约90个基因。
这些基因可以分为早期基因、延迟基因和晚期基因三类。
早期基因主要参与病毒的复制和转录调控,它们在感染宿主细胞后很快被表达出来。
早期基因的转录产物可以促进细胞周期的进程,使细胞进入S期,从而为病毒的复制提供条件。
延迟基因主要参与病毒的潜伏感染和细胞转化。
延迟基因的表达在感染初期较低,当细胞处于生长状态时,延迟基因的表达会逐渐增加。
这些基因编码的蛋白质可以干扰宿主细胞的免疫应答,抑制细胞凋亡,促进细胞的增殖和生存,从而为病毒的潜伏感染提供条件。
晚期基因主要参与病毒的包装和释放。
晚期基因的表达在感染后较晚才开始,它们编码的蛋白质可以组装成病毒颗粒,并通过细胞膜释放到外部环境中,从而传播给其他细胞。
EBV基因组的编码蛋白质在病毒感染和疾病发生中起着重要的作用。
例如,病毒编码的蛋白质EBNA1可以与宿主细胞基因组结合,稳定病毒基因组的存在;LMP1蛋白可以模拟宿主细胞的活化信号,促进细胞的增殖和生存;EBNA2蛋白可以调控细胞周期和基因转录,从而影响宿主细胞的生理功能。
研究人员对EBV基因组的研究有助于揭示病毒的感染机制和致病机理,为疾病的预防和治疗提供理论基础。
通过对EBV基因组的深入了解,科学家们可以寻找到针对病毒的新型药物靶点,研发更有效的抗病毒药物。
此外,对EBV基因组的研究还可以为病毒性肿瘤的防治提供新的思路和方法。
EBV基因组是一项重要的研究课题,它关系到人类健康和疾病的发生发展。
通过对EBV基因组的研究,我们可以更好地理解病毒的感染机制和致病机理,为相关疾病的预防和治疗提供新的思路和方法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
20.1 概述 20.2 EBV基本结构及其表达产物 20.2.1 基本结构 20.2.2 表达产物 20.3 EBV感染和复制 20.3.1 感染 20.3.2 EBV转化外周血B细胞 20.4 EBV对B细胞的生长转化作用 20.4.1 对B细胞的激活和转化作用 20.4.2 与转化功能有关的病毒基因 20.4.3 LCLs与细胞永生化机制研究 20.4.3.1 LCLs与 p53及细胞周期调控相关基因 20.4.3.2 LCLs与端粒酶活性 20.4.3.3 LCLs与异常核型 20.5 EB病毒和人类肿瘤 20.6 展望
20.2.2
表达产物
EBV 基 因 结 构 中 有 8 4 个 开 放 读 码 结 构 (ORF),包括100多个基因,但只有9个基因能 在体外感染转化的B细胞中表达蛋白质。这9 个基因能编码6个EBV核抗原(EBNArb)和3个 潜在膜蛋白(LMP1~3),其在细胞增生转化过 程中作用不相同,以EBNA1、EBNA2、EBNA-LP和 LMP1作用更加重要。
ቤተ መጻሕፍቲ ባይዱ
EBNA2:EBNA2是一种Mr为(78~90)X103,富含脯氨酸 的核蛋白。有2个功能区,位于450~464残基间和425~252残 基间,前者为酸性反式活化区域,后者是EB-MA2反应元件 (E2RE)活化区域,是生长和转化E2RE的功能区,能与细胞结 合蛋白结合。所以EBNA2是通过与细胞结合蛋白结合,通过 该蛋白与E2RE结合。而E2RE又位于LMP1、LMP2、CD23基因上 游,随着EBNA2的表达,CD21、CD23、LMP1、LMP2的基因表达也 增强,EBNA2在EBV潜伏感染和细胞转化中起反式激活剂的 作用。EBNA2基因以及 EBNA-LP基因的最后两个外显子缺失 的突变的 EBV病毒株P3HR1不能使 B细胞永生化;而将从 B95-8 病 毒 株 获 得的 EBNA2 基因和 EBNA-LP 基因导入P3 HRl基因组就会使其获得完全的永生化能力。EBNA2是一转 录激活因子,实验结果显示其转录激活功能和转化功能不 可分割,表明后者很可能是通过前者来实现的。
EBNA-LP(EBNA-5):EBNA-LP 由 每 一 种 EBNA m RNAs的前导序列编码,分子遗传学研究表明,虽 然 EBNA-LP并不是体外 B细胞转化所必需的,但它 却是 LCLs的高效生长所需要的。EBNA-LP和 EBNA2 瞬时感染初级 B细胞会引起细胞由 G0 期向 G1 期的转化,表现为细胞周期蛋白D2表达的上调。 EBNA-LP与p Rb和 p53都存在相互作用,有 EBNALP基因缺失的病毒永生化 B细胞的能力会降低。
50年代末期,Burkitt发现儿童淋巴瘤的区域分布等特 点,提出了其致病因子可能为病毒的假说。经过数年的努 力,Epstein和Barr于1964年首次成功地将Burkitt非洲儿 童淋巴瘤细胞通过体外悬浮培养而建株,并在建株细胞涂 片中用电镜观察到了疱疹病毒颗粒,从而发现了EB病毒。 Old等在1966年用免疫扩散法揭示了EB病毒和鼻咽癌的血 清学关系。70年代初,Henle夫妇建立起最初的EB病毒血清 学检查方法,为EB病毒的检测提供了重要的手段,并进而证 实了本病毒是传染性单核细胞增多症的病原体。进入80年 代,分子病毒学的发展使EB病毒的研究进入了新的层次。随 着其基因组测序的完成,以及蛋白质组学的飞速发展,多基 因产物的鉴定和分析,对EB病毒的相关基因和蛋白质有了 初步的了解。
EBNA3A,EBNA3B(EBNA-4), EBNA 3C(EBNA-6): EBNA3A,EBNA3B和EBNA3C是由有着共同起源的三个 基因在 Cp或Wp启动子的作用下转录并翻译出来的三种 亲水性核蛋白。EBNA3家族的成员都是转录调节因子,能 抑制或者激活转录;它们可以通过抑制 RBP-Jκ蛋白与 DNA的结合间接性的抑制 EBNA2介导的TP1和 LMP1启 动子的激活过程。对 EBV重组体的研究表明,EBNA3 A和 EBNA3 C对于 B细胞的体外转化是必需的,其中 EBNA3 C能够使细胞基因 (CD2 1 )和病毒基因 (LMP1 )的表达 上调、抑制启动子 Cp、与视网膜母细胞瘤蛋白 (p Rb)相互 作用而促进转化。EBNA3 B虽然不是转化所必需的,但它 能诱导波形蛋白和 CD40的表达。
20.1
概述
Epstein-Barr病毒(EB病毒)是疱疹病毒科嗜淋巴细胞病 毒属的成员。其感染十分普遍。在发达国家,EBV的感染多发生 于青春期,易引起传染性单核细胞增多症(IM);而在发展中国 家,EBV的感染通常发生在5岁之前,多为亚临床感染,成人的感 染率高达98%,病毒可携带终身。EBV之所以引起全世界的广泛 关注,不仅因为EB病毒是IM的病原,而是由于EB病毒参与了人 类多种恶性肿瘤的形成,包括Burkitt's淋巴瘤(BL)、鼻烟癌 (NPC)、免疫耐受个体的B淋巴细胞瘤及何杰金氏病(HD)、非 Hodgkin性 T细胞淋巴瘤(NHL)、胃癌。乳腺癌、肝细胞癌和免疫 缺陷患者发生的平滑肌细胞瘤等可能与 EBV感染相关。
EB病毒的形态、理化性状及生物学特性都和疱疹病毒科 的其他成员有类似之处,能和它们一样在感染机体后,建立起 长期的潜伏感染。EBV还有一个与其他 DNA病毒不同的特点, 就是它具有在体内,以及体外感染人及某些灵长类B细胞的专 一性,并能刺激受感染细胞持续性生长并引起细胞无限期传 代达到”永生”,从而形成淋巴母细胞样细胞系 (lymphoblastoid cell lines,LCLs)。由于肿瘤与EBV的确切 关系极为复杂且存在争议,而LCLs没有肿瘤形成过程中的复 杂因素,使其成为了研究 EBV介导的细胞永生的最佳模型。
3)病毒分型 EB病毒分为两个亚型,A型和B型,亚型之间 存在明显差异:①从基因结构上看,在EB病毒的一些基因组 中(如EBNA-2,EBNA-3A,EBNA-3B,EBNA-3C和EBERs)存在碱 基对的缺失或/和插入。②蛋白水平上的差异,如上述的编 码基因的差异必然导致相应蛋白的结构差异。③不同的蛋 白结构引起不同的抗原抗体反应,因而用血清学方法可间 接区分开A型和B型EB病毒感染。④在生物学上,B型EB病毒 转化B淋巴细胞的能力较A型弱,因此建立B型EB病毒细胞株 较困难。⑤从地区分布上看,A型遍布全球,B型多集中在非 洲中部一带。⑥从EB病毒相关疾病看,A型感染的疾病较 广,B型则集中在部分非洲的Burkitt淋巴瘤、部分人体免疫 缺陷病毒(HIV)阳性淋巴瘤和爱斯基摩人鼻咽癌中。
20.2 基本结构及其表达产物
20.2.1基本结构 (1)形态结构和理化特性
成熟的EB病毒颗粒为直径180nm的球 形。其基本结构可分为核样物、核衣壳和包 膜三部分。
(2)病毒基因组的结构 80年代初,EB病毒的基因组即已被分段克隆。1983年 ,Barr等完成了对其整个基因组的序列测定。 1)大体结构 EB病毒基因组的大体结构可分为如下几个部 分(图1):①末端重复序列(TR);②内重复序列(IR)③DL和 DR。 在不同的病毒株具有以上重复序列的个数不一,这一特 点可被用于不同病毒株的鉴别和确定有无两种病毒株的双 重感染。
20.2.2.1 潜伏期的基因表达
1)核抗原家族(EBNA) 是一组核蛋白,目前 共检出6种。他们都有共同的转录启动子和5’ 端,然而它们的主要编码区则由于不同的转录 剪切而完全不同,由此而产生完全不同的核抗 原。核抗原往往携带不同数量的重复片断,因而 其Mr可以有较大的差异。
EBNA1:EBNA1是一种序列特异性 DNA结合磷蛋白, 由BKPF1编 码。可分为四部分:由89个氨基酸组成的N端,富有碱性残基;由 多个”甘氨酸和丙氨酸”所组成的重复序列,长度约250个氨基 酸;主要由碱性残基组成的短区域;一较长的主要由酸性或碱 性氨基酸组成的C端。EBNA1在所有 EBV感染的细胞中唯一始终 表达的蛋白质。它对于具有回文结构的同源序列 (TAGGATAGCATATGCTACCCAGATCCAG)具有很强的亲和性,与同源 序列结合后可以诱导病毒基因组游离体的复制、启动多个潜伏 感染期病毒基因的转录,并能调节宿主细胞基因的转录。有研究 证实 EBNA1缺失的重组病毒会丧失使 B细胞永生化的能力。 EBNA1的核心部分的 Gly-Ala重复序列,是主要组织相容性复合 体 I型限制性递呈的顺式抑制因子,它能阻抑蛋白酶体对蛋白 质的加工过程,影响抗原多肽的产生,从而防止EBV感染的细胞 被细胞毒性 T细胞杀伤。
由于LMP1位于细胞膜上 ,从而推测它在细胞间信号的传递过程 中起到重要作用 ,也是它发挥重要的生物学功能的物质基础和结构 基 础 。 近 年 来 对 LMP1 的 生 物 学 功 能 进 行 了 大 量 的 研 究 。 研 究 表 明 ,LMP1能使鼠类成纤维细胞株发生转化 ,主要表现在细胞形态改 变、细胞间接触抑制丧失等 ,证明LMP1与细胞的转化、增殖以及去分 化有关。在EB病毒转化B细胞的研究中发现 ,LMP1具有促进及维持B细 胞转化及永生化的重要作用 ,能引起B细胞标志CD40、CD2 3及CD54等 的表达增加 ,使CD10的表达减少 ,能引起细胞粘附分子LFA1、LFA3及 ICAM-1的表达受到激活。进一步研究发现 ,LMP1在细胞中基因转录过 程中具有重要作用。它能诱导NF-kB核转录因子的表达活化, NF-κ B 进而激活A20基因的表达,产物能拮抗TNF-a细胞毒作用。LMP1还能跨 域激活某些病毒的启动子 ,如HPV启动子、HIV-1LTR的启动子、人类T 细胞白血病Ⅰ型病毒 (HTLV-1 )的启动子受到诱导表达。这是由于 LMP1能选择性地修饰抑制分子IkBa ,通过使其失活而消除IkBa对NFκ B的抑制作用 ,并使NF-κ B活化表达 ,进而使病毒启动子的表达得 以活化。
2)病毒基因组序列 EB病毒基因组在疱疹病毒科成员 中最早被全部测序,所用的病毒株是用枭猴B细胞经病毒转 化后获得的B95—8,它亦是最为广泛使用的实验EB病毒株。 本病毒的核酸序列主要特征为:①总长度为172 282bp(B95—8株有一段约10kb的缺失区,据此估计野生型 的长度应在185kb左右);②根据序列测定结果分析,可确定 有约80个ORF。后者的命名方式见(图1)。③与疱疹病毒科 其他成员的序列比较显示出明显进化上的联系。尽管总的 序列同源性很低,但在基因组的不少区域,不仅功能相同的 基因之间有同源性,而且整个区域内的基因排列也极其相 似。④病毒基因组成至少携有2个和人细胞基因同源性很高 的基因。
