初三化学1-8单元知识总结(思维导图)新选
初三化学思维导图知识讲解

初三化学思维导图第一章走进化学世界第二章我们周围的空气第三章物质构成的奥秘第四章自然界的水第五章化学方程式第六章碳和碳的氧化物第七章燃料及其利用第八章金属和金属材料第九章溶液第十第十章酸碱盐一、化学用语1、电离方程式:H2SO4=2H++SO42-;NaOH=NA++OH-;Al2(SO4)=2Al3++3SO42-2、物质的俗称和主要成分:生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4·5H2O;碳酸钠晶体Na2CO3·10H2O;氨水NH3H2O。
二、金属活动性1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na 除外)。
三、酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物Ca(OH)2(石灰水注明“澄清”的原因);CaSO4(实验室制二氧化碳时不用稀硫酸的原因);Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因);MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)。
初三化学思维导图
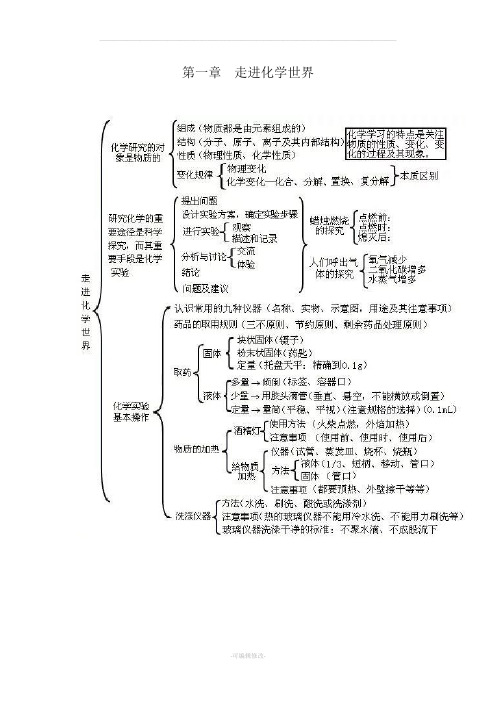
第一章走进化学世界第二章我们周围的空气第三章物质构成的奥秘第四章自然界的水第五章化学方程式第六章碳和碳的氧化物第七章燃料及其利用第八章金属和金属材料第九章溶液第十第十章酸碱盐一、化学用语1、电离方程式:H2SO4=2H++SO42-;NaOH=NA++OH-;Al2(SO4)=2Al3++3SO42-2、物质的俗称和主要成分:生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4·5H2O;碳酸钠晶体Na2CO3·10H2O;氨水NH3H2O。
二、金属活动性1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na除外)。
三、酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁。
初三化学思维导图
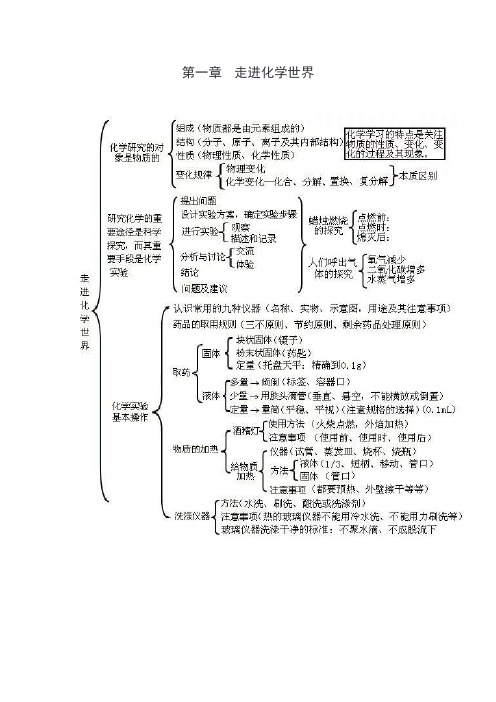
第一章走进化学世界第二章我们周围的空气第三章物质构成的奥秘第四章自然界的水第五章化学方程式第六章碳和碳的氧化物第七章燃料及其利用第八章金属和金属材料第九章溶液第十第十章酸碱盐一、化学用语1、电离方程式:H2SO4=2H++SO42-;NaOH=NA++OH-;Al2(SO4)=2Al3++3SO42-2、物质的俗称和主要成分:生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4·5H2O;碳酸钠晶体Na2CO3·10H2O;氨水NH3H2O。
二、金属活动性1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na除外)。
三、酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物Ca(OH)2(石灰水注明“澄清”的原因);CaSO4(实验室制二氧化碳时不用稀硫酸的原因);Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因);MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)。
九年级化学1-10单元知识脉络图

第一单元走进化学世界知识脉络图第二单元我们周围的空气知识脉络图第三单元自然界的水知识脉络图第四单元物质构成的奥秘知识脉络图第五单元化学方程式知识脉络图第六单元碳和碳的氧化物知识脉络图第七单元 燃料及其利用第八单元金属和金属材料第十单元酸和碱知识脉络图:酸和碱酸酸的通性酸溶液可与酸碱指示剂作用,可使紫色石蕊试液变红,无色酚酞试液变色。
酸溶液可与某些金属反应生成盐和氢气。
如:H2SO4+Zn====ZnSO4+H2↑酸溶液可与某些金属氧化物反应生成盐和水。
如:6HCl+Fe2O3===2FeCl3+3H2O酸溶液可与碱反应生成盐和水。
如:HCl+NaOH===NaCl+H2O酸溶液与某些盐反应生成新盐和新酸。
如:HCl +AgNO3===AgCl↓+HNO3 酸的含义:酸→H++酸根离子常见的酸硫酸盐酸物理性质:无色液体,有刺激性气味,有酸味,具有挥发性化学性质:可与酸碱指示剂、金属、金属氧化物、碱、盐等发生化学反应用途:重要化工产品,用于金属表面除锈、制药物等浓硫酸的特性:具有吸水性、脱水性、强氧化性,溶于水时放出大量热稀硫酸的化学性质:可与酸碱指示剂、金属、金属氧化物、碱、盐等发生化学反应用途:重要化工原料,用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等,浓硫酸常用作干燥剂碱的通性碱溶液可与酸碱指示剂作用,可使紫色石蕊试液变蓝色,无色酚酞试液变红色碱溶液可与某些非金属氧化物反应生成盐和水。
如:2NaOH+CO2===Na2CO3+H2O碱溶液可与酸反应生成盐和水。
如:Ca(OH)2+2HCl===CaCl2+2H2O碱溶液可与某些盐反应生成新盐和新碱。
如:2NaOH+CuSO4===Na2SO4+Cu(OH)2↓碱碱的含义:碱→金属离子+OH-氢氧化钙物理性质:白色粉末状物质,微溶于水,有腐蚀性化学性质:可与酸碱指示剂、非金属氧化物、酸、盐等发生化学反应用途:建筑业上常用熟石灰、黏土和沙子混合制成三合土,或用石灰砂浆来砌砖、抹墙;工业上把它作为原料来制造漂白粉、氢氧化钠;农业上用它来降低土壤的酸性,改进土壤结构,还用它来配制农药波尔多液和石硫合剂。
