中国药典纯化水制药用水标准
中国药典纯化水制药用水标准

中国药典纯化水(制药用水)标准本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【总有机碳】不得过0.50mg/L。
【易氧化物】取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
以上总有机碳和易氧化物两项可选做一项。
【重金属】取本品100ml,加水19ml,蒸发至20ml,放冷,加醋酸盐缓冲液(pH3.5)2ml与水适量使成25ml,加硫代乙酰胺试液2ml,摇匀,放置2分钟,与标准铅溶液1.0ml加水19ml用同一方法处理后的颜色比较,不得更深(0.000 01%)。
【电导率】应符合规定(附录)【铝盐】(供透析液生产用水需检查)取本品400ml,置分液漏斗中,加醋酸盐缓冲液(pH 6.0)10ml和水100ml ,用0.5% 8-羟基喹啉三氯甲烷溶液提取3次(20ml,20ml,10ml),合并三氯甲烷提取液于50ml量瓶中,加三氯甲烷至刻度,摇匀,即得供试品溶液;另取标准铝盐溶液[称取硫酸铝钾0.352g,置100ml量瓶中,加1mol/L硫酸溶液10ml溶解后,用水稀释至刻度,摇匀,作为贮备液。
临用前,精密量取贮备液1ml,置100ml量瓶中,用水稀释至刻度,摇匀,即得(每1ml相当于2μg的Al)]2.0ml,置分液漏斗中,加醋酸盐缓冲液(pH 6.0)10ml和水98ml,同法操作,即得标准溶液;取醋酸盐缓冲液(pH 6.0)10ml和水100ml,置分液漏斗中,同法操作,作为空白溶液。
取上述溶液,照荧光分析法(附录ⅣE),在激发光波长392nm与发射光波长518nm处分别测定荧光强度。
供试品溶液的荧光强度不得大于标准溶液的荧光强度(0.000 001%)。
制药用水有哪些分类和水质标准

制药用水分类和水质标准:制药用水(加工用水:药品制造过程中使用的水,如饮用水,纯净水和注射用水)分类1.饮用水:自来水或深井水,通常由自来水公司提供,也称为原水,其水质必须符合国家标准GB5749-85“饮用水卫生标准”。
有。
根据《2010年中国药典》,饮用水不能直接用于制备或测试。
2.纯化水(Purified Water):制药用水,由原水通过蒸馏,离子交换,反渗透或任何其他合适的方法制成,无任何添加剂。
纯化水可用作制备普通药物制剂的溶剂或测试水。
它不能用于准备注射剂。
通过非热处理(例如离子交换,反渗透和超滤)制备的纯净水通常也称为去离子水。
通过使用特殊设计的蒸馏器蒸馏制备的纯净水通常称为蒸馏水。
3. 注射用水:通过将水纯化为原水,再用专门设计的蒸馏水蒸馏,冷凝和冷却后通过膜过滤得到的水。
注射用水可以用作注射溶剂。
4. 无菌注射用水:根据注射液的生产工艺准备注射用水。
注射用无菌水是用于粉末消毒的溶剂或稀释剂。
制药用水的水质标准:1.饮用水:应符合中华人民共和国国家标准《生活饮用水卫生标准》(GB5749-85)2.纯化水:应符合《2010中国药典》所收载的纯化水标准。
在制水工艺中通常采用在线检测纯化水的电阻率值的大小,来反映水中各种离子的浓度。
制药行业的纯化水的电阻率通常应≥0.5MΩ.CM/25℃,对于注射剂、滴眼液容器冲洗用的纯化水的电阻率应≥1MΩ.CM/25℃。
3.注射用水:应符合2010中国药典所收载的注射用水标准二:2010年中国药典对纯水、注射用水、灭菌注射用水的pH、电导率、总有机碳(TOC)的检测提出如下要求:1. 药典对pH检测的新要求:pH值应处在5.0~7.0。
2.药典对电导率检测的新要求:调节待测样品的温度至25℃。
标示装量为10ml或10ml以下时,电导率限度为25μS/cm;标示装量为10ml以上时,电导率限度为5μS/cm。
测定的电导率值不大于限度值,则判为符合规定;如电导率值大于限度值,则判为不符合规定。
制药用水的分类全套

制药用水的分类全套《中国药典》将制药用水分为饮用水、纯化水、注射用水和灭菌注射用水。
(1)饮用水(drinkingwater):天然水经净化处理所得的水.(2)纯化水(purifiedwater):为饮用水经蒸馆法、离子交换法、反渗透法或其它适宜方法制得的制药用水,不含任I可附加剂,其质量应符合《中国药典》纯化水项下的规定。
(3)注射用水(waterforinjection):为纯化水经蒸憎所得的水。
应符合细菌内毒素试验要求。
其质量应符合注射用水项下的规定。
(4)灭菌注射用水(sterilewaterforinjection):为注射用水按照注射剂生产工艺制备所得,不含任何添加剂。
灭菌注射用水灌装规格应该适应临床需要,避免大规格、多次使用造成的污染。
2、制药用水的应用范围见表3-1表3-1制药用水的应用范围类别应用范围饮用可作为药材净制时的漂洗、制药用具的粗洗用水,除水另有规定外,也可作为药材的提取溶剂可作为配制普通药物制剂用的溶剂或试验用水;中药注射剂、中药滴眼剂等灭菌制剂所用饮片的提取溶剂;口服、外用制剂配制用溶剂或稀释剂;非灭菌制剂用器具的精洗用水。
也可以作为非灭菌制剂所用饮片纯化的提取溶剂。
纯化水不得用于注射剂的配制与稀水释。
注射可作为配制注射剂、滴眼剂等的溶剂或稀释剂及容器用水的精洗。
灭菌可作为注射用灭菌粉末的溶剂或注射液的稀释剂。
注射用水3、注射用水的质量要求注射用水除一般蒸留水的检查项目如pH值、氨、氯化物、硫酸盐与钙盐、硝酸盐与亚硝酸盐、二氧化碳、易氧化物、不挥发物及重金属等均应符合规定外,还必须通过细菌内毒素(热原)检查和无菌检查。
4、注射用水的收集和保存目前国内仍用蒸憎法制备注射用水,接收蒸馆水时,初情液应弃去一部分,检查合格后,方能收集,收集时应注意防止空气中灰尘及其他污物落入,最好采用带有无菌过滤装置的密闭收集系统。
注射用水一般需新鲜制备,在70。
C以上保温循环存放,保存时间一般不得超过12小时,灭菌后贮放不宜超过24小时。
制药行业对纯化水设备的要求及水质指标

制药行业对纯化水设备的要求及水质指标一:制药用水分类及水质指标1、制药用水(工艺用水:药品生产工艺中使用的水,包括饮用水、纯化水、注射用水)分类1)饮用水(Potable-Water):通常为自来水公司供应的自来水或深井水,又称原水,其质量必须符合国家标准GB5749-85《生活饮用水卫生标准》。
2)纯化水(Purified Water):为原水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用的水、不含任何附加剂。
纯化水可作为配制普通药物制剂的溶剂或试验用水,不得用于注射剂的配制。
采用离子交换法、反渗透法、超滤法等非热处理制备的纯化水一般又称去离子水。
纯化水设备采用特殊设计的蒸馏器用蒸馏法制备的纯化水一般又称蒸馏水。
3)注射用水(Water for Injection):是以纯化水作为原水,经特殊设计的蒸馏器蒸馏冷凝冷却后经膜过滤制备而得的水。
注射用水可作为配制注射剂用的溶剂。
4)灭菌注射用水(Sterile Water for Injection):为注射用水依照注射剂生产工艺制备所得的水。
灭菌注射用水用于灭菌粉末的溶剂或注射液的稀释剂。
2、制药用水的水质标准1)饮用水:应符合中华人民共和国国家标准《生活饮用水卫生标准》(GB5749-85)2)纯化水:应符合《2000中国药典》所收载的纯化水标准。
在制水工艺中通常采用在线检测纯化水的电阻率值的大小,来反映水中各种离子的浓度。
制药行业的纯化水的电阻率通常应≥0.5MΩ.CM/25℃,对于注射剂、滴眼液容器冲洗用的纯化水的电阻率应≥1MΩ.CM/25℃。
3)注射用水:应符合2000中国药典所收载的注射用水标准。
二:GMP对制药用水制备装置的要求1、结构设计应简单、可靠、拆装简便。
2、为便于拆装、更换、清洗零件,执行机构的设计尽量采用的标准化、通用化、系统化零部件。
3、设备内外壁表面,要求光滑平整、无死角,容易清洗、灭菌。
零件表面应做镀铬等表面处理,以耐腐蚀,防止生锈。
制药用水的定义等级划分

制药用水的定义等级划分
一、制药用水的定义
制药用水是指用于药品生产、制备过程中使用的各种水源,其质量要求严格,以确保药品的安全性和有效性。
根据国家相关法规和标准,制药用水主要包括饮用水、纯化水、注射用水和超纯水等几个等级。
二、制药用水的等级划分
1.饮用水:作为制药用水的基础,饮用水经过了初步的净化处理,去除了其中的悬浮物、杂质、细菌等有害物质,但仍然保留了水中的矿物质和微量元素。
在药品生产中,饮用水主要用于设备的清洗、洗涤剂的制备等一些对水质要求不高的辅助性用途。
2.纯化水:纯化水是制药用水中最常见的一种,其水质应符合国家相关法规和标准的要求。
纯化水主要通过蒸馏、离子交换、反渗透等工艺方法制备而成,具有较高的纯度和洁净度。
在药品生产中,纯化水主要用于配制溶液、清洗设备、制备中间体等。
3.注射用水:注射用水是制药用水中最为特殊的一种,其水质需经过严格的控制和处理,以保证药品的安全性和有效性。
注射用水主要通过蒸馏或反渗透等工艺方法制备而成,具有高度的纯度和洁净度。
在药品生产中,注射用水主要用于配制注射用溶液、直接接触药品的设备清洗等。
4.超纯水:超纯水是制药用水中最高级别的一种,其水质需经过更为严格的净化处理和检测,以满足高标准的生产要求。
超纯水主要通过高效过滤、离子交换、紫外消毒等工艺方法制备而成,具有极高的纯度和洁净度。
在药品生产中,超纯水主要用于制备高纯度药物、生化试剂等特殊药品。
药典中水的分类

药典中水的分类药典是医药行业中非常重要的参考工具,它规定了药品和医药用品的质量标准、检验方法、使用范围等信息。
在药典中,水也是一个非常重要的分类。
药典对水的分类主要是根据净水处理工艺和应用范围进行的。
接下来,我将对药典中关于水的分类进行详细介绍。
一、制药用水1.注射用水:注射用水是制备无菌注射剂时所需的一种无菌水,它必须完全无菌,并且要符合注射剂的质量标准。
注射用水主要用于注射剂的稀释、配制以及清洗生产设备等。
2.原水:原水是制药用水的起始材料,它的质量决定了最终制药用水的质量。
药典中规定了不同类型的原水,如自来水、纯水、双重蒸馏水等。
3.纯化水:纯化水是经过初级、中级和高级除盐处理的水,在生产过程中用于制备药品、设备清洗、制药设备供应等。
4.蒸馏水:蒸馏水是通过蒸馏过程从原水中去除杂质得到的水,它的离子含量非常低,适用于一些高纯度药品的制备。
5.双重蒸馏水:双重蒸馏水是经过两次蒸馏过程得到的水,它的纯度更高,用于制备一些高纯度、高灵敏度的药品。
6.灭菌水:灭菌水是经过灭菌处理的水,用于制备灭菌药品和灭菌设备清洗。
7.超纯水:超纯水是经过超纯水制备系统处理的水,通过多种工艺去除所有的杂质和离子,得到的水具有非常高的纯度,适用于制备特殊要求的药品。
二、医用水1.外科手术洗手用水:外科手术洗手用水是用于医务人员在手术前进行手部清洁和消毒的水。
2.制备外科仪器灭菌用水:制备外科仪器灭菌用水是用于清洗和消毒外科手术器械和设备的水。
3.病房和手术室供水:病房和手术室供水是用于医院病房、手术室等场所的供水。
三、实验室水实验室水是用于实验室科研活动的水,主要分为实验用水和纯化用水两类。
1.实验用水:实验用水是供实验室常用仪器、设备和实验室试剂使用的水。
2.纯化用水:纯化用水是用于实验室高纯度试剂的配制及实验仪器的清洗、冲洗等。
四、药物配制用水药物配制用水是指制药过程中用于制备药品的水。
主要包括稀释用水、配制用水等。
中国药典 纯化水标准

中国药典纯化水标准中国药典规定了纯化水的标准,纯化水是制药工业中常用的一种水质。
它是通过多种工艺方法处理而成的,具有一定的纯净度和稳定性,可以用于制药生产中的各个环节,如药物生产、药物溶液配制、药物稀释等。
纯化水的标准对于保证药品的质量和安全具有重要意义。
首先,中国药典规定了纯化水的外观要求。
纯化水应该是透明无色的,不应该有悬浮物和沉淀物。
这是因为在制药过程中,如果纯化水出现浑浊或有杂质,就会对药品的制备和质量产生影响,甚至可能引起药品的变质。
其次,纯化水的化学成分也受到了严格的控制。
中国药典规定了纯化水的PH值范围,一般在5.0-7.0之间。
PH值的过高或者过低都会影响药品的稳定性和安全性。
此外,纯化水中的有机物、无机物、细菌总数、重金属离子等也都有详细的要求,这些指标的合格与否直接关系到纯化水是否符合药品生产的要求。
最后,中国药典还规定了纯化水的微生物指标。
微生物的存在会导致纯化水的污染,从而影响药品的质量。
因此,纯化水中的细菌总数、大肠菌群、霉菌和酵母菌等微生物指标也都有具体的要求。
这些要求的制定,旨在保证制药过程中使用的纯化水符合一定的卫生标准,不会对药品的安全性和有效性造成影响。
总的来说,中国药典对纯化水的标准制定得非常严格,这是为了保证药品的质量和安全。
制药企业在生产过程中,应该严格按照这些标准要求来生产和使用纯化水,确保药品的质量符合国家的相关标准,为人们的健康提供保障。
同时,相关部门也应该加强对纯化水质量的监督和检测,确保纯化水的质量符合规定标准。
只有这样,才能保证纯化水在药品生产中的作用得到充分发挥,为人们的健康保驾护航。
纯化水(药典标准)

纯化水Chunhuashui Purified waterH2O 18.02本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【性状】本品为无色的澄清液体;无臭、无味。
【检查】酸碱度取本品10ml加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液〔取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO3)〕0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000 006%)亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)lml与盐酸萘乙二胺溶液(0.1→100)lml,产生的粉红色,与标准亚硝酸盐溶液〔取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释至100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μgNO2 )〕0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(0.000 002%)氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.000 03%)电导率应符合规定(附录ⅧS)总有机碳不得超过0.50mg/l(附录ⅧR)易氧化物取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
纯化水制药用水质标准

纯化水是制药行业常用的水质标准,其制备过程通常包括预处理、反渗透、离子交换、电去离子等步骤。
纯化水的水质标准主要包括以下几个方面:
1. 颜色:无色透明。
2. pH值:5.0-7.5。
3. 电导率:≤1.3μS/cm(25℃)。
4. 硝酸盐:≤0.05mg/L。
5. 砷:≤0.01mg/L。
6. 铅:≤0.01mg/L。
7. 铜:≤0.02mg/L。
8. 硅酸盐:≤0.02mg/L。
9. 微生物指标:细菌总数≤10CFU/mL,霉菌和酵母菌总数≤10CFU/mL,大肠杆菌阴性,金黄色葡萄球菌阴性,铜绿假单胞菌阴性。
10. 热原检查:符合规定。
以上是纯化水制药用水质标准的主要要求。
在实际生产过程中,还需要根据具体药品的生产工艺和质量要求,对水质进行严格控制。
制药用水分类水质标准及检测要求

制药用水分类、水质标准及检测要求制药用水分类及水质标准水是药物生产中用量最大,使用最广的一种原料,用于生产过程及药物制剂的制备,而且生产过程中的用水量很大,其中工艺用水量占相当比例。
水在药品生产中是保证药品质量的关键因素之一,尤其是输液生产中工艺用水显得更为重要。
对于一家申报GMP认证的制药企业,其生产厂房所能达到的洁净级别及制药用水所能达到的标准,是制药企业在GMP认证中将要重点检查的两个主要项目。
制药用水分类制药用水通常可分为:饮用水、纯化水、注射用水。
按《中华人民共和国药典(2023年版)》(以下简称20235中国药典)所收载的制药用水中又另列“杀菌注射用水”一项。
它们的含义是:(1)饮用水(Potab1e-Water):通常为自来水公司供应的自来水,又称原水。
按2000中国药典规定;饮用水不能直接用作制剂和制备或试验用水。
(2)纯化水(PurifideWater):为饮用水经蒸僭法、离子交换法、反渗透法或其他适宜的方法制得的制药用的水,不含任何附加剂。
采用离子交换法、反渗透法、超滤法等非热处理制备的纯化水,一般又称去离子水。
采用特殊设计的蒸储器用蒸储法制备的纯化水,一般又称蒸得水。
纯化水可作为配制普通药物制剂用的溶剂或试验用水,不得用于注射剂的配制。
(3)注射用水(WaterforInjection):是以纯化水作为原水,经特殊设计的蒸馆器蒸储,冷凝冷却后经膜过滤制备而得的水。
目前一般的蒸用器有多效蒸俺水机和气压式蒸用水机等。
经蒸储后的水需再经徽孔过滤方可作注射用水,徽孔过滤膜的孔径应为≤0.45μm.注射用水可作为配制注射剂用的溶剂O(4)灭菌注射用水(SteriIeWaterforInjec-1ion):为注射用水依照注射剂生产工艺制备所得的水。
灭菌注射用水用于灭菌粉末的溶剂或注射液的稀释剂。
制药用水的水质标准1、饮用水:应符合中华人民共和国国家标准《生活饮用水卫生标准》(GB5749-2023)o需定期检测饮用水水质,在当前原水水质遭受有机物等污染日益加剧的情况下,应针对不同的污染物,采取有效措施,不使因饮用水水质波动而影响药品质量。
制药用水的标准和解释说、使用和解释说明
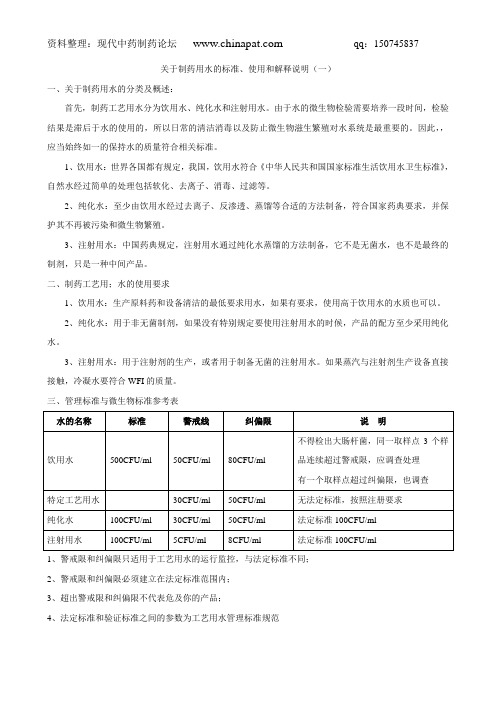
关于制药用水的标准、使用和解释说明(一)一、关于制药用水的分类及概述:首先,制药工艺用水分为饮用水、纯化水和注射用水。
由于水的微生物检验需要培养一段时间,检验结果是滞后于水的使用的,所以日常的清洁消毒以及防止微生物滋生繁殖对水系统是最重要的。
因此,,应当始终如一的保持水的质量符合相关标准。
1、饮用水:世界各国都有规定,我国,饮用水符合《中华人民共和国国家标准生活饮用水卫生标准》,自然水经过简单的处理包括软化、去离子、消毒、过滤等。
2、纯化水:至少由饮用水经过去离子、反渗透、蒸馏等合适的方法制备,符合国家药典要求,并保护其不再被污染和微生物繁殖。
3、注射用水:中国药典规定,注射用水通过纯化水蒸馏的方法制备,它不是无菌水,也不是最终的制剂,只是一种中间产品。
二、制药工艺用;水的使用要求1、饮用水:生产原料药和设备清洁的最低要求用水,如果有要求,使用高于饮用水的水质也可以。
2、纯化水:用于非无菌制剂,如果没有特别规定要使用注射用水的时候,产品的配方至少采用纯化水。
3、注射用水:用于注射剂的生产,或者用于制备无菌的注射用水。
如果蒸汽与注射剂生产设备直接接触,冷凝水要符合WFI的质量。
三、管理标准与微生物标准参考表水的名称标准警戒线纠偏限说明饮用水500CFU/ml 50CFU/ml 80CFU/ml 不得检出大肠杆菌,同一取样点3个样品连续超过警戒限,应调查处理有一个取样点超过纠偏限,也调查特定工艺用水30CFU/ml 50CFU/ml 无法定标准,按照注册要求纯化水100CFU/ml 30CFU/ml 50CFU/ml 法定标准100CFU/ml注射用水100CFU/ml 5CFU/ml 8CFU/ml 法定标准100CFU/ml1、警戒限和纠偏限只适用于工艺用水的运行监控,与法定标准不同;2、警戒限和纠偏限必须建立在法定标准范围内;3、超出警戒限和纠偏限不代表危及你的产品;4、法定标准和验证标准之间的参数为工艺用水管理标准规范以上对于制药工艺用水的初步描述关于制药工艺用水的设计、日常监控、取样、管理、维护等问题将在以后逐步完善请各位批评指正,或登录现代中药制药论坛参与讨论本资料为整理,拥有版权及解释权。
制药用医药用水设备制水标准

制药用医药用水设备制水标准一:制药用水分类及水质标1、制药用水(工艺用水:药品生产工艺中使用的水,包括饮用水、纯化水、注射用水)分类1)饮用水(Potable-Water):通常为自来水公司供应的自来水或深井水,又称原水,其质量必须符合国家标准GB5749-85《生活饮用水卫生标准》。
按2000中国药典规定,饮用水不能直截了当用作制剂的制备或试验用水。
2)纯化水(Purified Water):为原水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用的水、不含任何附加剂。
纯化水可作为配制一般药物制剂的溶剂或试验用水,不得用于注射剂的配制。
采纳离子交换法、反渗透法、超滤法等非热水处理设备的纯化水一样又称去离子水。
采纳专门设计的蒸馏器用蒸馏法制备的纯化水一样又称蒸馏水。
3)注射用水(Water for Injection):是以纯化水作为原水,经专门设计的蒸馏器蒸馏冷凝冷却后经膜过滤制备而得的水。
注射用水可作为配制注射剂用的溶剂。
4)灭菌注射用水(Sterile Water for Injection):为注射用水依照注射剂生产工艺制备所得的水。
灭菌注射用水用于灭菌粉末的溶剂或注射液的稀释剂。
2、制药用水的水质标准1)饮用水:应符合中华人民共和国国家标准《生活饮用水卫生标准》(GB5749-85)2)纯化水:应符合《2000中国药典》所收载的纯化水标准。
在制水工艺中通常采纳在线检测纯化水的电阻率值的大小,来反映水中各种离子的浓度。
制药行业的纯化水的电阻率通常应≥0.5MΩ.CM/25℃,关于注射剂、滴眼液容器冲洗用的纯化水的电阻率应≥1MΩ.CM/25℃。
3)注射用水:应符合2000中国药典所收载的注射用水标准。
二:GMP对制药用水制备装置的要求1、结构设计应简单、可靠、拆装简便。
2、为便于拆装、更换、清洗零件,执行机构的设计尽量采纳的标准化、通用化、系统化零部件。
3、设备内外壁表面,要求光滑平坦、无死角,容易清洗、灭菌。
中华人民共和国药典2000年版对制药用水的要求

中华人民共和国药典2000年版对制药用水的要求一:纯化水:(P344)检查:1酸碱度:取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
2氯化物、硫酸盐与钙盐:取本品,分置三支试管中,每管各50ml第一管中加硝酸5滴与硝酸银试液1ml,第二管中加氯化钡试液2ml,第三管中加草酸铵试液2ml,均不得发生浑浊。
3硝酸盐:取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50oC水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100 ml,再精密量取10 ml加水稀释成100 ml摇匀,即得(每1 ml 相当于1µgNO3)]0.3ml,加无硝酸盐的水4.7 ml,用同一方法处理后的颜色比较,不得更深( 0.000006%)。
4亚硝酸盐:取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml及盐酸萘乙二胺溶液(0.1→100)1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100 ml,摇匀,精密量取1 ml,加水稀释成100 ml,摇匀,再精密量取1 ml,加水稀释成50 ml,摇匀,即得(每1 ml相当于1µgNO2)]0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(0.000002%)。
5氨:取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.00003%)。
6二氧化碳:取本品25ml,置50ml具塞量筒中,加氢氧化钙试液25ml,密塞振摇,放置,1小时内不得发生浑浊。
中国药典(GMP)制药用水要求详解(精选5篇)

中国药典(GMP)制药用水要求详解(精选5篇)第一篇:中国药典(GMP)制药用水要求详解中国药典(GMP)制药用水要求详解制药企业的生产工艺用水,涉及到的是制剂生产过程当中容器清洗、配液及原料药精制纯化等所需要使用的水,此类用水一般分成纯化水和注射用水两大类。
中国药典对此两类制药用水的制备工艺有具体的一个要求。
对于注射用水,中国药典要求使用蒸馏的方法制备,通常是使用多效蒸馏器。
此要求与FDA、UP和JP的要求差别较大,本文在此就不详谈制备方面的差别,下文主要谈一谈中国药典(GMP)对制药用水的各方面要求,尤其对纯化水和注射用水的TOC检测要求.一、同制药用水的用途差别 1.1纯化水的用途:1、制备注射用水(纯蒸汽)的水源2、非无菌药品直接接触药品的设备、器具和包装材料最后一次洗涤用水3、注射剂、无菌药品瓶子的初洗4、非无菌药品的配料5、非无菌药品原料精制 1.2注射用水的的用途1、无菌产品直接接触药品的包装材料最后一次精洗用水2、注射剂、无菌冲洗剂配料3、无菌原料药精制4、无菌原料药直接接触无菌原料的包装材料的最后洗涤用水1.3纯蒸汽的用途1、无菌药品物料、容器、设备、无菌衣或其他物品需进入无菌作业区的湿热无菌处理2、培养基的湿热灭菌二、2010年版中国药典(GMP)对注射用水中总有机碳(TOC)的新要求2.1为什么需要检测总有机碳(TOC)微生物超标纠正标准是指微生物污染达到某一数值,表明注射用水系统已经偏离了正常运行的条件,应采取纠偏措施,使系统回到正常的运行状态。
“热原”通常是由细菌产生的,是那些能致热的微生物的代谢产物,以“细菌内霉素”指标来表示。
大多数细菌和许多霉菌都能产生热,致热能力最强的是革兰阴性杆菌的产物。
微生物代谢产物中的内毒素是造成热原反应的最主要因素。
细菌内毒素耐热性强,其尺寸大小约在1-50μm之间,故可通过一般滤器进入滤液中,但能被活性炭、硅藻土滤器等吸附。
热原本身不挥发,但能在蒸馏时被汽化的水滴带入蒸馏水中。
2020中国药典中纯化水、注射用水和灭菌注射用水的要求

2020中国药典中纯化水、注射用水和灭菌注射用水的要求1. 引言1.1 概述本篇长文旨在探讨2020年中国药典中对纯化水、注射用水以及灭菌注射用水的要求。
随着医疗技术的不断发展和进步,药品生产质量与安全性成为人们关注的焦点。
作为一种广泛应用于制药工业的重要溶剂和辅助原料,水的质量和纯度对药品的质量具有重要影响。
因此,本文将详细介绍纯化水、注射用水以及灭菌注射用水在制药工业中所需符合的标准和规定。
1.2 文章结构本文共分为五个部分。
除了引言外,还包括纯化水、注射用水、灭菌注射用水以及结论部分。
每一部分都将针对相关要求进行详细探讨,并涵盖定义和用途、生产要求以及检测方法等方面内容。
1.3 目的本文的目的是使读者更加全面了解2020年中国药典中关于纯化水、注射用水以及灭菌注射用水的相关要求。
通过阐述这些标准和规定,可以帮助制药企业、研究人员以及相关从业人员加强水质管理,确保药品生产环节中的安全性和可靠性。
同时,读者还能了解到各种水质要求的检测方法,以便合理选择并进行相应检验。
以上是文章“1. 引言”部分的内容。
2. 纯化水的要求:2.1 定义和用途:纯化水是指通过物理、化学及生物学方法处理后符合一定质量标准并适用于药品制造过程中的水。
在药品制造中,纯化水主要用于洗涤、稀释、溶解以及成分调整等工艺步骤中。
它应该没有任何对人体有害的杂质,并且能够满足相应的药典标准。
2.2 生产要求:纯化水的生产过程需要遵循一系列严格的要求。
首先,必须使用适当的设备和工艺进行制备,并确保所有操作都符合卫生标准。
此外,应该采取有效控制措施,例如使用紫外线照射或超滤等方法来消除微生物污染。
同时,在纯化水系统运行期间,需定期监测关键参数,如溶解氧、电导率和总菌落计数等,以确保其达到所需纯度标准。
2.3 检测方法:为了评估纯化水是否符合药典要求,需要进行各项必要的检测。
常见的检测项目包括菌落总数、大肠菌群、重金属含量、有机物含量以及细菌内毒素等。
药品生产纯化水、注射用水验证要求

第三章药品生产纯化水、注射用水(清洁蒸汽)系统的验证标准第一节概述水是药物生产中用量最大、使用最广的一种原料,用于生产过程及药物制剂的制备。
中国药典(年版)中所收载的制药用水,因其使用的范围不同而分为纯化水、注射用水及灭菌注射用水。
制药用水的原水通常为自来水公司供应的自来水或深井水,其质量必须符合中华人民共和国国家标准—《生活饮用水卫生标准》。
原水不能直接用作制剂的制备或试验用水。
纯化水为原水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的供药用的水,不含任何附加剂。
由于各种生产方法存在不同的污染的可能性,因此对各生产装置要特别注意是否有微生物污染,对其各个部位及流出的水应经常监测,尤其是当这些部位停用几小时后再使用时。
纯化水可作为配制普通药物制剂用的溶剂或试验用水,不得用于注射剂的配制。
注射用水为纯化水经蒸馏所得的水,应符合细菌内毒素试验要求。
注射用水必须在防止内毒素产生的设计条件下生产、贮藏及分装。
注射用水可作为配制注射剂用的溶剂。
灭菌注射用水为注射用水照注射剂生产工艺制备所得,主要用于注射用灭菌粉末的溶剂或注射液的稀释剂。
我国《规范》(年修订)规定的工艺用水为药品生产工艺中使用的水,包括饮用水、纯化水、注射用水。
此外工艺用水还有:——第三章药品生产纯化水、注射用水(清洁蒸汽)系统的验证标准初淋水(大容量注射剂规定,菌落数);终淋水(大容量注射剂规定,菌落数);灭菌锅冷却用水(大容量注射剂规定,菌落数);其他用途的软化水、冷却用氨水等。
水处理系统的规模取决于原水水质、生产用水量及工艺对水质的要求,其中原水水质和工艺对水质的要求决定制水流程的繁简,而用水量只决定设备的大小。
一般来说当原水为自来水时,预处理的设备较少,而当工艺对水质的要求较高时,用于去离子、除菌及除微粒的设备较全。
水处理系统动态变化较大,原水几天前的抽样结果往往在几天后是无效的;而另一方面,这些原水却又被用来大批量地生产极其昂贵的药品,因此从某种程度而言,水处理装置又是不可靠的,必须事先进行验证,然后进行日常严密地监测和控制。
制药用水分类及水质标准

制药用水分类及水质标准水是药物生产中用量最大,使用最广的一种原料,用于生产过程及药物制剂的制备,而且生产过程中的用水量很大,其中工艺用水量占相当比例。
水在药品生产中是保证药品质量的关键因素之一,尤其是输液生产中工艺用水显得更为重要。
对于一家申报GMP认证的制药企业,其生产厂房所能达到的洁净级别及制药用水所能达到的标准,是制药企业在GMP认证中将要重点检查的两个主要项目。
一、制药用水分类及水质标准1、制药用水分类制药用水通常可分为:饮用水、纯化水、注射用水。
按《中华人民共和国药典(2000年版)》(以下简称2000中国药典)所收载的制药用水中又另列“杀菌注射用水"一项。
它们的含义是:1.l饮用水(Potable-Water):通常为自来水公司供应的自来水,又称原水。
按2000中国药典规定;饮用水不能直接用作制剂和制备或试验用水。
1.2纯化水(Purifide Water):为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用的水,不含任何附加剂。
采用离子交换法、反渗透法、超滤法等非热处理制备的纯化水,一般又称去离子水。
采用特殊设计的蒸馏器用蒸馏法制备的纯化水,一般又称蒸馏水。
纯化水可作为配制普通药物制剂用的溶剂或试验用水,不得用于注射剂的配制。
1.3注射用水(Water for Injection):是以纯化水作为原水,经特殊设计的蒸馏器蒸馏,冷凝冷却后经膜过滤制备而得的水。
目前一般的蒸馏器有多效蒸馏水机和气压式蒸馏水机等。
经蒸馏后的水需再经徽孔过滤方可作注射用水,徽孔过滤膜的孔径应为≤0.45μm。
注射用水可作为配制注射剂用的溶剂。
1.4 灭菌注射用水(Sterile Water for Injec-tion):为注射用水依照注射剂生产工艺制备所得的水。
灭菌注射用水用于灭菌粉末的溶剂或注射液的稀释剂。
2、制药用水的水质标准2.l 饮用水:应符合中华人民共和国国家标准《生活饮用水卫生标准》(GB5749-85)。
中国药典医药用水标准
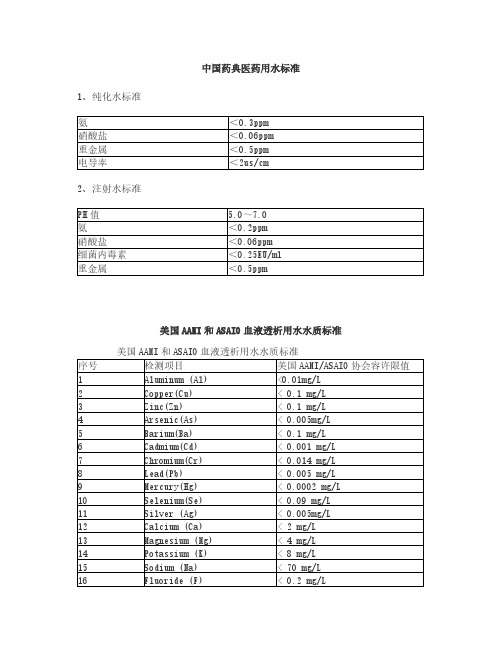
中国药典医药用水标准1、纯化水标准氨<0.3ppm硝酸盐<0.06ppm重金属<0.5ppm电导率<2us/cm2、注射水标准PH值 5.0~7.0氨<0.2ppm硝酸盐<0.06ppm细菌内毒素<0.25EU/ml重金属<0.5ppm美国AAMI和ASAIO血液透析用水水质标准美国AAMI和ASAIO血液透析用水水质标准序号检测项目美国AAMI/ASAIO协会容许限值1 Aluminum (Al) <0.01mg/L2 Copper(Cu) < 0.1 mg/L3 Zinc(Zn) < 0.1 mg/L4 Arsenic(As) < 0.005mg/L5 Barium(Ba) < 0.1 mg/L6 Cadmium(Cd) < 0.001 mg/L7 Chromium(Cr) < 0.014 mg/L8 Lead(Pb) < 0.005 mg/L9 Mercury(Hg) < 0.0002 mg/L10 Selenium(Se) < 0.09 mg/L11 Silver (Ag) < 0.005mg/L12 Calcium (Ca) < 2 mg/L13 Magnesium (Mg) < 4 mg/L14 Potassium (K) < 8 mg/L15 Sodium (Na) < 70 mg/L16 Fluoride (F) < 0.2 mg/L17 Nitrate (NO3) < 2 mg/L18 Sulfate (SO42) < 100 mg/L19 Chlorine (R-Cl2) < 0.5 mg/L20 Chloramines(X-NH2) < 0.1 mg/L21 Culture/colony count < 100 CFU/mLAAMI Maximum Allowable Levels of Contaminants in waterAAMI允许肾透析水中最大杂质含量(肾透析水质要求标准)级别Contaminant AAMI Maximum for Dialysis Water (mg/L)(AAMI 1993)Calcium(钙)2(0.1 mEq/L)Magnesium(镁)4(0.3 mEq/L) Sodium(钠)70(3.0 mEq/L) Potassium(钾)8(0.2 mEq/L) Fluoride(氟)0.2 Chlorine(氯)0.5 Chloramine(氯胺)0.1 Nitrate(硝酸盐)2 Sulfate(硫酸盐)100 Copper(铜)0.1 Barium(钡)0.1Zinc(锌)0.1 Aluminum(铝)0.01 Arsenic(砷)0.005 Lead(铅)0.005 Silver(银)0.005 Cadmium(镉)0.001 Chromium(铬) 0.014 Selenium(硒)0.09 Mercury(汞)0.0002细菌含量<200cfu/ml专业词汇:BOD生化需氧量又称生化耗氧量,英文(biochemical oxygen demand)缩写BOD,表示水中有机物等需氧污染物质含量的一个综合指标,它说明水中有机物出于微生物的生化作用进行氧化分解,使之无机化或气体化时所消耗水中溶解氧的总数量,其单位以ppm(毫克/升)表示。
纯化水水质标准

纯化水水质标准
纯化水水质标准主要包括以下几个方面:
1. 化学指标:纯化水应符合中华人民共和国药典2010版制药纯化水要求。
电导率应控制在2S/cm(电阻率0.5M Ω·cm),总有机碳(TOC)应达到较低水平。
2. 卫生学检查:微生物含量应控制在10CFU/100ml,内毒素含量应小于0.25EU/ml。
3. 酸碱度:纯化水的酸碱度应在一定范围内。
取10ml 纯化水,加入甲基红指示液2滴,不得显红色;另取10ml,加入溴麝香草酚蓝指示液5滴,不得显蓝色。
4. 硝酸盐:取5ml纯化水,加入10%氯化钾溶液0.4ml 与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50-65℃水浴中加热15分钟,冷却后,溶液颜色不得深于标准硝酸盐溶液。
5. 重金属:纯化水中的重金属含量应控制在0.5g/ml 以下。
此外,生物工程用纯化水的水质标准还包括:电阻率0.5MΩ·cm,氨0.3g/ml,硝酸盐0.06g/ml,重金属0.5g/ml 等。
需要注意,不同领域和应用场景对纯化水的水质标准可能有所不同,例如制药、食品加工、化妆品生产等。
因此,在实际应用中,要根据具体行业和需求来确定纯化水的水质标准。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
中国药典纯化水(制药用水)标准
本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【总有机碳】不得过0.50mg/L。
【易氧化物】取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
以上总有机碳和易氧化物两项可选做一项。
【重金属】取本品100ml,加水19ml,蒸发至20ml,放冷,加醋酸盐缓冲液(pH3.5)2ml与水适量使成25ml,加硫代乙酰胺试液2ml,摇匀,放置2分钟,与标准铅溶液1.0ml加水19ml用同一方法处理后的颜色比较,不得更深(0.000 01%)。
【电导率】应符合规定(附录)
【铝盐】(供透析液生产用水需检查)
取本品400ml,置分液漏斗中,加醋酸盐缓冲液(pH 6.0)10ml和水100ml ,用0.5% 8-羟基喹啉三氯甲烷溶液提取3次(20ml,20ml,10ml),合并三氯甲烷提取液于50ml量瓶中,加三氯甲烷至刻度,摇匀,即得供试品溶液;另取标准铝盐溶液[称取硫酸铝钾0.352g,置100ml量瓶中,加1mol/L硫酸溶液10ml溶解后,用水稀释至刻度,摇匀,作为贮备液。
临用前,精密量取贮备液1ml,置100ml量瓶中,用水稀释至刻度,摇匀,即得(每1ml相当于2μg的Al)]2.0ml,置分液漏斗中,加醋酸盐缓冲液(pH 6.0)10ml和水98ml,同法操作,即得标准溶液;取醋酸盐缓冲液(pH 6.0)10ml和水100ml,置分液漏斗中,同法操作,作为空白溶液。
取上述溶液,照荧光分析法(附录ⅣE),在激发光波长392nm与发射光波长518nm处分别测定荧光强度。
供试品溶液的荧光强度不得大于标准溶液的荧光强度(0.000 001%)。
