金属的电化学腐蚀与防护习题
高二化学重难点训练金属的电化学腐蚀与防护试题及答案

金属的电化学腐蚀与防护一、选择题(每小题只有一个正确选项,共10*6 分)1.(2020 江苏高考真题)将金属M 连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。
在题图所示的情境中,下列有关说法正确的是A.阴极的电极反应式为Fe - 2e-= Fe2+B.金属M 的活动性比Fe 的活动性弱C.钢铁设施表面因积累大量电子而被保护D.钢铁设施在河水中的腐蚀速率比在海水中的快【答案】C【解析】该装置为原电池原理的金属防护措施,为牺牲阳极的阴极保护法,金属 M 作负极,钢铁设备作正极。
A.阴极的钢铁设施实际作原电池的正极,正极金属被保护不失电子,故 A 错误;B.阳极金属 M 实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,因此 M 活动性比 Fe 的活动性强,故 B 错误;C.金属M 失电子,电子经导线流入钢铁设备,从而使钢铁设施表面积累大量电子,自身金属不再失电子从而被保护,故C 正确;D.海水中的离子浓度大于河水中的离子浓度,离子浓度越大,溶液的导电性越强,因此钢铁设施在海水中的腐蚀速率比在河水中快,故D 错误;故选:C。
2.下列有关钢铁腐蚀与防护的说法正确的是()A.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用B.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法C.钢铁发生析氢腐蚀时,负极反应式Fe-3e-=Fe3+D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀【答案】B【解析】A、根据金属活动顺序表,铁比 Sn 活泼,镀层破损后,构成原电池,铁作负极,Sn 为正极,加速铁制品腐蚀,故A 错误;B、锌比铁活泼,锌作负极,铁作正极,铁被保护起来,这种方法称为牺牲阳极的3- -2 2 23 阴极保护法,故 B 正确;C 、钢铁发生吸氢腐蚀时,负极反应式为 Fe -2e -=Fe 2+,故 C 错误;D 、根据电解池的原理,如果活动性金属作阳极,活动性金属先失电子,加速腐蚀,因此输油钢管与外加直流电源的负极相连,故 D 错误;答案选 B 。
金属的电化学腐蚀与防护测试题(含答案)

金属的电化学腐蚀与防护测试题(含答案)《金属的电化学腐蚀与防护》一、选择题 1. 为了防止钢铁锈蚀,下列防护方法中正确的是 A. 在精密机床的铁床上安装铜螺钉 B. 在排放海水的钢铁阀门上用导线连接一块石墨,一同浸入海水中 C. 在海轮舷上用铁丝系住锌板浸在海水里 D. 在地下输油的铸铁管上接直流电源的负极 2. 以下现象与电化学腐蚀无关的是 A. 黄铜(铜锌合金)制作的铜锣不易产生铜绿 B. 生铁比软铁芯(几乎是纯铁)容易生锈 C. 铁制器件附有铜制配件,在接触处易生铁锈 D. 银制奖牌久置后表面变暗 3. 埋在地下的铸铁输油管道,在下列各种情况下被腐蚀的速度最慢的是 A. 在含铁元素较多的酸性土壤中 B. 在潮湿疏松透气的土壤中 C. 在干燥致密不透气的土壤中 D. 含碳粒较多、潮湿透气的中性土壤中 4. 下列各方法中能对金属起到防止或减缓腐蚀作用的是①金属表面涂抹油漆②改变金属的内部结构③保持金属表面清洁干燥④在金属表面进行电镀⑤使金属表面形成致密的氧化物薄膜 A.①②③④ B.①③④⑤ C.①②④⑤ D.全部 5. 下列对金属及其制品的防护措施中,错误的是 A. 铁锅用完后,用水刷去其表面的油污,置于潮湿处 B. 通过特殊工艺,增加铝制品表面的氧化膜 C. 对于易生锈的铁制品要定期刷防护漆 D. 把Cr、Ni等金属加入到普通钢里制成不锈钢 6. 为研究金属腐蚀的条件和速率,某课外小组学生用金属丝将三根大小相同的铁钉分别固定在图示的三个装置中,再放置于玻璃钟罩里保存一星期后,下列对实验结束时现象描述不正确的是 A.装置Ⅰ左侧的液面一定会上升 B.左侧液面装置Ⅰ比装置Ⅱ的低 C.装置Ⅱ中的铁钉腐蚀最严重 D.装置Ⅲ中的铁钉几乎没被腐蚀 7. 下列关于金属腐蚀正确的是: A. 金属在潮湿的空气中腐蚀的实质是:M + n H2O === M(OH)n + n/2 H2↑ B. 金属的化学腐蚀的实质是:M �C ne- = Mn+ ,电子直接转移给氧化剂 C. 金属的化学腐蚀必须在酸性条件下进行 D. 在潮湿的中性环境中,金属的电化学腐蚀主要是吸氧腐蚀 8. 随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提上议事日程,其首要原因是 A.利用电池外壳的金属材料 B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 C.不使电池中渗泄的电解液腐蚀其他物品 D.回收其中石墨电极 9. 将金属A和金属B分别放入稀H2SO4中均有氢气生成.若将金属A和金属B相连后投入稀H2SO4中发现A被腐蚀;B未被腐蚀.关于B的叙述正确的是 A.金属活动性A>B B.还原性B>A C.在后者装置中金属A发生还原反应,金属B发生氧化反应 D.金属B的表面上明显有气泡产生,金属A表面无明显现象 10.铜片和锌片用导线连接后插入稀硫酸中,锌片是 A.阴极B.正极 C.阳极D.负极 11.下列叙述中不正确的是 A.金属的电化腐蚀比化学腐蚀普遍 B.钢铁在干燥空气里不易腐蚀 C.用铝质铆钉铆接铁板,铁板易被腐蚀 D.原电池中电子由正极流入负极 12.分别放置在图所示装置(都盛有0.1 mol•L-1的H2SO4溶液)中的四个相同的纯锌片,腐蚀最快的是 13.下列过程中,需要通电后才能进行的是①电离②电解③电镀④电泳⑤电化腐蚀 A.①②③ B.②③④ C.②④⑤ D.全部 14.用下列实验装置进行的实验中,能达到相应实验目的的是A.装置甲:防止铁钉生锈B.装置乙:除去乙烯中混有的乙炔C.装置丙:验证HCl气体在水中的溶解性D.装置丁:实验室制取乙酸乙酯15.在通常条件下,下列各组物质的性质排列正确的是①熔点:钾钠合金<钾 <钠② 沸点:己烷>戊烷>2-甲基丁烷③ 密度:苯<水<1,1,2,2-四溴乙烷④ 硬度:镁 < 铝 < 镁铝合金⑤ 在潮湿空气中铁的腐蚀速率:生铁 > 纯铁 > 铁锌合金 A.①②③④⑤B.①③④⑤ C.③④⑤ D.以上组合均不正确 16.下列叙述的方法不正确的是 A.金属的电化学腐蚀比化学腐蚀更普遍 B.用铝质铆钉铆接铁板,铁板易被腐蚀 C.钢铁在干燥空气中不易被腐蚀 D.用牺牲锌块的方法来保护船身 17.钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2 = 2Fe2++4OH-。
高三化学金属的电化学腐蚀与防护试题

高三化学金属的电化学腐蚀与防护试题1.食品包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。
下列分析正确的是A.脱氧过程是吸热反应,可降低温度,延长食品保质期B.脱氧过程中铁作原电池正极,电极反应为:Fe-3e-=Fe3+C.脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e-=4OH-D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)【答案】A【解析】脱氧原理与钢铁的吸氧腐蚀相类似,故铁做负极,发生氧化反应生成亚铁离子,1.12g铁的物质的量为0.02mol,失去0.04mol电子,碳做正极,氧气发生还原反应,氧气若得到0.04mol电子,氧气的物质的量为0.01mol,标况下的体积为224mL,B、C、D均错误;故选A。
【考点】吸氧腐蚀的原理与氧化还原的相关计算2.下图是研究铁钉腐蚀的装置图,下列说法不正确的是A.铁钉在两处的腐蚀速率:a < bB.a、b两处铁钉中碳均正极C.a、b两处铁钉中的铁均失电子被氧化D.a、b两处的正极反应式均为O2+4e-+4H+ ===2H2O【答案】D【解析】A、b中的氢离子浓度较大,所以腐蚀速率b>a,正确;B、ab中都发生原电池反应,铁钉中的碳作正极,铁作负极,正确;C、铁作负极,发生氧化反应,失电子,正确;D、a中发生吸氧腐蚀,正极反应是O2+4e-+2H2O ="4" OH-;b中发生析氢腐蚀,正极反应是2H++2e-==H2↑;错误,答案选D。
【考点】考查金属腐蚀的种类及正负极的判断,电极反应式的书写判断3.下列说法正确的是A.工业上常通过电解熔融的MgO冶炼金属镁B.合金的硬度一般比其成分金属的硬度大C.钢铁发生吸氧腐蚀时,正极反应是4OH--4e-=2H2O+O2↑D.在铁上镀铜,应选用铜作阴极【答案】B【解析】A、氧化镁的熔点高熔融需要消耗大量的能源,因此工业上常通过电解熔融的氯化镁冶炼金属镁,A不正确;B、合金的硬度一般比其成分金属的硬度大,B正确;C、钢铁发生吸氧腐蚀时,正极反应是O2+4e-+2H2O=4OH-,C不正确;D、在铁上镀铜,应选用铜作阳极,铁做阴极,硫酸铜溶液作电镀液,D不正确,答案选B。
高二化学金属的电化学腐蚀与防护试题答案及解析

高二化学金属的电化学腐蚀与防护试题答案及解析1.下列物质的说法正确的是A.芳香烃可以来自于煤干馏产品中的煤焦油B.聚氯乙烯可用于制作食品包装袋C.镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀D.在铁的吸氧腐蚀中,负极是炭,电极反应为2H2O+O2+4eˉ=" 4OHˉ"【答案】A【解析】B聚氯乙烯是有毒物,C锌比铁活泼,可以起到保护铁的作用,而锡的活泼性比铁弱,不能起到保护铁作用。
D铁是负极,碳是正极。
所以答案选A【考点】考查化学的基本概念和基本理论的相关知识点2.如下图各烧杯中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )A.④>②>①>③B.②>①>③>④C.④>②>③>①D.③>②>④>①【答案】A【解析】以①作参照物,进行比较。
在②中构成了原电池。
由于活动性Fe>Sn,所以Fe作负极,加快了Fe的腐蚀,因此②>①,在③中构成了原电池。
由于活动性Zn>Fe,所以Zn作负极,首先被腐蚀的的是Zn Fe得到了保护,腐蚀比原来慢。
因此腐蚀速率①>③。
④构成的是电解池,Fe是活性电极。
由于Fe与电源的正极连接,作阳极,发生反应:Fe-2e-=Fe2+.腐蚀的速率比作原电池的负极还要快。
因此腐蚀速率④>②。
所以铁在其中被腐蚀时由快到慢的顺序是④>②>①>③。
选项为A。
【考点】考查铁在不同情况下被腐蚀的快慢的顺序的知识。
3. [双选题]下列说法正确的是()A.钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀B.原电池反应是导致金属腐蚀的主要原因,故不能用原电池原理来减缓金属的腐蚀C.钢铁电化学腐蚀的两种类型主要区别在于水膜的酸性不同,引起的正极反应不同D.无论哪种类型的腐蚀,其实质都是金属被氧化【答案】CD【解析】金属的腐蚀就是金属失电子被氧化的过程,因此D正确;析氢腐蚀和吸氧腐蚀是由于水膜酸性不同,正极反应就不同,C正确;原电池反应既可以加快金属的腐蚀,也可用于防止金属的腐蚀,如轮船外壳镶嵌锌块;不锈钢、镀锌铁等中的Fe均不易被腐蚀,A、B不正确。
人教版高二化学第一学期第四章电化学基础第四节金属的电化学腐蚀与防护课后练习
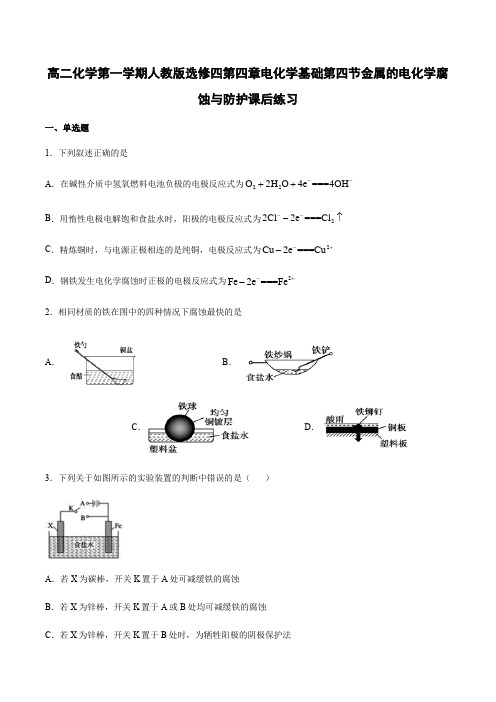
高二化学第一学期人教版选修四第四章电化学基础第四节金属的电化学腐蚀与防护课后练习一、单选题1.下列叙述正确的是A .在碱性介质中氢氧燃料电池负极的电极反应式为22O 2H O 4e ===4OH --++B .用惰性电极电解饱和食盐水时,阳极的电极反应式为22Cl 2e Cl ===---↑C .精炼铜时,与电源正极相连的是纯铜,电极反应式为2===Cu 2e Cu -+-D .钢铁发生电化学腐蚀时正极的电极反应式为2===Fe 2e Fe -+-2.相同材质的铁在图中的四种情况下腐蚀最快的是A .B .C .D . 3.下列关于如图所示的实验装置的判断中错误的是( )A .若X 为碳棒,开关K 置于A 处可减缓铁的腐蚀B .若X 为锌棒,开关K 置于A 或B 处均可减缓铁的腐蚀C .若X 为锌棒,开关K 置于B 处时,为牺牲阳极的阴极保护法D.若X为碳棒,开关K置于B处时,铁电极上发生的反应为2H++2e-=H2↑4.下列有关金属的腐蚀和防护说法正确的是A.当镀锡铁皮的镀层破损时,减慢铁的腐蚀速率B.钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀C.石油管道常常通过连接一块锌块以达到防腐的作用D.将青铜器放在银质托盘上可以避免铜绿的生成5.控制反应速率使其有利于我们的生活生产,其中理解不正确的是A.铁质水桶表面镀锡,可以减缓水桶生锈B.工业合成氨中使用铁触媒做催化剂可以加快反应速率C.放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关D.工业生产中,将矿石粉碎进行煅烧不会加快反应速率6.下列有关金属腐蚀的说法正确的是A.电化学腐蚀是在外加电流作用下不纯金属发生化学反应被损耗的过程B.金属的电化学腐蚀和化学腐蚀本质相同,但电化学腐蚀伴有电流产生C.钢铁腐蚀最普遍的是吸氧腐蚀,负极吸收氧气,产物最终转化为铁锈D.镀锌的铁板比镀锡的铁板更容易被腐蚀7.下列说法正确的是A.Na2O2在空气中久置,因分解成Na2O 和O2而变成白色固体B.接触室里面采用粗管里面嵌套细管,主要为了增大接触面积,加快反应速率C.电热水器用镁棒防止金属内胆腐蚀,原理是外加电源的阴极保护法D.稀有气体比较稳定,只能以单质形式存在8.下列说法正确的是( )A.钢铁设施在河水中的腐蚀速率比在海水中的快B.H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ·mol-1,可知:含1molCH3COOH的溶液与含1molNaOH的溶液混合,放出热量等于57.3kJC.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不相同D.升高温度,一般可使活化分子的百分数增大,因而反应速率增大9.下列叙述正确的是()A.为保护钢闸门,应将钢闸门与外接电源的正极相连B.氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH-C.若要在银上镀铜,与负极相连的一极是银,电解质溶液可以是氯化铜溶液D.钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+10.将金属M 连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。
4.4金属的电化学腐蚀与防护(练习)(解析版)

4.4 金属的电化学腐蚀与防护1.(福建省永泰县第一中学2019-2020学年高二上学期期中考试)下列化学用语或说法正确的是()A .用铁作阳极电解熔融Al 2O 3生产金属铝B .钢铁吸氧腐蚀的正极反应:--22O +2H O+4e =4OHC .粗铜(含Zn 、Fe 、Ag 、Au 杂质)精炼阳极泥的成分只有AuD .石墨作电极电解饱和食盐水:+222H +Cl Cl + H 通电【答案】B【解析】A 、用铁作阳极电解熔融Al 2O 3,阳极反应式为:Fe -2e -=Fe2+,电极被损耗,不符合生产实际,故A 错误;B 、钢铁吸氧腐蚀的正极发生还原反应,其电极反应式为:O 2+2H 2O +4e -=4OH -,故B 正确;C 、粗铜(含Zn 、Fe 、Ag 、Au 杂质)精炼阳极泥的成分主要为失电子能力比铜弱的金属(Au 、Ag 等),故C 错误;D 、石墨作电极电解饱和食盐水,阳极上是Cl -失去电子生成Cl 2,阴极为水电离出的H +得到电子,其电解总反应为:2Cl -+2H 2O H 2↑+Cl 2↑+2OH -,故D 错误。
2.(江苏省邗江中学2019-2020学年高二上学期期中考试)下列叙述正确的是()①锌跟稀硫酸反应制H 2,加入少量硫酸铜溶液能加快反应速率②镀层破损后,白口铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀③电镀时,应把镀件置于电解槽的阴极④冶炼铝时,把氧化铝加入液态冰晶石中熔融后电解⑤钢铁表面常易腐蚀生成Fe 2O 3·nH 2OA.全部B.①③④⑤C.①②⑤D.②④【答案】B【解析】Zn+Cu=Cu+Zn,形成原电池,加快反①锌与硫酸铜溶液发生置换反应,其离子反应方程式为:2+2+应速率,①正确;②金属活动性:Zn>Fe>Sn,镀层破损后,白口铁(镀锌的铁)中Zn为原电池的负极,仍能保护Fe,而马口铁(镀锡的铁)中Fe为原电池的负极,加快Fe的腐蚀,马口铁(镀锡的铁)比白口铁(镀锌的铁)更易腐蚀,②错误;③电镀时,镀件金属为电解池的阴极,镀层金属为电解池的阳极,在阴极上析出镀层金属,③正确;Na AlF)熔融后电④冶炼金属铝,电解熔融的氧化铝,为了降低其熔点,氧化铝加入液态冰晶石(36解;④正确;⑤钢铁表面常因发生原电池而被腐蚀,由于Fe比杂质C活泼,所以Fe作原电池的负极被氧化,最终Fe O nH O),⑤正确。
高三化学金属的电化学腐蚀与防护试题答案及解析

高三化学金属的电化学腐蚀与防护试题答案及解析1.一定条件下,碳钢腐蚀与溶液pH的关系如下:A.在pH<4溶液中,碳钢主要发生析氢腐蚀B.存pH>6溶液中,碳钢主要发生吸氧腐蚀C.在pH>14溶液中,碳钢腐蚀的正极反应为O2+4H++4e-=2H2OD.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减缓【答案】C【解析】A、酸性条件下,碳钢发生析氢腐蚀,Fe-2e-= Fe2+,正确;B、当pH>6溶液中,碳钢主要发生吸氧腐蚀,负极电极反应式为:Fe-2e-=Fe2+,正极上电极反应式为:O2+2H2O+4e-=4OH-,正确;C.在pH>14溶液中,碳钢腐蚀的正极反应O2+2H2O+4e-=4OH-,错误;D.在煮沸除氧气后的碱性溶液中,正极上氧气生成氢氧根离子速率减小,所以碳钢腐蚀速率会减缓,正确,答案选C。
【考点】考查金属的电化学腐蚀的种类与发生条件的判断2.铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如下。
下列说法不正确的是A.因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀B.若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小C.铜极上的反应是2H+ + 2e- ="=" H2↑,O2+ 4e- + 4H+ ="=" 2H2OD.在金属表面涂一层油脂,能防止铁铆钉被腐蚀【答案】B【解析】A、因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀,正确;B、若水膜中溶解了SO2,使溶液酸性增强,氢离子浓度增大,则铁铆钉腐蚀的速率变大,错误;C、从图中可看出,铁同时发生析氢和吸氧腐蚀,铜极是正极,发生的反应是2H+ + 2e- ="=" H2↑,O2+ 4e- + 4H+ ="="2H2O ,正确;D、在金属表面涂一层油脂,隔绝氧气,能防止铁铆钉被腐蚀,正确,答案选B。
【考点】考查金属腐蚀原理及防护3.下列说法不正确的是:A.通过煤的干馏可获得苯、甲苯等芳香烃B.在海轮外壳装上锌块,可减缓船体的腐蚀速率C.电渗析法、离子交换法中,只有后者可以应用于海水的淡化D.我国城市推广使用清洁燃料是压缩天然气类和液化石油气类【答案】C【解析】A、煤干馏可得煤焦油,煤焦油中含有苯、甲苯等芳香烃,正确;B、在海轮外壳装上锌块,形成原电池时,Zn为负极,Fe为正极,可减缓船体的腐蚀速率,正确;C、电渗析法、离子交换法都可用于海水的淡化,错误;D、压缩天然气类主要成分是甲烷,液化石油气主要成分是丙烷、丙烯、丁烷、丁烯,燃烧时产生污染物较少,是我国城市推广使用的清洁燃料,正确。
高二化学金属的电化学腐蚀与防护试题

高二化学金属的电化学腐蚀与防护试题1.为防止钢铁锈蚀,下列防护方法中正确的是( )A.在精密机床的铁床上安装铜螺钉B.在排放海水的钢铁阀门上用导线连接一块石墨,一同浸入海水中C.在海轮舷上用铁丝系住锌板浸在海水里D.在电动输油管的铸铁管上接直流电源的正极【答案】C【解析】A、B中形成原电池都是铁作负极,加速铁的腐蚀;D中铸铁管作阳极,加速腐蚀;C中锌比铁活泼,铁作正极,受到保护。
2.下图所示各烧杯中盛有海水,铁在其中被腐蚀的速率由快到慢的顺序为()。
A.⑤②①③④B.④③①②⑤C.⑤④②①③D.③②④①⑤【答案】C【解析】判断金属腐蚀快慢,首先判断该金属是充当原电池还是电解池的电极,若是电解池的阳极,金属腐蚀速率最快,其次是充当原电池的负极腐蚀较快,而作为电解池的阴极和原电池的正极不被腐蚀。
其中第⑤,Fe作为电解池的阳极,腐蚀最快,②③④均为原电池,第③中,Fe为正极,不被腐蚀,②④中Fe均为负极被腐蚀,Fe和Cu的金属活动性差别较Fe和Sn大,④中铁腐蚀较快,其腐蚀速率由快到慢的顺序为⑤④②①③。
3.下列防腐措施中,属于化学保护法的为 ()。
A.用氧化剂使金属表面生成致密稳定的氧化物保护膜B.在金属中加入一些铬或镍制成合金C.在轮船的船壳吃水线以下部分,装上锌块D.金属表面喷漆【答案】A【解析】化学保护法,指的是通过化学反应,阻止进一步被腐蚀。
B选项是改变了物质的内部结构;C选项是牺牲阳极的阴极保护法;D选项是利用隔离层隔绝空气。
4.下图各烧杯中盛有海水,铁(含杂质C)在其中被腐蚀由快到慢的顺序为【答案】B【解析】①第一个是正常的腐蚀;②形成原电池,锌作电池的负极,铁就受到保护;③形成原电池,铁作负极,腐蚀加剧;④外加电源促进铁的溶解,这个装置腐蚀最历害;⑤外加电源对铁起到了保护作用。
最不易被腐蚀。
因此选B。
【考点】考查金属的腐蚀。
5.钢铁发生电化腐蚀时,正极上发生的反应是A.2H++2e-=H2↑B.2H2O+O2+4e-=4OH-C.Fe-2e-=Fe2+D.4OH--4e-=O2↑+2H2O【答案】B【解析】原电池中较活泼的金属做负极,失去电子发生氧化反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
金属的电化学腐蚀与防护习题集团文件版本号:(M928-T898-M248-WU2669-I2896-DQ586-M1988)训练5 金属的电化学腐蚀与防护一、金属的腐蚀1.关于金属腐蚀的叙述中,正确的是( ) A .金属被腐蚀的本质是M +n H 2O===M(OH)n +n 2H 2↑ B .马口铁(镀锡铁)镀层破损后被腐蚀时,首先是镀层被氧化C .金属在一般情况下发生的电化学腐蚀主要是吸氧腐蚀D .常温下,置于空气中的金属主要发生化学腐蚀2.下列事实与电化学腐蚀无关的是( )A .光亮的自行车钢圈不易生锈B .黄铜(Cu 、Zn 合金)制的铜锣不易生锈C .铜、铝电线一般不连接起来作导线D .生铁比熟铁(几乎是纯铁)容易生锈3.出土的锡青铜(铜锡合金)文物常有Cu 2(OH)3Cl 覆盖在其表面。
下列说法不正确的是( )A .锡青铜的熔点比纯铜低B .在自然环境中,锡青铜中的锡可对铜起保护作用C .锡青铜文物在潮湿环境中的腐蚀比干燥环境中快D .生成Cu 2(OH)3Cl 覆盖物是电化学腐蚀过程,但不是化学反应过程二、铁的析氢腐蚀和吸氧腐蚀4.下列关于钢铁的析氢腐蚀的说法中正确的是( )A .铁为正极B .碳为正极C .溶液中氢离子浓度不变D .析氢腐蚀在任何溶液中都会发生5.在铁的吸氧腐蚀过程中,下列5种变化可能发生的是( )①Fe 由+2价转化成+3价 ②O 2被还原 ③产生H 2 ④Fe(OH)3失水形成Fe 2O 3·x H 2O ⑤杂质C 被氧化除去A .①②④B .③④C .①②③④D .①②③④⑤6.钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为2Fe +2H 2O +O 2===2Fe(OH)2。
以下说法正确的是( )A .负极发生的反应为Fe -2e -===Fe 2+B.正极发生的反应为2H2O+O2+2e-===4OH-C.原电池是将电能转变为化学能的装置D.钢柱在水下部分比在空气与水交界处更容易腐蚀7.如图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。
下列有关描述错误的是( )A.生铁块中的碳是原电池的正极B.红墨水水柱两边的液面变为左低右高C.两试管中相同的电极反应式是Fe-2e-===Fe2+D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀三、金属的防护方法8.下列金属的防护方法不正确的是( )A.对健身器材涂油漆以防止生锈B.对某些工具的“机械转动部位”选用刷油漆的方法来防锈C.用牺牲锌块的方法来保护船体D.自行车的钢圈上镀上一层Cr防锈9.下列举措不能防止或减缓钢铁腐蚀的是( )A.在钢铁制品表面镀一层金属锌B.将钢铁制品放置在潮湿处C.在钢铁中加入锰、铬等金属,以改变钢铁结构D.将钢铁制品与电源负极相连10.为了防止钢铁锈蚀,下列防护方法中正确的是( )A.在精密机床的铁床上安装铜螺钉B.在排放海水的钢铁阀门上用导线连接一块石墨,一同浸入海水中C.在海轮舷上用铁丝系住锌板浸在海水里D.在地下输油的铸铁管上接直流电源的正极11.镁、铝、铁是重要的金属,在工业生产中用途广泛。
(1)镁与稀硫酸反应的离子方程式为________________________________________________________________________________________________________ ____________。
(2)铝与氧化铁发生铝热反应的化学方程式为_________________________________________________________________________________________________ ____________。
(3)在潮湿的空气里,钢铁表面有一层水膜,很容易发生电化学腐蚀。
其中正极的电极反应式为_____________________________________________________________ _______。
(4)在海洋工程上,通常用铝合金(Al-Zn-Cd)保护海底钢铁设施,其原理如图所示:其中负极发生的电极反应为___________________________________________________;在实际应用中,用铝合金而不选用纯铝,纯铝不能很好地起到保护作用,其原因是_____________________________________________________________ _______________________________________________________________________ ____________。
12.对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:铝材脱脂, 碱洗,水洗,除灰,电解H2SO4溶液耐蚀铝材废电解液槽液①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是_____________________________________________________________ ___________(用离子方程式表示)。
为将碱洗后槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的________。
a.NH3b.CO2c.NaOH d.HNO3②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极的电极反应式为_____________________________________________________________ ___________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是______________________________________________________________________________ ______________。
(3)利用右图装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应置于处。
若X为锌,开关K置于M处,该电化学防护法称为________________________________________________________________________。
13.钢铁工业是国家工业的基础,请回答钢铁腐蚀与防护过程中的有关问题。
(1)生产中可用盐酸来除铁锈。
现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式是______________________________________________________________________。
(2)下列哪个装置可防止铁棒被腐蚀________。
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。
装置示意图如右:①A电极对应的金属是(写元素名称),B电极的电极反应式是___________________________________________________________。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为 5.12 g,则电镀时电路中通过的电子为mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因:_____________________________________________________________ _______________________________________________________________________ ____________。
14.如何防止铁的锈蚀是工业上研究的重点内容。
为研究铁锈蚀的影响因素,某同学做了如序号内容实验现象1常温下将铁丝放在干燥空气中一个月干燥的铁丝表面依然光亮2常温下将铁丝放在潮湿空气中一小时铁丝表面依然光亮3常温下将铁丝放在潮湿空气中一个月铁丝表面已变得灰暗4将潮湿的铁丝放在常温的氧气流中一小时铁丝表面略显灰暗5将潮湿的铁丝放在高于常温的氧气流中一小时铁丝表面已变得灰暗6将浸过氯化钠溶液的铁丝放在高于常温的氧气流中一小时铁丝表面灰暗程度比实验5严重回答以下问题:(1)上述实验中发生了电化学腐蚀的是(填实验序号)____________;在电化学腐蚀中,负极反应是_____________________________________________________________ ______;正极反应是_____________________________________________________________ ____;(2)由该实验可知,可以影响铁锈蚀速率的因素是___________________________________________________________________________________________ ____________;(3)为防止铁的锈蚀,工业上普遍采用的方法是____________________________________________________________________________________________ ____________(答两种方法)。
15.某研究小组对铁生锈进行研究。
(1)甲同学设计了A、B、C一组实验(如图),探究铁生锈的条件。
经过较长时间后,甲同学观察到的现象是A中铁钉生锈;B中铁钉不生锈;C中铁钉不生锈。
①通过上述实验现象分析,可得出铁生锈的外部条件是____________________________________________________________ ____________;②铁钉发生电化学腐蚀的正极电极反应式为__________________________________________________________________________________________________ ___________;③实验B所用的水要经过__________处理;植物油的作用是____________________________________________________________________;④实验C中碱石灰的作用是____________________________________________________ ____________________。
(2)乙同学为了达到同样目的,设计了实验D(如图),发现一段时间后,试管中的液面升高,其原因是___________________________________________________________ ____________________________________________________________ ____________,该实验________(填“能”或“不能”)说明水对铁钉生锈产生影响。
