有机化学芳烃芳香性
有机化学-芳香烃

CH3
HNO3
HOAc
CH3
CH3 CH3
NO2 +
+
NO2
NO2
63% 34% 3%
Cl
Cl
Cl
Cl
HNO3
H2SO4
NO2 +
+ NO2
30%
NO2
69% 1%
(2) 第二类定位基─间位定位基
使新进入苯环的取代基主要进入它的 间位,并使苯环致钝。
例如: −CF3, −N(CH3)3+, −NO2, −CN, −SO3H, −CHO, −COCH3, −COOH, −COOCH3, −CONH2, −NH3+。
NO2
NO2
CH3 C CH3 CH3 无 α-H
KMnO4 H+
COOH
氧化剂: KMnO4 铬酸等
4.2.4 苯环上亲电取代反应的定位规则
Y
一取代苯:
芳环上的取代基既影响亲电 取代反应的速率又决定着亲电试 剂进入芳环的位置。
1. 两类定位基
芳环上的取代基分为两类:
(1)第一类定位基 ─ 邻、对位定位基 使得新进入苯环的取代基主要进入它的
均化,闭合共轭
苯
苯的分子结构 体系(环状大π键)
6 个C–C σ键: sp2–sp2相互交盖,6 个C –H σ键: sp2–1s 相互交盖。 6 个2p 轨道的对称轴垂直于环所在平面, 彼此相互平行,两侧进行侧面交盖,形成闭合的π轨道。 6个π电子离域在六个C原子上。由此形成一个闭合的
共轭体系。
2. 苯的构性相关分析
CH3
CH3
CH3
CH3
1,2-二甲苯 邻二甲苯 o-二甲苯
有机化学第四篇芳香烃
第四章芳香烃芳烃,也叫芳香烃,一般是指分子中含苯环结构的碳氢化合物。
现代芳烃的概念是指具有芳香性的一类环状化合物,它们不必然具有香味,也不必然含有苯环结构。
分类:芳香烃按照分子中是不是含有苯环,可分为苯系芳烃和非苯系芳烃。
苯系芳烃按所含苯环的数量和结合方式分为单环芳烃、稠环芳烃和多环芳烃。
1.单环芳烃:指分子中仅含一个苯环的芳烃,包括苯、苯的同系物和苯基取代的不饱和烃。
例如:CH3CH2CH3CH=CH2苯甲苯乙苯苯乙烯2.多环芳烃:指分子中含两个或两个以上苯环的芳烃,多环芳烃按照分子中苯环的连接方式不同分为多苯代脂肪烃,联苯烃和稠环芳烃(1)多苯代脂肪烃:能够看做脂肪烃分子中两个或两个以上氢原子被苯基取代的化合物。
CH2HC CH二苯甲烷1,2-二苯乙烯(1)联苯烃:指两个或两个以上苯环别离以单键相连而成的多环芳烃例如:联苯1,4-三联苯(2)稠环芳烃:两个或两个以上苯环彼此共用两个碳原子而成的多环芳烃,例如:萘蒽菲3.非苯芳烃:指分子中不含苯环的芳香烃,例如:环戊二烯负离子环庚三烯正离子第一节单环芳烃一,单环芳烃的异构现象和命名苯是最简单的单环芳烃。
单环芳烃包括苯、苯的同系物和苯基取代的不饱和烃。
1.异构现象(1)烃基苯有烃基的异构例如:CH2CH2CH3CHCH3CH3(2)二烃基苯有三种位置异构例如:RR'RRR'R'(3)三取代苯有三种位置异构例如: R R'RRR''R''R''R'R'2. 命名(1)苯基的概念芳烃分子去掉一个氢原子所剩下的基团称为芳基(Aryl)用Ar 表示。
重要的芳基有:CH 2(C 6H 5CH 2-)苄基(苯甲基),用Bz 表示苯基, 用Ph 或 表示ф(2)一元取代苯的命名a 当苯环上连的是烷基(R-),-NO 2,-X 等基团时,则以苯环为母体,叫做某基苯。
例如:CH CH 33NO 2Cl异丙基苯叔丁基苯硝基苯氯苯b 当苯环上连有-COOH ,-SO 3H ,-NH 2,-OH ,-CHO ,-CH=CH 2或R 较复杂时,则把苯环作为取代基。
大学有机化学重点知识总结第五章 芳烃 芳香性

NH2
Cl
OCH3
2-甲 氧 基 -6- 氯 苯 胺
OH
CH3
1
COCH3
3-甲基-4-羟基苯乙酮
大学有机化学重点知识总结第五章 芳烃 芳香性
§5.2 苯的结构
3H2
208.5 kJ/mol
H2
119.3 kJ/mol
苯的氢化热:208.5 kJ • mol-1 环己烯氢化热的3倍:
3×119.3 =357.9 kJ•mol-1
* 5、芳烃侧链的反应
大学有机化学重点知识总结第五章 芳烃 芳香性
一、 芳环上亲电取代反应
试剂中的亲电部分从芳环上取代一个H原子
4–羟基–3–甲氧基苯甲醛
大学有机化学重点知识总结第五章 芳烃 芳香性
C O O H> SO 3H> C O O R> C O C l > C O N H 2> C H O> CO> O H> N H 2> CC >
COOH
1
CC> O R> C l > N O 2
对 -甲 酰 基 苯 甲 酸
CHO
轨道; 6 个π 电子离域在6个C原子上。
p6 6
大学有机化学重点知识总结第五章 芳烃 芳香性
图 5.2 苯的闭合的π轨道 4.环状的共轭体系导致苯分子具有相当高的稳 定性。电子云完全平均化,故无单双键之分。
大学有机化学重点知识总结第五章 芳烃 芳香性
苯分子中的骨架
大学有机化学重点知识总结第五章 芳烃 芳香性
CH3 C CHCH3
2–甲基–3–苯基戊烷 2–苯基–2–丁烯
PhC CH
苯乙炔
CH2
芳烃与芳香性

氢化热的三倍低得多(3×119.3-208.5=149.4 kj· -1),这 mol
149.4 kj· -1即为苯的共轭能。 mol
有机化学
芳香烃
23
由于苯形成了一个环状键,使6个碳-碳键、
6个碳-氢键都相同,其碳-碳键较烷烃中 短,比烯烃中碳-碳双键长,导致其性质与 烷烃、烯烃都有较大区别,苯的这种难加成、 难氧化、易取代的性质,就被称为芳香性。
芳香烃 33
有机化学
5.4 单环芳烃的化学性质
5.4.1 芳烃苯环上的反应
(一)亲电取 代 反 应 1. 卤代:
+ X2
FeX3 或 Fe
X
+
HX
F2 > Br2 > C l2 > I2 例: C H3 + Br2
FeB r3, CH3COOH
C H3 Br +
C H3 +
C H3
25℃
32.9 %
有机化学
芳香烃
30
苯中毒事件
2002年1月,浙江省温岭市制鞋企业发生苯中毒事件, 中毒28人,4人死亡。 2002年 3月,北京市某包装制品发 生苯中毒事件,13人中毒,两人死亡。2005年5月,山东 聊城时风集团公司共31人中毒,其中2人死亡。现存活 的29人(男28人,女1人;年龄18岁至39岁;工龄最 短的2个月,最长的4年)中,慢性重度苯中毒13人, 慢性中度苯中毒11人,慢性轻度苯中毒5人。…….
OH
Cl SO3H
NO2
间氯苯酚
对甲苯磺酸
邻氨基苯甲醛
间硝基甲苯
有机化学
芳香烃
12
三 1)三基团相同 1,2,3-(连) 取 代 2)三基团不同 苯 ① 先定主官能团并编号为1; ② 取代基位号尽可能小;
有机化学基础知识点芳香性与芳香烃的性质

有机化学基础知识点芳香性与芳香烃的性质有机化学基础知识点——芳香性与芳香烃的性质有机化学是研究有机物质及其反应机理的一门学科,其中芳香性与芳香烃是其中重要的知识点之一。
本文将着重介绍芳香性以及芳香烃的性质,帮助读者更好地理解有机化学中的这一概念。
一、芳香性的定义与特点芳香性是指具有特殊结构和性质的有机化合物所表现出的香味和稳定的π电子结构。
根据芳香性的定义,芳香性化合物需要满足以下几个条件:1. 分子结构中含有一个或多个芳环(由6个共轭π电子组成的环状结构);2. 芳环中每个原子都以杂化sp2形式存在,磁性势能相对稳定;3. 芳环中的每个杂化的p轨道上都有一个未被配对的π电子。
值得注意的是,非芳香性化合物虽然可能具有香味,但其分子结构不符合芳香性的定义。
二、芳香烃的分类与性质芳香烃是一类基础的有机化合物,其分子中至少含有一个芳环。
根据芳香烃分子中芳环的个数及其它官能团,芳香烃可以分为以下几类:1. 单核芳香烃:只含有一个芳环的芳香烃。
例如,苯(C6H6)是最简单的芳香烃,其分子结构中含有一个六元环。
2. 多核芳香烃:含有两个或多个连接在一起的芳环的芳香烃。
最常见的多核芳香烃是萘(C10H8),它由一个苯环和一个呈共轭连结的五元环组成。
3. 取代芳香烃:分子中的芳环上存在取代基的芳香烃。
通过对芳环中的氢原子进行取代,可以获得各种不同性质和用途的化合物。
芳香烃的一些重要性质包括:1. 稳定性:芳香烃具有相对较高的稳定性,这是因为芳香烃分子中的共轭π电子系统能够稳定结构和分子。
2. 可溶性:大多数芳香烃在非极性溶剂中具有较好的溶解性,但在水中溶解度较低。
3. 反应性:芳香烃在化学反应中常常表现出亲电取代反应、脱氢反应等特性。
三、应用与实际意义芳香烃是有机化学中重要的化合物类别之一,其应用领域非常广泛。
以下是一些芳香烃的应用和实际意义:1. 燃料:芳香烃类化合物广泛应用于燃料行业,用作汽车燃料和燃气等能源。
有机化学第七章 芳烃

H
H
H
H
H
H
可以解释:为什么苯分子特别稳定? 为什么苯分子中碳碳键长完全等同? 为什么邻位二取代物只有一种?
(b)分子轨道理论 分子轨道理论认为:苯分子形成σ键后,苯的
六个碳原子上的六个P 轨道经线性组合可以形成六 个分子轨道,其中ψ1 、ψ2 和ψ3 是成键轨道,ψ4、 ψ5和 ψ6是反键轨道。当苯分子处于基态时六个电 子填满三个成键轨道,反键轨道则是空的。
-络合物
(b)硝化反应
2 H2SO4 HNO3
NO2
HNO3 H2SO4,45℃
CH3
HNO3 H2SO4,30℃
NO2
CH3 NO2
CH3
NO2
HNO3 H2SO4,95℃
NO2
NO2
NO2
H3O 2 HSO4
反应比苯容易 反应比苯困难
硝化反应机理
硝化反应中进攻试剂是NO2+,浓硫酸的作 用促进NO2+的生成:
苯环的特殊稳定性可以从它具有较低的氢化热 得到证明:
环己三烯氢化热=360kj/mol(假想值) 苯环氢化热=208kj/mol 相差152kj/mol
氢化热简图:
环己三烯+3H2
环己二烯+2H2
苯+3H2
环己烯+H2
231kj/mol
120kj/mol
208kj/mol
360kj/mol
环己烷
苯分子的近代概念
ቤተ መጻሕፍቲ ባይዱ
(1)煤的干馏
煤隔绝空气加热至1000~1300℃时分解所得到的 液态产物——煤焦油,其中含有大量芳烃化合物。 再经分馏得到各类芳烃。
馏分名称 轻油 酚油 萘油 洗油 蒽油
有机化学 第六章 芳香烃

(一) 芳烃的构造异构和命名 (二) 苯的结构 (三) 单环芳烃的来源 (四) 单环芳烃的物理性质 (五) 单环芳烃的化学性质 (六) 苯环上取代反应的定位规则 (七) 稠环芳烃 (八) 芳香性 (九) 富勒烯
第六章 芳烃 芳香性
• 芳烃——芳香族碳氢化合物。含有苯环的一 大类C、H化合物。 “芳香”二字的含义:
1,2,4,5-四甲苯
(2) 命名
命名时,一般以芳环为取代基,也可以芳环为母体。具
体情况,具体对待:
CH=CH2
CH=CH2
苯乙烯
对二乙烯基苯 CH=CH2
CH2Cl
CH2OH
苯氯甲烷 氯苄
苯甲醇 苄醇
• C6H5- 苯基(Ph-) ;
C6H5CH2- 苄基 ;
Ar- 芳基(芳环上去掉一个氢后,所剩下的原子团);
O
慢
H
SO3-
快 HSO4-
+
σ-络合物
SO3- 快
H3O+
SO3H + H2O
(丁) 烷基化反应机理
苯环烷基化反应中,AlCl3的作用是与卤烷起反应, 加速R+的生成:
RCl + AlCl3
R+ + AlCl4-
亲电试剂
+ R+
R
+H
σ-络合物
AlCl4-
R + HCl + AlCl3
苯环烷基化反应时,产生异构化的原因:
Br
p-二溴苯
注意:第二个卤素原子进入第一个卤素原子的邻、对位。
(乙) 硝化
+ HNO3
浓H2SO。4
50-60 C
有机化学-芳烃(全面剖析)
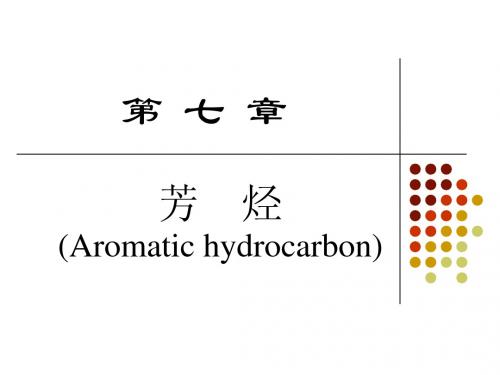
苯的氢化热预计: 120 * 3 = 360 kJ/mol 苯的氢化热实测: 208 kJ/mol 离域能(或共轭能) :360 - 208 = 152 kJ/mol
五、苯的共振式和共振论的简介 基本要点: 1.当一个分子、离子或游离基按照理论可以写出两 个以上经典结构式时,这些经典结构式构成了一个 共振杂化体,共振杂化体接近实际分子。
H H H
H
闭 合 H共 轭 体 系 H
三、苯的分子轨道模型
y6=0.408(-f1+f2-f3+f4-f5+f6) y5=0.289(-2f1+f2+f3-2f4+φ5+f6) y4=0.500(f2-f3+f5-f6)
反键轨道
成键轨道
y3=0.500(f2+f3-f5-f6) y2=0.289(2f1+f2-f3-2f4-f5+f6) y1=0.408(f1+f2+f3+f4+f5+f6)
SO3H
﹢ + H3O
+ H2O ……④
4. 傅瑞德—克拉夫茨(Friedel-Crafts)反应
包括 烷基化—— 被 -R 取代 O 酰基化—— 被 R-C- 取代 催化剂:AlCl3 、 FeCl3 、BF3等路易斯酸 烷基化试剂:卤代烷、烯、醇等
C2H5
① 烷基化反应
+ C2H5Br
AlCl3
甲苯基--甲苯分子中苯环上减去一个H所得基团叫甲苯基.
CH2Cl
CH2OH
苄氯(氯化苄)
苄醇(苯甲醇)
5. 苯的衍生物命名 a. -NO2 、-NO、-X 与苯相连时,苯作母体
有机化学第8版第六章芳香烃

CH3 混酸
30 ℃
CH3
HNO3 NO2 发烟 H SO 2 4 95 ℃
NO2 NO2
SO3H SO3H 发烟 H2SO4 使苯环易发生亲电取代的定位基叫活化基,如-CH3。 200~230℃ SO3H
使苯环难发生亲电取代的定位基叫钝化基,如-NO2 。
(1) 第一类定位基(邻、对位定位基)
NR2,
根据休克儿规则,苯具有6 ∏电子环状平面共轭大
∏体系 ,具有芳香性。
苯系以外的芳香体系统称为非苯芳香体系。
环丁二烯
环辛二烯
+
-
SP2碳
SP3碳
SP2碳
+
++
-
环丙烯正离子
∏电子数 2
环丁二烯双正离子
2
环丁二烯双负离子
6
-
环戊二烯负离子 ∏电子数 6
环庚二烯正离子 6
环辛四烯双负离子 10
本章重点
5、苯的酰基化
+ CH3COCl AlCl3 COCH3
H 总结 : + E+ 慢
+
E -H
快
E
+ H
+
正碳离子中间体 (σ-配合物)
(二)苯侧链烃基的反应
1、烷基苯的氧化
CH3 KMnO4 COOH
CH3 KMnO4 CH2CH3
COOH
C(CH3)3 KMnO4
COOH
Br CHCH3
CH2CH3
两个(以上)苯环稠并成的多环芳香烃。如:萘、 蒽、菲等。
萘 蒽 菲 (Naphthalene)(Anthracene)(Phenanthrene)
有机化学第五章芳烃芳香性

芳烃与混酸作用,芳环上H原子被硝基取代生成硝基取代芳烃。
硝化反应
硝化剂:浓HNO3 + 浓H2SO4(简称混酸) 底物活性:烷基苯>苯>硝基苯
硝化反应机理
硝化反应
(c) 磺化反应
Sulfonation
芳烃与浓H2SO4作用,芳环上H原子被磺(酸)基-SO3H取代生成芳磺酸。
a. 磺化剂: 浓H2SO4 或 发烟H2SO4 b. 底物活性:烷基苯>苯>苯磺酸
氯苯的亲电取代定位分析
稳定 稳定
硝基苯的亲电取代定位分析
极不稳定 极不稳定
小结
决定性的极限结构
决定性的极限结构
Z供电,亲电试剂进攻邻对位有利 Z吸电,进攻邻对位不利
(2) 空间效应
空间效应越大,邻位异构体越少
R
p-
m-
CH3
58.4
37.2
4.4
CH2CH3
45
48.5
6.5
CH(CH3)2
磺化反应机理
机理:
取代反应的位置
磺化反应可逆
磺化反应是可逆的:强酸利于磺化,热的稀酸水溶液利于脱磺酸基。
(d). Friedel-Crafts 反应 在催化剂作用下,芳烃中芳环上氢原子被烷基或酰基取代的反应。 a. 常用催化剂:AlCl3、FeCl3、ZnCl2、(HF、BF3、H2SO4) b. 常用烷基化剂:卤代烃、烯烃(醇) c. 常用酰基化剂:酰卤、酸酐(酸)
烷基化反应可以通过醇或烯烃生成碳正离子,发生烷基化反应。
Friedel-Crafts酰基化反应
酰基化不可逆,产物单一。
AlCl3用量: 用酰氯时,用量 > 1 eqv. 用酸酐时,用量 > 2 eqv.
有机化学--第八章芳烃

课件
20
(I)和(Ⅱ)是键长和键角完全相等的等价结构,贡献大, 故苯的极限结构通常用(I)和(Ⅱ)式表示。共振使苯的能 量比假想的1,3,5-环己三烯低149.4 kJ· mol-1,此即苯 的共振能或离域能,因此苯比较稳定。 由于共振的结果,苯分子中的碳碳键,既不是单键也
不是双键,而是介于两者之间,六个碳碳键完全相等,
课件
29
8.4.1取代反应
1.卤化
在三卤化铁等催化剂作用下,苯与卤素作用生成 卤(代)苯,此反应称为卤化反应。例如:
课件
30
对于不同的卤素,与苯环发生取代反应的活性次序
是:氟>氯>溴>碘。其中氟化反应很猛烈;碘化反应不
仅较慢,同时生成的碘化氢是还原剂,从而使反应成为 可逆反应,且以逆反应为主。因此氟化物和碘化物通常
课件
62
SO3因为极化使硫原子显正性,通过硫原子进攻苯环。磺 化反应是可逆的。在浓硫酸中,磺化反应机理可能如下:
课件
63
4.烷基化和酰基化反应的机理
①烷基化反应的机理 例如,用1-氯丙烷作烷基化试剂时,其反应机理如下:
sp2杂化轨道,分别与一个氢原 子的1s轨道相互交盖,构成六 个相同的碳氢σ 键。
课件
14
这六个碳原子和六个氢
原于是共平面的。每一个碳
原子剩下的一个p轨道,其 对称轴垂直于这个平面,彼
此相互平行,并于两侧相互
交盖,形成一个闭合的π轨 道,如图 (Ⅱ)所示。
课件
15
这样处于该 π 轨道中的 π
电子能够高度离域,使π电子
第八章 芳烃 芳香性
一般把苯及其衍生物总称为芳香族化合物。芳烃是 芳香族碳氢化合物的简称,亦称芳香烃。
芳烃饱和率-概述说明以及解释

芳烃饱和率-概述说明以及解释1.引言1.1 概述芳烃饱和率是指芳烃分子中饱和碳氢键的比例,即芳烃分子中有多少碳氢键是饱和状态的。
饱和率是一个重要的指标,可以用于评估和描述芳烃分子的饱和程度和稳定性。
在石油化工和有机化学领域,芳烃饱和率的研究和应用具有重要的理论意义和实际价值。
芳烃是指含有芳香环结构的化合物,其分子结构中通常含有苯环或其衍生物。
芳烃具有一系列特殊的化学性质和物理性质,例如高稳定性、难于被氧化、热稳定性好等。
然而,芳烃也存在一定的不稳定性,其中芳香环上的碳氢键易受到热、光、氧等外界因素的影响而发生部分饱和或饱和反应。
芳烃饱和率的概念是指芳烃分子中饱和碳氢键的数量与总碳氢键的比值。
简单来说,饱和率越高,芳烃分子中的饱和碳氢键占比就越高,分子结构就越稳定。
而饱和率越低,芳烃分子中的饱和碳氢键占比就越低,分子结构则更容易发生不稳定性变化。
芳烃饱和率的研究与应用在石油化工领域具有重要意义。
饱和率的高低直接影响到芳烃分子的稳定性和化学性质,进而影响到石油化工产品的质量和性能。
在催化剂的设计与选择、反应工艺的优化与控制以及产品的加工和利用等方面,芳烃饱和率都是十分关键的因素。
此外,芳烃饱和率的研究也对于环境保护和能源可持续发展有一定的意义。
本文将对芳烃饱和率的定义和特性进行详细介绍,探讨影响芳烃饱和率的因素,并对芳烃饱和率的重要性与未来研究展望进行总结与归纳,以期为石油化工研究和应用提供一定的指导和参考。
1.2 文章结构本文主要分为引言、正文和结论三个部分,每个部分的内容如下:引言部分首先概述了本文要探讨的主题——芳烃饱和率,并介绍了芳烃和饱和率的基本概念。
接着,给出了本文的结构和目的,以便读者能够对文章内容有一个简单的了解。
正文部分详细讨论了芳烃的定义和特性,以及饱和率的概念。
在芳烃的定义和特性中,将介绍什么是芳烃以及其结构特点、性质等内容。
而在饱和率的概念中,将说明饱和率在有机化学中的重要性,以及计算饱和率的方法和应用等。
第十二讲 第五章 芳烃 芳香性(3)
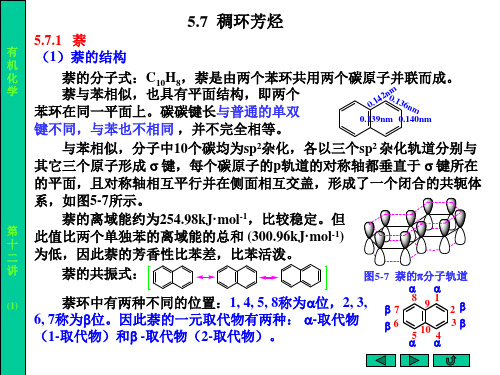
H H
1,4-二氢萘 伯奇 二氢萘 伯奇(Birch)还原,优 还原, 还原 孤立双键不被 先还原较活泼的环。 先还原较活泼的环。 进一步还原。 进一步还原。
H2, Rh-C或Pt-C - 或 ,加 压
在强烈条件下加氢时,催化剂和反应条件不同,可得四氢化萘或十氢化萘: 在强烈条件下加氢时,催化剂和反应条件不同,可得四氢化萘或十氢化萘:
α-萘乙酸 萘乙酸
萘乙酸简称NAA:无色针状或粉末状晶体,m.p. 134. 5~135. 3℃, α-萘乙酸简称 萘乙酸简称 :无色针状或粉末状晶体, ℃ 难溶于冷水,易溶于热水、乙醇和乙酸等。是一种植物生长激素, 难溶于冷水,易溶于热水、乙醇和乙酸等。是一种植物生长激素,能促进 植物生根、开花、早熟、高产,对人畜无害。 植物生根、开花、早熟、高产,对人畜无害。 (b)氧化反应 ) ① 在较温和的条件下氧化得醌,产率较低。例如: 在较温和的条件下氧化得醌,产率较低。例如:
空间相互作用较大
H SO3H
H
空间相互作用较小
SO3H H
(3)
α-萘磺酸 萘磺酸
β-萘磺酸 萘磺酸
有 机 化 学
同时由于磺化反应是可逆反应,故高温使成为β 萘磺酸主要产物 萘磺酸主要产物。 同时由于磺化反应是可逆反应,故高温使成为β-萘磺酸主要产物。且 萘磺酸的热稳定性好于α 萘磺酸, β-萘磺酸的热稳定性好于α-萘磺酸,该反应是热力学控制的反应。 萘磺酸的热稳定性好于 萘磺酸 该反应是热力学控制的反应。 磺基易被其它基团取代,因此高温制得的β 萘磺酸是制备某些 取代 萘磺酸是制备某些β 磺基易被其它基团取代,因此高温制得的β-萘磺酸是制备某些β-取代 萘的桥梁。 制备β 萘酚 萘的桥梁。如:制备β-萘酚
有机化学》(第四版)第五章 芳烃(习题答案)
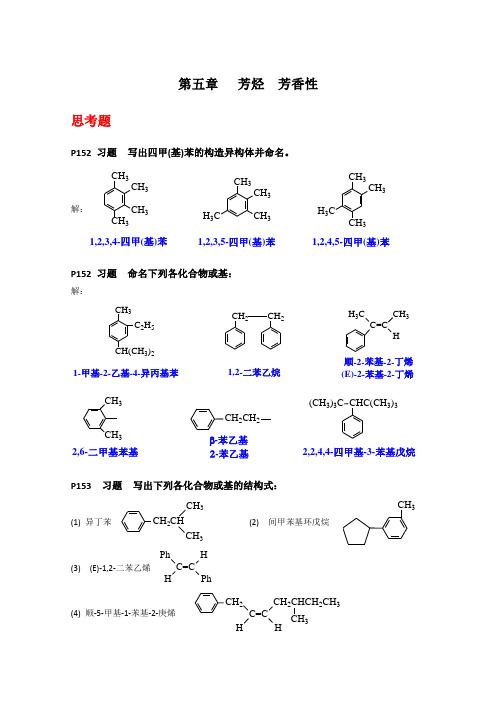
第五章 芳烃 芳香性思考题P152 习题 写出四甲(基)苯的构造异构体并命名。
解:CH 3CH 3CH 3CH 3CH 3CH 3CH 3H 3CCH 3CH 33H 3C1,2,3,5-四甲(基)苯1,2,3,4-四甲(基)苯1,2,4,5-四甲(基)苯P152 习题 命名下列各化合物或基:解:CH 3C 2H 5CH(CH 3)2CH 2CH 2C=C3HH 3C1-甲基-2-乙基-4-异丙基苯1,2-二苯乙烷顺-2-苯基-2-丁烯(E)-2-苯基-2-丁烯CH 3CH 3CHC(CH 3)3(CH 3)3C 2,6-二甲基苯基β-苯乙基2,2,4,4-四甲基-3-苯基戊烷CH 2CH 22-苯乙基P153 习题 写出下列各化合物或基的结构式:(1) 异丁苯CH 2CHCH 3CH 3(2) 间甲苯基环戊烷CH 3(3) (E)-1,2-二苯乙烯C=CH PhPhH(4) 顺-5-甲基-1-苯基-2-庚烯C=CHHCH 2CHCH 2CH 3CH 23(5) 二苯甲基CH C 6H 5C 6H 5(6) 3-苯基-2-丙烯基CH 2CH=CH C 6H 5P156 习题 甲苯的沸点比苯高30.5℃,而熔点低~100℃,为什么解:甲苯的相对分子质量大于苯,分子间色散力大于苯,因比甲苯的沸点也高于苯;但苯分子的对称性好,晶格能大于甲苯,因此苯的熔点高于苯。
P161 习题 写出乙苯与下列试剂作用的反应式(括号内是催化剂):(1) Cl 2(FeCl 3) (2) 混酸 (3) 正丁醇(BF 3) (4) 丙烯(无水AlCl 3) (5) 丙酸酐(CH 3CH 2CO)2O(无水AlCl 3) (6) 丙酰氯CH 3CH 2COCl(无水AlCl 3) 解:(1)CH 3CH 2CH 3CH 2ClClCH 2CH 3Cl FeCl 3+(2) 混酸CH 3CH 2CH 3CH 2NO 2+NO 2CH 2CH 3(3)BF 3CH 3(CH 2)3OHC 2H 5CHCH 2CH 33CH 2CH 3+CHCH 2CH 3CH 2CH 3CH 3(4)233+CH(CH 3)2CH 2CH 3CH 2CH 3CH 2CH 33)2(5)3223+COCH 2CH 3CH 2CH 3CH 2CH 3CH 2CH 32CH 3O(6)323CH 2CH 3+COCH 2CH 3CH 2CH 3CH 2CH 32CH 3OP161习题 由苯和必要的原料合成下列化合物:(1)解:HO H SO +(或环己烯)(2) 叔丁苯解:C CH 33CH 3+ CH 2CH 3CH 3H SO (3) CH 2(CH 2)5CH 3解:HCl+2)5CH 3OCH 3(CH 2)5C OCH 2(CH 2)5CH 3(4)CH 2CH 2OOH O解:OOO+3CH 2CH 2OH OOP164 习题 试以苯和必要的原料合成正丙苯。
有机化学高教第四版第四章环烃(芳香烃)

C H3
C H3
C H3 CO CH 3
CH3COCl AlCl 3 CH3COCl AlCl 3
难以进行
b. 烷基化反应,当R≥3时易发生重排;而酰 基化反应则不发生重排。如:
C H(C H)2 3 + C H3C H2C H2C l
AlCl 3
C H2C H2C H3
+ (主 ) C O C HC H3 2 (次 ) C H2C H2C H3
加 成 反 应
1. 加氢反应
+ 3 H2
Ni 。 180 ~ 210 C, 18MPa
2. 加氯反应:
+ 3 Cl2
紫外光
Cl Cl Cl Cl 六氯化苯 Cl Cl
氧 化 反 应
1. 苯环氧化:
+ 9 O2
。 400 ~ 500 C V2O5
O 顺丁烯二酸酐
2. 烷基苯的氧化( 侧链氧化 ):
C H2C H3
Z―基团可分为两类: 1.第一类定位基(即邻对位定位基) ―O-、 ―N(CH3)2 > ―NH2 > ―OH > ―OCH3 > ―NHCOCH3 >―OCOCH3 > ―CH3 > ―Cl > ―Br >―I 、 ― C6H5 ┄等。 这类定位基可使苯环活化(卤素除外)。其特点为: a. 带负电荷的离子。如:
HNO3+H2SO4 。 50~60 C
NO2
+
R
NO2
X2
NO2 X NO2 NO2
NO2
Fe 或 FeX3
HNO3+H2SO4 。 100~110 C
由此可见,当一取代苯(C6H5Z)通过亲电取代 反应引入第二个取代基时,它所进入的位置, 受第一个取代基Z的指令,由Z决定第二个取代 基进入的位置。
第五章 芳烃 芳香性

• 第二类定位基-间位位定位基: (钝化
苯环) -N+(CH3)3, -NO2, -CN, -SO3H, -CHO, COCH3, COOH, -COOCH3, -CONH2, N +H 3 ;
B:苯环上取代反应定位规则的理论解释
• (1)电子效应
Z H Z E+ Z + E+ E Z
+ Z E + H E H
常用烷基化试剂:卤代烷,烯烃,醇, Cl 环醚; CH2=CH-Cl
不能做烷基化试剂
烷基化反应历程:
CH3CH2Cl + AlCl3 CH3CH2+AlCl4CH2CH3 + CH3CH2+AlCl4CH2CH3 + H+ + H
特点:可逆,歧化,重排
1). 可逆:芳烃可以在催化条件下烷 基化成为烷基苯,烷基苯也可在同 一催化剂存在下脱烷基成为芳烃。
二硝化主要产物为间二硝基苯;
NO2 + 浓 HNO3 浓 H2SO4 100~110℃ 93% NO2 + NO2 NO2 1% NO2 + NO2
NO2
6%
CH3 浓 HNO3 浓H2SO4 30℃
CH3 NO2 +
CH3 +
CH3
NO2 NO2
59%
37%
4%
硝化反应历程
H2SO4 + HONO2 H2O+ NO2 H2O + H2SO4 2H 2SO4 HNO3
• (一)苯系芳烃分类:
1.单环芳烃:分子中含有一个苯环;
2.多环芳烃:分子中含有两个或两个以上独立苯 环;
3.稠环芳烃:分子中两个或多个苯环彼此间共用 两个相邻碳原子而成的芳烃;
有机化学第六章 芳香烃02R

C. 大小次序规则:
• 大小次序规则见烯烃的Z,E-命名法(P43)。 • 有多个取代基或官能团时,其列出顺序遵守“大 小次序规则”,较大的基团后列出。
官能团大小次序规则:
① 把双键碳上的取代基按原子序数排列,同位素:D>H, 大的基团在同侧者为Z,大基团不在同侧者为E。
Z—Zuasmmen,共同;E — Entgengen,相反。
-Cl >
-SO3H >
-F >
-OCOR
举例:
HO
NH2
p-氨基苯酚
H3C
Cl
对氯甲苯
Cl
NO2
对硝基氯苯
CH3 NH2
Cl
2-甲基-4-氯苯胺
OH CH3
COCH3 3-甲基-4-羟基苯乙酮
OH Br 4 3 SO3H
5 2
1
SO3H
4-羟基-5-溴-1,3-苯二磺酸
CHO O2N
Cl
4-硝基-3-氯苯甲醛
Cl
SO3H
Br
4-氯-3-溴苯磺酸
CH3
O
Cl 3-甲基-5-氯环己酮
OCH2COONa Cl
Cl 2,4-二氯苯氧基乙酸钠
O C-NHCH3
CH3 N-甲基-1-(4-甲萘基)甲酰胺
(十)富勒烯(fullene)
富勒烯(fullerene)亦称为足球烯,是由C60、C70、C50等一 类化合物的总称。(动画, C60的结构)
而环丁二烯和环辛四烯却化学性质活泼,不具有芳香性。
问题:有芳性的化合物一定要含有苯环吗?
答案:不一定!!
平面结构的环状离域体系,如果其π电子数符合休克 尔(Hückel)规则,就具有芳香性。
(1)Hückel规则
有机化学 芳香烃

芳香烃分类
苯系芳烃
单环芳烃 苯
CH2CH3
CHCH3 CH3
乙苯
异丙苯
CH=CH2 苯乙烯
联苯
联苯
对三联苯
多环芳烃 稠环芳烃
萘
蒽
多苯代脂烃
非苯芳烃
环戊二烯 环庚三烯
薁
负离子 正离子
CH2 二苯甲烷
苯的发现
Kekule式
苯的 结 构 )
杜瓦苯
• 1825年,迈克尔·法拉第 (Michael Faraday,1791-1867)从鱼油等类似物质的 热裂解产品中分离出了较高纯度的苯,称之为“氢的重碳化物” (Bicarburet of hydrogen)。并测定了苯的一些物理性质和它的化学组成, 阐述了苯分子的碳氢比为C︰H=1︰1,实验式(最简式)为CH。
• 1865年,弗里德里希·凯库勒在论文《关于芳香族化合物的研究》中,再次 确认了四年前苯的结构,为此,苯的这种结构被命名为“凯库勒式”。此 外,詹姆斯·杜瓦发现了一种苯的类似物;命名为“杜瓦苯”,现已被证实, 可由苯经光照得到。
凯库勒 (1829-1896)
史上最著名有机化学家之一。1829年9月7日生于达姆施 塔特,1896年6月13日卒于波恩。1852年获博士学位。后来 去巴黎深造,结识了C.-F.热拉尔。1856年在汉德堡大学任讲 师。1858年任比利时根特大学化学教授。1867年任波恩大 学化学研究所所长。
4-2 单环芳烃的异构和命名 异构现象
1.烃基苯有烃基的构造异构 例如:
CH2CH2CH3
CH3 CH
CH3
2.二烃基苯有三中位置异构
R R'
R
R
例如:
R'
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CH2CH3
2 3
CH2CH2CH3
1
CH3CH2CH2CH2 4 5 6
2–乙基–1–丙基–4–丁基苯
CH2CH3
1
6
2
5
3
4
CH2CH2CH3
1–乙基–4–丙基苯
苯作为取代基
当苯环与较长、较复杂烃基相连或烃基连有多个苯环,或是与不饱和 基相连时,苯环作取代基。
6 54 3 21
CH3CHCH2CH2CHCH3
x3 357.9 kJ/mol
119.3 kJ/mol
208.5 kJ/mol
5.2.1 价键理论
6 个C-C σ 键: sp2–sp2, 6 个C-H σ 键: sp2–1s , 6个2p轨道侧面交盖形成闭合π 体系
5.2.2 分子轨道理论
6
4
能 量
2
1
苯的π 分子轨道和能级
反 键
5 轨
道
3 成
CH2CH2 1,2二苯乙烷
1,3,5 三苯基苯
萘
蒽
菲
补充内容
5.1 芳烃的构造异构和命名
5.1.1 构造异构 侧链异构
CH2CH2CH3
CH3CHCH3
丙苯
侧链位置异构
CH3 CH3
CH3
1,2,3–三甲苯 连三甲苯
异丙苯 枯烯
CH3
H3C
CH3
1,3,5–三甲苯 均三甲苯
CH3 CH3
CH3
CH3
6 54 3
21
CH3CH2CH2CH C CH
CH3 CH3
2–甲基–5–苯基己烷
1 CH3 C CHCH3
2 34
2–苯基–2–丁烯
2,3 –二甲基–1–苯基–1–己烯
CH2
二苯基甲烷
其他命名示例
苯环为母体的一部分
CH CH2 Ph CH CH2
苯乙烯 CHO
O C CH3
苯甲醛
苯乙酮
C CH 苯乙炔
供电体: 苯环,Lewis碱 亲电体: E+, Lewis酸
(一) 亲电取代反应
electrophilic aromatic substitution 试剂中的亲电部分从芳环上取代一个H原子。
磺化 SO3H
硝化 NO2
卤化
R 烷基化
Cl氯甲基化XFra bibliotek卤化H
OR
酰基化
(a) 卤化
halogenation
CH3
CH3
1,3–二甲苯 间二甲苯 m–二甲苯
o– : ortho-; m– : meta-; p– : para-
CH3
CH3
1,4–二甲苯 对二甲苯 p–二甲苯
命名时的编号
尽量使各取代基编号最小,若有可能,让较最不优先取代基为1位。
CH2CH3 CH2CH2CH3
CH3CH2CH2CH2
CH2CH3 CH2CH2CH3
内容
苯的结构 单环芳烃的化学性质(亲电取代及侧链反应) 亲电取代反应:定位规则及应用,动力学和热力学控制 稠环芳烃 芳香性 多官能团化合物的命名
芳烃的分类
(1) 单环芳烃
CH3
甲苯
(2) 多环芳烃
联苯
(3) 稠环芳烃
Cl 氯苯
CH3 CH CH3 异丙(基)苯
CH3 CH3
邻二甲苯
CH CH (E) 1,2 二苯乙烯
H
X
+ XX
Fe Or FeX3
+ HX
a.催化剂:Fe、FeCl3 、FeBr3 、AlCl3等 b.卤素活性:F>Cl>Br>I c.芳烃活性:烷基苯>苯>卤代苯
H
Fe + Br Br
Br + H Br
75%
卤化反应机理
H Fe
+ Br Br
机理:
Br Br + FeBr3
H + -
+ Br Br FeBr3
BrH
+ Br FeBr3
H
Br
+ H Br
75%
+ Br Br FeBr3
BrH + Br FeBr3
H
Br + H Br + FeBr3
H
第一步 Br2分子的极化
Br2 与FeBr3 的络合,Br2分子的极化。
Br Br + FeBr3
+ Br Br FeBr3
第二步 溴进攻苯环
H + -
FeCl3
CH3 Cl2 , FeCl3 CH3COOH 25C
CH3 Br2, FeCl3 CH3COOH 25C
Cl Cl +
39% CH3
Cl +
60% CH3
Br +
33%
Cl
Cl
+ Cl
6% CH3
Cl 55%
CH3
+ Cl
+ Br Br FeBr3
BrH + Br FeBr3
H
BrH
BrH
BrH
H
H
H
p,π–共轭π电子的离域产生共振杂化体.
第三步 失去质子恢复芳香体系
BrH
+ Br FeBr3
H
Br
+ H Br + FeBr3 H
卤化反应位置
烷基苯和卤代苯的卤代物主要为邻对位异构体,溴化比氯化更倾向对位。
Cl Cl Cl
CH3
Cl
甲苯 (toluene)
CH3CHCH3
异丙苯 (isopropylbenzene)
氯苯 (chlorobenzene)
NO2
硝基苯
(nitrobenzene)
多取代苯的命名
当苯环上连有两个以上取代基时,需标明取代基位次或取代基间的相 对位置 。以二取代苯为例:
CH3 CH3
1,2–二甲苯 邻二甲苯 o–二甲苯 (o-Xylene)
键 轨 道
量子化学计算的苯分子轨道示意图
6
4
5
2
3
1
5.2.3 共振论对苯分子结构的解释
多个经典结构构成的共振杂化体
极限结构能量相同 极限结构能量相同
共振能:3 x 119.3 – 208.5 = 149.4 kJ·mol
5.3 单环芳烃的物理性质
芳烃为液体或固体; 密度小于1; 有特殊气味、有毒; 不溶于水,易溶于有机溶剂。
COOH 苯甲酸
OCH3 苯甲醚
NH2 苯胺
SO3H 苯磺酸
5.2 苯的结构
H
120° 0.108 nm
H
H
120° 0.140 nm
H
H
H
正六边形、共平面 键角120° 键长0.140nm
C‒C: 0.154 nm C=C: 0.134 nm
苯具有特殊稳定性
+ H2 + H2
+ 119.3 kJ/mol + 208.5 kJ/mol
1,2,4–三甲苯 偏三甲苯
5.1.2 命名
芳基:芳烃去掉一个氢原子剩下部分。
苯
苯基
苯甲基
(phenyl)
(苄基)
(Ph)
(benzyl, Bn)
2–甲苯基 邻甲苯基
o-tolyl
3–甲苯基 间甲苯基
m-tolyl
4–甲苯基 对甲苯基
p-tolyl
简单的芳烃的命名
简单的芳烃以苯环为母体,烷基等为取代基,称“某苯”。
在二取代苯之中,对位异构体对称性高、 结晶能大,熔点高;因此可以利用结晶方法从邻间
位异构体中分离对位异构体。
5.4 单环芳烃的化学性质
5.4.1 芳烃苯环上的反应
苯的π 电子云分别位于环的上下方,相当于电子源
(Lewis碱)。
当芳环与亲电试剂作用时,发生取代反应:
H + E Nu
E + H Nu
