齐逸翎 112017316002126 “蓝瓶子实验”最佳反应条件的探究
蓝瓶子实验

水/ml
Байду номын сангаас
1号
50
2号
50
3号
葡萄糖/g
氢氧化钠溶液 亚甲基蓝滴数 蓝色消失时间
2
2ml30% 10
1
2ml30% 10
结论2:通过上述实验现象说明溶 液碱性越强,蓝色消失时间越短
【实验二】溶液碱性强弱的影响
锥形瓶
水/ml
葡萄糖/g 氢氧化钠溶液 1号 2号 3号
亚甲基蓝滴数
蓝色消失时间
50 2 2ml30% 10
《蓝瓶子》实验
湖溪镇中 郭蓉美
一、本节课的主要内容包括 1、亚甲基蓝的变色原理 2、不同因素对实验快慢的影响 等实验过程与操作 。
二、实验目的:
1 、了解控制化学反应条件的作用 2 、通过观察亚甲基蓝和亚甲基白 在不同条件下的相互转化,学习 观察方法,体验对比实验法
仪器:托盘天平、药匙、烧杯、温度计、 锥形瓶三个、试管3支、橡皮塞、量筒 (50ml和10ml各一个)、秒表2块、胶 头滴管、酒精灯等 药品:0.1%亚甲基蓝、葡萄糖、蒸馏 水、30%NaOH溶液 、 20%NaOH溶液
五、蓝瓶子实验的影响因素 1.葡萄糖的加入量 2.溶液碱性的强弱 3.空气的量 4.亚甲基蓝的量
5.溶液的温度?
实验五现象:振荡后迅速变蓝,然后 迅速褪色,振荡周期时间明显加快。
结论5:实验五现象说明在一定温度 内溶液温度越高,蓝色消失时间越短
六、本实验注意事项
1、NaOH的用量不能太多,否则,溶 液变黄失效,NaOH浓度太高也会使 葡萄糖还原能力过强而导致无法变蓝。 2、水浴加热至40℃左右,水温不能 太高。否则,溶液变黄失效。 3、混合液静置较长时间后也会变成金 黄色而失效
实验五趣味实验三则蓝色振荡冰袋与固体汽水

趣味实验三则:蓝色振荡、冰袋与固体汽水一、实验教学目标了解并掌握本实验趣味实验的原理及其操作。
熟练各仪器的操作以及其中各种技能手段的的运用,试着去发现问题并体会其种种乐趣,感受我们的化学生活,生活化学。
二、实验原理1. 蓝色振荡亚甲基蓝的水溶液呈蓝色,在碱性条件下,葡萄糖可把它还原为无色,搅拌条件下空气会把无色产物(亚甲基白)氧化为蓝色,蓝色又被还原为无色,如此反应,实验能多次重复。
如果有酚酞试剂滴加的话,我们会发现颜色变化中还会多了红色与紫色。
原因是当溶液在碱性条件下时,滴加酚酞试剂滴加后溶液显红色。
所以:①当葡萄糖可把亚甲基蓝还原为无色时,由于溶液显强碱性,此时溶液呈红色;②搅拌或略微震荡条件下空气会把部分无色产物氧化为蓝色,由于紫色与蓝色相混,由于颜色的混合效应,我们将看到此时溶液显紫色③剧烈震荡后,将会有更多的无色产物被氧化为蓝色的亚甲基蓝,这时由于蓝色过深,将会遮掩酚酞的红色,结果我们将会看到溶液呈蓝色。
2. 便携式化学“冰袋”硝酸铵、氯化铵等铵盐,溶于水时具有强烈吸热降温的性质,它们还可以从与其相接触的晶体盐中夺取结晶水而溶解吸热,利用这种性质,可以通过简单地混合两种或两种以上的盐而制冷,制成化学“冰袋”。
该种便携式“冰袋”可应用于需简便制冷的场合,如外出郊游时,对饮料与食品的保鲜、制冷。
该实验主要是通过观察NaSO4·10H2O, NH4NO3, (NH4)2SO4混合后的制冷效果以及添加NaHSO4混合后的制冷效果,从而进行比较。
3. 固体汽水由于液体汽水运输昂贵,携带不太方便,因此我们根据液体汽水的配方及其生产流程略微改变一下,就是将其中的加压压缩CO2变为临时释放CO2气体。
其中实验药品很多跟实际生产中原料相同,有香精,蔗糖,柠檬酸,色素等。
其制备主要原理是将碳酸氢钠分散在明胶溶液中,然后烘干,接着于各种所需药品(香精,蔗糖,柠檬酸,色素)混合,饮用时取其部分,置于饮水器皿,倒入水溶解时柠檬酸会与碳酸氢钠反应,进而放出CO2。
蓝瓶子实验

光的波粒二象性是量子力学的基本原理之一
• 光既具有波动性,又具有粒子性
• 波粒二象性在20世纪初被爱因斯坦等科学家提出
⌛️
蓝瓶子实验是验证光波粒二象性的重要实验
• 实验由德布罗意提出
• 实验通过观察光在屏幕上形成的干涉图案来验证光的波动性
蓝瓶子实验在量子力学研究中的重要性
蓝瓶子实验为量子力学的发展提供了重要证据
蓝瓶子实验对科学发展的启示
蓝瓶子实验对科学教育的启示
• 实验强调了理论与实践相结合的重要性
• 实验培养了学生的创新意识和实践能力
蓝瓶子实验强调了实验在科学发展中的重要性
• 实验为理论提供证据,推动科学的发展
• 实验为科学技术的应用提供支持
蓝瓶子实验揭示了科学研究中的创新思维
• 实验提出了新的实验方法,拓展了科学研究的领域
• 实验培养了学生的创新意识和实践能力
谢谢观看
T H A N K Y O U F O R WATC H I N G
CREATE TOGETHER
DOCS
蓝瓶子实验的技术创新与改进
蓝瓶子实验的技术创新
• 实验采用光纤、激光等新技术
• 实验改进了实验装置,提高了实验精度
蓝瓶子实验的技术改进
• 实验优化了实验方法,提高了实验效率
• 实验提高了实验结果的可靠性
蓝瓶子实验在量子力学研究中的新进展
蓝瓶子实验在量子力学研究中的新进展
• 实验验证了光的波动性
• 实验为量子力学的基本原理提供了证据
D O C S S M A RT C R E AT E
蓝瓶子实验:探索光的波粒二象性
CREATE TOGETHER
DOCS
01
蓝瓶子实验的实验原理

蓝瓶子实验的实验原理1.引言蓝瓶子实验是一种简单而经典的化学实验,通过观察蓝瓶子溶液的变化,我们可以了解其中的化学反应原理。
本文将详细介绍蓝瓶子实验的实验原理及步骤,并解释其中的化学反应过程。
2.实验材料-蓝瓶子溶液(包含稀硫酸和过氧化氢)-碘化钾溶液-淀粉溶液-试管-实验台-比色皿-手套、安全眼镜等实验防护用品3.实验步骤1.在实验台上准备好碘化钾溶液和淀粉溶液,并将蓝瓶子溶液倒入试管中。
2.将试管倾斜放置,并缓慢加入碘化钾溶液。
观察试管内溶液的变化。
3.当溶液颜色变化停止时,停止加入碘化钾溶液,并记录下所需的碘化钾溶液的体积。
4.将溶液倒入比色皿中,并加入适量的淀粉溶液。
5.根据淀粉与碘的复合反应,观察溶液颜色的变化,并记录下颜色的深浅程度。
4.实验原理解析蓝瓶子实验是基于二氧化碳的生成反应原理进行的。
实验中的蓝瓶子溶液实际上是稀硫酸和过氧化氢的混合物。
以下是实验的化学反应过程:1.过氧化氢(H2O2)在稀硫酸(H2SO4)的催化下分解为水和氧气:```2H2O2(aq)→2H2O(l)+O2(g)```2.分解反应产生的氧气进一步与稀硫酸反应,生成二氧化硫(S O2):```H2SO4(aq)+O2(g)→S O2(g)+H2O(l)```3.二氧化硫与碘化钾反应生成碘酸钾(K I O3)、硫酸(H2SO4)和碘化氢(H I):```5S O2(g)+2K I(aq)+4H2O(l)→2K IO3(aq)+4H2SO4(aq)+2HI(aq)```4.碘酸钾与淀粉发生反应,形成蓝色络合物:```2K IO3(aq)+3H2S O4(a q)+3CH2O(n)→2I3-(a q)+3CO2(g)+3H2O(l)+3H+(a q)+K+(a q)+3H CO OH(a q)```综上所述,蓝瓶子实验通过二氧化碳生成及碘酸钾与淀粉的反应,形成了蓝色络合物的过程。
5.结论蓝瓶子实验的实验原理是基于稀硫酸和过氧化氢的分解反应和生成二氧化硫,进一步与碘酸钾反应形成蓝色络合物的化学反应过程。
蓝瓶子实验资料

【实验五】溶液温度的影响 将A、C试管置于40℃左右的水浴 中,几分钟后,再振荡,又静置 试管于水浴中,观察试管中蓝色 消失的时间
【 现象分析 】
由于亚甲基蓝被葡萄糖还原转化为还 原型,溶液褪色;振荡后,溶液上方的 氧气进入溶液,亚甲基蓝又转化为氧化 型,溶液又呈蓝色。在振荡与静置之间, 溶液中的氧气的量发生变化,溶液的颜 色也随之变化,直至溶液中的葡萄糖或 瓶中的氧气被耗尽,如此反复作用 。
锥形瓶
水/ml
1号
50
2号
50
3号
葡萄糖/g
氢氧化钠溶液 亚甲基蓝滴数 蓝色消失时间
2
2ml30% 10
1
2ml30% Βιβλιοθήκη 0结论2:通过上述实验现象说明溶 液碱性越强,蓝色消失时间越短
【实验二】溶液碱性强弱的影响
锥形瓶
水/ml
葡萄糖/g 氢氧化钠溶液 1号 2号 3号
亚甲基蓝滴数
蓝色消失时间
50 2 2ml30% 10
蓝瓶子实验原理:亚甲基蓝是一种氧化 还原指示剂,其氧化型呈蓝色,还原型 呈无色。从原理来看,亚甲基蓝的氧化 还原是一个可逆反应 。 亚甲基蓝
还原剂(葡萄糖) 亚甲基白 氧化剂(氧气)
说明:
1、蓝瓶子实验在碱性条件下才能 进行。
2、计时时间:从静置开始到溶液 褪色时间
结论1:通过上述实验现象说明葡 萄糖加入量越多,蓝色消失时间越 短 【实验一】葡萄糖加入量的影响
五、蓝瓶子实验的影响因素 1.葡萄糖的加入量 2.溶液碱性的强弱 3.空气的量 4.亚甲基蓝的量
5.溶液的温度?
实验五现象:振荡后迅速变蓝,然后 迅速褪色,振荡周期时间明显加快。
结论5:实验五现象说明在一定温度 内溶液温度越高,蓝色消失时间越短
蓝瓶子实验原理及过程

蓝瓶子实验原理及过程
嘿,朋友们!今天咱来聊聊超有趣的蓝瓶子实验呀!
你知道吗,这个蓝瓶子实验就像一场奇妙的魔法秀呢!想象一下,我们就像小小的魔法师,能让溶液在蓝色和无色之间变来变去,多神奇呀!
做这个实验,需要的东西也不复杂。
咱得有亚甲基蓝、葡萄糖、氢氧化钠这些玩意儿。
就像做饭需要食材一样,这些就是我们这场魔法的“原料”啦。
实验开始咯!先把亚甲基蓝、葡萄糖和氢氧化钠溶解在水里,这就好比是给魔法搭好了舞台。
然后呢,你就会看到溶液变成了蓝色,哇哦,就好像蓝色的小精灵在瓶子里跳舞呢!
接着神奇的事情发生啦!把溶液静置一会儿,它居然慢慢就变成无色了!这是为啥呢?嘿嘿,这就是这个实验的奥秘所在呀!其实呀,这是因为溶液里发生了一系列复杂的化学反应呢。
亚甲基蓝在氧气的作用下会变成蓝色,而葡萄糖呢,就像个小助手,能把氧气消耗掉,这样亚甲基蓝又变回无色啦。
是不是很有意思呀?
然后你再晃一晃瓶子,哇,又变蓝啦!就像给魔法施了一个咒语,蓝色瞬间又回来啦。
你可以不停地重复这个过程,看着蓝色和无色交替出现,就像一场色彩的狂欢!
这实验多好玩呀,不仅能让我们看到奇妙的化学现象,还能让我们感受到科学的魅力呢!在家里就可以做,叫上小伙伴一起,那得多有意思呀!而且通过这个实验,我们还能学到不少化学知识呢,这可不是死记硬背能比的哦。
做实验的时候,可得小心点,别把溶液洒出来啦。
就像走路要小心别摔跤一样,我们对待实验也要认真又谨慎呀。
所以呀,大家都快来试试这个蓝瓶子实验吧,让我们一起成为神奇的小魔法师,在化学的世界里尽情探索和玩耍!这绝对会是一次超级棒的体验,你难道不想试试吗?相信我,你一定会爱上这个有趣的实验的!。
化学实验11 蓝瓶子实验教案(版选修6)

实验1-1 蓝瓶子实验要点剖析蓝瓶子实验原理:亚甲基蓝是一种暗绿色晶体,溶于水和乙醇,在碱性溶液中蓝色亚甲基蓝很容易被葡萄糖还原为无色亚甲基白。
振荡此无色溶液时,溶液与空气中的接触面积增大,溶液中氧气的溶解量就增多,氧气把亚甲基白氧化为亚甲基蓝,溶液又呈蓝色。
静置溶液时,有一部分溶解的氧气逸出,亚甲基蓝又被葡萄糖还原为亚甲基白。
若重复振荡和静置溶液,其颜色交替出现蓝色—无色—蓝色—无色……的现象,这称为亚甲基蓝的化学振荡。
它是化学反应体系交替发生氧化与还原反应的结果。
由蓝色出现至变成无色所需要的时间是振荡周期,振荡周期的长短受反应条件如溶液的酸碱度、反应物浓度和温度等因素的显著影响。
典例剖析[例1]化学中有许多有趣的实验,如下介绍的“蓝瓶子”实验就是一例。
在250 mL平底烧瓶中依次加入2g氢氧化钠、100mL蒸馏水、2g葡萄糖(粉末),振荡使其溶解。
滴入4~6滴0.2%的亚甲基蓝溶液,塞上瓶塞(如图),振荡烧瓶,溶液呈蓝色。
静置,约3分钟后蓝色消失,变为无色。
再次振荡,无色溶液又呈蓝色。
可反复多次。
为探究是什么原因引起的,有人做了以下实验。
(1)从烧瓶中取出溶液注满一支试管,塞上橡皮塞。
试管中的溶液由蓝色变为无色,再振荡试管溶液不能变蓝。
(2)在原烧瓶中经A处鼓入空气,又慢慢变蓝了。
静置片刻后,蓝色又消失。
再次鼓入空气,又慢慢变蓝。
(3)为了进一步弄清是何种成分引起的,他又继续探索。
从A处改通纯净的N2、CO2,都不能使烧瓶中的无色溶液变蓝。
把制得的氧气从A处通入,发现上述无色溶液慢慢变为蓝色,到此为止,“蓝瓶子”实验原理有了科学结论,请总结“蓝瓶子”实验的变色原理:。
剖析:亚甲基蓝在碱性溶液中很容易被葡萄糖还原为无色亚甲基白,振荡此无色溶液时,溶液与空气的接触面积增大,溶液中氧气的溶解量就增多,氧气把亚甲基白氧化为亚甲基蓝,溶液又呈蓝色。
静置此溶液时有一部分溶解的氧气逸出,亚甲基蓝又被葡萄糖还原为亚甲基白,所以蓝色消失,变为无色。
蓝瓶子实验报告

蓝瓶子实验报告蓝瓶子实验报告引言:在科学研究中,实验是获取数据和验证理论的重要手段之一。
本次实验我们将进行蓝瓶子实验,通过观察和记录实验数据,探究蓝瓶子的特性和反应。
本文将详细介绍实验的步骤、结果和分析。
实验步骤:1. 准备工作:收集所需材料,包括蓝瓶子、水、酸、碱等。
2. 实验一:将蓝瓶子放入水中,观察其浮沉情况,并记录下来。
3. 实验二:将蓝瓶子放入酸中,观察其是否发生反应,并记录下来。
4. 实验三:将蓝瓶子放入碱中,观察其是否发生反应,并记录下来。
实验结果:1. 实验一结果表明,蓝瓶子在水中浮起,没有沉入底部。
2. 实验二结果显示,蓝瓶子与酸没有发生明显的反应。
3. 实验三结果表明,蓝瓶子与碱发生了反应,产生了气泡并溶解。
实验分析:1. 实验一中,蓝瓶子在水中浮起,这可能是由于蓝瓶子的密度小于水的密度,导致其浮力大于重力。
2. 实验二中,蓝瓶子与酸没有发生反应,这可能是因为蓝瓶子的材质不与酸发生化学反应。
3. 实验三中,蓝瓶子与碱发生了反应,产生了气泡并溶解。
这可能是由于蓝瓶子的材质与碱发生化学反应,产生了气体和溶液。
结论:通过本次实验,我们得出了以下结论:1. 蓝瓶子的密度小于水的密度,导致其在水中浮起。
2. 蓝瓶子的材质与酸不发生化学反应。
3. 蓝瓶子的材质与碱发生化学反应,产生气泡并溶解。
实验的意义和应用:蓝瓶子实验是对物质特性进行观察和分析的一种方法。
通过实验可以了解物质的密度、化学反应等特性,为后续的研究和应用提供基础。
在实际应用中,了解物质的特性可以帮助我们选择合适的材料、进行正确的处理和储存等。
实验的局限性和改进:本次实验虽然对蓝瓶子的特性进行了初步的观察和分析,但仍存在一些局限性。
首先,实验过程中可能存在人为误差,需要进行多次重复实验以提高结果的准确性。
其次,实验中使用的酸和碱种类有限,可以尝试使用更多种类的酸碱进行实验,以全面了解蓝瓶子的反应性质。
结语:通过蓝瓶子实验,我们对蓝瓶子的特性和反应进行了初步的了解。
蓝瓶子实验ppt课件

蓝瓶子实验原理:亚甲基蓝是一种氧化 还原指示剂,其氧化型呈蓝色,还原型 呈无色。从原理来看,亚甲基蓝的氧化 还原是一个可逆反应 。 亚甲基蓝
还原剂(葡萄糖) 亚甲基白 氧化剂(氧气)
说明:
1、蓝瓶子实验在碱性条件下才能 进行。
2、计时时间:从静置开始到溶液 褪色时间
结论1:通过上述实验现象说明葡 萄糖加入量越多,蓝色消失时间越 短 【实验一】葡萄糖加入量的影响
蓝瓶子实验
一、本节课的主要内容包括 1、亚甲基蓝的变色原理 2、不同因素对实验快慢的影响 等实验过程与操作 。
二、实验目的:
1 、了解控制化学反应条件的作用 2 、通过观察亚甲基蓝和亚甲基白 在不同条件下的相互转化,学习 观察方法,体验对比实验法
仪器:托盘天平、药匙、烧杯、温度计、 锥形瓶三个、试管3支、橡皮塞、量筒 (50ml和10ml各一个)、秒表2块、胶 头滴管、酒精灯等 药品:0.1%亚甲基蓝、葡萄糖、蒸馏 水、30%NaOH溶液 、 20%NaOH溶液
【实验五】溶液温度的影响 将A、C试管置于40℃左右的水浴 中,几分钟后,再振荡,又静置 试管于水浴中,观察试管中蓝色 消失的时间
【 现象分析 】
由于亚甲基蓝被葡萄糖还原转化为还 原型,溶液褪色;振荡后,溶液上方的 氧气进入溶液,亚甲基蓝又转化为氧化 型,溶液又呈蓝色。在振荡与静置之间, 溶液中的氧气的量发生变化,溶液的颜 色也随之变化,直至溶液中的葡萄糖或 瓶中的氧气被耗尽,如此反复作用 。
红瓶子实验
可用碱性藏花红代替亚甲基蓝会发 生红色-无色-红色反应 道理同上
锥形瓶
水/ml
1号
50
2号
50
3号
葡萄糖/g
氢氧化钠溶液 亚甲基蓝滴数 蓝色消失时间
《初探蓝瓶子实验》教学设计(省级优质课获奖案例)
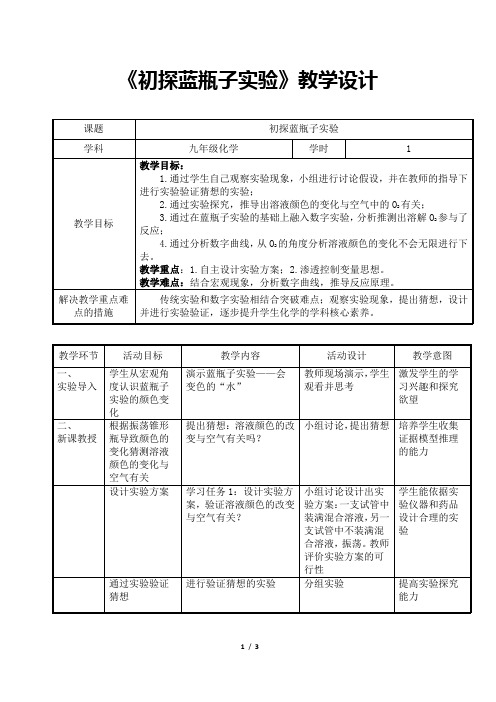
学生能依据实 验仪器和药品 设计合理的实 验
提高实验探究 能力
1/3
得出实验结论 根据所学化学 知识做出合理 猜想
得出结论:溶液颜色的改 学生汇报实验现象 变与空气有关 并得出结论 猜想溶液颜色的改变与 空气中的哪种气体有 关? 学生做出猜想: 1.N2;2.O2;3.稀有 气体;4.CO2;5.水 蒸气。 依据所学知识 排除稀有气体和水 蒸气 学习任务 2:设计验证实 设计出实验方案: 向 验方案,验证溶液颜色的 混合液中分别通入 改变与空气中的那种气 N2,O2,CO2 体有关? 学生分为 N2 组、O2 组、CO2 组进行实验 探究 得出结论:溶液颜色的改 学生汇报实验现象 变与空气中的 O2 有关 并得出结论 通过数字实验,利用氧气 和光学溶解氧传感器进 行定量实验 学生分析坐标系,观察数 字实验 学习任务 3:溶解 O2 参与 反应了吗? A- B 区域: B- C 区域: 始态气体 O2 和溶解 O2 与终 态气体 O2 和溶解 O2 之间的 关系 溶解 O2 参与了反应
三、 新课总结 四、 课后作业
提升能力
学生畅谈收获
学生自由发言
培养学生的证 据推理的化学 核心素养 用事实说明溶 液颜色的交替 出现不会无限 进行下去 提升学生的学 科素养 巩固落实 培养学生独立 思考敢于质疑 的科学精神
习题巩固
学生解答 2018 年安徽中 考化学第 14 题节选;还 想继续探究蓝瓶子实验 中的哪些方面
《初探蓝瓶子实验》教学设计
课题 学科 九年级化学 初探蓝瓶子实验 学时 1
教学目标
教学目标: 1.通过学生自己观察实验现象,小组进行讨论假设,并在教师的指导下 进行实验验证猜想的实验; 2.通过实验探究,推导出溶液颜色的变化与空气中的 O2 有关; 3.通过在蓝瓶子实验的基础上融入数字实验, 分析推测出溶解 O2 参与了 反应; 4.通过分析数字曲线, 从 O2 的角度分析溶液颜色的变化不会无限进行下 去。 教学重点:1.自主设计实验方案;2.渗透控制变量思想。 教学难点:结合宏观现象,分析数字曲线,推导反应原理。 传统实验和数字实验相结合突破难点;观察实验现象,提出猜想,设计 并进行实验验证,逐步提升学生化学的学科核心素养。
高中化学实验“蓝瓶子”实验学案

“蓝瓶子”实验学习目标:1、认识硫代硫酸钠和强酸反应的离子方程式和实验过程中产生的现象。
2、学会用对比的方法探究影响硫代硫酸钠与酸反应速率的诸因素。
3、体验观察和分析实验现象在化学实验研究中的重要作用。
4、能分析影响一个具体的化学反应的因素,并能设计简单的实验加以证实。
情感目标:通过硫代硫酸钠与酸反应速率的影响因素的学习,培养细致,认真的科学态度。
学习重点难点:硫代硫酸钠与酸反应速率的影响因素“蓝瓶子”实验原理:学习过程:【操作】(1)称取2g氢氧化钠固体,放入250mL锥形瓶中,加入100mL水使它溶解。
再加入2g葡萄糖,最后加入几滴亚甲蓝溶液(0.2%)到溶液呈蓝色。
溶液静置几分钟后变成无色。
(2)塞上橡皮塞,振荡后溶液变成蓝色,再静置一段时间,溶液中的蓝色又逐渐消失,再振荡溶液,蓝色又出现。
溶液的颜色能在蓝色和无色之间反复发生变化。
(3)称取4g氢氧化钠固体,放在250mL的锥形瓶中,加入100mL水使它溶解。
再加入2g葡萄糖,最后滴入1~2滴0.5%的碱性藏花红指示液。
塞上橡皮塞后按照上述相同方法操作。
刚振荡时溶液呈红色,静置片刻变成无色。
溶液的颜色也可以反复变化。
【说明】(1)用葡萄糖作还原剂,溶液应是碱性介质,在酸性介质或中性介质中不会产生变色现象。
(2)为了增加演示效果,可适当增大碱量,这样变色周期短,现象明显。
(3)碱性藏花红试剂用量宜少,只要略显出红色即可。
(4)上述两个变色反应的最佳温度是25℃,所以冬天演示要略加热。
一、药品:30%氢氧化钠,0.1%亚甲基蓝,蔗糖二、教材实验流程:(实验时室温16oC)步骤操作现象褪色周期注意点1 锥形瓶中加50mL水,1.5克葡萄糖,逐滴滴入8~10滴0.1%亚甲基蓝,振荡溶液呈蓝色2 加入2mL30%NaOH溶液,振荡试管,静置溶液褪色约25秒 NaOH的用量不能太多3 将溶液分装在两个小试管中,1号试管装满,2号试管装半管,均用塞子塞好,振荡,静置 1试管始终呈无色2试管振荡后变蓝,然后之下而上褪色约45秒4 把1号试管溶液分一半到3号试管中,再在3号试管中加5滴0.1%亚甲基蓝,塞好两支试管,振荡、静置 1试管振荡后变蓝,然后之下而上褪色 19秒3试管振荡试管后蓝色较1试管深,然后自下而上褪色 16秒5 将1、3号试管置于40oC水浴中,约2~3min后振荡、静置振荡后迅速变蓝,然后迅速褪色 2~3秒水浴加热至40oC,水温不能太高。
拓展课题4-1“蓝瓶子”的实验-苏教版选修实验化学教案

拓展课题4-1“蓝瓶子”的实验-苏教版选修实验化学教案1. 实验目的通过本次实验,学生将会学习以下内容:•学习硝酸银和氢氧化钠反应的化学方程式和反应类型;•了解沉淀反应,并通过实验观察产生的沉淀性质;•学习如何制备蓝色溶液。
2. 实验原理本实验中所用的“蓝瓶子”为硝酸银的水溶液,标记为AgNO3。
硝酸银的分子式为AgNO3,是一种无机化合物。
当硝酸银与氢氧化钠进行反应时,产生的生成物为AgOH和NaNO3。
同时,在该反应中,产生了白色的沉淀物,这是由于AgOH的产生造成的。
因此,此次实验是一种典型的沉淀反应实验。
学生可以通过实验观察产生的白色沉淀物性质,从而了解反应的特征及产物类型。
3. 实验步骤3.1 材料和设备•硝酸银水溶液(AgNO3);•氢氧化钠水溶液(NaOH);•蒸馏水;•酒精灯和灯盖;•火柴;•玻璃棒;•试管;•试管架。
3.2 操作步骤1.取两支试管,放入 2 mL 的AgNO3 溶液和 2 mL 的NaOH 溶液;2.用玻璃棒搅拌,观察溶液的变化和是否产生沉淀;3.用酒精灯加热制得的蓝色溶液,倒入已经生成沉淀的试管中;4.观察蓝色溶液与沉淀产生的反应。
4. 实验注意事项•实验中使用的试管和试管架需事先清洗干净;•氢氧化钠和硝酸银溶液为强腐蚀剂,请避免直接接触皮肤;•实验中的产生的气体有可能对人体产生危害,需进行适当通风;•酒精灯的使用要格外小心,避免发生火灾事故。
5. 实验结果和分析通过本次实验,我们观察到了二者反应的结果,产生的白色沉淀物及蓝色溶液。
白色沉淀物为纳米级的颗粒状,无臭,不溶于水,在光照下有着银镜一样的光泽,证明其为纳米 AgOH。
纳米 AgOH在光照下可以发生光催化反应,具有不错的催化活性。
蓝色溶液为含有配体的银配合物,经由 AgNO3 的原子和配体分子中的某一原子配位连接而成。
“蓝瓶子”颜色对着的某些颜色天然或荧光光源具有很强的发光作用。
此发光源在催化科技和有机发光领域具有很大的应用前景。
实验1-1蓝瓶子实验-人教版选修6实验化学教案

实验1-1蓝瓶子实验-人教版选修6 实验化学教案一、实验目的1.了解电解质概念。
2.掌握电解质溶液的导电性与浓度之间的关系。
3.了解电离程度的概念,初步了解不同电离程度的电解质的导电性表现。
二、实验原理蓝瓶子实验是一种用于观察强电解质与弱电解质的实验。
强电解质的电离程度比较高,能完全电离;而弱电解质只能部分电离,电离程度比较低。
这些性质会影响电解质在溶液中的导电性。
本实验利用电化学原理,测量浓度不同的强酸和弱酸所形成的电解质溶液的导电性,讨论不同浓度、不同电离程度的电解质导电性表现。
三、实验操作步骤3.1 实验器材与试剂准备1.带有刻度的量筒2.电导仪3.游离盐酸(HCl)和苯甲酸(C6H5COOH)标准溶液4.蒸馏水5.250mL锥形瓶6.滴定管3.2 操作步骤1.取一定的标准溶液测定其电导率,用量筒分别取出1mL、2mL、3mL、4mL、5mL5种体积的游离盐酸溶液,加入到250mL锥形瓶中,再用蒸馏水补至标线处,摇匀。
2.用同样方法制备苯甲酸溶液,各取1mL、2mL、3mL、4mL、5mL5种体积,加水至500mL,摇匀。
3.将制备好的游离盐酸和苯甲酸溶液置于电导仪内,记录其电导率,并用滴定管加入少量游离盐酸和苯甲酸到溶液内,继续测定其电导率。
4.分析不同浓度和不同酸的电离程度与导电性之间的关系。
四、实验记录与数据处理4.1 实验记录•测试游离盐酸溶液时,记录各浓度下的电导率。
•测试苯甲酸溶液时,记录各浓度下的电导率。
4.2 数据处理1.统计两组数据中的最小值与最大值,并求出平均值。
2.通过计算不同溶液的电导率之差,比较不同浓度和不同酸的电离程度与导电性之间的关系。
五、实验注意事项1.实验器材与试剂准备要充分。
2.操作时要保持仪器干净卫生。
3.操作过程中不要过分用力,避免损坏实验设备。
4.保存好实验样品和数据记录,注意实验室卫生和安全。
六、实验总结实验结果表明,浓度较高的电解质溶液导电能力更强,强酸的电离程度比弱酸的电离程度高,导电能力也更好。
蓝瓶子实验原理

蓝瓶子实验原理一、引言蓝瓶子实验是一种常见的化学实验,它可以用来检测硫酸根离子的存在。
在这个实验中,我们需要使用一些化学试剂和仪器,以便准确地测量样品中硫酸根离子的含量。
本文将详细介绍蓝瓶子实验的原理及其操作步骤。
二、实验所需物品1. 硫酸钠标准溶液2. 氯化钴红溶液3. 氢氧化钠溶液4. 蒸馏水5. 量筒、分析天平、滴定管、试管等三、实验原理1. 硫酸根离子检测原理:硫酸根离子(SO4^2-)与氯化钴红反应生成蓝色络合物(CoSO4·NH3)2·H2O),其反应方程式为:CoCl2·6H2O + Na2SO4 → CoSO4·NH3)2·H2O + 2NaCl + 6H2O其中,氯化钴红是指CoCl_2·6H_2O和氨水混合后形成的复配物。
在该反应中,硫酸根离子与氯化钴红反应生成的蓝色络合物,是一种可见光谱区间内的吸收峰,因此可以通过光谱分析来测量硫酸根离子的浓度。
2. 氢氧化钠溶液作用原理:在实验中,我们需要使用氢氧化钠溶液将样品中的硫酸根离子沉淀出来。
这是因为在碱性条件下,硫酸根离子会与铵盐反应生成不溶于水的沉淀(NH4)2SO4)。
(NH4)2SO4 + 2NaOH → Na2SO4 + 2NH3↑+ 2H2O由此可见,氢氧化钠溶液可以将硫酸根离子转化为不溶于水的沉淀,从而使其与其他物质分离开来。
四、实验操作步骤1. 样品制备:取一定量的待测样品,并将其加入到量筒中。
然后加入适量的蒸馏水,并搅拌均匀。
2. 滴定操作:取一定体积的待测样品,并加入适量的氯化钴红溶液。
然后滴加氢氧化钠溶液,直到出现棕色沉淀为止。
这表明硫酸根离子已经全部沉淀出来了。
3. 氯化钴红指示剂的加入:将氯化钴红指示剂加入到样品中,搅拌均匀。
此时,溶液会变成蓝色。
4. 光谱分析:使用光谱仪对样品进行测量,并记录吸光度值。
然后根据标准曲线计算出硫酸根离子的浓度。
五、实验注意事项1. 操作前应认真阅读实验操作步骤,并按照要求正确操作。
最新-测控设计2021学年高中化学选修6课件:112蓝瓶子实验 精品

亚甲基蓝
亚甲基白
一二
在碱性溶液中,蓝色亚甲基蓝很容易被葡萄糖还原为无色亚甲基 白。振荡此溶液时,溶液与空气的接触面积增大,溶液中氧气的溶 解量就增多,氧气把亚甲基白氧化为亚甲基蓝,溶液又呈蓝色。当 瓶子静置时,有一部分溶解的氧气逸出,溶液里葡萄糖所起的还原 作用渐渐起主导作用,其颜色将由蓝色变为无色。颜色可以重复变 化,直到所有的葡萄糖都被氧化完毕或溶液内的氧气耗尽为止。
第2课时 蓝瓶子实验
1.形成严谨求实的科学态度,具有批判精神和创新意识。 2.认识反应条件的控制在化学研究中的作用和意义,初步掌握控 制反应条件的一些方法。
一二
一、实验成功的关键 对每一个具体的化学实验而言,控制好实验条件极为重要。控制 一些条件不变,研究某一因素对反应影响的实验方法已经成为最常 用的一种科学方法。控制实验的条件可以从以下几个方面来考虑: 控制实验的外界条件,如温度、压强、浓度等;控制实验的操作方 法,如操作的顺序、操作的要点。
一二
二、蓝瓶子实验 1.影响化学反应速率的因素 (1)内因:物质的性质,是化学反应速率的决定性因素,因此,不同的 化学反应具有不同的反应速率。 (2)外因:浓度、温度、压强、催化剂等外界条件。由于受这些外 界条件的影响,同一个化学反应在不同的外界条件下可能会有不同 的化学反应速率。 2.蓝瓶子实验原理
由于温度升高,反应速率加大,所以在40 ℃的水浴中溶液的褪色 速率加大,振荡周期变短,这时操作计时器的动作要快速准确。另 外水浴加热时温度计应放在水浴的中间位置,控制温度在40 ℃左 右。水浴的温度不宜太高,否则振荡的周期过短,不利于记录实验 现象。
5.振荡过程中由于蓝色并不是立刻全部褪去,所以必须振荡至蓝 色完全褪去。认真记录实验现象,对于振荡周期的记录要仔细。
“蓝瓶子”实验的改进及其在食品化学实验教学中的应用

“蓝瓶子”实验的改进及其在食品化学实验教学中的应用顾颖颖;崔雷【期刊名称】《广州化工》【年(卷),期】2016(000)003【摘要】Erioglaucine disodium salt can be used instead of methylene blue in the classic blue bottle experiment demonstration. Food items containing brilliant blue and reducing species such as sugars or vitamin C can therefore be used at the heart of this demonstration, which simply requires the addition of strong base such as sodium hydroxide. The use of foods in experiments can greatly enhance students’ interest and improve the understanding of food chemistry.%为了提高学生对相关食品化学的理解,设计使用了食品添加剂亮蓝取代传统“蓝瓶子”实验中所使用的染料———亚甲基蓝。
直接采用含有亮蓝和一些还原试剂(蔗糖或维生素C)的食品和饮料在外加氢氧化钠的作用下可以成功的重复“蓝瓶子”实验。
该实验在食品化学实验教学中的应用,能大大加深学生对氧化还原反应的理解,增强实验的兴趣并提高对食品添加剂的认识。
【总页数】2页(P198-199)【作者】顾颖颖;崔雷【作者单位】上海理工大学理学院,上海 200093;上海理工大学理学院,上海200093【正文语种】中文【中图分类】G642【相关文献】1.利用数字化实验探究"蓝瓶子"实验的影响因素——以碱的浓度对其影响为例 [J], 沈小祥2.“蓝瓶子”变“彩瓶子”的实验探究 [J], 刘文明;王应红;李佳芳;万东海3.基于问题的教学模式在食品化学实验教学中的应用——以淀粉性质实验为例 [J], 冯霞4.中学化学中"蓝瓶子"实验的探究性实验教学 [J], 王兴高5."蓝瓶子"实验的教学功能及改进 [J], 任有良;张国春;周春生因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《化学实验教学研究》实验报告
实验项目“蓝瓶子实验”最佳反应条件的探究实验日期星期四上午□√下午□晚上□姓名学号同组人台号
实验目的:
1.了解“蓝瓶子实验”的反应原理
2.初步学习用简单比较法探究“蓝瓶子实验”的最佳反应条件实验教学目标:
知识与技能:
1.了解亚甲基蓝的变色原理及蓝瓶子实验的实验基本原理;2.知道简单比较法的原理并能够较为熟练地运用;
3.掌握“蓝瓶子实验”的最佳反应条件。
过程与方法:
1.学习通过简单比较法对实验最佳条件进行探索的方法;2.通过设计实验培养学生的实验探索能力、逻辑思维能力以及动手能力。
情感态度与价值观:
1. 通过团队合作培养学生的团队合作意识,提高科学素养;
2. 通过化学知识点的应用,增强学生学习化学的兴趣,感受化
学的神奇魅力。
实验原理:
亚甲蓝是一种氧化还原指示剂,易溶于水,能溶于乙醇。
在碱性条件下,盛放在锥形瓶中的蓝色的亚甲蓝溶液可以被葡萄糖还原成无色的亚甲白溶液。
亚甲蓝与亚甲白的结构式分别如图1和图2所示:
振荡锥形瓶中的混合液时,使其溶入空气或氧气后,亚甲白被氧气氧化成亚甲蓝,致使该混合液又呈现蓝色。
若静置混合液,亚甲蓝又被葡萄糖原成无色的亚甲白。
如此反复振荡、静置锥形瓶,其混合液在蓝色与无色之间互变,故称为蓝瓶子实验。
其变色原理为:
这种现象又称为亚甲蓝的化学振荡。
由蓝色出现至变成无色所需要的时间称之为振荡周期,振荡周期的长短受反应条件如亚甲蓝溶液的最佳溶剂选择、反应温度、氢氧化钠的用量等因素的影响。
其中,亚甲蓝在葡萄糖与氧气反应中起着催化作用。
实验设计(或改进)思路:
在125ml的锥形瓶中加入一定量的3%的葡萄糖溶液、30%的氢氧化钠溶液,再滴加一定量的0.1%的亚甲基蓝溶液后精致,观察溶液颜色由蓝色变为无色后,在一定时间内以一定频率震荡锥形瓶至溶液的颜色又变为蓝色,如此反复,记录经历5个震荡周期所需要的时间。
第一,教材中给出的记录方式是记录在5min或10min内的震荡周期,但是在实际操作中,我们是记录5个震荡周期所需要的时间,我认为这样的方法更加方便直观,而且主观性没有那么强;第二,在进行实验操作时,因为本实验设计颜色变化,在震荡锥形瓶时应该以一张白色的A4纸为背景,这样方便观察颜色变化。
这两点是对教材实验设计内容的改进。
在本实验中,影响震荡周期有这几个主要因素:亚甲基蓝的用量、葡萄糖溶液的用量、氢氧化钠溶液的用量、温度等等。
此次实验我们探究的是前三个影响因素对震荡周期的影响。
实验研究的主要内容:
1.3%的葡萄糖溶液用量的探究;
2. 30%的氢氧化钠溶液用量的探究;
3.0.1%的亚甲基蓝溶液用量的探究
实验研究方案及实验记录:
实验内容:应用简单比较法,在3%葡萄糖溶液用量、30%氢氧化钠溶液用量、0.1%亚甲基蓝溶液这三个变量中,固定两个因素、改变一个因素的方法,通过记录5个振荡周期所需要的时间来探索蓝瓶子实验的最佳条件。
(本实验周期记为溶液由“蓝色——无色——蓝色”为一个周期)具体实验设计如下:
一、葡萄糖浓度探究
序号3% C6H12O6
/mL
3% NaOH
/mL
0.1% 亚甲基蓝
/滴
5个振荡周期所需要的
时间/s
1 30
3 6 150
2 20+10 ml蒸馏水179
3 10+20 ml蒸馏水187 结论加入30ml 30%葡萄糖时,变色周期最短。
二、氢氧化钠浓度探究
序号3% C6H12O6
/mL
3% NaOH
/mL
0.1% 亚甲基蓝
/滴
5个振荡周期所需要的
时间/s
1
30 3
6
152
2 2 159
3 1 183 结论加入3ml 3%氢氧化钠溶液时,变色周期最短。
三、亚甲基蓝浓度探究
序号3% C6H12O6
/mL
3% NaOH
/mL
0.1% 亚甲基蓝
/滴
5个振荡周期所需要的
时间/s
1
30 3 6 152
2 4 133
3 2 129 结论加入2滴亚甲基蓝溶液时,变色周期最短。
问题与讨论:
1.实验采用的是简单比较法,探究“蓝瓶子实验”的最佳反应条件。
在反应过程中,需要不断震荡锥形瓶,但是由于人为因素,不可能保证每次实验的震荡频率都相同,即不可能保证每次氧气的进入量都相同。
因此也会带来一定的实验误差;
2.温度也是本实验一个重要影响因素。
在实验过程中,是默认了室温不会改变,但是温度也会随着实验时间的改变而改变。
因此也会产生一定的实验误差;
3.在探究3%葡萄糖溶液用量的时候,为了保持总体积一致,可以控制溶液的浓度,能够准确地控制变量,例如在葡萄糖用量的探究中,在加入20 ml或者10 ml的葡萄糖溶液时,要相应地加上蒸馏水。
参考文献:
[1]熊言林,王闯.2010.蓝瓶子实验最佳反应条件的探究.化学教学,(10):16—18.
[2]熊言林.2001.一个激趣启思的化学实验设计——亚甲基蓝反复变色的实验.化学教育,(2):37-38
[3]张燕,韩金根.“蓝瓶子”实验拓展[J]. 化学教与学,2012,10:93+61.
[4]高仲虹. 《蓝瓶子实验》剖析[J]. 中学生数理化(高二版),2011,04:37-39.
[5]张守林,马宏佳. 围绕“蓝瓶子”实验的探究活动设计[J]. 化学教学,2003,04:24-25.。
