分子光谱分析Chapter01
分子发光光谱法

内转换
内转换:同多重度电子能级中,等能级间的无辐 射能级交换。 通过内转换和振动弛豫,高激发单重态的电子 跃回第一激发单重态的最低振动能级。
外转换 外转换:激发分子与溶剂或其他 分子之间产生相互作用而转移能 量的非辐射跃迁; 外转换使荧光或磷光减弱或“ 猝灭”。
系间跨越 系间跨越:不同多重态,有重叠的转动能级间的非 辐射跃迁。 改变电子自旋,禁阻跃迁,通过自旋—轨道 耦合进行。
荧光强度对温度变化敏感。
一般地,随温度降低,溶液中荧光物质的量子效率和荧光强
度将增大,并伴随光谱的蓝移。温度增加,碰撞频率增加, 使外转换的去激发几率增加。
(3) pH的影响
对酸碱化合物,溶液pH的影响较大,需要严格控制; 如苯胺:在pH 5-12溶液中,以分子形式存在,有荧光。
pH< 5时以苯胺阳离子形式存在,无荧光
ex em
(3)可变波长同步扫描荧光法:使两单色器在扫描过程中以 不同的速率同时进行扫描,即波长可变。
同步扫描荧光法的特点:
优点:
(1)使光谱简化; (2)使谱带窄化;
(3)减小光谱的重叠现象;
(4)减小散射光的影响。
例如:采用同步扫描技 术检测如图萘、蒽、菲 、芘混合物,可简化光 谱,减少光谱重叠,提 高分辨率。 缺点: 因为同步扫描荧光损失了 其它光谱带所含的信息, 对光谱学的研究不利。
比较法:
在线性范围内,测定标样和试样的荧光强度,直接
比较。
三、荧光分析法的应用
可采用直接测定法或间接测定(荧光猝灭)法
1、无机化合物的分析
与有机试剂配合物后测量;可测量约60多种元素。 铍、铝、硼、镓、硒、镁、稀土常采用荧光分析法; 氟、硫、铁、银、钴、镍采用荧光熄灭法测定; 铜、铍、铁、钴、锇及过氧化氢采用催化荧光法测定; 铬、铌、铀、碲采用低温荧光法测定; 铈、铕、锑、钒、铀采用固体荧光法测定
分子荧光与磷光光谱分析法

2.激发态→基态的能量传递途径
电子处于激发态是不稳定状态,返回基态时,通过辐射 跃迁(发光)和无辐射跃迁等方式失去能量; 传递途径 辐射跃迁 无辐射跃迁
荧光
延迟荧光
磷光
系间跨越 内转移
外转移
振动弛预
激发态停留时间短、返回速度快的途径,发生的几率大, 发光强度相对大。 荧光:10-7~10 -9 s,第一激发单重态的最低振动能级→基态 磷光:10-4~10s;第一激发三重态的最低振动能级→基态
5.溶液荧光的猝灭
碰撞猝灭; 氧的熄灭作用等。
2018/8/27
一、 仪器与结构流程 第二节 instrument and general 分子荧光与磷光分析法 process 二、 荧光分析法和应用 molecular fluorescence and fluorescence analysis and phosphorescence analysis application 三、 磷光分析法的应用 phosphorescence analysis and application
迁也然。
2018/8/27
荧光激发光谱
荧光发射光谱
200
250
300
350
400
450
蒽的激发光谱和荧光光谱
500 nm
2018/8/27
三、荧光的产生与分子结构的关系
relation between fluorescence and molecular structure
1.分子产生荧光必须具备的条件
外转换使荧光或磷光减弱或“猝灭”。
系间跨越:不同多重态,有重叠的转动能级间的非辐射跃迁。 改变电子自旋,禁阻跃迁,通过自旋—轨道耦合进行。
仪器分析——第一章紫外-可见分子吸收光谱法课件

PPT学习交流
3
一.紫外光 (ultraviolet light) 和可见光 (visible light)
光是一种电磁辐射(Electromagnetic radiation)或 叫电磁波(Electromagnetic wave) 能被人们看见的光称为可见光。
各种看不见的光,如紫外光、红外光、X-射线、 -射线等,它们也都是某一波长区域的电磁辐射。
吸光光度法按所用的和测量光的 单色程度不同,可分为比色法和分光 光度法。光的单色程度是指光的波长 范围的宽窄程度。
PPT学习交流
10
1.比色法 (Colorimetric method)
比色法是指应用单色性较差的光 与被测物质作用建立起来的分析方法, 它只能在可见光区使用。
PPT学习交流
11
(1).目视比色法
PPT学习交流
6
(1)复合光(Polychromatic light) 与单色光(Single - color light)
如果让一束白光通过三棱镜,它将分解为红、橙、 黄、绿、青、蓝、紫七种颜色的光,这种现象称为光 的色散(Chromatic dispersion)。我们把白光叫做 复合光,把只具有一种颜色的光叫做单色光。
18
2. 分子吸收光谱
(Molecular Absorption Spectrum)
(1) 产生及分类 紫外、可见光的能量与分子中价电子 跃迁吸收的能量相适应,所以紫外-可见 光谱属于分子吸收光谱。
PPT学习交流
19
分子内部的运动可分为价电子运动、分子
内原子在平衡位置附近的振动和分子绕其重心
的转动,则分子中存在三种能量,而三种能量
PPT学习交流
13
分子光谱分析Chapter01

0.3 Differences between emission and absorption of radiation 吸光:基态→电子各激发态跃迁 吸光:基态→电子各激发态跃迁; 发射: υ 发射:S1(υ=0)→S0(υ=i)的辐射跃迁 υ 的辐射跃迁;
分别携带被观察物体的激发态或基态信息 信息, 分别携带被观察物体的激发态或基态信息,可以从不同侧面 激发态 了解物质的内部结构。 了解物质的内部结构。
发光概述?chp1荧光分析?principleoffluorimetry荧光的原理?thefluorescencemechanism荧光方法?characteristicsoffluorescencespectrum荧光光谱特性?fluorescencedecayandlifetime荧光衰减和寿命?quantumyield量子产率?fluorescenceintensity荧光强度01发光现象luminescentphenomena煤气燃烧蓝色火焰炽热铁丝黄色火焰煤气燃烧蓝色火焰炽热铁丝黄色火焰发光介绍introductiontoluminescence荧光灯管电激发发光白炽灯泡发光汞灯365nm3brcarbazole奇特磷光奇特磷光ex363nm光棒化学反应发光汞灯365nmfonkos菌悬浮液takenfromdrternuraevenmanysinglecelledorganismsarebioluminescent
二、发光的类型 (Type of luminescence )? • Photoluminescence (光致发光 光致发光): 光致发光 Fluorescence/Fluorimetry; Phosphorescence/Phosphorimetry; • Chemiluminescence (化学发光 化学发光); 化学发光 • Bioluminescence (生物发光 生物发光); 生物发光 • Radioluminescence (辐射发光 辐射发光); 辐射发光 • Electroluminescence(电致发光 电致发光); 电致发光 • Sonoluminescence(声致发光 声致发光); 声致发光
分子荧光光谱法

菲
线状环结构比非线状 结构的荧光波长长
• 芳香族化合物因具有共轭的不饱和体系, 芳香族化合物因具有共轭的不饱和体系, 多数能发生荧光 • 多环芳烃是重要的环境污染物,可用荧光 多环芳烃是重要的环境污染物, 法测定 • 3,4 - 苯并芘是强致癌物 , 苯并芘是强致癌物
λ ex = 386 nm λem = 430 nm
(二)荧光与有机化合物结构的关系
物质只有吸收了紫外可见光,产生π 物质只有吸收了紫外可见光,产生π → π*,n → π* 跃迁, 跃迁,产生荧光 跃迁相比,摩尔吸收系数大10 π → π*与n → π*跃迁相比,摩尔吸收系数大102~103, 寿命短 跃迁常产生较强的荧光, π → π*跃迁常产生较强的荧光, n → π*跃迁产生的 荧光弱
1. 电子自旋状态的多重性
大多数分子含有偶数电子,基态分子每一个轨道 大多数分子含有偶数电子, 中两个电子自旋方向总是相反的↑↓ 中两个电子自旋方向总是相反的↑↓ ,处于基态单 重态。 当物质受光照射时, 重态。用 “S0” 表示 ;当物质受光照射时,基态 分子吸收光能产生电子能级跃迁, 分子吸收光能产生电子能级跃迁,由基态跃迁至 更高的单重态,电子自旋方向没有改变, 更高的单重态,电子自旋方向没有改变,净自旋 = 0 .这种跃迁是符合光谱选律的 第一激发单重态 S1
VR S2 IC VR S1 ISC
VR:振动驰豫 : IC:内部转换 : ISC:系间窜跃 :
T1
S0 吸光 吸光
S0
3. 荧光光谱的产生—辐射去激 荧光光谱的产生—
处于S 处于S1或T1态的电子返回S0态时,伴随有发光现 态的电子返回S 态时, 象,这种过程叫辐射去激 发光 S0 S1或T1 荧光: (1)荧光: 当电子从第一激发单重态S 当电子从第一激发单重态S1的最低振动能级回到基 态S0各振动能级所产生的光辐射叫荧光 荧光是相同多重态间的允许跃迁,产生速度快, 荧光是相同多重态间的允许跃迁,产生速度快, 10-9~10-6s,又叫快速荧光或瞬时荧光,外部光源停 又叫快速荧光或瞬时荧光, 止照射, 止照射,荧光马上熄灭 无论开始电子被激发至什么高能级,它都经过无辐 无论开始电子被激发至什么高能级, 射去激消耗能量后到S 的最低振动能级,发射荧光, 射去激消耗能量后到S1的最低振动能级,发射荧光, 荧光波长比激发光波长长。 荧光波长比激发光波长长。 λ 荧>λ激
分子荧光光谱分析

分子荧光光谱分析分子荧光光谱分析的原理是基于分子的激发态能级和基态能级之间的电子跃迁。
当分子受到外界的激发能量(如光能)时,部分分子中的电子从基态跃迁到激发态。
当电子从激发态返回基态时,会释放出荧光光子,其能量与激发态的能级差相关。
这种发光现象被称为荧光。
荧光光谱是通过测量荧光发射的强度和波长来获得的。
通常情况下,荧光光谱的波长范围较宽,可以从紫外到可见光甚至红外。
荧光峰的位置和强度可以提供分子的结构信息,如它们的共振结构、官能团的位置和取代基的影响等。
因此,荧光光谱分析被广泛应用于有机分析化学、生物化学、医药化学等领域。
在分子荧光光谱分析中,常用的实验方法包括荧光激发光谱、荧光发射光谱和荧光寿命测量。
荧光激发光谱是测量分子在不同激发波长下产生的荧光发射强度的方法。
通过测量不同波长的激发光强度和相应的荧光发射强度,可以绘制激发光谱图。
从激发光谱图中,可以确定最佳的激发波长和激发强度,以获得最大的荧光发射信号。
荧光发射光谱是测量荧光信号的强度和波长的方法。
在荧光发射光谱实验中,分子在固定的激发波长下,通过改变检测器的波长来测量荧光光谱。
从荧光发射光谱图中,可以观察到不同波长下的荧光发射峰,并判断荧光光谱的特征。
荧光寿命测量是测量分子从激发态退激发到基态的时间的方法。
荧光寿命是荧光信号从达到最大强度到减少到原始强度的时间。
荧光寿命的测量可以提供有关分子动力学和化学反应速率的信息。
分子荧光光谱分析在许多领域有着广泛的应用。
例如,在环境监测中,可以通过测量水中有机物的荧光光谱来检测水中有机污染物的存在和浓度。
在生物药物研究中,荧光标记的分子可以用于检测和定量分析生物标志物的表达和鉴定。
此外,荧光光谱分析还可以用于材料科学、食品分析等许多其他领域。
总之,分子荧光光谱分析是一种重要且常用的分析方法,通过测量荧光发射的强度和波长可以获得分子的结构和性质信息。
不同的实验方法可以用于研究不同的分子特性和反应过程。
仪器分析原理4分子电子光谱分析

(d)
s轨道 重叠
p轨道 重叠
未成键电子称为非键电子或n电子。
有机化合物分析吸收紫外-可见辐射后,主要涉及两种 类型的电子跃迁:
(1) 成键轨道和反键轨道之间的跃迁 σ→σ*、π→π*
(2) 非键电子激发到反键轨道的跃迁
n→σ*、n→π*
*
反键
* * *
反键
* *
能量 n
n
n 非键
成键
原因: 极性溶剂使π、π*轨道和n电子的能级都下降,但
是n电子由于与极性溶剂形成氢键,使n电子基态的能
量降低更多(稳定),所以,n→π*能量差增加,吸收带
紫移,而π→π*跃迁能量差变小,所以,吸收带红移。
如图:
无溶剂效应
*
E1 E2
能量
n
溶剂效应
*
E1' E2'
n
溶剂的选择 : (1) 尽量选择极性低的溶剂; (2) 能很好地溶解被测物,并且有良好的化学和 光化学稳定性; (3) 溶剂在样品的吸收光谱区无明显吸收。
§4.1.2 金属配合物的吸收带 (有机显色剂与金属配合物)
电荷转移跃迁
金属配合物的吸收
配位场跃迁
键合跃迁
1. 电荷转移跃迁 配合物由配合中心离子M和配位体L组成。配合物分子吸 收辐射后,分子中的电子从主要定域在金属离子M的轨 道上转移到配位体的轨道上,或按相反方向转移,这种 跃迁叫做电荷转移,产生的光谱为电荷转移光谱。
2020/6/2
3. 非平行光束引起的偏离 非平行光使入射角增大,反射光的强度随之而增加,从而 增加了反射分数,使吸光度增大,产生正偏差。 另外,非平行使光程增加引起的系统误差(正偏差)。
分子光谱

E
注意到上述方程中的第一和第二项都和电子坐标无关。采用 分离变量处理,得到两个方程:
核运动方程
N
2 2MN
2 N
VNN
Ee (R)N
(R)
EN
(R)
该方程中包含了分子的平动、振动和转动,它 决定了分子的振动光谱和转动光谱。
电子运动方程
电子运动方程决定了分子的电子光谱。
Hˆ(R, r) E(R, r)
Hˆ N N (R) EN N (R)
Hˆ ee (R, r) Eee (R, r)
质心坐标 (扣除体系平动)
球极坐标 (分离转动振动)
单电子独立近似
hˆii (R, ri ) ii (R, ri )
LCAO-MO 如EHMO,HMO等
SCF-MO 如ab-initio等
1.1.2 分子光谱的分布和特征
红
短波红外
外
中红外
线
热红外
1.3~3 微米 3~8 微米 8~14 微米
转动光谱 <10cm-1
远红外
14 微米~1 毫米
分子的总能量主要由以下三项组成
E Ee Er Ev
分子在两个能级之间的跃迁给出 了光谱:
~ 1/ (E2 E1) / ~e ~v ~r
转动光谱:同一振动态内不同转动能级之间跃迁所产生的光
显然,只有当 x mn 、 y mn和 z mn 不全为零时,跃迁才可
能发生,称为跃迁允许,反之,称为跃迁禁阻。
使 x mn 、 y mn 和 z mn 不全为零的条件,称为光谱选律。
光谱选律的确定,还可以借助群论作为工具
1.1.4 线形和线宽
谱线不是线,它有一定的宽度
频率 不同温度下的光谱线宽
光学分析法---分子光谱分析法1

磷光发射
激发态分子经过系间跨跃到达激发三重态后, 并经过迅速的振动弛豫到达第一激发三重态(T1) 的最低振动能级上,从T1态分子经发射光子返 回基态.此过程称为磷光发射。 磷光发射是不同多重态之间的跃迁.(即T1-S0) 故属于“禁阻”跃迁,因此磷光的寿命比荧光 要长得多,约为10-3到10s。所以,将激发光从 磷光样品移走后,还常可观察到后发光现象, 而荧光发射却观察不到该现象。
化学发光分析仪
系间跨越
系间跃迁是不同多重态之间的一种无辐射跃 迁.该过程是激发态电子改变其自旋态,分子 的多重性发生变化的结果.当两种能态的振动 能级重叠时,这种跃迁的概率增大. S1-T1跃迁就是系间跨跃的例子,即单重态到三 重态的跃迁.即较低单重态振动能级与较高的 三重态振动能级重叠.这种跃迁是“禁阻” 的.
分光光度法的灵敏度
灵敏度值标准曲线的斜率,即A=εbc中的 系数εb,在分光光度法中主要由ε决定, 及待测物质或显色剂的本身特性决定 由于吸光度A不受光源强度的影响,分光 光度法的灵敏度与光源强度无关,但光 源强度可以影响灵敏度检测的准确性和 稳定性。
It A = εbc = − lg T = − lg I0
荧光强度与浓度成正比
I f = 2.303Φ f I 0εbc
上述关系只适用于低浓度溶液,高浓度 时荧光强度与浓度不成线性关系 可通过提高光源强度来提高荧光分析的 灵敏度 通常使用标准曲线法进行荧光定量分析
分子磷光分析简介
磷光强度受环境的影响非常明显 分析方法:低温磷光,室温磷光 磷光强度与浓度的关系与荧光强度相同
分子荧光分析
荧光量子产率 荧光激发光谱、发射光谱及其特征 荧光光谱仪 荧光光谱法的应用
荧光量子产率
发荧光的分子数与总的激发态分子数之 比,或物质吸光后发射荧光的光子数与 吸收的激发光的光子数之比。
分子光谱法

有d→d* 跃迁和f→f*跃迁。这类跃迁 必须在配体的配位场作用下才有可能产生。
3. 金属离子影响下的配位体π→π*跃迁
吸光光度法中,所使用的显色剂大多数都 含有生色团,其本身为有色化合物,当与金属 离子配位时,作为配体的显色剂,其共轭结构 发生了变化,导致吸收光谱的红移或紫移。
二、 紫外可见分光光度计
2. 分子磷光:处于最低单重激发态的分子以无辐 射弛豫方式进入第一最低三重激发态,再由三重 激发态跃迁回到基态而发出的光。
分子荧光和磷光同属光致发光,磷光发射则 在超过10-5s后发生,并且在激发的电磁辐射停止 照射后,仍能持续数分钟至数小时。
3. 化学发光:是化学反应物或反应产物受反应释 放的化学能激发而产生的光辐射。
1. 电子跃迁的类型
基态有机化合物的价电子包括成键电子、成键 电子和非键电子(以 n表示)。分子的空轨道包括 反键 *轨道和反键*轨道,因此,可能的跃迁为 *、*、n* n*等。
* *
跃迁能量大小:
n
σ→σ* > n→σ* > π→π* >
n→π*
*
*
n
1) σ→ σ* 跃迁:
饱和烃(甲烷,乙烷)
5)稠环芳烃及杂环化合物
稠环芳烃,如奈、蒽、芘等,均显示苯的三个吸收带, 但是与苯本身相比较,这三个吸收带均发生红移,且强度 增加。随着苯环数目的增多,吸收波长红移越多,吸收强 度也相应增加。
当芳环上的-CH基团被氮原子取代后,则相应的氮杂 环化合物(如吡啶、喹啉)的吸收光谱,与相应的碳化合 物极为相似,即吡啶与苯相似,喹啉与奈相似。此外,由 于引入含有n电子的N原子的,这类杂环化合物还可能产 生n*吸收带。
能量最小,λ 200~400nm(近紫外区)
12-分子光谱分析法
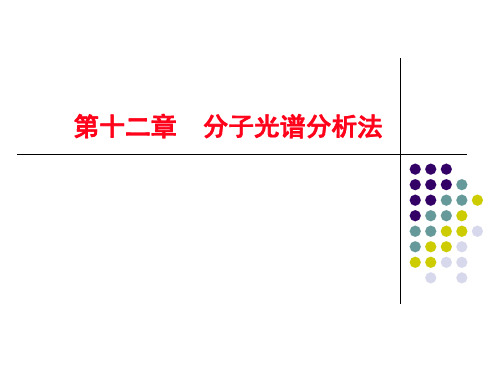
3.定量基本关系式
稀溶液中,样品的荧光强度If正比于浓度c,据朗白-比耳 定律可导出 If=kqI0bc (12-9) 式中:k——荧光仪器常数; q——荧光量子产率,表征处在电子激发态的分子 发射荧光的几率。分子荧光量子产率(q)的定义为 q=发射的光子数/吸收的光子数 (12-10) 由于q值测量很困难,因而在实际工作中经常使用相对荧 光强度,而不用绝对荧光强。
分子荧光与有机化合物结构的关系
在苯环上有取代基时会 表12-6 取代基对苯环荧光的影响 引起最大吸收波长位移。 取代基常常影响荧光效 率。
荧光强度随卤素相对原 子质量的增加而降低 羧酸或羰基取代基对荧 光发射起抑制作用
分子荧光与有机化合物结构的关系
具有刚性结构的分子特别有利于荧光增强,例如在类似测 试条件下芴和联苯的量子效率分别为1.0和0.2。 将荧光染料吸附到固体表面上会增加荧光强度。 升高体系的温度对大多数分子都会降低荧光量子效率 。 溶剂极性也对荧光有重要影响。含重原子(如Br、I)的溶剂 或其它溶质会减小分子的荧光强度 顺磁性分子的存在(例如溶液中分子氧)会增强系间窜跃机 会,结果会使荧光强度减小。 另外,带酸或碱取代基的芳香化合物的荧光一般是pH值 敏感性的。对于离子化和非离子化的化合物形式,其波长 和发射强度二者都不相同。
什么是助色团?
有些官能团(含有未共享电子,即非键电子,亦称 为n电子或p电子)本身并不在紫外区产生吸收,但 它们具有能使生色团的光谱峰移向长波区并使其强 度增加的作用,这种官能团叫做助色团。 例如,-OH和-NH2等都对苯生色团具有助色作用, 使B带显著红移。 由于孤立的生色团吸收带往往位于紫外光域(除非 若干生色团共轭相连),在引入某些助色团时光吸 收移向可见光域,由此得名。 常见的助色团按其“助色”效应的强弱可大致排列 为下述秩序:
分子光谱分析

3.判断异构体 ⑴结构异构体:多利用双键位置不同推断,例:
λmax 208nm ε 5000~15000 同环双烯
295.5nm 12000~28000 异环双烯
⑵顺反异构体: 反式λmax和ε >顺式λmax和ε 例:
H
C H
λmax ε
C
C C H
H 顺式 280nm 10500
反式 295.5nm 29000
二、分子光谱产生原因: 分子能级跃迁
三、分子光谱分析: 利用分子的电子、振动、转动能级跃迁所产生的分子光谱对物质进行定 性、定量和结构分析的方法。 1.一般过程: 光源
单色分光
样 品 池
检测器
信号显示记录
2.分类:分为三类 ⑴吸收光谱:红外、紫外-可见吸收光谱分析 ⑵发射光谱:分子荧光光谱分析 ⑶散射光谱:拉曼光谱分析
例:测定m、n两物质的UV谱,得: 溶液 浓度(mol/L) A(450nm) m 5×10-4 0.8 n 2×10-4 0.6 m、n混合 未知 1.0 求:混合液中m、n的浓度Cm、Cn (吸收池厚1cm) 解: A450=ε450mCm L+ε450nCnL ⑴ A700=ε700mCm L+ε700nCnL ⑵ 又:A450m =ε450mCm0 L= 5×10-4 ε450m=0.8 A450n =ε450nCn0 L= 2×10-4 ε450n=0.6 A700m =ε700mCm0 L= 5×10-4 ε700m=0.3 A700n =ε700nCn0 L= 2×10-4 ε700n=0.3 将求得的4个ε和L=1cm代入式⑴、⑵得: A450=1600Cm+3000Cn=1.0 A700= 600Cm+1500Cn=0.4 解之可得:Cm和Cn (mol/L)
分子光谱学

当入射光的 ,吸光物质的c 一定时,溶 液的吸光度A与液层厚度b成正比.
比尔定律(1852) A=lg(I0/It)=k2c
当入射光的 ,液层厚度b 一定时,溶液 的吸光度A与吸光物质的c成正比.
16
朗伯-比尔定律
A=lg(I0/It)=kbc
单重态
三重态 T2
S1
可见
荧光
振 v3
Ee 红外
S0
动 能 级
v2 v1
Ev 转动 rrr213
Er
分子吸光与发光示意图
磷光 T1
12
光谱种类
原子光谱:吸收、发射、荧光
线状光谱
分子光谱:紫外、可见、红外等吸收光谱
I
带状光谱
黑体辐射:白炽灯、液、固灼热发光
连续光谱
13
分子对光的吸收与吸收光谱
不同颜色的可见光波长及其互补光
出
光栅衍射示意图
射
狭
缝 30
吸收池(比色皿):用于盛待测及参比溶液。
可见光区:光学玻璃池 紫外区:石英池
检测器:利用光电效应,将光能转换成 电流讯号。
光电池,光电管,光电倍增管
检流计(指示器):
低档仪器:刻度显示 中高档仪器:数字显示,自动扫描记录
31
硒光电池(Barrier-layer photocell)
10
物质对光的吸收与发射
物质分子内部3 种运动形式及其对应能级:
1. 电子相对于原子核的运动--电子能级;
单重态:激发态与基态中的电子自旋方向相反. 三重态:激发态与基态中的电子自旋方向相同.
2. 原子核在其平衡位置附近的相对振动 --振动能级;
分子光谱解析

7.6 分子光譜由前述,分子的總能量=諸原子核的動能+電子能量,其中「電子能量」(electronic energy )=e E ,...),(1312R R E α籠統包括電子的動能及諸粒子間的庫倫勢能。
從力學知,諸核的動能又可分為三大項:質心移動的動能(translational energy )、以質心為心的轉動的能量(rotational energy )、振動的能量(vibrational energy )。
r t e E E E E E +++=υ。
由於分子的質量大,在放光時,t E 可視為不變──如同原子光譜時。
因此研究分子光譜時,只考慮三項能量:r e E E E ,,υ。
分子光譜大別為三類:純轉動光譜(pure rotational spectrum ):只牽涉r E 的改變。
振動─轉動光譜(vibration-rotation spectrum ):只牽涉r E E +υ的改變。
電子光譜(electronic spectrum ):牽涉r e E E E ++υ的改變。
又,依方法的不同,分子光譜又可區分為:吸收光譜(absorption spectrum )、發射光譜(emission spectrum )與拉曼光譜(Raman spectrum )。
7.7 純轉動光譜假想分子為一剛性轉子(rigid rotator )。
323222121222I LI L I L H ++=. 1,2,3表示三個主軸(principal axes ),1I ,2I 與3I 各表示沿主軸轉動時的轉動慣量。
雙原分子:03→I (03=⇒L ),I I I ==21。
()222212121L IL L I H =+=⇒ 2ˆ21ˆL I H =⇒.,r 稱為 rotational quantum number 。
20R I μ=。
態幅()φθ,r m r Y ,故例如當0=r ,分子取向的或然率分布具球面稱。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Chapter 1 Fluorescence and Fluorimetry 荧光分析法
1.1 Principle of Fluorimetry(荧光的原理 荧光的原理) 荧光的原理
什么是荧光?
当用一种波长的光照射某种物质时, 当用一种波长的光照射某种物质时 , 这个物质 能在极短的时间内发射出比照射波长更长的光; 能在极短的时间内发射出比照射波长更长的光; 物质吸收紫外光后所发出的光; 物质吸收紫外光后所发出的光; 物质吸收波长较短的可见光后发出波长较长的 可见光; 可见光;
0.2 The Characterization of luminescence • 光谱 (Spectrum) I(λ) • 强度 (Intensity) φ(quantum yield) • 衰减 (Decay) τ or k • 偏振 (Polarization)(各向异性 各向异性anisotropy) 各向异性 • 相干 (Coherence) • 散射 (Raman or Rayleigh) • 猝灭 (quench)
0.4.2 具有更好的选择性 具有更好的选择性. 并非所有的生色团都产生发射; 并非所有的生色团都产生发射; 激发或发射波长可供选择…; 激发或发射波长可供选择 ;
0.4.3 广泛的应用 广泛的应用. 无机离子测定 基因工程 生物分析 有机物分析
蛋白组学计划 免疫分析
食品安全! 临床! 公安 食品安全 临床
Figure 3. Fluorescence spectra (λex 363 nm) of probes 1 (a) and 2 (b) (25 µm) in DPBS at room temperature upon addition of increasing amounts of Mg2+ ions (0, 5, 10, 30, 50, 87, 280, 480, 850, and 1030 µm).
Laser
Fluorescence
A--T C--G G--C T--A
Laser induced Fluorescence detection
发光分析在科学研究中发挥重要作用: 发光分析在科学研究中发挥重要作用: 探针、 探针、传感器和检测器 基因组学 蛋白组学 Proteomic 免疫分析 生命过程
二、发光的类型 (Type of luminescence )? • Photoluminescence (光致发光 光致发光): 光致发光 Fluorescence/Fluorimetry; Phosphorescence/Phosphorimetry; • Chemiluminescence (化学发光 化学发光); 化学发光 • Bioluminescence (生物发光 生物发光); 生物发光 • Radioluminescence (辐射发光 辐射发光); 辐射发光 • Electroluminescence(电致发光 电致发光); 电致发光 • Sonoluminescence(声致发光 声致发光); 声致发光
History of fluorimetry
历史: 历史: • 1575年 Spain内科医生 内科医生Nicholas Monardes观察 1575 年 , Spain 内科医生 Nicholas Monardes 观察
到贮存在由菲律宾紫檀木制成的杯中的水会发出一种 神奇迷人的光; 神奇迷人的光;
内容介绍
0.发光概述 发光概述 CHP.1 荧光分析
Principle of Fluorimetry(荧光的原理 荧光的原理) 荧光的原理 The Fluorescence Mechanism(荧光方法 荧光方法) 荧光方法 Characteristics of fluorescence spectrum (荧光光谱特性 荧光光谱特性) 荧光光谱特性 Fluorescence decay and lifetime(荧光衰减和寿命) (荧光衰减和寿命) Quantum yield(量子产率) (量子产率) Fluorescence Intensity (荧光强度 荧光强度) 荧光强度
0.4 Characteristics of Luminescence Analysis
0.4.1 与吸光相比,灵敏度更高。 与吸光相比,灵敏度更高。 Alimit= ε bC (0.1~1 ,一般仪器 一般仪器); (0.010~3 ,with care and expensive instrumentation) CLOD=Amin/εb ε =0.10~0.010/105 =10-6~10-7mol/L. 化学发光:可检测 化学发光:可检测10-17 mol/L ATP, 相当于一个细 胞中的ATP量; 荧光单分子检测 !!! 量 胞中的
光棒光棒-化学反应发光
汞灯365nm汞灯 Fonkos菌悬浮液 菌悬浮液 Taken from Dr Ternura
Firebug(萤火虫) (萤火虫)
Even many single-celled organisms are bioluminescent. The radiolarian Tuscaridium cygneum forms colonies such as this one in the deep-sea and glows when disturbed. (Diameter approx. 1.2 cm)
What is luminescence?
Luminescence is the emission of light from any substance and occurs from electronically excited states. Luminescence is formally divided into two categories, fluorescence and phosphorescence, depending on the nature of the excited states.
分子发射光谱分析
Molecular Luminescence Spectroscopy Analysis
What does luminescence analysis do?
8-Hydroxyquinoline Derivatives( 衍 生 物 )as Fluorescent ( Sensors for Magnesium(Mg) in Living Cells Giovanna Farruggia, Stefano Iotti, Luca Prodi, Marco Montalti, Nelsi Zaccheroni, Paul B. Savage, Valentina Trapani, Patrizio Sale, and Federica I. Wolf. Web Release Date: 08-Dec-2005; (Article) DOI: 10.1021/ja056523u
热辐射( 热辐射(Thermoradiation): ):
处于较高温度的物体所发射出的可见光。 处于较高温度的物体所发射出的可见光。其共同特征是 随着温度的升高,辐射的总功率增大, 随着温度的升高,辐射的总功率增大,辐射的光谱分布向短 波长方向移动. 波长方向移动
分别指出前面所示发光的类型? 分别指出前面所示发光的类型?
Tab. 1.2. Early stages in the history of fluorescence and phosphorescencea) Year Scientist Observation or achievement
1565 N. Monardes Emission of light by an infusion of wood Lignum Nephriticum (.rst reported observation of .uorescence) 1602 V. Cascariolo 1640 Licetus 1833 D. Brewster 1845 J. Herschel 1842 E. Becquerel Emission of light by Bolognese stone (.rst reported observation of phosphorescence) Study of Bolognese stone. First de.nition as a non-thermal light emission Emission of light by chlorophyll solutions and .uorspar crystals Emission of light by quinine sulfate solutions (epipolic dispersion) Emission of light by calcium sul.de upon excitation in the UV. First statement that the emitted light is of longer wavelength than the incident light 1852 G. G. Stokes light) 1853 G. G. Stokes 1858 E. Becquerel 1867 F. Goppelsroder chelate) 1871 A. Von Baeyer Emission of light by quinine sulfate solutions upon excitation in the UV (refrangibility of Introduction of the term .uorescence First phosphoroscope First .uorometric analysis (determination of Al(III) by the .uorescence of its morin Synthesis of .uorescein
