有机化学典型习题及解答——胡宏纹
胡宏纹《有机化学》章节题库(卤代烷)【圣才出品】

因为(A)与 NaOH 易发生反应,说明分子内原子在烯丙位的可能性较大。再考虑到 产物为(C)和(D),所以(A)的最可能结构为:
过渡态比伯卤代烷发生消除反应的过渡态稳定。
(2)
前者 β-碳上的氢有较强酸
性,易被碱脱去,同时,在形成烯烃的过渡态中双键已部分形成,这种部分形成的双键与原
有双键因共轭而稳定。
(3)
前者虽不如后者稳定,但这种构象
很容易发生反式共平面的 E2 反应,生成相应烯烃。
反式的 4-叔丁基-1-氯环己烷虽然较稳定,但必须要翻转为不稳定的构象,才能发生反 式共平面的 E2 反应,这就要求较高的反应活化能。
答:
4.如何从相应的烷烃、环烷烃来制备下列化合物?
5 / 25
圣才电子书 十万种考研考证电子书、题库视频学习平台
答
:
5.完成下列反应。
答:(1)
(
2
பைடு நூலகம்
)
6 / 25
圣才电子书 十万种考研考证电子书、题库视频学习平台
6.如何从相应的烷烃、环烷烃来制备下列化合物?
答: (2)第一个反应较快。因为 CH3CH2O-的亲核性强。 (3)第一个反应较快。因为 HS-的亲核性比 CH3CH2O-强。 (4)等摩尔的溴丙烷与(a)1.0 mol 和(b)2.0 mol CH3CH2O-在乙醇中反应,后 者反应速率较快。因为 SN2 反应与亲核试剂的浓度有关。 3.按稳定性大小排列下述各组正碳离子的顺序。
胡宏纹《有机化学》章节题库(6-10章)【圣才出品】

第6章烯烃一、选择题1.化合物中最稳定的是()。
A.CH3CH2CH=CH2B.顺-2-丁烯C.反-2-丁烯【答案】C【解析】连接在双键上的烃基越多越稳定,且反式比顺式稳定。
2.下列化合物与溴发生加成反应,活性最高的是()。
A.丙烯B.乙烯C.氯乙烯【答案】A【解析】当双键上连有给电子基时易加成,连吸电子基时难加成。
3.己三烯与1 mol溴加成,最不易形成的产物是()。
【答案】(C)【解析】考虑反应中间体碳正离子的稳定性,生成(C)的反应中间体碳正离子只能与一个碳碳双键共轭,稳定性较差,故其最不易生成。
二、填空题1.命名______。
【答案】(E)-3-戊烯酸【解析】要以羧酸作主体进行命名。
2.命名______。
【答案】(E)-3-甲基-4-叔丁基-3-辛烯-5-炔【解析】注意烯烃顺反异构的命名,烯炔烃的命名一般以烯烃作为主体进行命名。
3.。
【答案】【解析】环丙烷不发生硼氢化反应。
4.。
【答案】Br—CH3CH CH2;CH3CH2CH2Br5.某烯烃C6H12经酸性高锰酸钾氧化后得等量丙酮和丙酸,该烯烃结构为______。
【答案】B6.下列反应的主要产物______。
【答案】【解析】这是烯烃的汞化反应生成醇。
三、简答题1.按要求排序。
(1)将下列化合物按亲电加成反应活性从大到小排序。
(2)按下列化合物与Br2加成活性从大到小排序。
(3)将下列烯烃按氢化热从大到小排序。
(4)写出反应产物(比较同一分子中不同烯烃氧化快慢)。
答:(1)B>A>D>C(2)B>A>C>D(3)a.C>B>A b.C>B>A2.给出下列基的中、英文名称。
答:(1)乙烯基;vinyl(2)3-甲基丁基(异戊基);3-methylbutyl(isopentyl)(3)烯丙基;allyl(4)1,1-二甲基丙基(叔戊基);tert-pentyl ortert-amyl(5)丙烯基;1-propenyl(6)异丙烯基;isopropenyl3.指出下列化合物中哪一个有立体异构现象。
胡宏纹《有机化学》章节题库(环烷烃)【圣才出品】

第3章环烷烃
一、选择题
1.两环烷烃的分子式均为C5H10,燃烧热较大的是()。
【答案】(a)
2.下列自由基中最稳定的是()。
【答案】B
【解析】p-π共轭使自由基稳定。
二、简答题
1.用系统命名法命名下列化合物。
答:(1)1-甲基-4-乙基-2-氯环己烷
(2)2-甲基螺[4.5]癸烷
(3)1,5-二(2-甲基环戊基)戊烷(4)1-甲基-3-溴二环[4.2.2]癸烷(5)2,9-二甲基二环[3.3.2]癸烷(6)二环[4.3.0]壬烷
2.写出符合下列名称的化合物的结构式。
(1)乙基环丙烷
(2)1,2-二甲基环丙烷
(3)反-1-氯-2-溴环丁烷
(4)二环[1.1.0]丁烷
(5)二环[3.1.1]庚烷
(6)顺二环[3.3.0]辛烷
(7)2-乙基-7-碘二环[2.2.1]庚烷(8)1,4-二甲基二环[2.2.2]辛烷(9)螺[2.5]辛烷
(10)5-甲基螺[3.4]辛烷
答:
3.写出下列化合物最稳定的构象式。
(1)异丙基环己烷(2)1,3-二甲基环己烷(3)1-甲基-4-叔丁基环己烷答:环己烷分子的最稳定构象式是椅型构象。
对于一取代环己烷分子,一般是取代基处于平伏键(e键)的构象最稳定。
对于多取代环己烷分子,通常是取代基(尤其是较大的取代基)处于e键的越多越稳定。
6.写出下列化合物的构象式。
(1)
(2)
(3)
(4)
(5)
(6)
答:。
胡宏纹《有机化学》章节题库(11-15章)【圣才出品】
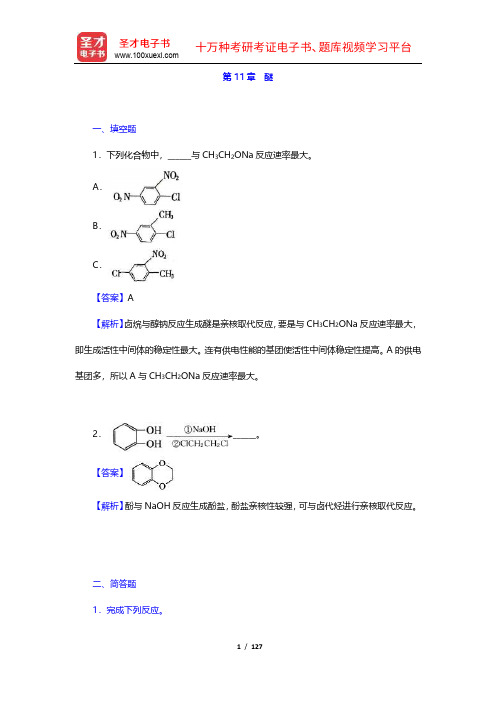
第11章醚一、填空题1.下列化合物中,______与CH3CH2ONa反应速率最大。
A.B.C.【答案】A【解析】卤烷与醇钠反应生成醚是亲核取代反应,要是与CH3CH2ONa反应速率最大,即生成活性中间体的稳定性最大。
连有供电性能的基团使活性中间体稳定性提高。
A的供电基团多,所以A与CH3CH2ONa反应速率最大。
2.______。
【答案】【解析】酚与NaOH反应生成酚盐,酚盐亲核性较强,可与卤代烃进行亲核取代反应。
二、简答题1.完成下列反应。
答:(5)ROH(4)、(5)反应很容易发生,(CH3)3COH及(CH3)3SiCl都可用作醇的保护剂。
2.下列化合物应如何合成?答:3.合成题。
(1)用乙炔为原料合成(无机试剂任选):(2)以乙烯和丙烯为原料(无机试剂任选)合成(CH3)2CHCH2CH2OH。
答:(1)乙炔为原料合成环氧烷烃,先用乙炔与NaNH2反应得到炔基钠,然后再与卤烷反应连上烷基,在生成烯烃。
烯烃与过氧化物反应即得到产物。
合成过程为:(2)要得到(CH3)2CHCH2CH2OH,使环氧乙烷与格氏试剂反应即可,环氧乙烷通过乙烯与氧气在银催化下加成得到;格式试剂通过卤烷与镁的醚溶液反应得到。
合成过程为:4.甲基数丁基醚在无水Et2O中与HI反应,生成的产物为碘甲烷和叔丁醇,而甲基叔丁基醚与浓HI反应则生成甲醇和叔丁基碘,为什么?答:在极性小的溶剂Et2O中,有利于S N2反应,亲核试剂I-进攻CH3的碳原子生成碘甲烷和叔丁醇。
在极性大的溶剂H2O中,有利于S N1反应,形成叔碳正离子,然后亲核试剂I-与叔碳正离子结合生成叔丁基碘。
表达方程式为:5.不对称醚一般不能用两个不同的醇与浓硫酸加热的方法制备,为什么?但叔丁醇在含有浓硫酸的甲醇中加热却高产率地得到了甲基叔丁基醚,试写出反应历程。
答:若用两个不同的醇直接制备不对称醚,除预期的混合醚外还会产生大量由同种醇反应生成的简单醚,一般不易分离或产率较低。
胡宏纹《有机化学》课后习题及详解(羧酸衍生物)【圣才出品】

第14章羧酸衍生物
1.推测下列化合物的结构。
提示:
答:各化合物的结构如下:
2.分离下列混合物。
(1)丁酸和丁酸丁酯
解:提纯一个化合物是要去掉其中的杂质。
分离一个混合物,则是要把其中各个组分一一分离,并使其达到一定的纯度。
例如,提纯由丁酸合成的丁酸丁酯,只要用碱洗去其中所含少量丁酸,而后蒸馏纯化,以得到丁酸丁酯。
而分离丁酸和丁酸丁酯的混合物,两种组分
都要分离提纯。
(2)苯甲醚、苯甲酸和苯酚。
(3)丁酸、苯酚、环己酮和丁醚。
(4)苯甲醇、苯甲醛和苯甲酸。
答:(1)略。
(2)分别用NaHCO3,NaOH溶液使三者分开,再各自分离提纯。
(3)分别用NaHCO3,NaOH和饱和NaHSO3溶液使四者分开,再各自分离提纯。
(4)分别用NaHCO3,饱和NaHSO3溶液使三者分开,再各自分离提纯。
3.推测下列反应的机理。
(提示:分子内的Claisen反应称为Dieckmann反应,它与Claisen反应都是可逆反应。
)
答:
(3)
4.下列化合物应如何合成?
答:(1)
(2)略。
(3)略。
胡宏纹《有机化学》章节题库(羧酸)【圣才出品】

第 13 章 羧 酸
一、选择题 1.比较下列脂肪酸的酸性,其中酸性最强的是( )。 【答案】(b)
2.实现下列反应的试剂是( )。
【答案】B
3.下列化合物酸性的强弱顺序是( )。
A.(1)>(2)>(3) B.(1)>(3)>(2) C.(3)>(2)>(1) D.(2)>(3)>(1) 【答案】D 【解析】羧基碳的缺电子程度越高,羧酸电离产生的阴离子越稳定,则羧酸的酸性越强。
答:
9 / 24
圣才电子书 十万种考研考证电子书、题库视频学习平台
7.完成下列反应。 答:
10 / 24
圣才电子书 十万种考研考证电子书、题库视频学习平台
8.用光谱法鉴别下列酸的异构体。 CH3(CH2)3CO2H、(CH3)2CHCH2CO2H、(CH3)3CCO2H
5.(多选)R,R-酒石酸与 S,S-酒石酸什么性质相同( )。 A.熔点 B.沸点 C.在水中的溶解度 D.比旋光度 【答案】ABC
二、填空题
1.
。
【答案】
【解析】在碱性条件下,乙酸乙酯与甲酸乙酯发生酯缩合反应,生成 α-甲酰基乙酸乙
2 / 24
圣才电子书 十万种考研考证电子书、题库视频学习平台
答:(1)3-丙基己酸 (2)5-硝基-2-羟基苯甲酸 (3)环癸烯基甲酸 (4)2,5-二甲基己二酸 2.按酸性由强到弱排列顺序。
答:磺酸属于强酸,酸性最强。取代苯甲酸羧基对位连有吸电子基团时,羧基酸性增强, 连有给电子基团时,羧基酸性减弱;-NO2、-Br 都属于吸电子基团,但-NO2 的吸电子作用 大于-Br,-CH 属于给电子基团。所以酸性强弱顺序为 f>d>c>a>b。
胡宏纹习题及问题解答

问题4.2 将下列式中的不对称碳原子用*号标出
Br
Br
D Br H
*
Cl Cl
F F
CH3 H
*
Br
* Br
D * Br H
Cl * Cl
F F
CH3 * H
问题 4.3 写出分子式为C5H11Br的构造异构体, 并用*号标出其中的不对称的碳原子
问题 4.4 下列构型式哪些是相同,哪些是对映体?
• (1)没有足够的能量来产生氯自由基,不 起自由基反应 • (2)光照射后,氯气产生了氯自由基,与 甲烷完成自由基取代反应 • (3)产生的氯自由基相互碰撞生成氯气分 子,氯自由基消失 • (4)能量不够,甲烷不能产生甲基自由基 • (5)链式循环反应
习题
1.写出分子式为C7H16的烷烃的各种异构体的构造式,
CHO, CH3CHO
H O OHC
H CHO
习题
• 1、写出下列反应中的产物、原料或试剂
(E)
HI
I
HBr, H2O2
Br
O
(1) O3 (2) Zn, CH3COOH O
Br HBr, RO-OR
Br2/ H2O
OH Br
B2H6
B
H2O2, OH
3
OH
(Z)
(1) O3 (2) Zn, H2O
并用系统命名法命名
2.将下列化合物用系统命名法命名
• 3.将烷烃中的一个氢原子用溴取代,得到通式为 CnH2n+1Br的一溴化物,试写出C4H9Br和C5H11Br的 所有构造异构体。
第三章 环烷烃
• 问题3.1 写出下列化合物的名称
问题3.2 写出下列化合物结构式
胡宏文版有机化学习题解答

1章思考题1.1 什么是同系列与同分异构现象?1.2 什么叫诱导效应?1.3 影响有机化学反应活性的主要因素有哪些?1.4 在沸点、熔点和溶解度方面,有机化合物和无机盐有哪些差别?1.5 正丁醇的沸点(118℃)比它的同分异构体乙醚的沸点(34℃)高得多,但这两个化合物在水中的溶解度却相同(每100克水溶解8克),怎样说明这些事实?1.6根据共价键的断裂方式推测反应机理的可能类型有哪些?习题1.1 用系统命名法命名下列化合物。
(1)CH3CH2CHCH3CHOHCHCH2CH2CH3OH(2)CH3CH2CHCH3CHOHCHClCH2CH2CH2CH3(3)CH3CH2CHCH3CHOHCHCH2CH2CH3CH2CH2CH2CH3(4)CH3CH2CHCH3CHCH2CH3CH2CHO(5) COOHCH3CH3(6) COOHCH3NH2(7) COOHNH2NO2(8) COOHNO2(9) COOHCH3(10) NH2(11) COOH(12) NH2CH3(13) SO3HClH2NCH3(14)C Cn-Bun-PrEtMe1.2 写出下列化合物的结构式。
(1)4-乙基-4-氯-己酸-4-甲基戊酯(2)N-(2-氨基丁基)-4-甲氧基苯胺(3)2,6,6-三甲基双环[3.1.1]-2庚烯(4)3-(1-甲基-8氨基-2-萘基)丁酸1.3 写出的(1)CH4O(2)CH2O(3)CH2O2(4)CH5N(5)CH2Br可能结构式并指出上述每一结构式中的官能团。
1.4 下列化合物有无极矩?如有指出其方向。
(a)CH2Cl2(b)CH3Cl(c)CH3OH(d)CF2Cl2(e) CH3CH2Br(f) H3CCClCCH3Cl(g)C2H5OH1.5 化合物Ⅰ、Ⅱ和Ⅲ都是NH3的衍生物,存在于某些鱼的分解产物中。
预测这三者中哪一个在水中的溶解度最小?CH3NH2(CH3)2NH(CH3)3NⅠⅡⅢ1.6 写出下列各化合物构型异构体。
胡宏纹《有机化学》名校考研真题及详解(醇和酚)【圣才出品】

第10章醇和酚一、选择题1.下列物种作为离去基团时最易离去的是()。
[大连理工大学2004研]【答案】(A)【解析】硝基为吸电子基,故(A)最稳定,作为离去基团,最易离去。
2.下列化合物中,酸性最强的是()。
[天津大学2000研]【答案】(D)【解析】硝基为吸电子基,使邻、对位的电子云密度降低,使酚羟基的酸性增强。
3.反应的主要产物是()。
[武汉大学2000研]【答案】(C)【解析】醇在酸作用下生成碳正离子,碳正离子重排成较稳定的三级碳正离子,再脱去一个氢离子后变成烯烃。
二、填空题1.______。
[浙江大学2003研]【答案】【解析】酚羟基可与酸酐、酰氯等反应生成相应的羧酸酯。
2.。
[中国科学院-中国科学技术大学2002研] 【答案】【解析】碱催化时,由甲氧离子进攻空间位阻较小的环碳原子,即产物中甲氧基与取代基较少的碳原子相连;酸催化时,氢离子与氧原子先生成盐,使碳氧键断裂,生成取代基较多的较稳定的碳正离子,故甲氧基与取代基较多的碳相连。
三、简答题1.请写出下面反应的主要产物及可能的副产物,并写出你认为合理的反应机理。
[华东理工大学2006研]答:醇在酸作用下发生分子内脱水形成双键,机理为:在酸性条件下,醇先质子化形成较好的离去基团H2O,产生碳正离子,正碳离子发生重排得到不同产物。
具体如下:2.某醇C5H10O(A)具有旋光性,催化加氢,生成的醇C5H12O(B)没有旋光性,试写出(A)、(B)的结构式。
[南京航空航天大学2008研]答:根据A的分子式和旋光性可推断出A的结构式为:CH3CH2CHCH CH2,B的结构式为:CH3CH2CHCH2CH3OH。
3.解释下面化合物的外消旋体具有很强的分子内氢键,而内消旋体却没有分子内氢键。
[清华大学2005研]答:外消旋体可采取邻位交叉构象,因两叔丁基处于对位,空间位阻不大,而由于分子内两羟基间存在较强的氢键,该构象最为稳定。
内消旋体若采取邻位交叉构象.两叔丁基间的空间位阻较大,不稳定,因此内消旋体一般采取对位交叉构象,此时不存在分子内氢键。
胡宏纹《有机化学》课后习题详解(9-15章)【圣才出品】

答:
1 / 31
2 / 31
第 10 章 醇和酚
1.推测下列反应的机理。
答:
3 / 31
2.如何完成下列转变?
答:
4 / 31
3.2,4,6-三叔丁基苯酚在醋酸溶液中与溴反应,生产化合物
22 / 31
(2)苯甲醚、苯甲酸和苯酚。 (3)丁酸、苯酚、环己酮和丁醚。 (4)苯甲醇、苯甲醛和苯甲酸。 答:(1)略。 (2)分别用 NaHCO3,NaOH 溶液使三者分开,再各自分离提纯。 (3)分别用 NaHCO3,NaOH 和饱和 NaHSO3 溶液使四者分开,再各自分离提纯。 (4)分别用 NaHCO3,饱和 NaHSO3 溶液使三者分开,再各自分离提纯。 3.推测下列反应的机理。
,产率
差不多是定量的。A 的红外光谱图中在 1630 cm-1 和 1650 cm-1 处有吸收峰,1H NMR 谱
图中有三个单峰,δH=1.19,1.26 和 6.90,其面积比为 9:18:2。试推测 A 的结构。
答:A 的结构为:
4.推测下列化合物的结构。
解:
不饱和度为 4,提示可能有苯环;IR,3350 cm-1 峰提示可能
有羟基,3070,1600,1490 cm-1 提示可能有苯环,830 cm-1 提示可能为对位二取代;1H
NMR 中δH:6.8(q,4H)与对位二取代苯相符合,其他的峰说明侧链为 CH2CH2CH3,δ
H:5.5 为羟基上的质子。
5 / 31
答:
6 / 31
(提示:分子内的 Claisen 反应称为 Dieckmann 反应,它与 Claisen 反应都是可逆反 应。)
胡宏纹《有机化学》章节题库(醇和酚)【圣才出品】

6.(多选)下列化合物与 Lucas 试剂作用,最快的为( ),最慢的为( )。 A.2-丁醇
2 / 27
圣才电子书
B.2-甲基-2-丁醇
十万种考研考证电子书、题库视频学习平台
C.2-甲基-1-丙醇
(2)由苯为主要原料制备三苯甲醇还有其他路线: ①经三苯甲基氯合成三苯甲醇 在无水三氯化铝存在下,苯与四氯化碳作用,生成三苯 甲基氯。三苯甲基氯在碱性条件下水解,生成三苯甲醇。 ②经二苯甲酮合成三苯甲醇 在无水三氯化铝存在下,苯与光气作用生成二苯甲酮。
在无水三氯化铝存在下,苯与四氯化碳作用生成二苯基二氯甲烷,然后水解生成二苯甲 酮。
圣才电子书 十万种考研考证电子书、题库视频学习平台
第 10 章 醇和酚
一、选择题 1.下列化合物在水中溶解度最大的是( )。 A.1-丁醇 B.1,3-丙二醇 C.乙醚 【答案】B 【解析】亲水基团越多,水中溶解度越大。
2.下列化合物中沸点最高的是( )。 A.2-甲基丙醇 B.正丁醇 C.1-氯丙烷 【答案】B 【解析】能形成分子内氢键的沸点较高,故醇比氯代烃高,且同数碳的醇支链越多,沸 点越低。
7 / 27
圣才电子书 十万种考研考证电子书、题库视频学习平台
苯溴代生成溴苯: 溴苯与镁作用,生成溴化苯基镁,溴化苯基镁与二苯甲酮作用,生成溴化三苯甲醇镁, 溴化三苯甲醇镁水解,生成三苯甲醇。 (3)溴苯与金属镁是放热反应,反应有诱导期,一旦反应开始,一般无需再加热。但 如果滴加溴苯的速度太慢,反应放出的热小于反应体系散失的热,导致反应温度下降,从而 造成反应速率下降,直至反应几乎停止。随着溴苯的滴加,体系中溴苯的浓度增加,如加热 反应体系,重新启动反应,将产生爆发式反应(即开始不反应,当加热到一定温度时,突然 反应,温度快速上升,反应很快结束),副反应增多。如果滴加溴苯的速度太快,局部溴苯 浓度增加,反应热增加,反应激烈,溴苯与金属镁作用生成的溴化苯基镁会与溴苯作用,生 成联苯。
有机化学典型习题及解答——胡宏纹

二烯烃
红外光谱
1. 以丙烯为唯一碳源合成: CH3CH2CH2
H
H C C CH3
解答: 利用炔钠与卤代烷的增碳反应先生成相应的炔烃,而后还原
得到反式烯烃。
CH3CH CH2
Br2
HBr O O
CH3CH2CH2Br
NaNH2 NaNH2
CH3CH CH2
CH3CH CH2Br Br
CH3C CH
CH3C CNa
CH3CH2CH2Br
CH3CH2CH2C CCH3
Na 液NH3
CH3CH2CH2 H
H C C CH3
2. 以所给的起始物为原料(其它化学试剂不限)完成下列合成:
解答:
产物为顺式结构,合成时必须考虑立体化学的控制,叁键还原时 不能用Na/NH3还原,而应用Lindlar催化剂进行催化加氢。
NaNH2 NH3(l)
Na
C2H5Br
H2 Lindlar
3. 以乙炔、丙烯为原料合成:
CH2CCH3 O
解答:
2CH CH
H2C CHC CH
H2 Lindlar
H2C CHCH CH2
CH CH
Na NH3
HC CNa
Cl2 hv
CH CCH2CH CH2
CH3CH CH2
CH2CH CH2 Cl
2. 以所给的起始物为原料(其它化学试剂不限)完成下列合成:
OH
解答:
利用Grignard试剂来进行增碳。
CHBrCH3
HBr
H3C CHMgBr
Mg O
H3C CHCH2CH2OMgBr
H3O
+
OH
3. 以所给的起始物为原料(其它化学试剂不限)完成下列合成:
南京大学胡宏纹版有机化学课后习题及答案

(8) CH3CHCH2C(CH3)3
(2)与(4): (3)与(5): (7)与(8):
3,3-二乙基戊烷 2-甲基戊烷 2,2,4-三甲基戊烷
问题 2.5 写出下列各化合物的构造式: (1)3,3-二乙基戊烷
(2)2,4-二甲基-3,3-二异丙基戊烷
C H
Cl
C
H
Cl Cl
Cl
C Cl
H
这六种结构都可以通过旋转变成一种结构,所以CH2Cl2只有一种。 CHCl3的四种结构:
这四种结构都可以通过旋转变成一种结构,所以CHCl3只有一种。
问题 1.3 如碳原子的四个价排列在一个平面上,即碳原子位于正方形 的中心,四个价指向正方形的四个顶点,CH2Cl2可能有几种异构体? 解答: 两种:一种两个氯原子位于正方形的同一条边上,另一种两个氯原子 位于正方形的一条对角线上。
经验式:CH3O
物质的量(n)/mol 33.6/12.01 = 2.80 5.6/1.008 = 5.56 49.6/35.45 = 1.40 11.2/16.00 = 0.70
最小整数比 2.80/0.70 = 4 5.56/0.70 = 8 1.40/0.70 = 2 0.70/0.70 = 1
问题 2.2 下列构造式中哪些代表同一化合物? 解答:
(1)与(6),(2)与(4),(3)与(5),(7)与(8)分别代表同一化合物。
问题 2.3 将问题 2.1 各化合物中的仲碳原子和叔碳原子分别用圆圈和
方框标示出来。
解答:
CH3CH2CH2CH2CH2CH3
CH3CH2CH2CH(CH3)2
CH3 CH3CH2CHCH2CH3
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
解答: cis -
Br
trans- Br
消除时,cis-可直接与β-H反式共平面消除:
-HBr
Br
trans-需构型翻转,Br与C(CH3)3均处于a键时方能消除,所需能量较大。
Br
顺式快于反式。
-HBr
Br
8. 完成下列反应:
H Br
(1)
CH3 C CH2CH3 + -SR
(
)
CH2CH3
(2)
浓 H2SO4
OCH3
Br2 Fe
SO3H
OCH3 Br
A. C2H5O- > OH- > C6H5O- > CH3COOB. OH- > C2H5O- > CH3COO- > C6H5OC. CH3COO- > C6H5O- > OH- > C2H5O解答:A。若亲核原子相同,则碱性与亲核性一致。
4. 排列下列化合物发生SN2反应活性顺序( )。
A. 溴甲烷 B. 溴乙烷 C. 2-溴丙烷 D. 2-溴-2-甲基丙烷
2. 解释等摩尔的甲烷和乙烷混合进行一氯代反应,得到CH3Cl和 C2H5Cl的比例为1∶400。
解答: CH3CH2·的稳定性大于CH3·,易于生成。
3. 试说明为什么甲烷氯代反应机理不太可能按下述方式进行:
光照
(1) Cl2
2Cl
(2) Cl + CH4
CH3Cl + H
(3) H + Cl2
CH3 H OH H OH
CH2CH3
CH2CH3 HO H HO H
CH3
解答: A。将A或B任何一个化合物在纸面上翻转180度后就变成了
另一个化合物。
2. 命名
CH3
H3C
H
H
Br
H
解答: S-2-溴丁烷。首先分析构造,为2-溴丁烷。根据Newman投影式 分析构型为S。
3. 写出化合物(2E,4S)-3-乙基-4-溴-2-戊烯的构型。
CH3
H
+
OH
CH2CH3
OH H
CH3 CH2CH3
SN1, 外消旋体
第十章 醇 和 醚
1. 按下列醇在硫酸存在下脱水活性从大到小排序:
OH
A
B
OH
C
D
OH
OH
E
CH2OH
解答: D>A>B>E>C。醇在硫酸作用下脱水反应,属于E1 历程,反应
速度快慢由中间体碳正离子稳定性决定。碳正离子愈稳定,决定 反应速度的第一步就容易进行。
CH3
(1)
CH3
CH(CH3)2
CH3 CH3
CH(CH3)2
C2H5
C2H5
(2)
H3C
Cl H3C
Cl
解答:
CH3
(1)
CH3 <
CH3 CH3
CH(CH3)2
CH(CH3)2
(2) H3C
C2H5
> Cl H3C
C2H5 Cl
第六章 单环芳烃
1. 判断下列化合物苯环上亲电取代反应活性的大小:
第二章 烷 烃
1. 由下列指定的化合物制备相应的卤代物,用Cl2还是Br2?为什么?
(1)
CH3 + X2 (1分子) 光照
CH3 X + HX
光照
(2)
+ X2
X + HX
解答:
(1) 用Br2。因氢原子活性有差异,溴原子活性适中,反应选择性强,主 要得到 :
CH3 Br
(2) 用Cl2。只有一种氢,氯原子反应活性高。
HCl + Cl
重复(2)、(3)。
解答: (2) Cl + CH3-H
435
CH3-Cl + H 349
ΔH=435-349= +86KJ/mol 因为控制反应的一步(2)高度吸热,所以这种历程可能性小。
第三章 烯 烃
1. 解释下列两反应的加成位置为何不同?
HCl
CF3CH CH2
CF3CH2CH2Cl
C.
CH2Cl D.
O2N
CH2Cl
解答: A > B > C > D。反应为SN1,比较碳正离子稳定性,苯环上有
吸电子基不利于碳正离子的稳定。
2.下列化合物中哪一个最容易发生SN1反应?
CH3
A. CH2 CHCH2ClB. CH3CH2CH2Cl
C.
CH2 CHCHCl
解答: C.
3.下列离子与CH3Br进行SN2反应活性顺序( )。
解答: 在3-溴戊烷中,溴原子与β-H应处于反式共平面消除。
Br
H
CH3
-HBr
H H
(A)
CH2CH3
顺式-2-戊烯
Br CH3
H H
(B)
H
-HBr
CH2CH3
反式-2-戊烯
(B)构型更稳定
7. 画出cis-和trans-4-叔丁基环己基溴的稳定的构象结构式,它们 发生消除时何者较快,为什么?
①
HCl
CH3OCH CH2
CH3OCHClCH3
②
解答: 碳正离子稳定性:
① CF3 CH CH2+ > CF3 CH CH2
H
H
-CF3基团有强的吸电子诱导效应,使碳正离子不稳定。
② CH3OCH CH2 > CH3OCHCH2+ ( CH3OCH CH2
H
H
H
CH3O CHCH3 )
氧原子未共用电子对的离域,使正电荷分散而体系稳定性增加。
2. 写出下列转变的机理:
CH3 CH3
Br2 NaCl
CH3 Br Cl +
CH3
CH3 Br
Br CH3
解答:
溴鎓离子中间体。Br-或Cl-从环鎓离子反面加成。
CH3
X-
Br+
(Br- 或 Cl-)
CH3
CH3 Br
X CH3
3. 写出下列转变的机理:
H+
解答:
H+
H+
第四章 炔烃 二烯烃 红外光谱
乙醚 萃取
水层(酚钠)HCl
乙醚 萃取
浓缩
醚层(2-甲基萘)
水层
醚层
浓缩 减压蒸馏
A
减压
B
蒸馏
3. 解释下列现象:
H
OH
OH
O
熔点(104℃)
OH
熔点(172℃) 分别形成分子内氢键、分子间氢键
3. 合成:
OH Br
解答:
磺化 碱熔
OH
(CH3)2SO4
1. H3O+ 2. HI
OH Br
OCH3
Na
CH3CH2CH2C CCH3 液NH3
CH3CH2CH2
H
CC
H
CH3
2. 以所给的起始物为原料(其它化学试剂不限)完成下列合成:
解答: 产物为顺式结构,合成时必须考虑立体化学的控制,叁键还原时 不能用Na/NH3还原,而应用Lindlar催化剂进行催化加氢。
NaNH2 NH3(l)
Na C2H5Br
△
O CCH3
4. 用化学方法区别下列化合物: 1-丁炔,2-丁炔和1,3-戊二烯
解答: 顺丁稀二酸酐; Ag(NH3)2NO3。
第五章 脂 环 烃
1. 命名
CH3
CH3
CH3
解答: 2,8,8-三甲基-双环[3.2.1]-6-辛烯。根据双环化合物命名原则,再
考虑取代基位次尽可能小。
2. 用化学方法鉴别下列化合物,并写出有关反应:
CH3
CH2CH2CH2C+CH2CH3 CH3
CH3
CH2CH2CH2CCH2+
CH3
H3C CH2CH3
H
H+
H3C
CH2CH3
4. 已知光照下乙苯和氯气反应时氯自由基夺取α-H比夺取β-H的速 度快14.5倍,试用反应历程解释。
解答:
Cl2
2 Cl
CH2CH3 Cl
CHCH3 Cl2 CH2CH2
H OH COOH
解答:
C。化合物A和B都有对称中心,化合物D有对称面和对称中心。
5. (S)-
CH2CHCH2CH3 Cl2
CH3
hv
(反应为芳烃侧链α-H卤代。中间体碳自由基为平面结构,产 物各占50%。
CH3 H Br H Br
CH3
CH3 Br H + H Br
CH3
H2 Lindlar
3. 以乙炔、丙烯为原料合成:
CH2CCH3 O
解答:
2CH CH
H2C CHC CH H2
Lindlar
H2C CHCH CH2
Na
CH CH
NH3
CH3CH CH2
HC CNa
Cl2
hv CH2CH CH2 Cl
CH CCH2CH CH2
O
HgSO4, H2SO4 H2O
CH3 CCH2CH CH2
Br
OH
D
OH
解答: 在进行Grignard反应时,注意保护羟基。
H+
Br
OH
Br
CH2 C(CH3)2
D2O
D
OC(CH3)3 H+
OC(CH3)3 Mg BrMg
干醚
D
OH
OC(CH3)3
