化学盐的化学性质复分解反应课件人教版下册九年级
合集下载
人教九下化学11.1 生活中常见的盐—— 复分解反应实质 课件(共42张PPT)
NO3-
NO3-
K+
K+
NO3-
K+
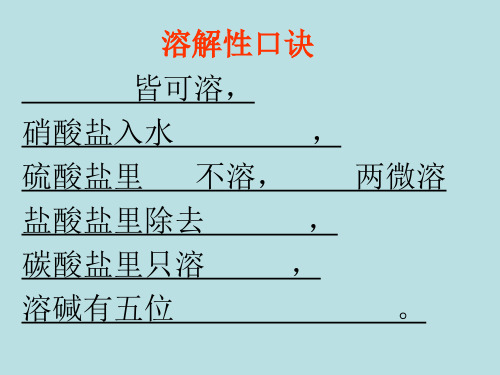
NaCl+KNO3 ——
K+ NO3-
Cl-
Na+
Na+ Cl-
K+
NO3-
NO3-
NO3K+
K+
NaCl+KNO3 ——
Cl-
Na+
K+ NO3-
NO3-
Na+
Cl-
NO3K+
K+
NO3-
K+
NaCl+KNO3——
K+ NO3-
ClNa+
NO3-
K+
Na+
Ca2+
HO-
HO-
HO-
Ca2+
HO-
Ca(OH)2+CuCO3 ——
Ca2+
CO3C2u- 2+CuC2O+ 32C-O3C2u- 2+ CuC2O+ 32C-O3C2u- 2+CuC2O+ 32-
HO-
Ca2+ HO-
HOHO-
Ca(OH)2+CuCO3 ——
HOCa2+
HO-
CO3C2u- 2+CuC2O+ 32C-O3C2u- 2+
⑹HCl + ⑺H2SO4 ⑻CaO +
NaOH == NaCl +CuO==CuSO4 H2O =Ca(OH)2
+ H2O +H2O
⑼BaCl2 + Na2SO4 == BaSO4↓+ 2NaCl
11.1生活中常见的盐(第2课时 盐的化学性质、复分解反应)课件-九年级化学人教版下册

BaCl2+H2SO4= BaSO4 +2HCl 2NaOH+H2SO4= Na2SO4 + 2H2O Na2CO3+H2SO4= Na2SO4 + H2O + CO2 BaCl2+ Na2CO3= BaCO3 + 2NaCl BaCl2+ NaOH =不反应 Na2CO3 + NaOH =不反应
Fe
+
H2
SO4
=
FeSO4
+
H2
↑
C.酸+碱==盐+水
CuO + H2SO4 ==== CuSO4 + H2 O
D.酸+盐==新盐+新酸 2HCl + Ca(OH) 2 ==== CaCl2 + 2H2 O ×EFG...碱碱盐+++非盐盐金====属新盐氧盐+盐化+新物碱==盐3+N水HaOCHl +2+NAFageONCHOl33+===C==O==2AF=ge=C(O=l↓=H)N+3a↓H2CN+OO333N+aHC2lO
沉淀
气体
水
×
√ ×
复分解反应发生的条件
复分解反应要发生,且能够进行到底,一般应考虑两方面的条件:
1.反应物要求的条件:有酸酸溶,无酸两溶
2.生成物的条件要求:
气体、沉淀、水一种 难电离的物质
两者缺 一不可
下列酸碱盐的性质中属于复分解反应的有( )
A.×酸+金属==盐+氢气 B.酸+金属氧化物==盐+水
√
×
最新人教版九年级下册化学PPT教学课件11.1.2复分解反应和盐的化学性质
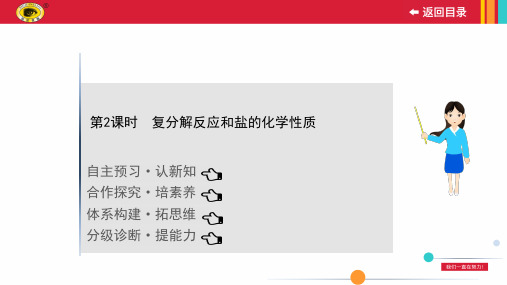
、CO32
、SO24
7.(1分)(2020·南阳模拟)用括号内的物质不能区分的一组是( A ) A.NaOH、NaCl、Na2SO4三种溶液(酚酞) B.Na2CO3、AgNO3、BaCl2三种溶液(稀盐酸) C.铁粉、碳粉、氧化铜粉末(稀硫酸) D.NaCl、NaOH、NH4NO3三种固体(水)
A.该溶液是一种碱的溶液
B.该溶液中含有 SO24 离子 C.该溶液中的溶质可能是Na2CO3 D.该溶液能使紫色石蕊溶液变红色
加入的物 酚酞溶 BaCl2
质
液
溶液
稀盐酸
实验现象 变红色
白色沉 淀
产生气 体
6.(3分)(2020·满洲里模拟)如图是生成盐的五种化学反应,请回答下列问题。
(1)若反应②中生成的盐是BaSO4,则所用的酸是___H_2S__O_4 __(写化学式); (2)若反应③用氢氧化钙与硫酸铜溶液反应,则生成的盐名称是___硫__酸__钙____;
(2)向第二支试管的滤液中滴入适量的___B_a_(_O_H_)_2 __溶液,反应方程式为 ___B_a_(_O_H_)_2+_K_2_C_O_3_=_=_=_=_B_a_C_O_3↓__+_2_K_O_H___,再经过滤、蒸干滤液,得到白色固 体氢氧化钾。
3.复分解反应发生的条件: 当两种化合物互相交换成分,生成物中有___沉__淀____、___气__体____或___水____生 成时,复分解反应才可以发生。
二、盐的化学性质 1.与某些金属发生置换反应生成另一种金属和另一种盐: 如铁与硫酸铜溶液反应的化学方程式为 ___F_e_+_C_u_S_O_4_=_=_=_=_C_u_+_F_e_S_O_4 __。 2.与某些酸发生复分解反应生成另一种盐和酸: 如氯化钡与硫酸溶液反应的化学方程式为 ___B_a_C_l_2+_H_2_S_O_4_=_=_=_=_B_a_S_O_4↓__+_2_H_C_l___。
10.3常见的盐(复分解反应)课件---2024-2025学年九年级化学人教版(2024)下册

3. M是一种金属元素,M2+与其他几种离子构成的化合
物的溶解性见下表。根据以上信息,判断下列反应肯
定不能发生的是
(C
)
A. MCl2+ NaOH M(NO ) +NaCl
B. MSO4+Ba (NO3)2C. D. MO+H SO
4. 判断下列反应是否能够发生,若能则写出反应方程式,
若不能则说明理由。
③Ba(OH)2溶液和Na2CO3溶液: _B_a_(_O_H__)2_+__N__a_2C__O_3_=_=_=_B__a_C_O__3↓_+__2_N__a_O_H____。
5. 电导率传感器可辅助探究复分解反应的实质。相同条件
下,离子浓度越大,电导率越大,溶液导电性越强。将 含有酚酞的Ba(OH)2溶液平均分成两份置于A、B两个烧 杯中,并插入电导率传感器,往烧杯A中滴加稀硫酸, 往烧杯B中滴加硫酸钠溶液,滴加过程中,这两份溶液 的滴加速率始终相同,测得溶液的电导率变化如图1所示。
考点1 复分解反应的定义 初中化学反应的基本类型包括化合反应、分解反应、
置换反应和复分解反应。下列反应属于复分解反应的是
( D) ACa. OFe++HC2uOS=点O=燃 4==C=a=(FOeHSO)24+D.C2uNaBO.H2H+2H+2OSO2 4===2NHa22OSOC4. +2H2O
知识拓展:(1)常见的碱和盐的溶解性:①碱溶钾钠铵钡 钙。②钾钠铵硝酸盐都可溶;碳酸盐中只溶钾钠铵;
盐酸盐中银不溶;硫酸盐中钡不溶。(BaSO4、AgCl 也不溶于酸)(2)初中常见的八大沉淀:红褐色沉淀: C_u_(O__H_)_2__;蓝色沉淀:F_e_(_O_H__)_3 _;白色沉淀: Al(OH)3、Mg(OH)2、CaCO3、BaCO3 、AgCl、 BaSO4。
九年级人教版下学期化学盐的化学性质复分解反应课件

①观察:上述几个反应有什么特点? ②讨论:由此,你又有哪些新发现? ③归纳:复分解反应的概念、一般形式与特点。
讲授新课
二 复分解反应
酸、碱、盐
复分解反应:由两种化合物互相交换成分,生成另 外两种化合物的反应。
+
+
AB + CD → AD + CB
思考:什么条件下复分解反应才能发生呢???
讲授新课
讲授新课
怎样检验这 些物质中含 有碳酸呢?
讲授新课
以检验碎蛋壳为例
实验用品 实验步骤 实验现象 实验结论
试管、导管 1.将碎蛋壳 1 .
。
连单孔塞、
。
铁架台 2 .
。 2.
。
。
讲授新课
小结
碳酸根或碳酸氢根离子检验方法:
某物质 +稀盐酸
(含碳酸根或碳 酸氢根离子)
+澄清石灰水
产生气体
变浑浊
CO2
CaCO3
讲授新课
2.与碱溶液反应
【实验11-2】向盛有少量碳酸钠溶液 的试管中滴入澄清石灰水,观察现象。
现象: 试管里出现白色沉淀。 分析: 碳酸钠与氢氧化钙反应,
生成一种难溶物碳酸钙。
Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
澄清石灰水 碳酸钠
这个原理常用作两种碱之间的相互转化
没发生改变
Na+、SO42- K+、NO3- K+、SO42- Na+、NO3-
反应前
反应后
讲授新课
盐在水中的溶解性各不相同
这些你都记 住了吗?
➢ 钾盐、钠盐、铵盐、硝酸盐都可溶; ➢ 盐酸盐只有氯化银不可溶; ➢ 硫酸盐只有硫酸钡不可溶; ➢ 碳酸盐只溶钾、钠、铵,剩下都不溶。
最新中考专项复习盐的性质与复分解反应 (共23张PPT)教育课件

性质
举例
碳酸钙与盐酸:_____________________ _C_a_C_O_3+__2_H_C_l=_=_=_C_a_C_l2_+_H_2_O_+CO2↑ 碳酸钠与盐酸:______________ __N_a_2_C_O_3+__2H__C_l=_=_=2_N_a_C_l+_ H2O+CO2↑ (4)盐+酸→ 碳酸氢钠与盐酸:_______________ 新盐+新酸 ____N_aH__C_O_3+__H_C_l=_=_=_N_aCl+H2O+CO2↑ 硝酸银与盐酸:______________
酸碱性 使紫色石蕊溶液变___蓝___,使酚酞溶液 变_红_____
碳酸氢钠受热分解(产物为碳酸钠、水和
(2)某些盐的 热不稳定性
C__O_2_2)_:N_a__H____C__O____3=___=_△_=__=__=___N__a_2_C_O__3+__H__2O__+__C_O_2_↑ 碳酸钙高温分解:___________________
④___白_色____ 用于玻璃、造 固体、易溶 纸、纺织和洗
于水 涤剂的生产等
碳酸氢钠⑤ ____N_a_H_C_O_3 _
小⑥苏打 _________
白色粉末状 固体、易溶 于水
焙制糕点所用 发酵粉的主要 成分之一,医 疗上用于治疗 ⑦____胃_酸___过 多症
名称、化 学式
俗称(成分)
物理性质
俗称(成分)
物理性质
主要用途
氯化钠① ___N_a_C_l__
食盐的主要 成分
白色固体、 易溶于水, 有咸味
作调味品,配 制医用生理盐 水,农业上用 来选种,工业 上制盐酸和氯 气等,消除公 路积雪
人教九年级化学下册第十一单元课题1 生活中常见的盐 第2课时 复分解反应(共24张PPT)

Cl
SO42- OH- CO32-
K+ Na+ ①钾,钠,铵,硝酸盐 4+ NH 都易溶 Ba2+ Ca2+ 碱溶
NO3Ba2+ Ca2+ Mg2+
. . . . . .
Cl- SO42- CO32- OH不溶
全 溶
不溶
不 溶
不 溶
Ag+
小口决
钾钠氨盐硝酸盐, 均能溶于水中间。 硫酸盐中钡不溶, 氯化盐中银不溶。 碳酸钾钠氨盐溶, 氢氧钾钠钙钡溶。
③盐+碱→ 新盐+新碱 条件:反应物两者均可溶; 生成物有沉淀或气体或水 ④盐+盐→ 新盐+新盐 条件:反应物两者均可溶; 生成物有沉淀或气体或水
OH-
NO3溶、挥
溶 溶 溶
Cl溶、挥
溶 溶 溶
SO42溶
溶 溶 溶
CO32溶、挥
溶 溶 溶
酸 、 碱 、 盐 的 溶 解 性 ( 20℃ )
H+
NH4+ K+ Na+ 溶、挥 溶 溶
分析
向盛有少量BaCl2溶液的试管 滴入硫酸钠溶液,观察现象。
现象 化学方程式
溶液产生白色沉淀
BaCl2 +Na2SO4=BaSO4↓+2NaCl
含有SO42--的溶液与BaCl2反应产生 白色沉淀,且沉淀不溶于硝酸,证明含 有SO42--
分析
Na2CO3 + 2 HCl === 2NaCl + CO2↑+H2O NaHCO3 + HCl === NaCl + CO2↑+H2O
溶液产生白色沉淀
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
人教版初中化学九下11.1 生活中常见的盐 -复分解反应 课件

14. 没有哪种教育能及得上逆境。 15. 拿望远镜看别人,拿放大镜看自己。 2. 在世界的历史中,每一伟大而高贵的时刻都是某种热忱的胜利。 10. 每天睁开眼看见你和阳光都在,那便是我想要的未来。 5. 你曾打开窗户,让我向外面的世界张望;你还用生硬的手拍打掉我从乡里带来的一身黄土,把你充满碳烟味的标志印烙在我的身上,老实说 ,你也没有能拍打净我身上的黄土;但我的身上确是烙下了你的印记! 15. 相信就是强大,怀疑只会抑制能力,而信仰就是力量。 4. 失去才是成长过程最坚硬的后台。 9. 如果你问一个善于溜冰的人怎样获得成功时,他会告诉你:“跌倒了,爬起来。”这就是成功。 2. 能力是挥出去的一把锋利的剑,素质则是握住剑柄的手。 6. 快乐是一时的。幸福是值得反复回味的。 6. 人之所以能,是相信能。 6. 只要瞄准了大方向,坚持不懈地做下去,才能够扫除挡在梦想前面的障碍,实现美好的人生蓝图。 6. 通过一段血火般的洗礼,他相信,自己历尽千辛万苦而酿造的生活之蜜,肯定比轻而易举哪来的更有滋味! 7. 觉得自己做的到和做不到,其实只在一念之间。 11. 人生只有创造才能前进;只有适应才能生存。
1、应用复分解反应预测反应是否能发生
判断下列两种物质是否能发生化学反应, 能反应的写出化学方程式。
Ca(OH)2+K2CO3 ==CaCO3 ↓+2KOH Na2SO4+Ba(NO3)2 ==BaSO4 ↓+2NaNO3 CuSO4+BaCl2 ==BaSO4 ↓+CuCl2 2Al(OH)3+3HCl ==2AlCl3+3H2O KNO3+NaCl 不能反应
Na2CO3 Na2CO3
KCl 不能 HCl 能,↑
KCl 不能
不能
1、应用复分解反应预测反应是否能发生
判断下列两种物质是否能发生化学反应, 能反应的写出化学方程式。
Ca(OH)2+K2CO3 ==CaCO3 ↓+2KOH Na2SO4+Ba(NO3)2 ==BaSO4 ↓+2NaNO3 CuSO4+BaCl2 ==BaSO4 ↓+CuCl2 2Al(OH)3+3HCl ==2AlCl3+3H2O KNO3+NaCl 不能反应
Na2CO3 Na2CO3
KCl 不能 HCl 能,↑
KCl 不能
不能
人教版九年级化学下册第11单元复习课件2盐的化学性质与复分解反应(共43张PPT)
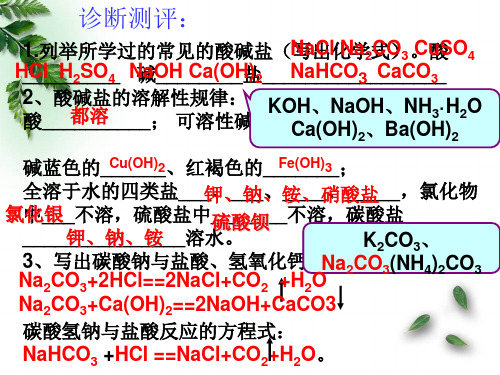
A.加入AgNO3溶液和几滴稀硝酸 B.加入紫色的石蕊试液 C.加入BaCl2溶液和几滴稀硝酸 D.先加入紫色的石蕊试液,再另取溶 液加入AgNO3溶液和几滴稀硝酸
A、产生白色AgCl沉淀只能鉴定有Cl-
B、紫色石蕊变红色只能鉴定有H+
C、不反应 D、紫色石蕊变红色鉴定有H+,产生白色 AgCl沉淀鉴定有Cl-
B.在氢氧化钠溶液中:H+、Mg2+、Cl-
C.在氯化钠溶液中:K+、Ca2+、NO3D.在硫酸铵溶液中:Na+、Cu2+、OH-
H+ OH-
NH4+
物质或离子共存题
2、下列各组物质分别加入足量的水中,能得到
无色透明溶液的是( )
D
A.FeCl3、NaOH、NaCl B.Na2SO4、HCl、BaCl2 C.CuSO4、KCl 、HCl D.Na2CO3、NaCl、Na2SO4
诊断测评:
1.列举所学过的常见的酸碱盐(N写a出Cl化N学a2式CO)3。Cu酸SO4 H_C_l__H_2_S_O_4_ N碱aO__H_C__a_(O__H盐)2___N_a_H__C_O_3__C_a_C__O_3_ 2酸、__酸_都碱__溶盐__的__溶_解;性可规溶律性:碱有K5O种CHa_、(_ON_H_a)_O2_、H_、B__aN,(OH不H3·)溶H22性O
A、Ca(OH)2
B、CaO
C、CaCO3
D、AgNO3
AgNO3+HCl=AgCl +HNO3
Ca(OH)2+2HCl=CaCl2+2H2O
复分解反应的产物--沉淀、气体或水
八大沉淀
不共存离子对
A、产生白色AgCl沉淀只能鉴定有Cl-
B、紫色石蕊变红色只能鉴定有H+
C、不反应 D、紫色石蕊变红色鉴定有H+,产生白色 AgCl沉淀鉴定有Cl-
B.在氢氧化钠溶液中:H+、Mg2+、Cl-
C.在氯化钠溶液中:K+、Ca2+、NO3D.在硫酸铵溶液中:Na+、Cu2+、OH-
H+ OH-
NH4+
物质或离子共存题
2、下列各组物质分别加入足量的水中,能得到
无色透明溶液的是( )
D
A.FeCl3、NaOH、NaCl B.Na2SO4、HCl、BaCl2 C.CuSO4、KCl 、HCl D.Na2CO3、NaCl、Na2SO4
诊断测评:
1.列举所学过的常见的酸碱盐(N写a出Cl化N学a2式CO)3。Cu酸SO4 H_C_l__H_2_S_O_4_ N碱aO__H_C__a_(O__H盐)2___N_a_H__C_O_3__C_a_C__O_3_ 2酸、__酸_都碱__溶盐__的__溶_解;性可规溶律性:碱有K5O种CHa_、(_ON_H_a)_O2_、H_、B__aN,(OH不H3·)溶H22性O
A、Ca(OH)2
B、CaO
C、CaCO3
D、AgNO3
AgNO3+HCl=AgCl +HNO3
Ca(OH)2+2HCl=CaCl2+2H2O
复分解反应的产物--沉淀、气体或水
八大沉淀
不共存离子对
11.1 生活中常见的盐 第3课时 复分解反应和盐的化学性质 课件 人教版九年级化学下册
随堂检测
知识点2:盐的化学性质 5.下列实验现象描述正确的是( C ) A.打开浓盐酸的瓶塞,可观察到瓶口有白烟 B.在滴有石蕊的氢氧化钠溶液中滴加过量的稀 硫酸可观察到溶液由蓝色逐渐变紫色 C.向小苏打固体中滴加稀盐酸可观察到白色固 体逐渐减少,固体表面有气泡产生 D.铁丝放入硫酸锌溶液中可观察到溶液由无色 变为浅绿色
课堂导案
随堂检测
知识点1:复分解反应及条件 1.下列关于复分解反应的说法正确的是
(D) A.中和反应不属于复分解反应 B.反应物必须都溶于水 C.反应物一定有酸 D.生成物一定有盐
随堂检测
2.下列反应属于复分解反应的是( C ) A.CaCO3+CO2+H2O===Ca(HCO3)2 B.2Fe(OH)3===Fe2O3+3H2O C.Na2CO3+BaCl2===BaCO3↓+2NaCl D.Fe+CuSO4===Cu+FeSO4
拓展提升
15.下图中的几种物质是常见的盐,请回答下 列问题。 (1)在碳酸钠溶液中滴入 氯化钙溶液,现象是 ___________白__色__沉__淀____________________。 (2)碳酸钙、碳酸钠均能与稀盐酸反应生成 CO2,是因为碳酸钙、碳酸钠中均含有__C_O_23-___ (写离子符号)
硫酸盐不溶钡和铅,碳酸盐只溶钾、钠、铵。
3.中考中常考的沉淀有:
白色沉淀:CaCO3、Mg(OH)2 不溶于稀酸的白色沉淀: AgCl
蓝色沉淀:____C_u_(_O_H_)_2___
红褐色沉淀:__F_e_(_O_H_)_3___
、__B_a_S_O_4____
课堂导案
知识点1:复分解反应及条件 1.定义:两种化合物互相交换成分,生成另外两种化
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
盐酸腐蚀含CaCO3的建材
导入新课
学习目标
1.掌握盐的化学性质; 2.知道复分解反应的概念、发生的条件和实质,能 判断复分解反应是否能发生。
讲授新课
一 盐的化学性质
1.与酸反应 【实验11-1】碳酸钠、碳酸氢钠分别与 盐酸反应,是否都能产生CO2 ?
碳酸钠+ 盐酸 碳酸氢钠+盐酸
现象
白色固体溶解,放出使澄清石灰水 变浑浊的无色气体
讲授新课
怎样检验这 些物质中含 有碳酸呢?
讲授新课
以检验碎蛋壳为例
实验用品 实验步骤 实验现象 实验结论
试管、导管 1.将碎蛋壳 1 .
。
连单孔塞、
。
铁架台 2 .
。 2.
。
。
讲授新课
小结
碳酸根或碳酸氢根离子检验方法:
某物质 +稀盐酸
(含碳酸根或碳 酸氢根离子)
+澄清石灰水
产生气体
变浑浊
CO2
反应物为多种 特 而生成物只有 征 一种,即“多
变一”
反应物只有一 种而生成物有 多种,即“一 变多”
反应物与生成物 反应物和生成物都 都是两种,且都 为化合物 是单质和化合物
讲授新课
我们已经学过,盐能与金属发生置换反应,如: Fe+CuSO4=Cu+FeSO4
今天学到了,盐能与酸发生复分解反应,如: Na2CO3+2HCl=2NaCl+CO2↑+H2O
九年级化学(RJ) 教学课件
第十一单元 盐 化肥
课题1 生活中常见的盐 第2课时 盐的化学性质 复分解反应
导入新课
讲授新课
课堂小结
随堂训练
导入新课
【回顾】 请书写出实验室制取CO2的方程式。
CaCO3 + 2 HCl === CaCl2 + H2CO3
CO2↑+H2O
【讨论】 根据上述反应,请
问Na2CO3和NaHCO3能 否与稀盐酸反应?如果 能反应,请问它们又会 生成什么物质?
盐能与碱发生复分解反应,如: Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
盐还能与盐发生复分解反应,如: Na2SO4+BaCl2=BaSO4↓+2NaCl
讲授新课
小结
盐的化学性质
1.盐溶液的酸碱性不确定。(如NaCl溶液呈中性, Na2CO3溶液呈碱性,NH4Cl溶液呈酸性)
①观察:上述几个反应有什么特点? ②讨论:由此,你又有哪些新发现? ③归纳:复分解反应的概念、一般形式与特点。
讲授新课
二 复分解反应
酸、碱、盐
复分解反应:由两种化合物互相交换成分,生成另 外两种化合物的反应。
+
+
AB + CD → AD + CB
思考:什么条件下复分解反应才能发生呢???
讲授新课
根据所提供的四种溶液,设计实验证明溶液两两之 间是否能发生反应。√表示反应,×表示不反应。
H2SO4 BaCl2 NaOH Na2CO3
H2SO4
√ √ √
BaCl2
√
× √
NaOH
√ ×
×
Na2CO3
√
√ ×
(1)BaCl2+H2SO4= (2)NaOH+H2SO4= (3)Na2CO3+H2SO4=
没发生改变
Na+、SO42- K+、NO3- K+、SO42- Na+、NO3-
反应前
反应后
讲授新课
盐在水中的溶解性各不相同
这些你都记 住了吗?
➢ 钾盐、钠盐、铵盐、硝酸盐都可溶; ➢ 盐酸盐只有氯化银不可溶; ➢ 硫酸盐只有硫酸钡不可溶; ➢ 碳酸盐只溶钾、钠、铵,剩下都不溶。
注意:AgCl、BaSO4既不溶于水,也不溶于稀硝酸。
CaCO3
讲授新课
2.与碱溶液反应
【实验11-2】向盛有少量碳酸钠溶液 的试管中滴入澄清石灰水,观察现象。
现象: 试管里出现白色沉淀。 分析: 碳酸钠与氢氧化钙反应,
生成一种难溶物碳酸钙。
Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
澄清石灰水 碳酸钠
这个原理常用作两种碱之间的相互转化
复分解反应发生的条件 ①生成水;②生成气体;③生成沉淀。(满足一条即可)
讲授新课
复分解反应发生时的离子变化
实质
2HCl+Na2CO3 ——√—— Na2SO4+ CO2↑+ H2O
H+、Cl- Na+、CO3 2 - Na+、SO42-
反应前
反应后
溶液中离子种类 发生改变
Na2SO4 + KNO3 —×— K2SO4 + NaNO3 溶液中离子种类
(4)BaCl2+ Na2CO3= (5)BaCl2+ NaOH = (6)Na2CO3 + NaOH =
讲授新课
实验现象及结论: BaCl2+H2SO4= BaSO4 +2HCl 有白色沉淀生成 2NaOH+H2SO4= Na2SO4 + 2H2O 有水生成 Na2CO3+H2SO4= Na2SO4 + H2O + CO2 有气体生成 BaCl2+ Na2CO3= BaCO3 + 2NaCl 有白色沉淀生成 BaCl2+ NaOH =不反应 Na2CO3 + NaOH =不反应
讲授新课
观察与思考
(1)CaCO3 +2HCl==CaCl2 + H2CO3
(2)Na2CO3
+
2HCl==2NaCl
+
H2O+CO2↑ H2COO+C3 O2↑
(3)NaHCO3 + HCl==NaCl + H2COO+C3 O2↑
(4)Na2CO3 + Ca(OH)2== 2NaOH + CaCO3↓
复分解反应
由两种或
由一种物质
定 两种以上物质 生成两种或两种
义 生成另一种物 以上其它物质的
质的反应
反应
由一种单质
与一种化合物反 应,生成另一种 单质与另一种化 合物的反应
由两种化合物
互相交换成分生成 另外两种化合物的 反应
类 型 A+B→AB
AB→A+B+ …. AB + C→A +BC AB + CD→ AD+ BC
分析
碳酸钠(或碳酸氢钠)与盐酸反应生 成了CO2气体
讲授新课
请同学们写出上述反应的化学方程式:
Na2CO3 + 2HCl = 2NaCl + H2COO+3CO2 ↑ NaHCO3 + HCl = NaCl + H2OCO+3 CO2 ↑
综上所述:含有碳酸根离子(CO32-)或碳酸氢根离子 (HCO3-)的盐都能与盐酸反应,产生CO2 气体。
讲授新课
练一练
判断下列复分解反应能否发生: H2SO4 + NaNO3—— 不能 Na2SO4 + BaCl2—— BaSO4↓+ 2NaCl 2HNO3 + K2CO3—— 2KNO3 + CO2↑+H2O KNO3 + NaOH—— 不能
讲授新课 化合反应
化学基本反应类型的比较
分解反应
置换反应
