荧光法测定乙酰水杨酸和水杨酸
分子荧光法测定水杨酸乙酰水杨酸1

分子荧光法测定水杨酸和乙酰水杨酸一、实验目的1、学习荧光分析法的基本原理。
2、掌握应用分子荧光法测定乙酰水杨酸、水杨酸的分析方法。
3、了解F-3501型荧光分光光度计的主要结构及工作原理,掌握其正确的使用方法。
二、实验原理某些物质经紫外光或波长较短的可见光照射后,会发射出较入射波长更长的荧光。
荧光光谱反映了物质的特性,建立在测量荧光光谱基础上的分析方法称为荧光分析法。
当进行荧光测定时,总要选择不同波长的光波进行测定,即一个为激发光——物质所吸收的光;另一个为物质吸收后发出的光称为发射光或荧光。
对同一物质而言,在稀溶液(即A = abc < 0.05)中,荧光的强度F与该物质的浓度C 有以下关系:F = 2.3φabcI0式中φ为荧光过程的量子效率,a为荧光分子的吸光系数,b为试样的吸收光程,I0为入射光的强度。
当I0及b 不变时,上式变为:F= KC其中,K为常数。
荧光分析法具有灵敏度高(一般超过分光光度法2~3个数量级)、取样少、方法快速等特点,现已成为食品、生物医药、天然产品、农业、环境保护、化工等领域中的重要分析方法之一。
但由于许多物质本身不会发生荧光,故在使用范围上受到一定的限制。
乙酰水杨酸(ASA,即阿司匹林)水解能生成水杨酸(SA),而在乙酰水杨酸中,或多或少都存在着水杨酸。
由于两者都有苯环,也有一定的荧光效率,因而在以三氯甲烷为溶剂的条件下,可用荧光法进行测定。
从乙酰水杨酸和水杨酸的激发光谱和荧光光谱中可以发现:乙酰水杨酸和水杨酸的激发波长和发射波长均不同,利用此性质,可在各自的激发波长和发射波长下分别测定。
三、仪器与试剂1、仪器F-3501型荧光分光光度计、电子天平、离心机、真空泵、石英比色皿、移液管、棕色容量瓶、比色管、烧杯、砂芯抽滤装置、量筒、洗耳球、洗瓶等。
阿司匹林中乙酰水杨酸含量的测定
荧光光度法测定阿司匹林中乙酰水杨酸的含量一、实验目的1.掌握用荧光法测定药物中的乙酰水杨酸含量的方法。
2.掌握970CRT 型荧光分光光度计的操作方法。
3.加深对荧光光度法原理的理解。
二、实验原理1.荧光光度法原理(1)常温下,处于基态的分子吸收一定的紫外可见光的辐射能成为激发态分子,激发态分子通过无辐射跃迁至第一激发态的最低振动能级,再以辐射跃迁的形式回到基态,发出比吸收光波长长的光而产生荧光。
在稀溶液中,当实验条件一定时,荧光强度I F 与物质的浓度c 成线性关系:即Kc I F (这是荧光光谱法定量分析的理论依据)。
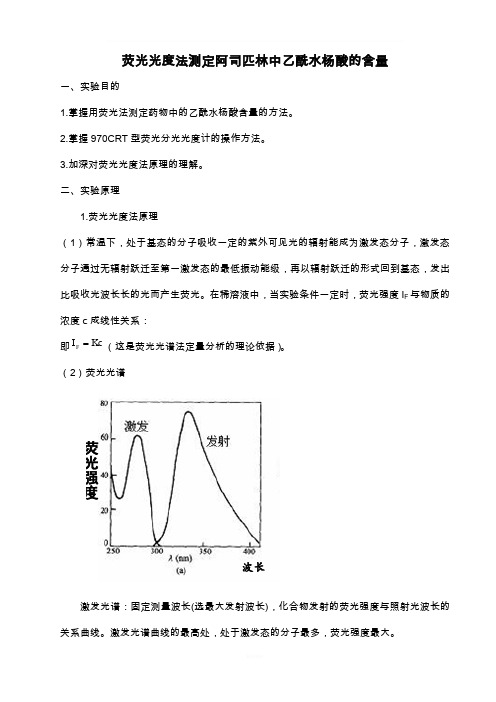
(2)荧光光谱激发光谱:固定测量波长(选最大发射波长),化合物发射的荧光强度与照射光波长的关系曲线。
激发光谱曲线的最高处,处于激发态的分子最多,荧光强度最大。
荧光强度波长发射光谱:固定激发光波长(选最大激发波长), 化合物发射的荧光强度与发射光波长关系曲线。
固定发射光波长进行激发光波长扫描,找出最大激发光波长,然后固定激发光波长进行荧光发射波长扫描,找出最大荧光发射波长。
激发光波长和发射荧光波长的选择是本实验的关键。
2. 荧光光度法测定阿司匹林中乙酰水杨酸的含量通常称为ASA 的乙酰水杨酸(阿司匹林)水解即生成水杨酸(SA )(如下式)。
而在阿司匹林中或多或少存在一些水杨酸,用醋酸—氯仿作为溶剂,然后用荧光法可以分别测定其含量,少许醋酸还可以增加二者的荧光强度(本次实验只测定阿司匹林中乙酰水杨酸的含量)。
在1%的乙酸—氯仿中乙酰水杨酸的激发光谱和荧光光谱如图所示:(为了消除药片之间的差异,可以取几片一起研磨,然后取部分由代表性的样品进行分析)三、仪器与试剂:仪器:970CRT 型荧光分光光度计及附件;容量瓶:1000mL 2只,100 mL 2只,50mL 8只;l0mL 吸管2支;铁架台;研钵;称量瓶;玻璃棒;烧杯;定量滤纸;电子天平。
试剂:冰醋酸;氯仿;乙酰水杨酸;阿司匹林;丙酮。
乙酰水杨酸含量的测定实验报告

一、实验目的1. 掌握乙酰水杨酸含量的测定方法;2. 熟悉酸碱滴定实验操作;3. 了解乙酰水杨酸的性质和应用。
二、实验原理乙酰水杨酸(Aspirin)是一种常用的解热镇痛药,其化学名称为乙酰水杨酸。
本实验采用酸碱滴定法测定乙酰水杨酸含量,原理如下:在强碱性溶液中,乙酰水杨酸中的酯结构在碱性条件下容易水解,生成水杨酸和乙酸盐。
水杨酸具有酸性,可与氢氧化钠(NaOH)反应,生成盐和水。
根据反应的化学计量关系,通过滴定过量的NaOH溶液,可以计算出乙酰水杨酸的含量。
三、实验器材与试剂1. 实验器材:电子天平、滴定管、锥形瓶、移液管、烧杯、漏斗、滤纸、玻璃棒等;2. 试剂:乙酰水杨酸标准品、氢氧化钠标准溶液、酚酞指示剂、蒸馏水等。
四、实验步骤1. 准备标准溶液:准确称取一定量的乙酰水杨酸标准品,溶解于适量蒸馏水中,转移至100mL容量瓶中,定容,配制成一定浓度的标准溶液。
2. 准备样品溶液:准确称取一定量的乙酰水杨酸样品,溶解于适量蒸馏水中,转移至100mL容量瓶中,定容,配制成一定浓度的样品溶液。
3. 滴定实验:(1)取一定量的样品溶液于锥形瓶中;(2)加入适量酚酞指示剂,用氢氧化钠标准溶液滴定至溶液由无色变为浅红色,记录消耗的氢氧化钠标准溶液体积;(3)重复滴定3次,计算平均值。
4. 计算结果:(1)根据滴定反应的化学计量关系,计算出样品中乙酰水杨酸的含量;(2)根据标准溶液的浓度和消耗的氢氧化钠标准溶液体积,计算出乙酰水杨酸的标准品含量;(3)根据样品溶液和标准溶液的浓度比,计算出样品中乙酰水杨酸的含量。
五、实验结果与分析1. 样品中乙酰水杨酸的含量为x mg/g;2. 标准品中乙酰水杨酸的含量为y mg/g;3. 样品中乙酰水杨酸的含量与标准品含量的相对偏差为z %。
六、实验总结通过本次实验,我们掌握了乙酰水杨酸含量的测定方法,熟悉了酸碱滴定实验操作。
实验结果表明,本实验方法具有较高的准确性和可靠性,为乙酰水杨酸的质量控制提供了有力保障。
乙酰水杨酸的合成和纯度检验实验报告

乙酰水杨酸的合成和纯度检验实验报告取少许样品配成乙酸乙酯的溶液待用。
将水杨酸、乙酰水杨酸标样(这两种样品溶液已经配好)和样品点点在硅胶板的同一条线上,在展开剂(石油醚(60-90):乙酸乙酯:冰醋酸=30:10:1)中展开,然后取出挥发干溶剂,在紫外灯下观察个样品点的位置,并标记计算各点的Rf值(哪种物质的Rf值大,为何?)。
[注意事项]
1.水杨酸应当干燥,乙酸酐应当是新蒸的(取用时应相当注意)。
2.反应要严格控制反应温度,温度过高,将增加副产物的生成,如生成水杨酰水
杨酸酯,乙酰水杨酰水杨酸酯。
3.乙酰水杨酸易受热分解,因此熔点不是很明显,它的分解温度为128-135℃,
熔点为136℃,在测熔点时,可先将热载体加热至120℃左右,然后放入样品测定。
乙酰水杨酸的测定与光谱分析

05
乙酰水杨酸测定中的干 扰因素及消除方法
共存离子的干扰及消除
要点一
共存离子的干扰
在测定乙酰水杨酸时,溶液中可能存在的其他离子会对其 产生干扰,影响测定的准确性。
要点二
消除方法
采用离子交换法、萃取法或共沉淀法等分离手段,将干扰 离子从溶液中去除,以减小其对乙酰水杨酸测定的影响。
有机溶剂的干扰及消除
利用超声波的空化作用加速溶剂渗透 和物质传递,可实现乙酰水杨酸的快 速提取和分离。
微波辅助萃取技术
利用微波能加速有机溶剂对样品中乙 酰水杨酸的提取,具有提取效率高、 操作简便、节省时间和溶剂等优点。
测定仪器设备的升级与改造
高性能液相色谱仪
具有高灵敏度、高分辨率和高自动化程度等优点,可实现乙酰水 杨酸的高效分离和准确检测。
可以实现对乙酰水杨酸结构的准确鉴别。
04
乙酰水杨酸测定中的样 品处理技术
萃取技术
液-液萃取
利用两种不混溶的液体(通常为水和有机溶剂) 对乙酰水杨酸进行分离和纯化。
固-液萃取
利用固体吸附剂吸附乙酰水杨酸,然后用溶剂洗 脱,达到分离和纯化的目的。
膜萃取
利用半透膜使水杨酸通过膜而留下乙酰水杨酸, 达到分离目的。
沉淀技术
盐析法
通过加入无机盐使水杨酸或乙酰水杨 酸以沉淀形式析出,再进行分离和纯 化。
共沉淀法
利用杂质离子与乙酰水杨酸形成共沉 淀,将乙酰水杨酸与其他杂质分离。
蒸馏技术
常压蒸馏
利用乙酰水杨酸与杂质的沸点差进行 分离,通过控制蒸馏温度和压力,收 集不同沸点的组分。
减压蒸馏
降低压力使沸点降低,有助于分离沸 点相近的组分和减少能耗。
紫外可见分光光度计
实验荧光法测定乙酰水杨酸和水杨酸

实验荧光法测定乙酰水杨酸和水杨酸一、目的要求1、掌握用荧光法测定药物中乙酰水杨酸和水杨酸的方法。
2、掌握RF-5301型荧光仪的操作方法。
二、原理通常称为ASA的乙酞水杨酸(阿司匹林)水解即生成水杨酸(SA),而在阿司匹林中,都或多或少存在一些水杨酸。
用氯仿作为溶剂,用荧光法可以分别测定它们。
加少许醋酸可以增加二者的荧光强度。
在1,醋酸一氯仿中,乙酞水杨酸和水杨酸的激发光谱和荧光光谱如图1.图1 在1,醋酸一氯仿中,乙酞水杨酸和水杨酸的激发光谱和荧光光谱为了消除药片之间的差异,可取几片药片一起研磨,然后取部分有代表性的样品进行分析。
三、仪器与试剂仪器 RF-5301型荧光仪,石英皿;容量瓶:1000mL 2只,100mL 8只,50mL 10只;l0mL吸管2支。
试剂乙酰水杨酸贮备液:称取0.4000g 乙酰水杨酸溶于1,醋酸一氯仿溶液中,用1,醋酸一氯仿溶液定容于1000mL容量瓶中;水杨酸贮备液:称取0.750g水杨酸溶于1,醋酸一氯仿溶液中,并用其定容于1000mL容量瓶中;醋酸;氯仿。
四、实验步骤1、绘制ASA和SA的激发光谱和荧光光谱将乙酰水杨酸和水杨酸贮备液分别稀释100倍(每次稀释10倍,分二次完成)。
用该溶液,分别绘制ASA和SA的激发光谱和荧光光谱曲线,并分别找到它们的最大激发波长和最大发射波长。
2、制作标准曲线(1) 乙酞水杨酸标准曲线在5只50mL容量瓶中,用吸量管分别加入4.00µg/mLASA溶液2、4、6、8、l0mL,用1,醋酸一氯仿溶液稀释至刻度,摇匀。
分别测量它们的荧光强度。
(2) 水杨酸标准曲线在5只50mL容量瓶中,用吸量管分别加入7.50µg/mL SA溶液2、4、6、8、l0mL,用1,醋酸一氯仿溶液稀释至刻度,摇匀。
分别测量它们的荧光强度。
、阿司匹林药片中乙酰水杨酸和水杨酸的测定 3将5片阿司匹林药片称量后磨成粉末,称取400.0mg用1,醋酸一氯仿溶液溶解,全部转移至100mL容量瓶中,用1,醋酸一氯仿溶液稀释至刻度。
乙酰水杨酸中游离水杨酸的检查原理

乙酰水杨酸中游离水杨酸的检查原理
乙酰水杨酸(Acetylsalicylic acid)是一种水杨酸类药物,它在体内通过代谢转化为游离水杨酸(Salicylic acid)。
游离水杨酸的检查原理一般是通过液相色谱法(HPLC)或气相色谱法(GC)进行分析。
液相色谱法(HPLC)是一种常用的分析方法,它基于样品中溶解的游离水杨酸在特定条件下经过固定相柱进行分离,通过测定出样品中游离水杨酸峰的面积或峰高与标准曲线进行定量分析。
气相色谱法(GC)也可用于游离水杨酸的检测,但是由于游离水杨酸是极性较低的物质,需要在样品前处理过程中采用衍生化技术,将游离水杨酸转化为易挥发性的衍生物,然后通过气相色谱分离并定量。
总之,游离水杨酸的检查原理是利用液相色谱法或气相色谱法对样品中的游离水杨酸进行分离和定量分析。
测定乙酰水杨酸实验报告

一、实验目的1. 学习并掌握乙酰水杨酸(阿司匹林)的提取、纯化和含量测定方法;2. 熟悉乙酰水杨酸的理化性质,加深对药物分析的理解;3. 培养实验操作技能,提高实验数据的处理和分析能力。
二、实验原理乙酰水杨酸(阿司匹林)是一种常用的非甾体抗炎药,具有解热、镇痛、抗炎、抗风湿等作用。
本实验采用酸碱滴定法测定乙酰水杨酸的含量。
乙酰水杨酸在碱性溶液中发生水解反应,生成水杨酸和乙酸盐。
水杨酸在碱性溶液中易升华,而乙酸盐不挥发,因此可以通过测定反应后剩余的乙酸盐含量,间接计算出乙酰水杨酸的含量。
三、实验仪器与试剂1. 仪器:分析天平、滴定管、锥形瓶、烧杯、电热恒温水浴锅、研钵、漏斗、滤纸等;2. 试剂:乙酰水杨酸片剂、氢氧化钠标准溶液、盐酸标准溶液、酚酞指示剂、蒸馏水等。
四、实验步骤1. 乙酰水杨酸提取:取乙酰水杨酸片剂10片,研磨成粉末,准确称取0.1g,置于锥形瓶中;2. 加水溶解:向锥形瓶中加入50ml蒸馏水,充分搅拌,使乙酰水杨酸溶解;3. 加碱水解:向锥形瓶中加入10ml氢氧化钠标准溶液,充分搅拌,使溶液呈碱性;4. 水解反应:将锥形瓶放入电热恒温水浴锅中,加热至80℃,维持水解反应30分钟;5. 冷却:将锥形瓶取出,放入冷水中冷却至室温;6. 加酸回滴:向锥形瓶中加入10ml盐酸标准溶液,充分搅拌,使溶液呈酸性;7. 滴定:用酚酞指示剂指示终点,用氢氧化钠标准溶液滴定至溶液颜色由红色变为无色;8. 计算乙酰水杨酸含量:根据消耗的氢氧化钠标准溶液的体积和浓度,计算出乙酰水杨酸的含量。
五、实验结果与分析1. 乙酰水杨酸提取:实验中,乙酰水杨酸片剂完全溶解,说明实验操作正确;2. 加碱水解:实验中,溶液呈碱性,符合水解反应条件;3. 水解反应:实验中,溶液颜色由红色变为无色,说明水解反应已完成;4. 加酸回滴:实验中,溶液呈酸性,符合回滴反应条件;5. 滴定:实验中,消耗的氢氧化钠标准溶液体积为V1,浓度为C1,计算乙酰水杨酸含量为:乙酰水杨酸含量= (V1 × C1 × 180.16) / 1000六、实验总结1. 本实验成功提取了乙酰水杨酸,并对其含量进行了测定;2. 通过实验,掌握了乙酰水杨酸的提取、纯化和含量测定方法;3. 加深了对乙酰水杨酸理化性质的理解,提高了实验操作技能和数据分析能力;4. 在实验过程中,应注意操作规范,保证实验结果的准确性。
水杨酸的检测方法

水杨酸的检测方法水杨酸可是个挺重要的玩意儿呢!咱得知道怎么检测它呀,不然怎么能放心使用呢!要说检测水杨酸,有一种常见的方法就是高效液相色谱法。
这就好比是一个超级侦探,能把水杨酸从一堆东西里精准地揪出来。
它通过让样品在特殊的柱子里“跑一跑”,然后根据各种信号来确定水杨酸的存在和含量。
就像你在人群中一下子认出你熟悉的朋友一样,高效液相色谱法能准确地识别水杨酸。
还有一种方法是分光光度法。
这个方法就像是一个有特殊眼光的观察者,它能根据水杨酸和某些试剂反应后产生的独特颜色变化来判断水杨酸的情况。
比如说,原本无色透明的溶液,遇到水杨酸后可能就会变得有颜色啦,这不就被发现了嘛!你想想,是不是有点像变魔术一样神奇呀!再说说滴定法,这就像是一场精确的较量。
通过加入特定的试剂,然后一点点地滴加,观察反应的变化,直到达到某个关键点,就能算出水杨酸的含量啦。
就好像你在和水杨酸进行一场拔河比赛,看谁更厉害。
咱检测水杨酸可不能马虎啊!这就好比你要去一个陌生的地方,你得有准确的地图和导航才能不迷路吧。
检测水杨酸就是给我们一个清晰的“地图”,让我们知道它到底在不在,有多少。
不然,用了含有水杨酸的产品,却不知道里面到底有没有水杨酸,或者有多少,那不就跟闭着眼睛走路一样危险嘛!检测水杨酸的方法还有很多呢,每一种都有它独特的本领和用处。
我们得根据具体情况选择合适的方法,就像你要根据不同的场合穿不同的衣服一样。
而且,这些方法也不是一成不变的呀,科学家们还在不断地研究和改进呢,让检测变得更准确、更方便。
所以啊,水杨酸的检测可真是个大学问!我们可得好好了解了解,这样才能在面对各种含有水杨酸的产品时心里有底呀!可别小瞧了这小小的水杨酸检测,它关系着我们的使用安全和效果呢!你说是不是?咱可不能稀里糊涂地就用了,得明明白白地知道里面的水杨酸到底是怎么回事儿!这才是对自己负责嘛!。
乙酰水杨酸中游离水杨酸的检查原理

乙酰水杨酸中游离水杨酸的检查原理
乙酰水杨酸(Acetylsalicylic acid)是一种非处方药物,也被称为阿司匹林(Aspirin)。
它是由水杨酸和乙酰化剂制成的化合物。
乙酰水杨酸通过酯化反应将乙酸基(Acetyl)引入水杨酸
的结构中。
检查乙酰水杨酸中游离水杨酸的主要原理是使用碱(如氢氧化钠溶液)将乙酰水杨酸中的乙酸基水解成乙酸和水杨酸。
随后,水杨酸会与一种酰基化试剂(如费城试剂)反应形成紫色化合物。
以下是检查乙酰水杨酸中游离水杨酸的大致步骤:
1. 取一定量的乙酰水杨酸样品。
2. 加入足量的氢氧化钠溶液,使乙酰水杨酸中的乙酸基水解。
3. 将乙酸和水杨酸混合溶液与酰基化试剂(如费城试剂)混合反应。
4. 反应中,水杨酸与酰基化试剂发生反应生成紫色化合物。
5. 通过比较样品的颜色与一个已知含水杨酸浓度的标准溶液的颜色来测定游离水杨酸的浓度。
需要注意的是,这只是一种简单的方法之一,实际检测中可能使用其他特定的分析方法或设备。
荧光法测定乙酰水杨酸和水杨酸

乙酰水杨酸:250350nm乙酰水杨酸(ASA)(EX)01020乙酰水杨酸(ASA)(EX) No. Start(nm) Apex(nm) End(nm) Height(Data) Valley(nm) Valley(Data)1 250.0 279.5 327.5 14.45 327.5 0.562 2 327.5 344.0 400.0 26.70 400.0 0.122发射光谱:250350nm乙酰水杨酸(ASA)(EM)01020乙酰水杨酸(ASA)(EM) No. Start(nm) Apex(nm) End(nm) Height(Data) Valley(nm) Valley(Data)1 250.0 347.5 400.0 26.21 400.0 1.002水杨酸的激发光谱:250350nm水杨酸(SA)(EX)0102030水杨酸(SA)(EX)No. Start(nm) Apex(nm) End(nm) Height(Data) Valley(nm) Valley(Data)1 250.0 255.0 285.5 10.71 285.5 1.7632 285.5 300.5 400.0 35.67 400.0 0.133发射光谱:250300350400nm水杨酸(SA)(EM)0102030405060708090 100水杨酸(SA)(EM)No. Start(nm) Apex(nm) End(nm) Height(Data) Valley(nm) Valley(Data)1 250.0 303.0 320.0 36.03 320.0 0.777乙酰水杨酸的标准曲线:Standard Calibration2010ug/mlStd.No. 344.0/347.0 Conc (ug/ml) diff RD t1 25.95 0.080 -0.065 -0.2467 -0.4993Comment:2 26.14 0.160 0.058 0.222 0.4492Comment:3 26.45 0.400 0.150 0.5701 1.154Comment:4 26.55 0.800 -0.143 -0.5454 -1.104Samp.No. 344.0/347.0 Conc (ug/ml)1 29.93 4.271Calibration type: 1st orderForce curve through zero: NoMin Conc (ug/ml): 0.080Max Conc (ug/ml): 0.800A0: -27.731A1: 1.0692R: 0.91582R2: 0.83873Lower concentration limit (ug/ml) : 0.000Upper concentration limit (ug/ml) : 1000.000水杨酸标准曲线:-0.10.10.20.30.40.50.60.70.80.91.11.21.3ug/mlStandard Calibration0102030 4050Std.No. 300.0/303.0 Conc (ug/ml) diff RD t 1 39.59 0.160 -0.084 -0.1968 -0.5092 Comment:2 42.61 0.400 0.247 0.5792 1.498 Comment:3 43.04 0.800 -0.072 -0.1695 -0.4385 Comment:4 45.06 1.200 -0.091 -0.2129 -0.5507Samp.No. 300.0/303.0 Conc (ug/ml) 1 47.85 1.636 Calibration type: 1st order Force curve through zero: No Min Conc (ug/ml): 0.160 Max Conc (ug/ml): 1.200 A0: -7.4015 A1: 0.18888 R: 0.93297 R2: 0.87043Lower concentration limit (ug/ml) : 0.000 Upper concentration limit (ug/ml) : 1000.000。
荧光分析法测定水杨酸...

荧光分析法测定药品中的羟基苯甲酸异构体含量一.实验目的1.学习荧光分析法的基本原理和操作;2.熟悉荧光分析法进行多组分含量的测定方法。
二.实验原理1、荧光分析法原理:当被测物质受到光照后,被测物分子吸收了具有特征频率的辐射能,分子从基态上升到激发态,分子在较高能级的激发态时,它可能处于激发态中各种振动状态的一种。
然而由于分子通过与溶剂分子、同类分子或其他分子的碰撞,而失去振动能级,降低至激发态时的最低振动能级,在此过程中并不发光。
但当分子从激发态的最低振动能级,即第一电子激发态的最低振动能级跃迁至基态的各个不同的振动能级时,则以光的形式辐射出能量,所辐射出的光既是荧光。
2、激发光谱和发射光谱:激发光谱:荧光是光致发光,因此必须选择合适的激发光波长,这可以从它们的激发光谱曲线来确定。
绘制激发光谱曲线时,选择荧光的最大发射波长为测量波长,改变激发光的波长,测量荧光强度的变化。
以激发波长为横坐标、荧光强度为纵坐标作图,即得到荧光化合物的激发光谱。
激发光谱的形状与吸收光谱的形状极为相似,经校正后的真实激发光谱与吸收关顾不仅形状相同,而且波长位置也一样。
这是因为物质分子吸收能量的过程就是激发过程。
发射光谱:发射光谱简称荧光光谱。
如果将激发光波长固定在最大激发波长处,然后扫描发射波长,测定不同发射波长处的荧光强度,即得到荧光光谱。
3、试验方法机理:邻- 羟基苯甲酸(亦称水杨酸)和间- 羟基苯甲酸分子组成相同,均含一个能发射荧光的苯环,但因其取代基的位置不同而具有不同的荧光性质。
在pH=12 的碱性溶液中,二者在310nm附近紫外光的激发下均会发射荧光;在pH=5.5的近中性溶液中,间-羟基苯甲酸不发荧光,邻-羟基苯甲酸因分子内形成氢键增加分子刚性而有较强荧光,且其荧光强度与pH=12时相同。
利用此性质,可在pH=5.5 时测定二者混合物中邻-羟基苯甲酸含量时,间-羟基苯甲酸不干扰。
另取同样量混合物溶液,测定pH=12 时的荧光强度,减去 pH=5.5时测得的邻-羟基苯甲酸的荧光强度,即可求出间-羟基苯甲酸的含量。
实验一-乙酰水杨酸的合成

实验一、乙酰水杨酸<阿司匹林>的合成、鉴定与含量的测定一、实验目的(1)学习O-酰化〔酯化〕单元反应的特点和基本知识.(2)了解阿司匹林的性质和工业制法,掌握O-酰化制备阿司匹林的实验方法.<3> 掌握水杨酸酰化反应的原理与实验操作以与乙酰水杨酸的鉴定、提纯与含量测定的方法.<4>了解紫外光谱法、红外光谱法、核磁共振法在有机合成中的应用,掌握紫外-可见分光光度法定量分析的基本原理和实验技术.<5> 进一步熟悉基础化学实验的重结晶与熔点测定等基本操作.二、实验原理乙酰水杨酸〔acetyl Salicylic acid〕,通常也称为阿司匹林<aspirin>,是由水杨酸<邻羟基苯甲酸>和乙酸酐合成的.早在18世纪,人们已从柳树皮中提取了水杨酸,并注意到它可以作为止痛、退热和抗炎药,不过对肠胃刺激作用较大.19世纪末,人们成功地合成了乙酰水杨酸,直到目前,阿司匹林仍然是一个广泛的具有解热镇痛作用的药物.水杨酸是一个具有酚羟基和羧基双官能团化合物,能进行两种不同的酯化反应,当与乙酸酐作用时,可以得到乙酰水杨酸〔即阿司匹林〕;如与过量的甲醇反应,生成水杨酸甲酯,它是第一个作为冬青树的香味成分被发现的,因此通称为冬青油.本实验将进行前一个反应的试验.反应式:在生成乙酰水杨酸的同时,水杨酸分子之间可以发生酯化反应,生成少量的聚合酯:乙酰水杨酸能与NaHCO3反应生成水溶性钠盐,而副产物聚合酯不能溶于NaHCO3,这种性质上的差别可用于阿司匹林的纯化.可能存在于最终产物中的杂质是水杨酸本身,这是由于乙酰化反应不完全或由于产物在分离步骤中发生水解造成的.它可以在各步纯化过程和产物的重结晶过程中被除去,与大多数酚类化合物一样,水杨酸可与FeCl3,形成深色配〔络〕合物,而阿司匹林因酚羟基已被酰化,不再与FeCl3发生颜色反应,因而未作用的水杨酸很容易被检出.乙酰水杨酸的红外光谱特征如图2-21所示:图2-21 乙酰水杨酸的红外光谱图乙酰水杨酸的核磁共振谱特征如图2-22所示.可由IR,1H NMR鉴定产物为乙酰水杨酸.为了测定产品中乙酰水杨酸的含量.产物用稀NaOH溶液溶解, 乙酰水杨酸水解生成水杨酸二钠.图2-22 乙酰水杨酸的核磁共振谱图该溶液在296.5nm左右有个吸收峰,测定稀释成一定浓度乙酰水杨酸的NaOH 水溶液的吸光度值,并用已知浓度的水杨酸的NaOH水溶液作一条标准曲线,可以从标准曲线上求出相当于水杨酸的含量.根据两者的相对分子质量,即可求出产物中乙酰水杨酸的含量,溶剂和其他成分不干扰测定.阿司匹灵乃是现代生活中最大众化的万应药〔治百病的药〕之一,而且,尽管它的奇妙历史开始于200年前,关于这个不可思议的药我们仍有许多东西该学.虽然至今仍然无人确切知道它究竟怎样或为什么会起作用,美国每年消耗的阿司匹灵量却在二千万磅以上.阿司匹灵药片通常由约0.32克乙酰水杨酸与少量淀粉混合并压紧而成.淀粉的作用在于使其粘合成片.加过缓冲剂的阿司匹灵通常含有一种碱性缓冲剂,以减少对胃壁粘膜的酸性刺激作用,因为乙酰化后的产物并非毫无刺激性.一种称为Bufferin的药片含阿司匹灵5谷、二羟胺基乙酸铝0.75谷和碳酸镁1.5谷.复合解痛片通常含阿司匹灵,非那西汀和咖啡因.例如,Empirin即是一号一种典型的APC〔取Aspirin,Phenactin和Caffein三者之字首并合而成〕,它含有阿司匹灵0.233克,非那西汀0.166克,咖啡因0.03克.三、实验仪器和药品UV-1201<或UV2600>紫外-可见分光光度计,电热数显熔点仪,抽滤装置〔玻璃砂芯漏斗〕,循环水式真空泵,电热熔点仪,吸量管,容量瓶<100mL>,锥形瓶<100mL>,石英比色皿,圆底烧瓶〔250mL,磨口〕,温度计,天平.水杨酸,浓硫酸,NaHCO3饱和水溶液,浓HCl,醋酸酐,1%FeCl3溶液,NaOH0.1mol/L,氯仿.四、实验步骤4.1 乙酰水杨酸的合成在干燥的100mL锥形瓶中加入7.0g干燥的水杨酸,10mL新蒸馏的醋酸酐和10滴浓硫酸,不断旋摇锥形瓶,在水浴上加热5-10min,使水杨酸全部溶解〔若不全溶解,则需补加浓硫酸和乙酸酐〕后,.控制水浴温度在80-85℃,维持反应20min,并经常摇动.冷却至室温,即有乙酰水杨酸结晶析出,如果无结晶,可用玻璃棒摩擦瓶壁并将反应物置于冰水浴中冷却使结晶产生.加入50mL冷H2O,混合物继续在冰水中冷却15min使结晶完全.减压过滤,用滤液反复淋洗锥形瓶,直至所有晶体被收集到布氏漏斗中,用少量冷水洗涤结晶,继续抽气将溶剂尽量抽干,称重,得乙酰水杨酸粗产品,呈白色雪花状.将上述粗产品转移到250mL圆底烧瓶中,在搅拌下加入25mLNaHCO3饱和溶液,加完后继续搅拌几分钟,直至无CO2气泡产生,减压抽滤,副产物聚合物应被滤出.用5-10mL水冲洗漏斗,合并滤液,倒入预先盛有5mL浓HCl和10mL水配成溶液的烧瓶中,搅拌均匀,即有乙酰水杨酸沉淀析出.将烧杯置于冰水浴中冷却,使结晶完全,抽滤,并用玻璃塞压干晶体,再用少量冷水洗涤2次,压干,将结晶移到表面皿上,干燥后重约2g.4.2 阿司匹林的鉴定<1>在电热熔点仪上测定熔点,文献值133-135℃, 乙酰水杨酸易受热分解,因此熔点不很明显,它的分解温度为128-138℃,测定熔点时,应将热载体加热至120℃左右,然后放入样品测定.〔2〕用KBr压片法录制产物的红外光谱图,指出各主要吸收特征峰的归属,并与乙酰水杨酸的标准图谱比较,〔3〕以CHCl3为溶剂,测定1H NMR谱图,解析谱图进一步证实产物为乙酰水杨酸.4.3 产物中乙酰水杨酸含量的测定<1> 准确称量0.1000g<准确至0.1mg>水杨酸<分析纯>溶于少量0.1mol/L NaOH〔40mL〕溶液中,摇匀,然后用蒸馏水定容于100mL容量瓶中,标记为"原始标准贮备液" .用 5.00mL吸量管分别吸取0.00mL,1.00mL ,2.00mL,3.00mL,4.00mL,5.00mL原始标准贮备液置于六只100mL 容量瓶中,标记每只容量瓶,用蒸馏水定容至刻度,摇匀,并计算出每只标准溶液的浓度<单位为mg/mL>.在UV-1201紫外分光光度计上扫描每一标准溶液在250-350nm范围的紫外吸收光谱,记录最大吸收波长λmax和最大吸光度Amax.然后在λmax处测定五个标准溶液的吸光度.〔注:应该在296.5nm左右有一个吸收峰〕.<2>准确称量0.1000g本实验合成的乙酰水杨酸,加0.1mol/LNaOH溶液40mL,搅拌数分钟,转移到100mL容量瓶中,用蒸馏水稀释至刻度,摇匀.用此稀释液作为试样,测试250-350nm范围的紫外吸收光谱,读出λmax的吸光度值.4.4 酚的重要性质与鉴定实验水杨酸既是酸又是酚,可利用水杨酸来进行酚的重要性质和鉴定的实验.阿司匹林由于不具酚羟基,因此就不再具备酚的特性.<1>酚的弱酸性实验:取0.1g水杨酸,加入1mL蒸馏水,振荡,用PH试纸测试其水溶液的酸碱性.逐渐加入10%NaOH溶液使其全部溶解,滴入10%盐酸溶液,观察现象并解释原因.同样取0.1g乙酰水杨酸作对比实验,观察并解释结果.<2>三氯化铁实验:在两个试管中分别加入1mL的1%水杨酸水溶液与1%阿司匹林稀释乙醇溶液,分别滴入2滴1%FeCl3溶液,摇动,观察现象并解释之.有颜色反应为正性反应.若结晶不纯,杂质主要为水杨酸,此时加1%FeCl3呈蓝色.<3>溴水实验:在装有1mL的1%水杨酸水溶液的试管中逐滴加入Br2-KBr/H2O,观察现象并解释之.溴水退色为正性反应,试分析该原因.〔注:本实验不做〕五、数据处理<1> 将有关实验数据填入表2-10.并请绘制出工作曲线.<2>计算乙酰水杨酸的含量:根据实验合成的乙酰水杨酸溶液在λmax处的吸光度值,从工作曲线上查到溶液的水杨酸质量浓度<单位为mg/mL>,然后换算成乙酰水杨酸的含量m<乙酰水杨酸>=ρ<乙酰水杨酸>×100×100/1000=ρ<水杨酸>×<180.15/138.12>×100×100/1000 乙酰水杨酸的百分含量η〔%〕=乙酰水杨酸/样品质量×100%=m〔乙酰水杨酸〕/m s〔样品〕×100% 式中m---乙酰水杨酸的质量,g;ρ---乙酰水杨酸密度,mg/mL.水杨酸的分子量是138.12;乙酰水杨酸的分子量是180.15.六、注意事项1. 由于分子内氢键的作用,水杨酸与乙酸酐直接反应需在150~160℃才能生成乙酰水杨酸.加入硫酸的目的主要是破坏氢键的存在,使反应在较低的温度下<90℃>就可以进行,而且可以大大减少副产物,因此实验中要注意控制好温度.2. 如果有水,易使乙酸酐水解,此反应开始时,锥形瓶应经过干燥处理,药品水杨酸也要事先经过干燥处理.3. 粗产品杂质主要是水杨酸〔因此若结晶不纯,则加入FeCl3时溶液显紫色〕,可用乙醇—水,或1:1<体积比>的稀盐酸,或苯和石油醚<30~60℃>的混合溶剂进行重结晶.思考题1. 在硫酸存在下,水杨酸与乙醇反应会得到什么产物?本试验加入硫酸的目的是什么?2. 本实验中,测定产品的乙酰水杨酸百分含量时,为什么加入NaOH稀溶液?3. 紫外分光光度计定量分析的基础是什么?4. 核磁共振和红外光谱定性分析乙酰水杨酸的原理是什么?尝试查阅相关资料〔有关有机化学、有机波谱分析方面的书籍〕来解析本试验红外光谱图和核磁共振谱图.5. 制备阿司匹林的工艺路线较多,请另举出一种制备方法.6. 纯净的阿司匹灵对10%FeCl3呈负结果.如果纯的阿司匹灵是从95%乙醇中结晶而来,回收的晶体有时对10%FeCl3溶液呈正结果.说明为什么会发生此结果,并写出发生的反应.7. 如果一瓶阿司匹林变质,你能否通过闻味来鉴定?8. 水杨酸的乙酰化反应中产生的副产物是什么?如何将产品与副产物分开?为什么水杨酸聚合物不能和碳酸氢钠反应生成水溶性产物?。
乙酰水杨酸的测定与光谱分析 共25页PPT资料
混合,调成糊状,夹在盐片中测定。液体石蜡本身有红外 吸收,此法不能用来研究饱和烷烃的红外吸收。
(3)薄膜法
主要用于高分子化合物的测定。可将它们直接加热熔 融后涂制或压制成膜。也可将试样溶解在低沸点的易挥 发溶剂中,涂在盐片上,待溶剂挥发后成膜测定。
(3)试样的浓度和测试厚度应选择适当,以使光 谱图中的大多数吸收峰的透射比处于10%~80% 范围内。
1 . 固体试样
(1)压片法 将1~2mg试样与200mg纯KBr研细均匀,置于模
具中,用(5~10)107Pa压力在油压机上压成透明薄片 ,即可用于测定。试样和KBr都应经干燥处理方法:酚羟基与三氯化铁溶液的显色反应 (1)物理方法:IR;1H-NMR;UV
3. 主要药品与仪器
乙酰水杨酸 三氯化铁溶液 溴化钾
试管 IR测定仪 NMR测定仪
4. 样品制备方法
要获得一张高质量红外光谱图,除了仪器本身的因 素外,还必须有合适的样品制备方法。 一、红外光谱法对试样的要求
盐片间成膜
3 .气体样品
气态样品 可在玻璃气槽内进行 测定,它的两端粘有红外透光的NaCl 或KBr窗片。先将气槽抽真空,再将 试样注入。
5. 乙酰水杨酸的特征红外吸收
乙酰水杨酸的1H-NMR谱
Assign. A B C D E F
Shift(ppm) 11. 8.125 7.624 7.356 7.142 2.352
定性及定量分析。不同的物质具有不 同的化学键,其吸收波长不同(定 性);而对光波吸收的多少与物质的 量成正比,因此可以用来定量。
END
当样品量特别少或样品面积特别小时,采用光束聚光 器,并配有微量液体池、微量固体池和微量气体池,采 用全反射系统或用带有卤化碱透镜的反射系统进行测量。
阿司匹林中乙酰水杨酸和水杨酸含量的测定(正式)
09级临床药学唐辰逍0929014、彭文星0929012、邸宣0929009
一、实验目的
1.掌握用紫外可见分光光度法测定药物中乙酰水杨酸的方法。
2.学会使用UV-2550紫外-可见分光光度计。
二、实验原理
阿司匹林是解热镇痛药,主要成分为乙酰水杨酸,摩尔质量180.16g/mol。阿司匹林少量水解成水杨酸,因而在阿司匹林样品中混有少量水杨酸。
本实验采用双波长法和校正曲线法。水杨酸干扰阿司匹林的吸光度测定,在选定的两波长下测定吸光度差值。配制一系列浓度不同的标准阿司匹林溶液,在测定条件相同的情况下,分别测定其在两个波长下的吸光度,以标准浓度为横坐标,以相应吸光度差值为纵坐标,绘制△A-C关系图,在相同条件下测出试样在两波长处的吸光度,可从校正曲线上查出试样液的浓度。
0.4188
C
40.24
60.36
80.48
100.6
120.72
x
2.标准曲线(△A-C关系图)
第一次测量
第二次测量
3.利用第一次测量得出的曲线,根据样品的吸光度值,在标准曲线上找到相应的浓度94.37μl/ml。
因样品稀释10倍,故原样品溶液浓度为943.7μl/ml=0.9437mg/ml。
故样品中阿司匹林的质量为0.9437*50=47.185mg。
样品溶液的配置:取1片阿司匹林研细,加入无水乙醇1~2ml分次研磨,使溶解。利用滤膜过滤后转入50ml容量瓶中,充分振摇,乙醇定容(浓度:800μl/ml)。取1ml定容后的样品溶液,转入10ml容量瓶,乙醇定容。配置成约为80μl/ml的样品溶液。
2.波长选择
使用紫外-可见分光光度计,先用95%乙醇进行基线校正。用阿司匹林标准品3和稀释过的水杨酸标准品进行光谱测量。将扫描波长范围定在200-400nm,分别找出两者的最大吸收峰。阿司匹林标准品在277.5nm、235.0nm处有最大吸收峰。因在277.5nm处,阿司匹林、水杨酸均有吸收,故采用双波长法。以277.5nm为λ1,从水杨酸的光谱中找到与277.5nm处A值相等的点所对应的波长值λ2=320nm。
乙酰水杨酸含量测定中避免水杨酸干扰的中和滴定法

乙酰水杨酸含量测定中避免水杨酸干扰的中和滴定法
乙酰水杨酸是一种常见的有机物,其含量测定中常常需要避免水杨酸的干扰。
下面介绍一种中和滴定法,可以有效地避免水杨酸的干扰。
步骤:
1. 准备样品:将乙酰水杨酸样品称取适量,溶解在适量的乙醇中,并转移至容量瓶中。
然后用乙醇稀释至初始体积,均匀混合。
2. 加入指示剂:向样品中加入几滴酚酞指示剂,使样品呈现淡红色。
3. 滴定:将标准氢氧化钠(NaOH)溶液灌入滴定管中,滴定管上缓慢滴加至样品中,同时轻轻摇晃容器直到样品颜色完全变为淡红色。
此时记录滴定管中氢氧化钠溶液的用量。
4. 控制实验:重复上述实验操作,不同的是将样品中的乙酰水杨酸改为相同浓度的水杨酸。
记录滴定管中氢氧化钠溶液的用量。
5. 结果计算:乙酰水杨酸的含量可以通过以下公式计算得出:乙酰水杨酸含量(%)=(实验1用量-实验2用量)* 相对分子质量 * 0.1 / 样品量(g)
这种中和滴定法可以消除水杨酸对乙酰水杨酸测定的干扰,因为水杨酸本身不参与滴定反应。
同时,选择合适的指示剂可以
使分析结果更加准确和可靠。
需要注意的是,在进行实验前要进行验证,确保该滴定法适用于乙酰水杨酸测定的条件。
荧光测定阿司匹林肠溶片中水杨酸实验的绿色化

荧光测定阿司匹林肠溶片中水杨酸实验的绿色化韩迎春;赵丽华;龚时琼;付世涛【摘要】以PEG800-PVP3000-(NH4)2 SO4-H2 O为体系,双水相萃取取代原氯仿萃取,分离富集待测物水杨酸,实现了荧光检测阿司匹林肠溶片中水杨酸含量的荧光光谱分析实验的绿色化.实验测定了水杨酸在PEG-PVP水相中最佳激发波长315nm,最佳发射波长386nm,水杨酸在0~10μg/mL浓度范围符合比尔定律,阿司匹林肠溶片中水杨酸的含量约为20%.实验培养了学生利用分析仪器检测实际样品的综合能力.【期刊名称】《实验室科学》【年(卷),期】2018(021)004【总页数】4页(P4-7)【关键词】双水相萃取;荧光光谱;水杨酸;绿色化【作者】韩迎春;赵丽华;龚时琼;付世涛【作者单位】华中科技大学化学与化工学院, 湖北武汉 430074;华中科技大学化学与化工学院, 湖北武汉 430074;华中科技大学化学与化工学院, 湖北武汉430074;华中科技大学化学与化工学院, 湖北武汉 430074【正文语种】中文【中图分类】O6-3阿司匹林是经典的镇痛解热药,同时发现具有抑制血小板聚集,防止血栓形成的作用[1-2]。
阿司匹林的主要成分为乙酰水杨酸,其中含有的少量水杨酸杂质对胃肠道有一定的刺激作用,药典中将其含量作为控制阿司匹林质量的重要指标,以液相色谱法进行定量检测。
传统大学仪器分析实验中利用1%醋酸-氯仿为溶剂,对阿司匹林片剂中的水杨酸进行检测[3],而氯仿有害人体健康,也对环境造成污染。
双水相萃取技术是20世纪初发现并发展起来的一种分离技术[4],很快发展到化工、生物、医药等多个领域[5-7],被证明是一种高效的分离方法。
本实验利用聚乙二醇800-PVP双水相体系萃取阿司匹林肠溶片中水杨酸,测定其含量[8-10],实现了该实验的绿色化。
1 实验目的(1)了解双水相萃取的特点、分类、方法原理以及主要应用,选取合适的双水相体系萃取阿司匹林中水杨酸;(2)熟悉荧光分析方法的操作步骤,测定水杨酸的含量;(3)学习使用分子荧光光谱仪,并进行定量检测。
荧光法测定乙酰水杨酸和水杨酸

长;
l
‘ 2
>
l
2
>
l
1
;
磷光发射:电子由第一激发三重态的最低0进入T1的可能过程:( S0 → T1禁阻跃迁)
S0 →激发→振动弛豫→内转移→系间跨越→振动弛豫→ T1 发光速度很慢: 10-3~10 s 。
光照停止后,可持续一段时间。
2019/5/24
试剂:乙酰水杨酸,水杨酸,乙醇,阿司 匹林药片。
2019/5/24
实验步骤
1、ASA和SA贮备溶液的配制 (1)ASA贮备液的配制:称取0.4000g乙酰水杨酸溶于1%醋酸-氯仿溶 液中,用 1%醋酸—氯仿溶液定容于1000mL容量瓶中,摇匀,备用; (2)SA贮备液的配制:称取0.750g水杨酸溶于1%醋酸—氯仿溶液中, 用 1%醋酸—氯仿溶液定容于1000mL容量瓶中,摇匀,备用。 2、ASA和SA激发光谱和荧光光谱的绘制 将ASA和SA贮备液分别稀释100倍(分二次完成,每次稀释10倍)。用得 到的溶液分别扫描ASA和SA的激发光谱和荧光光谱曲线,并分别确定 它们的最大激发波长和最大发射波长。 3、标准曲线的制作 (1) ASA标准曲线的制作
6、比色皿的检测面和放入检测腔的位置一定要 固定。
2019/5/24
荧光法测定乙酰水杨酸和水杨 酸
实验化学3-2 (仪器分析实验)
2019/5/24
1、实验目的 (1)掌握荧光法测定药物中乙酰水杨酸
的方法 (2)了解Cary Eclipse型荧光光谱仪的
基本操作 (3)强化称量、移液、配溶液等基本操
作
2019/5/24
实验原理
电子处于激发态是不稳定状态,返回基态时,通过辐射 跃迁(发光)和无辐射跃迁等方式失去能量;
荧光法测定水杨酸片中水杨酸的含量

第41卷第2期吉林师范大学学报(自然科学版)Vol.41ꎬNo.2㊀2020年5月JournalofJilinNormalUniversity(NaturalScienceEdition)Mayꎬ2020收稿日期:2020 ̄02 ̄27基金项目:国家青年自然科学基金项目(51609100)ꎻ吉林省科技发展计划项目(20160101287JC)第一作者简介:孙艳涛(1979 )ꎬ女ꎬ吉林省辽源市人ꎬ教授ꎬ博士ꎬ硕士生导师.研究方向:色谱与光谱分析.doi:10.16862/j.cnki.issn1674 ̄3873.2020.02.011荧光法测定水杨酸片中水杨酸的含量孙艳涛1ꎬ李美锡1ꎬ刘仕聪1ꎬ李㊀林1ꎬ刘㊀洋2(1.吉林师范大学化学学院ꎬ吉林四平136000ꎻ2.吉林师范大学物理学院ꎬ吉林四平136000)摘㊀要:利用荧光法测定水杨酸片中水杨酸的含量.用甲醇作为水杨酸的溶剂ꎬ对溶液的酸碱性㊁稳定性及其线性范围等条件进行了考察.结果表明ꎬ水杨酸含量在(0.387~1.935)ˑ10-8mol L-1范围内具有良好的线性关ꎬ水杨酸片中水杨酸的含量为1.636ˑ10-8mol L-1.关键词:荧光法ꎻ水杨酸ꎻ含量测定中图分类号:O65㊀㊀文献标志码:A㊀㊀文章编号:1674 ̄3873 ̄(2020)02 ̄0083 ̄06㊀㊀水杨酸(其结构如图1所示)是一种天然的消炎药ꎬ可以祛角质㊁杀菌㊁消炎等ꎬ因而在消炎等需求的用药及化妆品中都含有适量的水杨酸.复方水杨酸片㊁阿司匹林㊁复方乙酰水杨酸片及尼美舒利等含水杨酸的制剂作为医院的处方药应用广泛[1 ̄6].文献报道制剂中水杨酸含量的测定方法主要有荧光光谱法ꎬ电位滴定法ꎬ紫外 ̄可见分光光度法ꎬ库伦滴定法及高相液相色谱法[7 ̄11].荧光分光光度测定法具有灵敏度高㊁选择性强㊁用量少和方法简便等优点[12 ̄13]ꎬ常用于有机物和无机物的定性定量分析.本实验利用荧光光谱法考察了水杨酸片中水杨酸的含量.OHO OH图1㊀水杨酸的结构式Fig.1㊀Molecularstructureofsalicylicacid1㊀实验1.1㊀仪器与试剂1.1.1㊀仪器PELS ̄55型荧光光谱仪ꎬpHS ̄3C数字酸度计ꎬShimadzuUV ̄2550型紫外分光光度计ꎬSK5200H超声波清洗器ꎬBT125D十万分之一电子天平ꎬ可调式移液器.1.1.2㊀试剂水杨酸片ꎬ水杨酸标准品ꎬ甲醇(色谱纯)ꎬ冰醋酸(分析纯)ꎬ氯仿(分析纯)ꎬ实验用水(二次蒸馏水).48吉林师范大学学报(自然科学版)第41卷1.2㊀配制溶液1.2.1㊀样品溶液的配制准确称取水杨酸片粉末0.00210g于10mL的容量瓶中ꎬ用甲醇定容ꎬ超声15minꎬ配制成1.522ˑ10-6mol L-1的水杨酸片溶液.1.2.2㊀标准品溶液的配制准确称取水杨酸标准品0.00267g于10mL的容量瓶中ꎬ用甲醇定容ꎬ超声15minꎬ配制成1.935ˑ10-6mol L-1的水杨酸标准品溶液ꎬ使用时适当稀释.1.3㊀设置参数1.3.1㊀二维荧光光谱参数将激发光谱范围设置为310~600nmꎬ发射和激发的狭缝均设为15.0nmꎬ荧光波长设为301nmꎬ扫描速度设为1000nm min-1.1.3.2㊀三维荧光光谱参数激发波长设置为200~400nmꎬ发射波长设置为310~600nmꎬ发射和激发的狭缝均设为15.0nmꎬ扫描步长设为10nmꎬ扫描次数设为20次ꎬ扫描速度设为1000nm min-1[13].1.4㊀优化条件1.4.1㊀溶剂的考察准确移取4份30μL水杨酸标准溶液ꎬ分别加入甲醇㊁1%醋酸 ̄甲醇溶液㊁氯仿和1%醋酸 ̄氯仿不同溶剂ꎬ总体积为3.5mL.1.4.2㊀酸度的考察准确移取20μL水杨酸标准溶液和10μL不同pH值的缓冲液ꎬ配制1.1056ˑ10-5mol L-1的水杨酸标准溶液.配制三组平行样ꎬ考察荧光强度随溶液酸度的变化情况.1.4.3㊀稳定性的考察分别准确移取2份20μL水杨酸标准溶液配制成浓度为1.1056ˑ10-5mol L-1的水杨酸溶液.在密封㊁避光和干燥条件下ꎬ考察其荧光强度在48h内的变化情况.1.5㊀绘制标准曲线分别准确移取100㊁300㊁500㊁700㊁900和1000μL的水杨酸标准溶液ꎬ用甲醇稀释配制成3mL一系列不同浓度的水杨酸标准溶液并进行检测ꎬ绘制纵坐标为荧光强度(F)ꎬ横坐标为浓度(c)的标准曲线.2㊀结果与讨论2.1㊀溶剂的选择水杨酸易溶于醇类试剂ꎬ实验考察了四种溶剂分别是甲醇㊁1%醋酸 ̄甲醇㊁氯仿和1%醋酸 ̄氯仿.图2为上述不同溶剂中水杨酸的二维荧光光谱.从图2可知不同溶剂中水杨酸的激发和发射光谱形状略有不同ꎬ以甲醇作为溶剂ꎬ从图2(A)中可知水杨酸的荧光强度为725ꎻ以氯仿作溶剂ꎬ从图2(C)中观察到水杨酸的最大发射波长发生蓝移ꎬ且其荧光强度为240ꎻ以1%醋酸 ̄甲醇和1%醋酸 ̄氯仿作为溶剂的水杨酸最大发射波长发生红移ꎬ荧光强度分别为177和128.由此可知ꎬ使用甲醇作溶剂ꎬ水杨酸的荧光性质稳定ꎬ强度较大.2.2㊀二维荧光光谱利用紫外分光光度计测得303nm为水杨酸的最大吸收波长ꎬ将激发波长设为303nmꎬ在300~600nm范围内绘制水杨酸的发射光谱ꎬ确定430nm为其最大发射波长.将发射波长设置为430nmꎬ在200~430nm范围内绘制水杨酸的激发光谱ꎬ确定其具有两个激发波长分别为210nm和303nm.再分别以210nm和303nm作为激发波长ꎬ绘制其发射波长ꎬ确定其最大发射波长分别为405nm和398nmꎬ结果见图3.最终选择荧光强度最大的发射波长405nm作为测量波长.第2期孙艳涛ꎬ等:光法测定水杨酸片中水杨酸的含量㊀㊀(A)甲醇ꎻ(B)1%醋酸 ̄甲醇ꎻ(C)氯仿ꎻ(D)1%醋酸 ̄氯仿图2㊀不同溶剂中水杨酸的二维荧光光谱Fig.2㊀Two ̄dimensionaldiagramofsalicylicacidinthedifferentsolvents(Ex1=303nmꎬEx2=210nmꎬEm1=405nmꎬEm2=398nm)图3㊀水杨酸的二维图Fig.3㊀Two ̄dimensionaldiagramofsalicylicacid2.3㊀三维荧光光谱三维荧光光谱图具有高的选择性ꎬ由于其坐标比二维的平面图多一个ꎬ故可用于多组份混合物的分析[14].水杨酸的三维荧光光谱如图4所示ꎬ其激发波长有两个ꎬ分别为303nm和210nmꎬ对应的发射波长分别为405nm和398nmꎬ与二维荧光光谱所得信息一致.58吉林师范大学学报(自然科学版)第41卷图4㊀水杨酸的三维图Fig.4㊀Three ̄dimensionaldiagramofsalicylicacid2.4㊀酸度的影响实验考虑了溶液酸度对水杨酸的影响.图5为15种不同pH条件下的水杨酸溶液的荧光变化趋势ꎬ每组数据平行测定三组.图中可以看出酸性越强水杨酸的荧光强度越弱ꎬ碱性越强荧光强度越强ꎬ但显碱性的溶液中出现了白色絮状物ꎬ证明其性质有所改变ꎬ因此实验选择在中性条件下进行测定.图5㊀不同pH下水杨酸的荧光强度Fig.5㊀FluorescenceintensityofsalicylicacidatdifferentpHvalues代表性酸度条件下(分别为pH=2.3㊁pH=7.0㊁pH=13.0)水杨酸的三维荧光光谱图如图6所示.㊀68第2期孙艳涛ꎬ等:光法测定水杨酸片中水杨酸的含量(A)pH=2.3㊁(B)pH=7.0㊁(C)pH=13.0图6㊀代表性酸度条件下水杨酸的三维荧光光谱图Fig.6㊀Three ̄dimensionalfluorescencespectrographofsalicylicacidunderrepresentativeacidityconditions2.5㊀稳定性的影响以甲醇作水杨酸的溶剂ꎬ在密封㊁避光㊁干燥条件下保存ꎬ考察其48h内的稳定性ꎬ从图7可看出水杨酸在48h内的稳定性良好.图7㊀水杨酸的稳定性Fig.7㊀Stabilityofsalicylicacid2.6㊀标准曲线从水杨酸的标准曲线(如图8)得知ꎬ在(0.387~1.935)ˑ10-8mol L-1的浓度范围内ꎬ水杨酸浓度与其强度呈良好的线性关系ꎬ线性方程为y=386.61x-33.553ꎬ相关系数R2=0.9912.图8㊀水杨酸的标准曲线Fig.8㊀Standardcurveofsalicylicacid2.7㊀含量测定将水杨酸片的荧光强度带入标准曲线方程ꎬ经计算可求出水杨酸片中水杨酸的含量是1.636ˑ10-8mol L-1.7888吉林师范大学学报(自然科学版)第41卷3㊀结㊀论本实验采用甲醇作为水杨酸的溶剂ꎬ对溶液的酸碱性㊁稳定性及其线性范围等条件进行考察.水杨酸在(0.387~1.935)ˑ10-8mol L-1范围内具有良好的线性关系ꎬ利用荧光法测定水杨酸片中水杨酸的含量为1.636ˑ10-8mol L-1.参㊀考㊀文㊀献[1]李本淳ꎬ王丹.HPLC法测定复方水杨酸苯甲酸搽剂中水杨酸和苯甲酸的含量[J].中国药物评价ꎬ2017ꎬ34(4):255 ̄257. [2]韩迎春ꎬ赵丽华ꎬ龚时琼ꎬ等.荧光测定阿司匹林肠溶片中水杨酸实验的绿色化[J].实验室科学ꎬ2018ꎬ21(4):4 ̄7.[3]马延.经久不衰的阿司匹林[J].生命世界ꎬ2013(2):84 ̄93.[4]邓雅晨ꎬ梁建英.复方乙酰水杨酸片含量测定学生实验方法的改进[J].教育教学论坛ꎬ2013(34):266 ̄268.[5]李彩兰.尼美舒利的临床应用与进展[J].医学信息(中旬刊)ꎬ2010ꎬ5(6):1531 ̄1532.[6]JANDAMꎬRUELLANDE.Magicalmysterytour:Salicylicacidsignalling[J].EnvironmentalandExperimentalBotanyꎬ2015ꎬ117 ̄128. [7]李蕾ꎬ陈江敏.荧光分光光度法测定阿司匹林中游离水杨酸 PEG1500 ̄OP ̄(NH4)2SO4 ̄H2O双水相体系萃取分离[J].理化检验(化学分册)ꎬ2008(1):58 ̄60.[8]贝琦华ꎬ李祎ꎬ刘逸韬ꎬ等.电位滴定法测定尼美舒利含量能力验证结果分析[J].中国药事ꎬ2019ꎬ33(3):290 ̄294.[9]王慧.紫外 ̄可见分光光度法测定复方苯甲酸软膏中水杨酸的含量[J].北方药学ꎬ2014ꎬ11(1):10 ̄10.[10]高从ꎬ杨宁ꎬ黄力.库仑滴定法测定水杨酸醇溶液中水杨酸的含量[J].中国医院药学杂志ꎬ2014ꎬ34(6):494 ̄496.[11]SUNLJꎬPANZQꎬXIEJꎬetal.ElectrocatalyticactivityofsalicylicacidonAu@Fe3O4nanocompositesmodifiedelectrodeanditsdetectionintomatoleavesinfectedwithBotrytiscinerea[J].JournalofElectroanalyticalChemistryꎬ2013:127 ̄132.[12]段沅杏ꎬ贺兵ꎬ李干鹏ꎬ等.食品中正二氢愈疮酸含量的高效液相色谱荧光法测定[J].云南化工ꎬ2011ꎬ38(1):42 ̄47.[13]王堃ꎬ陈瑾ꎬ赵春晓ꎬ等.荧光分光光度法测定斯达舒中铝的含量[J].中国民族民间医药ꎬ2018ꎬ27(8):34 ̄36.[14]孙艳涛ꎬ王丽秋ꎬ赵磊ꎬ等.甘草次酸的荧光光谱研究[J].时珍国医国药ꎬ2013ꎬ24(3):621 ̄622.[15]于晓娟.微囊藻抑制 AgBiO3应急处置与酵母菌生态抑制法的研究[D].上海:上海交通大学ꎬ2011.DeterminationofsalicylicacidinsalicylicacidtabletsbyfluorescencespectrometrySUNYan ̄tao1ꎬLIMei ̄xi1ꎬLIUShi ̄cong1ꎬLILin1ꎬLIUYang2(1.CollegeofChemistryꎬJilinNormalUniversityꎬSiping136000ꎬChinaꎻ2.CollegeofPhysicsꎬJilinNormalUniversityꎬSiping136000ꎬChina)Abstract:Useingfluorescencespectrometrytodeterminationthesalicylicacidinsalicylicacidtablets.Usingmethanolasasolventforsalicylicacid.Theacidalkalinitystabilityandlinearrangeofsolutionwereinvestigated.Salicylicacidhasagoodlinearrelationshipintherangeof(0.387~1.935)ˑ10-8mol L-1.Determinationofsalicylicacidinsalicylicacidtabletsbyfluorescencewas1.636ˑ10-8mol L-1.Studentshavemasteredtheroutinetreatmentmethodofdrugsampleandthebasicoperationoffluorescenceinstrumentthroughexperimentꎬfurtherunderstandingofthequalitativeandquantitativeprinciplesofdeepfluorescencespectrometry.Keywords:fluorescencemethodꎻsalicylicacidꎻdeterminationofcontent(责任编辑:林险峰)。
阿司匹林的合成

实验一阿司匹林(乙酰水杨酸)的合成一:阿司匹林的简介阿司匹林(Aspirin)化学名称叫乙酰水杨酸。
也叫乙酰基柳酸、醋柳酸。
纯品为白色针状或板状结晶,或为白色结晶性粉末,无臭微带酸味,密度1.35,熔点135~138℃,在干燥空气中稳定,遇潮会缓慢水解生成水杨酸和乙酸,微溶于水,在醇、乙醚和氯仿中溶解,在氢氧化钠和碳酸钠溶液中溶解并分解。
阿司匹林目前主要由水杨酸和醋酸酐经酰化反应制得,在世界医疗史上是一种老资格的药品。
植物含有水杨酸类物质是在长期的进化和自然选择过程中形成的,这类化学物质对植物而言是天然驱虫剂,用来抵御寻食的动物,以保存自身物种的存在和繁衍。
1835年卡尔·娄卫希(Karl Lowig)从绣线菊中提取出了纯的水杨酸;1838年意大利人拉菲尔·皮瑞阿(Raffaele Piria)在实验室里将从柳树皮中提取的水杨苷转化成水杨酸。
当时纯的水杨酸已经开始作止痛药使用,它的降热止痛抗炎疗效比水杨苷要好得多。
然而从天然植物中分离提取水杨酸耗时耗力成本亦高。
此外作为治病药物水杨酸的副作用很强,对胃刺激性大,会导致胃痛甚至出血,当时认为是水杨酸的酸性所致。
1853年法国化学家热拉尔最早用水杨酸和乙酸酐反应制得乙酰水杨酸,这就是后来大名鼎鼎的阿司匹林。
以后又有化学家在乙酰水杨酸的合成和分离提纯上有所改进,遗憾的是没有进行专利登记,也没有提出它在医疗上的使用前景。
但是热拉尔发明的方法却一直沿用到了今天。
二、合成原理及方法目前主要用水杨酸和乙酸酐或乙酰氯在硫酸催化下经酰化制备阿司匹林,硫酸催化法虽然是经典方法,工艺成熟,但是产品收率不高,一般在65%~67%,副反应多,产品品质不好,设备腐蚀严重,同时产生大量废液污染环境,合成方法如下:实验原理:水杨酸与乙酸酐在H+催化下反应生成乙酰水杨酸。
主要试剂:水杨酸,3 g 、乙酸酐,4.5 mL 、浓硫酸,数滴、饱和NaHCO 3水溶液、浓盐酸,5 mL阿斯匹林是由水杨酸(邻羟基苯甲酸)与醋酸酐进行酯化反应而得的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
用移液管分别准确移取浓度为7.5μg·mL-1 的SA溶液2、4、6、8、 l0mL至5只50mL容量瓶中,用 1%醋酸—氯仿溶液稀释至刻度,摇匀。 分别2019测/5/2量4 它们的荧光强度.
试剂:乙酰水杨酸,水杨酸,乙醇,阿司 匹林药片。
2019/5/24
实验步骤
1、ASA和SA贮备溶液的配制 (1)ASA贮备液的配制:称取0.4000g乙酰水杨酸溶于1%醋酸-氯仿溶 液中,用 1%醋酸—氯仿溶液定容于1000mL容量瓶中,摇匀,备用; (2)SA贮备液的配制:称取0.750g水杨酸溶于1%醋酸—氯仿溶液中, 用 1%醋酸—氯仿溶液定容于1000mL容量瓶中,摇匀,备用。 2、ASA和SA激发光谱和荧光光谱的绘制 将ASA和SA贮备液分别稀释100倍(分二次完成,每次稀释10倍)。用得 到的溶液分别扫描ASA和SA的激发光谱和荧光光谱曲线,并分别确定 它们的最大激发波长和最大发射波长。 3、标准曲线的制作 (1) ASA标准曲线的制作
If = 2.3 I0 l c = Kc
分子产生荧光必须具备的条件
1)具有合适的结构; 2)具有一定的荧光量子产率。
荧光量子产率():
发射的光量子数
吸收的光量子数
荧光量子产率与激发态能量释放各过程的速率常数有关 ,如外转换过程速度快,不出现荧光发射;
2019/5/24
仪器结构流程
长;
l
‘ 2
>
l
2
>
l
1
;
磷光发射:电子由第一激发三重态的最低振动能级→基态(
T1 → S0跃迁); 电子由S0进入T1的可能过程:( S0 → T1禁阻跃迁)
S0 →激发→振动弛豫→内转移→系间跨越→振动弛豫→ T1 发光速度很慢: 10-3~10 s 。
光照停止后,可持续一段时间。
2019/5/24
数据处理
1、从绘制的ASA和SA激发光谱和荧光光谱曲线上,确定 它们的最大激发波长和最大发射波长。 2、分别绘制ASA和SA的标准曲线,从标准曲线上确定试 样溶液中ASA和SA的浓度,并计算每片阿斯匹林药片中 ASA和SA的含量(mg),将ASA测定值与说明书上的值比 较。 2019/5/24
实验指导
振动弛豫 内转换
S2
系间跨越
S1
能
T1 T2
量
吸 收
发
射
外转换
荧
光
发 射 磷 振动弛豫 光
S0
l3
l 1 2019/5/24
l 2 l 2
辐射能量传递过程
荧光发射:电子由第一激发单重态的最低振动能级→基态(
多为 S1→ S0跃迁),发射波长为 l ‘2的荧光; 10-7~10 -9 s 。
由图可见,发射荧光的能量比分子吸收的能量小,波长
荧光法测定乙酰水杨酸和水杨 酸
实验化学3-2 (仪器分析实验)
2019/5/24
1、实验目的 (1)掌握荧光法测定药物中乙酰水杨酸
的方法 (2)了解Cary Eclipse型荧光光谱仪的
基本操作 (3)强化称量、移液、配溶液等基本操
作
2019/5/24
实验原理
电子处于激发态是不稳定状态,返回基态时,通过辐射 跃迁(发光)和无辐射跃迁等方式失去能量;
1、溶剂用量控制在600mL,要求提高清洗效率, 减少移取溶剂时的损失,以节约试剂,同时保 护健康和环境。
2、用加长的胶头滴管移取少量的试剂,切忌直 接倾倒。
3、容量瓶使用25mL,注意相应液体体积的改动 4、要保证实验过程无水 5、在做标准曲线时,在做每一个点前,一定要
用这个点的溶液清洗比色皿至少三次,以保证 能作出曲线。
测量荧光的仪器主要由四个部分组成:激发光源、样品 池、双单色器系统、检测器。
特殊点:有两个单色器,光源与检测器通常成直角。 基本流程如图: 单色器:选择激发光波长 的第一单色器和选择发射 光(测量)波长的第二单色 器; 光源:灯和高压汞灯,染 料激光器(可见与紫外区) 检测器:光电倍增管。
2019/5/24
4、阿斯匹林药片中乙酰水杨酸和水杨酸的测定 取5片阿司匹林药片磨成粉末,准确称取0.40mg用1%醋
酸—氯仿溶液溶解,全部转移至100mL容量瓶中,用1%醋 酸—氯仿溶液稀释至刻度。迅速通过定量滤纸干过滤,用 该滤液在与标准溶液同样的测定条件下测量SA荧光强度。
将上述滤液稀释1000倍(用三次稀释来完成),在与标准溶 液同样的测定条件下测量ASA荧光强度。
6、比色皿的检测面和放入检测腔的位置一定要 固定。
2019/光光度法高2~4个数量级;为什么? 检测下限:0.1~0.1g/cm-3 相对灵敏度:0.05mol/L 奎宁硫酸氢盐的硫酸溶液。
2)选择性强 既可依据特征发射光谱,又可根据特征吸收光谱;
3)试样量少 缺点:应用范围小。
2019/5/24
仪器与试剂
仪器:Cary Eclipse荧光光谱仪,石英比 色皿,容量瓶,移液管,玻璃注射器, 漏斗,量筒,滤纸。
传递途径
辐射跃迁
无辐射跃迁
荧光 延迟荧光 磷光
系间跨越 内转移 外转移 振动弛预
激发态停留时间短、返回速度快的途径,发生的几率大, 发光强度相对大; 荧光:10-7~10 -9 s,第一激发单重态的最低振动能级→基态; 磷光20:19/51/240-3~10s;第一激发三重态的最低振动能级→基态;
内转换
溶液浓度与荧光强度的关系
有线性关系:
荧光强度 If正比于吸收的光量Ia和荧光量子效率 : If = Ia
由朗-比耳定律: Ia = I0(1-10- l c ) If = I0(1-10- l c ) = I0(1-e-2.3
lc)
浓度很低时,将括号项近似处理后:
2019/5/24
