浙江化学学考27题无机框图推断汇编
高三化学无机框图推断专题

高三化学无机框图推断专题文件编码(TTU-UITID-GGBKT-POIU-WUUI-0089)高三化学无机框图推断专题第1题:第2题:无色晶体A与黑色固体B可发生如下图所示的反应,除图中所示物质及反应条件外,其余反应物或生成物及反应条件均已略去。
其中D、L为固态单质,C、H为气态单质。
J的焰色反应为紫色。
第3题:如下图示:A、E、H是白色固体,且H不溶于水;G是一种微溶于水的白色固体;B、D、F是无色气体,且B能使湿润的红色石蕊试纸变蓝;C在常温下呈液态。
第4题:甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,它们之间存在如下转化关系:A与丙反应时,若A过量,则生成C和乙;若丙过量,则生成B和乙。
已知乙是双原子分子中键能最大的分子,C 为固体。
(1)写出下列物质的化学式:甲.__________,丙.__________,C.__________。
(2)写出A过量时丙与A反应的化学方程式:____________________。
(3)向C的溶液中加入镁粉有甲生成,其原因是____________________。
第5题:甲、乙、丙是三种常见的单质,X、Y、Z是三种常见的化合物,它们在一定条件下的相互转化关系如右图所示:请填写以下空白:(1)在X、Y、Z三种化合物中肯定含有乙、丙两种元素的化合物是___________。
(2)当X为两种非金属元素组成的化合物时,写出X跟甲反应的化学反应方程式:________________,丙跟乙反应的化学反应方程式:___________。
(3)当X为金属元素与非金属元素组成的化合物时,写出X跟甲反应的离子方程式。
第6题:下图的转化关系的每一方框表示有关的反应物或生成物,其中A是由短周期元素组成的化合物。
第7题:图中的每一个子母表示一种物质或者同种物质不同浓度的溶液。
已知D 是一种盐,焰色反应呈浅紫色,E 、F 常温下是气体。
A B C DEFG AB C H催化①②第8题:根据图2-2-1关系,确C DO 2定A 、B 、C 、D 、E 、F 的化学式第9题:根据图2-2-2,指出A 、B 、C 、D 、E 各是什么物质第10题:A 、B 、C 、D 分别是NaNO 3、NaOH 、HNO 3、Ba(NO 3)2中的一种。
高中化学学测真题分类汇编(无机框图推断)

18-20学测真题分类训练十九、无机框图1.(6分)下图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如下转化关系。
(反应中生成的水已略去)请回答以下问题:(1)E是_____________,F是_____________,H是_____________。
(填化学式)(2)C物质在日常生活中可作_____________________剂。
(3)写出反应①的化学方程式:_______________________________________2.(6分)下图是由短周期元素组成的一些单质及其化合物之间的转化关系图。
常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D 中燃烧生成的淡黄色固体。
(反应中生成的部分物质已略去)请回答下列问题:(1)物质A的化学式为_____ _____。
(2)化合物B的电子式为____ ______。
(3)反应①的离子方程式为_______ ______ ________ ______ ________ _____;反应②的化学方程式为____ ________ ________ ________ ________ ____。
3.下图是一些常见的单质.化合物之间的转化关系图,有些反应中的部分物质被略去。
常温常压下,A 为无色有毒气体,B 为红棕色粉末,C 、E 为金属单质。
反应①②均为工业上的重要反应。
请回答下列问题:(1)D 的电子式为_______________。
(2)K 的化学式为_______________。
(3)写出B 与C 高温反应生成E 和F 的化学方程式:________________________________。
(4)写出D 与J 的稀溶液反应生成G 的离子方程式:________________________________。
4.在下图所示的物质转化关系中,A 是常见的气态氢化物,B 是能使带火星的木条复燃的无色无味气体,E 的相对分子质量比D 大17,G 是一种紫红色金属单质。
浙江化学学考历年真题分类汇编(无机推断题)

浙江化学学考历年真题分类汇编(无机推断题)16.4.27.(6分)下图中,固体A是铁锈的主要成分。
请回答:(1)白色沉淀E的化学式(2)写出A的化学方程式(3)写出C在溶液中发生氧化还原反应的离子方程式15.7.34(4分)某混合物X由A12O3、Fe2O3和Cu组成。
进行如下实验:步骤I:取5.56 g混合物X,加入过量NaOH溶液,充分反应后,经过滤、洗涤、干燥,称量得3.52 g固体Y。
步骤Ⅱ:向3.52 g固体Y中加入过量稀硫酸,充分反应,形成蓝色溶液,不溶物经过滤、洗涤、干燥,称量得1.28 g固体Z。
请回答下列问题:▲。
(1)固体Z的成分是________▲。
(2)混合物X中n(A12O3):n(Fe2O3):n(Cu)=________15.1.33.(4分)向炭粉、Cu和Fe2O3组成的混合粉末中加入一定量的稀硫酸,充分反应后过滤,得到溶液A,将沉淀物洗涤、干燥,得到固体B。
(1)溶液A中一定存在的金属阳离子是_______________________。
(2)关于固体B的成分,下列选项中可能的有_______________________。
A.炭粉 B.炭粉和Cu C.炭粉和Fe2O3 D.Cu和Fe2O3 E.炭粉、Cu和Fe2O314.7.33.[4分]将有Mg、Al、Cu组成的粉末状混合物按下图所示进行实验。
根据实验流程回答下列问题:(1)固体C是________________。
(2)溶液D中溶质是____________________。
参考答案:16.4.15.7.34 ⑴Cu(或铜) ⑵2︰1︰315.1.33(1)Fe2+、Cu2+ (2)ABCE14.7.33(1)Cu (2)NaAlO2、NaCl、NaOH。
第27题有机推断-2023年7月浙江省普通高中学业水平考试化学分题(原卷版)
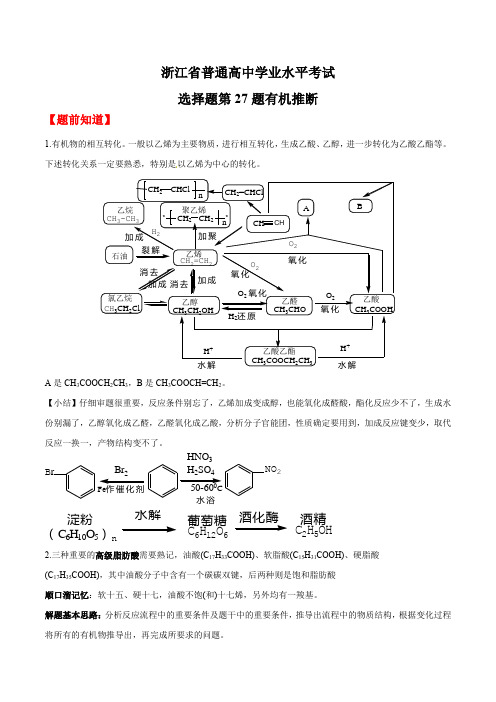
浙江省普通高中学业水平考试 选择题第27题有机推断【题前知道】1.有机物的相互转化。
一般以乙烯为主要物质,进行相互转化,生成乙酸、乙醇,进一步转化为乙酸乙酯等。
下述转化关系一定要熟悉,特别是以乙烯为中心的转化。
A 是CH 3COOCH 2CH 3,B 是CH 3COOCH=CH 2。
【小结】仔细审题很重要,反应条件别忘了,乙烯加成变成醇,也能氧化成醛酸,酯化反应少不了,生成水份别漏了,乙醇氧化成乙醛,乙醛氧化成乙酸,分析分子官能团,性质确定要用到,加成反应键变少,取代反应一换一,产物结构变不了。
2.三种重要的高级脂肪酸需要熟记,油酸(C 17H 33COOH)、软脂酸(C 15H 31COOH)、硬脂酸 (C 17H 35COOH),其中油酸分子中含有一个碳碳双键,后两种则是饱和脂肪酸 顺口溜记忆:软十五、硬十七,油酸不饱(和)十七烯,另外均有一羧基。
解题基本思路:分析反应流程中的重要条件及题干中的重要条件,推导出流程中的物质结构,根据变化过程将所有的有机物推导出,再完成所要求的问题。
NO 2B rHNO 3H SO 水浴Br 淀粉(C 6H 10O 5)n水解葡萄糖C 6H 12O 6酒精C 2H 5OH【真题回顾】1.(2022年7月浙江学考)土豆丝放入水中浸泡,水变浑浊并产生白色沉淀,其主要成分是有机物A,A 遇碘会变蓝。
以A为原料获得有机物E的转化关系如下图,已知E是有香味的无色油状液体。
请回答:(1)有机物A的名称是_______。
(2)有机物B的分子式是_______。
(3)有机物C与D反应生成E的化学方程式是_______。
(4)下列说法正确的是_______。
A. 仅用Na2CO3溶液无法鉴别有机物C、D和EB. 有机物A的分子式为C6H10O5C. 有机物B能发生银镜反应D. 工业上可以利用乙烯与水的加成反应制取有机物C2.(2021年7月浙江学考)烃A的相对分子质量为28,B是一种高分子化合物。
浙江学考第27无机推断【学考专练】

特训2第27题元素及化合物应用题专练领悟学考真题1.(2016·浙江10月选考,27)为探究不溶性盐X(仅含四种元素)的组成和性质,设计并完成如下实验:请回答:(1)X 的组成元素为H 、O 和__________(用元素符号表示),化学式为______________________。
(2)写出经一步反应能得到X 的化学方程式(要求非氧化还原反应)_______________________。
2.为探究黑色固体X(仅含两种元素)的组成和性质,设计并完成如下实验:隔绝空气高温稀硫酸稀NaOH 溶液加热固体甲(28.8g )溶液固体乙(12.8g )沉淀固体(16.0g )(蓝色)(蓝色)(黑色)(紫红色)气体(能使带火星木条复X (32.0g )第2题图(1)X 的化学式是________。
(2)固体甲与稀硫酸反应的离子方程式是________。
(3)加热条件下氨气被固体X 氧化成一种气体单质,写出该反应的化学方程式______。
仿真模拟集训1(北仑中学模考).K 2EO 4(E 代表某种元素)在工业上有重要的应用,以下是制备该物质的工艺流程图:已知:A 和C 是由同一主族元素组成的化合物,x 是工业上制D 的重要原料。
(1)x 的化学式是▲。
(2)写出F→G 的离子反应方程式▲。
(3)要工业上实现B→E 的转化,y 的化学式可能是▲。
2(衢州二模).X 常温下是一种无色液体,极易水解,遇潮湿空气会产生白雾。
实验室制备X 可用A 、C 两种气体发生化合反应制得,物质转化过程如下:为探究X的组成,取13.5gX与足量水完全反应,在生成物中加入1.0mol/L的NaOH溶液40.0mL恰好显中性。
继续加入过量BaCl2溶液,产生沉淀2.33g。
(1)由Na2SO3和B反应生成C的离子方程式(2)X的分子式是。
在生成X的反应中,C表现了性。
3(嘉兴一中模考).利用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2等)制备铁红,大致生产过程如下:请回答:⑴检验滤液A中含有Fe2+的方法是。
选考无机推断化学第27题

1.(6分)为了探究不溶性盐X(仅含5种元素)的组成和性质,设计并完成如下实验(所加试剂均过量,气体体积均在标准状况下测定)。
请回答:(1)X的组成元素为H、O和(用元素符号表示),气体C的电子式为。
(2)写出反应①的离子方程式:。
2.(6分)已知A、B、C是金属单质,甲、乙、丙为常见气体,其中B是地壳中含量居第二位的金属元素。
它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:(1)写出下列物质的化学式:B__________________,气体丙________________。
(2)写出反应④的化学方程式:______________,写出反应⑥的化学方程式:________________________________________________________________________。
3.(6分)(2017·浙江省五校高三上学期第一次联考)铁橄榄石是天然的铁矿石,由实验测得铁橄榄石的摩尔质量为204 g·mol-1,其中铁元素的质量分数为54.9%,可以通过如下反应和相应的数据推知它的化学式。
其中A~J是中学化学中的常见物质,G是一种红褐色固体,D是一种难溶于水的含氧酸,J是一种主要的温室气体,A为强碱,其焰色反应呈黄色,E和B分别与酸化的硝酸银溶液反应时的实验现象相同,均有白色沉淀产生,流程中的部分生成物已略去。
回答下列问题:(1)A的电子式:________________。
(2)铁橄榄石的化学式:_______________________________________________________。
(3)写出H → G的化学方程式:______________________________________________4.(6分)已知甲、乙、丙为常见单质,A、B、C、D、E、F、G、X均为常见的化合物;B和X的摩尔质量相同,E 的相对分子质量比D的相对分子质量大16。
浙江高三模拟试题汇编《无机框图推断》doc

2009浙江高三模拟试题汇编《无机框图推断》安徽省萧县一中李洪波2352001.(2008年杭州学军中学高考模拟测试5月)A 、B 、C 、D 为中学化学常见的物质,其组成元素均为主族元素。
它们间的反应关系如下图所示。
(1)若A 是可溶性强碱,B 是正盐,D 不溶于稀硝酸,则A 与B 共热的化学方程式为。
(2)若A 是碳化钙(CaC 2),B 是一种盐,A 与B 的溶液反应时只生成气体C 、CaCO 3和水;则B 的化学式为 ;C 分子是 分子(填“极性”或“非极性”),所含共价键的类型为 ___________。
(3)若B 是正盐,D 既可溶于盐酸又可溶于NaOH 溶液,A 的相对分子质量与D 相同。
向一定量的B 溶液中逐渐加入固体粉末A ,当 A 与B 以物质的量之比3∶1反应时,生成的D 的量最多。
则A 的化学式为 , B 的化学式为 。
答案 (1)Ba (OH )2 + (NH 4)2SO 4 === BaSO 4↓+2NH 3↑+ 2H 2O[ 3分,写(NH 4)2SO 3也可,BaSO 4沉淀符合可以不写](2)Ca (HCO 3)2 (3分);非极性(2分);极性键和非极性键(3分,只写一个得1分)(3)Na 2O 2 Al 2(SO 4)3 (各2分)2. (2008年温州市高三4月适应性测试)已知无水盐D 是常见的中性干燥剂,常温下E 为无色无味的液体,F 为淡黄色粉末,G 为常见的气体单质。
从A ~H 的所有物质之间存在如下的转化关系(反应条件均已省略)。
请回答下列问题:(1)写出物质G 化学式 ;在反应② 中.当去39g F 参加反应时,转移电子的物质的量为 mol .(2)若C 是能使澄清石灰水变浑浊的无色无味气体,写出反应① 的离子方程式 。
(3)若C 是能使湿润的红色石蕊试纸变蓝的气体,写出反应① 的化学力程式 。
(4)若C 是一种常见漂自剂的有效成分,写出反应① 的化学方程式 。
浙江省理综27题无机推断题目专题训练

理综化学27题专题训练(一)(二)(三)(四)(五)(六)(七)(八)27.某含氯化合物A由两种短周期元素组成,常温下该物质为气态,测得该气体对空气的相对密度为3.0,A溶于水可得只含单一溶质B的弱酸性溶液,B溶液在放置过程中其酸性会增强.常温下,气体A与NH3反应生成离子晶体C、气体单质D和常见液体E,D为空气中含量最多的物质。
气体A可用某一气体单质与潮湿的Na2CO3反应制得,同时生成两种钠盐。
请回答下列问题:(1)气体A的化学式为,气体单质D对应元素在周期表中的位置为。
(2)写出A溶于水生成弱酸B的化学方程式。
(3)气体A与NH3反应的化学方程式为,该反应体现气体A具有性。
(4)试写出制取气体A的化学方程式为。
(5)设计实验探究离子晶体C的成分为。
(九)27.(18分)I.A、B、C、D、E、F 是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分反应条件略去):(1)若所有转化都是非氧化还原反应,B、D、E含有同种金属元素,F为强碱(部分产物略去)则A+B→C+D的离子反应式为▲,C为同周期元素构成的1:1第27题图型化合物,则C的电子式为▲。
(2)若A、D、F 为单质,B、C、E为化合物,B为两种非金属元素所组成的化合物,则E的化学式为▲,A + B→C+D的化学方程式为▲。
II.甲、乙都是二元固体化合物,将32g的粉末加入足量浓硝酸并加热,完全溶解得蓝色溶液,向该溶液中加入足量Ba(NO3)2溶液,过滤、洗涤、干燥得沉淀46.6g;滤液中再滴加NaOH溶液,又出现蓝色沉淀。
含乙的矿石自然界中储量较多,称取一定量的乙,加入稀盐酸使其完全溶解,溶液分为A、B两等分,向A中加入足量NaOH溶液,过滤、洗涤、灼烧得到红棕色固体28g,经分析乙与红棕色固体组成元素相同,向B中加入8.0g铜粉充分反应后过滤、洗涤、干燥得固体1.6g。
(1)写出构成甲的阴离子的结构示意图▲,32g甲在足量浓硝酸中反应转移的电子数为▲。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
浙江化学学考27题无机框图推断汇编
work Information Technology Company.2020YEAR
无机推断
1、磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
请回答:
(1)A的组成元素为_________(用元素符号表示),化学式为______。
(2)溶液C可溶解铜片,例举该反应的一个实际应用____________。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为
1.518 g·L-1),该气体的电子式为_ __ _。
写出该反应的离子方程式_ _
__ __ __ _ __。
(4)写出F→G反应的化学方程式__________ _____。
2、电镀工业中往往产生大量的有毒废水,必须经过严格处理后才可以排放.某种含A离子(阴离子)废水在排放前的处理过程如下:
已知:9.0g沉淀D在氧气中灼烧后,产生8.0g黑色固体,生成的气体通过足量澄清石灰水时,产生10.0g白色沉淀,最后得到的混合气体除去氧气后,还剩余标况下密度为1.25g•L﹣1的气体E 1.12L.
(1)E的结构式
(2)沉淀D的化学式
(3)写出沉淀D在氧气中灼烧发生的化学方程式
(4)滤液C中还含有微量的A离子,通过反应②,可将其转化为对环境无害的物质,试用离子方程式表示该原理
(5)反应①为制得某种元素的低价X离子,试从氧化还原反应的角度分析,是否可以用Na2SO3溶液来代替B溶液,说明理由.
3、为探究不溶性盐X(仅含四种元素)的组成和性质,设计并完成如下实验:
已知,各步反应所需试剂均过量,请回答:
(1)X的化学式为。
(2)写出X与稀硫酸反应的离子方程式。
(3)红色固体B的硫酸盐溶液与纯碱溶液反应能得到X,该反应的化学方程式为。
4、为探究固体A的组成和性质,设计实验并完成如下转化。
已知:X由两种化合物组成,若将X通入品红溶液,溶液褪色。
若将X通入足量双氧水中,X可全部被吸收且只得到一种强酸,再稀释到1000mL,测得溶液的PH=1。
在溶液2中滴加KSCN溶液,溶液呈血红色。
请回答:
(1)固体A的化学式。
(2)写出反应①的化学方程式。
(3)写出反应④中生成A的离子方程式。
5、某研究小组为了探究一种无机矿物质X(仅含四种元素)的组成和性质,设计并完成如下实验:
另取10.80gX在惰性气流中加热至完全分解,得到6.40g固体1.请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图_______,
(2)X的化学式是______,在惰性气流中加热X至完全分解的化学反应方程式为
________________________。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是__________________________(用化学反应方程式表示)。
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式_________________________________________,并设计实验方案验证该反应的产物_______。
6、某含氧物质X仅含三种元素,在198℃以下比较稳定,温度高时易分解.,某研究小组设计并完成如下实验:
试回答如下问题:
(1)X的化学式为______________,写出X与H2O反应的离子方程式
_______________________________
(2)工业上由红棕色固体2可以制备其单质,写出化学方程式
______________________________________
(3)保存X时应注意______________________,写出X在实际生活中的一种应用
______________________
7、X常温下是一种无色液体,极易水解,遇潮湿空气会产生白雾。
实验室制备X可用A、C两种气体发生化
合反应制得,物质转化过程如下:
为探究X的组成,取13.5gX与足量水完全反应,在生成物中加入1.0mol/L的NaOH溶液40.0mL恰好显中性。
继续加入过量BaCl2溶液,产生沉淀2.33g。
请回答:
(1)由Na2SO3和B反应生成C的离子方程式
(2)X的分子式是。
在生成X的反应中,C表现了性。
8、为探究含结晶水的化合物X(含四种元素,摩尔质量为180 g·mol-1)的组成和性质,某兴趣小组设计并
完成如下实验:
请回答:
(1)黑色固体Y的化学式为________,气体C的电子式为________________。
(2)晶体X隔绝空气受热分解的化学方程式为__________________。
9、为了确定黄钾铁矾的化学式[KFe3(SO4)x(OH)y],某兴趣小组设计了如下实验:
请回答:
(1)黄钾铁矾的化学式中x=________,y=________。
(2)写出溶液B中所含溶质的化学式________。
(3)红褐色沉淀能溶于HI溶液,并发生氧化还原反应,写出该反应的离子方程式________。
10、由两种元素组成的矿物A,测定A的组成及制取化合物D的流程如下:
请回答:
(1)A的化学式为_________________。
(2)写出②的化学方程式:_________________。
(3)写出③的离子方程式:_________________。
11、磁性材料A由两种元素组成,为探究其组成和性质,设计并完成如下实验:
(1) A的化学式为_______________________;
(2) 固体氧化物B的颜色;
(3) 用离子方程式表达气体C与氯水反应生成D的过程_____________________________。
12、凤凰石是一种用于建材装饰的硅酸盐矿物,已知某地出产的凤凰石可看作由主要成分硅酸铜盐X·3H2O(摩尔质量=334g/mol)与含氧酸盐杂质Y共同组成,X、Y均含三种元素,工业上利用下列流程制备铜盐,在溶液Ⅱ中滴入KSCN溶液显血红色。
请回答:
(1)杂质Y中除氧以外还含有的元素为(填元素符号),x的化学式为。
(2)如果王溶液Ⅱ中继续加入H2O2,发现有气泡产生,有观点认为是Y中的某元素离子将H2O2氧化所导致,写出反应的离子方程式。
