紫外分光光度计法测定果蔬中维生素C的含量
紫外分光光度计法测定果蔬中维生素c的含量

紫外分光光度计法测定果蔬中维生素c的含量紫外分光光度计法是一种常用的测定果蔬中维生素C含量的方法。
维生素C具有强的紫外吸收性质,在265nm处有最大吸收峰。
通过测定样品溶液与标准溶液在相同条件下的吸光度,可以比较它们的维生素C含量。
以下是该方法的详细步骤:一、目的本实验的目的是通过紫外分光光度计法测定果蔬中维生素C的含量,了解其含量变化情况,为科学饮食提供参考。
二、原理维生素C具有强的紫外吸收性质,在265nm处有最大吸收峰。
在实验条件下,一定浓度的维生素C溶液与其吸光度呈线性关系。
通过比较样品溶液与标准溶液在相同条件下的吸光度,可以求出样品中维生素C的含量。
三、实验步骤1.标准曲线的制作(1)配制不同浓度的维生素C标准溶液。
分别称取0.05g、0.1g、0.2g、0.3g、0.4g的维生素C,用蒸馏水定容至100mL,得到浓度分别为5mg/mL、10mg/mL、20mg/mL、30mg/mL、40mg/mL的溶液。
(2)用1cm石英比色皿分别在紫外分光光度计上测定各标准溶液在265nm处的吸光度。
(3)以维生素C浓度为横坐标,吸光度为纵坐标绘制标准曲线。
2.样品处理(1)将果蔬样品洗净,晾干表面水分。
(2)将样品切成小块,放入榨汁机中榨汁,收集榨出的汁液。
(3)用纱布过滤,去除汁液中的杂质和果肉颗粒。
(4)将滤液倒入50mL容量瓶中,用蒸馏水定容至刻度线。
3.测定样品吸光度(1)用移液管准确移取5mL样品溶液于1cm石英比色皿中。
(2)在紫外分光光度计上测定样品溶液在265nm处的吸光度。
4.计算样品中维生素C的含量(1)从标准曲线上查得相应的维生素C浓度(mg/mL)。
(2)计算样品中维生素C的含量(mg/100g),公式如下:维生素C含量 = 查得浓度× 溶液体积× 稀释倍数 / 样品质量其中,溶液体积为50mL,稀释倍数为100(即5mL样品溶液稀释成50mL),样品质量为榨出的果蔬质量。
紫外分光光度法测定常见水果维生素C的含量

紫外分光光度法测定常见水果维生素C的含量1 序言1.1 研究的目的和意义维生素是必须得从食物中获取并且在物质代谢过程中起到了极其重要的作用的一种物质[1]。
这类物质在生物体内不能合成或者合成量特别少,不足以维持生物体的正常的生理功能,虽然生物体对维生素的需要量很少,但所需量必须经常从食物中获得,所以我们研究维生素具有重要的意义[2]。
维生素C是维生素的一种,维生素C在医学上被称作抗坏血酸,具有防治坏血病的功效,它是显示抗坏血酸生物活性的一类有机化合物的总称[3]。
维生素C广泛的存在于我们常见的水果和蔬菜中,所以我们能够准确地测定出水果中地维生素C的含量,对我们的日常饮食和健康的生活具有重要的指导意义。
1.2维生素C含量的研究史中国是人口众多的国家,人口密度相对较大,病毒发病率较高,我国在对抗病毒的战争中起到一个关键作用。
SARS病毒首先出现在我们中国,死于SARS 病毒的90%是我们中国人。
国内对于维生素C的生产水平已经处于领先地位,可以彻底解决病毒的问题,只是生产的维生素C大部分都外销,我们中国人服用维生素C的平均剂量,远远低于一些欧美国家和日本。
目前,围绕着维生素C 含量的测定产生了一系列的研究课题和任务,因为它对人们日常饮食具有重要指导意义,成为了现今国内外研究的热点,现在主要有2,4-二硝基苯肼比色法、碘量法、高效液相色谱法、紫外分光光度法等来测定维生素C的含量。
1.2.1碘量法武文等[4]利用I₂的氧化性,用淀粉作指示剂,采用I₂作标准溶液进行直接滴定,这叫做直接碘量法。
直接碘量法的滴定原理:维生素C分子中的二烯醇基可被I₂氧化成二酮基,当维生素C分子中的二烯醇基被I₂完全氧化后,过量的I₂与淀粉指示剂发生显色作用,使溶液变蓝,所以当滴定到溶液中有蓝色出现时,即为滴定终点。
直接碘量法测定水果和蔬菜中维生素C的含量时,要求所测的果蔬溶液为无色和浅色的是样溶液或者提取液,该方法测维生素C不需要特殊的测定仪器,操作非常简便、准确。
紫外光度法测定维生素C实验报告

紫外光度法测定维生素C实验报告Revised at 16:25 am on June 10, 2019紫外分光光度法测定维生素C片维生素C的含量一、实验目的1.学习利用紫外吸收光谱测定物质含量的原理和方法;2.熟练紫外-可见分光光度计的操作;二、实验原理维生素CVC是一种酸性己糖衍生物,具有烯醇式己糖内酯立体结构,分D和L两种立体构型,但只有L型有生理功效;维生素C具有较强的还原性,在一定条件下氧化型和还原型可以互变 ,两者均具有生物活性结构式见图1,其C2和C3位上两个相邻的烯醇式羟基极易解离而释放出H+,故维生素C虽然不含自由羧基,仍具有有机酸的性质;维生素C呈无色无臭的片状结晶体,易溶于水,不溶于脂;在酸性环境中稳定,遇空气中氧、热、光、碱性物质,特别是有氧化酶及痕量铜、铁等金属离子存在时可促进其破坏速度;具有π电子的共轭双键化合物、芳香烃化合物等,在紫外光谱区都有强烈吸收,其摩尔吸收系数k可达104-106数量级;利用紫外吸收光谱进行定量分析,要借助朗伯-比尔定律;根据维生素C在稀硫酸溶液维生素C水溶液在pH 5~ 6之间稳定中,在245 nm 波长处有最大吸收的特性,建立了紫外分光光度法测定维生素C片含量的方法;三、实验仪器及试剂实验仪器:容量瓶100 ml、1000 ml、移液管 ml、5 ml、烧杯、紫外分光光度计实验用品:98%浓硫酸分析纯,1.84 g/ml、维生素C对照品系以原料药经105 ℃干燥至恒重含量为 %、维生素C片2片、去离子水四、实验步骤1. 0.005 mol·L-1硫酸溶液的配制用 ml移液管移取 ml 98%浓硫酸放入事先已盛有蒸馏水的烧杯中,搅拌,冷却至室温后移入1000 ml容量瓶,稀释至刻度,待用;2. 0.5 g·L-1对照品溶液的配制精密称取105℃干燥至恒重的维生素C对照品50 mg置100 ml量瓶中,加 mol·L-1硫酸溶液制成0.5 g·L-1对照品溶液;3. 维生素C对照品标准溶液的配制用5 ml移液管精密量取0.5 g·L-1对照品溶液、、、、 ml,分别置100 ml量瓶中,用mol·L-1硫酸溶液稀释至刻度,摇匀,待用;4. 测定波长及标准曲线以 mol·L-1硫酸溶液为空白,测定维生素C在稀硫酸溶液中最大吸收波长,并在此波长处测定维生素C对照品标准溶液的吸光度,以浓度对吸光度作线性回归;5. 样品含量测定取维生素C片2片,精密称定,研细,精密称取适量0.06g,约相当于维生素C 50 mg置100 ml容量瓶中,加 mol·L-1硫酸溶液适量,超声5 min使溶解,再加 mol·L-1硫酸溶液至刻度,摇匀,滤过,弃去初滤液,精密量取续滤液 ml置100 ml量瓶中,加 mol·L-1硫酸溶液至刻度,摇匀,在最大吸收波长处测定吸光度;6.空白试验模拟维生素C片处方比例,精密称取辅料适量置100 ml量瓶中,与步骤5样品含量测定同法操作,在最大吸收波长处测定吸收度为0;7.回收率试验先测得2 ml样品溶液的吸光度A1C1,再取0.0125 g/L 的VC 标液200 μl,于2 ml 已测得吸光度A1的样品溶液中,再测得吸光度A2C2;五、实验数据记录及处理1.维生素的吸收波长在紫外可见分光光度计上扫描测定VC标准样品的吸收光谱,结果显示VC在244nm 波长处的吸光度值最大;2. 维生素C对照品标准曲线y = x - R=3.样品中维生素C含量测定4.回收率试验先测得2 ml样品溶液的吸光度A1C1,再取0.0125 g/L 的VC 标液200 μl,于2 ml 已测得吸光度A1的样品溶液中,再测得吸光度A2C2;六、实验结果及讨论1. 维生素C 还原性很强,在空气中易被氧化,在酸性介质中氧化作用减慢,水溶液在pH = 5~6 之间稳定,故本实验选用 mol·L-1硫酸溶液pH = 为溶剂,维生素C稳定性好;2. 标准曲线R=,且测定的未知样品的吸光度均落在标准曲线有效的范围内,实验结果表明,维生素C在-0.0125 gL范围内与吸光度呈良好的线性关系;3. 由于对加标回收率的原理及概念模糊,导致实验在这一环节消耗较多的时间;本实验测得维生素C的平均回收率为%,相对标准偏差为%;4. 利用紫外分光光度法测定维生素C片维生素C的含量,该法操作简便,快速,准确,所用试剂价格低廉、易得,适合维生素C 片剂含量测定的快速分析;。
紫外分光光度法测定猕猴桃中Vc含量

紫外分光光度法测定猕猴桃中维C含量实验报告书摘要利用维生素C对紫外产生吸收和对碱不稳定的特性,用紫外分光光度法测定猕猴桃中Vc含量,最大吸收波长为245nm,标准曲线方程为y=19.132x,相关系数R2=0.9968,一个猕猴桃中维生素C含量约为87毫克。
关键词:紫外分光光度法、猕猴桃、维C、含量1 前言维生素C又称抗坏血酸,是一种水溶性维生素。
能预防牙龈出血及萎缩,提高人体免疫力;对坏血病、动脉硬化、贫血等有一定疗效[1]。
维生素C的主要作用是提高免疫力,预防癌症、心脏病、中风,保护牙齿和牙龈等。
另外,坚持按时服用维生素C还可以使皮肤黑色素沉着减少,从而减少黑斑和雀斑,使皮肤白皙。
富含维生素C的食物有猕猴桃、青辣椒、橙子、葡萄汁、西红柿等,可以说,在所有的蔬菜、水果中,维生素c含量都不少。
美国专家认为,每人每天维生素C的最佳摄入量应为200-300毫克,最低不少于60毫克[2]。
2 实验目的猕猴桃是一种营养价值极高的水果,其可溶性固形物质含量为20%,含亮氨酸、苯丙氨酸、异亮氨酸、酪氨酸、缬氨酸、丙氨酸等十多种氨基酸,含有丰富的矿物质。
每100克果肉含钙27毫克,磷26毫克,铁1.2毫克,还含有胡萝卜素和多种维生素,其中维生素C的含量达100毫克,有的品种高达300毫克以上,是柑桔的5--10倍,苹果等水果的15--30倍,因而在世界上被誉为“水果之王”[3]。
常见的Vc的测定方法有2,6一二氯靛酚法、2,4一二硝基苯肼法、铅硫化氢法、碘量法以及荧光光度法…,近来也有报道利用分光光度法测定Vc含量。
本实验采用紫外分光光度法测定猕猴桃中Vc含量。
3 实验原理1.紫外吸收光谱是基于物质的生色团和助色团的特性对紫外光谱的吸收,可用于物质的鉴定和结构分析。
2.维C在紫外光区(200-400nm)显示特征的吸收谱带,最大光吸收(λmax)为245nm。
因此可以用标准曲线法在245nm测样品吸光度,测得维C含量。
紫外分光光度法测定水果或蔬菜中的维生素C含量

2. 标准曲线的
绘制
1
2
3
4
5
6
7
8
标准抗坏血酸溶液加入体
积/mL
0.1 0.2 0.3 0.4 0.5 0.6 0.8 1.0
9.9 9.8 9.7 9.6 9.5 9.4 9.2 9.0
总体积/mL
抗坏血酸溶液浓度 /(μg·mL-1)
10.0 10.0 10.0 10.0 10.0 10.0 10.0 10.0 1.0 2.0 3.0 4.0 5.0 6.0 8.0 10.0
3.消光值的测定:以蒸馏水为空白,在243 nm处 测定标准系列抗坏血酸溶液的消光值,以抗坏血酸的含 量(μg)为横坐标,以相应的消光值为纵坐标作标准 曲线。
(二)样品的测定
1.样品的提取:将果蔬样品洗净、擦 干、切碎、混匀。称取5.00 g于研体中, 加入2~5 mL 1% HCl,匀浆,转移到25 mL 容量瓶中,稀释至刻度。若提取液澄清透明, 则可直接取样测定,若有浑浊现象,可通过 离心(10000 g, 10 min)来消除。
样品液与碱处理样品液两者消光值之差,通过查标准
曲线,即可计算样品中维生素标准曲线的制作 1.抗坏血酸标准溶液的配制:用分析 天平准确称取抗坏血酸10 mg,加2 mL 10%盐酸,加蒸馏水定容至100 mL,混匀。 此抗坏血酸溶液的浓度为100 μg·mL-1。
93.4 计算
μ×V总
实验一-紫外分光光度法测定维生素C片中的VC含量

紫外分光光度法测定维生素一、实验目的1、了解紫外分光光度计的主要结构及工作原理。
C片中的VC含量2、掌握紫外分光光度计的操作方法及紫外定性定量分析方法3.掌握紫外分光光度法测定水中维生素C含量的原理与分析条件的选择。
二、实验原理维生素C是人体重要的维生素之一,它影响胶元蛋白的形成,参与人体多种氧化-还原反应,并且有解毒作用。
人体不能自身制造Vc,所以人体必须不断地从食物中摄入Vc,通常还需储藏能维持一个月左右的Vc。
缺乏时会产生坏血病,故又称抗坏血酸。
维生素C属水溶性维生素,分子式C6H8O6。
分子结构中具有二烯醇结构,其结构如下:它易溶于水,微溶于乙醇,不溶于氯仿或乙醚。
分子中的二烯醇基具极强的还原性,性质活泼,易被氧化为二酮基而成为脱氢抗坏血酸。
维生素C分子结构中有共轭双键,固在紫外光区有较强的吸收。
根据维生素C在稀盐酸溶液中,Vc吸收曲线比较稳定,在最大吸收波长处,其吸收值A的大小与维生素C的浓度c的大小成正比,符合郎伯—比尔定律:A=εbc其中A为吸收度;c为试样中维生素C的浓度,mol·L-1;b为吸收池厚度,cm;ε为摩尔吸收系数,L·mol-1·cm-1。
若在最大吸收波长下,首先绘制出维生素C在最大吸收波长下的标准曲线,然后在相同条件下测定出吸光度A,由测得的吸光度A在标准曲线上查得浓度,换算为药品中含量(mg/片)。
三、实验仪器与试剂1.仪器TU1810型紫外分光光度计。
电子天平1台,研钵1个,50mL容量瓶7只和500mL容量瓶1只,10mL移液管2支,100mL、1000mL烧杯2只。
2.试剂维生素C标准品(抗坏血酸),市售维生素C含片(100mg/片),冰醋酸,蒸馏水。
四、实验步骤1.配制维生素C标准贮备液500mL(浓度约为1.5×10-4mol/L):称取约0.0132g维生素C标准品于100mL的烧杯中,用超声波助溶后定容于500mL容量瓶中,摇匀,配成贮备液。
紫外分光光度法测定水果中维生素C的含量毕业论文

题 目:紫外分光光度法测定水果中维生素C 的含量的含量摘 要:目前研究维生素研究维生C 的测定方法的报道较多,如滴定法、光度分度法、高效液相色谱法等,特别是紫外分光度测定法。
本论文利用维生素C 具有对紫外产生吸收和对碱不稳定的特性有对紫外产生吸收和对碱不稳定的特性, , 建立了紫外分光光度快速测定水果维生素C 含量的新方法。
维生素C 浓度在1.001.00—12.0µg/mL 范围内与吸收值呈良—12.0µg/mL 范围内与吸收值呈良好的线性关系;检出限为0.014µg/ mL;加标回收率在97.9% —99.0% 之间。
该法操作简单法操作简单,,结果准确结果准确,,应用于维生素C 含量的测定含量的测定, ,结果令人满意。
关键词:维生素C ,紫外分光度测定法,水果前言维生素C 是可溶于水的无色结晶,是一种分子结构最简单的维生素。
维生素C 有防治坏血病的功能,所以在医药上常把它叫做抗坏血酸。
维生素C 能保能保持巯基酶的活性和谷胱甘肽的还原状态,还有解毒作用等。
其广泛存在于植物组织中,新鲜的水果、蔬菜,特别是枣、辣椒、苦瓜、柿子叶、猕猴桃、柑橘等食品中含量尤为丰富,品中含量尤为丰富,对饮食健康、对饮食健康、对饮食健康、医疗保健都具有十分重要意义。
医疗保健都具有十分重要意义。
医疗保健都具有十分重要意义。
近年来测定维近年来测定维生素C 的方法主要有滴定法、光度法、高效液相色谱法等。
的方法主要有滴定法、光度法、高效液相色谱法等。
1 维生素维生素C 的性质及测定方法的性质及测定方法1.1 维生素维生素C 概述概述维生素C 又叫抗坏血酸(又叫抗坏血酸(Ascorbicid Ascorbicid Ascorbicid),广泛存在于植物组织中,新鲜的水),广泛存在于植物组织中,新鲜的水果、蔬菜中含量较多,蔬菜中含量较多,是一种水可溶性小分子生物活性物质,是一种水可溶性小分子生物活性物质,是一种水可溶性小分子生物活性物质,也是人体需要量最也是人体需要量最大的一种维生素。
分光光度法测定蔬菜中维生素C的含量

仪器分析综合 实训(一) 项目二 分光光度法测定蔬菜中维生素C 的含量 报告 班级: 学号: 姓名: 实验日期:. 成绩:化学工程学院3分光光度法测定蔬菜中维生素C 的含量一、实验目的学习在紫外光谱区测定蔬菜中维生素C 二、实习原理三、仪器与试剂(1)仪器:紫外-可见分光光度计,石英吸收池一对,50mL 容量瓶 10只,1 000 mL 容量瓶2只,10 mL 吸量管2只。
(2)试剂:维生素C 。
四、实验步骤: (1)准备工作①清洗容量瓶等需要使用的玻璃仪器,晾干待用。
②检查仪器,开机预热20min ,并调试至正常工作状态。
(2)配置系列标准溶液(3)绘制吸收光谱曲线 以蒸馏水为参比,在220-320 nm 范围绘制维生素C 的吸收光谱曲线,并确定入射光波长max λ。
(4)绘制工作曲线 以蒸馏水为参比,在max λ测定维生素C 系列标准的各溶液的吸光度并记录测定结果和实验条件。
(5)试样的测定(6)结束工作①实验完毕,关闭电源。
取出吸收池,清洗晾干后入盒保存。
②清理工作台,罩上仪器防尘罩,填写仪器使用记录。
仪器分析综合 实训(一) 项目二 分光光度法测定蔬菜中维生素C 的含量 报告 班级: 学号: 姓名: 实验日期:. 成绩:化学工程学院4六、数据处理(1)绘制维生素C 的吸收曲线。
(2)计算蔬菜中V-C 的含量。
1133c 00.501000.50100010100.1005000.0----⋅=⋅⨯=⨯⨯=mL g L g μρ标液维 从A-ρ工作曲线上查得番茄,x ρ,则nx •=番茄,番茄汁ρρ (n 为稀释倍数)从A-ρ工作曲线上查得黄瓜,x ρ,则n x •=黄瓜,黄瓜汁ρρ (n 为稀释倍数)结论:仪器分析综合实训(一)项目二分光光度法测定蔬菜中维生素C的含量报告班级:学号:姓名:实验日期:. 成绩:化学工程学院5。
紫外分光光度法测定五种果蔬中维生素C的含量

关 键 词 : 外 分光 光 度 法 ; 生素 C 果 蔬 紫 维 ;
中图 分 类 号 : 5 . 2 Q 6 73 文 献标 识 码 : A 文 章 编 号 :62 52 ( 02 0 -0 9 -0 1 7 — 4 52 1) 8 02 3
维 生素 C又 称 抗 坏 血 酸 , 一 种水 溶 性 维 生 素 。 是 能预防牙 龈 出血及 萎缩 、 高 人 体免 疫 力 , 坏 血 病 、 提 对
溶 解 , 蒸 馏 水 定 容至 5 0mL, 匀 , 用 0 混 即得 1 0 g・ 0
mL 维 生素 C标 准溶液 。 1 2 2 吸收 曲线 的绘制 .. 移取 1 0mL维生素 C标 准 溶 液 于 5 0mL 比色 管 中, 稀释 至刻度 , 混匀 。用 1c 石英 比色皿 , m 以蒸馏 水 为参 比 , 2 0 0 m 波长 范 围内用 紫 外可 见分 光 在 0  ̄3 0F l 光度计 自动扫 描 。绘 制 吸光 度 与 波 长关 系 曲线 , 以最 大吸收 波长作 为测定 波长 。 1 2 3 标 准 曲线 的绘制 ..
1 实验
1 1 材 料 、 剂 与 仪 器 . 试
浓度为 横坐标 、 吸光 度为纵 坐标 , 制标 准曲线 。 绘
1 2 4 果 蔬 样 品 的 处 理 ..
将 青椒 、 西红柿 、 黄瓜洗 净 晾干 , 子和苹果 取 肉 , 橙 分别称 取 】 . 0g于研 钵 中 , 加入 1 HC 0mL 0O 各 1 , l
青椒、 子、 橙 黄瓜 、 苹果 、 红柿 , 西 市售 。
抗 坏血 酸 、 1Na HC 、 OH 均 为 分 析 纯 , 验用 水 为 实 二次蒸 馏水 。 UV1 0 1 2型 紫外 可见 分 光 光 度 计 , 海 天 美 科 学 上 仪器有 限公 司 ; B 2 4型 电子 天 平 , 京赛 多 利 斯 仪 T 一1 北
紫外分光光度法测定维生素C的含量

紫外分光光度法测定维生素C的含量维生素C(VitC)又名抗坏血酸,可降低毛细血管通透性,降低血脂,增强机体的抵抗能力,并有一定的解毒功能和抗组胺作用[1]。
临床主要用于坏血病、急慢性中毒、心肌炎、慢性肝炎等病症。
对于其含量测定,纵观各种质量标准均采用2,6-二氯吲哚酚滴定法等滴定分析法,该方法简便、快速、准确,中国药典(2000年版)也采用碘量法。
虽然不甚满意了。
由于维生素C易被空气中的氧所氧化,再加上制剂辅料对测定的干扰,测定前必须先做处理。
采用紫外分光光度法测定维生素C时,存在于维生素C或复合维生素制剂中的辅料一般不对测定产生干扰[2]。
所以本法既可以测定维生素C各种制剂及复合维生素片剂,也可以测定多种饮料中的维生素C的含量。
1 仪器与试剂UV-260紫外分光光度计,VitC对照品及VitC片(规格:50mg)均由河南某药厂提供,硫酸溶液(pH=6)。
2 实验操作2.1 标准曲线的绘制精密称取VitC对照品0.05g溶于100ml硫酸溶液,再稀释成一系列不同浓度的对照品溶液(0~14μg/ml),分别测出其吸光度。
然后以浓度为横坐标,以相应的吸光度为纵坐标绘制出标准曲线。
该曲线是经过原点的一条直线,可求出该曲线的斜率。
2.2 样品测定取VitC20片,精密称定,研细,精密称出适量(相当于VitC50mg),置于100ml量瓶中,加硫酸溶液溶解并稀释至刻度,滤过,精密量取续滤液2ml置于另一100ml量瓶中,加硫酸溶液稀释至刻度,测出其吸光度A 样。
由标准曲线查出样品的浓度C 样品[3]。
2.3 结果计算根据精密称出的样品的质量、溶解及稀释的体积可求出C 样。
VitC含量=C 样品/C 样或VitC含量=A 样/K×C 样注:K为标准曲线的斜率。
3 讨论维生素C的还原能力强而易被氧化,特别是在碱性溶液中易被氧化。
另外在碱性溶液或强酸性溶液中还能进一步发生水解。
因此,选择硫酸溶液使成弱酸性。
紫外分光光度法测定维生素c的含量

紫外分光光度法测定维生素c的含量紫外分光光度法是一种常用的定量分析方法,可以用于测定维生素C的含量。
维生素C是一种具有还原性的物质,具有吸收紫外光的特性。
在一定波长下,其吸光度与浓度呈线性关系,因此可以利用紫外分光光度法测定维生素C的含量。
以下是测定维生素C含量的具体步骤:一、实验准备1.实验仪器:紫外分光光度计、100mL容量瓶、50mL移液管、30mL比色皿。
2.实验试剂:维生素C标准品、待测样品溶液、超纯水。
3.实验环境:室温、避光环境。
二、实验步骤1.制作标准曲线:取6个100mL容量瓶,分别加入0mL、0.5mL、1.0mL、2.0mL、4.0mL和8.0mL的维生素C标准品,用超纯水定容至100mL。
在紫外分光光度计上分别测量这6个容量瓶中溶液的吸光度,绘制吸光度与浓度之间的关系曲线,得到标准曲线。
2.测定待测样品:取30mL比色皿,加入待测样品溶液,用超纯水定容至30mL。
在紫外分光光度计上测量该溶液的吸光度。
3.数据处理:将待测样品溶液的吸光度代入标准曲线中,得出待测样品中维生素C的含量。
三、实验结果与分析1.结果记录:将待测样品溶液的吸光度代入标准曲线中,得到待测样品中维生素C的含量。
2.结果分析:通过比较待测样品中维生素C的含量与标准品中维生素C的含量,可以得出待测样品的纯度或浓度是否符合要求。
如果待测样品中维生素C的含量高于或低于标准品中维生素C的含量,则说明待测样品的纯度或浓度存在问题。
四、实验结论通过本次实验,我们成功地利用紫外分光光度法测定了维生素C的含量。
实验结果表明,待测样品中维生素C的含量符合要求,证明了紫外分光光度法的可行性和准确性。
该方法具有操作简便、快速、准确等优点,可以广泛应用于维生素C含量的测定。
需要注意的是,实验过程中要保持避光环境,避免阳光直接照射导致维生素C分解。
同时,实验操作过程中要注意卫生,避免样品污染导致测定结果不准确。
紫外分光光度法测猕猴桃中维生素C的含量

紫外分光光度计法测猕猴桃中维生素C一:实验目的1、了解从果蔬中提取VC的方法.2、掌握用紫外分光光度法测定猕猴桃中Vc的原理、基本过程及操作关键。
3、利用猕猴桃中Vc的含量来评价猕猴桃的营养价值。
二、实验原理紫外快速测定维生素C法,是根据维生素C具有对紫外产生吸收和对碱不稳定的特性,于243 nm处测定样品液与碱处理样品液两者消光值之差,通过查标准曲线,即可计算样品中维生素C的含量。
三:仪器和试剂紫外分光光度计,分析天平,0.2~0.4 mL 10%盐酸,0.6~0.8 mL 1 mol·L-1 NaOH 溶液四:操作步骤(一)标准曲线的制作1.抗坏血酸标准溶液的配制:用分析天平准确称取抗坏血酸10 mg,加2 mL 10%盐酸,加蒸馏水定容至100 mL,混匀。
此抗坏血酸溶液的浓度为100 μg·mL-1 2、标准曲线的绘制3.消光值的测定:以蒸馏水为空白,在243 nm处测定标准系列抗坏血酸溶液的消光值,以抗坏血酸的含量(μg)为横坐标,以相应的消光值为纵坐标作标准曲线。
(二)样品的测定1.样品的提取:将猕猴桃样品洗净、去皮、切碎、混匀。
称取5.00 g于研体中,加入2~5 mL 1% HCl,匀浆,转移到25 mL容量瓶中,稀释至刻度。
若提取液澄清透明,则可直接取样测定,若有浑浊现象,可通过离心(10000 g, 10 min)来消除。
2.样品的测定:取0.1~0.2 mL提取液,放入盛有0.2~0.4 mL 10%盐酸的10 mL容量瓶中,用蒸馏水稀释至刻度后摇匀。
以蒸馏水为空白,在243 nm处测定其消光值。
3.待测碱处理液的制备:分别吸取0.1~0.2 mL提取液,2 mL蒸馏水和0.6~0.8 mL 1 mol·L-1 NaOH溶液依次放入10 mL容量瓶中,混匀,15min后加入0.6~0.8 mL 10% HCl,混匀,并定容至刻度。
以蒸馏水为空白。
实验一-紫外分光光度法测定维生素c片中的vc含量

实验一-紫外分光光度法测定维生素c片中的vc含量一. 实验目的1. 学习维生素C的理化性质和紫外分光光度法测定原理;2. 掌握维生素C片中VC含量的测定方法,加深对常用分析仪器的理解和操作技能。
二. 实验原理维生素C,化学名为抗坏血酸,是一种弱酸性的有机物,化学式为C6H8O6,分子量为176.12g/mol。
维生素C在常温下为白色或淡黄色晶体或粉末,极易溶于水,难溶于乙醇、氯仿和乙醚。
维生素C具有氧化还原性,容易被氧化。
加热、酸、光线等条件都可以使其分解失效。
2. 紫外分光光度法原理紫外分光光度法是一种用于测定化学物质浓度和用于确定化学分子的结构的常用分析方法之一。
本实验以维生素C的最大吸收波长为265nm进行测定。
根据比尔-朗伯定律,紫外分光光度法可以根据化合物在特定波长下吸收的光的数量来计算化合物的浓度。
根据计算所需的吸光度和吸收系数值,可以使用比尔-朗伯定律推导出样品中所含物质的浓度。
3. 维生素C片中VC含量的测定方法本实验采用紫外分光光度法测定维生素C片中VC含量。
样品的制备包括提取和过滤,检测前需要检查仪器的性能,然后以样品的最大吸收波长(λmax)为265nm进行测定。
使用对照溶液、标准曲线和工作曲线进行测定,最后计算出样品中VC的含量。
操作步骤如下:(1)样品制备取约1.0g维生素C片粉末,将其加入50mL锥形瓶中,并据以加入3-5mL1%酒石酸溶液和40mL去离子水,摇晃均匀备用。
(2)对照溶液的制备(3)标准曲线的制备取维生素C标准品0.020g,溶于水中,定容至100mL,得到储存浓度为0.200mg/mL的维生素C标准溶液。
(5)测定样品将对照溶液、标准曲线各用0.45μm滤膜过滤,然后加入分别从10mL量筒中取出1.0mL样品溶液,水定容至10mL。
调节测试波长到265nm处。
测量对照液吸光度为A1,标准解各吸光度为A2、A3、A4、A5、A6;样品吸光度为Ax。
三. 实验步骤(1)仪器操作准备1) 打开仪器电源,拓扑显示屏显示后,启动UV-VIS1000分光光度计软件程序,并用移液管加入100μL试剂至样品池;2) 在菜单选项中选择"致动器",点击"参照制备",将10mM硝酸钾对比池放入槽中,并通过菜单项中"参照制备"对参照对比。
紫外分光光度法测定五种果蔬中维生素C的含量

紫外分光光度法测定五种果蔬中维生素C的含量一、本文概述维生素C,也被称为抗坏血酸,是一种重要的水溶性维生素,对人体健康具有多种重要作用,包括增强免疫力、促进铁的吸收和利用、参与胶原蛋白的合成等。
由于其对人体健康的重要性,了解各种食物中维生素C的含量对于合理搭配膳食、保障人体维生素C的充足摄入具有重要意义。
因此,本研究采用紫外分光光度法测定了五种常见果蔬中维生素C的含量,旨在为公众提供更为准确、科学的膳食指南。
紫外分光光度法是一种基于物质对紫外光的吸收特性进行定量分析的方法。
该方法具有操作简便、灵敏度高、重现性好等优点,因此被广泛应用于各种生物化学分析中。
在本研究中,我们通过对五种果蔬样品进行前处理,提取其中的维生素C,并利用紫外分光光度计测定其吸光度,从而计算出样品中维生素C的含量。
本研究选取的五种果蔬分别为苹果、橙子、草莓、菠菜和番茄,它们都是人们日常膳食中常见的富含维生素C的食物。
通过对这些果蔬中维生素C含量的测定,我们可以了解不同食物中维生素C含量的差异,为人们在日常饮食中合理搭配食物提供参考。
本文旨在利用紫外分光光度法测定五种常见果蔬中维生素C的含量,为公众提供更为准确、科学的膳食指南,以促进人们的健康。
二、实验材料与方法选择了五种具有代表性的果蔬样品,包括苹果、橙子、草莓、菠菜和青椒。
这些果蔬因其维生素C含量高且易得而被选中。
实验所需的主要试剂包括2,6-二氯靛酚钠、草酸、偏磷酸等。
设备方面,使用了紫外可见分光光度计、离心机、电子天平、研钵、容量瓶、移液管等。
将每种果蔬样品洗净、切碎,并去除不可食部分。
然后,将样品用偏磷酸-草酸混合液研磨,离心取上清液,用于后续的维生素C含量测定。
采用偏磷酸-草酸混合液作为提取液,通过研磨和离心,使果蔬中的维生素C充分溶解在提取液中。
准确称取一定量的2,6-二氯靛酚钠标准品,用蒸馏水溶解并定容,得到不同浓度的标准溶液。
然后,在紫外可见分光光度计上,以蒸馏水为空白对照,测定各标准溶液的吸光度,绘制标准曲线。
实验93紫外分光光度法测定水果(或蔬菜)中的维生素C含量

2 mL 蒸馏水和 0.6~ 0.8 mL 1 mol·L-1 NaOH 溶液依次放入 10
mL 容量瓶中,混匀, 15min 后加入 0.6 ~ 0.8 mL 10% HCl ,混 匀,并定容至刻度。以蒸馏水为空白。在 243 nm 处测定其消
光值。
4 .由待测样品与待测碱处理样品的消光值之差和
93.5 问题讨论
(1)除了本实验中的方法外,抗坏血酸还有哪些
测定方法?
93.6 参考答案
(1)除了本实验中的方法外,抗坏血酸还有哪些测定方法? 答:一、氧化还原法 1. 直接碘量法 2. 2,6-二氯酚靛酚滴定法 二、分光光度法 1. 紫外快速测定法 2. 2,4-二硝基苯肼法 3. 高铁还原法测定血浆中的抗坏血酸 三、光电比浊法 四、电化学法 五、荧光分析法 1. 抗坏铁酸的微量荧光测定法 2. 抗坏铁酸总量的荧光测定法
测定标准系列抗坏血酸溶液的消光值,以抗坏血酸的含
量(μg)为横坐标,以相应的消光值为纵坐标作标准 曲线。
(二)样品的测定 1.样品的提取:将果蔬样品洗净、擦干、切碎、混匀。 称取 5.00 g 于研体中,加入 2 ~ 5 mL 1% HCl ,匀浆,转移到 25 mL容量瓶中,稀释至刻度。若提取液澄清透明,则可直接
取样测定,若有浑浊现象,可通过离心(10000 g, 10 min)
来消除。 2.样品的测定:取0.1~0.2 mL提取液,放入盛有0.2~
0.4 mL 10%盐酸的10 mL容量瓶中,用蒸馏水稀释至刻度后摇
匀。以蒸馏水为空白,在243 nm处测定其消光值。 3 .待测碱处理液的制备:分别吸取 0.1 ~ 0.2 mL 提取液,
0.2
0.3
0.4
0.5
0.6
紫外分光光度法测定水果中维生素C含量

山 东 化 工 收稿日期:2020-09-08基金项目:营口理工学院2018年院级科研课题:紫外分光光度法在食品检测中的应用(YYL201809);营口理工学院2020年校级大学生创业项目:基于天然色素的食品级儿童彩泥的研制作者简介:付晓伟(1984—),女,辽宁营口人,毕业于辽宁师范大学,硕士,高级实验师,研究方向:现代仪器分析;通信作者:刘海燕(1972—),女,辽宁营口人,教授,博士,化学与材料工程系主任,研究方向:主要从事功能配位化学的研究。
紫外分光光度法测定水果中维生素C含量付晓伟,吴 晓,姜莉莉,苑 蕾,张静玉,刘凤翊,刘海燕(营口理工学院化学与环境工程学院,辽宁营口 115014)摘要:维生素C(VC)是人体生理代谢所必需的一种化合物,它可以使人体生理机能保持稳定。
本文采用醋酸为浸提剂,通过单因素和正交实验对提取样品的料液比、浓度、时间、温度进行考察,确定了VC的最佳提取条件:浸提浓度为2%,浸提温度为20℃,料液比为1∶2(g∶mL),提取时间为30min。
利用紫外-可见分光光度法在最佳提取条件下对10种水果样品的VC含量进行测定,结果表明VC含量:猕猴桃>冰糖橙>橙子>桔子>红心火龙果>草莓>油桃>菠萝>梨>苹果,其中猕猴桃的VC含量最丰富,为407.58mg/100g,苹果的最少为144.95mg/100g。
该方法检出限为0.003mg/mL,RSD<1%,回收率在96.6%-106.8%之间。
关键词:紫外分光光度法;维生素C;含量测定中图分类号:O657.32 文献标识码:A 文章编号:1008-021X(2020)24-0102-02DeterminationofVitaminCinFruitsbyUVspectrophotometryFuXiaowei,WuXiao,JiangLili,YuanLei,ZhangJingyu,LiuFengyi,LiuHaiyan(DepartmentofChemicalandMaterialEngineering,YingkouInstituteofTechnology,Yingkou 115014,China)Abstract:VitaminC(VC)isacompoundessentialforphysiologicalmetabolismofthehumanbody,whichcanstabilizethephysiologicalfunctionsofthehumanbody.Inthispaper,aceticacidwasusedastheextractingagent.Theratioofmaterialtoliquid,concentration,timeandtemperatureoftheextractedsampleswereinvestigatedbysinglefactorandorthogonalexperiments.TheoptimalextractionconditionsofVCweredetermined:theconcentrationofextractionwas2%,Thetemperaturewasraisedto20℃,theratioofmaterialtoliquidwas1∶2(g∶mL),andtheleachingtimewas30min.ThevitaminCcontentof10fruitsampleswasdeterminedbyUV-visiblespectrophotometryunderoptimalextractionconditions.TheresultsshowedthatVCcontent:kiwifruit>rocksugarorange>orange>orange>redheartdragonfruit>strawberry>nectarine>pineapple>Pear>Apple,ofwhichkiwifruitisthemostabundant,407.58mg/100g,andappleisatleast144.95mg/100g.Thedetectionlimitofthemethodis0.003mg/mL,theRSDis<1%,andtherecoveryrateisbetween96.6%and106.8%.Keywords:ultravioletspectrophotometry;vitaminC;betermination 维生素C又称L-抗坏血酸,是人体正常生理代谢所必不可少的一种维生素,能调节人体氧化还原代谢反应,增强人体对外界环境的抗应激能力以及免疫能力,水果中VC含量丰富,是人体VC重要摄取来源之一。
果蔬中维生素C含量的测定方法

HENANNONGYE河南农业2012年第1期(下)维生素C 又名抗坏血酸,无色晶体,分子式C 6H 8O 6,是一种重要的水溶性维生素。
它与人体的多种代谢有关。
维生素C 能增强人体免疫功能,对某些有毒物质具有解毒作用,具有抗衰老作用,具有防癌抗癌作用等。
维生素C 摄入不足、吸收障碍都可以致病。
人体不能合成及贮存维生素C ,故必需从外界摄取。
维生素C 在自然界分布很广,主要存在于植物性食物的果实、浆果和蔬菜中。
不同的水果、蔬菜中维生素C 的含量不同。
测定果蔬中维生素的含量对评定其营养具有重要的意义。
果蔬中维生素C 的测定方法主要有高效液相色谱法、分光光度法、原子吸收光谱法、荧光分光光度法、滴定分析法等。
一、高效液相色谱法高效液相色谱法是近年来发展起来的一种测定维生素C 含量的方法,具有高效、快速、稳定、结构准确、操作简便等特点。
高效液相色谱法测定维生素C 含量通常采用C 18柱或C 8柱,由于维生素C 对紫外光有吸收,故检测器常用紫外检测器。
此测定方法特别适用于颜色较深的提取液样品的测定。
刘贵花等应用反相高效液相色谱法对时令水果中维生素C 含量进行直接测定。
结果表明:维生素C 在10~640μg/ml 范围内呈良好线性,回收率为99.3%~104.5%,RSD 为1.65%;本法操作简便,结果准确,重现性好,为测定水果中维生素C 的含量提供了一种有效方法。
徐琅等应用反相高效液相色谱法对5种野生蔬菜中维生素C 含量进行测定。
维生素C 在浓度为50~750μg/ml 范围内线性良好,回收率为99.5%~101.8%,RSD 为1.07%;该法操作简便,结果准确。
胡应杰等建立了一种高效液相色谱测定辣椒中维生素C 含量的方法,采用0.1%的草酸作为提取剂,DAD 检测器,检测波长254nm 。
维生素C 在20~100mg/l 内有良好的线性关系,回收率为91.24%~105.6%,RSD 小于2%;该测定方法简便、快速,能准确测定辣椒中维生素C 的含量。
实验三 果蔬中维生素C的定量测定

实验三果蔬中维生素C的定量测定(紫外法)(4学时)一、实验目的1. 学习用铜离子氧化法测定维生素C(Vc)(紫外法);2. 了解Vc定量测定的其他方法,如:磷钼酸比色法、碘量法、2,6-二氯酚靛酚滴定法(近年来用全自动电位滴定仪进行电位滴定)、紫外法、2,4-二硝基苯肼测定总抗坏血酸量、高效液相色谱法、毛细管电泳法、荧光法、Flinb近红外分光光度法等。
二、实验原理抗坏血酸在波长243~267nm处有较高的吸收值,但在样品成分比较复杂时,因有强烈的背景吸收而不适宜用紫外法测定其Vc含量。
用碱加热法等处理法都存在试剂较贵、操作复杂、时问长等一系列问题而不能广泛应用。
利用铜离子消除背景误差,能直接测定一些水果蔬菜样品中的Vc含量而不需要进行前处理,操作简单干扰少。
附加说明:在测定Vc的国标方法中,荧光法为测定食物中Vc含量的第一标准方法,2,4-二硝基苯肼法作为第二法。
三、实验器材与试剂实验材料桔子实验器材紫外/可见分光光度计;涡旋混合仪;高速冷冻离心机;榨汁器;电热恒温水浴锅;试管与试管架;胶头器长滴管及移液管;250mL烧杯等。
实验试剂1. 120μg/mL Vc贮液:120mg Vc,加适量蒸馏水溶解,然后用1000毫升容量瓶定容。
存4℃备用。
2. 5μg/mL的铜离子溶液:①先配成1000μg/mL的硫酸铜溶液;②取上述硫酸铜溶液5mL,加入1mol/L的醋酸溶液7mL及1mol/L醋酸钠200mL,用蒸馏水定容。
③5×104mol/L的EDTA溶液:36.5mgEDTA溶于适量蒸馏水,250 mL 馏水定容。
④铜离子-EDTA混合液(6.2×105mol/L):使用前将上述铜离子溶液和EDTA以4:1(v/v)混合而成(现用现配)。
四、实验步骤1. 标准曲线制作取12支试管(大试管)分成2组,按下表进行操作。
维生素C溶液浓度为120μg/mL。
2. 样品测试取一定量的桔子瓣记录克数。
紫外分光光度法测定水果蔬菜中维生素C含量测定
70 生物技术世界 BI OTECHWORLD
白茹 邹本春 (辽宁丹东 118008)
摘要 : 利用维 生素 C对 紫外 产生吸 收和 对碱不 稳定 的特 性,用 紫外 分光光 度法 测定五 种常 见果 蔬中维 生素 C的 含量 。该方 法具有 准确 、快速 、稳
定、试剂易 得等优点。
关键词:紫外分光光度法 水果蔬菜 维生素C
中图 分类 号: TS25 5.7
文 献标识码: A
文章编号:1 674 -20 60( 201 3)03 -00 70- 01
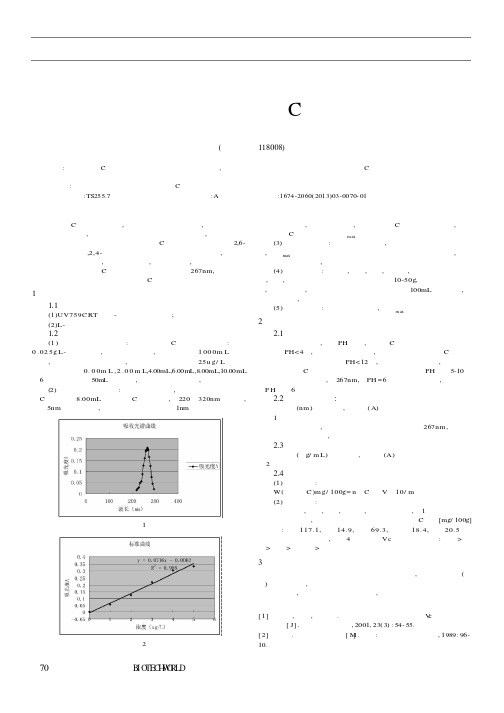
维生素C又叫抗坏血酸,广泛存在 于植物组织中,新 鲜的水果、 蔬菜中 含量较多,是一种水溶性 小分子生物活性 物质,也是人体需 要量最大 的一种维生素。果蔬中维生素C含量的测定一般 采用2,6二氯 靛酚滴定 法,2,4-二 硝基苯肼 法和荧光 粉光光度 法等,这些方 法都有所用试 剂不稳,操作程序复杂,费时等缺点,笔者采用吸收光 谱曲线法确定 维生素C的水溶性的最大吸收波长267nm,进而通过 工作曲线法快速 测定果蔬中维生素C的含量。 1 实验部分
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
紫外分光光度计法
测定几种常见果蔬中维生素C的含量
摘要:利用维生素C对紫外产生吸收和对碱不稳定的特性,用紫外分光光度法测定5种常见果蔬中维生素C的含量。
最大吸收波长为243nm,标准曲线方程为A=0.00537c,相关系数为R^2=0.99539。
9种果蔬中维生素C含量[mg·(100g)-1]分别为:青尖椒111.8、上海青104.2、韭菜82.5、小白菜78.9、西芹59.70、胡萝卜49.8、西兰花28、茄子26.4、山药14.9。
该方法简单、快速,结果令人满意。
1.前言
维生素C又称抗坏血酸,是一种水溶性维生素。
能预防牙龈出血及萎缩、提高人体免疫力,对坏血病、动脉硬化、贫血等有一定疗效。
天然存在的抗坏血酸有L型和D型2种,后者无生物活性。
维生素C 是呈无色无臭的片状晶体,易溶于水,不溶于有机溶剂。
在酸性环境中稳定,遇空气中氧、热、光、碱性物质,特别是由氧化酶及痕量铜、铁等金属离子存在时,可促进其氧化破坏。
氧化酶一般在蔬菜中含量较多,故蔬菜储存过程中都有不同程度流失。
但在某些果实中含有的生物类黄酮,能保护其稳定性。
维生素C的测定方法主要有紫外分光光度法、红外光谱法、2,6-二氯靛酚滴定法、高效液相色谱法、钼蓝比色法、原子吸收法、碘量法、电位滴定法、荧光光度法、毛细管电泳法、流动注射化学发光法[2-12]等。
其中原子吸收法、高效液相色谱法和荧光光度法仪器相对昂贵;碘量法和电位滴定法操作步骤较繁琐,而且受其它还原性物质、样品色素颜色和测定时间的影响;紫外分光光度法是根据维生素C对紫外产生吸收和对碱不稳定的特性,于243nm处测定样品液与碱处理样品液两者吸光度之差,通过标准曲线方程,即可计算样品中维
生素C的含量。
本实验采用市售的西芹为研究材料,用紫外分光光度法测定韭菜中维生素C的含量。
2.实验
2.1 材料、试剂和仪器
市售西芹
10%HCl、抗坏血酸、1mol/lNaOH、蒸馏水
UV2000-紫外可见分光光度计、KDC-40-电子天平、FA1104-离心机
2.2 方法
2.2.1 标准溶液的配制
准确称取0.050g抗坏血酸,加10ml 10%HCl溶解,用蒸馏水定容至500ml,混匀,即得100ug/ml维生素C标准溶液。
2.2.2 标准曲线的绘制
分别准确移取100ug/ml维生素C标准溶液0ml、0.03ml、0.06ml、0.09ml、0.12ml、0.15ml、0.18ml、0.24ml、0.30ml于试管中,分别加入蒸馏水至总体积为3ml。
以水为参比,在243nm处测定吸光度,以维生素C浓度为横坐标、吸光度为纵坐标,绘制标准曲线。
2.2.3 果蔬样品的处理
将西芹洗净晾干,取10.4489g于研钵中,先加入10%HCl 5ml,再加入5ml,研磨匀浆,转移至50ml容量瓶中,稀释至刻度,混匀。
移至离心管中3000r/min离心10min,取上清液即为待测果蔬提取液。
2.2.4 待测果蔬提取液吸光度的测量
取0.1ml待测果蔬提取液,放入盛有0.2ml 10%HCl的试管中,再加入蒸馏水4.7ml,摇匀。
以蒸馏水为空白对照,在243nm处测定其吸光度(A₁)。
2.2.5 碱处理果蔬提取液吸光度的测量
依次吸取0.1ml待测果蔬提取液、1ml蒸馏水和0.4ml 1mol/l NaOH溶液放入试管中,摇匀;静置20min后加入0.4ml 10%HCl,混匀,再加入3.1g蒸馏水。
以蒸馏水为空白对照,在243nm处测定其吸光度(A₂)。
2.2.6 吸光度确定
果蔬样品吸光度=待测果蔬提取液吸光度(A₁)-碱处理果蔬提取液吸光度(A₂)
2.2.7 维生素C含量的计算
测得果蔬样品的吸光度后,依据标准曲线方程,即可计算出果蔬中维生素C的含量[mg/100g]。
维生素C含量=(c·V总·V待测总·100)/(V₁·W总·1000)式中:c为依标准曲线方程计算得到的维生素C浓度,ug/ml
V₁为测吸光度时吸取样品溶液的体积,ml;
V总为吸取样品定容总体积,ml;
V待测总为待测样品总体积,ml;
W总为果蔬质量,g;
100为100g果蔬。
3.结果
3.1 标准曲线
由标准曲线可得线性回归方程为A=0.05371x,相关系数R²=0.99539。
3.2 维生素C含量的测定
由图可知,蔬菜中的维生素C含量分别为[mg/100g]:青尖椒111.8、上海青104.2、韭菜82.5、小白菜78.9、西芹59.70、胡萝卜49.8、西兰花28、茄子26.4、山药14.9。
9种蔬菜中维生素c的含量关系为:青尖椒>上海青>韭菜>小白菜>西芹>胡萝卜>西兰花>茄子>山药。
3.3 结论与分析
3.3.1 结论
利用维生素C在紫外光区有明显的吸收和对碱不稳定的特性,建立了果蔬中维生素C含量的测定方法。
在一定浓度范围内,维生素C浓度与紫外吸光度呈良好的线性关系,回归方程为A=0.05371x,相关系数R²=0.99539。
9种蔬菜中Vc含量大小依次为:青尖椒>上海青>韭菜>小白菜>
西芹>胡萝卜>西兰花>茄子>山药。
3.3.2 误差分析
(1). 碾磨不充分,研钵上有残留,导致部分维生素C残留在蔬菜内,故测Vc含量值偏低。
(2).将研钵中的研磨液转移至容量瓶中时有部分研磨液漏出,仪器清洗不干净,导致定容后容量瓶内Vc 浓度偏低。
(3)取上清液时有少量底层物质吸入其中,导致测吸光光度值有误差。
该方法简单易行、灵敏度高、结果准确,可快速测定果蔬中维生素C的含量。
